Симптомы свищей при болезни крона
Обновлено: 18.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Колит: причины появления, симптомы, диагностика и способы лечения.
Определение
Колит – это общее название группы заболеваний, для которых характерно острое или хроническое воспаление слизистой оболочки толстого кишечника.
Причины возникновения колита
Колит может развиться в результате инфекции, недостаточности кровоснабжения кишечника (ишемии), лекарственного поражения, бывает вторичным по отношению к иммунодефицитным состояниям, может возникать после лучевой терапии органов малого таза при гинекологическом, урологическом и ректальном раке.
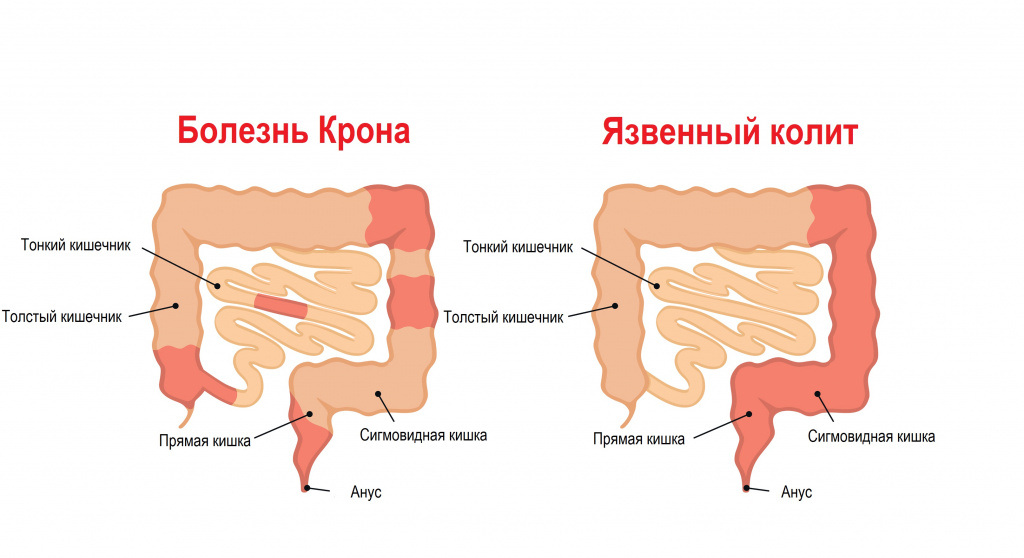
Воспаление слизистой толстого кишечника характерно для болезни Крона (БК) и неспецифического язвенного колита (НЯК).
Выделяют также микроскопический колит, при котором данные рентгенологических и эндоскопических исследований кишечника не показывают отклонений, а признаки воспаления определяются с помощью биопсии.
Инфекционное поражение кишечника могут вызывать бактерии (чаще всего Campylobacter jejuni), вирусы, простейшие и паразиты. Заражение бактерией Campylobacter jejuni происходит в результате употребления грязных продуктов или воды. Развитие колита зависит от количества попавших в кишечник бактерий, их вирулентности (способности вызвать заболевания) и иммунитета человека. Инкубационный период составляет 2-4 дня. Бактерии размножаются в желчи, а затем проникают через слизистую оболочку в кишечник, вызывая выраженное воспаление.
Причиной развития инфекционных колитов у пациентов с ослабленным иммунитетом, у больных с заболеваниями крови, новообразованиями, лучевой болезнью могут стать условно-патогенные микроорганизмы (представители нормальной микрофлоры кишечника) - стафилококки, протеи, кишечная палочка.
Анаэробные бактерии Clostridium difficile, продуцирующие токсины, вызывают псевдомембранозный колит. Заболевание возникает на фоне изменений нормальной микрофлоры кишечника, в основном под влиянием антибиотиков (цефалоспоринов, бета-лактамных препаратов), которые подавляют рост других микроорганизмов и обеспечивают рост Clostridium difficile.
Среди вирусов, способных вызвать колит, выделяют цитомегаловирус, среди простейших – дизентерийную амебу (Entamoeba histolytica). К паразитам, результатом жизнедеятельности которых становится колит, относятся острицы, аскариды, власоглав, среди циркулирующих в крови – шистосомы.
Ишемический колит возникает при недостаточном кровоснабжении толстого кишечника, что приводит к воспалению слизистой, появлению язв и кровоизлияний.
Чем продолжительнее нарушение кровоснабжения, тем тяжелее поражается кишечник. При возобновлении нормального кровообращения может возникнуть реперфузионный синдром, который приводит к дальнейшим тяжелым повреждениям кишки. Пациенты с ишемическим колитом обычно страдают заболеваниями сердечно-сосудистой системы (сердечной недостаточностью, атеросклерозом, фибрилляцией предсердий), могут иметь злокачественные новообразования и патологии свертывающей системы крови, ведущие к тромбозам. Кроме того, ишемические повреждения кишечника определяются при так называемых ятрогенных (связанных с оказанием медицинской помощи) вмешательствах – операциях по устранению аневризмы брюшного отдела аорты, в ходе подготовки к колоноскопии или во время ее проведения.
К лекарственному колиту может привести прием нестероидных противовоспалительных препаратов, аспирина, ингибиторов протонной помпы, бета-блокаторов, статинов, иммуносупрессивных препаратов.
Развитие микроскопического колита связано с аутоиммунными заболеваниями, такими как целиакия, сахарный диабет 1-го типа, псориаз, нарушения функции щитовидной железы. Выделяют два основных подтипа микроскопического колита – коллагенозный и лимфоцитарный.
НЯК и БК относят к так называемым воспалительным заболеваниям кишечника. Точные причины развития этих заболеваний неизвестны, однако, вероятно, при НЯК повреждение стенки кишки сопровождается аутоиммунной реакцией с продукцией антител к собственным клеткам кишечника. Среди причин развития БК обсуждаются наследственные, инфекционные, иммунологические и др., но ни одна из теорий на настоящий момент не является абсолютно подтвержденной.
Классификация заболевания
Помимо этиологического (причинного) фактора, колиты подразделяют в зависимости от остроты процесса (острые и хронические) и степени тяжести. Хронические колиты классифицируют по характеру течения заболевания (непрерывное, рецидивирующее, перемежающееся) и по фазам (обострение или ремиссия). В зависимости от того, насколько поражен толстый кишечник при хроническом колите, выделяют тифлит (воспаление слепой кишки), трансверзит (воспаление поперечно-ободочной кишки), сигмоидит (воспаление сигмовидной кишки), проктит (воспаление прямой кишки), угловой колит (лево- и правосторонний в зависимости от пораженного изгиба поперечно-ободочной кишки), причем нередко они могут сочетаться (проктосигмоидит). При панколите поражены все отделы толстого кишечника.
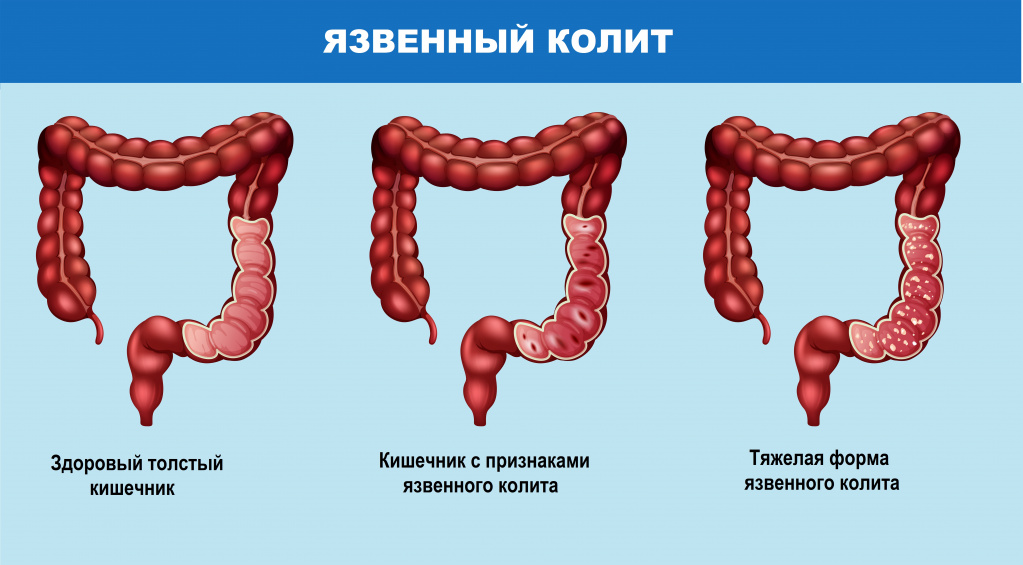
Симптомы колита
Острый колит сопровождается сильными болезненными ощущениями, пациенты отмечают резь и спазмы в животе и в области прямой кишки (тенезмы). Для хронического воспаления характерны колики и ощущение тяжести в животе. У пациентов могут наблюдаться запоры, водянистая диарея, иногда с кровью и слизью, бурление в животе, ложные позывы к дефекации, усталость, повышение температуры тела.
При болезни Крона присутствуют ректальные кровотечения, боль в животе, диарея, лихорадка, анемия, поражения анальной и перианальной области с формированием свищей, язв, анальных трещин. Нередко бывают внекишечные проявления – артриты, поражения глаз, афтозный стоматит, узловатая эритема – эти поражения отмечены у трети пациентов с БК и неразрывно связаны с воспалением кишечника.
В клинической картине неспецифического язвенного колита также отмечаются боли, тенезмы, появление крови в кале и диарея в ночные часы. Как и при БК, развитие НЯК сопровождается внекишечными поражениями кожи, полости рта, суставов, органов зрения.
Диагностика колита
Диагностика колита основывается на клинических и лабораторных данных, эндоскопии и биопсии.
В первую очередь необходимо провести микробиологические исследования и посевы для исключения инфекционного поражения.
Синонимы: Общий анализ кала. Stool analysis, Fecal analysis. Краткая характеристика исследования «Копрограмма» Кал – конечный продукт, образующийся в результате сложных биохимических процессов расщепления пищи, всасывания продуктов переваривания в желудочно-кишечном тракте и в.

- Запись опубликована: 09.10.2020
- Reading time: 4 минут чтения
Болезнь Крона – хроническое воспалительное заболевание кишечника неизвестной этиологии. Воспаление может поражать весь желудочно-кишечный тракт: ротовую полость, пищевод, желудок, двенадцатиперстную кишку, тощую кишку, и чаще всего поражения расположены в подвздошной кишке, а также могут присутствовать по всей толстой и прямой кишке.
Патология встречается у людей разных возрастных групп, но чаще всего поражает молодых пациентов в возрасте от 20 до 30 лет и между 5 и 7 десятилетиями. Благодаря соответствующему лечению больные могут достичь длительного периода ремиссии, в течение которого симптомы не проявляются. Однако предсказать, когда болезнь будет прогрессировать, невозможно.
Что такое болезнь Крона
Болезнь Крона – хроническое кишечное заболевание, характеризующееся воспалением, которое поражает не только поверхностные, но и глубокие слои стенки кишечника. Хотя воспалительные поражения или язвы могут возникать в любом месте кишечника от рта до заднего прохода, обычно поражаются задняя часть тонкой кишки и начало толстой кишки. Кроме того, характерно сегментарное поражение – когда воспаление охватывает не весь кишечник, а лишь некоторые его части.
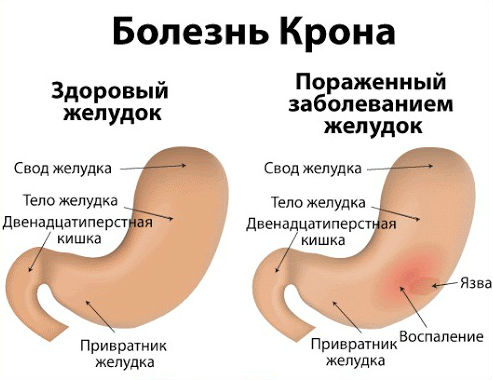
Что такое болезнь Крона
Кто болеет болезнью Крона?
Патология доминирует, прежде всего, в высокоразвитых городских агломерациях Западной и Северной Европы. Примерно у 20% пациентов это генетически обусловленное заболевание, связанное с наличием гена NOD2/CARD15, расположенного на хромосоме 16 (IBD1), что увеличивает вероятность заболеваемости примерно в 20-40 раз.
Также было доказано, что у курильщиков сигарет вероятность развития этого заболевания в два раза выше, и его течение в этих случаях намного тяжелее.
В чем причина болезни Крона
Факторы, ответственные за воспалительные заболевания кишечника, в т. ч. язвенный колит и болезнь Крона, до сих пор полностью не изучены. Считается, что следует учитывать несколько компонентов, способных повлиять на развитие болезни. К ним относятся семейные, генетические, экологические, бактериальные, иммунологические и психологические факторы.
Считается, что начало болезни Крона может быть связано с определенными нарушениями иммунной системы организма.
Несмотря на многочисленные попытки выделить генетический маркер, полезный для идентификации людей, предрасположенных к развитию болезни Крона, не удалось обнаружить ни одного причинного фактора, который оказал бы фундаментальное влияние на развитие болезни.
Симптомы болезни Крона
Из-за протяженности и мультифокальности болезненного процесса клиническая картина при БК зависит от анатомической локализации поражений.
У пациентов с изменениями тонкого кишечника наблюдаются:
В случае локализации высыпаний в толстом кишечнике преобладают боли в животе, метеоризм, диарея с примесью слизи, крови, анемия и общая слабость наряду с похуданием. В остальных случаях первыми симптомами заболевания могут быть свищи, трещины и перианальные абсцессы.
Наиболее частые симптомы болезни Крона:
- боль в правом бедре;
- понос;
- повышенная температура тела;
- потеря веса;
- метеоризм;
- анальная боль;
- перианальные свищи и абсцессы;
- изменения кожи;
- боли в суставах.
Течение болезни
Болезнь Крона может повредить любую часть пищеварительного тракта, но наиболее частые участки поражения – подвздошная кишка и аппендикс. Течение этого заболевания может быть хроническим и рецидивирующим. Обострения обычно чередуются с ремиссиями (временным выздоровлением).
От легкой до умеренной формы заболевания проявляются легкие клинические симптомы. Умеренно-тяжелая форма заболевания протекает с лихорадкой, анемией, похуданием, тошнотой, рвотой.
Тяжелая форма заболевания – сильный жар, боли в животе, рвота, кишечная непроходимость , резкое похудание.

Кишечная непроходимость
Диагностика
Анализы крови могут показывать снижение гемоглобина из-за недостатка железа, фолиевой кислоты или витамина B12, увеличение количества лейкоцитов и изменения скорости оседания эритроцитов.
Поражения кишечника выявляют при рентгенологическом и эндоскопическом исследованиях. Во время эндоскопического исследования (колоноскопия, гастроскопия) для микроскопического исследования берется участок слизистой оболочки (биопсия). Также для определения наличия бактерий, вызывающих воспаление кишечника, проводится посев фекалий.
Как лечится болезнь Крона?
Учитывая сложность воспалительного процесса, степень поражения и отсутствие четкого причинного фактора заболевания, идеальное лекарство для модификации лечения болезни Крона еще не разработано. В настоящее время можно выделить два метода лечения: консервативный и оперативный. Цели лечения – контролировать воспаление в кишечнике, восстанавливать нутритивный статус и предотвращать рецидивы (продление времени ремиссии).
Комплексное консервативное лечение включает: правильное питание, восполнение дефицита, противовоспалительное, иммунодепрессивное, биологическое и симптоматическое лечение. В настоящее время в консервативном лечении используются 5 групп препаратов для поддержания ремиссии заболевания:
- 5-аминосалицилаты – сульфасалазин и 5-аминосалициновая кислота (5-АСК, месалазин);
- глюкокортикостероиды;
- метронидазол, ципрофлоксацин;
- азатиоприн (AZA) и его метаболиты, 6-меркаптопурин (6-MP) и 6-тиогуанин (6-TG);
- биологические препараты (инфликсимаб).
Подсчитано, что примерно 75% пациентов с болезнью Крона в какой-то момент жизни потребуют хирургического вмешательств а.

Хирургическое лечение осложнений болезни Крона
Показания к хирургическому лечению включают:
- устойчивость к консервативному лечению со значительным прогрессированием заболевания;
- кишечная непроходимость;
- внутрибрюшинный абсцесс;
- свищ;
- перфорация желудочно-кишечного тракта;
- желудочно-кишечное кровотечение;
- перианальные изменения;
- дисплазия и трансформация опухоли.
В этих случаях операция служит только для облегчения симптомов, но не излечивает само заболевание. Основным принципом хирургического лечения является щадящее удаление воспалительных поражений кишечника, создание новых широких кишечных анастомозов, иссечение перианальных свищей и дренирование абсцесса.
Осложнения
Осложнения могут возникнуть при болезни Крона даже при лечении. Например, часто сужается просвет кишечника, что может привести к кишечной непроходимости.
Также болезнь Крона характеризуется глубокими язвами, которые проникают через всю стенку кишечника в соседние органы – мочевой пузырь, влагалище, кожа, другие кишечники, образуя проток – свищ, который часто загнаивается. Свищи обычно возникают между кишечником и кожей вокруг заднего прохода, а также между тонкой и прямой кишкой. Менее часто возникают кровотечения из кишечника.
При болезни Крона воспаление тонкой кишки приводит к ухудшению всасывания некоторых питательных веществ или их потере с диареей, что приводит к нехватке белка, витаминов, микроэлементов (цинка, магния, кальция, железа), нарушению развития и роста в детстве. Поскольку витамин B12 плохо усваивается, начинается анемия.
Болезнь Крона также может вызывать поражение других органов: воспаление глаз, суставов, поражения кожи, заболевания печени (обычно первичный склерозирующий холангит с поражением желчных протоков), почек и желчных камней.
Затяжная болезнь Крона увеличивает риск рака кишечника, но это осложнение встречается реже, чем при язвенном колите.
Профилактика
Меры по предотвращению болезни Крона неизвестны.
Специальной диеты, помогающей предотвратить усугубление болезни, нет, но у некоторых пациентов симптомы ухудшаются от молока, алкоголя, пряных специй и т. д. Желательно избегать таких продуктов, а во время обострений есть меньше продуктов с высоким содержанием клетчатки. Важно потреблять достаточное количество недостающих витаминов и микроэлементов.
Следует знать, что даже после исчезновения симптомов болезни нужно регулярно принимать лекарства, так как болезнь может вернуться в любой момент.
ГБУЗ "Московский клинический научно-практический центр" Департамента здравоохранения Москвы
ГБУЗ "Московский клинический научно-практический центр" Департамента здравоохранения Москвы
ГБУЗ "Московский клинический научно-практический центр" Департамента здравоохранения Москвы
ФГАОУ ВО «Российский университет дружбы народов» Министерства науки и высшего образования Российской Федерации, Москва, Россия
ГБУЗ "Московский клинический научно-практический центр" Департамента здравоохранения Москвы
Московский клинический научно-практический центр. ЦНИИ гастроэнтерологии Департамента здравоохранения Москвы
Комбинированная биологическая терапия свищевой формы болезни Крона. Клиническая демонстрация
Журнал: Терапевтический архив. 2014;86(2): 102‑105
Князев О.В., Парфенов А.И., Щербаков П.Л., Коноплянников А.Г., Ручкина И.Н., Лищинская А.А. Комбинированная биологическая терапия свищевой формы болезни Крона. Клиническая демонстрация. Терапевтический архив. 2014;86(2):102‑105.
Kniazev OV, Parfenov AI, Shcherbakov PL, Konoplyannikov AG, Ruchkina IN, Lishchinskaia AA. Combination biological therapy for fistular Crohn's disease: Clinical demonstration. Terapevticheskii Arkhiv. 2014;86(2):102‑105. (In Russ.).
ГБУЗ "Московский клинический научно-практический центр" Департамента здравоохранения Москвы
Аннотация. Перианальные свищи - наиболее распространенные и часто встречающиеся типы свищей при болезни Крона (БК). Они с трудом поддаются лечению, ухудшают качество жизни больного и повышают риск тотальной резекции кишки. Несмотря на значительный эффект от биологической (антицитокиновой) терапии свищевой формы БК, лечение данной категории больных остается трудной задачей, с высоким риском развития рецидива БК. Мезенхимальные стромальные клетки (МСК), обладающие иммуномодулирующими свойствами и большим регенеративным потенциалом, в настоящее время также применяются для лечения свищевой БК и перианальных свищей другой этиологии. Приведенный клинический случай демонстрирует, что полного заживления свища удалось достигнуть лишь после нескольких местных введений МСК, в комбинации с инфликсимабом и азатиоприном. Мировой и наш клинический опыт демонстрирует, что необходимы рандомизированные контролируемые исследования с достаточным количеством пациентов для того, чтобы доказать эффективность МСК в комплексной терапии свищевой формы БК.
ГБУЗ "Московский клинический научно-практический центр" Департамента здравоохранения Москвы
ГБУЗ "Московский клинический научно-практический центр" Департамента здравоохранения Москвы
ГБУЗ "Московский клинический научно-практический центр" Департамента здравоохранения Москвы
ФГАОУ ВО «Российский университет дружбы народов» Министерства науки и высшего образования Российской Федерации, Москва, Россия
ГБУЗ "Московский клинический научно-практический центр" Департамента здравоохранения Москвы
Московский клинический научно-практический центр. ЦНИИ гастроэнтерологии Департамента здравоохранения Москвы
Болезнь Крона (БК) - хроническое воспалительное прогрессирующее заболевание желудочно-кишечного тракта с преимущественным поражением терминального отдела подвздошной кишки. В зависимости от течения различают 3 фенотипа (формы) БК: воспалительную, стенозирующую и пенетрирующую [1]. В большинстве случаев начальный этап БК характеризуется гранулематозным воспалением слизистой оболочки (СО) кишки, однако со временем у многих больных формируются стриктуры или свищи/фистулы как результат неконтролируемого прогрессирования воспалительного процесса в кишке [2].
В течение 20 лет у 88% пациентов развиваются стриктуры (18%) и свищи/фистулы (70%) [2]. Клиническое течение БК и темпы ее прогрессирования значительно варьируют у пациентов. У 43% больных заболевание начинается с тяжелого приступа, сменяющегося появлением относительно редких симптомов на протяжении последующих 10 лет [3]. Однако у 51% больных БК имеет хроническое течение (19%) или рецидивирующий характер (32%) [3]. Наблюдая исходную группу из 373 пациентов с БК, Р. Munkholm и соавт. [4] показали, что у 45% с активной формой заболевания в первые годы после возникновения оно сохраняется как активное хроническое состояние в течение последующего времени (период отдаленного наблюдения составлял 8 лет). Из этих пациентов у 50% течение заболевания носило перемежающий характер, и только спустя 8 лет у 5% пациентов отмечалась ремиссия БК.
Конечной целью лечения БК является заживление СО кишки, увеличение продолжительности ремиссии заболевания, уменьшение частоты и тяжести осложнений, при которых требуется госпитализация и хирургическое вмешательство и, как следствие, улучшение качества жизни больных. Эти цели могут быть достигнуты с помощью адекватной и своевременной противовоспалительной терапии 5.
Лечение пациентов с БК должно проводиться с учетом прогностических факторов прогрессирования заболевания. Согласно Консенсусу ЕССО (The European Crohn's and Colitis Organization) клиническое течение БК можно прогнозировать на основании клинических симптомов в момент установления диагноза, возраста пациентов, анамнеза, внекишечных проявлений, а также наличия стеноза и свищей. Данные показатели необходимо принимать во внимание при выборе начальной терапевтической тактики [8]. В нескольких исследованиях подтверждено, что молодой возраст (моложе 40 лет) и наличие перианальных свищей (ПС) могут служить предикторами неблагоприятного исхода заболевания и/или инвалидизации больных 11. ПС - наиболее распространенные и часто встречающиеся типы свищей при БК [12]. Они с трудом поддаются лечению, ухудшают качество жизни больного и повышают риск тотальной резекции кишки [12, 13].
ПС подразделяются на простые и сложные. К простым ПС относят неректовагинальные поверхностные, низкие интра- и транссфинктерные свищи, имеющие единственное наружное отверстие, без клинических признаков абсцедирования и острого воспалительного процесса в отсутствие стриктуры анального канала. В то же время к сложным относят любые формы (по отношению к анальному сфинктеру) высоких свищей с множественными наружными отверстиями, с признаками абсцедирования, ректовагинальные свищи, а также свищи со стриктурой анального канала. Кроме того, если при эндоскопической верификации диагноза определяется выраженный специфический проктит Крона, то данный свищ относится к категории сложного [14].
Согласно рекомендациям ГНЦК также целесообразно выделять 2 типа свищей прямой кишки, обусловленных особенностями этиопатогенеза БК.
1. Высокие (реже - низкие) свищи, обусловленные грануломатозным процессом, при котором внутреннее отверстие возникает на фоне активного неспецифического деструктивного процесса из язв-трещин.
2. Низкие (банальные) свищи, исходящие из области крипт Морганьи, развитие которых связано с инфицированием анальных желез через крипты или поврежденную кожу анального канала на фоне БК.
В настоящее время свищевая форма БК служит показанием к назначению биологической терапии генно-инженерными биологическими препаратами (ГИБП) в момент установления диагноза (терапия «top-down»).
Клиническое исследование по оценке эффективности инфликсимаба для лечения пациентов со свищевой формой БК (АССЕNТ II) продемонстрировало эффективное действие этого препарата при данной форме заболевания. Включенные в это рандомизированное двойное слепое контролируемое исследование 306 взрослых пациентов с БК, имевших один или несколько дренирующих абдоминальных свищей или ПС, при продолжительности заболевания по меньшей мере 3 мес были рандомизированы для введения инфликсимаба по схеме 0, 2 и 6-я неделя. На введение инфликсимаба ответили (закрытие 50% дренирующих свищей) 195 (65%) из 282 пациентов. Спустя 14 нед эти пациенты были произвольно распределены на группы для получения поддерживающих доз плацебо (n=99) или поддерживающей терапии инфликсимабом (n=96). Пациенты, которые исходно не реагировали на инфликсимаб (n=87), также были разделены на группы для получения поддерживающих доз инфликсимаба (n=43) или плацебо (n=44) вплоть до 54-й недели после начала исследования [15]. К 54-й неделе число пациентов, у которых уменьшилось количество свищей, среди получавших инфликсимаб было достоверно больше, чем в группе плацебо: соответственно 46 и 23% (р=0,001). Сходная эффективность отмечалась у пациентов с полной ремиссией (отсутствие дренирующих свищей) - 36 и 23% соответственно (р=0,009) [15]. Исследование АССЕNТ II показало также, что терапия инфликсимабом значительно уменьшает частоту госпитализаций и хирургических вмешательств у больных со свищевой формой БК. Несмотря на значительный эффект от биологической (антицитокиновой) терапии свищевой формы БК, которая характеризуется рецидивирующим и агрессивным течением, лечение больных данной категории остается трудной задачей, сохраняется высокий риск развития рецидива БК. Данное обстоятельство обусловливает необходимость поиска новых подходов и методов консервативной терапии свищевой формы БК [16].
Мезенхимальные стволовые клетки (МСК), обладающие иммуномодулирующими свойствами и большим регенеративным потенциалом, также применяются для лечения свищевой формы БК и ПС [17].
В другом исследовании 10 пациентам с рефрактерной формой БК, у которых имелись ПС, местно в зону свищей были введены аутологичные МСК КМ с интервалом 4 нед [18]. Каждый пациент получил в среднем 4 инъекции по 20 млн МСК. У всех больных наблюдалось одновременное снижение ИАБК и ИПАБК, сопровождающееся заживлением СО прямой кишки.
Ряд исследований демонстрирует, что существуют различия по эффективности между системным и местным введением МСК для лечения свищевой формы БК. В экспериментальной модели колита Е. Gonzalez-Rey и соавт. [21] показали, что МСК, полученные из жировой ткани, при внутрибрюшинном введении мигрируют по принципу «хоуминга», именно в зону воспаления толстой кишки. М. Duijvestein и соавт. [22] наблюдали аналогичный эффект «хоуминга» с использованием МСК КМ человека при системном введении. Тем не менее лишь небольшое количество меченых МСК обнаружено в воспаленном кишечнике при системном введении культуры клеток. Считается, что внутривенное введение МСК оказывает системный иммуномодулирующий эффект, в итоге способствуя восстановлению поврежденных тканей. При местном введении МСК бо'льшее количество клеток достигает поврежденных тканей по сравнению с системным введением, что, вероятно, обеспечивает более интенсивную регенерацию тканей благодаря наличию высокой концентрации растворимых факторов роста в зоне повреждения.
Приводим собственный клинический опыт, демонстрирующий эффективность местного введения МСК у больной со свищевой формой БК.
Больная П., 1974 года рождения считает себя больной с октября 2007 г., когда появились боли в животе без четкой локализации, жидкий стул с примесью слизи и крови, выделение гноя из заднего прохода, боли в локтевых и коленных суставах. Госпитализирована в Главный военный клинический госпиталь им. Н.Н.Бурденко. При ирригоскопии в нисходящем отделе ободочной кишки выявлено циркулярное сужение просвета до 1,5 см на протяжении 2,5 см. По данным колоноскопии: СО терминального отдела подвздошной кишки отечная, розовая. Баугиниева заслонка зияет. СО ободочной кишки с многочисленными продольными, щелевидными язвами и поперечными трещинами, бугристая, имеет вид «булыжной мостовой». В сигмовидной кишке - участок сужения с циркулярным отеком. В нижнеампулярном отделе прямой кишки на переднеправой стенке определяется отверстие свищевого хода на расстоянии 4 см от ануса, СО вокруг свища умеренно инфильтрирована, при надавливании выделяется гноевидное отделяемое.
Ано- и ректосигмоскопия: справа от анального канала виден свищевой ход, при надавливании определяется умеренная болезненность, выделяется гноевидное отделяемое. Зонд, введенный в наружное свищевое отверстие, свободно проходит в просвет кишки через внутреннее отверстие. Ректоскоп введен на 16 см, катаральный сфинктерит, умеренная гиперемия СО на всем протяжении. Сосудистый рисунок смазан, контактной кровоточивости нет. На уровне 3 см от заднего прохода определяется ректовагинальный свищ, подтвержденный с помощью пробы с 1% раствором метиленового синего.
Таким образом, согласно классификации, предложенной Американской ассоциацией гастроэнтерологов [23], у больной имелись простой ПС с единственным наружным отверстием и сложный ректовагинальный свищ.
Установлен диагноз: БК толстой кишки, осложненная хроническим ректовагинальным свищом и наружным ПС, хроническое непрерывное течение, высокая активность. Внекишечные проявления - полиартрит.
Назначена антибактериальная терапия: метронидазол 1 г/сут и ципрофлоксацин 1 г/сут, а также буденофальк 18 мг/сут. Отмечена положительная динамика: боли в животе и суставах уменьшились, стул полуоформленный, до 4 раз в сутки с незначительным количеством слизи, из свища также отмечалось умеренное выделение слизи. Пациентка самостоятельно отменила прием буденофалька и через 2 мес наступил рецидив: вновь появились боли в животе, диарея до 15 раз в сутки с примесью слизи и крови. В марте 2008 г. больная повторно госпитализирована в ГВКГ им. Н.Н. Бурденко. Проведена комплексная терапия с применением преднизолона, антибактериальных препаратов - метронидазол и ципрофлоксацин, коррекция белково-энергетических нарушений. Достигнута ремиссия заболевания. Выписана с рекомендацией принимать азатиоприн 2,5 мг на 1 кг массы тела. В октябре 2008 г. - повторная госпитализация в ГВКГ им. Н.Н. Бурденко в связи с рецидивом заболевания. С учетом непрерывного характера течения, внекишечных проявлений (полиартрит), наличия ректовагинального свища, ПС и стеноза сигмовидной кишки проведен индукционный курс инфликсимабом в дозе 5 мг/кг. В ноябре 2008 г. госпитализирована в ЦНИИ гастроэнтерологии для дальнейшего продолжения лечения инфликсимабом. ИАБК на момент поступления составил 343 балла. Уровень С-реактивного белка 46,6 мкм/л. Отмечалось слизистое и гнойное отделяемое из свищевого хода, ощущала дискомфорт в зоне свища, умеренное уплотнение в области наружного отверстия свищевого хода, значительное ограничение половой активности. ИАПБК 12 баллов. На фоне терапии инфликсимабом в дозе 5 мг/кг в комбинации с азатиоприном 2,5 мг/кг достигнута ремиссия заболевания - ИАБК составил 126 баллов, ИПАБК снизился до 5 баллов.
В августе 2009 г. во время очередного введения инфликсимаба проведена контрольная колоноскопия. СО подвздошной кишки отечная, розовая. СО ободочной кишки с многочисленными псевдополипами. В нижнеампулярном отделе по переднеправой стенке - отверстие свищевого хода диаметром 1 мм на расстоянии 4 см от ануса, СО вокруг хода умеренно гиперемирована и инфильтрирована, при надавливании выделяется серозное отделяемое.
Ано- и ректосигмоскопия: справа от анального канала виден свищевой ход, при надавливании выделяется серозное отделяемое. Ректоскоп введен на 18 см, умеренная гиперемия СО на всем протяжении. Контактная кровоточивость отсутствует. Сосудистый рисунок стушеван. На уровне 3 см от заднего прохода - ректовагинальный свищ.
В октябре 2009 г. после перенесенной ОРВИ появились диарея до 7-10 раз в сутки, схваткообразные боли внизу живота в вечерние часы и ночью, вздутие живота, лихорадка до 37,5-37,8 °С по вечерам, боли в коленных суставах, гнойное выделение из свищевого хода. Самостоятельно начала принимать преднизолон 20 мг/сут, продолжая принимать азатиоприн 100 мг/сут.
В связи с обострением заболевания на фоне биологической терапии увеличена доза инфликсимаба до 10 мг/кг. В комбинации с антицитокиновой терапией дважды выполнено системное введение 200 млн аллогенных МСК КМ. Состояние больной улучшилось - стул полуоформленный, не более 3-4 раз в сутки, без патологических примесей; масса тела увеличилась на 7 кг, стихли боли в животе, температура тела нормализовалась, уменьшилось выделение слизи из свищевого хода.
На протяжении 2010-2011 гг. продолжалась поддерживающая терапия инфликсимабом в дозе 10 мг/кг в комбинации с азатиоприном 2,5 мг/кг, обеспечивающая ремиссию: ИАБК находился в диапазоне от 98 до 120 баллов, уровень С-реактивного белка - 2,0-8,6 мкм/л. Количество отделяемого из свища уменьшилось более чем на 50%, что могло быть расценено в соответствии с данными литературы, как «ответ на терапию» [24], хотя полного заживления свища не наступило.
В марте 2012 г. при осмотре анальной области справа вокруг анального канала отмечалась болезненная припухлость и виден свищевой ход, вокруг свищевого хода мацерация кожных покровов, мокнутие и экскориации, при надавливании выделялось слизистое отделяемое. СО прямой и дистального отдела сигмовидной кишки гиперемирована, контактная кровоточивость отсутствовала. ИПАБК 8 баллов.
20.03 проведена лечебно-диагностическая колоноскопия. СО подвздошной кишки розовая, умеренно отечна. СО кишки с множественными псевдополипами во всех отделах, язв и эрозий нет. На расстоянии 3-4 см от ануса (см. рисунок, а на цв. вклейке) в нижнеампулярном отделе по переднеправой стенке определяется отверстие свищевого хода. Рисунок 1. Данные колонофиброскопии у больной П., 38 лет. а - внутреннее отверстие свищевого хода в нижнеампулярном отделе прямой кишки до введения МСК. По периметру свищевого хода осуществлено введение 40 млн МСК - 4 точки вкола по 1 мл изотонического раствора натрия хлорида, содержащего 10 млн МСК. Через 4 и 8 нед больной повторно введено по 40 млн МСК в область свища. Через 12 нед проведена контрольная ано- и ректосигмоскопия. При осмотре анальной области отмечено закрытие наружного отверстия свища. Кожа в области бывшего свищевого хода изменена минимально - снижен тургор. При эндоанальном ультразвуковом исследовании и ректоскопии свищевой ход не определялся (см. рисунок, б на цв. вклейке). Рисунок 1. Данные колонофиброскопии у больной П., 38 лет. б - заживший свищ прямой кишки через 12 нед после введения МСК. Таким образом, зафиксировано полное заживления свища. ИПАБК 3 балла.
Следует отметить, что, несмотря на лечение, у больной сохраняется ректовагинальный свищ.
Приведенное клиническое наблюдение демонстрирует сложности лечения перианальной БК, которое должно осуществляться совместно гастроэнтерологом и эндоскопистом. Несмотря на полный объем медикаментозной терапии перианальной БК, проводимой в соответствии с рекомендуемым алгоритмом [25], заживления свища удалось достигнуть лишь после нескольких местных введений МСК. Тем не менее, чтобы доказать эффективность МСК в комплексной терапии свищевой формы БК, необходимы рандомизированные контролируемые исследования с участием достаточного числа пациентов.
УЗИ — ультразвуковое исследование
ФКП — фекальный кальпротектин
ЯК — язвенный колит
ANCA — антинейтрофильные эндоплазматические антитела
ASCA — антитела к Saccharomyces cerevisiae
α-ФНО — α-фактор некроза опухоли

В 1932 г. Беррилл Бернард Крон (рис. 1) Рисунок 1. Беррилл Бернард Крон (1884—1983). описал и представил американской Медицинской ассоциации 14 больных под рубрикой «Терминальный илеит: новый клинический синдром». В том же году он в соавторстве с коллегами Леоном Гинзбергом и Гордоном Оппенгеймером опубликовал статью «Региональный илеит: патологическая и клиническая сущность». В этих работах был впервые описан терминальный илеит, получивший в дальнейшем имя Б. Крона. Клинические и патологические проявления болезни соответствовали современным представлениям. В последствии оказалось, что болезнь Крона (БК) может локализоваться во всех отделах желудочно-кишечного тракта (ЖКТ). Она характеризуется разнообразными кишечными и внекишечными проявлениями, которые зависят от глубины, протяженности пораженного органа и особенностей иммунных (системных) осложнений.
Распространенность. Заболеваемость БК имеет тенденцию к повышению. Это особенно заметно в странах с высокоразвитой индустрией. В конце прошлого века заболеваемость находилась в пределах от 0,7 до 14,6 на 100 000 населения в год, а в настоящее время в США и Европе достигает 67,1—149 на 100 000 [1]. Результаты эпидемиологических наблюдений дают основания полагать, что в регионах Москвы, Санкт-Петербурга и других крупных городов Российской Федерации заболеваемость воспалительными заболеваниями кишечника — ВЗК (язвенным колитом и БК) сопоставима с заболеваемостью в США и Европе.
Этиология и патогенез. Этиология БК неизвестна, но со времени ее описания и до сих пор актуален вопрос об участии микрофлоры. Так, вновь обсуждается роль одной из разновидностей микобактерии паратуберкулеза (Mycobacterium avium subspecies paratuberculosis), которая вызывает похожую болезнь у рогатого скота [2]. Ген NOD2, ответственный за генетическую восприимчивость БК, подавляет способность макрофагов поглощать эти микроорганизмы, подавляет ответ врожденной и адаптивной иммунной системы на внутриклеточную инвазию микобактерий паратуберкулеза. У лиц, генетически предрасположенных к инфекциям Mycobacterium avium subsp., повышен риск развития БК. Макрофаги, пораженные микобактериями, усиленно экспрессируют α-фактор некроза опухоли (α-ФНО) [3].
В предрасположенности к БК имеют значение и генетически детерминированные дефекты барьерной функции кишечного эпителия, облегчающие проникновение бактериальных антигенов. Ген, ответственный за восприимчивость к БК, с помощью внутриклеточного белка NOD2/CARD15 реагирует на присутствие бактериальных антигенов. Бактериальные антигены вызывают иммунный ответ T-лимфоцитов CD4+. Активируются цитокины α-ФНО, интерферон-γ, интерлейкин-4, 13, 23, 27 и 3, инициирующие воспалительный процесс [4].
Определенное значение в патогенезе БК придают факторам окружающей среды. Рост заболеваемости БК в индустриальных странах мира уже давно и не без оснований связывают с загрязнением окружающей среды, воды и воздуха, ранним переводом грудных детей на искусственное вскармливание, увеличенным потреблением углеводов, животного и молочного белка, увеличенным соотношением ω-6 и ω-3 полиненасыщенных жирных кислот в пище. Люди, употребляющие преимущественно белки растительного происхождения, реже болеют БК. Риск развития БК увеличивают курение и гормональная контрацепция, а также чрезмерно тщательное соблюдение личной гигиены, снижающее активность Т-хелперов 2-го типа, обеспечивающих защиту от инфекций и увеличивающее риск развития ВЗК.
Классификация. Европейским обществом по изучению ВЗК (ECCO) рекомендована Венская классификация БК (1998) с Монреальской модификацией (2005). Выделены варианты БК в зависимости от возраста больного (А), локализации процесса (L) и фенотипа заболевания (B). Время установления окончательного диагноза: A1 — 16 лет или младше; А2 — 17 — 40 лет; А3 — старше 40 лет. У большинства БК устанавливают в возрасте 17—40 лет (А2). Локализация воспалительного процесса: L1 — терминальный илеит; L2 — колит; L3 — илеоколит; L4 — верхний отдел ЖКТ проксимальнее терминального отдела. БК в форме илеита (L1) возникает примерно у 45%, в форме илеоколита (L3) — у 19%, в форме колита (L2) — у 32% и в верхнем отделе ЖКТ (L4) — у 4% [5].
Фенотип (форма) заболевания: В1 — воспалительная (люминальная) форма; B2 — cтенозирующая форма; B3 — пенетрирующая, или свищевая (экстралюминальная), форма (возникновение межкишечных и иных свищей, абсцессов и инфильтратов в брюшной полости), В3p — перианальная форма. Кроме того, с перианальным поражением может сочетаться каждый из фенотипов БК.
Степень тяжести (активность) БК оценивают в баллах. Индекс активности болезни Крона (ИАБК) менее 150 баллов — ремиссия, 150—220 баллов — легкая, 220—450 баллов — умеренная, более 450 баллов — высокая активность. Новейшие исследования показывают, что клинические критерии ремиссии совпадают с эндоскопическими лишь у 1 /5 больных [6]. У остальных больных при колоноскопии (КФС) и илеоскопии наблюдаются признаки воспаления. Поэтому для оценки надежности ремиссии и принятия решения об изменении лечебной тактики уже используют высокочувствительные биомаркеры воспаления — C-реактивный белок (СРБ), фекальный кальпротектин (ФКП) и лактоферритин (ЛФ). Эндоскопический контроль ремиссии оценивают с помощью конфокального лазерного эндомикроскопа. Он дает возможность получить увеличенное изображение слизистой оболочки (СО) и ее сканограмму на глубине до 250 мкм.
Патоморфология. Для БК в отличие от язвенного колита (ЯК), характерно поражение всех слоев кишечной стенки. Особенностью является также мозаичность поражения с формированием четких границ с неповрежденными сегментами кишки. При гистологическом исследовании биоптатов СО пораженной кишки воспаление характеризуется очаговой инфильтрацией нейтрофилами поверхностного эпителия с развитием абсцессов в криптах. В собственной пластинке и более глубоких отделах стенка кишки инфильтрирована лимфоидными клетками. Инфильтрация стенки кишки лимфоидными клетками настолько массивная, что делает рельеф кишки неровным, получившим название «булыжная мостовая». В инфильтрате образуются гранулемы вокруг гигантских клеток Лангханса макрофагального происхождения — характерный признак гранулематозного воспаления. В отличие от туберкулезных и других инфекционных гранулем в них отсутствуют очаги казеозного некроза. Гранулематозное воспаление при БК возникает в подслизистой основе, постепенно распространяется как в сторону СО, так и серозной оболочки кишки, вызывает сужение просвета и/или пенетрацию кишки с образованием свищей. Гранулемы обнаруживают, как правило, только в операционном материале, так как биоптаты, получаемые во время внутрипросветной эндоскопии, ограничиваются только СО. При БК тонкой кишки в биоптатах также можно видеть признаки хронического повреждения СО, укорочение ворсинок, метаплазию эпителия, в частности клеток Панета, являющихся регуляторами кишечной микробиоты.
Клиническая картина. Клинические проявления БК зависят от фенотипа и локализации БК.
Воспалительная (люминальная) форма долгое время ограничивается преимущественно подслизистой основой кишки. Длительное время протекает с неопределенными болями в животе и внекишечными манифестациями (эпизоды немотивированной лихорадки, боли в суставах, узловатая эритема и др.). Заболевание может оставаться неустановленным много лет. Если БК начинается в детстве, то больной отстает в физическом развитии. Первыми клиническими проявлениями болезни служат лихорадка, увеличенная СОЭ, лейкоцитоз и другие симптомы воспалительного заболевания. По мере распространения воспаления на СО, мышечную и серозную оболочки появляются хроническая диарея, кишечные кровотечения, приступообразные боли, свидетельствующие об изъязвлении и сужении пораженного сегмента кишки. Появляются симптомы мальабсорбции: анемия, гипопротеинемия, отеки и снижение массы тела. Иногда развивается картина непроходимости кишечника. Поражение пищевода, желудка и двенадцатиперстной кишки создает картину язвенной болезни, отличающейся множественностью язвенно-эрозивных поражений, резистентных к стандартной терапии. При локализации в аноректальной области образуются незаживающие трещины прямой кишки и парапроктиты.
Стенозирующая форма характеризуется симптомами непроходимости кишечника. В клинической картине преобладают приступообразные боли, чаще в правой подвздошной области, сопровождающиеся рвотой, вздутием живота, громким урчанием, переливанием с задержкой стула и газов. Появляется видимая на глаз перистальтика с периодически поднимающимися «валами». При пальпации живота иногда удается обнаружить инфильтрат в брюшной полости. Диагноз подтверждается при рентгенологическом исследовании или во время лапаротомии. СО приобретает неровный рельеф. Рубцовые изменения стенки приводят к сужению просвета кишки, развитию частичной и даже полной непроходимости кишечника.
Свищевая (экстралюминальная) форма отличается тяжелым течением, трансмуральным поражением стенки кишки с формированием межкишечных сращений, абсцессов и межпетлевых слепых и наружных кишечных свищей.
Внекишечные проявления. Внекишечные или системные проявления встречаются у большинства пациентов с БК. Аутоиммунные системные реакции и генетические нарушения возникают приблизительно у 25% больных.

К аутоиммунным относятся артриты, васкулиты, аутоиммунный гепатит, эписклерит, афтозный стоматит, узловая эритема, гангренозная пиодермия. Генетически детерминированные нарушения, связанные с HLA-B27, вызывают анкилозирующий спондилит и сакроилеит, увеит, первичный склерозирующий холангит. Внекишечные проявления, обусловленные мальабсорбцией (остеопороз, мочекаменная и желчнокаменная болезни, анемия, нарушения свертывания крови, тромбозы и др.), энтеропатией с потерей белка и/или амилоидозом (гипопротеинемия, гипоальбуминемия, отеки) появляются у большинства больных еюнитом и илеитом Крона. Внекишечные манифестации и аутоиммунные нарушения, возникающие при БК, в разное время описаны в литературе (см. таблицу).
Особенности течения. БК представляет собой рецидивирующее или непрерывно текущее заболевание, дающее спонтанную (без лечения) ремиссию у 30% больных.
У 50% из них продолжительность ремиссии может достигать 2 лет и более. Фенотипы БК не являются постоянными. При несвоевременном распознавании болезни и запоздалом начале ее лечения (через 3 года от времени появления первых симптомов или позднее) осложнения развиваются практически у всех больных. С течением времени стенка кишки подвергается фиброзу и изначально воспалительный тип трансформируется в стенозирующий или пенетрирующий. У некоторых больных сужение и свищи обнаруживают уже при первом обращении к врачу. У других воспалительный тип может продолжаться на протяжении десятилетий без сужений и свищей. J. Cosnes и соавт. [7] провели ретроспективное исследование эволюции БК у 2002 больных на протяжении 20 лет. У 84% из них была воспалительная (В1), у 4% — стенозирующая (В2) и у 12% — свищевая (В3) форма заболевания. В последующие годы у 60% больных с воспалительной формой БК наблюдалась тенденция к развитию стенозов и свищей. Из них у 79% течение болезни осложнилось свищами, а у 21% — стенозом. В целом через 20 лет воспалительная форма осталась лишь у 12% больных, свищи появились у 70%, стеноз — у 15%. Таким образом, у 60% больных возникает необходимость в хирургическом лечении, причем почти 50% из них нуждаются в повторной операции.
Методы диагностики. Визуализация пораженного участка ЖКТ осуществляется с помощью эндоскопического, рентгенологического и ультразвукового методов. Каждый из них имеет преимущества и недостатки и дополняют друг друга. Глубокая эндоскопия тонкой кишки и капсульная эндоскопия обладают очень высокой чувствительностью и специфичностью в обнаружении воспалительных проявлений СО кишечника. Более глубокие слои кишечной стенки доступны оценке при изображении кишки в поперечном сечении, позволяющем обнаружить стриктуры, свищи и абсцессы. Поэтому при БК одинаково важную роль играют как осмотр поверхности кишки, позволяющий увидеть афты, изменение рельефа и диаметра просвета кишки, доступные эндоскопическому методу, так и оценка толщины всей стенки кишки с помощью ультразвукового исследования (УЗИ), компьютерной томографии (КТ) и магнитно-резонансной томографии (МРТ), особенно с использованием контрастных растворов, введенных внутривенно.
Позитронно-эмиссионная томография (ПЭТ) с использованием меченной фтором-18 ФДГ (2-фтор-2-дезокси-D-глюкозы) является функциональным методом визуализации, который чувствителен к метаболизму глюкозы. ФДГ накапливается в местах активного воспалительного процесса в связи с гиперэкспрессией лейкоцитов в зоне переносчиков глюкозы и увеличением метаболической активности. С помощью ПЭТ можно определить воспаленные участки кишки и, что особенно важно, объективно оценить степень активности БК и определить конечную точку ремиссии, необходимую для оценки качества лечения. ПЭТ позволяет различить воспалительные и фиброзные стриктуры, т.е. связать результаты с адекватностью проводимой терапии, а также осуществить скрининг рака [8].
Предложены также серологические тесты, облегчающие диагностику и прогноз БК. Исследуют уровень антител к Saccharomyces cerevisiae (ASCA) и антинейтрофильных эндоплазматических антител (ANCA) [9]. Появление ASCA, а также антител к ламинарибиозиду [Glc(β1,3)Glb(β); ALCA], хитобиозиду (GlcNAc(β1,4) GlcNAc(β); ACCA], маннобиозиду [Man(α1,3)Man(α); AMCA], ламинарину [Glc(β1,3))3n(Glc(β1,6); anti-L] и хитину [(GlcNAc (β1,4)n; anti-C] характерно для БК, а уровень их повышения отражает тяжесть течения БК и прогноз [10].

На рис. 2 Рисунок 2. Алгоритм диагностики БК. представлен алгоритм диагностики БК с применением рентгенологических и эндоскопических методов.
БК следует предполагать в следующих случаях:
а) имеются клинические симптомы (приступообразная боль в животе с задержкой стула и газов, вздутием живота и локализующаяся в правой подвздошной области, хроническая диарея (необязательно с кровью), пальпируемый инфильтрат (необязательно), парапроктит или хроническая трещина прямой кишки; б) наличие признаков воспалительного процесса (лихорадка, лейкоцитоз, повышенный уровень СРБ, ФКП и ЛФ); в) определяются внекишечные манифестации и системные (аутоиммунные) нарушения (см. таблицу).
Исследование следует начинать с проктологического осмотра и ректороманоскопии. Затем независимо от результатов нужно выполнить рентгенологическое исследование с тугим заполнением контрастной взвесью толстой кишки и дистального отдела подвздошной кишки. Третий этап — КФС с илеоскопией. С помощью этих исследований устанавливают колит Крона (L2) и илеоколит (L3).
Четвертый этап предназначен для диагностики БК тонкой кишки (L1), пищевода и желудка (L4) и также является обязательным вне зависимости от результатов предыдущих этапов. Больному выполняют рентгенологическое исследование тонкой кишки и при возможности — глубокую антеградную энтероскопию и видеокапсульную энтероскопию (в отсутствие признаков стеноза при эндоскопии). Исследование с помощью видеокапсулы позволяет визуализировать минимально выраженные повреждения СО тонкой кишки.
Дифференциальный диагноз. В основе решения диагностической концепции БК лежит сложный дифференциально-диагностический поиск, в ходе которого должны быть обсуждены многие болезни, сопровождающиеся эрозивно-язвенными поражениями тонкой и толстой кишки, указанными ниже.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Болезнь Крона: причины появления, классификация, симптомы, диагностика и способы лечения.
Определение
Болезнь Крона – это хроническое воспалительное заболевание желудочно-кишечного тракта, для которого характерно чередование периодов ремиссии (хорошего самочувствия) и рецидивов (острых состояний). Воспалительный процесс может возникать в любом отделе ЖКТ - от ротовой полости до анального отверстия, но наиболее распространенной областью поражения является окончание подвздошной кишки и толстая кишка.
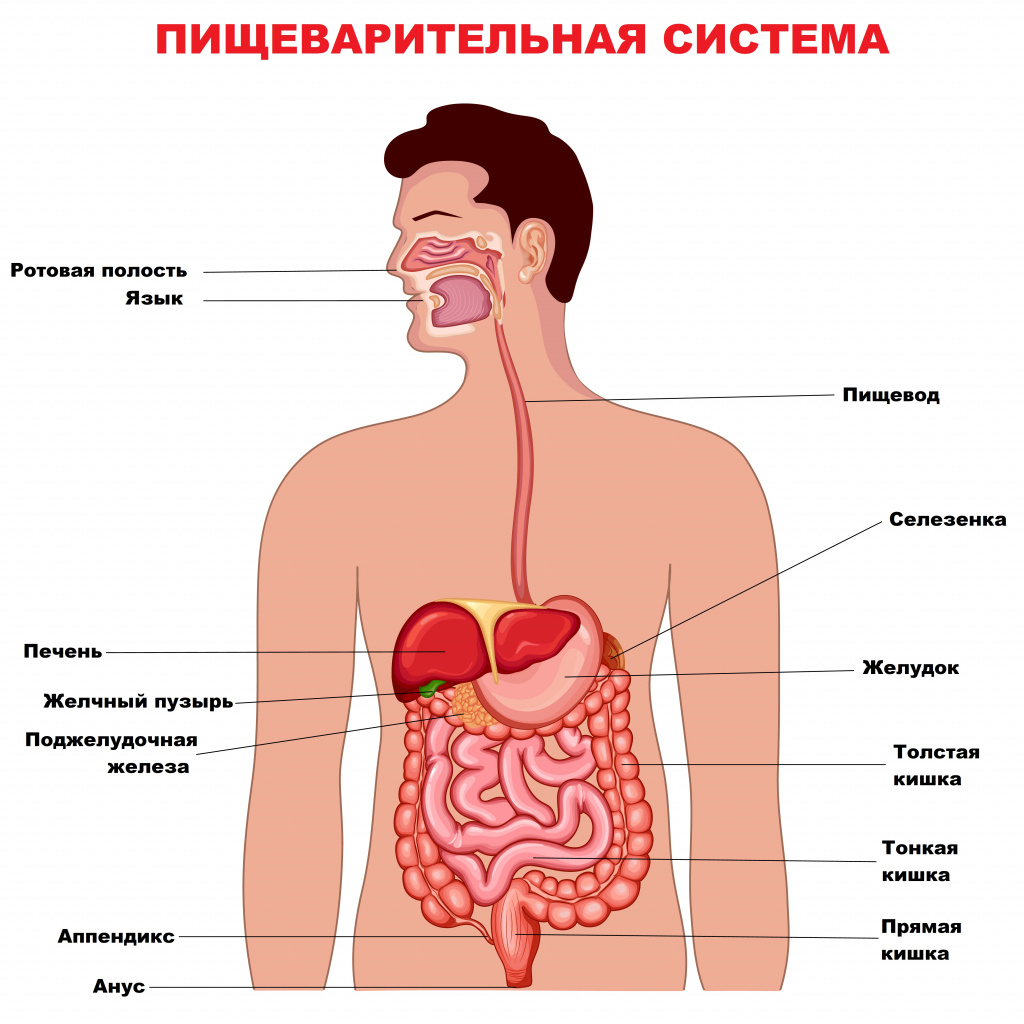
Полностью излечиться от болезни Крона нельзя, но правильно подобранная терапия может значительно уменьшить симптомы заболевания и привести к длительной ремиссии.
Причины появления болезни Крона
Несмотря на множество исследований, до сих пор точная причина возникновения болезни Крона не установлена.
В настоящее время предполагается, что болезнь Крона вызывают следующие провоцирующие факторы:
- Генетическая предрасположенность.
- Патологическая реакция иммунной системы на определенные бактерии, присутствующие в кишечнике.
- Кишечные вирусы.
- Питание с преобладанием фастфуда и жареной пищи.
- Табакокурение.
- Стрессовое воздействие.
- болезнь Крона чаще встречается у жителей городов развитых стран;
- заболевание чаще выявляется у людей европеоидной расы;
- болезнь может начаться в любом возрасте, но обычно манифестирует в период 10-40 лет.
- локализованную форму - поражение протяженностью менее 30 см;
- распространенную форму - поражение протяженностью более 100 см.
- конечный отдел подвздошной кишки;
- илеоцекальный отдел кишечника (место перехода тонкой кишки в толстую);
- толстый отдел кишечника (колит), в том числе прямая кишка;
- тонкая кишка (илеит);
- другие локализации (пищевод, желудок);
- редкие локализации (ротовая полость, губы, язык) в сочетании с поражением кишечника;
- одновременное поражение толстой и тонкой кишки (илеоколит).
- острое течение (менее 6 месяцев от начала заболевания);
- хроническое непрерывное течение (периоды ремиссии продолжительностью менее 6 месяцев на фоне адекватной терапии);
- хроническое рецидивирующее течение (периоды ремиссии продолжительностью более 6 месяцев).
- воспалительную форму (без образования сужений кишечника и отверстий в стенке кишки);
- стенозирующая (с образованием сужений в кишечнике и симптомами непроходимости);
- пенетрирующая (с образованием свищей и свищевых ходов в кишечнике);
- перианальная (поражения кожи наблюдаются в области ануса, свищи, язвы, абсцессы в этой области).
- меньше 150 баллов - неактивная болезнь Крона (клиническая ремиссия);
- 150–300 баллов - заболевание низкой активности (легкое);
- 301–450 баллов - заболевание умеренной активности (средней тяжести);
- больше 450 баллов – заболевание высокой активности (тяжелое).
Признаки и симптомы болезни Крона могут варьировать от легких до тяжелых. Обычно они развиваются постепенно, но иногда появляются внезапно, без предпосылок. В периоды ремиссии симптомы выражены слабо или совсем отсутствуют.
В активный период могут отмечаться следующие симптомы болезни Крона:
- диарея;
- лихорадка;
- хроническая усталость;
- чувство тяжести и/или распирания в животе;
- боли в животе и спазмы;
- примесь крови в стуле;
- язвочки в ротовой полости;
- снижение аппетита и потеря веса;
- боль в области заднего прохода.
- воспаление кожи в виде болезненных подкожных узелков, чаще всего в области голеней (узловатая эритема), гнойничков или язв (гангренозная пиодермия);
- поражение глаз, сопровождающееся сильной болью, слезотечением, снижением остроты зрения;
- воспаление суставов;
- воспаление печени или желчных протоков (склерозирующий холангит);
- тромбозы вен нижних конечностей, тромбоэмболию легочной артерии;
- задержку роста или полового развития у детей.
Лабораторно-инструментальное обследование может включать:
-
Клинический анализ крови с развернутой лейкоцитарной формулой для выявления воспалительных процессов.
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Читайте также:

