Радиационные ожоги что это такое
Обновлено: 24.04.2024
Хиросима, Нагасаки, Чернобыль – это черные страницы в истории человечества, связанные с атомными взрывами. Среди пострадавшего населения наблюдались негативные радиационные эффекты. Влияние ионизирующего излучения имеет острый характер, когда в течение короткого времени разрушается организм и наступает смерть, или хронический (облучение небольшими дозами). Третий вид влияния – долгосрочный. Он вызывает генетические последствия радиации.
Воздействие ионизирующих частиц бывает разное. В небольших дозах радиоактивное излучение применяют в медицине для борьбы с онкологией. Но почти всегда оно негативно влияет на здоровье. Малые дозы атомных частиц являются катализаторами (ускорителями) развития рака и поломки генетического материала. Большие дозы приводят к частичной или полной гибели клеток, тканей и всего организма. Сложность в контроле и отслеживании патологических изменений заключается в том, что при получении малых доз радиации симптомы отсутствуют. Последствия могут проявляться через годы и даже десятилетия.
Радиационные эффекты облучения людей имеют такие последствия:
- Мутации.
- Раковые заболевания щитовидной железы, лейкозы, молочной железы, легких, желудка, кишечника.
- Наследственные нарушения и генетического кода.
- Нарушение обмена веществ и гормонального равновесия.
- Поражение органов зрения (катаракта), нервов, кровеносных и лимфатических сосудов.
- Ускоренное старение организма.
- Стерильность яичников у женщин.
- Слабоумие.
- Нарушение психического и умственного развития.
Пути и степень облучения
Облучение человека происходит двумя путями – внешним и внутренним.
Внешняя радиация, которую получает организм, исходит от излучающих объектов:

- космос;
- радиоактивные отходы;
- испытания ядерного оружия;
- естественная радиация атмосферы и грунта;
- аварии и утечки на атомных реакторах.
Внутреннее облучение радиацией осуществляется изнутри организма. Радиационные частицы содержатся в пищевых продуктах, которые человек употребляет (до 97%), и в небольшом количестве в воде и воздухе. Для того чтобы понять, что происходит с человеком после облучения радиацией, нужно понимать механизм ее воздействия.
Мощное излучение вызывает в организме процесс ионизации. Это значит, что в клетках образуются свободные радикалы – атомы, у которых не хватает электрона. Чтобы восполнить недостающую частицу, свободные радикалы отбирают ее у соседних атомов. Так возникает цепная реакция. Этот процесс приводит к нарушению целостности молекул ДНК и клеток. Как результат – развитие атипичных клеток (раковых), массовая гибель клеток, генетические мутации.
Дозы облучения в Гр (грей) и их последствия:

- 0,0007-0,002 – норма получения организмом радиации за год;
- 0,05 – предельно допустимая доза для человека;
- 0,1 – доза, при которой риск развития генных мутаций удваивается;
- 0,25 – максимально допустимая однократная доза в чрезвычайных условиях;
- 1,0 – развитие острой лучевой болезни;
- 3-5 – ½ пострадавших от радиации погибает в течение первых двух месяцев из-за поражения костного мозга и, как следствие, нарушения процесса кроветворения;
- 10-50 – летальный исход наступает через 10-14 дней из-за поражения ЖКТ (желудочно-кишечный тракт);
- 100 – смерть наступает в первые часы, иногда через 2-3 дня из-за повреждения ЦНС (центральная нервная система).
Классификация поражений при радиационном облучении
Облучение радиаций приводит к повреждению внутриклеточного аппарата и функций клеток, что впоследствии вызывает их гибель. Наиболее чувствительны клетки, которые быстро делятся – лейкоциты, эпителий кишечника, кожа, волосы, ногти. Более устойчивы к радиации гепатоциты (печень), кардиоциты (сердце) и нефроны (почки).
Радиационные эффекты облучения
- острая и хроническая лучевая болезнь;
- поражение глаз (катаракта);
- лучевые ожоги;
- атрофия и уплотнение облученных участков кожи, сосудов, легких;
- фиброз (разрастание) и склероз (замена соединительной структурой) мягких тканей;
- уменьшения количественного состава клеток;
- дисфункция фибробластов (матрица клетки, основа при ее появлении и развитии).

- опухоли внутренних органов;
- злокачественные изменения крови;
- умственная отсталость;
- врожденные уродства и аномалии развития;
- рак у плода вследствие его облучения;
- сокращение продолжительности жизни.
- изменение наследственности;
- доминантные и рецессивные мутации генов;
- хромосомные перестройки (изменение числа и структуры хромосом).
Симптомы радиационного поражения
Симптомы облучения радиацией зависят в первую очередь от радиоактивной дозы, а также от площади поражения и продолжительности однократного воздействия. Дети более восприимчивы к радиации. Если у человека есть такие внутренние болезни, как сахарный диабет, аутоиммунные патологии (ревматоидный артрит, красная волчанка), это усугубит влияние радиоактивных частиц.
Однократная радиационная доза наносит большую травму, чем такая же доза, но полученная в течение нескольких дней, недель или месяцев.
При однократном воздействии большой дозы или при поражении обширной площади кожи развиваются патологические синдромы.
Цереброваскулярный синдром
Это признаки облучения радиацией, связанные с поражением сосудов головного мозга и нарушением мозгового кровообращения. Просвет сосудов сужается, поступление кислорода и глюкозы в мозг ограничивается.

- кровоизлияния в мозжечок – рвота, головная боль, нарушение координации, косоглазие в сторону поражения;
- кровоизлияние в мост – глаза не двигаются в стороны, расположены только посередине, зрачки не расширяются, реакция на свет слабая;
- кровоизлияние в таламус – полный паралич половины тела, зрачки не реагируют на свет, глаза опущены к носу, исход всегда летальный;
- кровоизлияние субарахноидальное – резкие интенсивные боли в голове, усиливающиеся при любых физических движениях, рвота, лихорадка, изменение ритмов сердца, скопление жидкости в мозге с последующим отеком, эпилептические припадки, повторные кровоизлияния;
- тромботический инсульт – нарушение чувствительности, отклонение глаз к очагу поражения, недержание мочи, нарушение координации и целенаправленности движений, психическая заторможенность, устойчивое повторение фраз или движений, амнезия.
Гастроинтестинальный синдром
- тошнота, снижение аппетита, рвота;
- вздутие живота, интенсивная диарея;
- нарушение водно-солевого баланса.
Впоследствии развивается некроз – омертвение слизистой кишечника, далее сепсис.
Синдром инфекционных осложнений
Это состояние развивается из-за нарушения формулы крови, как следствие, снижение естественного иммунитета. Возрастает риск экзогенной (внешней) инфекции.
Осложнения при лучевой болезни:

- ротовая полость – стоматит, гингивит;
- органы дыхания – тонзиллит, бронхит, пневмония;
- ЖКТ – энтерит;
- лучевой сепсис – усиливается гноеобразование, на коже и внутренних органах появляются гнойнички.
Орофарингеальный синдром
Это язвенное кровоточащее поражение мягких тканей ротовой и носовой полости. У пострадавшего отечная слизистая, щеки, язык. Десны становятся рыхлыми.
- сильная боль в ротовой полости, при глотании;
- продуцируется много вязкой слизи;
- нарушение дыхания;
- развитие пульмонита (поражение альвеол легких) – одышка, хрипы, вентиляционная недостаточность.
Геморрагический синдром
Определяет степень тяжести и исход лучевой болезни. Нарушается свертываемость крови, стенки сосудов становятся проницаемыми.
Симптомы – в легких случаях мелкие, точечные кровоизлияния во рту, в области заднего прохода, с внутренней стороны голеней. В тяжелых случаях радиационное облучение вызывает массивные кровотечения из десен, матки, желудка легких.
Радиационное поражение кожи
При небольших дозах развивается эритема – выраженное покраснение кожи из-за расширения кровеносных сосудов, позже наблюдаются некротические изменения. Спустя полгода после облучения появляется пигментация, разрастание соединительной ткани, появляются стойкие телеангиэктазии – расширение капилляров.
Кожа человека после радиации атрофируется, становится тонкой, легко повреждается при механическом воздействии. Лучевые ожоги кожи не поддаются лечению. Кожные покровы не заживают и очень болезненны.
Генетические мутации от воздействия радиации

Еще одни признаки радиационного облучения – это генные мутации, нарушение структуры ДНК, а именно одно его звена. Такое ничтожное, на первый взгляд, изменение приводит к серьезным последствиям. Генные мутации необратимо изменяют состояние организма и в большинстве случаев приводят к его гибели. Мутантный ген вызывает такие заболевания – дальтонизм, идиопатия, альбинизм. Проявляются в первом поколении.
Хромосомные мутации – изменение размеров, количества и организации хромосом. Происходит перестройка их участков. Они напрямую влияют на рост, развитие и функциональность внутренних органов. Носители хромосомных поломок погибают в детском возрасте.
Последствия облучения радиацией в глобальном масштабе:
- Падение рождаемости, ухудшение демографической ситуации.
- Стремительный рост онкологической патологии среди населения.
- Тенденция к ухудшению здоровья детей.
- Серьезные нарушения иммунного статуса среди детского населения, которое находится в зонах влияния радиации.
- Заметное сокращение показателей средней продолжительности жизни.
- Генетические сбои и мутации.
Значительная часть изменений, вызванная влиянием радиоактивных частиц, является необратимой.
Риск возникновения рака после облучения прямо пропорционален дозе облучения. Радиация даже в минимальных дозах негативно сказывается на самочувствии и работе внутренних органов. Люди часто списывают свое состояние на синдром хронической усталости. Поэтому после диагностических или лечебных мероприятий, связанных с облучением, необходимо принимать меры по ее выведению из организма и укреплять иммунитет.
Кожа при общем лучевом воздействии. Заживление лучевых ожогов
Что касается поражения кожи при общем воздействии излучении с большой энергией (гамма-лучи, быстрые нейтроны), то возникновение в таких случаях грубых некробиотических и деструктивных изменений в подкожной клетчатке и скелетных мышцах препятствует формированию оптимальных условий для эпителизацпи и развития грануляционной ткани.
Как было установлено В. В. Шиходыровым (1958, 1960), даже при равномерном облучении рентгеновскими лучами в минимальной смертельной дозе происходит длительное угнетение пролиферации и дифференцировки фибробластов, и тем самым нарушается образование полноценной соединительной ткани.
Особенно неблагоприятные условия для рубцевания и эпителизации создаются при неравномерном гамма-нейтронном или нейтронном облучении в зонах наибольшего непосредственного воздействия излучения. В таких местах, как указывалось выше, наступает полная гибель мягких тканей по типу восковидного некроза, и таким образом полностью исключается трофическая связь вновь, образованного эпителия с подлежащими тканями.
Тем не менее, несмотря на прогрессирование местных структурных изменений и общее глубокое подавление репарационных процессов в облученном организме, пролиферация эпителия по краям некротически-язвенных дефектов кожи начинается уже в период разгара лучевого заболевания. Макроскопически это проявляется в виде возникновения отдельных небольших белесоватых бляшек и валиков по краям язвенного дефекта из вновь образованного эпителия.

Кроме специфических моментов, связанных с особенностями действия того или иного вида ионизирующих излучений и условиями их воздействия, исход лучевых поражений кожи в такой же мере зависит и от общих причин, определяющих заживление кожных дефектов любого происхождения. В частности, немаловажное значение имеют размеры пораженной поверхности тела, как в отношении общего токсического воздействия, так и возможности репарации.
Разбирая вопросы заживления лучевых поражений кожи, нельзя не упомянуть о развитии келоидов в исходе заживления комбинированных ожогов у пострадавших во время взрывов атомных бомб. Как известно, в таких случаях имело место сочетание воздействия на мягкие ткани лучистой энергии, световой вспышки и термического фактора. Через 6 мес после взрыва ожоги зажили у 94% пораженных людей, а спустя 10 мес и позже на месте ожогов образовались келоиды, причем больше всего их возникло у молодых людей [Tsuxuki M., 1956; Ilarda .Т., 1960].
В свое время были высказаны различные мнения о причине образования келоидов. Очевидно, что данную особенность нельзя считать характерной для лучевых ожогов. Достаточно напомнить об образовании обезображивающих рубцов на месте обширных термических ожогов кожи у танкистов или летчиков, полученных в горящих танках или самолетах в Великую Отечественную войну. Вероятнее всего, образование келоидов у пострадавших при атомных взрывах обусловлено длительным течением местного воспалительного процесса, присоединением инфекции, особенностями воспалительной реакции и развития грануляционной ткани в условиях лучевой болезни, неправильным лечением пострадавших.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Радиационное поражение в Чернобыле и его последствия
Взрыв и пожар на 4-м энергоблоке Чернобыльской атомной станции 26 апреля 1986 г. стали самой страшной со времен бомбардировки Хиросимы и Нагасаки ядерной катастрофой. Это касается числа пострадавших, тяжести проявления острой лучевой болезни и гибели людей от нее, огромной массы радиоактивных осадков, вырвавшихся из реактора и распространившихся в окружающую среду, беспрецедентных масштабов зараженной зоны.
Кроме того, речь идет и о колоссальной численности лиц, которым могут грозить отдаленные последствия облучения. Это было самой страшной аварией на коммерческой атомной электростанции за всю историю человечества и второй по счету, при которой произошло расплавление ядерного топлива. За 7 лет до этого в 1979 г. произошла первая подобная авария на о-ве Три-Майл.
а) Дозы облучения в Чернобыле. Согласно проведенной оценке, приблизительно 50 человек получили дозу выше 500 рад (5 Гр), приблизительно 100 человек — от 300 (3 Гр) до 500 рад и, возможно, еще 100 - от 100 (1 Гр) до 300 рад (R. P. Gale, в заявлении для московской прессы 6 июня 1986 г.).
Очень многие дети во время аварии получили относительно малые дозы облучения. Некоторые предварительные данные указывают, что у 80 000 детей лучевая нагрузка на щитовидную железу за счет радиоактивного йода составила менее 200 рем (2 Зв), у 12 000 — от 200 до 500 рем (от 2 до 5 Зв), у 4000 — более 500 рем (5 Зв).
б) Радионуклиды. Заражение произошло в основном йодом-131 и -132, цезием-134 и -137, ниобием-95, церием-144, рутением-103 и -106, плутонием-239. Среди этих изотопов преобладали цезий и йод, они составляли 90 % всей поглощенной организмом людей дозы.

в) Лечение пораженных в Чернобыле. Трансплантация костного мозга в первую очередь потребовалась пострадавшим, которые получили 500 рад или более. В основном лечение включало в себя противоожоговые мероприятия, введение тромбоцитарной и эритро-цитарной массы, профилактическое применение антибиотиков и целенаправленную антибиотикотерапию при развитии инфекций, а также поддержание водно-электролитного баланса и парентеральное питание.
Больных помещали в стерильные одноместные палаты с ламинарным потоком воздуха. Во всех случаях, когда в итоге наступала смерть, поглощенная костным мозгом и кожей (за счет мощного воздействия бета-радиации) доза превышала 600 рад (6 Гр). Смертность во многом была также обусловлена термическими ожогами. Большой части населения, проживавшей поблизости от места аварии, выдавали йодид калия.
В результате аварии на Чернобыльской АЭС погиб 31 человек. Столько же умерло из-за радиационного облучения в мире за предшествовавшие 42 года. Примерно у половины пострадавших в Чернобыле были умеренно выраженные или сильные термические или радиационные ожоги кожи; у 203 человек, как сообщалось, развилась острая лучевая болезнь различной степени тяжести, что потребовало госпитализации. Согласно проведенному анализу, 29 наиболее тяжелых больных с острой лучевой патологией получили дозы в 6 Гр (600 рад) или более.
г) Рак щитовидной железы после Чернобыля. У тех детей, доза облучения которых за счет проникновения изотопов в организм перорально или ингаляционно осталась неизвестной, может развиться гипотиреоз или рак щитовидной железы. Об общей заболеваемости последним можно будет судить только по прошествии 30 лет.
В начале лета 1989 г. в грунтовых водах в районе Красного Леса был обнаружен плутоний. Однако в связи с тем, что он характеризуется способностью распадаться с образованием америция, опасность для здоровья человека возрастает наряду с увеличением вероятности попадания радиации в используемую населением воду. Более того, америций-241 обладает более продолжительным периодом полураспада (423 года). В 2060 г. излучение альфа-частиц, обусловленное америцием-241, станет в 2 раза сильнее, чем от плутония.
Заболеваемость раком щитовидной железы среди детей в тех районах бывшего Советского Союза, на которые выпали радиоактивные осадки из чернобыльского реактора, продолжает расти.
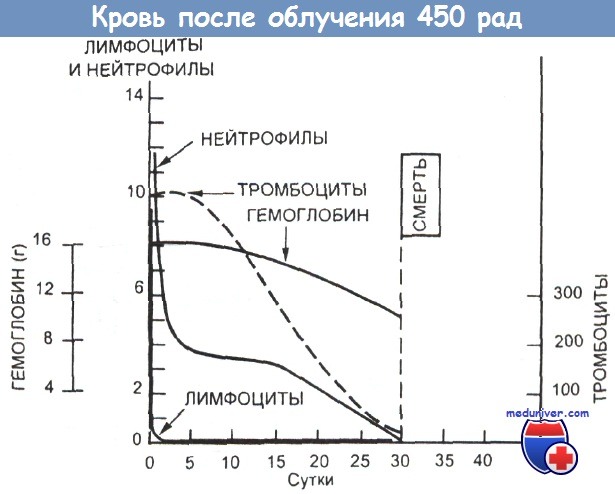
Типичные изменения гематологической картины после облучения всего тела в дозе 450 рад.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Введение
Материал и методы
В Центре накоплена информация о 232 больных с МЛП, которые находились на лечении в этом учреждении в остром периоде лучевого поражения, а также наблюдались в отдаленные сроки после радиационной аварии. Длительность наблюдения колебалась от 1 до 43,5 (в среднем 13,3 ± 1,3) лет. Периодом отдаленных последствий считался период, начинавшийся спустя 1 год после лучевого воздействия. 75 человек пострадали в результате воздействия гамма‑ бета‑излучения, 99 – от гамма‑излучения, 16 – от гамма‑нейтронного, 18 – от рентгеновского, 12 – от бета‑излучения, 8 – от воздействия пучка электронов, 4 – от воздействия пучка протонов.
МЛП I (легкой) степени тяжести выявлены у 74 больных, МЛП II (средней) степени – у 132 больных, МЛП III (тяжелой) степени – у 127 больных и МЛП IV (крайне тяжелой) степени – у 49 больных (табл. 1). Необходимо отметить, что у одного больного, как правило, наблюдались очаги поражения разной степени тяжести (например, МЛП I–IV или МЛП I, II степени), поэтому в приводимых таблицах число случаев МЛП различной степени тяжести может превышать количество больных в группе.
Количество случаев МЛП различной степени тяжести в компьютерной базе данных Центра
Из 232 больных у 72 человек наряду с МЛП была диагностирована острая лучевая болезнь (ОЛБ) различной степени тяжести (табл. 1). Среди больных, у которых была диагностирована ОЛБ, наблюдалось 49 случаев МЛП I, 34 – МЛП II, 26 – МЛП III, 17 – МЛП IV степени тяжести. Среди них 45 человек пострадали от гамма‑бета‑, 13 – от гамма‑, 14 – от гамма‑нейтронного воздействия. В работе использованы методы вариационной статистики (программа для ПК Biostat).
Результаты
Клиническая картина МЛП различной степени тяжести в периоде основных клинических проявлений
Клинические признаки МЛП, соответствующие различным степеням тяжести раневого процесса, приведены в табл. 2.
Основные клинические проявления по периодам развития и уровни поглощенных доз (кратковременное гамма-облучение) при МЛП различных степеней тяжести
Минимальные клинические проявления в виде гиперемии и слабого отека характерны для МЛП легкой степени тяжести. При подобном поражении эпителизация наступает всегда. развитие раневого процесса заканчивается сухим шелушением.
При средней, тяжелой и крайне тяжелой степенях МЛП на фоне отёка и гиперемии возникает отслойка эпидермиса и формируются пузыри. Пузыри вскрываются самостоятельно, обнажается язвенная поверхность. Самопроизвольная эпителизация происходит при МЛП средней степени тяжести. При тяжелой и крайне тяжелой степени поражения язвы превращаются в некротические, инфицируются и практически не заживают при консервативном лечении.
В отдаленном периоде на месте бывших острых лучевых язв и эрозий можно наблюдать выраженные рубцово‑атрофические изменения с пигментацией, множественными телеангиоэктазиями, гиперкератозом, поздними лучевыми язвами. В отдельных случаях возможно злокачественное перерождение тканей, особенно при гиперкератозе [5–8]. Однако следует указать, что развитие лучевого рака более характерно для последствий многолетнего хронического переоблучения [9–11].
Отдаленные последствия МЛП
Последствия МЛП являются основной причиной стойкой инвалидизации в отдаленные сроки у пострадавших в радиационных авариях.
Частота и клинические проявления отдаленных последствий МЛП различной степени тяжести (I–IV), вызванных действием различных видов ионизирующего излучения, по данным компьютерной базы данных клиники Центра, представлены на рис. 1–4.
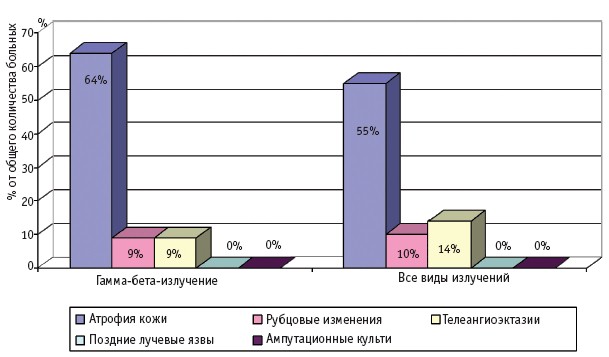
Рис. 1. Отдаленные последствия МЛП I степени тяжести
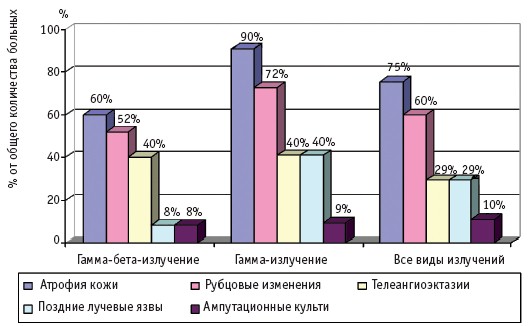
Рис. 2. Отдаленные последствия МЛП II степени тяжести
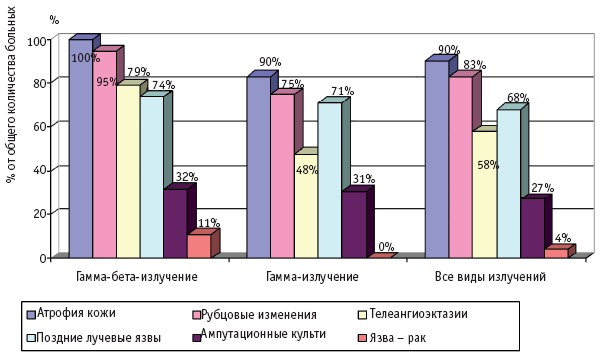
Рис. 3. Отдаленные последствия МЛП III степени тяжести
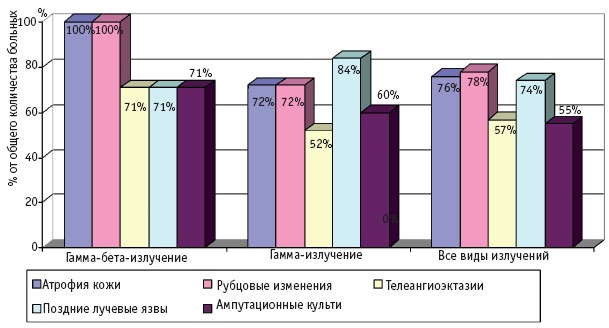
Рис. 4. Отдаленные последствия МЛП IV степени тяжести
Интересной находкой явилось обнаружение в периоде отдаленных последствий новообразований кожи: у 4 больных (у двух больных с МЛП, у двух с сочетанием ОЛБ и МЛП) в области длительно существовавших, не леченных хирургическим путем поздних лучевых язв был обнаружен высокодифференцированный плоскоклеточный рак кожи (рис. 3); у 5 больных – базальноклеточный рак кожи. Базалиомы были обнаружены у больных, перенесших ОЛБ I–IV степени и МЛП IV. Надо отметить, что появление базалиом отмечено на коже вне зоны последствий МЛП, поэтому эта нозология не вынесена на рис. 4.
Лечение МЛП и их отдаленных последствий
Несмотря на более чем столетнюю историю изучения МЛП, вопрос выбора тактики лечения остается очень сложным. С целью оценки эффективности лечения МЛП были проанализированы все группы больных с поражениями различной степени тяжести. Из исследования исключены пострадавшие, которые находились в клинике только в остром периоде и не наблюдались в периоде последствий.
Выбор методов лечения производится в зависимости от локализации МЛП, стадии развития раневого процесса, состояния окружающих тканей и площади МЛП.
Консервативное лечение в той или иной степени проводилось у всех 232 больных. На разных стадиях развития раневого процесса оно включало применение противоожоговых средств (лиоксазоль, пантенол), ингибиторов протеаз (контрикал, гордокс, октреотид), обезболивающих препаратов, антибиотиков, пентоксифиллина, средств, стимулирующих регенерацию (метилурацил, солкосерил, актовегин), антисептических растворов, различных перевязочных средств с нанесенными лекарственными препаратами и др.
Консервативными методами ограничивалось лечение только при МЛП легкой степени тяжести. Проанализированы случаи МЛП I степени тяжести от воздействия различных видов ионизирующего излучения. Условием подбора группы было наличие у пациентов только МЛП легкой степени. При наличии у одного пациента очагов МЛП различной степени тяжести больной включался в группу по максимальной степени тяжести (например, при МЛП II–III степени тяжести – в группу МЛП III степени), так как считалось, что наиболее выраженные последствия МЛП у данного пациента будут следствием острого МЛП наибольшей степени тяжести.
Консервативное лечение при МЛП легкой степени не требовало большой активности и в острой фазе приводило к полной эпителизации дефекта. Хирургическое лечение у этих больных не проводилось. У 16 из 30 пациентов отдаленные последствия МЛП легкой степени тяжести были представлены трофическими изменениями в виде легкой атрофии и сухости кожи, единичных телеангиоэктазий, которые также не требовали никакого лечения. У 14 больных последствия МЛП легкой степени отсутствовали.
Проанализированы медицинские сведения о лечении 59 больных с последствиями МЛП II (средней) степени тяжести. У 47 из 59 больных с МЛП II степени лечение также ограничивалось консервативными средствами. В результате его применения была достигнута полная эпителизация раневой поверхности. Однако у 12 больных в дальнейшем потребовалось проведение оперативного вмешательства, при этом консервативные методы лечения использовались для ускорения заживления раневой поверхности, либо для профилактики развития поздних лучевых язв.
У больных с МЛП III–IV степени тяжести основным видом лечения являлось хирургическое. Консервативная терапия использовалась для ускорения заживления раневой поверхности и для профилактики развития лучевого фиброза и поздних лучевых язв. тяжесть исходов и отдаленных последствий МЛП, несомненно, зависит от дозы лучевого воздействия, площади (табл. 3) и анатомического расположения МЛП. Последнее также определяет возможность использования близко расположенного к очагу поражения аутолоскута.
Большинство больных с МЛП тяжелой степени, пострадавших от всех видов ионизирующего излучения, подвергались хирургическому лечению. Самопроизвольное заживление без развития поздних лучевых язв наблюдалось только при малых площадях МЛП. Среди 41 пострадавшего от гамма‑излучения с МЛП III степени хирургическое лечение не проводилось у 8 (19,5 %) человек. У этих пациентов поражения имели малую площадь – менее 0,25 % поверхности тела. Отдаленные последствия были представлены выраженной атрофией кожи и мягких тканей, лучевым фиброзом, нарушением пигментации, телеангиоэктазиями, рубцами, остеопорозом, наличием контрактур. У остальных 33 больных хирургическое лечение проводилось в связи с появлением незаживающих поздних лучевых язв.
Критерии прогноза непосредственных и отдаленных последствий МЛП (гамма – бета облучения) в зависимости от объема (степени тяжести и площади) поражения
При МЛП IV степени тяжести уже в остром периоде течения раневого про‑ цесса может потребоваться проведение инвалидизирующих больного операций (некрэктомия тканей и инфицированных язв, ампутация пальцев или конечностей, аутодермопластика для закрытия раневого дефекта) с целью удаления очага некроза, инфекции и интоксикации, нередко для спасения его жизни.
Ампутация в области здоровых тканей дает стойкий эффект, профилактируя развитие поздних лучевых язв, но приводит к инвалидизации больного и снижению качества его жизни.
Если некрэктомия и ампутация проводятся не в границах здоровых тканей (II гистологическая зона МЛП [12]), то возникает рецидив поздних лучевых язв с необходимостью реампутаций и повторных аутодерматопластических операций (свободным лоскутом или филатовским стеблем), что требует повторных госпитализаций, перевязок, сопровождается болевым синдромом и приводит к глубокой десоциализации пациентов.
В группе из 6 пациентов с МЛП IV степени тяжести от гамма‑нейтронного излучения у трех больных острые лучевые язвы с большими дефектами самопроизвольно эпителизировались с последующим развитием гиперкератоза, индуративного отека, гиперпигментации, сухого некроза, и рубцов, которые постепенно увеличивались. Через несколько месяцев или год на фоне прогрессирования этих проявлений развились незаживающие поздние язвы, приведшие к необходимости ампутаций двух и более конечностей. У трех пациентов ампутации конечностей были произведены в остром периоде, в некоторых случаях были произведены реампутации конечностей из‑за развития поздних лучевых язв на культях с септическими осложнениями (септический эндокардит, амилоидоз почек и т.д.). таким образом, у всех больных IV ст. МЛП от гамма‑нейтронного излучения были произведены ампутации 2–3 конечностей.
У 5 человек МЛП IV степени тяжести от гамма‑бета‑излучения возникли в результате радиационных аварий, произошедших до 1987 г. раневой процесс у этих больных характеризовался развитием незаживающих острых лучевых язв или медленного заживления язв с последующими дефектами в виде гиперкератоза, лучевого фиброза, нарушения пигментации, телеангиоэктазий, контрактур. Больным проводилось хирургическое лечение в виде повторных некрэктомий, пластики свободным лоскутом, ампутаций и реампутаций пальцев верхних и нижних конечностей, пластики мостовидным лоскутом, ампутации кисти. У одного пациента из этой группы произошла малигнизация длительно существующей поздней лучевой язвы.
После 1988 г. у 10 пострадавших для сохранения целой конечности или ее большего сегмента, оптимального для дальнейшего протезирования, при МЛП III и IV cтепени тяжести, наряду с некрэктомией и ампутациями, кроме аутотрансплантаций свободным лоскутом, сотрудники Центра вместе с коллегами из отделения микрохирургии рЦХ им. Б.В. Петровского начали проводить трансплантации микрохирургическим полнослойным лоскутом на сосудистой ножке или другими васкуляризированными лоскутами, что позволило сократить объем ампутации и некрэктомии и избежать множественных реампутаций.
Если у 13 пострадавших с МЛП IV ст. от гамма‑излучения было проведено от 3 до 12 реампутаций и аутопластических операций свободными и стебельчатыми лоскутами, то среди 10 пострадавших, которым были произведены экономные некрэктомии и микрохирургическая аутодермопластика на сосудистой (питающей) ножке в 1–2 этапа, у одного пациента конечность была полностью сохранена, в других 9 случаях наблюдался стойкий эффект без рецидива поздних лучевых язв и с хорошей функцией конечностей.
Три человека с МЛП IV степени пострадали от рентгеновского излучения во время аварийных ситуаций после 2005 г. Всем пациентам в остром периоде произведены экономные некрэктомии и ампутации отдельных фаланг со сложными пластиками микрохирургическими полнослойными аутолоскутами с сосудистыми питающими ножками или реваскулизированной фасцией (рис. 5). Всем троим пациентам удалось сохранить конечности или большие их фрагменты (рис. 6). Одному – конечность (правую руку) с полной функциональной состоятельностью (9 лет наблюдения). Второму и третьему пациентам удалось сохранить правую и левую кисти, за исключением концевой фаланги I и средней фаланги II пальца и II и III левой кисти с формированием сухожилий разгибателей пальцев правой кисти из разгибателей правой стопы с частичным восстановлением функций (10 лет наблюдения).
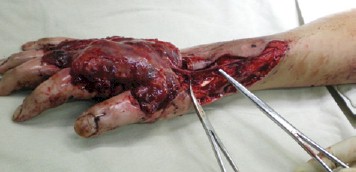
Рис. 5. Хирургическое вмешательство при МЛП III–IV степени тяжести
от рентгеновского облучения

Рис. 6. Восстановление функции правой кисти после хирургического лечения
При сравнении эффективности различных видов операций, применяемых при МЛП, в двух группах больных с аналогичной степенью тяжести и площадью поражения аутотранспланция с применением микрохирургической техники дает явные преимущества перед аутотрансплантацией свободным лоскутом, значительно сокращая число повторных операций (табл. 4). Больные, включенные в это исследование, были подобраны по полу, возрасту, степени тяжести МЛП, площади поражения.
Кроме того, аутопластические операции с применением микрохирургической техники позволяют сохранить большие сегменты конечности, что важно для дальнейшего функционирования ее культи, в том числе и для использования протеза.
Количество повторных оперативных вмешательств при Млп в зависимости от типа первичных операций
Примечания: * – некоторые больные имели МЛП 2 и 3 конечностей
** – отдельным больным проводилось до 20 операций – повторные реампутации с последующей аутопластикой свободным лоскутом
Необходимо отметить, что в связи с закономерными изменениями в последние годы структуры лучевых поражений в виде сокращения доли лиц с ОЛБ и увеличением количества пострадавших с МЛП, меняется и контингент больных. если многие десятилетия основным «поставщиком» пострадавших с лучевыми поражениями была атомная промышленность, то позднее мы стали чаще видеть среди больных работников нефтегазовой отрасли (дефектоскописты). В последнее десятилетие среди наших больных появились пациенты с осложнениями медицинского облучения. тяжелый соматический статус этих больных не позволяет проводить адекватное хирургическое лечение. В связи с этим с 2007 г. в лаборатории успешно применяется методика лечения поздних лучевых язв с помощью мезенхимальных стволовых клеток.
Заключение
Таким образом, правильный и своевременный диагноз при МЛП является очень важным звеном в системе оказания помощи пострадавшим в радиационных авариях, так как от этого зависит выбор адекватной схемы лечения.
Лечение МЛП легкой степени является исключительно консервативным. Может проводиться в любом лечебно‑профилактическом учреждении. Однако, учитывая частое сочетание МЛП с ОЛБ достаточно часто возникает необходимость в проведении обследования и лечения в условиях специализированного стационара.
Хирургическое лечение в комплексе с консервативным применяется у 30 % больных с МЛП средней степени при наличии поздних лучевых язв и практически у всех больных с поздними лучевыми язвами как последствиями МЛП тяжелой степени.
Методом выбора при тяжелых и крайне тяжелых МЛП в остром периоде и при рецидивирующих поздних лучевых язвах в отдаленном периоде являются оперативные вмешательства, основой которых является аутопластика толстыми лоскутами на сосудистой ножке с применением микрохирургической техники, что значительно улучшает исходы и минимизирует тяжелые отдаленные последствия. Кроме того, для профилактики развития поздних лучевых язв больным назначается каждые 6 месяцев внутривенное введение пентоксифиллина и актовегина.
При МЛП крайне тяжелой степени хирургическое лечение является основным методом не только в периоде отдаленных последствий, но уже и в остром периоде течения раневого процесса. Из видов оперативных вмешательств применяются все возможные: некрэктомии, ампутации, аутопластики полнослойным микрохирургическим лоскутом на питающей ножке, сдвижные лоскуты, реваскулизированные лоскуты, свободные для временного закрытия дефекта или на реваскулизированную фасцию, филатовским стеблем, мостовидным лоскутом. Для сохранения больших сегментов, иногда и целой конечности, методом выбора является применение полнослойных лоскутов на питающей ножке, полученных микрохирургическим методом или реваскулизированные лоскуты (фасциальные), т.е. способные нормализовать трофику в области пораженных тканей. Консервативное лечение является вспомогательным.
Лечение МЛП средней и тяжелой степени должно проводиться в специализированном стационаре, обладающим полным арсеналом диагностических и лечебных методов.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Ожоги: причины появления, симптомы, диагностика и способы лечения.
Определение
Ожоги - это травмы, возникающие в результате высокотемпературного, химического, электрического или радиационного воздействия, которое повреждает кожу и подлежащие ткани. Ингаляционной травмой называют повреждение слизистой оболочки дыхательных путей и/или легочной ткани за счет воздействия термических и/или токсикохимических факторов.
Причины появления ожогов
К наиболее частым относят термические ожоги, которые связаны с воздействием высоких температур. Обычно это ожоги горячими жидкостями и паром, реже – открытым пламенем. Контактные термические ожоги развиваются при контакте с горячими предметами или веществами, например, раскаленным металлом, горячей смолой, битумом, асфальтом и т.д.
Химические ожоги возникают вследствие агрессивного воздействия на кожу или слизистые оболочки химических веществ. Кроме ожогов эти вещества вызывают и другие поражения кожи - контактные дерматиты и экземы.
Электротравма (травма в результате действия на организм электрического тока) также может привести к ожогу и сопровождаться местной и общей реакцией. У взрослых электротравмы, как правило, связаны с профессиональной деятельностью, у детей - с использованием домашних электроприборов.
Поражения молнией встречаются с одинаковой частотой у лиц всех возрастных групп, чаще это происходит за городом у жителей сельской местности.
Лучевые ожоги вызывает ультрафиолетовое, инфракрасное и ионизирующее излучение. Солнечные ожоги кожи знакомы многим, они обусловленные чрезмерным воздействием на нее солнечных лучей. Ионизирующее излучение приводит как к местным, так и к общим изменениям в организме, получившим название «лучевая болезнь».
Ингаляционные травмы происходят при вдыхании горячего воздуха, пара и/или под действием токсичных химических соединений (продуктов горения), попадающих в дыхательные пути вместе с дымом.
Классификация ожогов
По этиологии (причинам) формирования:
- Термические ожоги (пламенем, кипятком, контактные).
- Электрические ожоги.
- Химические ожоги.
- Лучевые ожоги.
- Смешанные ожоги.
- Ингаляционные травмы:
- термические (термоингаляционное поражение дыхательных путей);
- токсикохимические (острые ингаляционные отравления продуктами горения);
- термохимические (смешанные).
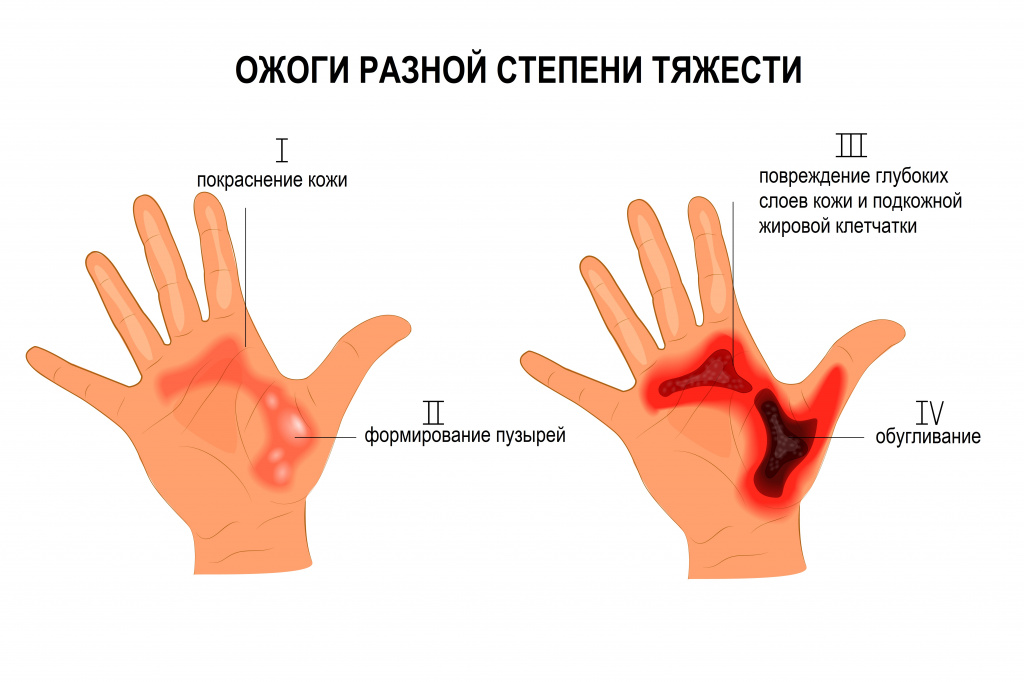
- I степень – ожоги на уровне верхних слоев эпидермиса.
- II степень – поражение на всю глубину эпидермиса.
- III степень – некроз (омертвление) поверхностных и/или глубоких слоев кожи, включая дерму.
- IV степень – некроз всех слоев тканей (обугливание).
По площади повреждения ожоги делятся на ограниченные (локальные) и обширные.
![Степени ожогов.jpg]()
Симптомы ожогов
Клиническая картина ожоговых состояний зависит от глубины и площади поражения и включает местные и общие проявления. Для поверхностных ожогов, площадь которых составляет менее 10% поверхности тела, характерны только местные проявления. Ожоги I степени проявляются отечностью, гиперемией (покраснением) кожи, выраженной болезненностью. При II степени образуются пузыри, заполненные прозрачной жидкостью. Для ожогов III и IV степени характерно появление пузырей с геморрагическим (кровянистым) содержимым, обугливание кожи, подкожной жировой клетчатки и подлежащих тканей вплоть до костей; болевая и тактильная чувствительность отсутствуют.
При поражении органов зрения больной жалуется на сильную резь в глазах, светобоязнь, отек и покраснение век и конъюнктивы.
При ингаляционных ожогах отмечается осиплость голоса, кашель со скудной вязкой, возможно, черной мокротой (копотью). Часто сопровождаются ожогами лица, шеи, передней поверхности грудной клетки.
Распространенные поверхностные ожоги (более 30% поверхности тела у взрослых) и глубокие ожоги (более 10% поверхности тела у взрослых), а также ожоги меньшей площади и глубины у детей и пожилых людей или у лиц с хроническими заболеваниями сопровождаются развитием ожоговой болезни.
Выделяют несколько стадий этого состояния.
Ожоговый шок продолжается от 12 до 72 часов и связан с нарушением кровообращения и водно-солевого баланса. Сразу после травмы пострадавший возбужден, у него может повышаться давление, учащаться пульс и дыхание, через 1-2 часа возбуждение сменяется заторможенностью, наблюдаются озноб, мышечная дрожь, повторяющаяся рвота, температура тела может как повышаться, так и снижаться. Отмечается уменьшение количества мочи, при этом моча приобретает темный цвет.
Следующая стадия – острая токсемия, которая развивается вследствие всасывания в кровь продуктов распада поврежденных тканей и длится до 10-15 дней. Эта стадия проявляется самыми разнообразными нарушениями психики (возбуждением, спутанностью сознания, галлюцинациями, нарушениями сна), а также поражением внутренних органов (сердца, легких, органов желудочно-кишечного тракта), поэтому у пациента наблюдаются перебои в работе сердца, кашель, одышка, боль в животе. Третий период – септикотоксемия, продолжающаяся от 2-3 недель до 2-3 месяцев. Проявления связаны с гнойными осложнениями (обильным гнойным отделяемым из раны, плохо заживающей раной), пациент испытывает вялость, отсутствие аппетита, снижается вес.
Прогноз в каждом конкретном случае определяется распространенностью поражения, исходным состоянием здоровья пострадавшего и адекватностью проводимого лечения.
Диагностика ожогов
Постановка диагноза, как правило, затруднений не вызывает. Для определения тактики лечения врач оценивает выраженность болевого синдрома, площадь и глубину ожогов, наличие признаков сочетанной травмы, поражения дыхательных путей, ожогового шока.Поскольку при обширных, глубоких ожогах в той или иной степени страдают все органы и системы организма, проводится расширенная лабораторная и инструментальная диагностика.
Лабораторная диагностика может включать самый разнообразный спектр анализов.
-
Клинический анализ крови.
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Читайте также: