При трении пальцами кожа
Обновлено: 27.04.2024
Повышенная тактильная чувствительность (гиперестезия) характеризуется обостренным восприятием при воздействии раздражителей. Наблюдается при мононевропатиях, полиневропатиях, ганглионитах, ганглионевритах, каузалгии, эритромелалгии, менингеальном синдроме, некоторых других неврологических, ревматических и инфекционных болезнях. Причину определяют по результатам беседы, неврологического осмотра, электромиографии, церебральной МРТ, лабораторных анализов и иных исследований. Лечение включает анальгетики, антимикробные средства, спазмолитики, ганглиоблокаторы, другие препараты. Проводят физиотерапию. В отдельных случаях выполняют операции.
Общая информация
Повышение тактильной чувствительности выявляется при снижении порога восприятия различных неспецифических стимулов: прикосновения, трения, изменения температуры и пр. При поражении периферической нервной системы, как правило, сочетается с другими сенсорными расстройствами: парестезиями, аллодинией, дизестезией. Развивается на начальных стадиях заболевания, в последующем сменяется гипестезией или анестезией.
У пациентов с патологиями ЦНС чаще возникает остро, дополняется общемозговыми и очаговыми проявлениями, признаками интоксикации или нарушения мозгового кровообращения. При ревматических и ортопедических заболеваниях появляется в зоне над очагом повреждения. Обусловлена отеком, воспалительными явлениями, постоянным перераздражением нервных окончаний.
Почему повышается тактильная чувствительность
Болезни периферических нервов
Тактильная гиперестезия характерна для синдрома Чарлина, сопровождающегося болевыми пароксизмами в зоне глазницы и близлежащих областях. Приступы провоцируются приемом пищи, надавливанием на крыло носа, продолжаются до 1 часа, дополняются слезотечением, светобоязнью, блефароспазмом, повышенной кожной чувствительностью. Признак также наблюдается при невралгии тригеминального нерва, при которой возникают приступообразные кратковременные, но очень интенсивные боли в половине лица.
Развитие тактильной гиперестезии возможно и при других мононевропатиях, однако, при поражении периферических нервов в области конечностей это проявление нечасто играет значимую роль в клинической картине болезни. Усиление тактильной чувствительности может отмечаться на начальной стадии полинейропатий, сочетается с другими сенсорными нарушениями, слабостью мышц, вегетативной дисфункцией.
Типично симметричное вовлечение дистальных отделов конечностей с последующим распространением симптоматики в проксимальном направлении. Причиной гиперестезии становятся такие полинейропатии, как:
- Токсические:алкогольная, при приеме наркотиков, действии профессиональных вредностей;
- Первичные воспалительные: мультифокальная сенсорная и моторная полиневропатии, при синдромах Гийена-Барре и Фишера;
- Вторичные воспалительные: при системном васкулите, болезни Шегрена, СКВ, вирусном гепатите С, ВИЧ-инфекции, онкологических заболеваниях (саркоидоз, гепатоцеллюлярная карцинома и др.).
- Метаболические: при сахарном диабете, гипотиреозе, тяжелых патологиях почек и печени.
Ганглиониты, ганглионевриты
Основным проявлением ганглионитов и ганглионевритов является диффузная жгучая боль с нечеткой локализацией, распространяющаяся за пределы зоны иннервации пораженного узла. Болезненные ощущения провоцируются сильными эмоциями, переменой погоды, приемом пищи. Не усиливаются при движениях. Дополняются парестезиями, гипестезией или гиперестезией, вазомоторными нарушениями.
Клиническая картина определяется расположением ганглия. При шейном ганглионеврите возможны офтальмологические проявления, парез гортани, боль в руке и верхней половине грудной клетки. При вовлечении верхнегрудных узлов отмечаются кардиалгии, тахикардия, одышка, при поражении нижнегрудных и поясничных – висцеральные расстройства, зуд половых органов, дизурия.
Вегетативные ганглиониты головы включают невралгию ушного, подчелюстного и подъязычного узлов. При опоясывающем герпесе с вовлечением коленчатого узла возможно развитие синдрома Рамсея-Ханта, который проявляется болями в зоне ушной раковины и парезом лицевого нерва. При ганглионите крылонебного узла определяются признаки невралгии тройничного нерва.

Каузалгия
Данное патологическое состояние возникает после травм, чаще всего – переломов и огнестрельных ранений. На начальном этапе пациента с каузалгией беспокоят продолжительные жгучие боли, развивающиеся без внешнего воздействия или при контакте с незначительными стимулами (например, прикосновением), уменьшающиеся при погружении в воду или наложении влажных повязок. Наряду с повышенной тактильной чувствительностью отмечаются гиперпатия, аллодиния и гипералгезия. Выявляются вегетативные и трофические расстройства. Со временем формируются дистрофические изменения мышц, парезы и контрактуры.
Эритромелалгия
Основным проявлением эритромелалгии считаются приступы пекущей или жгучей боли продолжительностью от нескольких часов до нескольких минут, дополняющейся отеком и гиперемией. Вначале страдает большой палец стопы, затем в процесс вовлекаются обе ступни, иногда – кисти рук, реже промежность, уши и нос. В дальнейшем пароксизмы учащаются, обнаруживаются гиперестезия, гиперпатия, парестезии. Прогрессируют трофические и сосудистые нарушения.
Менингеальный синдром
Возникает при поражении мозговых оболочек, провоцируется инфекциями, травмами, токсическими воздействиями и другими причинами. Включает характерные болевые проявления, усиление тонуса мышц и гиперестезию. Наряду с повышенной чувствительностью наблюдаются свето- и звукобоязнь. Пациент принимает типичную позу (на боку, с запрокинутой головой, согнутыми руками и ногами). Причиной развития менингеального синдрома становятся:
- Серозный менингит. Часто сопровождается признаками ОРВИ. Манифестирует остро с интенсивной головной боли, интоксикации и повышенной температуры. Могут определяться сонливость, легкая оглушенность, косоглазие, диплопия.
- Гнойный менингит. Провоцируется менингококковой инфекцией, другими бактериальными возбудителями. Наряду с ознобами, лихорадкой и гипертермией выявляются нарушения сознания, бред, психомоторное возбуждение, иногда – судороги. Специфические симптомы выражены ярче, чем при серозной форме. Обнаруживаются признаки поражения тех или иных черепно-мозговых нервов.
- Менингоэнцефалит. Специфические и общие неспецифические проявления дополняются тяжелыми расстройствами сознания. При неблагоприятном развитии событий возможна кома. Клиническая картина напоминает гнойный менингит, но очаговые симптомы более разнообразные, могут включать гемипарезы, гиперкинезы, вестибулярную атаксию, мозжечковые расстройства.
- Туберкулезный менингит. В отличие от других форм, наблюдается продром длительностью 1-2 недели, включающий апатию, раздражительность, цефалгии, слабость. Затем наступает резкое ухудшение с появлением менингеальных симптомов. В терминальной стадии формируются парезы и параличи, нарушается дыхание и сердечный ритм.
- Менингит у детей. Пациенты становятся плаксивыми, капризными. Обнаруживаются менингеальные, общемозговые и общеинфекционные проявления. Часто возникают судороги. Возможны нарушения сознания, гиперкинезы, гемипарез, глазодвигательные расстройства.
Другие причины
В число других заболеваний и патологических состояний, при которых определяется повышенная тактильная чувствительность, входят:
- Неврологические болезни:мигренозный инсульт, аневризмы церебральных сосудов, первичные и метастатические опухоли головного мозга.
- Ревматологические и ортопедические проблемы: артриты различного генеза, болезнь Шинца, эпикондилит локтевого сустава.
- Травматические повреждения:электротравма (удар молнией), состояние в период восстановления после ожогов.
- Инфекционные патологии:лихорадка паппатачи.
Диагностика
Установлением этиологии тактильной гиперестезии занимается врач-невролог. Больных с провоцирующими соматическими заболеваниями и травмами направляют на консультацию к соответствующим специалистам: терапевту, эндокринологу, травматологу. Врач выясняет, когда впервые появилась повышенная чувствительность, с какими симптомами сочеталась, как болезнь развивалась с течением времени. Диагностическая программа предусматривает проведение следующих манипуляций:
- Неврологический осмотр. Для определения наличия и зоны тактильной гиперестезии проводятся специальные пробы (прикосновения, давление, движения). Кроме того, методика предусматривает обнаружение других сенсорных расстройств, исследование рефлексов и мышечной силы.
- Электрофизиологические методы. Установить локализацию, распространенность и тяжесть повреждения, остроту патологического процесса помогают электромиография и электронейрография. Исследования применяются для дифференцировки повреждений периферических нервов и ЦНС. Повторно используются в процессе лечения для оценки эффективности терапевтических мероприятий.
- Визуализационные методики.МРТ головного мозга проводится при менингитах, опухолях, аневризмах. МР-ангиография показательна при болезнях внутримозговых сосудов. КТ черепа информативна при исключении компрессии нерва в костном канале, как причины развития тригеминальной невралгии. При артритах и эпикондилите рекомендованы рентгенография или КТ суставов.
- Лабораторные анализы. Для фибромиалгии характерно уменьшение количества серотонина в крови. Для установления этиологии полиневропатий может потребоваться проведение генетических тестов, анализов на антитела, биохимического исследования крови на сахар, гормоны поджелудочной железы, печеночные ферменты, мочевину и креатинин. Возбудителя менингита устанавливают по данным ПЦР или посева ликвора.

Лечение
Консервативная терапия
В зависимости от причины повышенной чувствительности кожи осуществляются следующие лечебные мероприятия:
- Фибромиалгия. Рекомендованы обезболивающие средства, антиконвульсанты, антидепрессанты. Местно выполняют орошения анестетиками и лечебные блокады. Проводят ЛФК, БОС-терапию, акупунктуру. При повышенной склонности к отрицательным переживаниям, сопутствующих психических расстройствах показана психотерапия.
- Полиневропатия. По возможности проводится этиопатогенетическая терапия: подбор адекватной схемы инсулинотерапии, введение гормональных препаратов и пр. Специфическое лечение воспалительных нейропатий не разработано, требуется введение человеческого иммуноглобулина, экстракорпоральная детоксикация. Для облегчения симптомов всем больным с множественным поражением нервов назначают нейротрофические препараты и витаминные средства.
- Ганглиониты, ганглионевриты. Болевой синдром купируют с помощью анальгетиков. В тяжелых случаях вводят новокаин внутривенно. Для борьбы с инфекционными агентами применяют противовирусные и антибактериальные средства. При повышении активности симпатического отдела НС рекомендуют нейролептики, спазмолитики, холинолитики и ганглиоблокаторы, при понижении – используют холиномиметики. Эффективны УФО, диадинамотерапия, грязевые аппликации, лекарственный электрофорез.
- Каузалгия. В схему лечения включают противовоспалительные препараты, наркотические и ненаркотические анальгетики, антиконвульсанты, анксиолитики, антидепрессанты. Выполняют лечебные блокады. В рамках физиотерапии проводят электроанальгезию, электрофорез с анальгетиками, амплипульстерапию, кинезиотерапию (ЛФК, гидрокинезиотерапию, при парезах – пассивную гимнастику).
- Эритромелалгия. Для купирования пароксизмов вводят сосудосуживающие средства. Для устранения отечности применяют антигистаминные препараты, осуществляют новокаиновые блокады. В программу комплексной терапии включают медикаменты для укрепления сосудистой стенки, рефлексотерапию, ножные ванны, лечебные грязи, дарсонвализацию.
- Менингеальный синдром. Требуется срочная госпитализация. Для устранения возбудителя в зависимости от этиологии назначают антибиотики широкого спектра действия, противовирусные или противогрибковые средства. Осуществляют детоксикацию. Для профилактики отека мозга вводят диуретики и глюкокортикостероиды. Симптоматическую терапию проводят с использованием антипиретиков, антиконвульсантов, противорвотных, гипотензивных препаратов.
Хирургическое лечение
Пациентам с тактильной гиперестезией на фоне ганглионеврита, эритромелалгии и каузалгии выполняют симпатэктомию. Церебральные опухоли иссекают с использованием открытых и малоинвазивных методик. При отеке мозга на фоне менингита для купирования повышенного внутричерепного давления осуществляют наружное вентрикулярное дренирование или декомпрессивную трепанацию черепа.
2. Методические рекомендации по диагностике и лечению невропатической боли/ под ред. Яхно Н.Н. – 2012.

Американские ученые теоретически и экспериментально исследовали процесс щелкания человеком пальцами. Они выяснили, что трение играет при этом ключевую роль. Оказалось также, что кожа человеческих пальцев обладает почти оптимальными характеристиками, чтобы щелчок был наиболее громким. Исследование опубликовано в Journal of the Royal Society Interface.
Щелчки пальцами известны человечеству как минимум со времен Древней Греции. Первое изображение щелчка, нанесенное на керамику, датируется 320 годом до н.э. С тех пор щелчки стали неотъемлемой частью искусства и коммуникации во множестве культур. Например, в Либерии они используются в качестве приветствия, будучи аналогом рукопожатия. Было предложено использовать щелчки для эхо-локации слепым людям, а также для биометрической аутентификации.
Щелчок как механический процесс накопления и высвобождения энергии для создания громкого звука свойственен не только людям, но и некоторым видам термитов и муравьев. Хотя разные виды используют его для разных целей, механизм, лежащий в его основе, можно охарактеризовать как систему с трущейся защелкой, приводимую в действие пружиной. И если роль геометрии защелки или упругости пружины уже освещалась в литературе, то насколько важно при этом трение до недавнего времени было неизвестно.
Группа американских физиков и биоинженеров под руководством Саада Бхамла (Saad Bhamla) из Технологического института Джорджии провела экспериментальное и теоретическое исследование, чтобы разобраться с ролью трения в щелчке пальцами. Они выяснили, что поверхность человеческих пальцев оптимальна для щелчка: она не слишком скользкая, чтобы успевала накопиться энергия, и не слишком шершавая, чтобы мешать движению пальца.
Чтобы выяснить это, ученые наклеивали кружки из светоотражающего материала в нескольких местах кисти рук трех человек, которые отслеживались с помощью высокоскоростной камеры. На средний и большой пальцы, участвовавшие в щелчках, с помощью перчаток и наперстков надевались различные материалы (латексная резина, нитрил, смазанный нитрил), чтобы достичь различного коэффициента трения, которые исследователи измеряли отдельно. В качестве смазки они применяли лубрикант на водной основе. Каждый испытуемый делал пять щелчков для каждого типа поверхности. Чтобы избежать усталости кистей, участники эксперимента отдыхали по одной минуте. Для каждого щелчка ученые использовали новые перчатки для предотвращения усталости материала. В дополнительной серии экспериментов они располагали между пальцами датчики для измерения силы при щелчках различной громкости.

Фотография светоотражающих меток, нанесенных на поверхность кисти участника эксперимента
Гиперкератоз стоп - чрезмерное ороговение и утолщение эпидермиса в области подошвенной поверхности стоп. Гиперкератоз стоп характеризуется огрубением и сухостью кожи, появлением омозолелостей, болезненных и кровоточащих трещин. Диагностика гиперкератоза основывается на внешнем осмотре стоп дерматологом, подологом или ортопедом; результатах биопсии кожи с последующим гистологическим исследованием материала. Лечение гиперкератоза стоп проводится комплексно: с этой целью эффективны ванночки для ног, пилинги стоп, проведение аппаратного медицинского педикюра, использование специальных косметических средств.
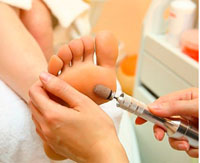



Общие сведения
Гиперкератоз стопы (жесткий роговой слой, сокращенно ЖРС) представляет собой патологическое разрастание рогового слоя эпидермиса, достигающего толщины до одного сантиметра и более. Осложнения гиперкератоза могут проявляться в виде мелких точечных геморрагий (кровоизлияний), мягких (межпальцевых, ногтевых) и твердых (корневых) мозолей, язв от повышенного давления на стопы. Кровоизлияния и мозоли неопасны для здоровья в целом, но представляют косметический дефект и доставляют неудобства при ходьбе. Они требуют удаления с помощью специальных процедур. Язвы стоп часто возникают у больных сахарным диабетом и помимо применения косметических методик требуют лечения основного заболевания.
Часто на фоне отвердение рогового слоя возникают трещины стопы, доставляющие немалый дискомфорт. Но их развитие не всегда напрямую связано с гиперкератозом, они могут являться и следствием недолжного ухода за кожей стоп.

Причины развития гиперкератоза стоп
В возникновении гиперкератоза выделяют две группы факторов:
Экзогенные факторы (внешние)
В данном случае причиной, обусловливающей развитие гиперкератоза, является повышенная и длительная нагрузка на некоторые участки стопы. Под воздействием давления ростковые клетки кожи начинают быстро размножаться. В норме верхние клетки эпидермиса постепенно отшелушиваются, уступая место вновь образованным. В случае чрезмерно активного деления клеток, верхние не успевают слущиваться, из-за чего роговой слой эпидермиса утолщается. Возникает гиперкератоз.
Одним из самых распространенных экзогенных факторов, вызывающих гиперкератоз, является неправильно подобранная обувь. Не только ношение узкой и тесной обуви оказывает избыточное давление на стопы, не менее коварна и стоптанная обувь, или туфли размером больше. В слишком свободной обуви нога внутри не фиксирована и подвижна при ходьбе, что вызывает давление и трение стопы и, как следствие, её патологические изменения.
Еще одной причиной избыточного давления на стопы служит конституция человека: повышенная масса тела и высокий рост. Также к гиперкератозу приводят и различные виды деформации стопы, как врожденного характера (плоскостопие или косолапость), так и приобретенные в процессе жизни (вследствие травм или операций). При этом нагрузка на некоторые участки стопы оказывается превышающей физиологическую норму в несколько раз и подвергает эти зоны чрезмерному давлению.
Эндогенные факторы (внутренние)
К ним относятся, прежде всего, эндокринные и кожные заболевания. При сахарном диабете в организме человека нарушается углеводный обмен. Это, в свою очередь, приводит к изменению болевой и тактильной чувствительности нижних конечностей, нарушению кровообращения и трофики тканей, сухости кожи, язвенным поражениям и другим факторам риска развития гиперкератоза.
Причиной гиперкератоза могут служить и различные заболевания кожи, среди которых псориаз, кератодермии ладонно-подошвенной области, ихтиоз, врожденные нарушения синтеза кератина.
Сочетание сразу нескольких факторов (эндо- и экзогенных) увеличивает риск образования и прогрессирования гиперкератоза. Например, ношение тесной обуви человеком, страдающим сахарным диабетом, может иметь самые неблагоприятные последствия в развитии ЖРС.
Способы лечения гиперкератоза стоп
Лечение в домашних условиях

Гиперкератоз стоп, помимо салонных процедур, требует тщательного домашнего ухода за ногами.
Врагами гиперкератоза являются регулярные гигиенические процедуры и препараты смягчающего действия. В качестве «домашнего доктора» рекомендуется использовать масляные препараты лаванды, горной сосны, розмарина и др. Наилучший результат дает комплексный уход за кожей ног, включающий в себя нанесение основного лекарственного средства на ночь, специальный тоник или лосьон – утром и ванночку для ног 1-2 раза в неделю.
Гигиенический уход за стопами дома должен включать в себя механическое удаление огрубевшей кожи пемзой различной степени жесткости. Ежедневное использование пемзы позволяет своевременно удалять наросший роговой слой. Для предупреждения гиперкератоза достаточно всего нескольких движений пемзой по всей поверхности стопы. Перед использованием пемзы ноги следует вымыть, но не высушивать, так как пемза «любит» влажную поверхность кожи.
Следуя этим несложным правилам домашнего ухода за стопами, вы сможете избежать образования гиперкератоза или существенно облегчить его течение.
Лечение в кабинете подолога

Лечением гиперкератоза стоп занимаются специалисты-подологи, имеющие медицинское образование. Схема лечения отработана многолетним опытом и включает в себя несколько этапов: размягчение огрубевшей кожи стопы, удаление жесткого рогового слоя и последующая шлифовка кожи.
Существует несколько способов размягчения жесткого рогового слоя. Классический способ предполагает использование в качестве размягчителя воды, иногда с добавлением солей или ароматизаторов - это доступно и приятно. В современной косметологии все чаще используются химические размягчители в виде растворов, гелей или пенящихся средств. Их неоспоримыми преимуществами являются обеззараживающее действие, экономичность и высокая эффективность.
Удаление ЖРС проводится одноразовым инструментарием: скальпелем и съемными лезвиями разного размера. Зоны поражения гиперкератозом, расположенные на подошве стопы, в межпальцевых промежутках или на плюсне-фаланговых суставах напоминают узкие ленты или рисовые зерна. Снятие жесткого рогового слоя на этих участках успешно проводится полыми лезвиями.
Мастер-подолог снимает огрубевшие слои кожи очень осторожно под тщательным визуальным контролем, чуть-чуть не доходя до молодой розовой кожи. При технически грамотном выполнении процедуры целостность мягких тканей не нарушается, а жесткий роговой слой удаляется бесследно.
Заключительным этапом подологического лечения гиперкератоза является шлифовка кожи. Она может проводиться как при помощи традиционных пилок, так и аппаратным методом при помощи керамических насадок одноразового применения. Аппаратные методики педикюра имеют преимущества в быстроте, гигиеничности и большей эффективности.
Что такое эксфолиативный кератолиз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Похлебкиной Алевтины Алексеевны, педиатра со стажем в 6 лет.
Над статьей доктора Похлебкиной Алевтины Алексеевны работали литературный редактор Вера Васина , научный редактор Владимир Горский и шеф-редактор Маргарита Тихонова
Определение болезни. Причины заболевания
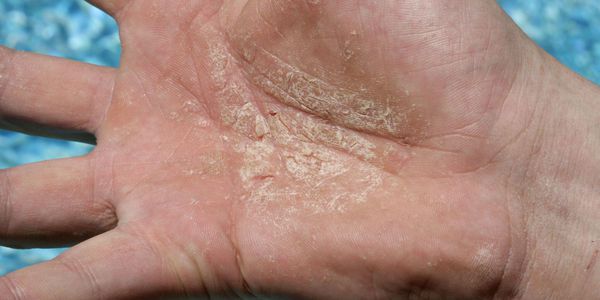
Эксфолиативный кератолиз — это очаговое симметричное шелушение кожи на ладонях, поверхности пальцев и, реже, на подошвах. Заболевание характеризуется сухостью кожи и поверхностными пузырями, заполненных воздухом.
Также эксфолиативный кератолиз называют рецидивирующей фокальной ладонной десквамацией, сухим пластинчатым дисгидрозом и рецидивирующей ладонной десквамацией.
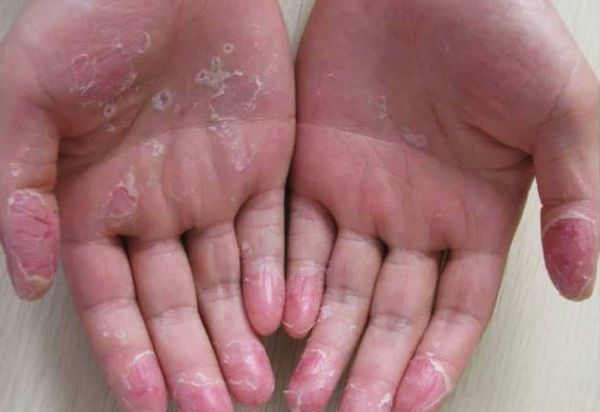
Заболевание широко распространено и часто носит хронический, но доброкачественный характер. Эксфолиативный кератолиз чаще встречается у детей и подростков, реже у взрослых. Нередко его ошибочно принимают за псориаз, экзему или хронический контактный дерматит. У людей с повышенной потливостью рук состояние ухудшается в тёплую погоду и может быть связано с гипергидрозом — усиленным потоотделением [1] .
Ранее эксфолиативный кератолиз называли дисгидротической экземой , и считалось, что заболевание вызвано нарушением работы потовых желёз. Эта связь уже опровергнута, но термин "дисгидротическая экзема" всё ещё используется [2] .
Дисгидротическая экзема, также называемая помфоликсом, может предшествовать эксфолиативному кератолизу. При этом состоянии на пальцах рук, ног, ладонях и подошвах образуются волдыри, наполненные жидкостью, и возникает сильный зуд [2] . Причина дисгидротической экземы неизвестна, но, вероятно, на развитие заболевания влияет множество факторов. В большинстве случаев причину и предрасполагающий фактор выделить невозможно [17] .
Причины эксфолиативного кератолиза
Предполагалось, что экфолиативный кератолиз может быть вызван грибковым поражением, но в дальнейших исследованиях эта гипотеза не подтвердилась.
Возможные провоцирующие факторы эксфолиативного кератолиза:
- трение и контакт с водой[3][6];
- мыло, моющие средства и растворители: химические вещества, содержащиеся в них, могут привести к появлению трещин и пузырей на руках;
- аллергия: продукты питания, загрязнение воздуха и другие вещества могут спровоцировать появление аллергии на коже;
- стресс: может не только вызвать, но и усугубить течение болезни;
- жаркий климат: при тёплой погоде потоотделение усиливается, что может привести к шелушению кожи;
- воздействие солёной воды;
- сухость кожи.
Эксфолиативный кератолиз не связан с дефицитом какого-либо витамина . Встречаются семейные случаи заболевания, однако генетическая роль в развитии эксфолиативного кератолиза изучена недостаточно [14] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы эксфолиативного кератолиза
Эксфолиативный кератолиз часто протекает без выраженных симптомов и проявляется незначительным поражением кожи ладонно-подошвенной области [5] . Отшелушиванию кожи предшествует появление наполненных воздухом пузырей, которые никогда не бывают заполнены жидкостью [3] . В некоторых случаях заболевание начинается только с очагового шелушения кожи, без образования пузырей.
После вскрытия пузырей остаются широкие сетчатые, круглые или овальные очаги. Они шелушатся, распространяются по периферии и образуют большие округлые участки, напоминающие кружева.
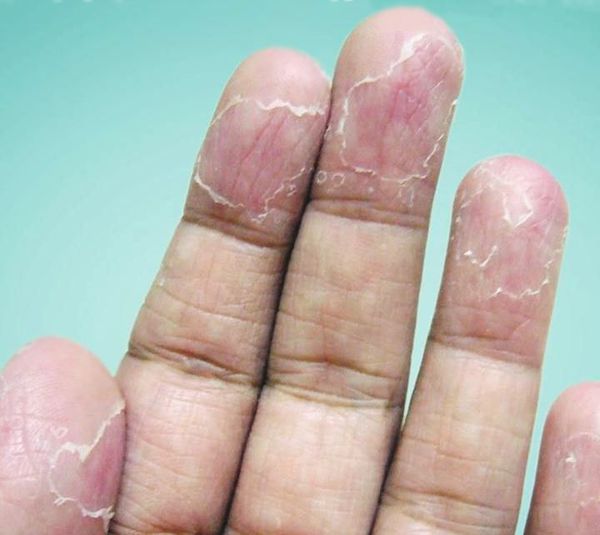
Участки слущенного эпителия теряют защитную функцию, становятся красными, сухими и покрываются трещинками. Шелушению может предшествовать небольшой зуд или жжение, в некоторых случаях область слущенного эпителия становится болезненной [3] .
Высыпания всегда симметричные. Иногда на кончиках пальцев образуются глубокие трещины, кожа становится жёсткой и немеет — в таком случае для полного заживления потребуется 1—3 недели. Эксфолиативный кератолиз может повториться через несколько недель после того, как на месте отшелушивания образовалась новая кожа.
Патогенез эксфолиативного кератолиза
Эпидермис — верхний наружный слой кожи, состоящий из кератиноцитов. Эти клетки содержат белок кератин, необходимый для прочности и эластичности кожи. Когда кератин разрушается, прочность кожи снижается, из-за чего она начинает шелушиться.
Также в эпидермисе содержатся корнеодесмосомы — белковые структуры, которые соединяют кератиноциты в сеть. В верхнем роговом слое кожи количество таких структур обычно уменьшается. Это нормальный физиологический процесс. Он называется десквамацией. Благодаря нему клетки кожи отшелушиваются, при этом поддерживается постоянная толщина рогового слоя [8] .
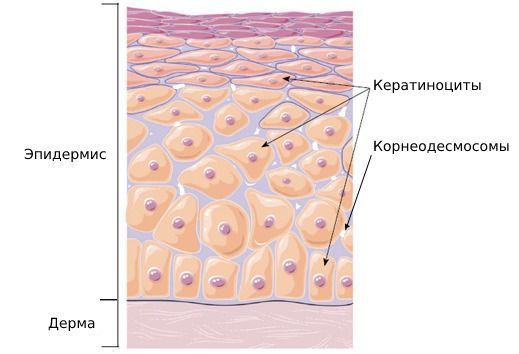
Исследование 24 пациентов с эксфолиативным кератолизом показало, что заболевание может возникать из-за дисбаланса активности ферментов, участвующих в процессе десквамации, особенно на коже ладоней [3] .
Точный механизм развития эксфолиативного кератолиза неизвестен. Прояснить возможные генетические или приобретённые причины заболевания помогут дальнейшие исследования десквамационных ферментов и ингибиторов — веществ, подавляющих или задерживающих течение ферментативных процессов. К таким веществам относятся ингибитор секреторной лейкоцитарной протеазы (SLPI), альфа-2 макроглобулин-1 (A2ML1), сульфат холестерина и ион цинка.
Классификация и стадии развития эксфолиативного кератолиза
По МКБ-10 (Международной классификации болезней) дерматологи часто кодируют эксфолиативный кератолиз как L26, относя заболевание к "другим эксфолиативным состояниям".
Классификации и стадийности эксфолиативный кератолиз не имеет. Заболевание иногда может приобретать хроническое течение с периодами ремиссии и обострения.
Осложнения эксфолиативного кератолиза
Эксфолиативный кератолиз не вызывает системных проявлений или осложнений. При заболевании может повреждаться кожа, в результате чего присоединяется бактериальная инфекция. Её признак — красные пятна, которые превращаются в гнойнички и пузырьки. Пузырьки безболезненные и легко вскрываются, образуются желтоватые чешуйки, так называемые "медовые корочки". При этом может возникать зуд.
Диагностика эксфолиативного кератолиза
Диагноз "эксфолиативный кератолиз" ставится на основании данных клинического обследования и сбора анамнеза [15] . Некоторые пациенты отмечают, что состояние усугубляется после воздействия химических или физических раздражителей, таких как вода, мыло и моющие средства. Другие ассоциируют шелушение кожи с повышенным потоотделением.
Эксфолиативный кератолиз, вероятно, распространён, но часто протекает бессимптомно, поэтому врачи его наблюдают редко.
При осмотре отмечаются симметричные округлые участки шелушения на ладонях и, реже, на стопах. При этом воспаление на коже отсутствует.
Обычно дополнительное диагностическое тестирование не требуется. Однако в более сложных случаях, при подозрении на грибковое поражение, может потребоваться исследование с гидроксидом калия (KOH).
Биопсия кожи при кератолизе показывает расщепление и частично разрушенные корнеодесмосомы в роговом слое.
Патч-тесты , оценивающие потенциальную контактную аллергию , при эксфолиативном кератолизе отрицательны.
Дифференциальную диагностику проводят со следующими заболеваниями:
- различные формы дерматита рук, включая контактный дерматит, — для него характерен зуд, воздействие провоцирующих факторов в анамнезе, положительный ответ на гормональные мази;
- дисгидроз — сопровождается зудом, появлением трещин и везикул, наполненных жидкостью; — бляшки с чёткими границами бордово-красного цвета, выступающие над поверхностью кожи;
- дерматофития рук — изменение ногтей на руках и ногах, положительный ответ на противогрибковые препараты, не всегда симметричное поражение;
- простой буллёзный эпидермолиз — пузыри на разных участках кожи младенцев, возникающие после трения;
- ограниченный ладонный гипокератоз — редкое состояние, характеризуется центральной розовой областью с тонкой кожей на ладонях или подошвах стопы, по краям резкий переход к нормальной коже;
- пальмоплантарная кератодерма — возникает на коже стоп и кистей, характеризуется выраженным утолщением кожи [11] ;
- синдром акрального шелушения кожи — генетическое заболевание с пожизненным отслаиванием кожи.
Лечение эксфолиативного кератолиза
Причин возникновения эксфолиативного кератолиза может быть несколько, и не всегда они очевидны. Поэтому лечение болезни направлено на устранение симптомов и усугубляющих факторов. Это достигается защитой рук от физических или химических раздражителей ношением перчаток, когда это возможно.
Активное увлажнение кожи — важный, безопасный и эффективный метод лечения [10] . Наиболее подходящим способом для большинства пациентов являются кератолитические кремы, содержащие мочевину, молочную кислоту, лактат аммония или салициловую кислоту. Кремы с мочевиной увлажняют кожу и предотвращают её сухость. Кремы могут содержать мочевину 20 % или 40 %, 12 % лактата аммония, 6 % салициловой кислоты и 12 % молочной кислоты. Любой из них применяют до двух раз в день.

Приём наружных гормональных препаратов (стероидов) не требуется, так как воспаление отсутствует.
В некоторых исследованиях упоминается использование фотохимиотерапии с псораленом и ультрафиолетовым светом (PUVA), но только при тяжёлых случаях, так как риски этой терапии превышают пользу [9] .
PUVA-терапия заключается в приёме пациентом фотоактивного материала псоралена с последующим воздействием на кожу UVA лучей. Данных, подтверждающих пользу фототерапии при эксфолиативном кератолизе, на сегодняшний день недостаточно.
Возможные побочные эффекты PUVA-терапии: покраснение кожи вплоть образования пузырей, зуд; к редкими побочными эффектам относятся головная боль, головокружение, учащённое сердцебиение и слабость [4] .
Также в литературе встречаются данные о лечении эксфолиативного кератолиза ацитретином [7] [14] . Но для рутинного применения ацитретина в качестве лечения кератолиза информации пока недостаточно. Ацитретин — это производное витамина А, которым лечат псориаз.
Прогноз. Профилактика
Прогноз благоприятный. Обычно симптомы эксфолиативного кератолиза проходят самостоятельно или после прекращения контакта с провоцирующим фактором. Спустя несколько недель или месяцев формируется здоровая кожа. Однако через несколько недель может возникнуть рецидив.
Иногда кератолиз приобретает хронический характер и длится много лет подряд. В таком случае заболевание трудно поддаётся лечению. С возрастом эксфолиативный кератолиз возникает реже [2] .
Меры профилактики:
- избегать веществ, которые способствуют шелушению, например растворителей, антибактериального мыла и некоторых тканей;
- соблюдать гигиену рук и ног с частой стрижкой ногтей — это поможет избежать вторичного инфицирования;
- использовать перчатки при контакте с химическими веществами;
- наносить увлажняющие кремы для рук, особенно полезны кремы, содержащие мочевину, молочную кислоту или силикон.

Роль продуктов питания в развитии эксфолиативного кератолиза не доказана, поэтому соблюдать диету не нужно.

Синдромы Стивенса–Джонсона и Лайелла – остро развивающиеся и опасные для жизни состояния, характеризующиеся обширным некрозом эпидермиса и эпителия слизистых оболочек с их последующей отслойкой. В США предлагают объединить эти состояния под общим названием эпидермальный некролиз (ЭН), при этом сам ЭН классифицируют на три группы в зависимости от площади отслойки эпидермиса: 1) синдром Стивенса–Джонсона, при котором отслойка эпидермиса составляет менее 10% площади поверхности тела; 2) переходный вариант между синдромом Стивенса-Джонсона и синдромом Лайелла – отслойка эпидермиса 10-30% площади поверхности тела и 3) синдром Лайелла (ТЭН) – более 30%.
Синонимы
синдром Лайелла – токсический эпидермальный некролиз (ТЭН); синдром Стивенса–Джонсона – дерматостоматит Бадера, злокачественная экссудативная эритема.
Эпидемиология
Возраст: любой, но чаще болеют люди старше 40 лет. Пол: не имеет значения, но есть указания, что женщины болеют несколько чаще мужчин. Частота встречаемости: синдром Стивенса–Джонсона: 1,2–6 случаев на 1 миллион человек в год. Синдром Лайелла 0,4–1,2 случая на 1 миллион человек в год.
Анамнез
От поступления в организм причинного агента (лекарственного препарата, продукта питания или другого вещества) до появления первых симптомов синдрома проходит различное время (от нескольких часов до нескольких недель). Заболевание начинается остро с продромальных явлений в виде лихорадки, гриппоподобного синдрома (слабости, головной боли, болей в мышцах и суставах) за 1–3 суток до появления высыпаний на коже и слизистых. Возможны также болезненность и жжение неизменённой на вид кожи, гиперемия, жжение и зуд конъюнктив, боли в горле. Впоследствии на коже появляется пятнисто-папулезная (кореподобная) сыпь или высыпания по типу полиморфной экссудативной эритемы, иногда – распространенная (сливная) эритема. На ранних стадиях участки некротизированного эпидермиса выглядят как воспалительные пятна с «гофрированной» поверхностью, впоследствии они увеличиваются в размерах и сливаются в сплошные очаги (при ТЭН). Развивается болезненная эритродермия (разлитое покраснение кожи), на фоне которой возникают дряблые пузыри и участки отслойки эпидермиса (в местах трения или давления кожи) с образованием легко кровоточащих обширных эрозий. Пораженная кожа приобретает вид ошпаренной кипятком (напоминает распространённый ожог II степени). Почти всегда в воспалительный процесс вовлекаются слизистые оболочки конъюнктив, реже – полости рта и половых органов, иногда носоглотки, пищевода, верхних дыхательных путей, желудочно-кишечного тракта, мочевого пузыря и уретры. Состояние больного становится тяжелым и требует проведения всего комплекса мероприятий интенсивной терапии.
Течение
заболевание прогрессирует в течение нескольких суток и во многом напоминает ожоговую болезнь. Прогноз зависит от распространенности некроза эпидермиса и степени выраженности метаболических нарушений во внутренних органах, а также от возможности присоединения вторичной бактериальной инфекции. У перенесших синдром Стивенса–Джонсона или синдром Лайелла повторное назначение того же препарата нередко вызывает рецидив. Реакция развивается быстрее (через несколько часов или суток) и по тяжести значительно превышает первую. Смертность при ЭН составляет около 30%, колеблясь от 5 до 12% при синдроме Стивенса-Джонсона и достигая 30% при ТЭН. Причины смерти: почечная недостаточность, бактериальные инфекции (сепсис), кахексия (из-за усиленного катаболизма), интерстициальная пневмония, желудочно-кишечные кровотечения. Предрасполагающие факторы: системная красная волчанка, наличие HLA-B12, ВИЧ-инфекция.
Этиология
- синдром Лайелла в 80% случаев, а синдром Стивенса–Джонсона в 50% случаев обусловлен лекарственными средствами. Наиболее часто синдром(ы) вызывают следующие медикаменты: противосудорожные средства (фенитоин, фенобарбитал, карбамазепин, ламотриджин), тетрациклины (доксициклин), пенициллины (бензилпенициллин, экстенциллин, амоксициллин, оксациллин), цефалоспорины (цефалексина, цефазолина, цефтриаксона), сульфаниламидные препараты (сульфадиметоксина, бисептола), антибактериальные препараты других групп (рифампицин, ванкомицин, офлоксацин, ципрофлоксацин, метронидазол, фурадонин), аллопуринол, нестероидные противовоспалительные средства (НПВС) (анальгин, аспирин, диклофенак, индометацин), других лекарственные препараты; - приём консервированной пищи (включая сосиски и рыбу); - работа с токсичными веществами (нитрокраски, растворители и др.); - контакт с бытовыми химическими веществами (средствами для мытья посуды, мылами, стиральными порошками); - герпес-вирусная инфекция, включая вирусы простого герпеса (1 и 2 типов), вирус опоясывающего лишая, цитомегаловирус и вирус Эбштейн-Бар; - кишечная инфекция, вызванная Shigella, Salmonella, Yersinia, Campylobacter; - Mycoplasma pneumoniae; - вакцинация;
Предрасполагающие факторы
Жалобы
На распространённые болезненные высыпания, сопровождающиеся жжением и зудом, иногда парестезиями. Характерна также болезненность нормальной на вид кожи, пациенты отмечают повышенную ранимость кожи к действию механических факторов. На коже и слизистых оболочках (конъюнктив, полости рта и реже – половых органов) возникает покраснение, а затем –эрозии и мокнутие вследствие отслойки эпидермиса (эпителия слизистой). Все больные отмечают ухудшение общего состояния (повышение температуры, озноб, общую слабость и недомогание), вялость, сонливость, похудание, головную боль, одышку, иногда тошноту и рвоту. Нередко беспокоит боль при глотании, гиперсаливация, светобоязнь, потеря (снижение остроты) зрения, болезненное мочеиспускание, насморк с гнойно-кровянистым отделяемым, носовые кровотечения. Могут выпадать ногти и волосы.
Дерматологический статус
патологический процесс носит распространенный или универсальный характер, захватывая кожу и слизистые оболочки, и располагается, как правило, симметрично, элементы кожной сыпи имеют тенденцию к слиянию с образованием сплошного очага, занимающего несколько анатомических областей.
Элементы сыпи на коже
- болезненные эритемы красного, розового, бурого или багрово-красного цвета, которые могут быть как равномерными, так и неравномерными (в центре - синюшными с розовым (красным) ободком по периферии), имеющие тенденцию к слиянию с такими же пятнами с развитием эритродермии. Форма пятен округлая или неправильная, границы ровные или нерезкие, при витропрессии (надавливании стеклом) пятна, как правило, исчезают полностью. На поверхности пятен нередко образуются вялые пузыри, быстро вскрывающиеся с образованием эрозий. Симптом Никольского (характеризуется отслойкой эпидермиса с образованием эрозии при трении пальцем кожи (эритем) вблизи пузырей) – положительный. В этом случае эпидермис сморщивается (симптом «смоченного белья») и сползает (симптом «сползания эпидермиса»), обнажая болезненную кровоточащую эрозивную поверхность. - вялые пузыри с серозным или серозно-геморрагическим содержимым, часто более 1 см в диаметре, расположенные на фоне воспалённой кожи, легко вскрывающиеся с образованием эрозий, нередко обширных, мокнущих (отделяющих серозный экссудат), легко кровоточащих или покрытых корками. Периферический симптом Никольского (характеризуется отслойкой эпидермиса с образованием эрозии при трении пальцем кожи вблизи пузырей) – положительный. Краевой симптом Никольского (определяется при потягивании за обрывки покрышки пузыря в виде отслойки эпидермиса) – положительный. Симптом Асбо-Хансена (увеличение пузыря по площади при надавливании на него пальцем) – положительный. Симптом груши (свисание пузыря, по форме напоминающее грушу, под тяжестью его содержимого при вертикальном положении тела) – положительный. Симптом периферического роста эрозий – положительный. - корки медово-желтого или бурого цвета, при удалении которых обнажаются эрозии; - болезненные эрозии (на месте вскрывшихся пузырей и/или на месте отслоившегося эпидермиса) размерами более 1 см в диаметре, имеющие тенденцию к периферическому росту (положительный симптом периферического роста эрозий), расположенные на фоне воспалённой или неизменённой кожи, обильно отделяющие серозный экссудат, склонные к кровоточивости при их малейшей травматизации. Эрозии разрешаются бесследно или с рубцеванием; - крупнопластинчатое (эксфолиативное) шелушение на поверхности воспалительных пятен (эритродермии) при разрешении патологического процесса. Чешуйки крупные (до 1 см в диаметре) серого цвета или цвета нормальной кожи.
Элементы сыпи на слизистых
- воспалительные эритемы ярко-красного цвета, имеющие равномерную окраску и исчезающие при витропрессии, имеющие тенденцию к периферическому росту и слиянию, образованию пузырей и эрозий на своей поверхности; - пузыри на поверхности воспалённой слизистой с напряжённой или дряблой покрышкой, размерами более 0,5 см, с серозным или серозно-геморрагическим содержимым. Пузыри настолько быстро вскрываются с образованием эрозий, что их почти не удается увидеть. - болезненные эрозии размерами более 0,5 см, располагающиеся на фоне воспалённой слизистой, отделяющие обильный серозный экссудат. Разрешение эрозий происходит или бесследно или с образованием рубцовых изменений слизистой. - образование плёнчатых налётов палевого цвета на поверхности эрозий; - нормо- (а-)трофические рубцы перламутрово-белого цвета или цвета нормальной слизистой на месте эрозий, очень часто - образование спаек (синехий) между веками и конъюнктивой; - редко корки бурого цвета (как правило, на губах) на поверхности эрозий.
Придатки кожи
ногти или не изменены, или все выпадают (тотальный онихолиз), возможно дуффузное поредение волос на голове или тотальная алопеция (полное выпадение волос на волосистой части головы и на лице (бровей, ресниц, бороды)).
Локализация
сначала вовлекаются лицо и конечности, затем сыпь становится генерализованной, особенно часто страдают участки кожи, подверженные трению и давлению. При синдроме Стивенса-Джонсона преимущественно поражаются слизистые оболочки: полости рта, конъюнктива глаз, реже – верхних дыхательных путей, а также кожа лица и туловища. При синдроме Лайелла отмечается генерализованное поражение кожи и слизистых оболочек.
Дифференциальный диагноз
Токсикодермии (пятнистая, папулезная или буллёзная), полиморфная экссудативная эритема, скарлатина, краснуха, инфекционный мононуклеоз, корь, фототоксическая реакция, стафилококковый синдром обваренной кожи (SSSS), реакция «трансплантат против хозяина», эксфолиативная эритродермия, распространенный ожог II степени.
Сопутствующие заболевания
ВИЧ-инфекция, микоплазменная пневмония, герпес-вирусная инфекция (включая инфекционный мононуклеоз), реакция трансплантат-против хозяина, состояние после трансплантации органов и тканей, сепсис, менингит (энцефалит), гепатит, диффузные болезни соединительной ткани (красная волчанка, дерматомиозит, склеродермия), кишечная инфекция, вызванная Shigella, Salmonella, Yersinia, Campylobacter.
Диагноз
Основан на клинической картине заболевания (при этом особое внимание уделяют положительному периферическому симптому Никольского) и анамнестических данных.
Патогенез
Полностью не изучен, однако известно, что в развитии как синдрома Стивенса-Джонсона, так синдрома Лайелла участвуют генетические факторы и иммунологические механизмы. Предполагается, что этиологический фактор или непосредственно оказывает цитотоксическое действие на кератиноциты, или изменяет их антигенные свойства, связываясь с их мембраной по типу гаптена. Ранняя стадия обоих синдромов характеризуется массивным апоптозом кератиноцитов, развивающимся под воздействием CD8+ Т-лимфоцитов (цитотоксических) при посредничестве перфорина и гранзима В. Установлено, что эта моноклональная экспансия CD8+ Т-лимфоцитов имеет отношение к специфической лекарственной цитотоксичности против кератиноцитов, связанной с главным комплексом гистосовместимости. В очагах поражения выявлены такие важные цитокины, как фактор некроза опухоли-α (TNF-α), интерлейкин 6 и Fas-лиганд. На поздних стадиях ЭН в зоне воспаления преобладают моноциты.
Материал подготовил: Раводин Роман Анатольевич, дерматовенеролог, дерматоонколог, дерматокосметолог. Доктор медицинских наук, доцент
Читайте также:

