При шанкриформной пиодермии регионарные лимфатические узлы исчезают
Обновлено: 18.04.2024
Для цитирования: Дворецкий Л.И. Лимфаденопатия: от синдрома к диагнозу. РМЖ. Медицинское обозрение. 2014;22(4):310.
В практике врачей различных специальностей нередко встречаются клинические ситуации, при которых выявляется увеличение периферических лимфоузлов (ЛУ), обнаруживаемое впервые либо самим пациентом, либо врачом во время осмотра. В подобных ситуациях возникает прежде всего дифференциально-диагностическая проблема, решение которой определяет тактику ведения больного. Увеличение размеров ЛУ, обозначаемое термином «лимфаденопатия» (ЛДП), является одним из симптомов целого ряда заболеваний, различных по своей причине, клиническим проявлениям, прогнозу, методам диагностики и лечения.
В основе увеличения размера ЛУ лежат различные патологические процессы, что определяет клиническую междисциплинарность синдрома ЛДП. В связи с этим реальными участниками диагностического процесса у пациента с наличием ЛДП могут становиться врачи различных специальностей (интернисты, инфекционисты, онкологи, гематологи, морфологи и др.). При этом успешное решение дифференциально-диагностической проблемы во многом зависит от конструктивного взаимодействия многих специалистов и их осведомленности о заболеваниях, проявляющихся увеличением ЛУ.
Основная проблема дифференциальной диагностики при ЛДП заключается прежде всего в сходстве клинической картины опухолевых и неопухолевых ЛДП. Лимфадениты и реактивные гиперплазии ЛУ являются важной составляющей синдрома ЛДП. По данным исследования в Гематологическом научном центре Минздравсоцразвития России, неопухолевые ЛДП составляют 30% среди причин первичных обращений к гематологу по поводу увеличенных ЛУ. Нозологический диагноз устанавливается лишь в 50% случаев у больных с неопухолевыми ЛДП.
Заболевания и патологические процессы, сопровождающиеся ЛДП
Основными патологическими процессами, вызывающими увеличение ЛУ, являются инфекции, опухолевые поражения (первичные или метастатические), иммунопролиферативные и дисметаболические процессы (рис. 1).
ЛДП инфекционного происхождения могут быть обусловлены непосредственным инфекционным поражением ЛУ с внедрением инфекционного агента гематогенным или лимфогенным путем в ткань ЛУ (туберкулез, актиномикоз, гнойные лимфадениты, вирусные инфекции) или реактивным воспалением в ответ на инфекционный очаг в соответствующей зоне (подмышечный лимфаденит при панариции, паховый лимфаденит при рожистом воспалении нижней конечности или генитальной инфекции, подчелюстной лимфаденит при ротоглоточной инфекции и т. д.). Четкое разграничение этих 2-х форм в известной степени условно и связано с уровнем диагностического обследования (морфологический, иммунологический, использование ПЦР и др.). При одной и той же инфекции ЛДП может носить как инфекционный, так и реактивный характер (первичный туберкулезный аффект, туберкулез ЛУ).
Опухолевое поражение ЛУ может быть первичным (лимфопролиферативные опухоли) либо вторичным – при лейкозах или раке (метастатический процесс). Опухолевые ЛДП составляют около 70% всех обращений больных в специализированные отделения по поводу увеличения ЛУ.
Иммунопролиферативные ЛДП. Этот термин не является общепринятым и может употребляться в тех случаях, когда увеличение ЛУ не связано ни с инфекцией, ни с опухолевым процессом. При этом в ЛУ происходит пролиферация иммунокомпетентных клеток или гранулематозное воспаление вследствие различных нарушений в системе клеточного, гуморального и неспецифического иммунитета.
Дисметаболические ЛДП обусловлены пролиферацией фагоцитирующих мононуклеаров в ЛУ или отложением амилоида при соответствующих заболеваниях.
Диагностический поиск у больных ЛДП
Направление диагностического поиска при ЛДП определяется прежде всего клинической ситуаций, т. е. информацией, полученной при первичном осмотре больного (анамнез, физикальное обследование), данными рутинного лабораторного исследования – главным образом показателями периферической крови. При дифференциальной диагностике ЛДП основными ориентирами являются:
- возраст больных;
- анамнестические сведения;
- характер ЛДП (локализация, распространенность, размеры, консистенция, болезненность, подвижность ЛУ);
- наличие других клинических признаков (увеличение селезенки, лихорадка, кожные высыпания, суставной синдром, поражение легких и др.);
- показатели периферической крови.
Каждый из вышеназванных признаков имеет различное и неоднозначное диагностическое значение. Так, лихорадка или анемия у больного с ЛДП могут быть проявлением не только инфекционного и опухолевого процесса, но и некоторых системных васкулитов (системная красная волчанка (СКВ), болезнь Стилла и др.). В то же время выявление в периферической крови бластных клеток практически однозначно свидетельствует о наличии у больного острого лейкоза и требует лишь уточнения его морфологического варианта. Диагностический поиск при ЛДП условно может включать несколько этапов, на каждом из которых решаются конкретные задачи для реализации конечной цели – нозологической диагностики у больного с наличием синдрома ЛДП.
I этап диагностического поиска. Выявление
увеличенного ЛУ и отличие его
от нелимфоидных образований
На данном этапе диагностического поиска при первичном обследовании больного следует отработать навыки и умения выявлять увеличенные ЛУ. При этом важным является умение отличать увеличенный ЛУ от нелимфоидных образований различной локализации. К таким нелимфоидным образованиям, представляющим трудности в дифференциальной диагностике, относятся кисты шеи, фибромы, липомы, добавочные дольки молочной железы, узлы щитовидной железы, гидраденит, увеличение околоушных слюнных желез и более редко встречающиеся нелимфоидные узловые образования (панникулит Вебера–Крисчена и др.). Нелимфоидные объемные образования в шейной и подмышечной областях встречаются почти в 5% случаев среди больных, направленных в специализированные учреждения в связи с «увеличением ЛУ».
II этап диагностического поиска.
Локализация и распространенность ЛДП
После верификации выявленного образования увеличенного ЛУ необходимо определить различную локализацию и оценить распространенность ЛДП. Это может иметь значение в определении направления дальнейшего диагностического поиска.
Локализация увеличенных ЛУ позволяет заподозрить круг заболеваний с целью проведения дальнейшего целенаправленного исследования. Так, заднешейные ЛУ обычно увеличиваются при инфекциях волосистой части головы, токсоплазмозе и краснухе, в то время как увеличение передних (околоушных) ЛУ предполагает инфекцию век и конъюнктивальной оболочки. Часто выявляемое местное увеличение шейных ЛУ является следствием инфекций верхних дыхательных путей, носоглотки, инфекционного мононуклеоза, однако при этом необходимо также исключать как лимфопролиферативные опухоли (лимфогранулематоз), так и метастазы в ЛУ опухолей различной локализации (голова и шея, легкие, молочная и щитовидная железы). В то же время увеличение надключичных и предлестничных ЛУ практически никогда не бывает реактивным, а чаще связано с лимфопролиферативными опухолями (лимфогранулематоз), метастатическим опухолевым процессом (опухоли желудка, яичников, легких, молочных желез).
В зависимости от распространенности следует различать следующие варианты ЛДП:
- локальная – увеличение одного ЛУ в одной из областей (единичные шейные, надключичные ЛУ);
- региональная – увеличение нескольких ЛУ одной или двух смежных областей (надключичные и подмышечные, надключичные и шейные, затылочные и подчелюстные ЛУ и т. д.);
- генерализованная – увеличение ЛУ трех и более областей (шейные, надключичные, подмышечные, паховые и др.).
При всей относительности такого разделения распространенность ЛДП может иметь значение при выдвижении предварительной диагностической гипотезы после первичного осмотра больного.
Анатомическое положение ЛУ при локализованной ЛДП позволяет во многих случаях сузить дифференциально-диагностический поиск. Так, например, для болезни кошачьих царапин характерно поражение шейных и подмышечных, а при инфекциях, передающихся половым путем, – паховых ЛУ. Увеличение одного ЛУ чаще требует исключения первичного или метастатического опухолевого процесса; может являться реактивным ответом на местный инфекционно-воспалительный процесс в соответствующей области (реактивный паховый лимфаденит при генитальных инфекциях, увеличение подчелюстных ЛУ при остром тонзиллите и т. д.). Регионарная ЛДП с преимущественным увеличением затылочных и заднешейных ЛУ более характерна для инфекционного мононуклеоза. Генерализованная ЛДП выявляется при различных заболеваниях: инфекционных (вирусные инфекции, токсоплазмоз), системных (СКВ), лимфопролиферативных опухолях (хронический лимфолейкоз).
Наряду с распространенностью ЛДП необходимо оценить размеры и консистенцию ЛУ. Это не является определяющими признаками, однако может служить обоснованием при выдвижении предварительной диагностической гипотезы (подозрение на опухолевый процесс при наличии плотного ЛУ размером более 1 см, болезненность при воспалении, флуктуация при абсцедировании и т. д.).
III этап диагностического поиска.
Выявление дополнительных признаков у больных ЛДП
При определении направления диагностического поиска важным является наличие у больного дополнительных клинических признаков, выявляемых при первичном осмотре (анамнестические, клинические) и проведении рутинного лабораторно-инструментального исследования (рентгенография грудной клетки, общий анализ крови).
Возраст больных может быть одним из ориентиров, определяющих направление диагностического поиска, поскольку ряд заболеваний, проявляющихся ЛДП, имеет определенную «возрастную привязанность». Известно, что инфекционный мононуклеоз чаще встречается в детском и юношеском возрасте, а хронический лимфолейкоз – у пожилых и стариков. Разумеется, возраст больного не может иметь решающего значения при постановке диагноза, он лишь служит одним из ориентиров.
Анамнестические сведения (травма конечностей, оперативные вмешательства, наличие имплантата, путешествия, контакт с некоторыми больными и т. д.) позволяют определить направление диагностического поиска, а в ряде случаев могут приобретать решающее значение при дифференциальной диагностике ЛДП (наличие у больного заболевания, проявляющегося увеличением ЛУ, прием некоторых медикаментов).
Клинические признаки. Необходимо тщательное клиническое обследование пациента с ЛДП с целью выявления различных дополнительных симптомов, среди которых диагностически наиболее важными являются:
- поражения кожи и слизистых (макулезно-папулезные высыпания, геморрагии, царапины, укусы, язвы и др.);
- увеличение печени;
- спленомегалия;
- суставной синдром;
- лихорадка;
- респираторная симптоматика;
- изменения со стороны ЛОР-органов;
- урогенитальные симптомы.
Выявление увеличенной селезенки у больного ЛДП более характерно для вирусных инфекций (инфекционный мононуклеоз), острого и хронического лимфолейкоза, системных заболеваний (СКВ, болезнь Стилла у взрослых). Суставной синдром чаще ассоциируется с системными заболеваниями (ревматоидный артрит, СКВ, болезнь Стилла). Наличие кожных высыпаний в первую очередь требует исключения вирусных инфекций, СКВ, болезни Стилла.
IV этап диагностического поиска.
Исследование периферической крови
Среди рутинных лабораторных методов дифференциальной диагностики у больных ЛДП обязательным является исследование показателей периферической крови. При трактовке выявленных изменений периферической крови необходимо учитывать их неодинаковую специфичность. Так, стойкий абсолютный лимфоцитоз с наличием клеток Гумпрехта является патогномоничным лабораторным признаком хронического лимфолейкоза, а наличие бластных клеток в крови может свидетельствовать либо о лимфобластном лейкозе, либо о лейкемизации лимфом. Такие признаки, как нейтрофильный лейкоцитоз, лейкопения (нейтропения), тромбоцитопения не являются специфичными, поскольку могут встречаться при более широком круге заболеваний, сопровождающихся ЛДП (табл. 1).
Наряду с общим анализом периферической крови при первичном обращении больного с ЛДП обязательными исследованиями являются: рентгенологическое исследование грудной клетки, УЗИ органов брюшной полости, иммуно-серологические исследования (сифилис, ВИЧ-инфекция, гепатит В и С). На рисунках 2 и 3 представлены алгоритмы диагностического поиска при локальных (регионарных) и генерализованных ЛДП.
Трудности дифференциальной диагностики при локальной или регионарной ЛДП заключаются прежде всего в умении выявлять местный воспалительный процесс инфекционного (чаще) или неинфекционного характера и ассоциировать выявленную местную патологию с увеличением ЛУ соответствующей области. Наиболее частыми местными воспалительными процессами, сопровождающимися увеличением регионарных ЛУ, на выявление которых необходимо ориентироваться, являются следующие:
- острый тонзиллит (тонзиллофарингит);
- стоматит;
- средние отиты;
- экземы лица, конечностей;
- конъюнктивит;
- острые тромбофлебиты конечностей;
- рожистое воспаление (лицо, конечности);
- фурункулы, карбункулы;
- панариции;
- царапины, укусы;
- воспалительный процесс наружных гениталий.
При выявлении местного воспалительного процесса у больных с увеличением регионарных ЛУ ситуация расценивается как реактивный лимфаденит. Методы цитологической и гистологической диагностики в острой фазе заболевания малоинформативны из-за трудностей трактовки морфологической картины на фоне реактивной гиперплазии лимфоидной ткани. Для окончательной верификации природы ЛДП необходима оценка динамики локального воспаления и регионарной ЛДП на фоне проводимой терапии (антибиотики, хирургическое лечение) или спонтанного обратного развития. В случаях сохраняющегося увеличения ЛУ, несмотря на регрессию местного воспалительного процесса, особенно при наличии ЛУ плотной консистенции, показана биопсия ЛУ для гистологического исследования. На рисунке 4 представлено диагностическое значение дополнительных клинических признаков, выявляемых при первичном осмотре у больных ЛДП.
Дополнительные методы обследования следует применять с учетом предварительной диагностической гипотезы, выдвинутой на основании характера ЛДП, наличия дополнительных признаков (анамнестических, клинических, лабораторных). Назначение антибиотиков больным с ЛДП показано только в случаях доказанной бактериальной инфекции. Применение глюкокортикоидов при неясных ЛДП нецелесообразно.
Глубокая пиодермия – группа гнойно-воспалительных поражений кожи (преимущественно ее глубоких слоев – дермы), обусловленных инфицированием тканей стафилококками, стрептококками или смешанной микрофлорой. Симптомы заболевания различаются в зависимости от выраженности воспаления и характера возбудителя, но обязательно включают в себя отек, болезненность, покраснение и образование гноя. Диагностика глубокой пиодермии основывается на внешних кожных проявлениях и микробиологических исследованиях для идентификации возбудителя. В лечении широко применяются хирургические приемы для обеспечения оттока гноя, местные и общие антибиотики, противомикробные и антисептические средства.
Общие сведения
Глубокая пиодермия – гнойное заболевание кожных покровов, особенностью которого является поражение дермы, подкожной клетчатки, глубоко расположенных волосяных фолликулов, потовых и сальных желез. Это состояние является одной из наиболее распространенных патологий в дерматологии – по разным данным, на нее приходится от 30 до 40% всех дерматологических заболеваний. Практически каждый человек минимум несколько раз в жизни страдал от проявлений различных форм глубокой пиодермии. Это объясняется высокой распространенностью возбудителей (стафилококков и стрептококков), их вирулентностью, огромным разнообразием штаммов. В большинстве случаев глубокая пиодермия не угрожает жизни человека и даже излечивается самостоятельно без специальной терапии, но иногда она может быть причиной интоксикации, источником метастатических гнойных очагов и даже причиной сепсиса.

Причины глубокой пиодермии
В широком плане, глубокая пиодермия – поражение кожи, обусловленное гноеродной микрофлорой, к которой относят стафилококков, стрептококков, синегнойную палочку и некоторые другие микроорганизмы. Однако более 95% случаев заболевания вызываются именно кокковой флорой, так как она широко распространена в окружающей среде и отчасти представлена даже на поверхности кожи здорового человека. При проникновении в ткани кожи через микротрещины, повреждения эпидермиса, вдоль волосяных стержней и по протокам кожных желез микроорганизмы начинают бурно размножаться. Выделяемые ими в процессе жизнедеятельности ферменты и различные токсины вызывают деструкцию клеток кожи. В результате этих процессов формируется первичный очаг, расположенный в дерме – симптомов глубокой пиодермии на этом этапе не наблюдается.
Сами микроорганизмы и выделяемые ими ферменты обладают сильными иммуногенными свойствами, поэтому практически сразу после формирования первичного очага происходит незамедлительная реакция иммунной системы. Традиционно первыми на инфицирование реагируют тканевые макрофаги, затем путем хемотаксиса в будущий очаг глубокой пиодермии попадают нейтрофилы, а затем и другие иммунокомпетентные клетки. Выделяемые ими биологически активные вещества приводят к местному отеку, покраснению, появлению болезненных ощущений. Клинически это соответствует первой стадии глубокой пиодермии – образованию воспалительного очага, который может иметь тенденцию к расширению.
На определенном этапе иммунитету удается локализовать воспаление, и его распространение в тканях останавливается. Нейтрофилы атакуют патогенные микроорганизмы и отчасти собственные ткани (вторичная альтерация) в очаге с формированием гноя – субстанции, состоящей из «осколков» возбудителей, разрушенных собственных клеток и погибших нейтрофилов. Развитие глубокой пиодермии облегчается при ряде обстоятельств – пониженном иммунитете, сахарном диабете, истощении, гиповитаминозах и других ослабляющих организм состояниях. Немаловажную роль играет пренебрежение правилами личной гигиены, избыточная продукция кожного сала, местное переохлаждение кожи. Для лиц с пониженным иммунитетом глубокая пиодермия опасна тем, что способна вызывать сильные поражения, стать причиной различных осложнений, некоторые из которых могут напрямую угрожать жизни человека.
Симптомы глубокой пиодермии
Существует несколько клинических разновидностей глубокой пиодермии, которые характеризуется разными возбудителями, выраженностью симптомов и типом поражаемых тканей. Все формы этого заболевания по характеру микрофлоры, вызвавшей воспаление, делят на стафилодермии, стрептодермии и смешанные разновидности, которые иногда называют стрептостафилодермиями. К глубоким пиодермиям, вызванным стафилококками, относят фурункулы, карбункулы, гидрадениты и глубокий фолликулит. Глубокие стрептодермии представлены вульгарной эктимой, а воспаления из-за смешанной микрофлоры – хронической язвенно-вегетирующей пиодермией.
Фурункул – разновидность глубокой пиодермии, особенностью которой является поражение волосяного фолликула гнойно-некротического характера с переходом на окружающие ткани. Его развитию может предшествовать поверхностное гнойное воспаление (фолликулит), однако возможно и первичное развитие глубокого процесса. На участке кожи, окружающей волос, формируется сначала очаг багрового цвета размером от нескольких миллиметров до 1-2 сантиметров, болезненный и плотный, его температура заметно выше окружающих кожных покровов. Затем глубокая пиодермия такого типа сопровождается появлением гноя, в центре которого будет стержень из некротизированной ткани. Гнойно-некротическое содержимое отторгается через 3-10 дней, на месте поражения кожи формируется небольшая язва, которая быстро рубцуется.
Карбункул – более тяжелая разновидность глубокой пиодермии, вызываемая стафилококковой флорой и характеризующаяся поражением глубоких слоев дермы и подкожной жировой клетчатки. В глубине кожи возникает плотный инфильтрат, кожные покровы над ним приобретают синюшно-багровый оттенок, становятся горячими и болезненными. Через несколько дней в очаге глубокой пиодермии начинают формироваться пустулы, происходит выделение гноя и некротических стержней, на месте поражения образуется язва. Все это сопровождается выраженными общими симптомами – интоксикацией, лихорадкой, болями стреляющего характера в месте карбункула. Отмечается регионарный лимфаденит и лимфангит. После разрешения этой формы глубокой пиодермии на месте поражения остается заметный рубец.
Гидраденит – форма глубокой пиодермии, при которой поражаются апокриновые потовые железы с развитием гнойного воспаления. Из-за этого характерная локализация патологических очагов – подмышечные впадины, околососковая и аногенитальная области. Гидраденит начинается с развития болезненного узла синюшного цвета, который за несколько дней значительно увеличивается в размерах и самопроизвольно вскрываются с выделением обильного количества гноя. Затем происходит постепенное заживление, рубцы образуются в крайне редких случаях. При этой форме глубокой пиодермии также отмечается регионарный лимфаденит и лимфангит, но общие симптомы выражены слабо. Гидрадениты, особенно в области подмышечных впадин, склонны к частым рецидивам.
Глубокий фолликулит – одна из наиболее легких форм глубокой пиодермии, которая отличается от обычного фолликулита более выраженным поражением волосяных луковиц. Симптоматика в целом сходна с фурункулом, однако проявления менее выраженные, общих симптомов практически никогда не наблюдается. Главный диагностический критерий, позволяющий дерматологу отличить фурункул от глубокого фолликулита – отсутствие гнойно-некротического воспаления, так как не образуется характерный некротический стержень.
Вульгарная эктима – форма глубокой пиодермии, вызываемая стрептококковой микрофлорой. Чаще всего поражает кожу голени у ослабленных больных, в крайне редких случаях возникает у здоровых людей. Эктима начинается с образования на поверхности кожных покровов пустулы с мутным содержимым серозного, иногда геморрагического характера. Затем пустула исчезает и на ее месте формируется типичный очаг глубокой пиодермии – болезненная язва с выраженным воспалительным ободком вокруг, дно образования покрыто слоем гноя. Через 2-3 недели после появления язвы начинается ее постепенное рубцевание с развитием заметного шрама.
Хроническая язвенно-вегетирующая пиодермия – кожное заболевание, возбудителями которого является смешанная микрофлора, наибольшую роль в развитии патологии играет золотистый стафилококк и стрептококки группы А. Глубокая пиодермия такого типа чаще всего развивается у ослабленных больных – истощенных лиц, страдающих алкоголизмом, пожилых людей. Характеризуется образованием на нижних конечностях эрозий неправильной формы с рваными краями, окруженных воспаленной кожей. Дно язвенных образований покрыто гноем, часто возникают выделения с неприятным зловонным запахом. Эрозии длительное время не заживают и склонны к частым рецидивам или поражению других участков кожных покровов.
Осложнениями любой разновидности глубокой пиодермии могут быть метастатические гнойные поражения регионарных лимфатических узлов и отдаленных органов. Особенно опасны в этом отношении глубокие фолликулиты и фурункулы, возникающие в пределах носогубного треугольника – имеющиеся там анастомозы кровеносных сосудов способствуют заносу инфекции в головной мозг и его оболочки. У ослабленных больных на фоне глубокой пиодермии могут возникать флегмоны и сепсис, являющиеся жизнеугрожающими состояниями. В редких случаях возможно развитие токсического шока.
Диагностика глубокой пиодермии
Диагностика различных форм глубокой пиодермии осуществляется посредством осмотра дерматолога (иногда может потребоваться консультация хирурга). Из дополнительных методов исследования наиболее часто применяют посев гноя для определения характера возбудителя и для выяснения его чувствительности к антибактериальным средствам. При развитии общих симптомов также в ряде случаев необходимо проведение общего анализа крови, в самых тяжелых случаях – бакпосев крови для диагностики сепсиса. Результаты осмотра зависят от формы глубокой пиодермии и стадии ее развития – это может быть просто воспалительный очаг, сформировавшийся гнойник, ранка или язва с гнойным отделяемым. При посеве определяются стафилококки или стрептококки, может обнаруживаться смешанная микрофлора. Микробиологические исследования посевов могут определить вид и штамм возбудителя, а также его чувствительность к антибиотикам.
Если имеется повышение температуры, головная боль, слабость то необходимо проведение общего анализа крови. Обычно при глубокой пиодермии определяются легкие неспецифические признаки воспаления – повышение скорости оседания эритроцитов, небольшой лейкоцитоз. В более тяжелых случаях наблюдаются уже выраженные изменения – значительный рост СОЭ, выраженный лейкоцитоз, выявляются изменения в распределении нейтрофилов. В крови появляется множество юных форм этой фракции лейкоцитов, что носит название нейтрофильного сдвига влево. Если есть подозрения, что глубокая пиодермия стала причиной сепсиса, производят посев крови на питательные среды – в норме кровь человека абсолютно стерильна, рост культур говорит о наличии возбудителя в крови. Для диагностики таких осложнений, как метастатические гнойные очаги могут применяться ультразвуковые, рентгенологические и другие методы клинических исследований.
Лечение глубокой пиодермии
При незначительных по выраженности гнойных поражениях без общих проявлений интоксикации рекомендуется ждать самопроизвольного разрешения глубокой пиодермии. Лечебные мероприятия сводятся к недопущению осложнений. При наличии волос вокруг гнойного очага их нужно аккуратно состричь – использование бритвы может привести к распространению инфекции. Мыть участок с очагом глубокой пиодермии не рекомендуется, допустимо только протирать кожу вокруг него дезинфицирующими растворами (хлоргексидином, раствором салициловой кислоты). Строго запрещается без участия дерматолога или хирурга самостоятельно вскрывать гнойник или каким-либо способом ускорять отделение гноя – это может привести к диссеминации возбудителя.
Если глубокая пиодермия характеризуется развитием крупных очагов с появлением общих симптомов (лихорадка, слабость, головные боли), то необходимо назначение антибактериальных средств, таких как эритромицин, тетрациклин, линкомицин – предварительно желательно сделать бактериальный посев и определить препарат, к которому наиболее чувствителен данный микроорганизм. Также при глубокой пиодермии применяют и противомикробные средства из группы сульфаниламидов – например, сульфаметоксазол+триметоприм. В последние годы в тяжелых случаях гнойных поражений кожи используют и иммунологические препараты – стафилококковый анатоксин, антистафилококковую гипериммунную плазму и ряд других.
При глубоком расположении значительного по размерам очага пиодермии прибегают к хирургическому вскрытию полости гнойника для формирования дренажа и оттока гноя. Кроме того, это позволяет доставлять антисептические и антибактериальные препараты непосредственно в область поражения, что ускоряет лечение. Вскрытие очага глубокой пиодермии должно происходить в стерильном помещении и осуществляться квалифицированным гнойным хирургом.
Прогноз и профилактика глубокой пиодермии
В большинстве случаев прогноз при развитии различных форм глубокой пиодермии благоприятный – после отделения гноя происходит заживление очага, довольно часто с образованием рубцов. Однако у ослабленных больных с низким уровнем иммунитета возможно развитие осложнений, некоторые из которых могут угрожать жизни и требуют лечения в условиях стационара. Для профилактики развития глубокой пиодермии необходимо придерживаться правил личной гигиены, своевременно обрабатывать кожные повреждения (ссадины, порезы) антисептиками. Кроме того, важно устранять возможные источники инфекции в организме – кариозные зубы, хронические инфекции ЛОР-органов.
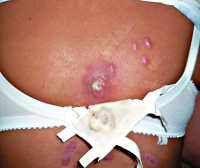
Шанкриформная пиодермия – это атипичное гнойно-воспалительное поражение кожи, характеризующееся схожестью клинических проявлений с сифилитическим твердым шанкром, что нашло отражение в названии. Симптомом этого заболевания является развитие одиночной язвы (реже множественных образований), чаще всего локализованной в области половых органов или на красной кайме губ, подбородке, шее. Диагностика шанкриформной пиодермии производится серологическими и микробиологическими методиками, вспомогательную роль также играют общеклинические анализы крови, дерматологический осмотр. Лечение данной патологии производят антибиотиками, антисептиками, противомикробными средствами.
МКБ-10
Общие сведения
Шанкриформная пиодермия – редкое дерматологическое заболевание гнойно-воспалительного характера, которое относится к хроническим язвенным стрептостафилодермиям (смешанным пиодермиям). Впервые данная патология была описана в 1934-м году Хоффманном, который отметил значительную схожесть ее клинических проявлений с твердым шанкром при сифилисе. В ряде случаев это обстоятельство приводило к неправильной диагностике и, как следствие, к неверному лечению шанкриформной пиодермии. Эта форма стрептостафилодермии встречается достаточно редко, с одинаковой частотой поражает как мужчин, так и женщин.
В клинической дерматологии шанкриформная пиодермия относится к атипичным разновидностям глубоких гнойно-воспалительных поражений кожи, к которым также причисляют язвенно-вегетирующую пиодермию и пиогенную гранулему. Заболевание может появиться в любом возрасте, немаловажную роль в его развитии играет снижение активности иммунитета и наличие других гнойных поражений кожи или иных органов.

Причины
Возбудителями шанкриформной пиодермии являются представители смешанной микрофлоры – чаще всего в язвах определяется золотистый стафилококк и различные представители стрептококков. Пути проникновения:
- через микроповреждения кожи, ссадины (в том числе и расчесы при чесотке или других заболеваниях, сопровождающихся зудом);
- в редких случаях возможен занос инфекции гематогенным путем.
Предрасполагающими факторами к развитию этой патологии служат снижение активности иммунитета в результате сахарного диабета, неправильного питания, изнурительных заболеваний. У мужчин шанкриформная пиодермия чаще развивается на фоне фимоза. Облегчает заражение несоблюдение правил личной гигиены.
Патогенез
После проникновения в ткани бактерии начинают бурно размножаться, возникает воспаление, что и приводит в конечном итоге к характерной клинической картине заболевания. На сегодняшний день достоверно неизвестны причины того, почему гнойно-воспалительный процесс при шанкриформной пиодермии протекает именно таким путем – предположительно, это связано с особенностями реактивности организма. Четкой взаимосвязи между этим заболеванием и определенными группами микроорганизмов выявить не удалось. По этой причине шанкриформная пиодермия относится к атипичным гнойно-воспалительным поражениям кожи.
Симптомы шанкриформной пиодермии
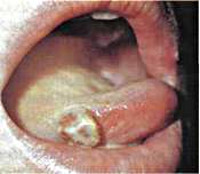
Шанкриформная пиодермия может возникать как у мужчин, так и у женщин разных возрастов. Чаще всего воспалительный процесс проявляется в области половых органов (на головке полового члена и крайней плоти у мужчин, половых губах и влагалище у женщин), но изредка возможна и другая локализация. Описаны случаи развития шанкриформной пиодермии на губах, подбородке, шее, слизистой оболочке полости рта. Наиболее часто эта патология возникает на фоне иных дерматологических или общих заболеваний, способствующих снижению иммунитета (например, сахарный диабет) или облегчающих заражение (другие формы пиодермии, чесотка).
Первоначально при шанкриформной пиодермии на поверхности кожи образуется пузырек размером 0,5-2 сантиметра, заполненный серозным содержимым. Довольно быстро (нередко – в первые часы после образования) он разрушается, обнажая эрозивное дно, на месте которого затем развивается язва диаметром 1-2 сантиметра. Никаких субъективных симптомов (зуд, болезненность, жжение) это образование при шанкриформной пиодермии не имеет, что придет ему дополнительную схожесть с твердым шанкром. Дно язвы чистое ярко-розовое или покрыто темными корками, имеется гнойное или геморрагическое отделяемое. Вокруг нее может определяться узкий воспалительный ободок.
Из других проявлений шанкриформной пиодермии наиболее часто отмечается наличие плотного инфильтрата в коже, расположенного под язвой, регионарный лимфаденит, иногда может возникать повышение температуры. Лимфаденит проявляется увеличением регионарных лимфатических узлов (паховых, шейных), их болезненностью при пальпации, но при этом они не спаяны с окружающими тканями и между собой. Повышение температуры при шанкриформной пиодермии регистрируется крайне редко, лихорадка может свидетельствовать об осложнении заболевания – присоединении сепсиса, метастатического переноса возбудителя с развитием абсцессов во внутренних органах.
Диагностика
Диагностика шанкриформной пиодермии в основном сводится к определению возбудителя этого заболевания и исключению сифилиса. Для этой цели применяют серологические, микробиологические и дерматологические методы исследования. Реакция Вассермана при шанкриформной пиодермии отрицательная, при микробиологическом изучении отделяемого из язв в нем отсутствуют бледные трепонемы, а содержатся только стафилококки и стрептококки.
Дерматолог при осмотре выявляет язву, локализованную чаще всего в области половых органов, при расспросе выясняется, что субъективные симптомы отсутствуют. Гистологическое исследование (при шанкриформной пиодермии производится только при стертой и неясной симптоматике) выявляет выраженный отек дермы, акантоз, диффузную инфильтрацию, состоящую, главным образом, из нейтрофилов и лимфоцитов.
Лечение шанкриформной пиодермии
К лечению шанкриформной пиодермии допустимо приступать только после точного и достоверного подтверждения диагноза и исключения сифилиса. Применяют как местные антисептические и антибактериальные средства в виде мазей и растворов, так и системные антибиотики.
- Чаще всего при заболевании применяют пенициллины, макролиды, тетрациклины, из других противомикробных средств – сульфаниламиды. Для наибольшей эффективности противомикробной терапии при шанкриформной пиодермии необходимо еще на этапе диагностики провести тесты на чувствительность возбудителей к различным антибиотикам.
- Важно повысить уровень иммунитета, поэтому в лечении больных используют витамины, иммуностимуляторы, нормализуют рацион и режим сна.
- Местно назначают растворы анилиновых красителей, хлоргексидин, для ускорения заживления и эпителизации назначают растворы и мази на основе гиалоруната цинка и биогенных стимуляторов.
- Физиотерапевтические методы лечения (УФО пораженной области, СВЧ-прогревание) также приводит к более быстрому заживлению язв при шанкриформной пиодермии.
Прогноз и профилактика
Прогноз при шанкриформной пиодермии обычно благоприятный – при правильно назначенном лечении гнойно-воспалительный процесс затухает, а эрозия заживает. При этом в случае ее развития на кожных покровах может оставаться более или менее заметный рубец, тогда как при локализации на слизистых оболочках язва заживает бесследно. Ухудшается прогноз шанкриформной пиодермии при наличии иммунодефицита, сахарного диабета и других подобных состояний – в этих случаях лечение патологии занимает много времени, а также повышается риск осложнений: новых язв, других форм пиодермии, сепсиса.
Для профилактики шанкриформной пиодермии следует придерживаться правил личной гигиены, поддерживать оптимальный уровень иммунитета, своевременно выявлять и лечить заболевания, способствующие развитию этого состояния.

Шанкриформная пиодермия – это атипическая пиодермия, вызываемая стафилококками и стрептококками, которая клинически напоминает сифилитический твердый шанкр.
Синонимы
Эпидемиология
Возраст: любой, но чаще в 17-50 лет.
Анамнез
Заболевание начинается с образования пузырька или пустулы, после вскрытия которых образуется поверхностная блюдцеобразная эрозия или язва округлой или овальной формы около 1-2 см в диаметре с уплотненным основанием и ровными приподнятыми краями. Дно её красного цвета, содержит серозное отделяемое, иногда покрыто сероватым (гнойным) налётом. Вокруг язвы (эрозии) нередко возникает узкий венчик гиперемии. Язва (эрозия) малоболезненна или вовсе безболезненна при пальпации. Поражение чаще всего одиночное, реже множественное. Регионарные лимфатические узлы, как правило, увеличиваются, оставаясь при этом безболезненными (или слегка болезненными) и подвижными при пальпации.
Течение
острое или постепенное начало с последующим персистирующим течением до нескольких недель (в среднем, около 6-8 недель), патологический процесс разрешается самостоятельно, а также под действием антимикробных препаратов.
Этиология
возбудителями шанкриформной пиодермии являются золотистый стафилококк и стрептококки.
Предрасполагающие факторы
- пиодермии в анамнезе;
- пиодермии у членов семьи;
- травматизация (повреждение) кожи (слизистой);
Жалобы
На наличие безболезненной или практически безболезненной язвы (эрозии) на слизистых оболочках половых органов (реже – в полости рта или на коже), нередко – увеличение регионарных лимфоузлов, которые при этом имеют плотноэластическую консистенцию, не спаиваются с окружающими тканями и остаются безболезненными.
Дерматологический статус
процесс поражения кожи (слизистой) носит, как правило, ограниченный характер и представлен чаще всего одиночным высыпанием (реже встречаются множественные высыпания).
Элементы сыпи на коже
- безболезненная блюдцеобразная язва, развивающаяся из пузырька или пустулы, достигающая 1-2 см в диаметре, с чистым, реже гнойным дном. В основании язвы имеется уплотнение в виде пластинки или узла хрящевой плотности, выходящее за её пределы, вокруг она окружена узким венчиком гиперемии (реже располагается на фоне неизменённой кожи). В неизменном виде язва существует несколько недель, а в дальнейшем рубцуется.
- реже может встречаться безболезненная блюдцеобразная эрозия, развивающаяся из пузырька или пустулы, достигающая 1-2 см в диаметре, с чистым, реже гнойным дном. В основании эрозии имеется уплотнение в виде пластинки или узла хрящевой плотности, выходящее за её пределы, вокруг эрозия окружена узким венчиком гиперемии (реже располагается на фоне неизменённой кожи). В неизменном виде эрозия существует несколько недель, а в дальнейшем либо трансформируется в язву, либо бесследно разрешается.
Элементы сыпи на слизистых
- безболезненная блюдцеобразная язва, развивающаяся из пузырька или пустулы, достигающая 1-2 см в диаметре, с чистым, реже гнойным дном. В основании язвы имеется уплотнение в виде пластинки или узла хрящевой плотности, выходящее за её пределы, вокруг она окружена узким венчиком гиперемии (реже располагается на фоне неизменённой слизистой). В неизменном виде язва существует несколько недель, а в дальнейшем рубцуется.
- реже встречается безболезненная блюдцеобразная эрозия, развивающаяся из пузырька или пустулы, достигающая 1-2 см в диаметре, с чистым, реже гнойным дном. В основании эрозии имеется уплотнение в виде пластинки или узла хрящевой плотности, выходящее за её пределы, вокруг эрозия окружена узким венчиком гиперемии (реже располагается на фоне неизменённой слизистой). В неизменном виде эрозия существует несколько недель, а в дальнейшем либо трансформируется в язву, либо бесследно разрешается.
Придатки кожи
Локализация
в области гениталий (у мужчин на головке полового члена, в венечной борозде и на крайней плоти, у женщин на больших и малых половых губах и на слизистой влагалища) и экстрагенитально (на подбородоке, спинке носа, веках, бровях, на красной кайме губ, на слизистой оболочке полости рта: на щеках, языке, в углах рта).
Дифференциальный диагноз
Твёрдый шанкр, мягкий шанкр, венерическая лимфогранулема, эрозивный баланопостит, эктима, афтозный стоматит.
Сопутствующие заболевания
лимфаденопатия регионарных лимфатических узлов, пиодермии (гнойничковые заболевания кожи), носительство S. аureus.
Диагноз
Клиническая картина, подтверждённая отрицательными результатами серологической диагностики и микроскопии, а также данными гистологического исследования.
Патогенез
Материал подготовил: Раводин Роман Анатольевич, дерматовенеролог, дерматоонколог, дерматокосметолог. Доктор медицинских наук, доцент
Предусматривает назначение антибиотиков в течение 10-14 дней в средних терапевтических дозировках:
Антибиотики группы пенициллина
- Бензилпенициллина натриевая соль 100 000; 125 000; 200 000; 250 000; 300 000; 500 000; 1 000 000 ЕД — детям в/м 25 000 — 50 000 Ед/кг массы тела в сутки, взрослым — 2 000 000 – 12 000 000 ЕД в сутки в/м. Препарат вводят каждые 4–6 часов. Курс лечения 7–10 дней или,
- Амоксициллина тригидрат 250; 500 мг — детям в возрасте до 2 лет — 20 мг/кг массы тела в сутки, от 2 до 5 лет — по 125 мг 3 раза в сутки, от 5 до 10 лет — по 250 мг 3 раза в сутки, старше 10 лет и взрослым по 500 мг 3 раза в сутки. Курс лечения 7–10 дней или,
- Амоксициллин 125; 250; 500 мг — детям в возрасте до 3 лет — 30 мг/кг/сут в 2–3 приема, от 3 до 10 лет — по 375 мг 2 раза в сутки, детям старше 10 лет и взрослым — по 500–750 мг 2 раза в сутки. Курс лечения 7–10 дней или,
- Амоксициллин тригидрат + клавулановая кислота 250+125 мг; 500+125 мг; в форме суспензии 125+31 мг (5 мл); суспензия форте 250+62,5 мг (5 мл) — детям от 3 месяцев до года по 2,5 мл суспензии 3 раза в сутки, от 1 года до 7 лет — по 5 мл суспензии 3 раза в сутки, от 7 до 14 лет — по 10 мл суспензии или по 5 мл суспензии форте 3 раза в сутки, детям старше 14 лет и взрослым — по 375–625 мг (1 табл.) 3 раза в сутки. Курс лечения 7–10 дней или,
- Оксациллина натриевая соль 250 мг и 500 мг таблетки и капсулы; порошок для инъекционных растворов во флаконах по 250 мг и 500 мг (в пересчёте на оксациллин) в комплекте с растворителем. Новорождённым дают внутрь по 90-150 мг/кг/сут, детям до 3 мес назначают в среднем до 200 мг/кг/сут, от 3 мес до 2 лет – 1 г/сут, от 2 до 6 лет – 2 г/сут, при этом суточную дозу делят на 4-6 приёмов. Взрослым и детям старше 6 лет назначают внутрь по 2-4 г/сут (в 4 приёма), при тяжёлых инфекциях дозу увеличивают до 6-8 грамм в сутки. При невозможности приёма препарата внутрь или его недостаточной эффективности при таком способе введения переходят на внутримышечное или внутривенное введение. Суточная доза для взрослых и детей старше 6 лет составляет 4-12 г (в 4-6 приёмов), для новорожденных и недоношенных детей – 20-40 мг/кг, для детей до 3 мес – 60-80 мг/кг, от 3 мес до 2 лет – 1 г, от 2 до 6 лет – 2 г.
Антибиотики группы цефалоспоринов
- Цефалексин 250; 500 мг — детям с массой тела менее 40 кг — 25–50 мг/кг/сут, взрослым по 250 — 500 мг 4 раза в сутки. Курс лечения 7–14 дней или,
- Цефадроксил 250 мг в 5 мл — детям с массой тела менее 40 кг — 25–50 мг/кг/сут, детям с массой тела более 40 кг и взрослым — 1–2 г в 1–2 раза в сутки. Курс лечения — 7–14 дней или,
- Цефазолин 500 мг; 1 г — детям 20–40 мг/кг/сут, суточная доза для взрослых — 1г. Частота введения 2–4 раза в сутки. Курс лечения 7–10 дней или,
- Цефаклор 125; 250; 500 мг — детям в возрасте до 6 лет 30 мг/кг/сут в 3 приема, от 6 до 10 лет — по 250 мг 3 раза в сутки, детям старше 10 лет и взрослым — по 500 мг 3 раза в сутки. Курс лечения 7–10 дней или,
- Цефуроксим 125, 250 мг; 750 мг, 1,5 г во флаконах в/м или в/в. При приеме внутрь — детям по 125–250 мг 2 раза в сутки, взрослым по 250–500 мг 2 раза в сутки. Кратность приема — 2 раза в сутки. При парентеральном введении — детям до 3 месяцев — 30 мг/кг/сут 2–3 раза в сутки, детям старше 3-х месяцев — 60 мг/кг/сут 3–4 раза в сутки, взрослым по 750 мг — 1,5 г 3 раза в сутки или,
- Цефиксим 100 мг (5 мл); 200; 400 мг — детям в возрасте до 12 лет — 8 мг/кг 1 раз в сутки в форме суспензии, детям старше 12 лет и взрослым — 400 мг 1 раз в сутки. Курс лечения 7–10 дней или,
- Цефотаксим 1 г в/м или в/в — детям с массой тела менее 50 мг — 50–100 мг/кг/сут с интервалом введения 6–8 часов, детям с массой тела более 50 кг и взрослым 2–6 г в сутки с интервалом введения 8–12 часов. Курс лечения 5–10 дней или,
- Цефтриаксон 250 мг; 1 г; 2 г в/м — детям в возрасте до 12 лет —50–75 мг/кг/сут 1 раз в сутки, детям старше 12 лет и взрослым — 1–2 г 1 раз в сутки. Курс лечения 7–10 дней или,
- Цефепима дигидрохлорида моногидрат 500 мг; 1 г в/м — детям с массой тела менее 40 кг — 100 мг/кг/сут, детям с массой тела более 40 кг и взрослым — 2 г в сутки. Частота введения 2 раза в сутки с интервалом 12 часов. Курс лечения 7–10 дней.
Антибиотики группы макролидов
- Эритромицин 200 мг — детям в возрасте до 3 месяцев — 20–40 мг/кг/сут, детям в возрасте от 3 месяцев до 18 лет — 30–50 мг/кг/сут, старше 18 лет — суточная доза 1–4 г. Кратность приема 4 раза в сутки. Курс лечения — 5–14 дней или,
- Азитромицин 125 (5 мл); 250; 500 мг — детям из расчета 10 мг/кг массы тела 1 раз в сутки в течение 3-х дней или в 1-й день 10 мг/кг, затем в течение 4 дней 5 мг/кг массы тела 1 раз в сутки, взрослым — 1 г в 1-й день, затем со 2-го по 5-й день 500 мг 1 раз в сутки или,
- Кларитромицин 125 (5 мл); 250; 500 мг — детям — 7,5 мг/кг/сут, взрослым — 500–1000 мг в сутки. Кратность приема 2 раза в сутки. Курс лечения — 7–10 дней.
Антибиотики группы тетрациклина
Доксициклина гидрохлорид, моногидрат 100 мг — детям старше 12 лет с массой тела менее 50 кг в 1-й день — 4 мг/кг массы тела 1 раз в сутки, в последующие дни — 2 мг/кг массы тела 1 раз в сутки. Детям старше 12 лет с массой тела более 50 кг и взрослым — в первые сутки 200 мг однократно, затем по 100 мг 1 раз в сутки. Курс лечения — 10–14 дней.
Фторхинолоны
- Ципрофлоксацин 250; 500; 750 мг per os; 2 мг (1 мл) в/м — детям старше 18 лет и взрослым по 250–500 мг 2 раза в сутки. Курс лечения — 5–15 дней или,
- Левофлоксацин 250; 500 мг per os; раствор для инъекций 5 мг (1 мл) — детям старше 18 лет и взрослым — по 250–500 мг 1–2 раза в сутки per os или в/в. Курс лечения — 7–14 дней или,
- Офлоксацин 200 мг; раствор для инфузий 2 мг (1 мл) — детям старше 18 лет и взрослым по 200–400 мг 2 раза в сутки. Курс лечения — 7–10 дней.
Антибиотики группы аминогликозидов
Гентамицина сульфат раствор для инъекций 40 мг (1 мл) — детям до 2 лет — 2–5 мг/кг/сут, детям старше 2 лет — 3–5 мг/кг/сут. Кратность введения 3 раза в сутки. Взрослым 3–5 мг/кг/сут, кратность введения 2–4 раза в сутки. Курс лечения 7–10 дней.
Антибиотики группы линкозамидов
Клиндамицин 150 мг — при приеме внутрь детям по 3–6 мг/кг 4 раза в сутки, взрослым по 150–450 мг 4 раза в сутки; при парентеральном введении детям 15–40 мг/кг/сут, взрослым — 600 мг — 2,7 г в сутки, кратность введения 3–4 раза в сутки. Курс лечения — 10 дней.
Наружное лечение
Проводят промывания язв растворами антисептиков (перекисью водорода, хлоргексидином, мирамистином или теплым раствором марганцевокислого калия) и туширование их поверхности растворами анилиновых красителей:
- Раствор бриллиантового зеленого спиртовой 1% или,
- Фукорцин спиртовой раствор или,
- Метиленовый синий 1–3% водный раствор или,
- Калия перманганата 0,01–0,1% раствор или,
- Раствор перекиси водорода или,
- Хлоргексидин 0,5% спиртовой, 1% водный раствор или,
- Хлорофиллипт масляный раствор 2%.
Затем на поверхность язвы наносят стимуляторы регенарции – мази ируксол, метилурациловую, Микулича, можно использовать повязки текасорб или цинк-желатиновые повязки (Zinci oxydi,Glycerini, Gelatinae aa 40,0, Aq. destillatae 100,0).
Режим
Режим больного шанкриформной пиодермией предполагает рациональный уход за кожей как в очаге поражения, так и вне его - кожу вокруг высыпаний (от здоровой к поражённой) обтирают 1-2% борным (салициловым) спиртом 1 раз в день ежедневно в течение 3-4 недель.
Диета
Питание должно быть полноценным, богатым витаминами, ограничивают количество потребляемой соли и углеводов, полностью исключается алкоголь.
Критерии эффективности лечения
Отсутствие свежих высыпаний, разрешение существующих элементов.
Показания для госпитализации
Распространенные высыпания, наличие осложнений.
Профилактика
- Первичная профилактика пиодермий состоит в своевременной антисептической обработке микротравм, трещин, раневых поверхностей. Следует проводить лечение выявленных общих заболеваний, на фоне которых могут развиться гнойничковые поражения кожи (сахарный диабет, болезни пищеварительного тракта, ЛОР-органов и др.);
- Вторичная профилактика пиодермий включает периодические медицинские осмотры, при необходимости проведение противорецидивной терапии (общие УФ-облучения, уход за кожей, санация очагов фокальной инфекции).
Материал подготовил: Раводин Роман Анатольевич, дерматовенеролог, дерматоонколог, дерматокосметолог. Доктор медицинских наук, доцент
Читайте также:

