При разлитом воспалении кожи наружного
Обновлено: 02.05.2024
Абсцесс – ограниченное капсулой скопление гноя, возникающее при острой или хронической очаговой инфекции и приводящее к тканевой деструкции в очаге (нередко с перифокальным отеком).
Абсцессы кожи и подкожной клетчатки: фурункул, карбункул. Staphylococcus aureus.
Фурункул – острое гнойно-некротическое воспаление волосяного фолликула и окружающих его тканей. В дальнейшем воспаление переходит на сальную железу и окружающую соединительную ткань. Наиболее часто наблюдается на участках кожи, подвергающихся загрязнению (предплечья, тыл кисти) и трению (задняя поверхность шеи, поясница, ягодичная область, бедра). Вызывается чаще Staphylococcus aureus, реже Staphylococcus pyogenes albus.
Фурункулез – множественное поражение фурункулами.
Карбункул – острое гнойно-некротическое воспаление нескольких волосяных фолликулов и сальных желез с образованием обширного некроза кожи и подкожной клетчатки. Карбункул чаще развивается на задней поверхности шеи, межлопаточной и лопаточной областях, на пояснице, ягодицах, реже на конечностях. Возбудители – Staphylococcus aureus или стафило-стрептококковая инфекция, реже стрептококк.
Код протокола: 09-101е "Абсцесс кожи, фурункул и карбункул других локализаций. Другие уточненные инфекции кожи и подкожной клетчатки"
Период протекания
Длительность лечения составляет 9 дней.
Факторы и группы риска
Истощение, гиповитаминоз, тяжелые общие заболевания, болезни обмена веществ (сахарный диабет, ожирение), загрязнение кожи и микротравмы.
Диагностика
Критерии диагностики
При фурункуле – болезненный конусовидный инфильтрат с формирующимся гнойным стержнем, на вершине инфильтрата отмечается небольшое скопление гноя с черной точкой (некроз) в центре. Пустула обычно прорывается и подсыхает, а на 3-7 сутки инфильтрат гнойно расплавляется и некротизированные ткани в виде стержня вместе с остатками волоса выделяются с гноем.
При карбункуле - вначале появляется небольшой воспалительный инфильтрат с поверхностной пустулой, который быстро увеличивается в размере. Напряжение тканей приводит к возникновению резких болей при пальпации, а также распирающей, рвущей, самостоятельной боли. Кожа в области инфильтрата приобретает базовый оттенок, напряжена, отечна. Эпидермис над очагом некроза прорывается в нескольких местах, образуется несколько отверстий ("сито"), из которых выделяется густой зеленовато-серый гной. В отверстиях видны некротизированные ткани. Отдельные отверстия сливаются, образуя большой дефект в коже, через который вытекает много гноя и отторгаются некротические ткани. Температура повышается до 40 С, отмечается значительная интоксикация (тошнота и рвота, потеря аппетита, сильная головная боль, бессонница, изредка бред и бессознательное состояние).
Лечение
При фурункуле операция выполняется редко. Однако при плохом отторжении гнойно-некротического стержня кожа рассекается острым скальпелем. Рассекать фурункул нельзя, так как гнойная инфекция может распространиться на окружающие ткани. Категорически запрещается выдавливать содержимое фурункула и делать массаж в области очага воспаления.
При карбункуле если консервативное лечение не эффективно, показанием для операции является нарастание интоксикации. Операция проводится под наркозом и заключается в крестообразном рассечении карбункула через всю толщу некроза до жизнеспособных тканей с иссечением некротических тканей и вскрытием затеков. Повязки с гипертоническим раствором натрия хлорида, мазью Вишневского или другим антисептиком.
Для вскрытия абсцесса выбирают самый короткий путь с учетом анатомических образований. Можно вначале пунктировать абсцесс, а затем по игле рассечь ткани. Удалив гной, разрез расширяют и иссекают некротические ткани. Полость обрабатывают растворами антисептиков и дренируют марлевыми тампонами с антисептиками, протеолитическими ферментами, антибиотиками, а также резиновыми дренажами. При плохом дренировании из основного разреза делают контрапертуру. Первые 2-3 дня рану перевязывают ежедневно и, когда она очистится от гноя и некротических тканей, переходят на редкие мазевые повязки. В некоторых случаях можно иссечь абсцесс в пределах здоровых тканей и наложить первичные швы с активной аспирацией из раны, что ускоряет ее заживление и позволяет добиться хорошего косметического эффекта.
Обосновано применение витаминов, обладающих противовоспалительным и иммуномодулирующим действием, улучшающих обмен веществ: аскорбиновая кислота 5% -2,0 в/м №10-15, поливит по 1 др. х 3 раза в день, 10 дней.
Антибиотики с учетом чувствительности микрофлоры:
- феноксиметилпенициллин – 0,25 г 4 раза/сут (при стрептококковой инфекции);
- амоксициллин/клавуланат – 0,375-0,625 г 3 раза/сут.;
- цефалексин 0,5-1,0 г 4 раза/сут.;
- цефуроксим аксетил – 0,5 г 2 раза/сут во время еды;
- эритромицин 0,5 г 4 раза/сут.;
- оксациллин 1-2 г 4-6 раз/сут. в/в, в/м;
- цефазолин 1-2 г 3 раза/сут. в/в, в/м;
- фузидиевая кислота 0,5-1 г 3 раза/сут. внутрь;
- цефтриаксон 1, 0 г 1 раз/сут. в/м.
- итраконазол оральный раствор 400 мг\сут – 7 дней (профилактика кандидоза).
Местно - 2% мазь или крем на основе мупироцина, 2% мазь или крем на основе натриевой соли фузидиевой кислоты.
Учитывая упорное течение заболевания, развитие воспалительного процесса в дерме и сенсибилизацию организма назначаются десенсибилизирующие средства: тиосульфат натрия 30% - 10,0 в/в ежедневно №10-15.
При гнойничковых заболеваниях имеет место нарушение периферического кровообращения и обмена веществ, в связи с чем назначается никотиновая кислота 1% 1,0 в/м №10-15 (улучшает углеводный обмен, микроциркуляцию, оказывает сосудорасширяющее действие и улучшает регенеративные свойства ткани). Назначаются препараты способные адсорбировать токсины: активированный уголь – 6 таб. утром натощак 10 дней.
Для уменьшения возбудимости ЦНС применяют успокаивающие средства – настойка пустырника по 20 кап. х 3 раза в день в течение месяца.
Учитывая, что в патогенезе существенное значение имеют иммуннодефицитные состояния, снижение реактивности организма назначают иммуномодуляторы – метилурацил 500 мг х 3 раза в день - 10 дней; метронидазол по 250 мг х 3 раза в день - 10 дней. С целью коррекции поражений поджелудочной железы, печени и желчевыводящих путей, при нарушении факторов неспецифической защиты и наличии сопутствующей патологии назначается панкреатин по 1 капс. х 4 раза в день, 10 дней.
С целью улучшения реологических свойств крови и микроциркуляции - декстран 400 мл в/в 1 р. в день, курсовая доза 800 мл. Наружно назначают бактерицидные, антисептические препараты – мази с антибиотиками, растворы анилиновых красителей (метиленовый синий, калия перманганат, перекись водорода), противовоспалительные - для улучшения трофики кожи.
Перечень основных медикаментов:
1. *Аскорбиновая кислота раствор для инъекций 5%, 10% в ампуле 2 мл, 5 мл
2. Феноксиметилпенициллин 500 мг табл.
3. *Амоксициллин+клавулановая кислота таблетка 625 мг; раствор для инъекций 600 мг во флаконе
4. *Цефалексин 250 мг, 500 мг табл., капс.; суспензия и сироп 125 мг, 250 мг/5 мл
5. *Цефуроксим 250 мг, 500 мг табл.; порошок для приготовления инъекционного раствора во флаконе 750 мг
6. *Эритромицин 250 мг, 500 мг табл; пероральная суспензия 250 мг/5 мл
7. *Цефазолин порошок для приготовления инъекционного раствора 1000 мг
8. *Цефтриаксон порошок для приготовления инъекционного раствора 250 мг, 500 мг, 1000 мг во флаконе
9. *Итраконазол оральный раствор 150 мл – 10 мг\мл
10. *Натрия тиосульфат раствор для инъекций 30% 5 мл, 10 мл в ампуле
11. *Никотиновая кислота 50 мг табл.; раствор в ампуле 1% 1 мл
12. *Активированный уголь 250 мг табл.
13. Настойка пустырника 30 мл, 50 мл фл.
14. *Метилурацил 10% мазь
15. *Метронидазол 250 мг табл; раствор для инфузий 0,5 во флаконе 100 мл
16. *Панкреатин таблетка, капсула с содержанием липазы не менее 4 500 ЕД
17. *Декстран раствор для инфузий во флаконе 200 мл, 400 мл
18. *Метиленовый синий раствор спиртовый 1% во флаконе 10 мл
19. *Калия перманганат водный раствор 1:10 000
20. *Перекись водорода раствор 3% во флаконе 25 мл, 40 мл
Критерии перевода на следующий этап: заживление операционной раны.
* – препараты, входящие в список основных жизненно важных лекарственных средств
Наружный отит — воспаление наружного уха диффузного или ограниченного характера. Ограниченный наружный отит проявляется образованием фурункула с резко выраженным болевым синдромом в стадии инфильтрации и возможностью развития фурункулеза при его вскрытии. Диффузный наружный отит характеризуется разлитым воспалением слухового прохода, которое сопровождается болью и распиранием в ухе, серозным, а затем гнойным отделяемым. С целью диагностики наружного отита проводится осмотр и пальпация околоушной области, отоскопия, аудиометрия, бакпосев отделяемого из уха. Лечебные мероприятия при наружном отите состоят в промывании слухового прохода антисептиками, закладывании в него турунд с лекарственными препаратами, проведении общей антибиотикотерапии, противовоспалительного и иммуностимулирующего лечения.
МКБ-10
Общие сведения
Наружное ухо является периферической частью слухового аппарата человека. Оно состоит из наружного слухового прохода, имеющего хрящевую и костную части, и ушной раковины. От полости среднего уха наружное ухо отделено барабанной перепонкой. При локальном воспалении наружного слухового прохода говорят об ограниченном наружном отите. Он представляет собой гнойно-воспалительный процесс в области волосяного фолликула — фурункул. Разлитое воспаление слухового прохода, охватывающее его хрящевую и костную часть, в отоларингологии носит название диффузного наружного отита. Диффузный наружный отит характеризуется воспалительными изменениями как в коже, так и в подкожной жировой клетчатке слухового прохода, может сопровождаться воспалением барабанной перепонки.

Причины возникновения наружного отита
Причиной наружного отита является инфицирование кожи наружного слухового прохода. Возбудителем ограниченного наружного отита чаще всего является пиогенный стафилококк. Диффузный наружный отит может быть вызван стафилококками, гемофильной палочкой, пневмококками, клебсиеллой, синегнойной палочкой, моракселлой, грибками рода Candida и др. Наиболее часто занос инфекции в слуховой проход с развитием наружного отита наблюдается при гноетечении из перфорированной барабанной перепонки при остром и хроническом гнойном среднем отите, гнойном лабиринтите.
Проникновению возбудителя внутрь кожного покрова, выстилающего наружный слуховой проход, осуществляется в местах повреждений и микротравм. В свою очередь травмирование кожи слухового прохода возможно при травме уха, наличие в нем инородного тела, попадании агрессивных химических веществ, неправильном проведении гигиены уха, самостоятельных попытках извлечения серной пробки, расчесывании уха при зудящих дерматозах (экземе, крапивнице, атопическом дерматите, аллергическом дерматите) и сахарном диабете.
Возникновению наружного отита способствует постоянное увлажнение слухового прохода попадающей в него водой, которое приводит к снижению барьерной функции кожи. Благоприятным фоном для развития наружного отита также является снижение общих защитных сил организма, что наблюдается при авитаминозе, иммунодефицитных состояниях (например, при ВИЧ-инфекции), хронических инфекциях (туберкулез, сифилис, хронический тонзиллит, хронический пиелонефрит), сильном переутомлении (синдром хронической усталости).
Ограниченный наружный отит
Симптомы ограниченного наружного отита
В своем развитии ограниченный наружный отит проходит те же стадии, что и фурункул на поверхности кожи. Однако замкнутое пространство и обильная иннервации слухового прохода, в котором располагается фурункул при наружном отите, обуславливают некоторые особенности его клинической картины. Обычно ограниченный наружный отит начинается с ощущения сильного зуда в слуховом проходе, который затем перерастает в боль. Увеличение размеров фурункула уха в стадии инфильтрации приводит к сдавлению нервных рецепторов и быстрому нарастанию болевого синдрома.
Боли в ухе при ограниченном наружном отите по своей интенсивности превосходят боли, отмечающиеся при остром среднем отите. Они иррадиируют в висок, затылок, верхнюю и нижнюю челюсть, захватывают всю половину головы со стороны больного уха. Отмечается усиление болевого синдрома при жевании, что в некоторых случаях заставляет пациента с наружным отитом отказаться от приема пищи. Характерно увеличение интенсивности болей в ночное время, в связи с чем происходит нарушение сна. Инфильтрация при ограниченном наружном отите может достигать значительного объема. При этом фурункул полностью перекрывает просвет слухового прохода и приводит к снижению слуха (тугоухости).
Вскрытие фурункула при наружном отите сопровождается истечением гноя из уха и резким уменьшением болевого синдрома. Однако при вскрытии фурункула часто происходит обсеменение других волосяных фолликулов слухового прохода с образованием множественных фурункулов и развитием фурункулеза, отличающегося упорным течением и стойкостью к проводимой терапии. Множественные фурункулы при наружном отите приводят к полной обтурации слухового прохода и усилению клинических симптомов заболевания. Развивается регионарный лимфаденит. Возможно появление отечности в заушной области и оттопыривание ушной раковины, что требует дифференцировки наружного отита от мастоидита.
Диагностика ограниченного наружного отита
В первую очередь отоларинголог проводит осмотр уха и отоскопию. Во время осмотра врач производит оттягивание ушной раковины, что при наружном отите приводит к появлению резкой боли в ухе. Возникновение боли при надавливании на козелок уха говорит о локализации ограниченного наружного отита на передней стенке слухового прохода. Резкая болезненность при пальпации за ухом свидетельствует в пользу того, что фурункул располагается на задне-верхней стенке слухового прохода. При наружном отите в области нижней стенки резко болезненна пальпация над углом нижней челюсти.
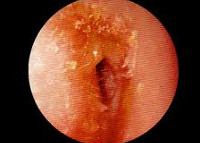
Отоскопия при ограниченном наружном отите обнаруживает наличие в слуховом проходе фурункула. В начальной стадии наружного отита фурункул имеет вид припухлости красного цвета. Созревший фурункул практически перекрывает слуховой проход, после его вскрытия отоскопия выявляет гной и наличие кратерообразного отверстия на вершине инфильтрата.
Аудиометрия и исследование слуха камертоном у пациентов с ограниченным наружным отитом определяет кондуктивный тип тугоухости и латерализацию звукопроведения в сторону пораженного уха. Для определения возбудителя проводится бактериологический посев гноя из фурункула. Дифференцировать ограниченный наружный отит следует от других видов отита, эпидемического паротита, мастоидита, экземы наружного уха.
Лечение ограниченного наружного отита
В стадии инфильтрации ограниченного наружного отита проводят туалет наружного уха и обработку пораженного участка нитратом серебра. В слуховой проход вводят турунду с антибактериальной мазью. Ухо закапывают ушными каплями, содержащими антибиотик (неомицин, офлоксацин и пр.). Для снятия болевого синдрома назначают анальгетики и противовоспалительные препараты. Возможно применение УВЧ-терапии. Созревший фурункул может быть вскрыт при помощи разреза. После его вскрытия наружный слуховой проход промывают растворами антибиотиков и антисептиков.
При наружном отите с множественными фурункулами показана антибиотикотерапия. При подтверждении стафилококковой природы отита применяют антистафилококковый анатоксин или вакцину. С целью повышения иммунитета рекомендована витаминотерапия, иммунокоррегирующее лечение, процедуры УФОК или ВЛОК, аутогемотерапия.
Диффузный наружный отит
Симптомы диффузного наружного отита
Диффузная форма наружного отита начинается с ощущения распирания, зуда и повышения температуры в слуховом проходе. Очень скоро возникает болевой синдром, который сопровождается иррадиацией боли во всю половину головы и ее значительным усилением во время жевания. Выраженный болевой синдром при диффузном наружном отите приводит к нарушению сна и анорексии. Значительная отечность воспаленных стенок слухового прохода суживает его просвет и является причиной снижения слуха. Диффузный наружный отит сопровождается небольшим количеством выделений из уха, которые в начале носят серозный характер, а затем становятся гнойными. Отмечается увеличение регионарных лимфоузлов. При тяжелом течении заболевания возможно распространение воспалительного процесса на ушную раковину и мягкие ткани околоушной области.
Острый период диффузного наружного отита длится 2-3 недели. Затем на фоне проводимого лечения или самопроизвольно может произойти уменьшение симптомов заболевания и полное выздоровление пациента. Также диффузный наружный отит может принять затяжное течение и перейти в хроническую форму. Хронический наружный отит сопровождается образованием рубцов, которые уменьшают просвет слухового прохода и могут стать причиной стойкого снижения слуха.
Диагностика диффузного наружного отита
Выраженная болезненность при надавливании на козелок, оттягивании ушной раковины, пальпации в заушной области и над углом верхней челюсти свидетельствует о разлитом воспалении слухового прохода. Отоскопия при диффузном наружном отите обнаруживает тотальное покраснение и отечность кожного покрова, выстилающего слуховой проход, наличие эрозий с серозным отделяемым. В более позднем периоде наружного отита выявляется обтурация слухового прохода из-за выраженного отека его стенок, визуализируются язвы и трещины, выделяющие зеленовато-желтый гной. Аудиометрия свидетельствует о наличие тугоухости по кондуктивному типу. Латерализация звука происходит к больному уху. Бактериологическое исследование отделяемого из уха позволяет верифицировать возбудителя и установить его чувствительность к основным антибактериальным препаратам.
Дифференциальный диагноз диффузного наружного отита проводят с гнойным средним отитом, рожей, острой экземой и фурункулом слухового прохода.
Лечение диффузного наружного отита
Терапия диффузного наружного отита проводится системным применением антибиотиков, поливитаминных и антигистаминных препаратов. При необходимости осуществляется иммунокоррегирующее лечение. Местное лечение диффузного наружного отита заключается в ведении в слуховой проход турунд с желтой ртутной мазью, жидкостью Бурова, антибактериальными и гормональными мазями, закапывании ушных капель с антибиотиками. Гнойный характер отделяемого из уха является показанием для промывания слухового прохода растворами антибиотиков.
Наружный отит грибковой этиологии лечится противогрибковыми препаратами системного и местно применения.
Профилактика наружного отита
Для предупреждения инфицирования кожи слухового прохода с развитием наружного отита необходимо избегать расчесывания ушной раковины, травмирования уха и попадания в него инородных тел. При купании следует беречь ухо от попадания в него воды. Ни в коем случае нельзя самостоятельно пытаться удалить инородное тело уха, поскольку это часто приводит к травмированию кожи слухового прохода. Не следует очищать ухо от серы не предназначенными для этого предметами: шпилькой, зубочисткой, спичкой, скрепкой и т. п. Туалет уха должен производиться специальной ушной палочкой на глубину не более, чем 0,5-1 см от начала слухового прохода.
Глубокая пиодермия – группа гнойно-воспалительных поражений кожи (преимущественно ее глубоких слоев – дермы), обусловленных инфицированием тканей стафилококками, стрептококками или смешанной микрофлорой. Симптомы заболевания различаются в зависимости от выраженности воспаления и характера возбудителя, но обязательно включают в себя отек, болезненность, покраснение и образование гноя. Диагностика глубокой пиодермии основывается на внешних кожных проявлениях и микробиологических исследованиях для идентификации возбудителя. В лечении широко применяются хирургические приемы для обеспечения оттока гноя, местные и общие антибиотики, противомикробные и антисептические средства.
Общие сведения
Глубокая пиодермия – гнойное заболевание кожных покровов, особенностью которого является поражение дермы, подкожной клетчатки, глубоко расположенных волосяных фолликулов, потовых и сальных желез. Это состояние является одной из наиболее распространенных патологий в дерматологии – по разным данным, на нее приходится от 30 до 40% всех дерматологических заболеваний. Практически каждый человек минимум несколько раз в жизни страдал от проявлений различных форм глубокой пиодермии. Это объясняется высокой распространенностью возбудителей (стафилококков и стрептококков), их вирулентностью, огромным разнообразием штаммов. В большинстве случаев глубокая пиодермия не угрожает жизни человека и даже излечивается самостоятельно без специальной терапии, но иногда она может быть причиной интоксикации, источником метастатических гнойных очагов и даже причиной сепсиса.

Причины глубокой пиодермии
В широком плане, глубокая пиодермия – поражение кожи, обусловленное гноеродной микрофлорой, к которой относят стафилококков, стрептококков, синегнойную палочку и некоторые другие микроорганизмы. Однако более 95% случаев заболевания вызываются именно кокковой флорой, так как она широко распространена в окружающей среде и отчасти представлена даже на поверхности кожи здорового человека. При проникновении в ткани кожи через микротрещины, повреждения эпидермиса, вдоль волосяных стержней и по протокам кожных желез микроорганизмы начинают бурно размножаться. Выделяемые ими в процессе жизнедеятельности ферменты и различные токсины вызывают деструкцию клеток кожи. В результате этих процессов формируется первичный очаг, расположенный в дерме – симптомов глубокой пиодермии на этом этапе не наблюдается.
Сами микроорганизмы и выделяемые ими ферменты обладают сильными иммуногенными свойствами, поэтому практически сразу после формирования первичного очага происходит незамедлительная реакция иммунной системы. Традиционно первыми на инфицирование реагируют тканевые макрофаги, затем путем хемотаксиса в будущий очаг глубокой пиодермии попадают нейтрофилы, а затем и другие иммунокомпетентные клетки. Выделяемые ими биологически активные вещества приводят к местному отеку, покраснению, появлению болезненных ощущений. Клинически это соответствует первой стадии глубокой пиодермии – образованию воспалительного очага, который может иметь тенденцию к расширению.
На определенном этапе иммунитету удается локализовать воспаление, и его распространение в тканях останавливается. Нейтрофилы атакуют патогенные микроорганизмы и отчасти собственные ткани (вторичная альтерация) в очаге с формированием гноя – субстанции, состоящей из «осколков» возбудителей, разрушенных собственных клеток и погибших нейтрофилов. Развитие глубокой пиодермии облегчается при ряде обстоятельств – пониженном иммунитете, сахарном диабете, истощении, гиповитаминозах и других ослабляющих организм состояниях. Немаловажную роль играет пренебрежение правилами личной гигиены, избыточная продукция кожного сала, местное переохлаждение кожи. Для лиц с пониженным иммунитетом глубокая пиодермия опасна тем, что способна вызывать сильные поражения, стать причиной различных осложнений, некоторые из которых могут напрямую угрожать жизни человека.
Симптомы глубокой пиодермии
Существует несколько клинических разновидностей глубокой пиодермии, которые характеризуется разными возбудителями, выраженностью симптомов и типом поражаемых тканей. Все формы этого заболевания по характеру микрофлоры, вызвавшей воспаление, делят на стафилодермии, стрептодермии и смешанные разновидности, которые иногда называют стрептостафилодермиями. К глубоким пиодермиям, вызванным стафилококками, относят фурункулы, карбункулы, гидрадениты и глубокий фолликулит. Глубокие стрептодермии представлены вульгарной эктимой, а воспаления из-за смешанной микрофлоры – хронической язвенно-вегетирующей пиодермией.
Фурункул – разновидность глубокой пиодермии, особенностью которой является поражение волосяного фолликула гнойно-некротического характера с переходом на окружающие ткани. Его развитию может предшествовать поверхностное гнойное воспаление (фолликулит), однако возможно и первичное развитие глубокого процесса. На участке кожи, окружающей волос, формируется сначала очаг багрового цвета размером от нескольких миллиметров до 1-2 сантиметров, болезненный и плотный, его температура заметно выше окружающих кожных покровов. Затем глубокая пиодермия такого типа сопровождается появлением гноя, в центре которого будет стержень из некротизированной ткани. Гнойно-некротическое содержимое отторгается через 3-10 дней, на месте поражения кожи формируется небольшая язва, которая быстро рубцуется.
Карбункул – более тяжелая разновидность глубокой пиодермии, вызываемая стафилококковой флорой и характеризующаяся поражением глубоких слоев дермы и подкожной жировой клетчатки. В глубине кожи возникает плотный инфильтрат, кожные покровы над ним приобретают синюшно-багровый оттенок, становятся горячими и болезненными. Через несколько дней в очаге глубокой пиодермии начинают формироваться пустулы, происходит выделение гноя и некротических стержней, на месте поражения образуется язва. Все это сопровождается выраженными общими симптомами – интоксикацией, лихорадкой, болями стреляющего характера в месте карбункула. Отмечается регионарный лимфаденит и лимфангит. После разрешения этой формы глубокой пиодермии на месте поражения остается заметный рубец.
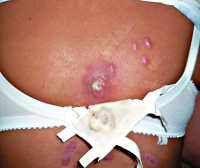
Гидраденит – форма глубокой пиодермии, при которой поражаются апокриновые потовые железы с развитием гнойного воспаления. Из-за этого характерная локализация патологических очагов – подмышечные впадины, околососковая и аногенитальная области. Гидраденит начинается с развития болезненного узла синюшного цвета, который за несколько дней значительно увеличивается в размерах и самопроизвольно вскрываются с выделением обильного количества гноя. Затем происходит постепенное заживление, рубцы образуются в крайне редких случаях. При этой форме глубокой пиодермии также отмечается регионарный лимфаденит и лимфангит, но общие симптомы выражены слабо. Гидрадениты, особенно в области подмышечных впадин, склонны к частым рецидивам.
Глубокий фолликулит – одна из наиболее легких форм глубокой пиодермии, которая отличается от обычного фолликулита более выраженным поражением волосяных луковиц. Симптоматика в целом сходна с фурункулом, однако проявления менее выраженные, общих симптомов практически никогда не наблюдается. Главный диагностический критерий, позволяющий дерматологу отличить фурункул от глубокого фолликулита – отсутствие гнойно-некротического воспаления, так как не образуется характерный некротический стержень.
Вульгарная эктима – форма глубокой пиодермии, вызываемая стрептококковой микрофлорой. Чаще всего поражает кожу голени у ослабленных больных, в крайне редких случаях возникает у здоровых людей. Эктима начинается с образования на поверхности кожных покровов пустулы с мутным содержимым серозного, иногда геморрагического характера. Затем пустула исчезает и на ее месте формируется типичный очаг глубокой пиодермии – болезненная язва с выраженным воспалительным ободком вокруг, дно образования покрыто слоем гноя. Через 2-3 недели после появления язвы начинается ее постепенное рубцевание с развитием заметного шрама.
Хроническая язвенно-вегетирующая пиодермия – кожное заболевание, возбудителями которого является смешанная микрофлора, наибольшую роль в развитии патологии играет золотистый стафилококк и стрептококки группы А. Глубокая пиодермия такого типа чаще всего развивается у ослабленных больных – истощенных лиц, страдающих алкоголизмом, пожилых людей. Характеризуется образованием на нижних конечностях эрозий неправильной формы с рваными краями, окруженных воспаленной кожей. Дно язвенных образований покрыто гноем, часто возникают выделения с неприятным зловонным запахом. Эрозии длительное время не заживают и склонны к частым рецидивам или поражению других участков кожных покровов.
Осложнениями любой разновидности глубокой пиодермии могут быть метастатические гнойные поражения регионарных лимфатических узлов и отдаленных органов. Особенно опасны в этом отношении глубокие фолликулиты и фурункулы, возникающие в пределах носогубного треугольника – имеющиеся там анастомозы кровеносных сосудов способствуют заносу инфекции в головной мозг и его оболочки. У ослабленных больных на фоне глубокой пиодермии могут возникать флегмоны и сепсис, являющиеся жизнеугрожающими состояниями. В редких случаях возможно развитие токсического шока.
Диагностика глубокой пиодермии
Диагностика различных форм глубокой пиодермии осуществляется посредством осмотра дерматолога (иногда может потребоваться консультация хирурга). Из дополнительных методов исследования наиболее часто применяют посев гноя для определения характера возбудителя и для выяснения его чувствительности к антибактериальным средствам. При развитии общих симптомов также в ряде случаев необходимо проведение общего анализа крови, в самых тяжелых случаях – бакпосев крови для диагностики сепсиса. Результаты осмотра зависят от формы глубокой пиодермии и стадии ее развития – это может быть просто воспалительный очаг, сформировавшийся гнойник, ранка или язва с гнойным отделяемым. При посеве определяются стафилококки или стрептококки, может обнаруживаться смешанная микрофлора. Микробиологические исследования посевов могут определить вид и штамм возбудителя, а также его чувствительность к антибиотикам.
Если имеется повышение температуры, головная боль, слабость то необходимо проведение общего анализа крови. Обычно при глубокой пиодермии определяются легкие неспецифические признаки воспаления – повышение скорости оседания эритроцитов, небольшой лейкоцитоз. В более тяжелых случаях наблюдаются уже выраженные изменения – значительный рост СОЭ, выраженный лейкоцитоз, выявляются изменения в распределении нейтрофилов. В крови появляется множество юных форм этой фракции лейкоцитов, что носит название нейтрофильного сдвига влево. Если есть подозрения, что глубокая пиодермия стала причиной сепсиса, производят посев крови на питательные среды – в норме кровь человека абсолютно стерильна, рост культур говорит о наличии возбудителя в крови. Для диагностики таких осложнений, как метастатические гнойные очаги могут применяться ультразвуковые, рентгенологические и другие методы клинических исследований.
Лечение глубокой пиодермии
При незначительных по выраженности гнойных поражениях без общих проявлений интоксикации рекомендуется ждать самопроизвольного разрешения глубокой пиодермии. Лечебные мероприятия сводятся к недопущению осложнений. При наличии волос вокруг гнойного очага их нужно аккуратно состричь – использование бритвы может привести к распространению инфекции. Мыть участок с очагом глубокой пиодермии не рекомендуется, допустимо только протирать кожу вокруг него дезинфицирующими растворами (хлоргексидином, раствором салициловой кислоты). Строго запрещается без участия дерматолога или хирурга самостоятельно вскрывать гнойник или каким-либо способом ускорять отделение гноя – это может привести к диссеминации возбудителя.
Если глубокая пиодермия характеризуется развитием крупных очагов с появлением общих симптомов (лихорадка, слабость, головные боли), то необходимо назначение антибактериальных средств, таких как эритромицин, тетрациклин, линкомицин – предварительно желательно сделать бактериальный посев и определить препарат, к которому наиболее чувствителен данный микроорганизм. Также при глубокой пиодермии применяют и противомикробные средства из группы сульфаниламидов – например, сульфаметоксазол+триметоприм. В последние годы в тяжелых случаях гнойных поражений кожи используют и иммунологические препараты – стафилококковый анатоксин, антистафилококковую гипериммунную плазму и ряд других.
При глубоком расположении значительного по размерам очага пиодермии прибегают к хирургическому вскрытию полости гнойника для формирования дренажа и оттока гноя. Кроме того, это позволяет доставлять антисептические и антибактериальные препараты непосредственно в область поражения, что ускоряет лечение. Вскрытие очага глубокой пиодермии должно происходить в стерильном помещении и осуществляться квалифицированным гнойным хирургом.
Прогноз и профилактика глубокой пиодермии
В большинстве случаев прогноз при развитии различных форм глубокой пиодермии благоприятный – после отделения гноя происходит заживление очага, довольно часто с образованием рубцов. Однако у ослабленных больных с низким уровнем иммунитета возможно развитие осложнений, некоторые из которых могут угрожать жизни и требуют лечения в условиях стационара. Для профилактики развития глубокой пиодермии необходимо придерживаться правил личной гигиены, своевременно обрабатывать кожные повреждения (ссадины, порезы) антисептиками. Кроме того, важно устранять возможные источники инфекции в организме – кариозные зубы, хронические инфекции ЛОР-органов.
Мокнущая экзема — это острая форма экземы, которая протекает с выраженным экссудативным компонентом. Она проявляется отечностью, гиперемией кожи, образованием множественных везикулярных высыпаний и эрозий, сливающихся в очаги мокнутия. Для диагностики дерматоза проводится комплексное лабораторное обследование, гистологическое исследование биоптатов пораженных участков кожи, консультации смежных специалистов. Для купирования острой формы мокнущей экземы показано местное применение вяжущих препаратов, системное лечение антигистаминными, гипосенсибилизирующими, противовоспалительными средствами.
МКБ-10
Общие сведения
Экзема — самое распространенное кожное заболевание, на долю которого приходится 25-40% всех кожных патологий. Термин «мокнущая экзема» не используется в официальных классификациях, поскольку он отражает один из этапов островоспалительной кожной реакции, которая возникает при острой стадии различных клинических форм патологического процесса. Лечение дерматоза представляет сложную задачу ввиду хронического течения, частых рецидивов, сложного этиопатогенеза, поэтому болезнь не теряет своей актуальности в практической дерматологии.

Причины
Конкретные этиологические факторы болезни до сих по не установлены. Согласно современной общепринятой концепции, мокнущая экзема представляет собой мультифакториальное кожное поражение, протекающее с нарушениями функций эпидермиса. Она развивается при сочетании эндогенных и экзогенных провоцирующих факторов, основными из которых являются следующие:
- Генетическая предрасположенность. Если патология диагностирована у одного из родителей, риск заболеть составляет 40%, при наличии заболевания у обоих родителей — повышается до 50-60%. Отягощенная наследственность проявляется определенными генами HLA, которые контролируют иммунный ответ.
- Экзогенные факторы. Заболевание провоцируется негативным воздействием химических веществ (бытовая химия, профессиональные вредности), физических факторов (повышенная инсоляция, температурные перепады), аллергизацией при употреблении некоторых продуктов питания, лекарственных препаратов.
- Инфекционно-аллергические факторы. Дерматоз может возникать при попадании в организм бактериальных или грибковых агентов извне. Нередко он начинается на фоне хронических очагов инфекции, особенно при отсутствии адекватного лечения. Во втором случае появления экзематозных симптомов вызвано хронической сенсибилизацией организма к антигенным детерминантам микробов.
- Неврологические нарушения. Функциональные нервные расстройства с преобладанием парасимпатических влияний повышают вероятность появления мокнущих высыпаний. Патология периферических нервов, сопровождающаяся ухудшением микроциркуляции, провоцирует возникновение клинических симптомов в пораженной зоне.
- Соматические заболевания. Стимулируют развитие кожного поражения и отягощают его течение при несоблюдении схемы лечения многие патологии внутренних органов: желудочно-кишечного тракта, панкреатобилиарной системы, мочевыделительной системы. Важная роль отводится нейроэндокринным нарушениям, метаболическим расстройствам, возникающим вследствие поражения желез внутренней секреции.
Патогенез
Основной патогенетический компонент мокнущей экземы — иммунное воспаление в коже, протекающее по типу реакции замедленного типа. В его формировании выделяют 4 предрасполагающих фактора: нарушения клеточного и гуморального иммунитета, сенсибилизация к эндо- или экзоантигенам, изменение функции ЦНС, генетически обусловленные особенности иммунного ответа.
Образование типичных мокнущих поражений кожного покрова связывают с дисфункцией Т-лимфоцитов, которые выделяют в ткани провоспалительные вещества: интерлейкины, интерферон, фактор некроза опухолей. Одновременно усиливается выброс лейкотриенов, простагландинов, гистамина, что завершается острой воспалительной реакцией с преобладаем экссудативного компонента.
В патогенезе дерматоза немаловажную роль играют иммунологические расстройства, ассоциированные с конкретными антигенами главного комплекса гистосовместимости. У пациентов снижается активность Т-лимфоцитов хелперов и супрессоров, что проявляется угнетением иммунологической реактивности. Вследствие этого происходит активация хронической инфекции, замедляется выведение антигенов из организма.
Также в механизме развития мокнущей экземы выделяют снижение активности неспецифических защитных факторов — комплемента, лизоцима, фагоцитов. При этом повышается риск присоединения вторичной инфекции, осложненного течения болезни. Отягощает ситуацию аллергическая перестройка организма, из-за которой кожа приобретает повышенную поливалентную чувствительность к антигенам.
Классификация
На сегодня отсутствует общепринятая систематизация, что обусловлено разнообразием клинических вариантов патологии, разными точками зрения экспертов на причины и механизмы формирования дерматоза, подбор схем лечения. Практикующие дерматологи используют несколько вариантов классификации, при которых учитываются следующие признаки:
- По течению процесс бывает острым, подострым, хроническим.
- По клиническим проявлениям болезнь подразделяется на истинную, микробную, детскую, профессиональную, варикозную формы.
- По классификации Хорнштейна существует экзогенная, эндогенная, дисрегуляторная экзема.
- По классификации Американской академии дерматовенерологии выделяются конкретные нозологические единицы дерматоза (астеатотическая экзема, нумулярный дерматит, белый питириаз и т. д.).
Симптомы мокнущей экземы
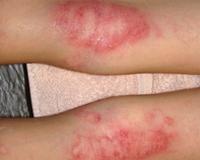
Мокнущая экзема манифестирует покраснением и отечностью кожи с последующим появлением высыпаний в виде мелких пузырьков. При механическом воздействии или самопроизвольно везикулы лопаются, обнажая эрозии с интенсивным мокнутием. Характерным симптомом острой формы дерматоза являются «серозные колодцы» — эрозии, из глубины которых выделяется прозрачная или слегка желтоватая жидкость.
Постепенно мокнущие поверхности подсыхают с образованием тонких корок. Одновременно с этим на пораженных участках могут появляться папулы — мелкие розовые узелки, пустулы со стерильным содержимым. Присутствие на кожном покрове различных морфологических элементов называется истинным полиморфизмом сыпи, этот признак считается типичным для истинной (идиопатической) экземы, не встречается при других формах дерматоза.
Из субъективных ощущений без лечения на первое место выходит сильный кожный зуд, вследствие которого больные расчесывают кожу до крови, усугубляя течение процесса. Зачастую в результате интенсивного зуда возникают нарушения работоспособности, раздражительность, сон становится прерывистым и не снимает усталость. Обширные мокнущие эрозии сопровождаются болезненностью, которая усиливается при соприкосновении пораженной кожи с одеждой.
В клинической картине мокнущего дерматоза выделяют особенности, связанные с конкретной формой. Истинная экземы характеризуется симметричным расположением элементов с их локализацией на коже туловища, верхних и нижних конечностей. Для микробного поражения типичны асимметричные очаги мокнущих высыпаний на нижних конечностях. При детской форме очаги мокнутия имеют блестящую, гиперемированную поверхность.
Осложнения
В периоде мокнутия пораженная кожа представляет открытую раневую поверхность, которая становится хорошими входными воротами для патогенных микроорганизмов. Поэтому самым распространенным осложнением в остром периоде без лечения является присоединение вторичной бактериальной инфекции, наиболее часто вызванной стафилококками или стрептококками. В тяжелых случаях возникает флегмона, регионарный лимфаденит.
У больных с длительным стажем патологии мокнущие элементы и расчесы приводят к утолщению кожи, усилению кожного рисунка, гиперпигментации, повышенной сухости. Такие дерматологические изменения приносят дискомфорт, поскольку кожа теряет эластичность, формируется значимый косметический дефект, что особенно беспокоит женщин.
Диагностика
Данные анамнеза и кожные проявления дерматоза дают врачу-дерматологу ценную информацию для постановки диагноза и выбора лечения. Наличие множественных эрозий, серозного отделяемого, сероватых корок является подтверждением мокнущей стадии экземы. В сомнительных случаях, а также для выявления возможных первопричин болезни показаны:
- Гистологический анализ. На мокнущей стадии в биоптатах кожи определяется спонгиоз, мелкие везикулы, внутриклеточный отек эпидермиса. В структуре дермы наблюдается лимфоидно-клеточная инфильтрация вокруг сосудов, расширение поверхностной сети капилляров.
- Анализы крови. Для подтверждения инфекционно-аллергической этиологии измеряется уровень иммуноглобулина Е, производится аллергологическое исследование для обнаружения антител к специфическим антигенам. Чтобы оценить общее состояние здоровья, назначается клинический, биохимический анализ крови.
- Микробиологические исследования. При подозрении на микробную экзему, осложнении процесса вторичной инфекцией необходим бакпосев отделяемого кожных элементов. По его результатам устанавливают точный вид патогенного возбудителя, чувствительность к антибактериальным препаратам, подбирают подходящее для лечения средство.
- Консультации специалистов. Если при первичной диагностике у человека присутствуют признаки поражения внутренних органов, которые потенциально могли стать провоцирующим фактором мокнущего дерматоза, дальнейшее обследование и лечение проводится с участием профильных врачей. Чаще всего требуется помощь гастроэнтеролога, психоневролога, эндокринолога.
Лечение мокнущей экземы
Системная терапия
Терапия мокнущей экземы подбирается индивидуально с учетом предположительных причин развития заболевания, степени тяжести клинических проявлений, наличия у больного сопутствующих патологий или осложнений. Для уменьшения сенсибилизации организма больным рекомендуется соблюдать гипоаллергенную диету, из которой исключают жирные сорта рыбы и мяса, устрицы и другие морепродукты, кофе и какао-продукты, цитрусовые, томаты, бобовые.
Если обострение болезни связано с воздействием экзогенных факторов, их устранение является необходимым условием для успешности лечения. Учитывая конкретную ситуацию, пациентам может потребоваться сменить место работы, исключить бытовые аллергены, переехать в более подходящие климатические условия. Комплексное лечение мокнущего аллергодерматоза требует применения ряда препаратов:
- Антигистаминные средства. Для ликвидации кожного зуда в острой фазе применяются гистаминоблокаторы первого поколения, а после купирования симптоматики возможно продолжение лечения медикаментами второго и третьего поколения.
- Десенсибилизирующие препараты. Используются растворы кальция, натрия тиосульфат. Лечение уменьшает проницаемость сосудов, оказывает противовоспалительный эффект, нормализует метаболические реакции в дерме.
- Стабилизаторы клеточных мембран. Чтобы усилить эффективность антигистаминных препаратов, показано лечение стабилизаторами мембран тучных клеток. Некоторые авторы советуют применять полиненасыщенные жирные кислоты омена-3 для нормализации структуры мембран клеток.
- Глюкокортикостероиды. При генерализованных формах мокнущей экземы, отсутствии эффекта от других вариантов лечения применяются гормоны в режиме пульс-терапии или длительного приема.
- Иммунокорригирующие средства. Рациональная иммунокоррекция назначается для облегчения состояния при непрерывно рецидивирующей форме мокнущей экземы. Лечение включает препараты тимуса, стимуляторы лейкопоэза.
- Антибиотики. Лечение антибактериальными средствами требуется при микробной форме дерматоза и доказанной инфекционно-аллергической природе болезни.
Поскольку в патогенезе мокнущей экземы играют роль различные соматические нарушения, лечение включает коррекцию этих патологий. Чтобы нормализовать работу пищеварительного тракта, целесообразно использовать заместительную ферментную терапию, пробиотики и синбиотики, витаминно-минеральные комплексы. Чтобы сбалансировать состояние центральной нервной системы, в схему лечения включаются легкие седативные средства, по отдельным показаниям назначаются транквилизаторы, антидепрессанты.
Местная терапия
В фазе мокнутия используются примочки с вяжущими препаратами, которые уменьшают экссудацию, способствуют более быстрому появлению корочек и регрессу болезни. В острой стадии назначаются ежедневные процедуры длительностью 1-1,5 часа, которые предполагают постоянную смену повязок по мере их подсыхания. Затем переходят к нанесению мазей с топическими кортикостероидами, антисептиками, ингибиторами кальциневрина.
Из физиотерапевтических методов лечения наибольшую результативность показывает селективная ультрафиолетовая терапия, во время которой облучение проводится светом узкого диапазона (311 нм). Также выполняется низкоинтенсивное лазерное облучение красного или инфракрасного спектра, электропунктура биологически активных точек, локальная гипертермия. На этапе ремиссии хороший эффект дает озонотерапия, бальнеотерапия, пелоидотерапия.
Прогноз и профилактика
Правильное лечение мокнущей острой экземы дает возможность быстро купировать кожную симптоматику и улучшить состояние пациентов в целом, поэтому прогноз благоприятный. Спустя 5-6 дней интенсивной терапии уменьшается выраженность зуда, сокращается объем кожных поражений, а выздоровление в неосложненных случаях наступает спустя 3-4 недели. Менее оптимистичный прогноз при развитии экземы у страдающих иммуносупрессией, хроническими патологиями.
Профилактика болезни предполагает соблюдение личной гигиены, исключение типичных пищевых, бытовых и профессиональных аллергенов. Пациентам с экземой в ряде случаев помогает молочно-растительная диета. Обязательными превентивными мерами являются лечение сопутствующих расстройств и правильный уход за кожей тела: применение смягчающих кремов, мягких очищающих продуктов, избегание массажа сухой щеткой и других агрессивных воздействий.
2. Экзема в практике семейного врача: клинические формы, дифференциальный диагноз, лечение/ Е.А. Бардова// Клиническая иммунологии, аллергологии, инфектологии. — 2013. — №1.
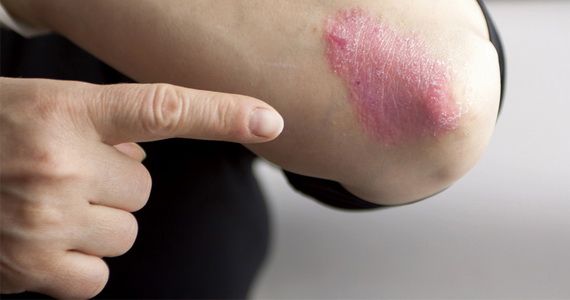
Рассматривая, какие мази применяют при дерматите, стоит сразу сказать, что они делятся на две большие группы: гормональные и негормональные. Они отличаются не только составом, но также степенью эффективности и безопасности.
Мазь считают лучшей от дерматита на коже у конкретного пациента, если она отвечает ряду требований:
- эффективно снимает жжение и зуд;
- купирует острые и хронические воспалительные процессы;
- увлажняет кожу;
- снижает выраженность болевых ощущений;
- препятствует проникновению в очаги воспалений вирусов, грибков и бактерий (об этом говорит отсутствие вторичных присоединившихся инфекций).
Какими негормональными мазями можно лечить дерматит
Негормональные мази считают более безопасными, поскольку они имеют относительно натуральный состав. Это позволяет использовать наружное средство в течение длительного времени без какого-либо вреда для здоровья.
Именно негормональные мази считают лучшими при атопическом дерматите у ребенка. У взрослых в большинстве случаев в начале лечения врачи тоже стараются назначать именно такие мази. По принципу действия они делятся на несколько групп:
- Антисептические. Действие направлено на то, чтобы обеззаразить кожу и исключить проникновение бактерий через образующиеся язвочки.
- Противовоспалительные. Направлены на снятие зуда и раздражения, устранение воспалительных процессов.
- Увлажняющие. Косвенно способствуют выздоровлению за счет восстановления водного баланса кожи.
- Регенерирующие. Их основное действие – стимуляция процессов заживления за счет активации естественной регенерации кожного покрова.
Поскольку средства с одним основным веществом могут снимать только один симптом, врачи часто назначают комбинированные мази. Они за счет нескольких активных компонентов могут оказывать не одно, а несколько эффектов. Примеры негормональных препаратов, претендующих на роль самой хорошей мази от дерматита:
- Бепантен,
- Пантенол,
- Цинковая мазь,
- Радевит,
- Видестим,
- Левосин,
- Фенистил,
- Топикрем.
Из плюсов негормональных мазей особое значение имеет минимум побочных эффектов. Еще большинство из них разрешены к применению у детей, беременных и кормящих женщин.
Главным минусом негормональных мазей часто выступает недостаточная эффективность. Из-за этого лечение может затянуться на несколько недель, месяц и даже дольше. При этом курс нельзя прерывать, иначе предыдущая терапия может оказаться неэффективной. В результате врачу все-таки приходится назначать более сильные гормональные средства.
Выбирая, какая мазь лучше от дерматита, нельзя игнорировать и другие недостатки негормональных мазей:
- могут вызывать аллергию у людей, склонных к аллергическим проявлениям;
- проявляют свое действие не при всех видах дерматита, чаще при контактном и аллергическом.
То есть при длительном лечении мазь вызывает аллергию, но при этом может не давать нужного эффекта.
Гормональные мази
Когда отсутствует положительная динамика от применения негормональных мазей, специалисты прибегают к гормональным препаратам. В их составе основным компонентом выступают глюкокорстикостероиды – гормоны, которые в теле человека вырабатываются надпочечниками. В основе механизма действия таких препаратов лежит влияние на обмен белков и углеводов. Гормональные мази восстанавливают уровень кортизона, при недостатке которого организм становится неспособен справляться с воспалительными процессами.
В зависимости от степени воздействия на кожу гормональные мази делятся на несколько категорий:
- слабые,
- средние,
- сильные,
- очень сильные.
Последние используют только при самых тяжелых формах дерматита, поэтому первыми их никогда не назначают. Примеры гормональных мазей:
- Гидрокортизоновая,
- Целестодерм,
- Акридерм,
- Адвантан,
- Элоком,
- Дермовейт,
- Фуцикорт.
Главные недостатки гормональных мазей при лечении дерматита:
- Привыкание. Самый главный минус, который заключается в том, что со временем мазь перестает быть эффективной для лечения конкретного пациента. Одни и те же активные компоненты гормональных мазей вызывают привыкание.
- Побочные эффекты. Ввиду гормональной природы такие мази имеют множество неприятных побочных действий. Они проявляются при неправильном или слишком долгом применении. В тяжелых случаях может развиться атрофия кожи и даже недостаточность надпочечников.
- Наличие синдрома отмены. Как и в случае с негормональным, при использовании гормональных мазей нельзя прерывать курс и пропускать нанесение. Особенно сильно синдром отмены проявляется при резком отказе от гормонального средства. Это проявляется в том, что симптомы дерматита могут внезапно вернуться. По этой причине гормональные средства отменяют постепенно, уменьшая дозу и количество нанесений.
- венерические заболевания;
- туберкулез;
- беременность и лактацию;
- герпес;
- бактериальные или грибковые поражения кожи.
Какую же мазь использовать
Как видно из обзора мазей от дерматита, и гормональные, и негормональные средства нельзя назвать идеальными для лечения такого заболевания. Клиника «ПсорМак» предлагает в качестве альтернативы и эффективную, и безопасную мазь. Она создана по собственной рецептуре и показывает свою эффективность уже в течение более 25 лет.

В составе мази отсутствуют гормоны. Вместо них только натуральные природные компоненты, которые делают мазь безопасной для детей, беременных и кормящих. Мазь не вызывает побочных эффектов, не приводит к аллергии и обострению симптомов.
Кроме того, мы комплексно подходим к лечению заболевания, прибегая к всесторонней работе с пациентом путем психотерапии, игло- и гирудотерапии. Еще мы разрабатываем для пациентов индивидуальную диету. Такой подход позволяет добиться стойкой ремиссии до 6 лет, что подтверждают отзывы и результаты лечения наших пациентов.
Читайте также:

