При повышении содержания адреналина в крови увеличивается просвет кровеносных сосудов кожи
Обновлено: 19.04.2024
Адренергические причины стенокардии и инфаркта миокарда. Влияние адреналина на коагуляцию
Гормональные влияния могут проявляться и в отношении таких осложнений атеросклероза, как стенокардия и инфаркт миокарда. Многие авторы находят повышение адренергических веществ в крови у больных со стенокардией (А. А. Дубинский и А. Е. Пащенко, 1958). Raab высказал предположение, что приступы стенокардии, вызванные физическим напряжением, действием холода или эмоциональным возбуждением, обусловлены внезапным повышением выделения адреналина, который оказывает гипоксическое действие на сердечную мышцу.
Это предположение базировалось на наблюдениях автора, установившего значительное повышение содержания катехоламинов в крови при приступах стенокардии напряжения, что может привести даже к тромбированию сосудов. Выраженный спазм сосудов повреждает эндотелий сосудистой стенки в связи с ишемией, что способствует прилипанию тромбоцитов к поврежденной поверхности и их агглютинации. Усиление процесса свертывания крови под влиянием адреналина было установлено также Adelson с соавт. (1961).
Спазм коронарных артерий, несомненно, играет главенствующую роль при их тромбозе, так как, помимо сужения просвета сосуда и замедления вследствие этого тока крови, спазм сосудов провоцирует также и рефлекторные изменения в свертывающей и антисвертывающей системе крови, а также в функциональном состоянии тромбоцитов.
Как показали наблюдения, проведенные в пашей клинике ассистентом Л. П. Ермиловым (1960), у больных с частыми приступами стенокардии наблюдается повышение содержания в крови прокоагулянтов и понижение антикоагулянтов. Такое состояние свертывающей системы крови можно расценивать как угрожающее в отношении тромбообразования.
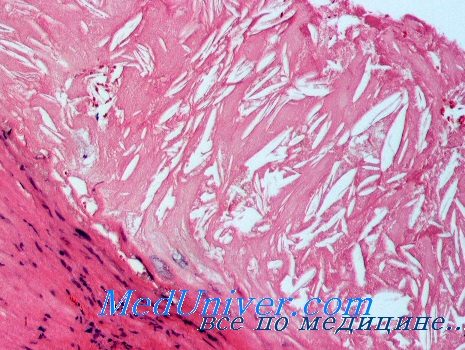
Эти данные были подтверждены также и в работе аспиранта Л. Л. Гущиной (1966), которая изучала функциональные свойства тромбоцитов у больных с приступами стенокардии и нашла повышение коагулябилыюсти пластинок непосредственно после болевого приступа — повышение агглютинабильности, адгезивности пластинок, их вязкого метаморфоза. Наблюдения Л. А. Гущиной стоят в соответствии с интересными данными McKay (1965), который установил влияние адреналина на функциональное состояние тромбоцитов. Приведенные им наблюдения с меченными по Р32 тромбоцитами показали, что под влиянием адреналина срок жизни этих клеток сокращается и резко повышается их разрушаемость, что свидетельствует о состоянии гиперкоагулябильности.
Усиливающее действие адреналина на процесс свертывания крови заключается также в его действии на сосудистый эндотелий, что способствует прилипанию пластинок.
Адренергическим воздействиям придается большое значение и в развитии инфаркта миокарда, который, согласно теории Селье, представляет собой пример тяжелой стрессовой ситуации, в особенности в первый период реакции «бедствия». Forssman (1954) и многие другие авторы считают, что эта реакция обусловлена внезапным поступлением в кровь больших количеств катехоламипов. Проявлениями этой гиперадреналемии считаются гипергликемия, глюкозурия, повышенный лейкоцитоз и анэозинемия.
За последние годы появилось много описаний случаев развития некроза миокарда не в результате тромбоза коронарных артерий, а вследствие повреждения миокарда с развитием его некроза. Считается, что примерно в 15—20% случаев погибших от инфаркта миокарда на секции не находят тромбоза коронарных артерий. Возможно, что повреждающим фактором в этих случаях являются катехоламины, вызывающие гипоксию сердечной мышцы.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.

Большинство людей слышали об адреналине, связанном с реакцией организма на внезапный стресс и экстремальные переживания. Однако не все знают о важной и сложной роли, которую он играет в организме как гормон, вырабатываемый надпочечниками, нейротрансмиттер катехоламинов и жизненно важный препарат.
Адреналин и норадреналин — в чем разница
Связь между адреналином и норадреналином не заканчивается схожим названием. Оба химических вещества принадлежат к группе катехоловых аминов, синтезируемых из аминокислоты тирозина в дофамин, превращающийся в норадреналин. Адреналин — аналог норадреналина, образующийся в результате его дальнейшей трансформации, благодаря катализирующему ферменту — N-метилтрансферазе.
Каждое из этих химических соединений имеет собственные функции в организме, и хотя они обычно стимулируют одни и те же рецепторы, они характеризуются различным сродством рецепторов и следовательно, показывают сходную, но различную физиологическую функциональность в симпатической нервной системе.
- Норадреналин . Отвечает за реакции состояния возбуждения, изменения настроения и участвует в центральной регуляции давления. Он стимулирует альфа-адренорецепторы.
- Адреналин . Обладает системным эффектом. Стимулирует все виды рецепторов -альфа-адренергических и бета-адренергических.
Структуры, производящие, хранящие и высвобождающие катехоловые амины в кровоток, включают ядро надпочечников и нейроны симпатической системы. Ядро надпочечников на 80% отвечает за выработку адреналина, а симпатическая система — за производство норадреналина.
За ингибирование (подавление) секреции инсулина и стимуляцию высвобождения глюкагона отвечают и адреналин, и норадреналин, вызывающий снижение уровня глюкозы в крови.
Адреналин — что это за гормон
Адреналин — это название гормона, вырабатываемого надпочечниковым ядром, что в свободном переводе с латинского и с греческого, означает «над почкой». Впервые он был выделен в 1895 году поляком Н. Цибульским. Гормон относится к биогенным аминам и также содержится в растениях. В разговорной речи его называют гормоном стресса, борьбы или бегства, поскольку его действие запускает защитные силы организма, характерные для угрожающих жизни состояний.
Секреция большого количества адреналина активируется сильными стрессовыми стимулами и заставляет организм быстро прилагать чрезвычайные усилия. Адреналин, высвобождаемый в кровь, работает быстро и быстро деактивируется и разлагается моноаминоксидазой и катехол-О-метилтрансферазой.
Повышение концентрации адреналина в крови вызывает:
- резкое повышение артериального давления, заставляющее мозг, сердце и мышцы получать более высокие дозы кислорода;
- повышение секреции АКТГ, т.е. адренокортикотропного гормона, запускающего ряд тревожных реакций в организме;
- тахикардию, проявляющуюся ускоренным сердцебиением;
- расширение гладкой мускулатуры бронхов, благодаря чему больной легче дышит, и зрачков;
- уменьшение зуда, ангио отека и симптомов крапивницы, являющихся последствиями контакта аллергика с сенсибилизирующим веществом;
- спазмы сосудов кровеносной системы: вен, артерий и капилляров;
- снижение секреции слизи и пищеварительных соков в пищеварительной системе и угнетение перистальтики кишечника и чувство голода;
- повышенный уровень сахара в крови (гипергликемию).
Адреналин – нейромедиатор
Нейромедиаторы – это вещества с разнообразной химической структурой, соответствующие определенным критериям:
- вырабатываются в телах нервных клеток и их окончаниях и хранятся в синаптических везикулах;
- реагируют на электрические раздражители, через которые высвобождаются, а затем соединяются со специфическими рецепторами, после чего индуцируют ответ в постсинаптических нейронах;
- при введении извне в организм действуют по аналогии с веществами, естественным образом вырабатываемыми организмом;
- после выполнения своей функции в организме удаляются с места действия определенным механизмом.
Адреналин соответствует всем вышеперечисленным критериям, являясь нейромедиатором, характеризующим синаптическое и экстрасинаптическое высвобождение. Он также относится к периферическим медиаторам боли, временно повышающим толерантность организма к боли.
Адреналин – это наркотик?
Адреналин – это препарат, продаваемый только по рецепту врача, со специфическими ограничениями на его применение у детей и взрослых. Относится к производным 2-фенилэтиламина.
Это лекарственное вещество с α- и β-адреномиметическим действием, т.е. стимулирующим симпатическую систему. Адреналин — жизненно важный препарат при внезапных состояниях анафилактического и септического шока, приступов бронхиальной астмы.
Показания к применению
Адреналин применяется во многих областях медицины:
Аллергология — во время возникновения острых аллергических реакций в ходе анафилактического шока, вызванного реакцией организма на аллергены, и анафилактоидные ситуации, способные возникнуть внезапно, в связи с реакцией организма на факторы, ранее не вызывающие сенсибилизацию;
Офтальмология — для лечения открытоугольной глаукомы;
Кардиология — в лечении кардиогенного шока;
Лор и стоматология — противоотечные средства слизистой оболочки. Применяют после кровоточащих процедур — удаления зубов, миндалин;
Анестезиология — поскольку в сочетании с местными обезболивающими препаратами продлевает болеутоляющий эффект.
Противопоказания к приему адреналина
Адреналин – это препарат, спасающий жизни, поэтому абсолютных противопоказаний к его применению нет. При угрожающих жизни состояниях, спровоцированных анафилактическим шоком или другими симптомами, перечисленными в показаниях, следует немедленно дать препарат и затем вызвать скорую.
В других случаях, если это возможно, перед введением адреналина следует исключить относительные факторы риска, к которым относятся:
- гипертиреоз;
- артериальная гипертензия;
- легочная эмболия;
- сердечно-сосудистые заболевания;
- почечная недостаточность;
- беременность;
- ишемическая болезнь сердца.
Дозировка и способы введения
Адреналин можно приобрести в аптеках в виде прозрачного раствора в предварительно заполненном шприце. Такая форма позволяет осуществлять быстрый, интуитивно понятный и самостоятельный, ввод препарата детям и взрослым.
Препарат с адреналином следует вводить только в мышцу, расположенную в антеролатеральной части бедра. Затем место инъекции массируют для более быстрого рассеивания препарата по всему телу.
Объем введения препарата рассчитывается исходя из массы тела пациента. Предполагается, что и дети, и взрослые с массой тела более 30 кг должны получать разовую дозу 0,3 мл адреналина. Каждый предварительно заполненный шприц представляет собой одноразовый продукт, содержащий 1 мл препарата.
Хотя количество препарата, рекомендуемое для однократного введения, т.е. 0,3 мл, меньше, чем в шприце, лекарство нельзя использовать повторно. Если симптомы не улучшаются или не усиливаются, может быть введена вторая, та же доза из следующего шприца.
Детям с массой тела менее 30 кг также необходимо принимать дозу 0,3 мл адреналина, поскольку конструкция шприца не позволяет вводить другое количество препарата.
Преимущество предварительно заполненного шприца заключается в том, что он имеет встроенную блокировку, не позволяя вводить большую дозу препарата, чем рекомендуется. Это огромное преимущество, ведь состояние больного, которому приходится вводить себе адреналин, часто мешает ясному мышлению и точным движениям.
Препарат следует применять сразу после появления симптомов шока: покраснения кожи, ангионевротического отека, нарушения дыхания, сердечно-сосудистых проблем и крапивницы. После приема адреналина всегда следует вызывать скорую помощь.
Другие пути введения адреналина (ингаляционная или сублингвальная форма) и дозы препарата могут использоваться только медиками.
Кто должен носить с собой шприц адреналина?
Два шприца с препаратом, содержащим адреналин, должны быть с собой у больных:
- имеющих пищевую аллергию – в любой купленной пище может быть минимальное количество сенсибилизирующих ингредиентов;
- с аллергией на яд насекомых – укус может произойти в любом месте и в любое время;
- когда-либо испытавших симптомы тяжелой аллергической реакции, независимо от вида аллергии;
- перенесших анафилаксию, вызванную физическими упражнениями.
Побочные эффекты и передозировка адреналина
Как и любой другой препарат, адреналин может вызывать побочные эффекты. Наиболее распространенные:
- тревожность, беспокойство, затрудненное дыхание;
- слабость организма, головные боли, головокружение, тремор тела;
- бледность кожи;
- тошнота и рвота;
- тахикардия и выраженное сердцебиение;
- ослабление кровообращения в виде холодных конечностей;
- повышенная работа потовых желез.
Передозировка адреналина затруднена, из-за точно отмеренных доз препарата в предварительно заполненных шприцах и их конструкции, мешающей вводить больше адреналина. Однако может произойти опасное ошибочное внутрисосудистое введение препарата, последствием которого может стать кровоизлияние в мозг.
Прием слишком большого количества адреналина также может вызвать острый отек легких, приводящий к смерти.
Последствия дефицита и избытка адреналина
Дефицит адреналина — редкое состояние, которое может быть результатом генетических дефектов и недостаточности надпочечников, которые его производят.
Повышенный уровень адреналина в крови тоже редок, однако, если он возникает, это может свидетельствовать о развитии опухолей в надпочечниках и нейроэндокринных опухолей и привести к гипертонии.
Последствия нелеченного длительного повышения уровня адреналина — повреждение почек и сердца. Симптомы повышенного адреналина в крови аналогичны увеличению его количества, вызванного стрессовыми ситуациями.
Анализ на адреналин
При возникновении симптомов — длительного ускорения сердцебиения, стойкого повышенного потоотделения, повышения артериального давления и сильных головных болей, следует провести тест на концентрацию метоксикатехоламинов (к которым относятся адреналин и норадреналин) в моче. Такой тест более адекватен, чем образцы, взятые из крови, так как сам акт взятия крови может быть стрессом для пациента, и таким образом концентрация адреналина в крови будет увеличиваться.
Примерно за 3 дня до обследования рекомендуется отказаться от кофе, чая, цитрусовых, шоколада и ванили. Также следует свести к минимуму подверженность стрессу и не заниматься интенсивными видами спорта.
В специальном контейнере для мочи, приобретенном в аптеке, образцы следует собирать в течение 24 часов. Между добавлением дополнительных порций мочи в контейнер, храните ее в закрытом виде в холодильнике, а затем сдайте в лабораторию.

Эти органы издавна привлекали внимание ученых. Впервые их описал в 1563 году выдающийся итальянский врач и анатом Бартоломео Евстахий. В 1855 году английский клиницист Томас Аддисон открыл, что поражение надпочечников вызывает тяжелое заболевание, которое впоследствии было названо его именем.
В настоящее время наука располагает многочисленными данными о строении и функции этих желез внутренней секреции, и, тем не менее, мы не можем с уверенностью сказать, что знаем о них решительно все.
Что такое надпочечники и как они устроены
Надпочечники — парный орган. Они располагаются в виде треугольных колпачков над почками. Надпочечники взрослого человека весят в среднем 12—13 граммов, а у новорожденных — 5—6 граммов. За первый год жизни ребенка вес его надпочечников уменьшается почти вдвое, а затем начинает постепенно возрастать, достигая максимума к двадцати годам.
По своему строению надпочечники неоднородны. В них различают наружный, так называемый корковый слой и внутреннюю часть — мозговое вещество. И хотя корковый слой и мозговое вещество объединены общей капсулой из соединительной ткани, они представляют собой два самостоятельных образования и выполняют различные важные функции.
Функции надпочечников
По количеству вырабатываемых гормонов и разнообразию влияния на многие процессы в организме человека, с надпочечниками не может сравниться ни одна другая желез внутренней секреции.
Кора надпочечников выделяет стероидные гормоны — особые органические соединения, в состав которых входят углерод, водород и кислород. Значение гормонов коркового слоя чрезвычайно велико для нормальной жизнедеятельности организма. Если у животного удалить кору надпочечников, то оно быстро погибнет.
Гормоны надпочечников
В настоящее время ученым удалось выделить из коры надпочечников более 40 стероидных соединений. Они оказывают разнообразное влияние на сложные процессы обмена веществ. Наибольшей активностью в этом направлении обладают гормоны гидрокортизон (кортизон), кортикостерон, альдостерон.
- Гидрокортизон участвует в регуляции всех видов обмена веществ в организме. Особенно заметно его воздействие на углеводный и белковый обмен: гидрокортизон способствует накоплению гликогена в печени и мышцах, тормозит синтезирование белка в одних тканях и ускоряет его образование в других. Он влияет также на обмен жиров, угнетает деятельность лимфоидной и соединительной тканей.
- Кортикостерон обладает сходным, но более слабым действием по сравнению с гидрокортизоном. Третий гормон надпочечников — альдостерон — влияет на водно-солевой обмен, регулируя соотношение натриевых и калиевых солей.
- Если альдостерона вырабатывается недостаточно, то из организма начинают выводиться натрий, хлориды и вода, а калий, наоборот, накапливается. Когда секреция этого гормона повышена, в организме задерживается натрий, и усиленно выделяется калий. И в том и в другом случае нарушается водно-солевой обмен, а это может вызвать различные болезненные симптомы.
Кора надпочечников продуцирует также гормоны, действие которых сходно с половыми. Правда, удельный вес их по сравнению с другими стероидами незначителен. Когда в результате различных причин содержание их превышает норму, то могут развиваться симптомы раннего полового созревания или признаки противоположного пола.
В мозговом веществе надпочечников вырабатываются два гормона: адреналин и норадреналин. Они, как и гормоны коркового слоя, обладают большой биологической активностью и влияют на важнейшие жизненные функции.
- Адреналин, например, повышает основной обмен, усиливает сокращения сердечной мышцы, увеличивает частоту пульса, поднимает артериальное давление крови. Он повышает возбудимость коры головного мозга и действует как быстрый пусковой механизм, когда организму необходимо в короткий срок мобилизовать свои резервы.
- Норадреналин по характеру своего действия близок к адреналину и прежде всего, оказывает влияние на деятельность сердечнососудистой системы.
Таким образом, гормоны надпочечников воздействуют на различные процессы, происходящие в организме, регулируют важнейшие жизненные функции. Они помогают нам быстро приспосабливаться к изменениям окружающей среды.
Особенно велика их роль в возникновении так называемого стресс-синдрома — общей защитной реакции организма в ответ на чрезмерное внешнее раздражение (stress — по-английски напряжение). В этот момент у человека значительно повышается устойчивость организма, мобилизуются сложные защитные механизмы, а это помогает преодолеть вредное воздействие неблагоприятных факторов.
Сигналы об угрожающей опасности воспринимаются центральной нервной системой, ее особым отделом — гипоталамусом, который координирует в организме деятельность желез внутренней секреции. Он воздействует на гипофиз, стимулируя секрецию адренокортикотропного гормона (АКТГ), а тот, в свою очередь, повышает выработку гормонов корой надпочечников.
Таким образом, за очень короткое время происходит мобилизация многих органов и систем организма, обеспечивающая ему надежную защиту от неблагоприятного воздействия внешней среды.
Чем опасны нарушения работы надпочечников
Различные нарушения функции надпочечников вызывают ряд эндокринных заболеваний. Причины таких нарушений разные.
Снижение секреции гормонов коры надпочечников может быть вызвано повреждением их ткани, поражением гипоталамуса, недостаточностью функции гипофиза.
Когда кора надпочечников начинает выделять повышенное количество гормонов и особенно гидрокортизона, у больных развивается так называемый синдром Иценко-Кушинга. При этом нарушаются все виды обмена — углеводный, белковый, жировой, солевой, — развивается ожирение, на коже живота, бедер появляются красно-синюшные полосы растяжения, повышается артериальное давление.
Известно заболевание, при котором снижается секреция гидрокортизона и резко увеличивается продукция половых гормонов, например, мужских (андрогенов). Эта патология может возникнуть в период внутриутробного развития.
И тогда после рождения девочки ее пол определяют неправильно. Такого ребёнка могут долгое время принимать за мальчика. Роковая ошибка обнаруживается лишь в подростковом возрасте, когда начинают развиваться женские вторичные половые признаки. Трагедия может не состоятся, если вовремя обратиться к врачу, который тщательно обследует ребенка и назначит ему необходимое лечение.
Как выявляются проблемы
Существуют два быстрых варианта диагностики заболеваний надпочечников: УЗИ и анализы на гормоны. Обследование, при подозрении на патологии этих органов, назначает уролог, гинеколог или эндокринолог.
Лечение гормонами
В настоящее время гормоны коры надпочечников, обладающие столь высокой биологической активностью, нашли широкое применение в клинической практике. Лечение препаратами, содержащими гормоны надпочечников, должно проводиться только по назначению врача и под его наблюдением. Бесконтрольный прием таких лекарственных средств может вызвать весьма тяжелые осложнения.
Адреналин. Норадреналин. APUD-система. Катехоламины. Контринсулярный гормон. Адреномедуллин. Гормоны мозгового вещества надпочечников и их эффекты в организме.
Мозговое вещество надпочечников содержит хромаффинные клетки, названные так из-за избирательной окраски хромом.
По происхождению и функции они являются постганглионарными нейронами симпатической нервной системы, однако, в отличие от типичных нейронов, клетки надпочечников:
1) синтезируют больше адреналина, а не норадреналина (отношение у человека между ними 6:1);
2) накапливая секрет в гранулах, после поступления нервного стимула они немедленно выбрасывают гормоны в кровь. Регуляция секреции гормонов мозгового вещества надпочечников осуществляется благодаря наличию гипоталамо-симпатоадреналовой оси, при этом симпатические нервы стимулируют хромаффинные клетки через холинорецепторы, выделяя медиатор ацетилхолин.
Хромаффинные клетки являются частью общей системы нейроэндокринных клеток организма, или APUD-системы (Amine and amine Precursors Uptake and Decarboxylation), т. е. системы поглощения и декарбокси-лирования аминов и их предшественников.
К этой системе относятся нейросекреторные клетки гипоталамуса, клетки желудочно-кишечного тракта (энтериноциты), продуцирующие кишечные гормоны, клетки островков Лангерганса поджелудочной железы и К-клетки щитовидной железы.
Гормоны мозгового вещества — катехоламины — образуются из аминокислоты тирозина поэтапно: тирозин—ДОФА—дофамин-норадреналин— адреналин. Хотя надпочечник и секретирует значительно больше адреналина, тем не менее в состоянии покоя в крови содержится в четыре раза больше норадреналина, так как он поступает в кровь и из симпатических окончаний.
Секреция катехоламинов в кровь хромаффинными клетками осуществляется с обязательным участием Са2+, кальмодулина и особого белка синексина, обеспечивающего агрегацию отдельных гранул и их связь с фосфолипидами мембраны клетки.
Катехоламины называют гормонами срочного приспособления к действию сверхпороговых раздражителей среды.
Физиологические эффекты катехоламинов обусловлены различиями в адренорецепторах (альфа и бета) клеточных мембран, при этом адреналин обладает большим сродством к бета-адренорецепторам, а норадреналин — к альфа.
Чувствительность адренорецепторов к адреналину увеличивают гормоны щитовидной железы и глюкокортикоиды. Основные функциональные эффекты адреналина проявляются в виде:
1) учащения и усиления сердечных сокращений,
2) сужения сосудов кожи и органов брюшной полости,
3) повышения теплообразования в тканях,
4) ослабления сокращений желудка и кишечника,
5) расслабления бронхиальной мускулатуры,
6) стимуляции секреции ренина почкой,
7) уменьшения образования мочи,
8) повышения возбудимости нервной системы, скорости рефлекторных процессов и эффективности приспособительных реакций.

Адреналин вызывает мощные метаболические эффекты в виде усиленного расщепления гликогена в печени и мышцах из-за активации фосфорилазы, а также подавление синтеза гликогена, угнетение потребления глюкозы тканями, что в целом ведет к гипергликемии.
Адреналин вызывает активацию распада жира, мобилизацию в кровь жирных кислот и их окисление. Все эти эффекты противоположны действию инсулина, поэтому адреналин называют контринсулярным гормоном. Адреналин усиливает окислительные процессы в тканях и повышает потребление ими кислорода.
Таким образом, как кортикостероиды, так и катехоламины обеспечивают активацию приспособительных защитных реакций организма и их энергоснабжение, повышая устойчивость организма к неблагоприятным влияниям среды.
В мозговом веществе надпочечников, кроме катехоламинов, образуется и пептидный гормон адреномедуллин. Кроме мозгового вещества надпочечников и плазмы крови он выявлен в тканях легких, почек и сердца, а также эндотелиальных клетках сосудов. Этот пептид состоит у человека из 52 аминокислот. Основное действие гормона заключается в мощном сосудорасширяющем эффекте, в связи с чем его называют гипотензивным пептидом.
Второй физиологический эффект гормона заключается в подавлении продукции альдостерона клетками клубочковой зоны коры надпочечников. При этом пептид подавляет не только базальный, фоновый уровень образования гормона, но и его секрецию, стимулированную высоким уровнем калия в плазме крови или действием ангиотензина-II.

Точная причина первичной (эссенциальной) гипертонии неизвестна, но мы знаем, что в развитии патологического состояния играют роль генетические, экологические и возрастные факторы. У большинства людей развивается именно этот тип артериальной гипертонии.
Вторичная артериальная гипертензия — тяжелое состояние, вызванное заболеваниями сердечно-сосудистой системы, почек и эндокринной системы.
Эндокринная гипертензия связана с гормональным дисбалансом, который развивается в эндокринных — внутренних секреторных — железах, особенно в надпочечниках, гипофизе, щитовидной железе. Чаще всего этот вид гипертонии развивается на фоне заболеваний щитовидной железы, хотя существуют и другие, редкие генетические формы эндокринной гипертензии.
Причина артериальной гипертонии — проблемы с надпочечниками
На этот раз мы будем обсуждать заболевания надпочечников, вызывающих эндокринную гипертонию.
Эндокринные железы вырабатывают специальные сигнальные вещества — гормоны, которые активно участвуют в поддержании целостности внутренней среды организма, в том числе в регуляции артериального давления. Причина артериальной гипертонии при эндокринных заболеваниях связана, прежде всего, с задержкой натрия и воды в организме. Кроме того, действие гормонов увеличивает частоту сердечных сокращений, сокращение мышц и уменьшает просвет кровеносных сосудов.
Эндокринная гипертензия может возникать, когда у пациента диагностируется:
- развитие артериальной гипертонии до 30 лет;
- существует семейный анамнез артериальной гипертонии;
- нарушение формирования надпочечников;
- низкое содержание калия в крови (гипокалиемия).
Также эндокринная гипертензия возможна, когда пациент плохо лечится 3-мя или более различными антигипертензивными препаратами (резистентная гипертония).
Роль надпочечников в организме
У надпочечников, как и у самой почки, есть пара. Эти железы расположены на верхушках почек и состоят из двух слоев — наружного, коркового и внутреннего — мозгового. Кора вырабатывает стероидные гормоны, в том числе кортизол и альдостерон, адреналин и норадреналин. Эти гормоны участвуют в поддержании нормального артериального давления, реакции на стресс, нормального уровня сахара в крови, иммунных реакций, обмена веществ, частоты сердечных сокращений и других жизненно важных для организма функций.
Рассмотрим наиболее распространенные заболевания надпочечников, которые вызывают артериальную гипертонию.
Альдостеронизм
Гиперальдостеронизм, или избыток гормона альдостерона в крови, является наиболее распространенным заболеванием, вызывающим эндокринную гипертензию. Существуют две формы патологии:
- первичная, связанная с опухолью надпочечника (чаще доброкачественная) или двустороннее расширение органов (гиперплазия);
- вторичная, связанная с заболеваниями почек, которые вызывают приток крови к нижним конечностям.
Дисфункция надпочечников приводит к избытку альдостерона. Этот гормон поддерживает нормальное кровяное давление, и его излишек вызывает задержку натрия и жидкости в организме, потерю калия (гипокалиемия) и гипертонию. Основной симптом заболевания — повышение артериального давления, которое иногда сопровождается головными болями, головокружением, нарушением зрения, болью в груди, одышкой. Давление постоянно увеличивается.
Гипокалиемия, или низкий уровень калия в крови, клинически проявляется мышечной слабостью и судорогами, сильной жаждой, повышенным мочеиспусканием, тремором и повышенной частотой сердечных сокращений. При альдостеронизме происходит расширение сердца.


Чтобы подтвердить диагноз, необходимо сдать анализы на калий, натрий, ренин, альдостерон. Также необходима визуализация надпочечников — УЗИ надпочечников, компьютерная томография, магнитно-резонансная томография.
Целью лечения является снижение уровня альдостерона в крови, восстановление артериального давления и уровня калия. Болезнь лечат мочегонными препаратами (спиронолактон). Также необходима корректировка образа жизни. Если причиной заболевания является опухоль, необходимо хирургическое вмешательство.
Синдром Кушинга
Синдром Кушинга развивается на фоне нарушений работы гипофиза или надпочечников, которые вырабатывают гормон кортизол, но его наиболее распространенной причиной по-прежнему остается большая доза принимаемых кортикостероидных препаратов (преднизолон, гидрокортизон, дексаметазон).
Эти лекарства назначаются врачами при некоторых воспалительных заболеваниях (таких как артрит) и после пересадки органов. При применении стероидов, которые используются в качестве астматических ингаляторов или при лечении кожных заболеваний, синдрома Кушинга, как правило, не возникает.
Гормон кортизол регулирует кровяное давление и сердечно-сосудистую систему, оказывает противовоспалительное действие, преобразует белки, жиры и углеводы в энергию, уравновешивает действие инсулина и стимулирует реакцию организма на стресс, поэтому его также называют гормоном стресса.
Избыток кортизола вызывают:
- стресс (острые заболевания, операции, травмы, беременность, особенно последний триместр);
- усиленная тренировка мышц;
- депрессия, приступ паники, эмоциональный стресс;
- недостаточное питание или алкоголизм.
При синдроме Кушинга артериальная гипертензия сопровождается:
- ожирением, характерным для лица и спины, между плечами;
- покраснением щек;
- гирсутизмом, прыщами;
- мышечной слабостью;
- переломами костей даже при незначительной травме;
- повышенным уровнем глюкозы в крови ;
- нарушениями менструального цикла;
- депрессией (не всегда).


Для диагностики уровня гормонов проводится анализ крови. Измеряется 24-часовой уровень свободного кортизола в моче. Также используются тесты и методы визуализации (компьютерная томография, магнитно-резонансная томография) с дексаметазоном.
Патологию лечат консервативными и хирургическими методами. Оперативное лечение в основном включает удаление опухоли гипофиза / надпочечников. Также для лечения болезни Кушинга была разработана лучевая терапия. Медикаментозное лечение, как правило, неэффективно и играет лишь вспомогательную роль в облегчении симптомов.
Без лечения болезни могут развиться такие осложнения, как переломы костей, диабет 2 типа, камни в почках.
Феохромоцитома
В мозговом слое надпочечников производятся гормоны страха и агрессии — адреналин и норадреналин. Они контролируют частоту сердечных сокращений, артериальное давление, реакцию на стресс и обмен веществ. Увеличение этих гормонов ставит организм в стрессовое состояние и, таким образом, повышает кровяное давление.
Если опухоль развивается в надпочечнике (9 из десяти) или вне его, начинается неконтролируемый выброс адреналина и норадреналина. В итоге развивается болезнь, называемая феохромоцитомой. Патология может быть обнаружена в любом возрасте, хотя чаще встречается у молодых людей и людей среднего возраста. Считается, что заболевание вызвано генетикой.

Феохромоцитома
Симптомы гипертонии, связанной с этой эндокринной патологией, — кризисы — эпизоды резкого повышения артериального давления. Причиной этого является катехоламины в крови.
В классическом случае кризисы сопровождаются сильными головными болями, потливостью, частотой сердечных сокращений, страхом, раздражительностью, беспокойством, болями в животе. Симптомы диагностируются на основании анамнеза и данных, полученных в результате лабораторной оценки промежуточных продуктов метаболизма гормонов (катехоламинов) и магнитно-резонансной томографии или компьютерной томографии надпочечников.
Лечение заключается в удалении опухоли. В одном из десяти случаев форма злокачественная, поэтому после операции может потребоваться лучевая и химическая терапия. Вскоре после операции может развиться дефицит гормонов надпочечников. В это время рекомендуется заместительная терапия стероидными препаратами.
Эндокринная артериальная гипертензия имеет четкую клиническую картину. Высокое кровяное давление всегда сопровождается признаками избытка гормонов. В диагностике и лечении этой патологии принимают участие врачи разных профилей, но основную роль играют эндокринологи. Лечение основного заболевания помогает регулировать кровяное давление, но наблюдаться у врача нужно всю жизнь.
Читайте также:

