При колите кишечника сыпь
Обновлено: 26.04.2024
Неспецифический язвенный колит (НЯК) — это хроническое воспалительное заболевание кишечника, этиология которого на сегодняшний день остается неизвестной. Частота неспецифического язвенного колита, по данным зарубежных исследователей, составляет 4–10 на 1
Неспецифический язвенный колит (НЯК) — это хроническое воспалительное заболевание кишечника, этиология которого на сегодняшний день остается неизвестной. Частота неспецифического язвенного колита, по данным зарубежных исследователей, составляет 4–10 на 100 тыс. детей [1]. Сложности в подборе терапии НЯК связаны с отсутствием знаний об этиологии и некоторых звеньях патогенеза заболевания [2].
В выборе наиболее оптимальной схемы лечения неспецифического язвенного колита в первую очередь помогает определение степени активности воспалительного процесса и его локализации. По данным литературы, при неспецифическом язвенном колите воспалительный процесс в 54% случаев локализуется в прямой и сигмовидной кишках, в 28% случаев отмечается левостороннее поражение толстой кишки, а у 18% больных встречается панколит. У детей раннего возраста (до трех лет) преимущественно поражаются правосторонние отделы толстой кишки [3].
Степень активности неспецифического язвенного колита определяется исходя из выраженности клинических и лабораторных показателей. Наиболее ярко выражены следующие клинические показатели: диарея, наличие крови в стуле, интенсивность болей в животе, потеря массы тела и повышение температуры. Лабораторные показатели неспецифического язвенного колита включают изменения уровня гемоглобина, альбумина, повышение СОЭ. В настоящее время выделяют три степени активности неспецифического язвенного колита: легкую, среднюю и высокая (см. таблицу 1) [4, 5].
Среди основных направлений в лечении неспецифического язвенного колита следует упомянуть коррекцию питания и диетотерапию. Принципы рационального питания предполагают отказ от жареных, жирных, соленых, острых блюд, молока и молочных продуктов.
В рацион больного ребенка нельзя включать также шоколад, бобовые продукты, грибы, фрукты и овощи, стимулирующие перистальтику (сливы, киви, курагу, свеклу). В периоды обострения ограничивается потребление клетчатки, сладкого, соков [6]. При длительной ремиссии рацион питания можно значительно расширить, однако молоко и молочные продукты больному противопоказаны на протяжении всей жизни [7].
Медикаментозная терапия как основной метод лечения неспецифического язвенного колита предполагает применение:
- препаратов 5-аминосалициловой кислоты (5-АСК);
- кортикостероидов;
- иммунодепрессантов (цитостатиков).
Симптоматическая и антибактериальная терапия назначается для восстановления структуры слизистой оболочки, нормализации перистальтики, восстановления процессов пищеварения и эубиоза толстой кишки, повышения общей иммунореактивности организма. При неэффективности диетотерапии и медикаментозной терапии показано хирургическое лечение.
Препараты 5-АСК в лечении неспецифического язвенного колита являются базисными. В 1942 году препарат сульфасалазин был впервые применен у больных с сочетанным поражением кишечника и крупных суставов, что дало выраженный положительный эффект: произошло купирование артралгий и гемоколита [8]. Сульфасалазин используется в терапии неспецифического язвенного колита до настоящего времени. Однако его применение ограничено из-за большого количества побочных эффектов, таких, как гемолитическая анемия, нейтропения, лекарственный гепатит, синдром Стивена-Джонсона, перикардит, интерстициальный нефрит, панкреатит. Частота побочных эффектов, по данным разных авторов, составляет от 5 до 55% [9]. В состав сульфасалазина входят месалазин (5-аминосалициловая кислота), обладающий противовоспалительным эффектом, и сульфапиридин, который обеспечивает доставку месалазина в толстую кишку,
в место локализации основного воспалительного процесса при неспецифическом язвенном колите. Сульфапиридин способствует развитию большого количества побочных эффектов [10]. Многочисленные исследования, проводившиеся в целях разработки препаратов, содержащих месалазин, позволили в конце 70-х — начале 80-х гг. создать препараты, в состав которых сульфапиридин не входил. Это привело к значительному снижению количества побочных эффектов, что, в свою очередь, сделало возможным применение более высоких доз месалазина и в некоторых случаях позволило отказаться от использования кортикостероидов. Месалазин активен при местном контакте со слизистой оболочкой кишечника, и его терапевтическая эффективность коррелируется с концентрацией в просвете кишечника. Эти особенности месалазина позволили разработать на его основе и успешно применять препараты как в острый период, так и в целях поддерживающей терапии местного действия, такие, как свечи, микроклизмы [11].
В таблице 2 представлены некоторые из препаратов 5-АСК [12], которые можно разделить на три группы. К первой группе относятся сульфасалазин и олсалазин, высвобождающиеся под действием кишечной флоры и действующие в толстой кишке. Ко второй группе можно отнести мезакол, салофальк, ровазу. Высвобождение этих препаратов зависит от рН среды, а их действие локализуется в терминальном отделе подвздошной кишки и в толстой кишке. К третьей группе относится препарат пентаса, который высвобождается медленно и действует на протяжении всего кишечника.
Механизм действия 5-АСК основывается на противовоспалительном эффекте, который реализуется через ингибирование образования простагландинов, снижение синтеза цитокинов IL-1, IL-2, IL-6, фактора некроза опухолей, торможение липооксигеназного пути метаболизма арахидоновой кислоты, снижение продукции свободных радикалов [13, 14, 15].
Показания к применению препаратов 5-АСК.
- Первичная терапия при легкой степени активности НЯК.
- Первичная терапия в комбинации со стероидами при НЯК средней и высокой степени активности.
- Поддерживающая терапия при НЯК.
В нашей стране из препаратов 5-АСК наиболее часто используются сульфасалазин, салофальк и пентаса. Как отмечалось ранее, сульфасалазин применяется в терапии НЯК уже на протяжении 60 лет. Расщепление сульфасалазина на месалазин и сульфапиридин зависит от состава кишечной флоры и происходит только в толстой кишке [16]. При локализации воспаления в слепой кишке и восходящих отделах толстой кишки (у детей раннего возраста) эффективность сульфасалазина значительно снижается.
Салофальк — действующим веществом у данного препарата является месалазин. Препарат представляет собой таблетки, покрытые оболочкой, устойчивой к действию желудочного сока. Его особенностью является отсутствие сульфокомпонента, что снижает количество побочных эффектов. Активация салофалька происходит при изменении кислотности среды (свыше 6). Место действия салофалька — преимущественно терминальный отдел подвздошной кишки и толстая кишка [17].
На российском рынке препарат пентаса появился относительно недавно. Действующее вещество — также месалазин, заключенный в микрогранулы, устойчивые к кислой среде желудка. Пентаса высвобождается медленно, постепенно, по ходу кишечника, начиная с двенадцатиперстной кишки. При этом изменения уровня внутрипросветного рН и ускорение транзита при диарее не влияют на скорость высвобождения препарата. Благодаря этим особенностям пентаса обеспечивает высокую терапевтическую концентрацию на протяжении всей тонкой и толстой кишок [18, 19].
При лечении неспецифического язвенного колита дозы препаратов 5-АСК подбираются индивидуально. Обычно доза сульфасалазина составляет 50–60 мг/кг/сут; максимальная суточная доза, при которой не отмечается развитие побочных эффектов, — до 6 г/сут [20]. Дозировка месалазина составляет от 20 до 50 мг/кг/сут, максимальная суточная доза — 4 г/сут. В данных дозировках препарат может применяться от одного до трех месяцев [21]. Салофальк и пентаса используются при местной терапии в свечах и микроклизмах: свечи — 250–500 мг один-два раза в сут, микроклизмы — 2–4 мг один раз в сут. Местная терапия проводится в течение 14–28 дней, при необходимости возможно назначение повторных курсов местной терапии. Поддерживающие дозы 5-АСК при неспецифическом язвенном колите составляют половину от терапевтической дозы: сульфасалазин — 20 мг/кг/сут, месалазин — 10 мг/кг/сут. Поддерживающую терапию назначают длительно, от шести месяцев до двух лет, при отсутствии активного воспалительного процесса [22].
Побочные эффекты при использовании месалазина встречаются достаточно редко (1–3%) [23]. При этом отмечаются боли в животе, диарея, метеоризм, тошнота, рвота, панкреатит. Встречаются аллергические реакции в виде кожного зуда, аллергической сыпи. Бронхоспазм, перикардит, миокардит, интерстициальный нефрит отмечаются крайне редко, их частота, по данным литературы, составляет 0,1-0,5% [24]. Для предупреждения побочных эффектов не рекомендуется превышать максимально допустимые терапевтические дозы препаратов, следует контролировать состояние периферической крови (общий анализ крови один раз в две недели). Также необходимы повторные биохимические анализы крови, включающие определение уровня общего белка, белковых фракций, мочевины, креатинина, трансаминаз, щелочной фосфатазы, электролитов, сывороточного железа.
Помимо препаратов 5-АСК в терапии неспецифического язвенного колита применяются кортикостероиды. Наиболее часто используются преднизолон, метилпреднизолон, гидрокортизон. Механизм действия кортикостероидов основывается на противовоспалительном эффекте, снижении образования простогландинов, ингибировании образования и действия цитокинов IL-1, IL-2, IL-3, фактора некроза опухолей и стабилизации лизосомальных мембран [25]. Показаниями к применению кортикостероидов при неспецифическом язвенном колите являются отсутствие эффекта от терапии месалазином при легкой степени активности НЯК (в сочетании с месалазином), первичная терапия при средней и высокой степени активности НЯК. Лечение кортикостероидами часто осложняется из-за множественных побочных эффектов, среди которых наиболее распространенными являются подавление гипоталамо-гипофизарной системы, синдром Кушинга, артериальная гипертензия, остеопороз, пептические язвы, электролитные нарушения, стероидный диабет [26]. Побочные эффекты носят дозозависимый характер и нарастают при увеличении длительности гормональной терапии. Для их профилактики необходим контроль состояния периферической крови, биохимических показателей, электролитного состояния крови.
Дозы глюкокортикоидов при лечении неспецифического язвенного колита для перорального и/или парентерального приема составляют: при назначении преднизолона — 1–2 мг/кг/сут, метилпреднизолона — 25–30 мг/сут. Для местной терапии возможно использование преднизолона в свечах 20-40 мг 1 раз в сутки и/или в микроклизмах 20 мг на 60-100 мл жидкости 1 раз в сутки. Гидрокортизон обычно применяется только при местной терапии в микроклизмах 100 мг на 60–100 мл воды 1 раз в сутки. Длительность терапии при пероральном приеме составляет 2-3 недели, затем необходимо постепенное снижение дозировки препаратов по 10 мг в неделю до уровня 0,75 мг/кг/сутки. В дальнейшем снижение проводится по 5 мг в неделю вплоть до полной отмены препарата. При этом доза 5-АСК не должна быть ниже 1/2 терапевтической дозы [27].
Гормональная терапия может привести к развитию гормональной зависимости, при которой положительный эффект или отсутствует, или сменяется реактивацией воспалительного процесса на фоне снижения дозы или отмены кортикостероидной терапии [28]. Выделяют две формы гормональной зависимости неспецифического язвенного колита (по отношению к стероидам): гормонорезистентную форму, которая является первичной, и гормонозависимую, которая часто оказывается вторичной. При этом чувствительность к препаратам 5-АСК может сохраняться или отсутствовать [29]. Для преодоления гормональной зависимости применяют повышенные дозы глюкокортикоидов, пульс-терапию, при неэффективности этих мер показана иммуносупрессивная терапия [19].
К иммуносупрессорам, применяемым в терапии неспецифического язвенного колита, относятся азатиоприн, 6-меркаптопурин, метотрексат, циклоспорин. Механизм действия этих препаратов различен. Азатиоприн и 6-меркаптопурин воздействуют на естественные киллеры [30], метотрексат нарушает синтез РНК и ДНК клеток [31], циклоспорин угнетает продукцию цитотоксических лимфоцитов и ингибирует интерлейкины IL-2, а также их рецепторы [32].
Показаниями к применению иммунодепрессантов при неспецифическом язвенном колите являются гормонорезистентные и гормонозависимые формы.
Дозы иммунодепрессантов при лечении неспецифического язвенного колита, по данным разных авторов, сильно различаются. Обычно азатиоприн назначается по 1-2 мг/кг/сутки, 6-меркаптопурин — в дозе 1,5 мг/кг/сутки. Режим дозирования устанавливается индивидуально. Эффект от терапии этими препаратами отмечается через 3 месяца. Метотрексат применяется по 2,5 мг/сутки, терапевтический эффект от применения метотрексата наступает гораздо раньше, чем у азатиоприна: через 3-4 недели. Циклоспорин обычно применяется коротким курсом для прерывания активности процесса с последующим переходом на иммунодепрессанты пролонгированного действия [33].
Токсические эффекты, возникающие при использовании антидепрессантов, очень разнообразны. К ним относятся анорексия, тошнота, рвота, угнетение кроветворения, кожная сыпь, артралгии, миалгии, панкреатит, токсический гепатит, синдром холестаза, оппортунистические инфекции, лимфоаденопатия, артериальная гипертензия, токсическое поражение почек, парастезии, тремор. Тяжесть проявления побочных эффектов иммуносупрессоров ограничивает их применение в лечении неспецифического язвенного колита [34]. Для предупреждения возникновения побочных эффектов необходимо контролировать функции кроветворения, печени, почек. Общий анализ крови, общий анализ мочи, биохимический анализ крови, включающий в себя определение уровня общего белка, белковых фракций, печеночных ферментов, щелочной фосфатазы, мочевины, креатинина, глюкозы, белков острой фазы, — все эти исследования необходимо проводить один раз в неделю.
Симптоматическая терапия при неспецифическом язвенном колите показана при любой степени активности воспалительного процесса. В каждом особом случае она подбирается индивидуально. Ферментные препараты (креон, мезим-форте) часто назначаются при наличии синдрома мальабсорбции и для разгрузки поджелудочной железы. Желчегонные препараты и гепатопротекторы применяются при наличии у больного синдрома холестаза и токсического гепатита. Для коррекции витаминной, метаболитной недостаточности и железодефицитной анемии применяются поливитамины, препараты железа (для парентерального введения), метаболитный комплекс. В комплекс лечебных воздействий желательно включать фитотерапию (калган, ромашку, кровохлебку, солодку). Антибактериальная терапия назначается при наличии вторичных инфекций, септических осложнений, перианальных воспалений. Применяются антибиотики, нитрофурановые препараты, метронидазол (трихопол) [27].
Схема терапии неспецифического язвенного колита, разработанная Европейской ассоциацией детских гастроэнтерологов, гепатологов и нутриологов (ESPGHAN) и применяемая в отделении гастроэнтерологии и гепатологии НЦЗД РАМН, основывается на различных степенях активности и локализации воспалительного процесса. При изолированных проктитах основным методом лечения является местная терапия в виде свечей и/или микроклизм. При легкой степени активности можно ограничиться применением только препаратов месалазина (салофалька, пентасы). Изменение кишечной флоры делает неэффективным лечение сульфасалазином в свечах. Схема терапии неспецифического язвенного колита при проктитах представлена в таблице 3.
При проктосигмоидитах средней и высокой степени активности помимо местной терапии показан пероральный прием месалазина или преднизолона в возрастных дозировках. Схема терапии проктосигмоидита приводится в табл. 4.
Панколит, или тотальное поражение кишечника, обычно имеет среднюю или высокую степень активности. При лечении панколита применяются месалазин или сульфасалазин перорально и преднизолон в больших дозах перорально или парентерально, при наличии поражения прямой кишки показана местная терапия (см. таблицы 3 и 4). Схема терапии панколита при неспецифическом язвенном колите представлена в таблице 5 Дозы препаратов 5-АСК даны для детей старше 12 лет. Для детей младше 12 лет дозировка препаратов рассчитывается исходя из массы тела: сульфасалазин — 60 мг/кг/сутки, месалазин — 30–40 мг/кг/сутки.
Таким образом, лечение неспецифического язвенного колита основывается на определении локализации воспалительного процесса и степени его активности. При легкой степени активности показано назначение препаратов месалазина, средняя и высокая степени активности требуют назначения кортикостероидной терапии. При отсутствии эффекта от терапии препаратами 5-АСК и стероидами и развитии гормональной зависимости применяется иммуносупрессивная терапия. При неэффективности медикаментозной терапии показано хирургическое лечение.
Литература
Е. Г. Цимбалова, кандидат медицинских наук
А. С. Потапов
П. Л. Щербаков, доктор медицинских наук
НЦЗД РАМН, Москва
Что такое колит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Куракина Александра Анатольевича, проктолога со стажем в 11 лет.
Над статьей доктора Куракина Александра Анатольевича работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Колит (лат. colitis, от греч. kolon (толстый кишечник) и itis (воспаление) — собирательное понятие, включающее большую группу заболеваний с одним общим признаком: воспалением толстого кишечника.
Основные признаки колита: частый жидкий стул с кровью, боль в животе и высокая температура.
Колиты встречаются в практике гастроэнтерологов, инфекционистов, терапевтов, колопроктологов, хирургов и других специалистов.
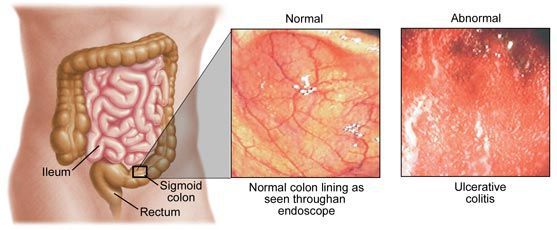
Этиология колита
Основные формы колитов можно описать только по отдельности, в зависимости от этиологического фактора. Размеры статьи не позволяют коснуться всех видов колита. Рассмотрим только основные из них.
Инфекционный колит — это заболевание кишечника, возникающее из-за активизации условно-патогенных микроорганизмов в кишечнике или попадания новых болезнетворных микробов из внешней среды. [1]
Инфекционный колит имеет очень широкое распространение: нет человека, ни разу не переносившего данное заболевание. Количество заболевших увеличивается в жаркий период, когда создаются благоприятные условия для распространения инфекции. Поэтому чаще болеют люди в регионах с жарким климатом (Африка, Юго-Восточная и Средняя Азия). Заболевание чаще встречается в детском возрасте, особенно у детей, посещающих учебные заведения (детские сады, школы и т. д.). Гастроэнтерологи и проктологи могут встречать в практике больных с данной патологией, но она не является профильной. Лечат заболевание обычно инфекционисты.
Причины инфекционного колита:
- бактерии (шигеллы, эшерихии, сальмонеллы, клостридии, иерсинии, брюшнотифозная палочка, кампилобактерии, протей, стафилококки);
- вирусы (аденовирус, энтеровирус, ротавирус);
- простейшие (амебы, лямблии и др.);
- возбудители туберкулеза и сифилиса;
- грибки (кандида, актиномицеты). Возникновение грибкового колита свидетельствует о снижении иммунитета и часто проявляется у лиц, страдающих СПИДом, получающих химиотерапию, стероидные гормоны;
- дисбактериоз.
Формы инфекционного колита:
- катаральная;
- фиброзная;
- катарально-геморрагическая;
- флегмонозная;
- флегмонозно-гангренозная;
- некротическая.
Воспалительные явления могут иметь стадийный характер, а могут сразу иметь картину запущенного воспаления. Его выраженность напрямую зависит от характера инфекции. Некротическое и флегмонозно-гангренозное воспаление встречается при клостридиальной инфекции. Катарально-геморрагическое — при дизентерии. Катаральное воспаление встречается чаще при вирусных заболеваниях. [2]
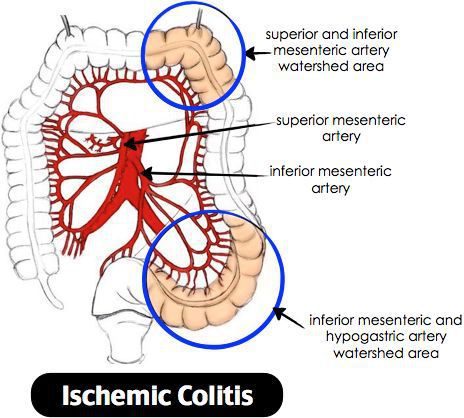
Ишемический колит — воспаление стенки толстого кишечника, возникающее из-за нарушения процессов кровобращения. Существует хроническое и острое нарушение кровообращения. [3]
Причиной нарушения кровообращения является полное прекращение или критическое снижение притока крови к толстой кишке, вследствие чего возникает воспаление. При тяжёлом течении может приводить к некрозу стенки кишечника. Причиной закупорки сосудов могут быть тромбы, но чаще всего к сужению просвета сосуда приводят атеросклеротические бляшки. Поэтому болезнь чаще проявляется у лиц пожилого возраста. Около 79% больных ишемическим колитом старше 48 лет. [4] Частота встречаемости не имеет связи с половой принадлежностью и регионом. Впервые открыт в 1966 году. Ишемический колит является профильным заболеванием для колопроктологов, но им также занимаются общие хирурги и гастроэнтерологи. [5]
Причины ишемического колита:
-
сосудов;
- закупорка брыжеечных сосудов вследствие эмболии или тромбоэмболии (в результате аллергических реакций, травм, осложнений операций, системного васкулита, ДВС-синдрома);
- снижение давления крови может приводить к нарушению питания стенки кишки.
Закупорка просвета сосуда приводит к ишемии стенки кишки, а как следствие — к некрозу и далее перфорации. [6]
Объём поражения зависит от размера питающей артерии, длительности закупорки. Если закупорка сосуда происходит постепенно (при образовании атеросклеротических бляшек в сосудах), то говорят о хроническом нарушении кровообращения, что в свою очередь приводит к стриктурам.
При критических состояниях и снижении давления крови (например, анафилактический шок, ДВС-синдром и т.д.), происходит централизация кровообращения, при этом резко снижается приток крови к кишечнику, что приводит к ишемии и некрозу.
При атеросклерозе чаще страдает сигмовидная и поперечная ободочная кишка. Воспаление начинается со слизистой оболочки, затем переходит на все слои. [7]
По характеру поражения выделяют:
- транзиторную форму (когда ишемические процессы обратимы);
- стенозирующую (когда формируются стриктуры);
- гангренозную (когда образуются язвы с дальнейшим развитием некроза, поражение носит необратимый характер). [8]
Лучевой колит — образуется в результате ионизирующего воздействия на стенку толстого кишечника.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы колита
Симптомы острого и хронического колита: боль в животе, кровь в кале, диарея, высокая температура, слабость, слизь и кровь в стуле, спазмы.
Симптомы язвенного колита: к перечисленным выше признакам добавляются боли в анусе и анемия.
Боли при колите кишечника:
Инфекционный колит
Клиника инфекционного колита напрямую зависит от возбудителя.
Для любого инфекционного колита независимо от этиологии характерно:
- начало заболевания, как правило, имеет острый характер;
- жидкий частый стул с примесью слизи в кале;
- боли локализуются чаще в левом подреберье, но могут также распространяться по всем отделам живота;
- боль имеет периодический, спазматический характер;
- высокая температура;
- чувство слабости, недомогания;
- сухость кожных покровов и слизистых;
- белый налет на корне языка;
- рвота как первый симптом колита кишечника (если в воспалительный процесс вовлечен желудок).
Для первичной оценки этиологии инфекционного колита оценивают характер дефекации, объём и особенности каловых масс.
- при дезентерии стул очень частый, малыми порциями (до 20 раз за день) со слизью и прожилками алой крови (ректальный «плевок»);
- при амебиазе кал имеет вид малинового желе;
- при сальмонеллезе кал напоминает болотную тину, имеет неприятный запах;
- при псевдомембранозном колите (вызыванном клостридиями) частый жидкий стул с запахом гнили.
Ишемический колит
Симптоматика очень вариабельна, характерно быстрое прогрессирование.
- болезненные ощущения в животе;
- кровь и слизь в стуле;
- неустойчивый, частый стул;
- выраженные боли в околопупочной и левой подвздошной области;
- при ректальном осмотре можно заметить кал с кровью, слизью или гноем;
- при хронической форме боли имеют низкую интенсивность, обычно возникают после еды;
- при длительной хронической ишемии появляются стриктуры в толстой кишке, которые в дальнейшем могут быть следствием непроходимости или малигнизации (раковому перерождению).
Лучевой колит
Обычно колит формируется у лиц, перенёсших курс лучевой терапии по поводу новообразований, локализующихся в области малого таза или брюшной полости. [12]
- большую чувствительность к излучению имеет тонкий кишечник, формируется лучевой энтерит, который клинически проявляется нарушением абсорбции в тонком кишечнике;
- повреждению кишечника свойствен избирательный характер, обычно воспаление локализуется в прямой и сигмовидной кишке, при этом клиника сопоставима с клиникой язвенного и ишемического колита. При воздействии больших доз радиации клиника развивается не сразу, проявляется обильным, жидким стулом, при этом нарушается всасывание в толстом кишечнике. [13]
Патогенез колита
Толстый кишечник очень восприимчив к ионизирующему излучению. [10] Лучевой колит возникает при воздействии малых доз облучения: происходит атрофия слизистой оболочки (сразу после облучения).
- Усиливаются процессы деления клеток, уменьшается длина ворсинок.
- Активизируются воспалительные процессы с нейтрофильной реакцией. Чаще всего эти процессы локализуются в прямой и сигмовидной кишке.
- При воздействии больших доз (более 40 Гр.) воспалительные процессы могут возникать спустя длительное время после облучения (до нескольких лет), в данной ситуации происходит воспаление мелких сосудов кишечника, что приводит к ишемизации кишечника. Развиваются язвы и стриктуры. Могут поражаться все отделы толстого и тонкого кишечника. [11]
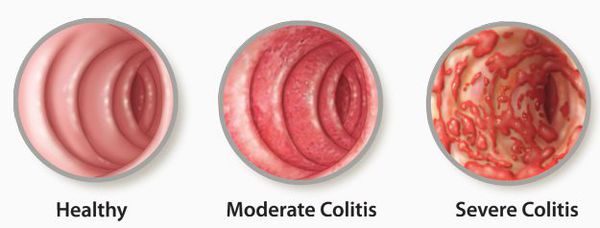
Классификация и стадии развития колита
По течению:
По этиологии:
- язвенный колит кишечника и болезнь Крона (воспалительные заболевания кишечника с неизвестной этиологией);
- инфекционный (этиологический фактор бактериальный, вирусный, грибковый, паразитарный);
- ишемический (развивается вследствие снижения притока крови к толстой кишке);
- спастический (из-за неправильного питания нарушается моторика толстого кишечника и возникают спазмы);
- токсический (при применении нестероидных противовоспалительных препаратов);
- лучевой (при поражении радиацией).
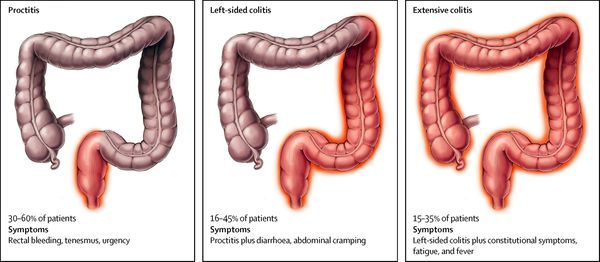
По локализации:
| Вид колита | Локализация |
|---|---|
| проктит | воспаление прямой кишки |
| панколит | тотальное поражение кишечника |
| тифлит | воспаление слепой кишки |
| трансверзит | воспаление поперечной ободочной кишки |
| сигмоидит | воспаление сигмовидной кишки |
| диффузный колит кишечника | охватывает два и более отдела кишечника |
Поражение кишечной стенки подразделяют на три вида:
- катаральный колит кишечника — слабое воспаление, слизистая краснеет, и возникает отёк;
- эрозивный колит кишечника — появляются эрозии;
- атрофический колит кишечника — слизистая атрофируется.
Осложнения колита
- сильное кровотечение;
- перфорация толстой кишки;
- сильное обезвоживание; ;
- воспаление кожи, суставов и глаз;
- повышенный риск рака толстой кишки;
- токсичный мегаколон;
- повышенный риск образования тромбов в венах и артериях [15] .
Диагностика колита
Инфекционный колит:
- Лабораторные методы:
- анализ кала на вирусы, бактерии, паразиты (позволяет точно поставить диагноз);
- серологическое исследование (определяют антитела к вирусам, паразитам);
- анализ крови на стерильность (при подозрении на сепсис);
- общеклинический анализ крови (высокое СОЭ, увеличение количества лимфоцитов при вирусной этиологии).
- Инструментальные методы:
- ректороманоскопия используется как дополнительный метод для дифференциальной диагностики;
- ультразвуковое исследование используется для исключения осложнений.
Ишемический колит:
- Ректороманоскопия дает возможность оценить состояние слизистой оболочки. При осмотре можно отметить наличие точечных кровоизлияний, сглаженность сосудистого рисунка, бледность слизистой. При обнаружении данных признаков показано взятие биопсии.
- Ирригоскопия — самое необходимое исследование. Обнаруживается симптом пальцевых вдавливаний. Признаки дефектов слизистой свидетельствуют о наличии язв, сужения просвета при стриктурах.
- Колоноскопия показана для уточнения распространенности воспаления, также показана биопсия в области измененного участка.
- Ангиография позволяет определить степень сужения сосуда и его локализацию. [9]
- Злокачественные новообразования. Опухоли развиваются достаточно длительное время, в течении многих лет.
- Инфекционный колит. Преобладают симптомы общей интоксикации (слабость, лихорадка и т.д.). Кроме того, имеет место эпидемический анамнез.
- Язвенный колит и болезнь Крона. Для них характерно достаточно медленное прогрессирование. Проявляются обычно в раннем возрасте.
Лучевой колит:
- При сборе анамнеза учитывают наличие факта облучения ионизирующей радиацией.
- Ректороманоскопия и колоноскопия с биопсией позволяют выявить воспаление слизистой оболочки толстого кишечника. При лучевом энтерите воспаление сочетается с атрофией слизистой. Крипты становятся менее глубокими, уменьшается длина ворсинок. При лучевом колите на слизистой обнаруживают язвы, стриктуры. [14]
- Энтерит лучевого генеза следует дифференцировать с болезнями тонкой кишки, при которых страдает функция всасывания (целиакия), при данных заболеваниях происходит атрофия по гиперрегенераторному типу, а при лучевом поражении преобладают гипорегенераторные процессы слизистой.
- Радиационные поражения толстого кишечника дифференцируют с язвенным колитом, болезнью Крона, новообразованиями толстого кишечника. [15]
Лечение колита
Инфекционный колит:
- антибактериальные, противогрибковые средства с учетом чувствительности микроорганизмов. Предпочтение отдают таблетированным формам препаратов;
- восполнение потерянной жидкости и минералов: растворами для приема внутрь (Регидрон и др.), внутривенное введение (раствор Рингера, Трисоль и др.);
- прием сорбентов;
- пробиотики и пребиотики;
- ферменты (креон, фестал);
- симптоматическая терапия (противовоспалительные средства, спазмолитики и др.)
Ишемический колит:
- консервативное лечение колита (щадящая диета, препараты, смягчающие стул, лекарства для улучшения кровотока, дезагреганты, витаминные препараты, дезинтоксикационное лечение, восполнение баланса электролитов и жидкости, гемотрансфузии (при показаниях), антибактериальные препараты);
- оперативное лечение колита.
Показаниями для срочного хирургического лечения служат:
- перфорация, толстокишечная непроходимость. В таком случае удаляется участок кишки, с последующей санацией и дренированием брюшной полости.
- плановое оперативное лечение колита кишечника показано больным в случае сужения (стриктуры) толстого кишечника без явлений острой кишечной непроходимости.
Терапия лучевого колита схожа с терапией язвенного колита и болезни Крона:
- лекарства, содержащие 5-аминосалициловую кислоту (месалазин, салофальк);
- антибактериальная терапия.
Может быть полезно вести дневник питания, чтобы отслеживать, что вы едите, а также свои чувства. Если вы обнаружите, что некоторые продукты вызывают обострение ваших симптомов, вы можете попробовать их устранить.
Диетотерапия
Убедительных доказательств того, что неправильное питание приводит к воспалению кишечника, нет. Но оно может усугубить симптомы болезни, особенно при обострении. Поэтому полезно вести дневник питания и отслеживать свои реакции на определённые продукты.
- есть меньше молочных продуктов — у пациента может быть непереносимость лактозы, т. е. организм не переваривает молочный сахар;
- есть небольшими порциями по 5–6 раз в день;
- пить больше жидкости — предпочтительнее вода; алкоголь и напитки, содержащие кофеин, стимулируют кишечник и могут усилить симптомы болезни [15] .
Прогноз. Профилактика
На сегодняшний день хорошо известны причины возникновения инфекционного колита, разработаны современные методики лечения. Поэтому при неосложненном течении и вовремя начатой терапии удается достигнуть полного выздоровления. Менее благоприятный прогноз у лиц с явлениями иммунодефицита и ослабленной иммунной системой (например, у людей пожилого возраста). Прогноз благоприятный.
Основными методами профилактики являются:
- гигиенические мероприятия (тщательное мытье рук);
- использование только свежих продуктов, чистой воды;
- уделение особого внимания термической обработке пищи.
При транзиторной форме ишемического колита прогноз благоприятный. При гангренозной форме — зависит от вовремя поставленного диагноза и проведенного лечения.
Так как ишемический колит является осложнением других болезней, то для его профилактики необходимо:
- своевременное лечение сопутствующих заболеваний;
- сбалансированное питание.
Лучевой колит приводит к постоянным, необратимым изменениям кишечной стенки, поэтому прогноз неблагоприятный.
При радиационном колите могут появляться язвы и стриктуры на слизистой оболочке толстого кишечника, что может привести к кишечной непроходимости. В таком случае необходимо хирургическое лечение, от своевременности которого зависит прогноз. При правильном и вовремя проведенном лечении прогноз благоприятный. Специальных методов профилактики лучевого колита не существует.
Что такое псевдомембранозный колит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Аверина Александра Анатольевича, гастроэнтеролога со стажем в 15 лет.
Над статьей доктора Аверина Александра Анатольевича работали литературный редактор Вера Васина , научный редактор Роман Васильев и шеф-редактор Маргарита Тихонова

Определение болезни. Причины заболевания
Псевдомембранозный колит (Pseudomembranous colitis) — это острое воспалительное заболевание толстого кишечника, вызываемое токсигенными штаммами бактерии Clostridium difficile [1] . Микроб вырабатывает токсины А и В, повреждающие кишечную стенку, и белок, угнетающий перистальтику кишечника. В результате возникает диарея, боль в животе, появляется слизь и иногда примесь крови в кале.
Характерным признаком заболевания являются фиброзные наложения на слизистой оболочке толстой кишки [27] [28] .

Псевдомембранозный колит (ПМК) чаще всего развивается после лечения антибиотиками. Его ещё называют Clostridium difficile-ассоциированным псевдомембранозным колитом, антибиотик-ассоциированным псевдомембранозным и клостридиозным колитом.
Эпидемиология
Заболеваемость ПМК лучше всего отслеживается в США и странах западной Европы [2] . В России статистический учёт заражения C. diff не ведётся. Согласно систематическому обзору за 2011 год, каждый 5-й случай из всех антибиотик-ассоциированных диарей (ААД) и каждый 2–3 случай внутрибольничной ААД в странах Европы и Северной Америки вызваны C. diff [3] .
В стационарах США среди внутрибольничных инфекций C. diff занимает первое место (12,1 % от общего количества), опережая K. pneumoniae (9, 7 %) и E. coli (9,3 %) [4] . В 2011 г. было зафиксировано более 450 тыс. случаев C. difficile-ассоциированной болезни и более 29 тыс. смертей от неё [29] .
В европейских странах заболеваемость C. diff составляет около 7 случаев на 10000 койко-дней, т. е. при средней госпитализации 10 дней, 7 случаев из 1000 госпитализаций заканчиваются ПМК. В 20 европейских странах это значение колеблется от 0,7 до 28,7 на 10000 койко-дней [5] .
В России в 2011 году было продано 295 млн упаковок антибиотиков, в 2019 — 379 млн [8] [26] . Антибактериальных препаратов потребляется всё больше, их продажа из аптек не контролируется, поэтому проблемы ААД и ПМК актуальны и в нашей стране.
В клиниках Санкт-Петербурга у пациентов с ААД тест на токсины C. diff был положительным в 47,7 % случаев [6] .
Смертность от ПМК колеблется от 9,3 до 22 % и зависит от возраста пациента, смерть чаще наступает при тяжёлом течении заболевания [7] [26] .
В настоящее время увеличилась внутри- и внебольничная заболеваемость C. difficile-ассоциированной болезнью, расширились группы риска, стали чаще встречаться рецидивы и тяжёлые формы, в том числе вызванные более патогенным штаммом BI/NAP1/027, возросла смертность [27] .
Причины псевдомембранозного колита
Основная причина болезни — это приём антибиотиков. ПМК могут вызывать любые антибактериальные препараты, но наиболее часто к нему приводит применение Клиндамицина, хинолонов, цефалоспоринов 2-го и 3-го поколения, карбапенемов. Реже ПМК развивается после приёма макролидов, пенициллина, Тетрациклина, Тигециклина.
К факторам риска, помимо приёма антибиотиков, относятся:
- возраст старше 65 лет;
- терапия ингибиторами протонной помпы и Н2-гистаминоблокаторами — препаратами, снижающими секрецию соляной кислоты в желудке;
- лечение в стационаре, особенно в отделениях реанимации, — каждые 7 дней госпитализации увеличивают риск ПМК на 8 % [1][9][10] ;
- наличие дополнительной патологии, в том числе воспалительных заболеваний кишечника, ВИЧ, сахарного диабета[31][32][33] ;
- хирургические вмешательства на органах ЖКТ;
- энтеральное питание, в том числе через назогастральный зонд;
- приём иммуносупрессивных препаратов (глюкокортикостероидов, Такролимуса) и противоопухолевых средств [31] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы псевдомембранозного колита
Наиболее частые симптомы лёгкого или умеренного псевдомембранозного колита:
- водянистая диарея (жидкие испражнения, похожие на кашицу) от трёх раз в сутки на протяжении двух и более дней в сочетании с болью в животе;
- лёгкие спазмы в животе, часто сопровождающиеся с позывами на стул, но не всегда приводящие к дефекации;
- примеси слизи, крови или гноя в испражнениях;
- температура тела 38,5 °С и более;
- тошнота или потеря аппетита.
При тяжёлом течении псевдомембранозного колита возникает водянистая диарея с кровью, уровень альбумина снижается менее 30 г/л, что сочетается с одним из следующих симптомов: высоким уровнем лейкоцитов в клиническом анализе крови (> 15×10 9 /л) и/или болезненностью при ощупывании живота. На фоне длительной диареи организм теряет много жидкости, что приводит к обезвоживанию и проявляется тёмно-жёлтой мочой, чувством жажды, усталости, головокружением, спутанностью сознания и заторможенностью [1] [9] .
При рецидиве болезни симптомы появляются повторно менее чем через 8 недель после окончания терапии.
Проявления псевдомембранозного колита схожи с симптомами других инфекций, поражающих толстый кишечник. Но в отличие от них признаки ПМК могут быть слабо выражены и, как правило, наблюдаются долго: от одной недели до нескольких месяцев. Также встречаются случаи, когда человек является носителем возбудителя ПМК — C. diff, но симптомы полностью отсутствуют.
Патогенез псевдомембранозного колита
В основе патогенеза ПМК лежит чрезмерное размножение бактерий C. diff на фоне уменьшения или гибели нормальной микробиоты толстого кишечника. C. diff вырабатывает токсины А и В, которые вызывают воспаление в кишечной стенке. На течение заболевания влияет состояние иммунной системы пациента и патогенные свойства бактерий, такие как вирулентность, наличие токсинов А и В.
Основной путь передачи инфекции — фекально-оральный. Бактерии попадают в организм с загрязнённых поверхностей, например с дверных ручек, смесителей, ручек смыва сливного бачка, мебели или медицинского инвентаря. Также переносить инфекцию может персонал больницы и заражённые пациенты.
Бактерии C.diff образуют споры, которые устойчивы к действию антибиотиков и могут длительно сохраняться в желудочно-кишечном тракте человека, заражая окружающих и вызывая рецидивы заболевания у самого пациента [12] .
Для некоторых людей C.diff — это часть нормальной микрофлоры ЖКТ, но в таком случае численность бактерий контролируется за счёт других микроорганизмов и работы иммунной системы.
Основные поражающие факторы C.diff — это выделяемые ею токсины [1] . Токсин А (энтеротоксин, белковая молекула с массой 308 кДа) влияет на секрецию жидкости, приводит к повреждению слизистой оболочки кишечника (мембран клеток) и вызывает воспалительный ответ со стороны иммунной системы.

Токсин В (цитотоксин, белковая молекула с массой от 250 до 270 кДа) в 1000 раз более цитотоксичен по сравнению с токсином А. Он вызывает распад филаментного актина — белка, поддерживающего целостность клеток. В результате клетки слизистой разрушаются и гибнут. Токсин В опасен для человека, но не приводит к воспалению и повреждению слизистой оболочки кишечника у животных.
Под действием токсинов в кишечной стенке развивается специфическое воспаление с характерными изменениями на поверхности слизистой. Она становится отёчной, разрыхляется, приобретает ярко-красный цвет, на ней исчезает сосудистый рисунок. При контакте эндоскопа со слизистой капельки крови не появляются. Наблюдается множество желтовато-белых бляшек диаметром 3–5 мм, которые плотно фиксированы к слизистой оболочке. При взятии биопсии они отрываются с трудом, торцом эндоскопа не снимаются. Преобладает два типа воспалительных реакций: диффузно-катаральное воспаление слизистой и очаги фибриноидного некроза — бело-жёлтые бляшки, или псевдомембраны, поэтому такой тип колита называется псевдомембранозным.
![Бляшки при ПМК [35]](https://probolezny.ru/media/bolezny/psevdomembranoznyy-kolit/blyashki-pri-pmk-35_s.jpg)
В биоптатах, полученных из воспалительно-изменённых участков слизистой, выявляют скопление иммунных клеток крови и слизистой, расширение капилляров и некроз клеток покровного эпителия [1] .
В биоптатах, взятых из бляшек, присутствует фибрин, обрывки некротизированного покровного эпителия, слизь, лейкоциты, плазматические клетки и колонии бактерий.
Чтобы определить патогенность клостридий, нужно выявить их токсины. Посев биоптатов на питательные среды удовлетворительных результатов не даёт. Метод в данном случае затратен и неинформативен, поэтому токсины C. diff определяют в кале.
Воспалительный процесс, как правило, захватывает несколько отделов толстого кишечника, но чаще поражена его прямая и сигмовидная часть, реже вовлекается вся толстая кишка. Протяжённость её поражения связана с тяжестью течения заболевания: чем больше толстого кишечника вовлечено в воспалительный процесс, тем тяжелее протекает колит и ярче симптомы.
Продолжительное воспаление в кишечной стенке приводит к следующим нарушениям:
- не всасывается жидкость, из-за чего развивается обезвоживание;
- потери крови из образующихся эрозий и язв приводят к анемии;
- кишечная стенка становится проницаемой для токсинов возбудителя и продуктов его жизнедеятельности, находящихся в просвете кишки, из-за чего нарастает общая интоксикация.
При тяжёлом течении прекращается перистальтика толстого кишечника, развивается токсический мегаколон и возникает полиорганная недостаточность, из-за чего пациент может погибнуть.
Классификация и стадии развития псевдомембранозного колита
ПМК входит в группу антибиотик-ассоциированных диарей. В Международной классификации болезней (МКБ-10) псевдомембранозный колит кодируется как АО 4.7 — Энтероколит, вызванный Clostridium difficile.
В зависимости от тяжести течения болезни и клинической картины выделяют следующие формы:
- ПМК лёгкой или умеренной тяжести. Проявляется диареей — неоформленным жидким, кашицеобразным стулом три или более раз в сутки и болью в животе.
- ПМК тяжёлого течения. Сопровождается водянистой диареей с кровью и изменениями в анализах. В биохимическом анализе крови отмечается низкий уровень альбумина (меньше 30 г/л), который сочетается с одним из следующих признаков: высоким уровнем лейкоцитов в клиническом анализе крови (> 15×10 9 /л) в клиническом анализе крови и/или болезненностью при ощупывании живота.
- Осложнённые формы ПМК. Протекают с водянистой диареей с кровью и одним из следующих симптомов: снижение артериального давления, температура тела ≥ 38,5 °C, отсутствие перистальтики тонкого кишечника, помрачение или угнетение сознания. В клиническом анализе крови лейкоциты повышены > 25×10 9 /л или снижены < 2×10 9 /л, возникает органная и почечная недостаточность, требуется искусственная вентиляция лёгких.
- Рецидивирующее течение ПМК. Заболевание развивается повторно менее чем через 8 недель после окончания терапии [1][14] .
Данная классификация используется для выбора схемы лечения.
Осложнения псевдомембранозного колита
Наиболее частые осложнения псевдомембранозного колита:
- Обезвоживание и электролитные нарушения — из-за сильной и длительной диареи нарушается ритм сердца, снижается артериальное давление и мышечный тонус. Чаще эти осложнения развиваются при недостаточном восполнении потерянной жидкости и солей.
- Почечная недостаточность — при стремительном обезвоживании нарушается работа почек, из-за чего снижается частота мочеиспусканий, появляются отёки, по анализам крови видно, что растёт содержание азотистых шлаков.
- Токсический мегаколон — расширение толстой кишки, редкое осложнение с плохим прогнозом. На фоне диареи частота стула резко урежается до одного раза в сутки, в дальнейшем дефекация прекращается полностью. Это происходит из-за замедления и полного прекращения перистальтики толстого кишечника. Из-за распирания толстого кишечника газами и содержимым нарастает вздутие живота, усиливается боль в нём. Интоксикация и электролитные нарушения приводят к резкому ухудшению самочувствия и выраженной слабости. В дальнейшем стенка кишки разрывается, содержимое изливается в брюшную полость (перфорация кишечника) и начинается перитонит. Как правило, это осложнение наблюдается у ослабленных пациентов, находящихся в отделении реанимации и хирургии.
- Перфорация кишечной стенки — образуется сквозное отверстие в кишечной стенке с излитием содержимого кишечника в брюшную полость и развитием перитонита.
- Полиорганная недостаточность — может привести к гибели пациента [1][15] .
Диагностика псевдомембранозного колита
Тесты на C. diff показаны при длительной диарее с болью в животе и/или примесью крови в стуле, возникшей спустя 3–60 суток после выписки из стационара и/или после приёма антибиотиков [1] .
Чтобы выявить токсигенные штаммы C. diff, токсины A и B определяют в кале [16] .
Для этого используют следующие методы:
- Цитотоксиновый копрологический тест. Чувствительность — 95 %, специфичность — 99 %, результат — в течение 2–3 дней.
- ELISA (Enzyme Linked Immuno Sorbent Assay) — фермент-связанный иммуносорбентный тест для определения токсинов. Чувствительность — 70–90 %, специфичность — 99 %, результат — через 4–6 часов.
- ПЦР (полимеразная цепная реакция) на токсин В. Чувствительность — 96 %, специфичность — 100 %, результат — в течение нескольких часов.
Чувствительность теста — это доля положительных результатов среди больных людей, т. е. вероятность правильно определить инфекцию у заболевших, отсутствие ложноотрицательных результатов. Специфичность — доля отрицательных результатов среди здоровых людей, т. е. отсутствие ложноположительных результатов.
Посев кала на C.diff не проводится, так как этим методом не удаётся определить токсигенные штаммы.
С помощью дополнительных методов можно оценить тяжесть состояния пациента и своевременно выявить осложнения.
К дополнительным обследованиям относятся:
- ректороманоскопия или сигмоидоскопия — позволяют обнаружить типичные изменения стенки кишки (множественные желтоватые бляшки 2–10 мм в диаметре, плотно фиксированные на поверхности слизистой оболочки);
- колоноскопия — помимо типичных изменений кишечной стенки, определяется распространённость процесса и поражение толстого кишечника выше сигмовидной кишки [17] ;
- обзорная рентгенография органов брюшной полости — используется, чтобы выявить признаки пареза кишечника и токсического расширения кишки;
- анализ крови — показывает уровень лейкоцитов (при ПМК повышен до 10–50 × 10 9 ), уровень креатинина (выше нормы) и альбумина (ниже нормы).
Гистологическое исследование биоптатов не является необходимым при C. difficile-ассоциированной болезни, но может быть крайне важным для дифференциальной диагностики.
Лечение псевдомембранозного колита
Методы лечения псевдомембранозного колита в российских и зарубежных клинических рекомендациях совпадают [1] [18] . При лёгком и среднетяжёлом течении его проводят в амбулаторных условиях (дома), при тяжёлом и/или осложнённом — в стационаре.
Для лечения ПМК назначаются антибиотики:
Антибиотики подавляют развитие C. diff. Бактерия чувствительна только к трём перечисленным антибактериальным препаратам.
При развитии осложнений ПМК могут применяться следующие методы:
- При токсическом мегаколоне показана колэктомия — удаление толстой кишки.
- Для лечения рецидивирующего ПМК в качестве экспериментального метода рассматривается трансплантация кишечной микробиоты (fecal microbiota transplantation, FMT) [23][24][25] . Кишечную микробиоту берут от здорового донора и при помощи назоинтестинального зонда, клизмы или колоноскопии переносят пациенту в кишечник. В России такое лечение считается экспериментальным. Проводится в научных клинических учреждениях, например в Федеральном научно-клиническом центре ФМБА России.

В качестве вспомогательных и симптоматических препаратов используются:
- Сорбенты (Диоктаэдрический смектит) — эффективно удаляет токсины C. diff, снижая их действие на кишечную стенку, улучшает качество стула.
- Пробиотики (Lactobacillus rhamnosus, Bifidobacterium longum, Bifidobacterium bifidum, Bifidobacterium infantis не менее 1×10 9 КОЕ/г) — подавляют активность C. diff. Данные об их эффективности пока противоречивы [22] .
- Препараты на основе дрожжей Saccharomyces cerevisiae (boulardii) — эффективны как вспомогательные и профилактические средства.
Прогноз. Профилактика
При лёгком или среднетяжёлом течении ПМК и хорошей реакции на стандартную терапию прогноз благоприятный, при тяжёлом и осложнённом — неблагоприятный. При рецидивирующем течении прогноз сомнительный, так как не разработаны эффективные схемы лечения.
Профилактика псевдомембранозного колита
Для профилактики развития ПМК следует:
- чаще мыть руки и соблюдать правила личной гигиены;
- рационально принимать антибиотики — строго по назначению врача с соблюдением всех указаний;
- изолировать пациентов с инфекцией C. diff в отдельные палаты, соблюдать меры санитарного режима;
- тщательно обрабатывать все поверхности хлорсодержащими или другими дезинфицирующими средствами, активными против спор C. diff;
- сокращать сроки госпитализации пациентов старше 65 лет [16] .
Чтобы предотвратить рецидив C. difficile-ассоциированной болезни, после завершения лечения Метронидазолом или Ванкомицином назначаются пробиотики курсом не менее трёх месяцев. Серьёзных побочных эффектов от них не выявлено [34] .
Читайте также:

