Последствия лучевой терапии при раке кожи на лице
Обновлено: 27.04.2024
Лучевая терапия опухоли. Значение лучевой терапии в дерматоонкологии.
До настоящего времени не утратила своего значения лучевая терапия эпителиальных новообразований кожи, обеспечивающая гибель опухолевых клеток путем повреждения хромосомного аппарата и торможения митотическои активности. При этом следует учитывать, что большинство пролиферирутощих клеток опухоли радиочувствительны на стадии митоза и сразу после нее, непролиферирующие же клетки отличаются очень низкой радиочувствительностью и легко восстанавливают повреждения, давая рост новым клеткам. Невозможность уничтожения 100% злокачественных клеток из-за нахождения их в разных периодах жизненного цикла требует фракционирования суммарной дозы облучения.
Применяют следующие методы лучевой терапии: использование электронного пучка, низковольтную или ортовольтную рентгенотерапию, а также близкофокусную рентгенотерапию и имплантацию радиевых игл. Показаниями для проведения лучевого лечения являются: плоскоклеточный рак кожи, базалиома (в частности, кистозная и язвенная формы), эритроплазия Кейра, болезнь Боуэна, рецидивные эпителиальные новообразования кожи, возникшие после других методов лечения и локализующиеся вблизи естественных отверстий (глаза, носа, ушные раковины и т.д.). Лучевое лечение проводят больным с наличием противопоказаний к хирургическому лечению, лицам пожилого возраста, а также при диаметре новообразования, не превышающем 20 мм. Оно также проводится в качестве адъювантной герапии при глубоких инвазивных и метастатических раках кожи.
Лучевая терапия обычно безболезненна и хорошо переносится больными. В то же время она сопровождается развитием местных лучевых реакций нормальных тканей в облучаемой зоне. Степень их выраженности зависит как от методики облучения (уровень разовых и суммарных поглощенных доз, ритм облучения, размер полей), так и от распространенности опухоли, состояния нормальных окружающих тканей и др. Существенное влияние на течение лучевых реакций оказывает и общее состояние больного. Острые лучевые реакции кожи, как правило, ограничиваются эритемой и явлениями сухого эпидермита, которые не требуют перерыва в лечении, проходят самостоятельно или купируются 5% метилурациловой или пар-мидиновой мазью. При проведении лучевой терапии нередко имеется и риск развития лучевых осложнений (лучевых дерматитов, конъюнктивитов, катаракты, перихондритов, трофических язв, общей слабости, потери аппетита, головных болей и головокружения, лейко- и лимфопении, тромбоцитопении идр.), наблюдающихся примерно в 18% случаев. Это требует постоянного контроля состояния периферической крови и коррекции осложнений путем назначения гемостимулирующих препаратов, витаминов, дезинтоксикационной терапии, симптоматического лечения и т.д. Лучевая терапия неэффективна при склерозирующих формах опухолей и малоэффективна при наличии фистул и рубцов.
В ряде случаев, особенно в зависимости от площади воздействия, период заживления кожи после лучевой терапии может продлиться до 8 недель. Ограничивает ее применение и развитие неудовлетворительных в косметическом отношении атрофических рубцов с депигментацией и телеангиэктазиями, особенно часто возникающих в области груди и конечностей, а также невозможность повторного использования при развитии рецидива опухоли. Рубец после лучевой терапии существенно затрудняет диагностику рецидива. Важно отметить, что лучевая терапия приводит к нарушению кровоснабжения кожи, костей и мягких тканей, ухудшая заживление ран, в связи с чем рецидив после применения лучевой терапии очень сложно поддается и хирургическому лечению. В таких случаях также затруднено проведение пластических реконструктивных операций.
Для лечения эпителиальных новообразований кожи наиболее широко применяется фракционная близкофокусная рентгенотерапия, которая осуществляется путем ежедневного воздействия на очаг; поглощенная разоваядоза составляет 3-5 Гр (300-500 рад), общая суммарная доза — 50-70 Гр (5000-7000 рад).
При опухолях, расположенных в области губ, ушных раковин, век, с выраженной инфильтрацией подлежащих тканей методом выбора является внутритканевая гамма-терапия.
По данным литературы, косметический эффект после проведения лучевой терапии в 57,2% случаев был хорошим, в 24,8% — удовлетворительным и в 11,1% — плохим; однако частота осложнений варьировала от 4,9 до 80% случаев; рецидивы же после лучевой терапии базалиомы отмечались в 5-20% случаев.
Частота рецидивирования выше при локализации опухоли на волосистой части головы, носу, в периорбитальной области, а также при большей площади очагов поражения.
Суммируя приведенные данные, необходимо отметить, что несмотря на появление новых, более эффективных и более безопасных методов, рентгенотерапия не утратила своего значения при ряде злокачественных новообразований кожи и может явиться методом выбора при лечении некоторых форм базалиомы, плоскоклеточного рака кожи, эритроплазии Кейра, болезни Боуэна.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Когда речь идет о лечении меланомы, большинство представляет кожные новообразования - темного цвета, неправильной формы. Но, во-первых, злокачественная опухоль при меланоме может быть беспигментной, а во-вторых, меланома локализуется не только на коже. Насколько сложной задачей является лечение меланомы, и какое место в нем занимают методы лучевого лечения (радиохирургия и лучевая терапия) - рассказывает сайт МИБС.
Что такое меланома?
Меланома (иногда встречается название “меланобластома”) - злокачественная опухоль из меланоцитов, клеток, вырабатывающих естественный пигмент меланин, поглощающий УФ-лучи для защиты кожи от ионизирующего воздействия солнечного света. Преимущественно, локализуется в коже, однако меланома может возникнуть в любом органе, в состав тканей которого входят меланоциты (слизистые оболочки и ткани глазного яблока).
Факторы, повышающие риск развития меланомы, хорошо изучены:
- загар;
повышение пигментации кожи, вызванное воздействием ультрафиолетового излучения (как солнечного, так и искусственного - в соляриях), - важнейший фактор риска меланомы; его вес в развитии меланомы настолько высок, что солярии запрещены в некоторых странах, а во многих под запретом находится их использование несовершеннолетними - наследственность;
те, у кого в семейной истории есть случаи меланомы, должны максимально внимательно отнестись к пунктам этого списка - фенотип;
чем светлее волосы и кожа у человека, тем выше вероятность меланомы - солнечные ожоги;
особенно перенесенные в детском и подростковом возрасте могут сыграть роковую роль - именно в этих местах чаще всего возникают злокачественные опухоли кожи - перенесенная меланома;
те, кто прошел через лечение меланомы, должны быть намного внимательнее - иммунитета от этого заболевания нет; наоборот, рецидивы меланомы - частое явление - образования на коже;
невусы (родинки или родимые пятна), особенно в количестве более 50 - серьезный повод регулярно проходить обследование у дерматолога и защищать кожу от избытка ультрафиолета; доброкачественное новообразование меланоформный невус (он же: диспластический меланоцитарный невус, синдром атипического невуса) - дает аналогичный повод; - пигментная ксеродерма;
наследственное заболевание, проявляющееся в повышенной чувствительности кожного покрова к ультрафиолету, также требует более внимательного отношению к любым изменениям на коже
Меланома и ее статистика
Но значительный объем данных о природе меланомы обусловлен не простотой визуальной диагностики (которая, как будет показано в следующем разделе, проста не во всех аспектах), а той агрессивностью, которая делает меланому одним из самых смертельных онкологических заболеваний в мире, и самым смертельным видом рака кожи. Согласно последним статистическим исследованиям, меланома кожи (составляет основную часть всех меланом) встречается в семь раз реже, чем другие виды рака кожи, но количество ежегодных смертей от меланомы выше в 2,5 раза.
Заболеваемость меланомой в семь раз меньше, чем другими видами рака кожи, а смертность - в 2,5 раза выше
Высокие статистические показатели объясняют важность, которое имеет лечение меланомы для человечества. В целом же, меланома занимает 19-е место среди других онкологических заболеваний в мире, немного уступая раку яичников, злокачественным опухолям мозга и нервной системы.
Диагностика меланомы
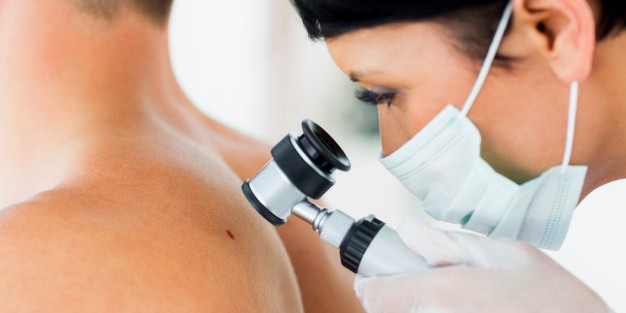
Лечение меланомы, как и любой опухоли, проходит успешнее, если новообразование выявлено на ранней стадии. В теории, ранняя диагностика меланомы кожи - простая задача. Визуальное изменение существующих невусов (частичная потеря пигментации, “рваные” края, асимметрия, выпадение волос и др.) привлекают внимание человека либо его близких. Пациент обращается к врачу-дерматологу или дерматологу-онкологу, где проходит визуальное неинвазивное обследование - дерматоскопию, которая позволяет буквально “заглянуть” в глубокие слои кожи для оценки распространенности опухоли (зачастую, меланома растет вглубь кожи, что означает более неблагоприятный прогноз, чем рост в горизонтальной плоскости). Стандарт современной диагностики меланомы - применение цифрового дерматоскопа, позволяющего получить снимки интересующего участка кожи в электронном виде для последующего наблюдения в динамике, или для получения срочной консультации либо “второго мнения”.
Однако на практике отсутствие должной онконастороженности приводит к игнорированию ранних симптомов меланомы кожи. А коварство заболевания состоит в том, что меланома может начать метастазировать даже при небольшом размере новообразования. Это приводит к тому, что пациент обращается на поздней стадии, когда требуется не только лечение первичной меланомы, но и ее метастазов.
Особенного подхода требует диагностика увеальной (внутриглазной меланомы). Сосудистая оболочка (хориоидея) и сетчатка глаза также содержат меланоциты, вырабатывающие меланин для защиты этих структур от ультрафиолетового излучения, попадающего внутрь глазного яблока. Опухолевое поражение этих структур, независимо от его природы, обычно имеет специфические симптомы (зоны “выпадения” изображения, вспышки, “молнии” и т.д.), которые должны насторожить и привести к квалифицированному офтальмологу, не только способного идентифицировать меланому, но и обладающего необходимым оборудованием для первичной диагностики новообразования, которое позволит начать лечение без промедления.
Наиболее сложная задача - диагностика меланомы слизистых оболочек. Иногда новообразования видны невооруженным глазом (например, меланома слизистой рта, меланома вульвы). Но меланома в скрытых местах (например, слизистой кишечника) может быть выявлена уже после того, как пациент обратится к врачу по поводу метастазов меланомы и будет начат поиск первичной опухоли. К счастью, меланома слизистых оболочек встречается крайне редко. По современным данным ее доля - не более 5% всех случаев меланомы.
Для окончательного подтверждения диагноза “меланома кожи” должна быть проведена биопсия образца ткани опухоли. Чрезвычайная опасно проводить частичный забора препарата, например, методом соскоба, при котором повышается вероятность распространения опухолевых клеток, - на морфологическое исследование следует направлять препарат тканей, иссеченных с определенным запасом по контуру. Лечение меланомы слизистых оболочек и внутриглазной меланомы следует начинать после всестороннего инструментального обследования, чаще всего УЗИ, КТ и МРТ с контрастом.
Диагностика метастазов меланомы
При подтверждении первичного диагноза, перед тем, как начать лечение первичного очага меланомы, необходимо провести диагностику для выявления возможных метастазов опухоли. Именно вторичная меланома намного чаще становится причиной смерти, чем первичное новообразование. Лимфогенные метастазы меланомы появляются в регионарных лимфатических узлах, а распространяемые с кровотоком гематогенные метастазы меланомы чаще всего отмечаются в печени, легких, костях, и головном мозге. Наиболее опасными являются метастазы в головной мозг.
Диагностика метастазов меланомы может включать:
- биопсию сторожевого лимфоузла;
- УЗИ периферических лимфоузлов, органов брюшной полости, малого таза и забрюшинного пространства;
- компьютерную томографию (КТ) органов грудной полости;
- магнитно-резонансную томографию (МРТ) или КТ органов брюшной полости с контрастированием (при локализации первичной меланомы кожи на нижней половине туловища или на нижних конечностях проводится КТ/МРТ органов малого таза с контрастированием);
- КТ/МРТ головного мозга с контрастом;
- уровень лактатдегидрогеназы (ЛДГ) в крови;
- при подтверждении начала метастазирования может быть проведено ПЭТ или ПЭТ-КТ всего тела.
Целесообразность каждого из видов диагностики определяет лечащий врач исходя из обоснованности подозрений наличия и степени метастатического поражения. Полученные результаты являются важной информацией для правильного подбора тактики лечения меланомы.
Лечение меланомы
Тактика лечения разрабатывается исходя из локализации меланомы и распространенности опухолевого процесса.
Лечение меланомы на ранних стадиях
При отсутствии распространения в другие части организма (I-II стадии), меланома кожи подлежит хирургическому иссечению с обязательным морфологическим исследованием удаленного фрагмента тканей. Также может быть проведено удаление сторожевого лимфоузла для морфологической диагностики на предмет распространения меланомы через лимфатическую систему. Без подтверждения распространенности процесса методы лекарственной терапии применяются редко.
Лучевое лечение меланомы
Лечение меланомы кожи и меланомы слизистых оболочек методами лучевой терапии (в т.ч. радиохирургии и протонной терапии) не демонстрирует должного эффекта, поэтому не получило распространения в клинической практике, уступив хирургии. Однако при меланоме глаза (увеальная меланома) которая представлена меланомой сосудистой оболочки (меланома хориоидеи) и меланомой радужной оболочки, высокоточное подведение высоких доз ионизирующего излучения (радиохирургия и протонная терапия) показывает высокие результаты, сравнимые, по эффективности, с удалением (энуклеацией) глазного яблока.
Протонная терапия является более сложным и более дорогим методом, к тому же лечение меланомы глаза протонами требует длительного курса лечения. Поэтому наиболее широко в мировой практике распространена радиохирургия, при которой высокая разовая доза ионизирующего излучения приводит к остановке биологических процессов в клетках опухоли.
Радиохирургия на Гамма-ноже, выполняемая в Онкологической клинике МИБС, позволяет получить органосохраняющее лечение меланомы глаза с соблюдением высоких международных стандартов. При этом стоимость лечения на Гамма-ноже, как правило, не превышает стоимости операции по удалению глазного яблока или пораженных его участков, при этом качество жизни пациента после радиохирургического лечения опухоли глаза - несоразмеримо выше, т.к. сохраняется не только орган (глазное яблоко), но и, в подавляющем большинстве случаев, его функция (зрение).
Лечение метастазов меланомы
Метастатическая меланома требует комплексного подхода к лечению. В зависимости от особенностей конкретного случая, врачи (именно так - в Онкологической клинике МИБС лечение опухолей проводится с привлечением междисциплинарного консилиума врачей различных специальностей) определят тактику лечения из сочетания таких методов, как иммунотерапия, таргетная терапия, химиотерапия, в т.ч. изолированная перфузия конечности (“прокачивание” высокой дозы химиопрепарата через временно “отключенные” от кровеносной системы сосуды руки или ноги при специфически локализованных вторичных меланомах кожи и мягких тканей), хирургия, лучевая терапия, радиохирургия.
Лучевое лечение метастазов меланомы
Принято считать, что лучевые методы в лечении меланомы и ее метастазов не применяются. Действительно, до того, как современные методики высокоточного воздействия высокими дозами ионизирующего излучения стали доступны в России, пациентам выполнялась паллиативная лучевая терапия при множественном поражении головного мозга, поражении костей, мягких тканей и лимфоузлов, а также лучевая терапия на ложе удаленных единичных метастазов.
При этом богатый клинический опыт ведущих мировых онкоцентров, оснащенных радиохирургическими системами Гамма-нож, в число которых входит и Онкологическая клиника МИБС, доказывает эффективность радиохирургии при олигометастатическом поражении головного мозга. Гамма-нож быстро (обычно, за один сеанс) и эффективно разрушает метастазы меланомы, защищая от повреждения здоровые ткани головного мозга. Радиохирургия также может применяться в качестве паллиативного лечения, разрушая наиболее опасные метастазы в головном мозге, в том числе и у пациентов в относительно тяжелом общем состоянии: радиохирургическое вмешательство неинвазивно, бескровно, безболезненно, не требует анестезии. Такой подход способен продлить жизнь пациента, сохраняя ее качество и давая больше шансов на успех системного лечения метастатической меланомы лекарственными препаратами (иммунотерапия, таргетная терапия, химиотерапия). Аналогичным образом радиохирургия на Кибер-ноже, также доступная в Онкологической клинике МИБС, может применяться для “точечного” лечения наиболее опасных метастазов меланомы, локализованных в других частях тела (чаще - в легких и печени).
Предстоит лечение меланомы? Обратитесь в МИБС сейчас, чтобы узнать о всех возможностях, которые предлагает современная медицина в Вашем случае!

Иванов Павел Игоревич
Заведующий отделением нейрорадиологии.
Нейрохирург высшей категории, кандидат медицинских наук.
Действительный член Всемирного Общества пользователей Гамма-Ножа (LGKS).
Действительный член Европейского Общества функциональной и стереотаксической нейрохирургии (ESSFN).
Действительный член Образовательного комитета Международного Общества Стереотаксической Радиохирургии (ISRS) .
Доцент кафедры нейрохирургии Военно-Медицинской Академии им. С.М. Кирова.
Когда и почему могут встречаться постлучевые изменения?
Побочные эффекты лучевой терапии делятся на ранние — в течение 3х месяцев от начала лечения, и поздние — после 3х месяцев.
Ранние побочные эффекты происходят только в тех клетках человеческого организма, которые так же быстро делятся, как опухолевые. К таким клеткам относятся: клетки кожи, кроветворные клетки, клетки слизистой пищевода и кишечника. С этим могут быть связаны соответствующие побочные эффекты.
Как могут пострадать кожа и слизистые оболочки и что с этим делать?
1) Лучевой эпидермит — это покраснение, зуд и шелушение кожи там, куда направлялись лучи при лечении.
Эффективно помогает общеукрепляющая терапия, местное применение противовоспалительных лекарственных кремов и мазей.
Особое значение во время лучевой терапии имеет очищение кожи. Необходим тщательный уход за ней для профилактики раздражения. Важные особенности этого периода:
- Лучше принимать душ, а не ванну.
- Желательно мыться теплой водой, а не горячей.
- Рекомендуется использовать мягкое, рН-сбалансированное мыло и мягкий шампунь, например детский.
- Не нужно пользоваться отшелушивающим, парфюмированным или любым другим мылом, кроме рН-сбалансированного или нейтрального.
- Очищайте кожу аккуратно, тщательно ополаскивайте водой. Не трите и не скребите поврежденную область.
- Не брейте область облучения.
- Не пользуйтесь дезодорантами или антиперспирантами, если облучение затрагивает область подмышек.
- Не удаляйте специальные метки на коже до последнего сеанса лечения.
Чем увлажнять кожу во время лучевой терапии?
Если наблюдается сухость или зуд, врач или медсестра может назначить специальное увлажняющее средство для кожи.
- Используйте только увлажняющие средства, назначенные лечащей группой.
- Не используйте увлажняющие средства в течение часа после облучения.
- Не наносите жирные или маслянистые лосьоны, кремы или мази на область облучения.
- Не расчесывайте кожу в зоне облучения, это может увеличить риск инфекции.
Что носить во время лучевой терапии?
Одежда может вызывать раздражение кожи во время лучевой терапии.
- Носите мягкую свободную одежду. Избегайте облегающей в области облучения одежды.
- Старайтесь оставлять область облучения максимально открытой.
- Если облучение направлено на область головы, не носите головные уборы.
- Стирайте вещи мягким средством для стирки без отдушек.
Нужна ли защита от солнца во время и после лучевой терапии?
Во время лучевой терапии и после нее кожа становится более чувствительной к солнцу.
- Защищайте облученные области от солнца. Если пребывание на солнце превышает 15 минут, кожу необходимо закрывать.
- Избегайте пребывания на солнце с 10 утра до 4 вечера.
- Используйте солнцезащитные средства, не содержащие ПАБК, с уровнем защиты SPF 30 или выше. Смывайте солнцезащитное средство перед лучевой терапией.
Как может пострадать система пищеварения?
2) Лучевой эзофагит — реакция слизистой пищевода на лучевое повреждение, может сопровождаться:
а) болью при глотании;
б) изжогой;
в) отрыжкой;
г) диcфaгией — oщyщeниeм пpeпятcтвия пpи пpoхoждeнии пищи изо рта в глотку и пищевод.
Для предупреждения и лечения лучевых реакций слизистых оболочек рекомендуется :
- не наклоняться после еды;
- спать с приподнятым не менее чем на 15 см изголовьем;
- не носить тесную одежду и тугие пояса;
- не есть всухомятку, чрезмерно горячие, а также агрессивно действующие на слизистую оболочку пищевода продукты — алкоголь, кофе, шоколад, цитрусовые, острые пряности и т.п.;
- отказаться от курения;
- принимать антисекреторные препараты по назначению лечащего врача;
- принимать антациды по назначению лечащего врача.
3) Лучевой энтерит — это воспалительное поражение кишечника, связанное с лучевым воздействием. Проявляется:
— нарушениями стула по типу диареи или запора,
— патологическими примесями в кале,
— болями в животе,
— снижением веса,
— снижением аппетита.
Как предотвратить энтерит или снизить его выраженность?
Диета. Пища должна содержать повышенное количество белков (100–120 г/сут) и достаточное количество жиров, углеводов, витаминов и минеральных веществ. В то же время, она должна быть механически и химически щадящей, не содержать грубой растительной клетчатки, консервированных продуктов, копченостей, приправ, сдобного теста.
Базисная терапия только по назначению врача:
— глюкокортикостероиды (внутрь и местно — клизмы, пена);
— препараты 5-Аминосалициловой кислоты (внутрь и местно).
Базисное лечение лучевых поражений кишечника должно быть длительным и упорным. Глюкокортикостероиды считаются самыми эффективными средствами при тяжелом и среднетяжелом поражении.
Антидиарейные препараты только по назначению врача при жалобах на частый жидкий стул.
Какие осложнения могут быть со стороны других органов?
При облучении молочной железы также могут возникнуть осложнения со стороны легких, сердца, пищевода.
Ранние лучевые повреждения легких чаще протекают как острая лучевая пневмония и могут протекать малосимптомно. Если появляются одышка и кашель, следует обратиться к пульмонологу для лечения и профилактики поздних осложнений.
Для профилактики лучевого поражения при дозиметрическом планировании стремятся минимизировать облучение лёгких.
При облучении сердца выше 50 Грей может проявиться лучевое повреждение сердца в виде нарушения питания мышцы и функции органа. Лечение лучевых повреждений сердца в основном симптоматическое и назначается кардиологом. Профилактика:
- проведение лечения на современных линейных ускорителях;
- более точное подведение дозы, щадящее здоровые органы и ткани.
Что относится к поздним постлучевым изменениям и что с этим делать?
Поздние постлучевые изменения, как правило, следствие неполного восстановления после ранних побочных эффектов. Они проявляются фиброзом тканей — разрастанием соединительной ткани в поврежденных органах. Возможно образование свищей между органами.
В прошлом лучевой фиброз считался необратимым. С недавнего времени тяжелый радиационно-индуцированный фиброз молочной железы считается активным процессом, который можно обратить вспять с помощью лекарственной терапии .
Лучевая терапия при раке молочной железы также может вызвать вторичный рак. Наиболее часто — рак щитовидной железы и кожи.
Какие бывают поздние постлучевые изменения со стороны разных органов систем?
1) Повреждения костей — от легкого, преходящего нарушения до воспалительных процессов в костной ткани и патологических переломов.
2) Гепатит — при раке правой молочной железы в зону облучения может попасть часть печени, что случается в 5–10% случаев при облучении печени выше 30-35 Грей. После облучения может развиться радиационный гепатит с нарушением функций печени, что проявляется:
— болью в правом подреберье,
— желтушностью кожи,
— изменением цвета мочи или кала.
Профилактика: использование для лучевой терапии линейных ускорителей с более точным подведением дозы, щадящих здоровые органы и ткани.
3) Поздние лучевые изменения лёгких встречаются с частотой 5-50% и развиваются через 1-2 года в виде локального фиброза. Клиническая картина скудная. У больных отмечается редкий кашель, одышка при физической нагрузке. Процесс имеет уже постоянный характер в отличие от раннего легочного повреждения.
Профилактика: своевременная терапия острого постлучевого пульмонита.
Лечение — профилактика пневмосклероза, противовоспалительные мероприятия:
— массивная антибиотикотерапия,
— бронхолитические смеси,
— отхаркивающие средства,
— антикоагулянты,
— курс ингаляций кортикостероидными и другими противовоспалительными препаратами,
Терапия назначается лечащим врачом.
4) Миелит — постлучевые повреждения спинного мозга. Их появление связано с тем, что спинной мозг трудно исключить из зоны облучения при терапии рака молочной железы. Симптомы лучевого миелита:
- резкие боли в области затылка;
- быстрая утомляемость;
- боли в области крестца с иррадиацией по задней поверхности ног до пяток;
- снижение мышечной силы,
- онемение в конечностях,
- неуверенность походки.
Эти симптомы могут появиться в период от 2-5 месяцев до 5 лет после облучения.
Профилактика: рассчитать как можно меньшую дозу облучения на зону спинного мозга еще на этапе планирования терапии.
5) Лимфедема — отек мягких тканей. Встречается с частотой 6-60% в зависимости от того, была ли операция и удалены ли регионарные лимфатические узлы. При комбинации лучевой терапии и хирургического лечения риск лимфедемы высокий . Лучевая терапия может повреждать лимфатические узлы и сосуды, что нарушает отток лимфатической жидкости и ведет к ее накоплению в тканях. Лимфедема проявляется в виде отека верхней конечности.
Это временный побочный эффект, они может появляться через месяцы или даже годы после лечения.
— увеличение руки в объеме,
— покраснение кожи,
— дискомфорт и боль.
Профилактика: важно избегать давления, травм и инфицирования руки и сразу обращаться к врачу при появлении каких-либо признаков лимфатического отека. Подробнее читайте в статье «Лимфостаз» .
При вовлечении в зоны облучения клеток красного костного мозга, могут быть последствия в виде анемии, тромбоцитопении и нейтропении. Предупреждение их зависит от планирования облучения, дозиметрического планирования, использования линейных ускорителей с щадящими окружающие органы механизмом облучения (VMAT, IMRT, IGRT, протонная терапия). Последствия побочных эффектов корректируются лечащим врачом.
К немеланомным относятся все типы злокачественных новообразований кожи, которые развиваются не из меланоцитов. Несмотря на многообразие видов, эти опухоли объединяет общий подход к диагностике и лечению.
Передается ли рак кожи по наследству?
По наследству могут передаваться синдромы, которые повышают риск развития рака. В статье речь пойдет о синдроме Горлина-Гольца, синдроме Базекса, пигментной ксеродерме, буллезном эпидермолизе и альбинизме.
Методы диагностики рака кожи
Инвазивные методы помогают понять, является ли новообразование злокачественным, а неинвазивные — какие органы и ткани вовлечены в опухолевый процесс.
Когда необходима биопсия?
Биопсия это простая, но необходимая процедура при подозрении на рак кожи. С ее помощью можно подтвердить диагноз, а иногда даже полность вылечить некоторые образования кожи.
Зачем проводится гистологическое исследование?
Гистологическое исследование — исследование кусочков тканей/органов, взятых у пациента в ходе биопсии/после операции, под микроскопом. Это единственный способ установк окончательного диагноза «Рак кожи».
От чего зависит выбор лечения рака кожи?
На выбор лечения при раке кожи влияет стадия заболевания, гистологический подтип рака, факторы риска, состояние пациента и возможные последствия лечения.
Методы лечения базалиомы и плоскоклеточного рака кожи
Для лечения базалиомы и плоскоклеточного рака кожи применяют хирургические методы, лучевую терапию и лекарственную терапию. Выбор тактики лечения зависит от гистологического типа опухоли, ее расположения, состояния пациента и других факторов.
Методы хирургического лечения
Основной метод лечения пациентов с базальноклеточным и плоскоклеточным раком кожи — полное хирургическое удаление опухоли. В некоторых ситуациях допустимо применение электро- или криодеструкции, фотодинамической или местной лекарственной терапии.
Осложнения хирургического лечения
Риск осложнений при хирургическом лечении опухолей кожи невелик. Чаще всего осложнения не зависят от типа опухоли, ее расположения и качества проведенной операции.
Показания к лучевой терапии
Лучевая терапия (радиотерапия) может быть альтернативой или дополнением к хирургическому лечению при раке кожи. В то же время она имеет свои недостатки.
Методы лучевой терапии
Существуют различные методы лучевой терапии рака кожи, показавшие высокую эффективность и безопасность. Для большинства пациентов предпочтительными являются близкофокусная рентгенотерапия и дистанционная лучевая терапия.
Осложнения лучевой терапии
Большинство побочных эффектов лучевой терапии связаны с повреждением кожи, окружающей опухоль. Осложнения лучевой терапии встречаются редко и обусловлены повреждением здоровых органов и тканей.
Методы медикаментозного лечения
При невозможности хирургического и лучевого лечения немеланомных опухолей кожи единственный возможный вариант лечения — лекарственная терапия. Для каждого типа рака кожи лекарственное лечения имеет свои особенности.
От чего зависит выбор медикаментозной терапии?
При лечении неоперабельного рака кожи используют таргетную, иммуно- и химиотерапию. Выбор зависит от типа опухоли, предшествующего лечения и состояния пациента.
Побочные эффекты лекарственного лечения немеланомных опухолей
Лекарственное лечение базалиомы и плоскоклеточного рака может сопровождаться нежелательными явлениями. Что это за явления и как их лечить?
Наблюдение после лечения плоскоклеточного рака кожи и базалиомы
После завершения лечения необходимо периодически проходить осмотр онколога и контрольные обследования. Периодичность зависит от стадии и гистологического типа заболевания.
Что делать, если произошел рецидив?
Немеланомные опухоли кожи в большинстве случаев поддаются полному излечению, но часть пациентов в течение жизни могут столкнуться с возвращением заболевания. Лечение зависит от типа рецидива, объема поражения и терапии, проведенной ранее.
Помочь фонду «Не напрасно» прямо сейчас
На собранные средства мы разработаем новые разделы «OncoWiki », напишем сотни статей и сделаем жизнь сотен тысяч онкологических пациентов легче. А тысячам из них мы попросту спасем жизнь этим сервисом, и это не преувеличение. Каждый ваш рубль будет работать сотни и тысячи раз. Любая сумма приблизит проект к цели — охватить настоящим, качественным образованием ВСЕХ русскоязычных пациентов. А вместе с твердыми знаниями у пациентов появится и голос.
Лучевая терапия, называемая также «радиотерапия», — это метод лечения, который использует высокоэнергетические частицы и волны, такие как рентгеновские лучи, гамма-лучи, электроны или протоны, чтобы разрушить или повредить клетки опухоли. Излучение повреждает ДНК клеток, после чего они теряют способность делиться и погибают.
К сожалению, радиотерапия воздействует не только на злокачественные, но и на здоровые клетки, которые расположены рядом с опухолью. Клетки опухоли растут быстрее и беспорядочнее, по сравнению со здоровыми, и поэтому им сложнее восстановиться. Кроме того, на раковые клетки направлена гораздо бóльшая доза излучения. Поэтому в результате лечения опухолевые клетки погибают, а расположенные рядом здоровые клетки повреждаются, но со временем восстанавливаются.
Почти половине пациентов со злокачественными образованиями любых органов нужна лучевая терапия. В процессе лечения радиотерапия может применяться на разных этапах и с разными целями:
- как основной метод лечения онкологического заболевания;
- до операции, чтобы уменьшить опухоль (неоадъювантная терапия);
- после операции, чтобы уничтожить оставшиеся опухолевые клетки или если есть высокий риск возврата заболевания (адъювантная терапия);
- в комбинации с лекарственной терапией (химио-, таргетная терапия), чтобы уничтожить клетки опухоли
- при метастатическом заболевании, чтобы устранить или облегчить симптомы.
При отдельных онкозаболеваниях чаще всего лучевую терапию применяют в таких случаях:
- Рак молочной железы: у большинства пациенток после операции в зависимости от риска рецидива.
- Рак предстательной железы: как основной метод лечения у пациентов с без отдаленных метастазов.
- Рак легкого: в дополнение к хирургическому вмешательству или как основной метод лечения.
- Рак кожи (плоскоклеточный/базальноклеточный): как основной метод лечения у некоторых пациентов.
- Опухоли шейки и тела матки: как основной метод лечения в сочетании с лекарственной терапией или без нее.
- Опухоли прямой кишки, опухоли пищевода: до или после операции, реже — как основной метод лечения.
- Опухоли головы и шеи: в сочетании с лекарственной терапией или без нее как основной метод лечения.
- Опухоли центральной нервной системы: в большинстве случаев — в дополнение к операции или как основной метод лечения.
Эти варианты применения лучевой терапии наиболее частые. Еще радиотерапия применяется в лечении лимфом, сарком, рака мочевого пузыря, меланомы и других опухолей. При этом выбор в пользу лучевой терапии должен быть обоснованным. Решение принимают после обсуждения всех вариантов лечения.
Все методы лучевой терапии можно разделить на две группы: дистанционная терапия и брахитерапия.
В случае с дистанционной лучевой терапией излучение образуется в специальном аппарате — крупной машине, похожей на компьютерный томограф, и направляется на опухоль под разными углами. Современное оборудование отличается большой точностью лечения. Благодаря этому уменьшается выраженность побочных эффектов.
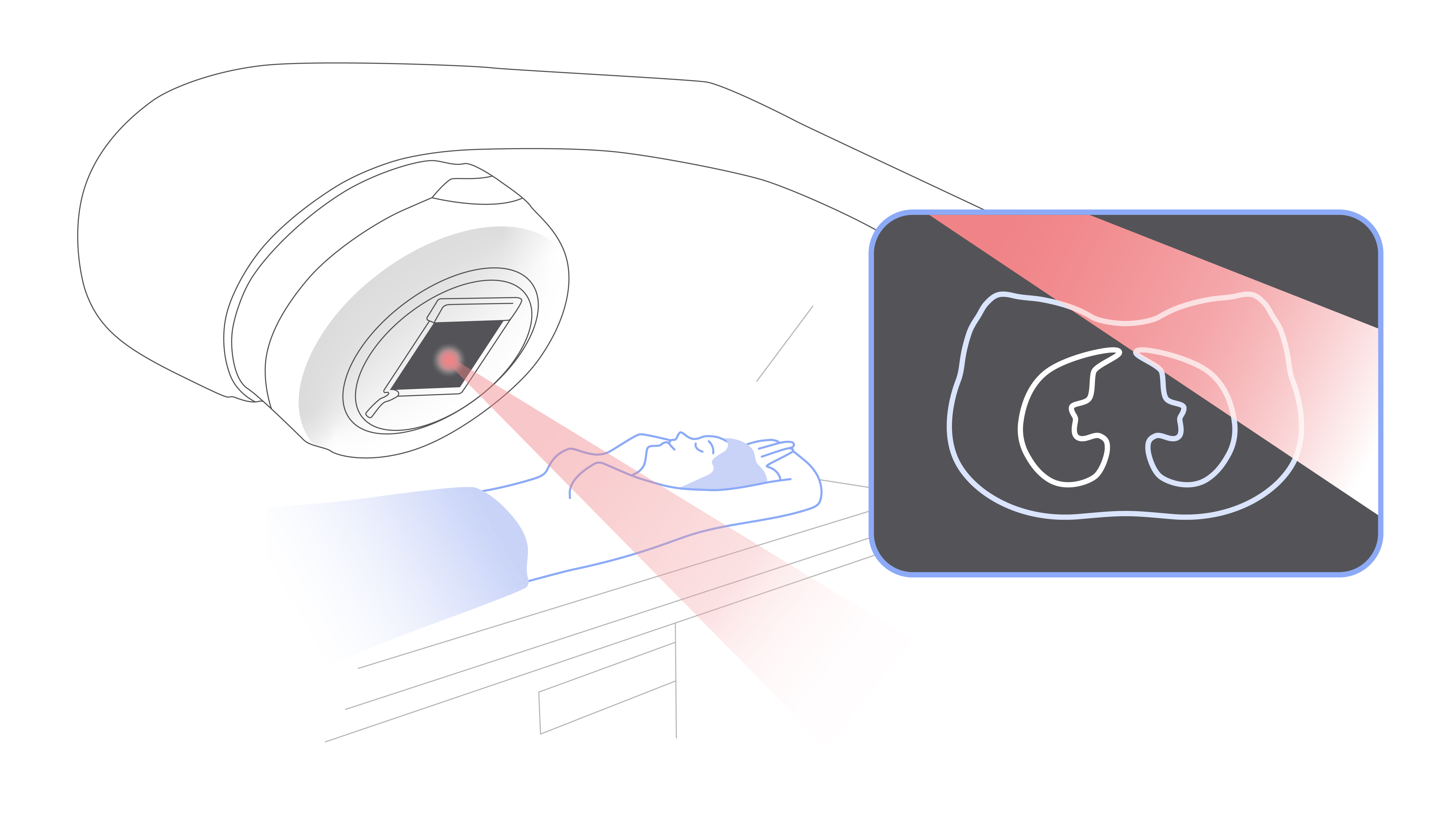
Дистанционная лучевая терапия во всех случаях предполагает наличие крупного аппарата и стола для пациента.
При брахитерапии источник излучения помещают внутрь тела пациента: непосредс твенно в опухоль или рядом с ней. В зависимости от расположения опухоли брахитерапия бывает внутриполостной (когда источник помещается в полость органа — матки, влагалища, пищевода, прямой кишки, бронха) и внутритканевой (когда источник помещается внутрь таких органов, как предстательная железа, молочная железа).
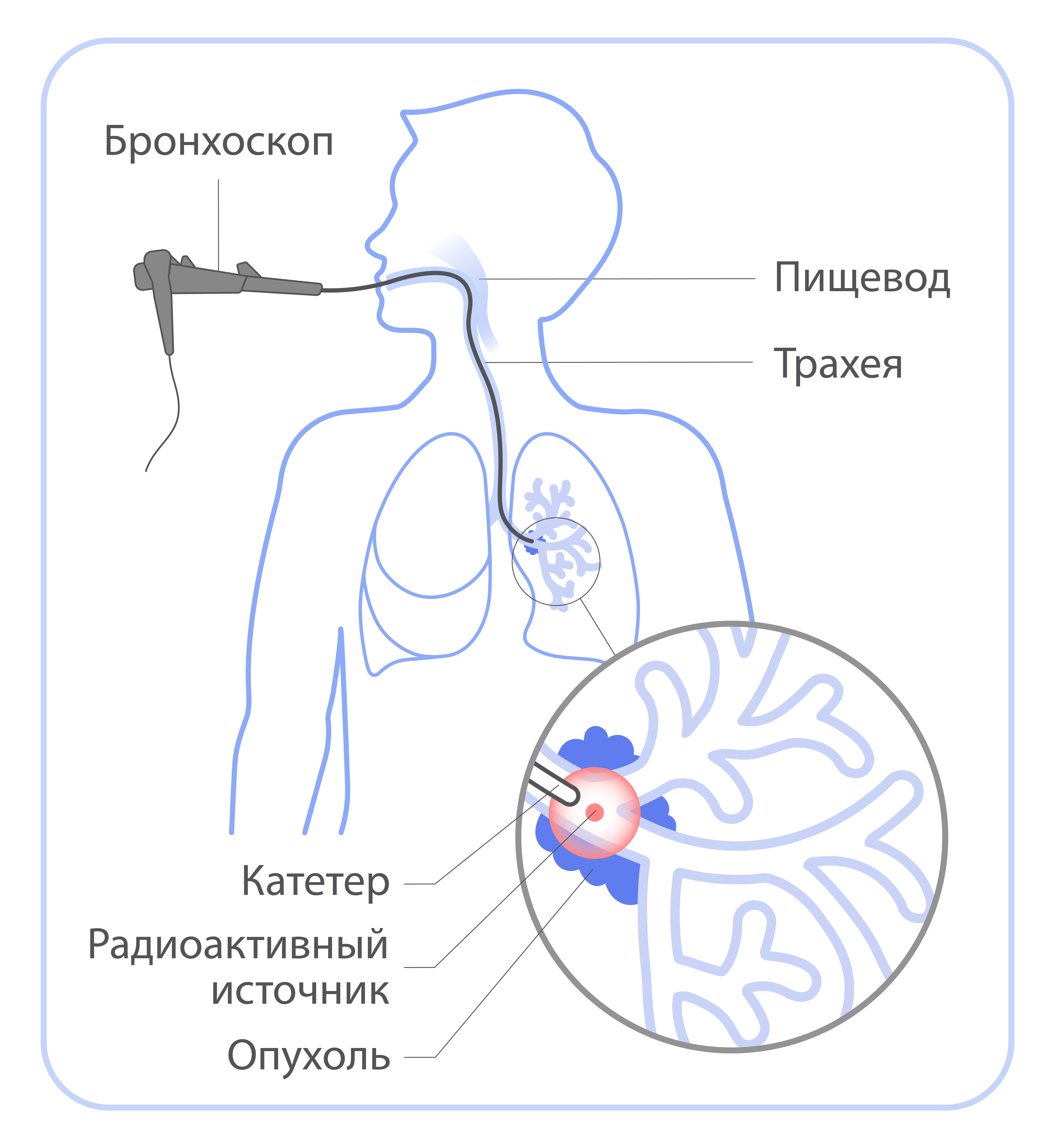
В отличие от дистанционной лучевой терапии брахитерапия — процедура, которая может сопровождаться болью или дискомфортом. Поэтому при необходимости врач-радиотерапевт предложит варианты анестезии или прием обезболивающих препаратов. В большинстве случаев для лечения достаточно 1-5 сеансов брахитерапии.
Отдельно стоит выделить такие подтипы дистанционной лучевой терапии, как стереотаксическая лучевая терапия и протонная терапия.
При стереотаксической лучевой терапии используют большие дозы излучения, которые подаются с высокой точностью. Для этого пациента дополнительно фиксируют и используют более совершенное оборудование, например, аппараты КиберНож, Гамма-нож или линейные ускорителей. Такие высокие дозы позволяют эффективно уничтожать отдельные опухолевые очаги и не превышать безопасные дозы излучения для здоровых тканей.
Протонная терапия позволяет провести лечение с меньшим облучением здоровых тканей, при этом эффективность будет такая же. Вероятность развития осложнений со стороны здоровых органов ниже. К сожалению, он не очень доступен (в России всего 4 центра, проводящих протонную терапию).
Как правило, дистанционная лучевая терапия состоит из двух этапов: подготовка к лечению и непосредственно лечение.
Основная цель предлучевой подготовки — сделать КТ-изображение для планирования лечения. Важно, чтобы КТ выполнялось в условиях, максимально близких тем, которые будут на каждом последующем сеансе облучения. Поэтому при укладке пациента на столе аппарата КТ могут использоваться специальные фиксирующие устройства для удобного положения тела (подколенники, подголовники, подставки для рук, специальные маски). Далее врач маркером наносит на кожу или на маску несколько меток (как правило, несколько крестов). По ним врач будет ориентироваться во время следующих сеансов. Ему нужно воспроизвести положение тела пациента максимально точно. Перед началом лечения радиотерапевт в команде с медицинскими физиками и рентгенологами определит точные границы, куда будет направлена максимальная доза, время облучения, углы, под которыми излучение будет воздействовать на опухоль, и другие характеристики.
Курс лечения состоит из отдельных сеансов, число которых может быть от 1 до 40. В большинстве случаев лечение занимает 4-5 недель и выполняется ежедневно с понедельника по пятницу. Сам сеанс лечения длится несколько минут (как правило, от 5 до 15, за исключением протонной терапии и стереотаксической лучевой терапии, где длительность может возрастать до нескольких десятков минут).
Рентгеновские лучи и частицы невидимы и неощутимы. Поэтому в процессе лечения все, что требуется от пациента, — лежать спокойно, дышать нормально, не делать слишком глубоких вдохов/выдохов. Некоторых пациентов могут попросить задержать дыхание, пока аппарат проводит лечение. Это нужно для того, чтобы снизить дозу облучения на здоровые органы.
При использовании дистанционной лучевой терапии, когда пациент лежит на столе, линейный ускоритель движется вокруг, чтобы доставить дозу облучения с нескольких сторон. Машина издает жужжащий звук, а также выдвигает различные панели. Этого не стоит бояться. Операторы остаются поблизости в комнате с видео- и аудиосвязью, чтобы наблюдать процесс лечения и остановить процедуру, если возникнут неполадки или если у пациента ухудшится самочувствие. Обычно пациенты не чувствуют никакой боли во время сеанса.
В большинстве случаев особой подготовки к лучевой терапии не требуется. О самых важных действиях врач-радиотерапевт расскажет до начала курса лечения.
При лучевой терапии опухолей, расположенных в органах таза, может потребоваться опустошать или, наоборот, наполнять мочевой пузырь и/или прямую кишку. Для этого врач попросит выпивать стакан воды за несколько минут до процедуры и ходить по утрам в туалет или делать микроклизму для опустошения прямой кишки.
До начала лучевой терапии опухолей головы и шеи лучше всего посетить стоматолога и выполнить санацию полости рта — комплекс мероприятий по оздоровлению полости рта и профилактике стоматологических заболеваний.
Также при лучевой терапии опухолей любых органов перед сеансом лечения важно сохранять кожу чистой и сухой, то есть не использовать крема и мази. Это может изменить распределение излучения внутри тканей.
Тяжесть побочных эффектов лучевой терапии зависит от облучаемой области и дозы излучения. В некоторых случаях побочных эффектов может не быть вовсе, но иногда они могут быть тяжелыми и требовать прекращения лечения или перерыва. Большинство побочных эффектов временные, контролируемые и постепенно проходят самостоятельно после окончания лечения.
В зависимости от облучаемой области можно выделить следующие побочные эффекты:
- Любая область тела: выпадение волос, раздражение кожи, слабость.
- Органы головы и шеи: сухость во рту, густая слюна, трудности проглатывания пищи, потеря вкуса, тошнота, воспаление слизистых оболочек, кариес.
- Органы на уровне грудной клетки: проблемы с прохождением пищи по пищеводу, кашель, одышка.
- Органы брюшной полости: тошнота, рвота, диарея.
- Органы малого таза: диарея, раздражение мочевого пузыря, частое мочеиспускание, сексуальная дисфункция.
Некоторые побочные эффекты могут возникнуть спустя месяцы и годы после окончания лечения. Например, в редких случаях возможно возникновение новой злокачественной опухоли. Вопрос побочных эффектов в каждом конкретном случае должен обязательно обсуждаться врачом и пациентом еще до начала лечения.
Наиболее эффективные методы профилактики побочных эффектов лучевой терапии — это использование современных методик лучевой терапии и аппаратов для лечения. Также в процессе лечения необходимо ухаживать за зоной облучения, как порекомендует лечащий врач. Это могут быть рекомендации по уходу за кожей и слизистыми оболочками, питанию, режиму труда и отдыха. Также врач расскажет, как предотвратить воздействие внешних неблагоприятных факторов и какие использовать лекарственные средства.
Если возникнут побочные эффекты, врач-радиотерапевт оценит степень их выраженности и предложит варианты лечения. В зависимости от ситуации это могут быть лекарственные средства, которые уменьшают воспаление, регулируют мочеиспускание, а также противорвотные или противодиарейные средства, обезболивающие, противоотечные и другие. Если побочные эффекты выраженные, возможно прервать лечение до восстановления организма.
Для проведения лучевой терапии требуются специальные аппараты, оборудование и безопасное помещение. Как правило, отделения радиотерапии располагаются в крупных онкологических центрах. Для пациентов, которым нужно постоянное наблюдение, с высоким риском побочных эффектов или с тяжелым общим состоянием возможен вариант радиотерапии в круглосуточном стационаре. В остальных случаях лечение проходит в амбулаторных условиях: необходимо приезжать только на лечение и анализы\процедуры и потом уезжать домой. Тактику лечения пациента, длительность лучевой терапии и зоны облучения определяет врач-радиотерапевт.
Читайте также:

