После какой операции остается шрам на шее
Обновлено: 27.04.2024
Шея - это самая подвижная часть позвоночника, состоящая из семи позвонков. Как и другие отделы позвоночника, шейный также страдает от разного рода травм и патологий, которые ограничивают подвижность шеи и доставляют массу дискомфорта. Хирургическое вмешательство в данной области назначают нечасто, но это не может служить поводом для занятий самолечением или отказом от посещения врача.
Какие симптомы указывают на проблемы в области шеи
Боли в шее могут указывать на разные факторы, начиная от образования грыжи или протрузии и заканчивая простыми судорогами мышц после сна в неправильной позе. Из-за обширной симптоматики и большого числа “полезных” рекомендаций, как лечить шею в домашних условиях, появляется халатное отношение пациента к здоровью шейных позвонков и последующие осложнения, с которыми он рано или поздно обращается к врачу из-за постоянных болей.
- в затылочной и височной части головы;
- в области шеи и отдают в кисть руки;
- между лопатками и под плечами.
При отсутствии лечения, боли становятся хроническими и переходят в острую стадию, вызывая онемение конечностей и частичный паралич. Большинство пациентов дотягивают именно до такой стадии, когда избежать операции невозможно.
Когда срочно нужно обращаться к врачу:
Если движение головы в определенном положении вызывает острую боль;
Если болевые ощущения или ограничения в подвижности головы возникли после травмы, то с большой долей вероятности в области шейных позвонков есть повреждения. Медицинская помощь в таком случае должна быть неотложной.
Разновидности операций на шее
Хирургическое вмешательство зачастую требуется, если:
- есть врожденная патология (сколиоз, наследственные аномалии в виде сращивания позвонков или клиновидных позвонков);
- наблюдаются воспалительные процессы в области шеи (артрит, инфекционные поражения мягких или костных тканей, острый ревматизм);
- обнаружены доброкачественные и злокачественные новообразования разной степени;
- случилась травма (перелом, ушиб, хлыстообразные повреждения шеи);
- имеются выраженные возрастные изменения в результате износа шейных позвонков (протрузии или грыжи, дислокация суставов межпозвоночных дисков шейного отдела, костные выросты и связочные нарушения).
Любое осложнение указанных патологий может привести к необходимости провести операцию.
Диагностика
Прежде, чем утверждать, что нужно хирургическое вмешательство, врач проводит осмотр пациента, знакомится с историей его болезни и дополнительно назначает:
- ультразвуковое исследование;
- электромиографию;
- магнитно-резонансную томографию.
Виды операций
Для лечения патологий шейного отдела есть три вида операций:
- нуклеопластика;
- эндопротезирование;
- спондилодез.
Одним из самых распространенных видов хирургического вмешательство в области шеи считается нуклеопластика. Операция предназначена для удаления протрузий и грыж. В ходе процедуры удаляется часть фиброзного образования из хрящевой ткани, которая нарастает вокруг ядра межпозвоночного диска и выступает наружу, вызывая боль. Операция позволяет избавиться от нароста и восстановить полную подвижность сегмента.
Эндопротезирование - это современный способ лечения травм и деформаций в области шеи. Операцию назначают в том случае, если возникла необходимость замены поврежденного участка или целого позвонка. Для этого используют протезы и фиксирующие конструкции.
Спондилодез - операция по расширению пространства межпозвонковых дисков, которое уменьшается в виду дегенеративных и возрастных изменений. Боль вызывает трение костной ткани соседних позвонков друг о друга.
Последствия и реабилитация после операции на шее
Практически любой вид хирургического вмешательства в области шеи избавляет пациента от болей и значительных физических ограничений. На реабилитацию уходит от пары дней до нескольких недель, в зависимости от сложности операции. Врач-реабилитолог в клинике назначает курс восстановления, в который входит курс ЛФК для улучшения подвижности шейных позвонков. Любой вид операции практически не имеет негативных последствий, если пациент своевременно обращается в клинику и следует всем наставлениям опытного врача-хирурга и реабилитолога.
НОУ ВППО «Тираспольский межрегиональный университет», Республика Молдова
Особенности наложения швов на раны челюстно-лицевой области
Журнал: Российская стоматология. 2016;9(2): 62‑63
Круду М.А. Особенности наложения швов на раны челюстно-лицевой области. Российская стоматология. 2016;9(2):62‑63.
Krudu MA. . Russian Stomatology. 2016;9(2):62‑63. (In Russ.).
НОУ ВППО «Тираспольский межрегиональный университет», Республика Молдова
НОУ ВППО «Тираспольский межрегиональный университет», Республика Молдова
Повреждения мягких тканей челюстно-лицевой области встречаются в 70% от всей челюстно-лицевой травмы. Дефекты и деформации лица вызывают не только анатомические и функциональные нарушения, но служат причиной тяжелых психологических переживаний больных. Степень этих нарушений и характер восстановительных операций зависят от величины и локализации дефекта, а также от сочетания повреждений отдельных органов и тканей лица. В зависимости от тяжести повреждения, разрушений скелета челюстно-лицевой области, мягких тканей, мышц, нервов, а также органов полости рта, пострадавшие нуждаются в различных способах реконструктивных вмешательств: от небольших местнопластических операций до длительной и многоэтапной пластики филатовскими стеблями, пересадки костных трансплантатов, жировой ткани и алло- и ксеноимплантатов. Хирургическую обработку ран челюстно-лицевой области необходимо проводить в ранние сроки. Это позволяет уменьшить опасность развития раневой инфекции и добиться первичного заживления раны. В зависимости от временного фактора первичная хирургическая обработка ран подразделяется на раннюю (в первые 24 ч), отсроченную (спустя 24—48 ч) и позднюю (после 48 ч).
Согласно общим принципам наложения швов на раны челюстно-лицевой области, при хирургических вмешательствах предусматривается: бережное отношение к краям сшиваемой раны; прецизионность — точное сопоставление и адаптация одноименных слоев сшиваемой раны; легкое приподнятие краев раны для предупреждения втяжения рубца в процессе контракции; обеспечение пролонгированной дермальной опоры для предупреждения расширения рубца в послеоперационном периоде; исключение странгуляционных меток от пролежней лигатуры на поверхности кожи.
Различают первичный шов, наложенный сразу после операции или ранения, и вторичный шов, применяемый на гранулирующую рану. Отсроченный первичный шов накладывают спустя 2—4 суток после первичной хирургической обработки раны. На кожу накладывают съемные швы, которые удаляют после заживления раны. Хирургические швы из нерассасывающегося материала, наложенные на глубокие ткани, обычно оставляют в тканях навсегда.
Узловые швы. Техника их выполнения требует проведения иглы двухмоментно. Прошивать оба края раны одним движением можно только в случае закрытия поверхностных ран малых размеров. Сближать края раны необходимо атравматично, помогая пальцами. Если хирург для этой цели использует глазной хирургический пинцет, им нельзя надавливать на края раны, а можно лишь изнутри приподнять края, или же снаружи поддерживать кожу напротив вкола иглы.
Требования, предъявляемые к завязыванию узла: 1) каждый хирург должен владеть основными способами завязывания узлов; концы лигатур в руках хирурга должны быть постоянно и равномерно натянуты. Если преобладает сила тяги за один конец, получится скользящий узел, который может развязаться; 2) узел следует затягивать до прекращения скольжения нити, но не сильно, так как нить может разорваться или наступит ишемия сшиваемых тканей, что приведет к избыточному рубцеванию и снижению эстетического эффекта; 3) при использовании дактильного метода завязывания узла необходимо помогать его движению указательным пальцем; 4) нельзя оставлять узел на линии сопоставленных тканей, так как он может спровоцировать дополнительную ишемию; 5) концы лигатур на коже должны быть не более 0,5—0,8 см. При более коротких их концах узел может развязаться, при более длинных — могут травмироваться окружающие ткани; 6) количество узлов определяется манипулятивными свойствами шовного материала. Как правило, фирмы изготовители шовного материала указывают оптимальное количество узлов.
Хирургический узел — это комбинация из двух горизонтальных перекрещиваний нитей и одного перекрещивания по вертикали. Наложение этого узла необходимо при некотором натяжении тканей, так как первый перекрест предупреждает ослабление узла до второго перекреста.
Простой (женский) узел — это комбинация из двух перекрещиваний нитей по вертикали.
Морской узел — достаточно надежный, однако в случае нарастающей отечности ткани он затягивается, что приводит к сильной ишемии соединенных краев раны.
Наложение узловых швов на слизистую оболочку полости рта отличается некоторыми особенностями. Так, если хирург соединяет слизисто-надкостничные лоскуты, то он сталкивается с проблемой натяжения тканей, даже при мобилизации надкостницы. В этом случае оптимальным является наложение П-образных швов, а в зонах без натяжения — узловых.
При зашивании таких участков как язык, небо, щечная область по линии смыкания зубов, оставление узла и концов лигатур, направленных в полость рта, может привести к травматизации линии шва (прикусывание зубами) и соприкасающихся поверхностей (язык—небо). Поэтому в таких случаях необходимо отдать предпочтение использованию рассасывающегося шовного материала и вворачивающемуся шву.
При наложении обычного узлового шва на глубокую рану возможно оставление остаточной полости. В этой полости может скапливаться раневое отделяемое и приводить к нагноению раны. При затруднении в сопоставлении краев кожной раны может использоваться горизонтальный матрацный П-образный шов. Этого можно избежать также зашиванием раны в несколько этажей. Поэтажное ушивание раны возможно как при узловом, так и при непрерывном шве.
Кроме поэтажного зашивания раны применяется вертикальный матрацный шов (по Донатти). При этом первый вкол производится на расстоянии 2 см и более от края раны, игла проводится как можно глубже для захвата дна раны. Выкол на противоположной стороне раны делается на таком же расстоянии. При проведении иглы в обратном направлении вкол и выкол производятся на расстоянии 0,5 см от краев раны так, чтобы нить прошла в слое собственно кожи. Завязывать нити при зашивании глубокой раны следует после наложения всех швов — это облегчает манипуляции в глубине раны. Применение шва Донатти позволяет сопоставлять края раны даже при их большом диастазе.
Хирургические швы, наложенные на рану, но не стянутые, называются провизорными. Их завязывают на 3—4-й день после наложения при отсутствии в ране воспалительного процесса.
Экстрадермальный непрерывный шов используется не для сближения краев раны, а лишь для их точного сопоставления при отсутствии натяжения на линии шва. При наложении такого шва используют тонкий шовный материал и средства оптического увеличения.
Двухрядный непрерывный шов. Глубокие раны могут быть закрыты двухрядными непрерывными швами. Первый ряд проходит в подкожной жировой клетчатке, приблизительно посередине плоскости разреза жировой ткани, второй ряд— в собственно коже (дерме). Концы нитей каждого ряда швов выводят на поверхность кожи и связывают друг с другом.
Игла при наложении внутрикожного шва вкалывается в область середины дермы. В дальнейшем для получения оптимального послеоперационного рубца выдерживают радиус стежка до 2 мм. Выкалывать иглу всегда нужно напротив места ее вкола так, чтобы при затягивании нити эти две точки совпадали. Закончив шов, два конца нити захватывают инструментом и натягивают до достижения полного сближения краев раны. Необходимым условием при наложении такого шва является исключение натяжения краев. Интрадермальный шов не рекомендуется налагать на раны менее 2 см длиной.
Сшивание ран при помощи скобок. Скобки состоят из металлических пластинок шириной в несколько миллиметров и длиной в 1 см и несколько больше. Концы скобок согнуты в виде колец и снабжены с внутренней стороны острием, которое проникает при накладывании в ткани и предупреждает соскальзывание скобок.
Техника наложения скобок. Для наложения скобок захватывают специальным пинцетом края раны, сводят их, хорошенько приладив друг к другу, затем одним пинцетом удерживают края раны, а другим, находящимся в правой руке, захватывают скобку, накладывают на линию шва и с силой сжимают концы пинцета, вследствие чего скобка сгибается и обхватывает края раны. Скобки накладывают на расстоянии 0,5—1 см и больше друг от друга.
Снятие скобок. Скобки снимают, так же как и швы, через 6—8 дней при помощи специального пинцета или крючков. При отсутствии специальных пинцетов скобки можно снять хирургическими пинцетами, беря ими за кольца скобок.
Важнейшую роль в процессе заживления раны играет отсутствие значительного натяжения на линии швов. Пренебрежение данного принципа приводит к нарушению кровообращения в краях и стенках раны, вызывает их некроз, что является предпосылкой к нагноению раны. Грубая и травматичная техника операции, обширная отслойка краев раны для уменьшения натяжения линии швов, также вызывает образования краевого некроза. Все это в значительной мере зависит от подготовки хирурга и от наличия необходимого оснащения. Сохранение достаточного кровообращения в тканях, образующих стенки раны, обеспечивает первичное заживление раны с формированием тонкого нежного рубца.
Удержание всех слоев раны в положении плотного соприкосновения в период формирования прочного рубца, во многом завит от правильности выбора шовного материала. Оптимальный рубец достигается использованием специальных разновидностей швов, накладываемых шовным материалом, биодеградация которого происходит в поздние сроки.
Клиника изучения и лечения боли ФГБНУ «Российский научный центр хирургии им. акад. Б.В. Петровского», Москва, Россия
Формирование хронической послеоперационной боли в отсроченном периоде (клиническое наблюдение)
Клиника изучения и лечения боли ФГБНУ «Российский научный центр хирургии им. акад. Б.В. Петровского», Москва, Россия
Широкое внедрение мультимодального подхода в периоперационном периоде позволяет достаточно эффективно контролировать боль в раннем периоде после перенесенного хирургического вмешательства. Но иногда возникают ситуации, когда при отсутствие боли в раннем послеоперационном периоде, формируется хроническая послеоперационная боль спустя 2—6 месяцев после хирургического вмешательства. Подобные клинические наблюдения, как например случай пациентки К., у которой спустя 5 мес после торакоскопического удаления гамартомы средней доли правого легкого, развилась интенсивная невропатическая боль, успешное лечение которой было возможным только при комплексном диагностическом и лечебном подходе с использованием адекватных инструментов диагностики и лечения.
Клиника изучения и лечения боли ФГБНУ «Российский научный центр хирургии им. акад. Б.В. Петровского», Москва, Россия
Дата принятия в печать:
Классификация хронической боли впервые была опубликована Международной ассоциацией по изучению боли (IASP) в 1986 г. В последующем претерпела несколько изменений в 1994 г. (второе издание) и в 2011—2012 гг. [1]. Согласно последнему определению IASP, хроническая послеоперационная боль — это боль, которая наблюдается как минимум через 3 месяца после операции, которая отсутствовала до хирургического вмешательства или имела другие характеристики, локализованная в месте операции при исключении других причин этой боли [2, 3].
Предполагается, что возникновению хронического послеоперационного болевого синдрома после торакотомических вмешательств, способствуют повреждение во время операции межреберных мышц [4], нервов [5], травма ребер [5], применение неоптимальных способов сопоставления ребер [6], наличие дренажей в плевральной полости [7], вывихи реберно-позвоночных суставов [8]. Известно, что на выраженность, частоту и длительность хронических болевых синдромов могут также влиять социодемографические, генетические факторы, индивидуальная болевая чувствительность, психоэмоциональный статус, а также качество обезболивания в послеоперационном периоде [9].
Накопление большого опыта «открытой» торакальной хирургии, появление новых инструментов и аппаратов для разъединения тканей позволило расширить показания к торакоскопическим операциям, а применение сверхтонких инструментов 3 и 5 мм и тончайшей гибкой оптики позволяет существенно снизить травматичность вмешательства, риск кровопотери и минимизировать повреждение межреберных нервов, вследствие чего торакоскопии сопровождаются меньшей интенсивностью боли и потребностью в анальгетиках у пациентов в раннем послеоперационном периоде при сравнении как с мышечносберегающей, так и со стандартной торакотомией [10]. Однако нет различий в частоте формирования хронической боли в послеоперационном периоде у пациентов после открытых торакотомических и торакоскопических вмешательств [8, 10—12].
Хронический постторакотомический болевой синдром — осложнение, возникающее у большинства пациентов, перенесших торакотомию (до 80%). Частота возникновения постторакотомического болевого синдрома (ПТБС) неуклонно возрастает, поскольку он развивается не только после торакотомии, но и у пациентов, перенесших торакоскопические вмешательства, при которых не производят стандартную торакотомию, а площадь межреберных отверстий для установки навигационных систем минимальна [13].
Несмотря на то, что пациенты часто описывают свою боль как слабую и умеренную, они отмечают значимое снижение качества жизни, трудовой и социальной активности.
В августе 2019 г. в Клинику изучения и лечения боли обратилась пациентка К., 52 лет, с жалобами на «жгучие» боли в правой половине грудной клетки, интенсивность которых по визуальной аналоговой шкале (ВАШ) составляла 54 мм. Болевой синдром носил практически постоянный характер и в значительной степени ограничивал ее повседневную активность, отмечалось нарушение сна в течение последних двух месяцев (частые пробуждения, чувство разбитости в утренние часы после сна). Из анамнеза известно, что в марте 2019 г. пациентка перенесла торакоскопическое удаление гамартомы средней доли правого легкого. В раннем послеоперационном периоде болевой синдром был умеренной интенсивности (около 45 мм по ВАШ), провоцировался двигательной активностью. Через две недели после операции боль регрессировала полностью. Около 3 мес назад (спустя 2 мес после перенесенного хирургического вмешательства) женщину стали беспокоить неприятные ощущения «горящего», «жгущего», «пекущего» характера в области послеоперационного рубца, практически постоянного характера, с некоторым усилением интенсивности в ночное время до 60 мм по ВАШ. Прием анальгетиков (простых и комбинированных) не уменьшал выраженность описанных жалоб. В этой связи в июне 2019 г. пациентка обратилась за консультацией к торакальному хирургу. С диагностической целью была проведена мультиспиральная компьютерная томография (МСКТ) органов грудной клетки с контрастным усилением, которая не выявила очаговых изменений; выполнены общеклинический и биохимический анализы крови, показатели которых были в пределах референсных значений; осмотрена кардиологом, эндокринологом, гастроэнтерологом — сопутствующей патологии со стороны сердечно-сосудистой, эндокринной систем и желудочно-кишечного тракта не выявлено. Пациентка продолжала наблюдаться терапевтом по месту жительства, получала нестероидные противовоспалительные препараты (нимесулид по 100 мг 2 раза в сутки в течение 7 дней) с кратковременным эффектом, проводила аппликации местноанестезирующих лекарственных средств (пластырь с 5% лидокаином), был проведен курс внутримышечных инъекций комплекс витаминов группы В (мильгамма 2 мл в/м 5 дней), назначен карбамазепин в дозе 400 мг в сутки на длительный прием. Пациентка принимала противоэпилептический препарат около месяца. На фоне терапии отметила снижение интенсивности боли (до 40—50 мм по ВАШ), но стала предъявлять жалобы на ощущение вялости, сонливости, что ограничивало активность в повседневной жизни, в связи с чем самостоятельно прекратила прием препарата. Болевой синдром сохранялся, в дальнейшем с целью коррекции терапии пациентка была направлена на консультацию в Клинику изучения и лечения боли.
На момент обращения в Клинику (22.08.19) больная предъявляла жалобы на сохраняющиеся «жгучие» боли постоянного характера в правой половине грудной клетки интенсивностью 60—70 мм по ВАШ, которые не усиливаются при дыхании, кашле, чихании и физических нагрузках. Пациентка описывает свои ощущения терминами «горит», «печет», «жжет», усиливающиеся в покое и во время ночного сна, значимо нарушая его качество. Кроме того, женщина жаловалась на чувство тревоги, страха в связи с «физическим неблагополучием», безысходности в сложившейся ситуации. При опросе данных за отягощенную наследственность не выявлено, пациентка имеет среднее образование, не работает, разведена, имеет двоих совершеннолетних детей, живет в частном доме.
Объективные данные при осмотре: повышенного питания (рост 162 см, вес 75 кг, индекс массы тела — 28,58 кг/м 2 ), кожные покровы и видимые слизистые обычной окраски, без патологических высыпаний, в области V—VI межреберных промежутков справа по переднеподмышечной и срединноключичной линиям имеются послеоперационные рубцы диаметром 15 мм в местах установки портов троакаров, болезненные при пальпации, имеется гипестезия в зоне рубцовых изменений и в радиусе 1—1,5 см, механическая аллодиния в этой зоне, тип дыхания смешанный, дыхательные движения грудной клетки симметричны, ритмичны, живот мягкий, безболезненный, расстройств мочеиспускания и дефекации не отмечает, ограничений двигательной активности нет, движения в суставах в полном объеме, со стороны черепных нервов без патологии, сухожильные рефлексы живые симметричные, патологических стопных знаков нет. При оценке когнитивного статуса с помощью Монреальской шкалы оценки когнитивных функций (MoCA) 28 баллов, что соответствует норме.
Для определения вида боли использовался опросник DN4: наличие сенсорных симптомов и выявленное сочетание гипестезии и аллодинии в зоне рубцовых изменений составило 6 баллов, что характеризует данную боль как невропатическую [14]. Для невропатической боли характерны эмоциональные и аффективные расстройства в виде тревоги и депрессии [15], для выявления которых у данной пациентки использовалась Госпитальная Шкала Тревоги и Депрессии (HADS). По шкале тревоги больная набрала 11 баллов, значит имеет место клинически выраженная тревога. По шкале депрессии — 9 баллов, что говорит о субклинически выраженной депрессии.
С учетом характера жалоб анамнестических данных, результатов инструментальных исследований, общего осмотра пациентки, неврологического и психоэмоционального статуса диагностирован хронический послеоперационный болевой синдром ассоциированный с тревожно-депрессивным расстройством.
Международные доказательные рекомендации по лечению невропатической боли в качестве терапии первой линии приводят 3 класса препаратов: трициклические антидепрессанты (ТЦА), селективные ингибиторы обратного захвата норадреналина и серотонина (СИОЗНС), α2-δ-лиганды кальциевых каналов (прегабалин, габапентин) и лидокаин местно (пластырь с 5% лидокаином) [15, 16]. Учитывая невропатический характер боли в сочетании с клинически выраженной тревогой, субклинически выраженной депрессией, препаратом нашего выбора стал дулоксетин — антидепрессант ингибирущий обратный захват серотонина и норадреналина, в результате чего повышается серотонинергическая и норадренергическая нейротрансмиссия в центральной нервной системе и обладает центральным механизмом подавления болевого синдрома, что в первую очередь проявляется повышением порога болевой чувствительности при болевом синдроме невропатической этиологии.
Дулоксетин был назначен в дозе 60 мг в сутки ежедневно на 3 мес, с рекомендацией динамического контроля выраженности болевых ощущений, повторного осмотра пациентки через 1 мес для оценки эффективности и коррекции проводимого лечения. Повторный осмотр был проведен 25.09.19 Пациентка отметила значительное улучшение самочувствия, нормализовался сон, интенсивность боли по ВАШ на момент осмотра 48 мм, сохранился ее невропатический характер (по шкале DN4 — 6 баллов), уровень тревоги снизился до субклинически выраженного (9 баллов), симптомы депрессии сохраняются (9 баллов).
Полученные результаты (снижение интенсивности боли с 60 до 48 мм по ВАШ, улучшение сна, снижение уровня тревоги) свидетельствуют об эффективности назначенной терапии. Учитывая данные других исследований [17—19] по эффективности дулоксетина при хронической нейропатической боли, было рекомендовано продолжить проводимое лечение еще в течение 3 мес.
На приеме 29.12.19 (через 4 мес от начала терапии) больная отметила регресс боли в дневное время суток, ночью боль беспокоит не постоянно, интенсивность ее 30—40 мм по ВАШ, характер боли сохранил невропатический компонент (по шкале DN4 — 4 балла), выраженность тревоги (9 баллов) и депрессии (9 баллов) соответствовали субклиническому уровню (см. рисунок).

Динамика показателей.
Динамический контроль психоэмоционального статуса пациентки, интенсивности боли ее беспокоящей на фоне приема дулоксетина показал эффективность данной монотерапии. Рекомендовано продолжить прием дулоксетина в дозе 60 мг в сутки в течение 2 мес (продолжительность общего курса — до 6 мес) с последующим контролем интенсивности болевого синдрома, психоэмоционального статуса больной для решения вопроса о постепенной отмене препарата.
Заключение
Хронический ПТБС может формироваться не только, как продолжение острой боли в послеоперационном периоде, но и развиваться после периода полного благополучия. Представленный клинический случай демонстрирует развитие подобного сценария, а также необходимость междисциплинарного подхода в диагностике и лечении.

Щитовидная железа — это небольшой, но очень важный для человека орган: он вырабатывает два тиреоидных гормона: тироксин (Т4) и трийодтиронин (Т3).
Они, в свою очередь, регулируют метаболизм, частоту дыхания и сокращений сердца, потребление клетками кислорода, процессы регенерации, работу иммунной и центральной нервной систем.
Однако заболевания щитовидной железы (а следовательно, патологии выработки данных гормонов) — очень распространенная проблема. По статистике Всемирной организации здравоохранения, патологии щитовидки находятся на втором месте по количеству случаев после сахарного диабета.
Часто они лечатся медикаментозно, однако при тяжелом течении заболевания требуется хирургическое вмешательство.
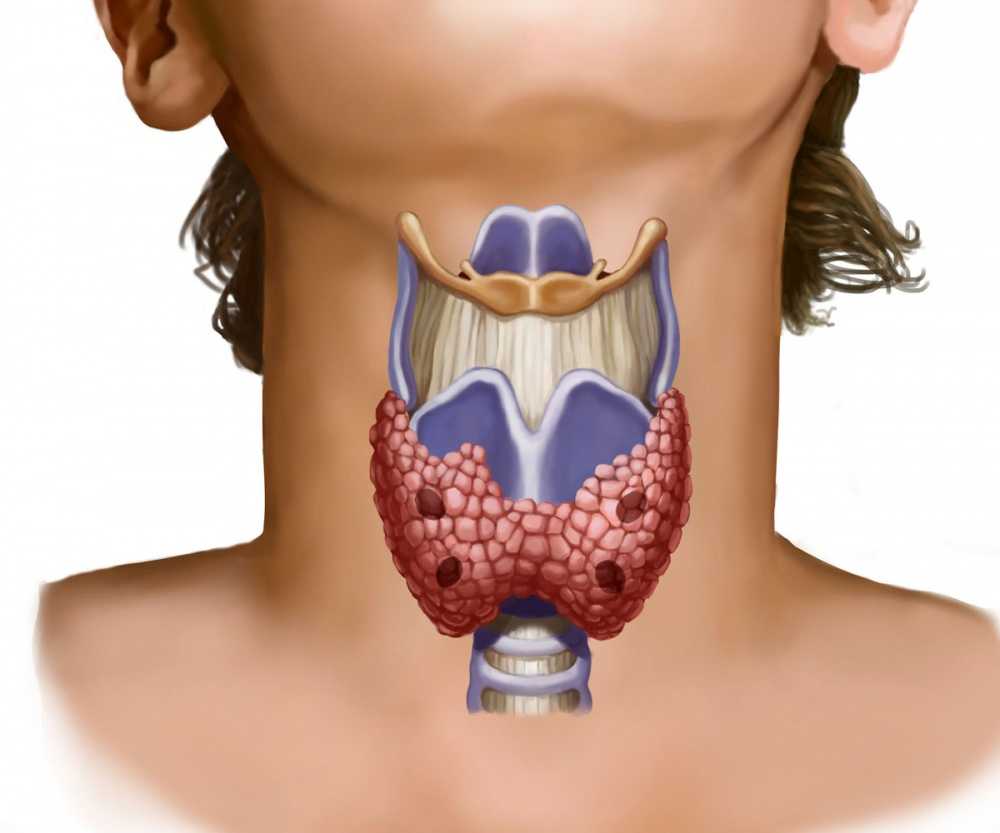
Орган уникален тем, что, в отличие от остальных частей тела, при удалении фрагмента щитовидной железы она функционирует как целая. По этой причине врачи стараются сохранить хотя бы небольшую долю щитовидки, чтобы пациент впоследствии вернулся к привычному образу жизни (в случае полного удаления придется проходить специальную гормональную терапию).
Но, независимо от масштабов операции, после нее всегда остается заметный след. Шея — один из самых открытых участков тела, а во многих культурах еще и показатель красоты и статуса женщины. Хирургическое вмешательство, безусловно, поправит здоровье, но оставит неприятный след.
Как свести рубец после операции на щитовидной железе, если большинство противорубцовых препаратов, особенно содержащих гормоны, противопоказано? Отвечает практикующий врач Светлана Огородникова.
Последствия после удаления щитовидной железы
В зависимости от размера органа, после операции остается шрам длиной от 3 до 7 см в области яремной ямки. Также могут возникнуть осложнения:
- Болевой синдром при движении головой
- Повышенная эмоциональность и нервная возбудимость, общее подавленное состояние
- Слабость и головокружение
- Учащенное сердцебиение
- Тремор рук
- Скачки веса в «+» или в «-»
- Судороги
- Ухудшение качества кожи и волос
При стабилизации выработки тироксина (после медикаментозной терапии) данные симптомы проходят.
При неосторожном обращении с раной могут возникнуть и другие осложнения:
- изменение либо потеря голоса;
- резкое снижение уровня кальция в организме;
- кровотечение;
- инфицирование;
- формирование грубого келоида.
Профилактика появления шрамов
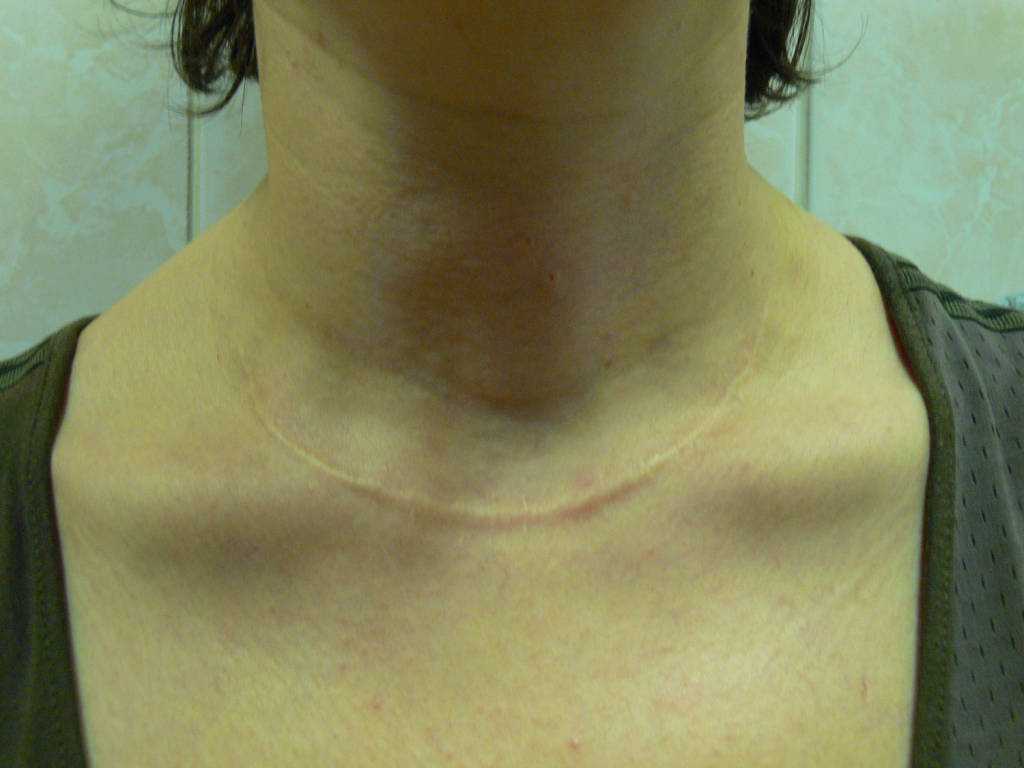
Келоидный рубец после удаления щитовидной железы не всегда удается спрятать под одеждой, к тому же этот вид шрамов при отсутствии лечения склонен разрастаться со временем и поражать соседнюю здоровую кожу.
Но сделать так, чтобы рубца не оказалось вовсе, тоже не получится. Однако, при успешной операции и правильном уходе в реабилитационный период, шрам представляет собой тонкую белую полоску, которая через полгода-год становится почти незаметной.
Чтобы рубец после удаления щитовидной железы не превратился в келоидный, необходимо:
- держать прооперированное место в чистоте;
- обрабатывать шрам стерильным раствором;
- не трогать его руками, избегать механических повреждений (например, натирание воротником или украшениями);
- носить одежду из натуральных тканей, не использовать синтетику и шерсть;
- не употреблять в пищу острых, жирных и соленых блюд;
- отказаться от курения и алкоголя;
- на время заживления раны ограничить физические нагрузки;
- не посещать бассейн, баню, сауну, солярий, фитнес;
- избегать открытых солнечных лучей.
Развитие келоида можно предотвратить, если вовремя начать применять противорубцовые средства. Чтобы определить этот тип шрама, следует обратить внимание на характерные признаки: зуд, локальное жжение, ярко-красный или фиолетовый цвет, активный рост рубцовой ткани с выходом за пределы изначальной раны. Иногда наблюдается местное повышение температуры.
Увеличение размера келоида наступает на 10–12 неделе после операции, но рекомендуется не дожидаться этого момента и при первых симптомах показаться специалисту.

Как убрать рубцы
Избавиться от шрама после операции на шее можно разными способами. Каждый имеет свои преимущества и недостатки и, конечно, подходит не всем. Разберем самые распространенные.
Косметологические методы

Среди косметологических процедур наиболее эффективны: лазерная шлифовка, микронидлинг, различные пилинги, дермабразия, криотерапия и мезотерапия.
Лазерная шлифовка — разрушение рубцовых клеток с помощью лазера. Процедура довольно болезненная, однако позволяет убрать до 70% келоидной ткани за один сеанс. Возможны рецидивы, поэтому специалисты рекомендуют сочетать лазерную шлифовку с аппликациями противорубцовым гелем и силиконовыми пластинами.
Из недостатков — помимо дискомфорта, процедура противопоказана детям, а также в случае обезвоженной кожи и во время беременности.
Криометодика предполагает применение жидкого азота. Это сильное обморожение локальных участков рубцовой ткани, благодаря которому ее клетки отмирают. Для достижения видимого эффекта понадобится от одного до трех сеансов.
Иногда криометодику совмещают с курсом инъекций глюкокортикостероидами. Это эффективный метод коррекции келоидных рубцов при помощи инъекций гормонов. Дает положительный, но временный результат.
Пилинги удаляют роговой слой эпидермиса, тем самым выравнивая рельеф кожи. Это контролируемый ожог, благодаря которому обновляются клетки. Эффективны в комплексной терапии. Возможны аллергические реакции, требуется период реабилитации.
Микронидлинг — стимуляция клеток за счет травматизации: происходит синтез свежего коллагена, эластина, гиалуроновой кислоты. Также при помощи микронидлинга можно доставить косметические средства в глубокие слои кожи, это происходит благодаря множественным проколам.
Мезотерапия — инъекции витаминных и противорубцовых средств непосредственно в шрам. Чаще всего используют гиалуронидазу и глюкокортикостероиды, которые угнетают рубцовую ткань и устраняют избыточную гиалуроновую кислоту.
Дермабразия — отшелушивание рогового слоя эпидермиса. Процедура болезненная, предполагает использование аппаратной техники и длительный период реабилитации. Насколько глубоко воздействовать на кожу и как долго проводить сеанс, решает врач-косметолог. Данный метод эффективен в комплексной терапии.
Домашние средства
От шрамов разной площади, локализации и возраста можно избавиться самостоятельно. К тому же использование домашних процедур увеличит эффект от манипуляций в кабинете косметолога. Например, апликации противорубцовыми средствами отлично сочетаются с микронидлингом, лазерной шлифовкой или мезотерапией.
Особенно хорошо себя зарекомендовал противорубцовый гель Ферменкол. Он применяется аппликационно либо в комплексе с физиотерапией (с электрофорезом или с фонофорезом).
Ферменкол устраняет патологический коллаген и избыточную гиалуроновую кислоту — основу рубцовой ткани, таким образом, выравнивается рельеф и цвет кожи, шрам постепенно разрушается.
Как воздействует Ферменкол на келоид после операции на щитовидной железе:
- уменьшает объем рубца;
- приостанавливает его рост;
- повышает эластичность тканей;
- нормализует цвет в зоне поражения;
- снижает зуд и неприятные локальные ощущения;
- восстанавливает кожу на 90%.
Заказать гель можно на официальном сайте либо в аптеке вашего города.
Важно! Свежие рубцы лучше и легче поддаются терапии, чем застарелые. Поэтому чем раньше вы начнете применять Ферменкол и заботиться о коже в кабинете косметолога, тем быстрее увидите свою шею в первозданном виде.
Не откладывайте покупку Ферменкола на потом! Для бесплатной консультации по выбору подходящего средства обратитесь в специальный раздел на сайте и получите ответ от практикующего врача Светланы Огородниковой. Обращайтесь!
Здесь можно ознакомиться с отзывами об использовании геля Ферменкол для лечения синехий у девочек. Закажите Ферменкол сейчас и будьте уверены, что ваша дочь уже через месяц сможет избавиться от синехий половых губ.

После удаления родинок, ожогов и других травмирующих действий на кожу остаются некрасивые рубцы. Они разные по форме, внешнему виду и причинам появления, но сегодня мы поговорим о самом неприятном из них — о келоидном рубце.
Что такое келоидный рубец и как он выглядит
Келоидный рубец представляет собой разрастание соединительной ткани на травмированном месте кожи. Это грубый рельефный шрам красного цвета, который со временем увеличивается, зудит, чешется и значительно превышает размеры первоначальной раны.
Чаще всего келоидные рубцы образуются в зоне декольте, на спине, шее, лице и на мочках ушей.
Причины появления келоидных рубцов
Есть люди, генетически предрасположенные к рубцам: это связано с повышенным синтезом коллагена при травмировании кожи. В месте заживления раны коллагеновых волокон образуется слишком много, поэтому быстро растет выпуклый рубец. Замечено, что темнокожие люди и люди с азиатской внешностью чаще других имеют склонность к образованию келоидных рубцов.
Некоторые специалисты считают, что кожа, склонная к келоидным рубцам, чаще встречается у людей, имеющих определенные пищевые привычки. Потребление мяса большими порциями и протеина (спортивное питание) способствует активной выработке коллагена.
Чтобы уберечь себя от образования келоидного рубца, важно знать несколько важных правил.
Рассмотрим факторы, которые влияют на заживление раны, а значит, и на формирование шрама. Они бывают локальные и общие.
- Кровоснабжение. Чем лучше кровь поступает к поврежденным тканям, тем быстрее идет процесс заживления.
- Направление раны. Если разрез располагается параллельно частым движениям конечностей (например, рана на лодыжке неизбежно задевается при ходьбе), то риск образования келоида увеличивается.
- Попадание грязи или инфекции.
- Гематома.
- Количество и качество хирургической нити, с помощью которой накладывались швы.
- Возраст. В детстве и юности организм вырабатывает достаточно коллагена и эластина, чтобы раны затягивались быстро и практически без следов. В зрелые годы необходимые вещества вырабатываются с нарушениями в сторону дефицита либо переизбытка, последнее фактически означает склонность к образованию рубцов.
- Иммунитет. При травме иммунная система уничтожает инородные микроорганизмы. Слабая защита способствует инфицированию поврежденного участка.
- Истощение и дефицит витаминов приводят к нарушению обменных процессов и затрудняют нормальное заживление ран, так как организму требуются источники энергии и материал для формирования новых тканей. Кожа, склонная к образованию рубцов, как правило, заметно истощена либо отличается повышенной жирностью и угревыми высыпаниями.
- Ряд заболеваний, например, сахарный диабет и почечная недостаточность. При них нарушается углеводный обмен в тканях, снижается иммунитет, и вследствие этого появляется предрасположенность к келоидным рубцам.
- Онкологические заболевания, гормональные нарушения и необходимость проведения химиотерапии или лучевой терапии.
Виды келоидных рубцов
Келоиды — самые трудные в лечении шрамы. Они отличаются патологически высокой выработкой коллагена и способностью разрастаться со временем, поражая здоровые участки кожи.
Выделяют несколько типов келоидов:
- Истинные (спонтанные). Видимых причин для их возникновения, как правило, нет. Специалисты считают, что склонность к рубцам возникает из-за микротравм. Чаще всего истинные келоиды наблюдаются на лице и груди. Шрамы имеют причудливую форму с ветвящимися отростками, отходящими от основного шрама.
- Ложные (рубцовые). Ложный келоид образуется после операций, порезов, ожогов, фурункулеза и акне. Линейный, может появиться на любом участке тела. Такой рубец может образоваться после выдавливания воспалительного элемента (прыщика) и даже от небольшой царапины.
- Келоидные акне. Обычно встречаются у мужчин. Представляет собой фолликулярный дерматит волосистой части головы. Высыпания (папулы и пустулы) обычно располагаются на затылке.
Также по времени и развитию рубцы классифицируются на активные (растущие) и неактивные.
Активный келоид увеличивается и вызывает зуд, боль, онемение, гиперемию.
Неактивный не беспокоит и находится в стабильном состоянии.
Келоиды классифицируют и по возрасту. Молодым рубцам менее 5 лет, они имеют красный цвет и блестящую поверхность. Старые рубцы образовались более 5 лет назад, их окраска приближается к цвету кожи, а поверхность неровная.

Профилактика келоидных рубцов
Предсказать поведение рубца после травмы невозможно, но можно сократить риски появления келоидных рубцов. В этом помогут силиконовые гели и пластыри, за счет давления на поврежденную область они препятствуют росту рубцовой ткани. Данный метод эффективен только в начале формирования рубца (первые полгода). Силиконовые средства улучшают гидратацию в рубцово-измененной коже и создают кислородное голодание, благодаря которому сосуды в рубце уменьшаются.
Начинать профилактику образования рубца рекомендуется через 3 — 4 недели, когда от ранки полностью отойдут корочки. Заживающее место надо держать в чистоте, мыть с мылом и ни в коем случае не снимать ороговевший слой с ранки — так вы занесете инфекцию, а это верный путь к образованию келоидного рубца!
Возможные методы лечения келоидных рубцов
Несмотря на обилие советов в интернете, народными средствами не избавиться от келоидных рубцов, они могут применяться лишь в комплексе с медикаментами, физиотерапией или косметологией.

Самые популярные способы избавления от келоидных рубцов — это медикаментозное лечение, то есть использование гелей, мазей, кремов и инъекций в сочетании с физиотерапией, например, с ультрафонофорезом или электрофорезом и введение под кожу гормонов-кортикостероидов. Также эффективна мезотерапия — инъекции в ткань рубца витаминных комплексов и лечебных веществ, рассасывающих избыточный коллаген и избыточную гиалуроновую кислоту.
Если консервативные методы не дают ожидаемого результата, то прибегают к хирургии.
Медикаментозное лечение

Аптечные и косметические средства бывают разных направлений:
- содержат интерферон;
- кортикостероиды;
- ферменты или ферментосодержащие препараты.
Содержащие интерферон средства затормаживают выработку коллагена. Иными словами, рубец перестает расти в размерах, однако, он остается на той стадии, до которой дорос сейчас. К подобному способу лечения келоидного рубца прибегают после хирургического вмешательства в виде инъекций альфа- и бета-интерферона.
Уколы делают через сантиметр по всей длине рубца, продолжительность курса длится 4 месяца.
Кортикостероиды могут вводиться как сами по себе, так и комплексно с другими веществами и какой-либо терапией. Их вводят не в сам келоидный рубец, а ближайшее место рядом с ним. Это оберегает от дальнейшего уплотнения шрама, и, несмотря на курс лечения – 5 недель, у 20–30% пациентов наблюдаются рецидивы.
В качестве профилактики повторного образования рубца терапию дополняют лазерным или хирургическим удалением шрама. Данные методы являются очень болезненными и не исключают рецидив (повторное образование рубца). Лазерная шлифовка требует длительного периода восстановления.
Ферментосодержащие препараты расщепляют избыточный коллаген и избыточную гиалуроновую кислоту – основные составляющие рубцовой ткани. За счет этого восстанавливается рельеф и цвет кожи. Рубец становится эластичным, предотвращается его активный рост.
Прессотерапия

Способ, скорее близкий к профилактике, чем к лечению, но некоторые специалисты отмечают положительный эффект.
На проблемное место накладывают различные силиконовые повязки, бинты и пластины. Считается, что постоянно сдавливаемый рубец уменьшается в размерах. К средствам прессотерапии причисляют:
- хлопчатобумажное белье и специальные бандажи (рекомендовано носить полгода, делаются по индивидуальным меркам);
- силиконовые и гелевые давящие пластины;
- жидкости на основе геля — коллодий с полисиликоном или силиконом.
Все это можно найти в любом ортопедическом салоне или аптеке, но данный способ сам по себе не сможет полностью убрать келоидный рубец. Метод прессотерапии эффективен только в комплексном терапии в сочетании с другими способами коррекции рубца.
Микротоковая физиотерапия
Во время процедуры на организм ведется воздействие слабым током, из-за чего стимулируются обменные процессы в тканях эпидермиса, келоид уменьшается в размере и разглаживается.
Этапы проведения терапии:
- обработка шрама антисептиком;
- нанесение препарата, разрушающего рубец;
- подключение прибора, воздействие на рубец током;
- удаление оставшегося лекарства салфеткой.
Процедура не сложная по исполнению, однако, к ней есть противопоказания:
- обостренные вирусные заболевания;
- плохая свертываемость крови;
- патологии с сердцем;
- обострение хронических заболеваний;
- неврологические отклонения от нормы.
Эта процедура считается малоэффективной, по сравнению с другими видами физиотерапии. К тому же она стоит недешево.
Лучевое воздействие
Подразумевает регулируемое рентгеновское излучение, разрушающее фибробласты внутри рубцовых тканей. Интенсивность лучей назначается исходя из серьезности проблемы: ведь 90% от всего потока поглотит эпидермис, и только 10% достигнут глубинных слоев кожи.
Однако терапия проводится лишь в комплексе с другим лечением, иначе риск рецидива повышается на 50%.
Противопоказания к применению:
- шрамы на лице, шее и груди;
- онкология;
- заболевания почек;
- нарушенное кровообращение.
Обычная доза облучения 15–20 Гр. Процедуру повторяют раз в 2 месяца, но не более 6 раз.
Однако лучевое воздействие считается одним из самых эффективных методов в борьбе с рубцами, независимо от причины их появления.
Удаление келоида лазером
Бывает нескольких видов лизерной шлифовки: аргоновая, углеродная и дермабразия. Цель процедуры состоит в выпаривании жидкости из соединительных тканей шрама, из-за чего он высыхает и уменьшается в размере. Мертвые клетки убирают хирургическим путем, а сама лазерная процедура проводится под местной анестезией.
Достоинства лазерного удаления:
- во время первого сеанса исчезает до 70% шрама, что говорит о быстром видимом результате;
- длительность терапии от 20 минут до полутора часов, в зависимости от сложности проблемы.
Процедура достаточно болезненная и требует длительного периода реабилитации.
Чтобы избежать рецидива, врачи советуют сочетать лазер с другими видами лечения келоидных рубцов: применение противорубцовых гелей станет отличным помощником на пути к здоровой коже.
Криометодика
Влияние на келоид жидким азотом. Он выжигает клетки рубцовой ткани, на месте которых образуется здоровая кожа. Время соприкасания рубца с азотом 10–30 секунд, при передозировке возможна пигментация, также велик риск заработать атрофический рубец. Нужно быть крайне осторожным с данным методом коррекции!
Видимый эффект достигается за 1–3 сеанса, но для лучшего результата криотерапию совмещают с гормональными уколами с глюкокортикостероидами.
Однако при больших шрамах прижигание азотом лучше совместить с хирургией. Главным недостатком метода является болезненность.
Косметология

Сделать рубец менее заметным помогут косметические процедуры. Полностью избавиться от рубца с их помощью не получится, но в сочетанной терапии эти методы очень даже эффективны:
- дермабразия;
- пилинг;
- мезотерапия.
Пилинг. С помощью пилингов можно отшлифовать рубец, выровнять рельеф кожи и устранить пигментацию. В результате кожа становится более гладкой, а рубец более эластичным.
Глубокая дермабразия — отшелушивание рогового слоя эпидермиса. Процедура чувствительная, предполагает использование аппаратной техники. Как глубоко и долго проводить сеанс, решает косметолог.
Мезотерапия — инъекции гепарина, иммуномодулятора или витаминного комплекса в проблемный участок. Оказывает противовоспалительный и смягчающий эффект.
При небольшом шраме рекомендована дермабразия или мезотерапия, а большие и застарелые келоиды удаляются в комплексе с медикаментозной терапией.
Хирургия
Назначается в крайнем случае когда другие терапии недостаточно эффективны. Иссечение келоида проводят через пару лет после его образования и в несколько этапов:
- небольшой надрез скальпелем на шраме под местным наркозом;
- края рубца сшиваются косметическими стежками для лучшего срастания надреза;
- после рассасывания швов — гормональные инъекции и ферментативная терапия.
После операции показана профилактика против рецидива, ведь свежий рубец лучше поддается коррекции. Во время реабилитационного периода часто прописывают лучевую терапию, инъекции с иммуномодуляторами и гормонами, а также наружные средства в виде гелей и мазей.
Лечение с Ферменколом

Вся продукция линейки Ферменкол содержит комплекс из 9 ферментов коллагеназы — вещества, расщепляющего избыточный коллаген и избыточную гиалуроновую кислоту до простейших элементов.
Ферменкол используют в виде аппликаций (просто мазать), а также в сочетании с физиотерапией. Так, гель Ферменкол подходит для процедур фонофореза, а Ферменкол в виде раствора — для электрофореза.
Чем быстрее вы начнете лечение келоидного рубца, тем проще и дешевле от него будет избавиться! Не упускайте возможность вернуть красивую кожу, как можно скорее.
Получить бесплатную консультацию по своей проблеме можно, задав вопрос специалисту. Вам ответят в ближайшие два дня и подскажут оптимальный метод коррекции келоидного рубца.
Помните! Молодые рубцы быстрее и проще поддаются коррекции, чем застарелые. Не упускайте время, начните заботиться о себе уже сегодня!
Читайте также:

