Пиодермия при сахарном диабете
Обновлено: 19.04.2024
Пиодермии (гнойничковые болезни кожи) являются наиболее распространенными кожными заболеваниями во всех возрастных группах. По-видимому, это обусловлено тем, что возбудители пиодермий – стафилококки и стрептококки – часто обнаруживаются в окружающей человека среде (в воздухе, пыли помещений, а также на одежде, коже человека).
Бактериальные инфекции кожи являются междисциплинарной проблемой, они встречаются в практике хирургов, терапевтов, педиатров, гинекологов.
Пиодермии (от греч. pyon – гной, derma – кожа) составляют обширную группу различных по клиническим формам, течению и прогнозу дерматозов, в основе которых лежит гнойное воспаление кожи, ее придатков и подкожной жировой клетчатки (рис. 1).
Заболевания кожи, связанные с деятельностью бактерий, как патогенных, так и условно-патогенных, характеризуются нозологическим многообразием. Инфекционный процесс при пиодермиях порой не ограничивается лишь локальным эффектом – развитием воспаления, но может нанести серьезный урон общему состоянию организма (например, синдромы стафилококкового и стрептококкового токсического шока), приводит к возникновению заболеваний, протекающих без воспалительных явлений (точечный кератолизис) [1, 2].
Возбудителями пиодермии являются в основном стафилококки и стрептококки, относящиеся к грамположительной микробной флоре. Возникновение нагноения кожи под влиянием стафилококков и стрептококков объясняется воздействием на нее различных продуктов метаболизма, выделяемых пиогенными кокками в процессе их жизнедеятельности (экзотоксины, энтеротоксины, ферменты и др.).
В российской дерматологии общепризнанной является классификация пиодермий, предложенная Jadasson (1949) в модификации А.А. Каламкаряна (1954) и С.Т. Павлова (1957), согласно которой пиодермии в зависимости от возбудителя традиционно разделяют по этиологическому принципу – стафилодермии и стрептодермии, а также смешанные – стрептостафилодермии. По протеканию заболевания выделяют острые и хронические формы; по глубине поражения – поверхностные и глубокие, а по механизму возникновения – первичные и вторичные.
Клинические проявления гнойничковых болезней кожи разнообразны. Наиболее распространенными являются фолликулиты, вульгарный сикоз, фурункул, карбункул, гидраденит, импетиго, хроническая язвенная пиодермия. У грудных детей может развиться эпидемическая пузырчатка новорожденных и др.
Пиодермия часто осложняет зудящие кожные заболевания (так называемая вторичная пиодермия), особенно чесотку, экзему, нейродермит, атопический дерматит. Нередко вторичная пиодермия наблюдается при пузырчатке, опоясывающем герпесе, микозах, язвенно-некротическом ангиите.
Лечение гнойничковых заболеваний кожи остается одним из актуальных вопросов терапии дерматозов [3].
Лечение пиодермий всегда должно быть комплексным и включать особый режим поведения и ухода за кожей, диету, местные и системные препараты, а также физиотерапевтические процедуры.
В лечении гнойничковых заболеваний кожи необходимо соблюдать основной принцип, а именно – проводить этиотропное лечение, т. е. воздействующее на возбудителя, и патогенетическое – для устранения способствующих пиодермии факторов и коррекции сопутствующей патологии.
Режим больного пиодермией в первую очередь предполагает рациональный уход за кожей, как в очаге поражения, так и вне его.
При локализованных формах заболевания не рекомендуется мыть кожу лишь в очаге поражения и вблизи него, а при диссеминированном процессе мытье запрещается вообще.
Волосы в области расположения пиодермических элементов необходимо состричь (не брить!).
Непораженную кожу обрабатывают, особенно тщательно в окружности очага поражения, дезинфицирующими растворами (1–2% спиртовой раствор салициловой кислоты, 0,1% водный раствор перманганата калия и др.).
С целью предотвращения распространения инфекции ногти должны быть коротко острижены, дважды в день их обрабатывают 2% спиртовым раствором йода.
При длительно текущих процессах, а также при множественных высыпаниях особое внимание следует уделить диете: питание должно быть регулярным, полноценным, богатым витаминами; резко ограничивают количество соли и углеводов; полностью исключается алкоголь.
Для местного лечения поверхностных форм пиодермий используют спиртовые растворы (салициловой кислоты, камфоры), анилиновые красители (фукорцин, 1% бриллиантовый зеленый, 0,1% калия перманганат), топические антисептические и антимикробные препараты. При необходимости, принимая асептические меры, вскрывают покрышку фликтен и пустул с последующим промыванием 3% раствором перекиси водорода (водорода пероксид) и смазыванием дезинфицирующими растворами: нитрофуралом 0,1%, йода раствором спиртовым 5%. В качестве антисептических средств широко применяют хлоргексидин (0,5% спиртовой или 1% водный раствор хлоргексидина биглюконата), диоксидин, эвкалипта листьев экстракт, микроцид, повидон-йод и др.; для наружного лечения также эффективны аэрозоли, т. к. они равномерно наносятся на поверхность, быстро проникают в кожу: триамцинолон, гидрокортизон + окситетрациклин, лифузоль, декспантенол. На распространенные множественные очаги наносят мази, содержащие антибиотики и сульфаниламиды: 2% мазь, крем фуцидина, 2% мазь мупироцина, сульфадиазин, бацитрацин + неомицин, сульфатиазол серебра, левомеколь, гелиомициновая мазь 4%, линкомициновая мазь 2%, гентамициновая мазь 0,1%. Курс лечения составляет 7–14 дней.
Топические комбинированные глюкокортикостероидные препараты с противовоспалительным и антибактериальным действием назначают при вторичной пиодермии основных дерматозов (атопического дерматита, чесотки, экземы и др.): фуцикорт, фузидовая кислота, гидрокортизон + окситетрациклин, лоринден С, целестодерм с гарамицином, травокорт и др. Курс лечения 7–14 дней.
При лечении поверхностных форм пиодермий (остиофолликулиты, фолликулиты, импетиго, эктима) хороший терапевтический эффект был получен при использовании сульфатиазола серебра – 2% крема аргосульфан [4].
После первичной обработки глубоких ограниченных очагов стафилококковой инфекции показаны также рассасывающие средства, ферменты, мази, ускоряющие репаративные процессы в коже, обеспечивающие глубокое проникновение лекарственного препарата и ограничивающие распространение гноя: ихтаммол, 0,25% раствор трипсина, химотрипсин, левосин, пиолизин, актовегин, солкосерил, цинка гиалуронат.
Для лечения язвенных поражений при пиодермии применяют эпителизирующие мази и повязки, для очищения от некротических масс – ируксол, трипсин, химотрипсин. В последнее время впечатляющий эффект при лечении язвенных дефектов при пиодермии получен от применения 2% крема аргосульфан. В качестве действующего начала содержит серебряную соль сульфатиазола, которая обладает мощным антибактериальным эффектом на грамотрицательные и грамположительные микроорганизмы (стафилококки, стрептококки, вульгарный протей, кишечная палочка, клостридии и др). и более чем на порядок превосходит аналогичное действие одних сульфаниламидов. Ионы серебра, содержащиеся в креме, ослабляют сенсибилизирующие свойства сульфаниламидов, а благодаря связыванию с РНК микробных клеток они обладают и бактериостатическим действием. Серебряная соль сульфатиазола обладает слабой растворимостью и всасываемостью с раневой поверхности, что позволяет длительно поддерживать более-менее постоянную концентрацию препарата в очаге воспаления. Сульфатиазол, как составная часть крема, подавляет размножение микроорганизмов. Гидрофильная основа крема, имеющая оптимальное значение рН и содержащая большое количество воды, обеспечивает местное анальгезирующее действие и увлажнение раны, способствуя репарации тканей. Препарат наносится на очаги поражения 2–3 р./сут.
Мы применяли аргосульфан при лечении гангренозной пиодермии. Его применение в составе комплексной терапии позволило добиться у всех больных полного или почти полного клинического излечения. Это выражалось в уменьшении или исчезновении болевых ощущений при перевязках и вне их, в очищении язвенного дефекта от некротических тканей и появлении зрелых грануляций и краевой эпителизации в области язв, а также в отсутствии или резком снижении роста микрофлоры. Использование аргосульфана у всех пациентов приводило к быстрому рубцеванию язв (в среднем в течение 20–22 дней в зависимости от глубины и обширности дефекта), при этом в процессе лечения больные не отмечали никаких побочных эффектов от проводимой местной терапии.
В целях санации всей кожи рекомендуют общее ультрафиолетовое облучение или обтирание визуально здоровой кожи дезинфицирующими средствами. При отсутствии эффекта от наружного лечения глубоких поражений на лице, шее (фурункул, карбункул), при пиодермиях, осложненных лимфангитом, лимфаденитом, показано этиотропное лечение антибиотиками широкого спектра действия (парентерально или внутрь).
Системные антибиотики при пиодермиях применяют при длительном хроническом течении процесса, большой его распространенности, наличии общих явлений (лихорадка, головная боль, недомогание) и регионарных осложнений (лимфаденит, лимфангиит), локализации глубоких пиодермий на лице, особенно в области носогубного треугольника.
Лечение больных хронической пиодермией системными антибактериальными препаратами должно быть основано на результатах бактериологического анализа с определением чувствительности к ним микрофлоры.
В последние годы препараты пенициллина практически не применяются в терапии пиодермии. В настоящее время наиболее эффективными и в то же время вызывающими наименьшее число побочных реакций являются антибиотики – макролиды (эритромицин, джозамицин, кларитромицин и др.), линкомицин, тетрациклины (тетрациклин, метациклин, доксициклин). Можно назначать также рифампицин, цепорин, цефазолин, цефалотин, цефотаксим, цефтриаксон и другие антибиотики, устойчивые к β-лактамазам и имеющие широкий спектр действия. Разовые и курсовые дозы антибиотиков, способ их введения подбирают индивидуально в зависимости от клинической картины и течения процесса.
Реже антибиотиков, обычно при их непереносимости, применяются сульфаниламидные препараты, которые менее эффективны и нередко вызывают токсидермии. Обычно используют препараты пролонгированного действия (сульфамонометоксин, ко-тримоксазол и др.).
В амбулаторной практике целесообразно применять только антибиотики для приема внутрь с высокой биодоступностью и длительным периодом полувыведения (что позволяет снизить количество приемов в течение суток), при этом воздействие на микрофлору кишечника должно быть минимальным.
При лечении в условиях стационара предпочтение отдают парентеральному введению антибактериальных препаратов. При ступенчатом лечении вначале антибиотик назначают парентерально, а при положительной динамике состояния больного (через 3–7 сут) переходят на его применение внутрь. При первичных инфекциях кожи выбирают антибиотики пенициллинового ряда, альтернативные препараты – цефалоспорины II и III поколения, линкозамиды и фторхинолоны. При легкой или средней форме протекания болезни назначают лекарственные формы для приема внутрь.
При остром течении болезни антибиотик назначается курсом не менее чем на 5–7 сут, при хроническом – на 7–10 сут.
Помимо антибактериальной терапии при хронических формах пиодермии широко применяется иммунотерапия. К средствам активной специфической иммунотерапии относятся стафилококковый анатоксин (нативный и адсорбированный) и стафилококковый антифагин, стафилопротектин, представляющий собой смесь цитоплазматического стафилококкового антигена и анатоксина (препарат вводят подкожно в область нижнего угла лопатки 2 р./нед.). Первая инъекция в дозе 0,3 г, последующие четыре – по 0,5 г. Больным с тяжелыми заболеваниями внутренних органов, что является противопоказанием для проведения активной иммунотерапии, назначают антистафилококковый γ-глобулин или антистафилококковую гипериммунную плазму.
С целью стимуляции неспецифических факторов иммунитета используют аутогемотерапию, пирогенал, продигиозан, диоксометилтетрагидропиримидин, спленин, настойку китайского лимонника, экстракт элеутерококка, гемотрансфузии.
В терапии рецидивирующих, упорно протекающих пиодермий широко применяются иммуностимуляторы, особенно в тех случаях, когда есть возможность подтвердить факт иммунных нарушений: препараты тимуса (тималин, тактивин и др.), препараты γ-глобулинов (γ–глобулин внутримышечный и др.), синтетические химические вещества (левамизол, диуцифон, изопринозин), стерильный фильтрат культуральной жидкости некоторых видов самопроизвольно лизирующихся актиномицет (актинолизат), азоксимера бромид (полиоксидоний). Перспективны стимуляторы выработки интерферонов (оксодигидроакридинилацетат натрия, меглюмина акридонацетат и др.). При всех хронических, вялотекущих формах пиодермии показаны аскорбиновая кислота и витамины группы В и препараты, улучшающие микроциркуляцию (пентоксифиллин, ксантинола никотинат и др.).
При различных формах хронических глубоких пиодермий (язвенно-вегетирующая, гангренозная пиодермии) к антибиотикотерапии присоединяют системные глюкокортикоиды (преднизолон 30–60 мг/cут, метилпреднизолон, бетаметазон), цитостатики (азатиоприн 150 мг/сут, проспидия хлорид).
При лечении абсцедирующего и подрывающего фолликулита Гоффманна применяют изотретиноин из расчета 0,5–1 мг/кг массы тела в течение нескольких месяцев или комбинацию системных антибиотиков и глюкокортикоидов.
В комплексную терапию пиодермий входят физиотерапевтические процедуры: ультрафиолетовое облучение, сухое тепло, УВЧ, низкоэнергетическое лазерное излучение, wiRA-терапия – коротковолновое инфракрасное излучение, прошедшее фильтрацию через воду (780–1400 нм).
Профилактика пиодермий, как первичная (у лиц без гнойничковых заболеваний в анамнезе), так и вторичная, предусматривающая предупреждение рецидивов пиодермии, заключается в проведении определенных мероприятий на производстве и в быту.
На производстве необходимо устранение факторов, приводящих к нарушению санитарно-технических и санитарно-гигиенических норм, производственному травматизму и микротравмам.
Одним из средств борьбы с пиодермиями является своевременная обработка микротравм, для чего применяют растворы анилиновых красителей, спиртовой раствор йода, а также пленкообразующий аэрозоль нитрофурал.
Следует проводить лечение выявленных общих заболеваний, на фоне которых могут развиться гнойничковые поражения кожи (сахарный диабет, болезни пищеварительного тракта, ЛОР-органов и др.).
Вторичная профилактика пиодермии включает периодические медицинские осмотры, учет и анализ заболеваемости, диспансеризацию больных, проведение противорецидивной терапии (стафилококковый анатоксин, витамины, общие УФО, уход за кожей, санация фокальной инфекции).
Пиодермии объединяют в себе гнойно-воспалительные кожные болезни, причиной которых является гноеродная микрофлора – пиококки, стафилококки и стрептококки. Примерно треть всех кожных заболеваний составляют различные пиодермии; первичные пиодермии возникают при поражении здоровой кожи, а вторичные являются осложнением заболеваний, при которых возможны повреждения кожи из-за зуда. Пиодермиями осложняется чесотка, экзема, а так же сахарный диабет и хроническая почечная недостаточность. Если пиодермия протекает с вовлечением глубоких слоев кожи, то после нее остаются стойкие рубцовые и пигментные изменения.
МКБ-10



Общие сведения
Пиодермии объединяют в себе гнойно-воспалительные кожные болезни, причиной которых является гноеродная микрофлора – пиококки, стафилококки и стрептококки. Примерно треть всех кожных заболеваний составляют различные пиодермии; первичные пиодермии возникают при поражении здоровой кожи, а вторичные являются осложнением заболеваний, при которых возможны повреждения кожи из-за зуда. Пиодермиями осложняется чесотка, экзема, а так же сахарный диабет и хроническая почечная недостаточность.
При неосложненных пиодермиях поражения кожи неглубокие и после выздоровления кожный покров полностью восстанавливается; если пиодермии принимают хроническое или затяжное течение, в процесс вовлекаются глубокие слои кожи, то остаются рубцы и пигментные пятна.
Причины пиодермий
На коже человека постоянно присутствует большое количество микроорганизмов, какие-то из них являются нормальной микрофлорой кожи, какие-то сапрофитной и транзиторной микрофлорой, которая при снижении защитных функций кожи способна вызывать пиодермии. В результате жизнедеятельности микроорганизмы выделяют ферменты, эндо- и экзотоксины, что и вызывает местную реакцию в виде пиодермий.
В патогенезе пиодермий важное место занимают условия труда и особенности кожи человека, возраст и состояние иммунной системы; снижение иммунологической реактивности человека и несоблюдение личной гигиены увеличивает вероятность возникновения пиодермий. В большинстве случаев пиодермии вызывает сапрофитная микрофлора, а потому пациенты не представляют опасности для окружающих.
Микротравмы, стрессовые ситуации, перегревание или переохлаждения являются факторами, которые снижают защитные функции кожи и повышают вероятность пиодермий; в группу риска попадают люди, страдающие сахарным диабетом, патологиями пищеварительной системы, нарушениями функции кроветворения и витаминного баланса, ожирение и истощение также угнетают местный иммунитет.
Кожа, склонная к выработке излишнего количества кожного сала, что случается при нарушениях ЦНС, наиболее уязвима для пиококков, так как изменение химического состава кожного сала снижает стерилизационные свойства кожи. Изменение гормонального фона или прием корткостероидов приводят к общим заболеваниям, которые являются предрасполагающими к пиодермиям.
Классификация пиодермий

Пиодермии классифицируют в зависимости от глубины и тяжести поражения, а так же в зависимости от возбудителя. Поверхностные пиодермии проявляющиеся остиофолликулитами, сикозами кожи – это чаще всего стафилодермии. Поверхностные стрептодермии и смешанные пиодермии клинически проявляются в виде импетиго вульгарного.
Глубокие стафилодермии проявляются в виде глубоких фолликулитов, гидраденитов, фурункулеза и карбункулеза. Глубокие воспаления кожи стрептококковой инфекцией заканчиваются язвенными поражениями кожи, протекающими по типу эктимы вульгарной. Язвенно-вегетатирующие хронические формы глубоких пиодермий чаще всего вызываются смешанной микрофлорой.
Лечение пиодермии

Лечением пиодермии занимается дерматолог. При пиодермиях волосы в очаге инфекции и вокруг него состригают, но не бреют, чтобы не допустить обсеменения патогенной микрофлорой участки здоровой кожи; если пиодермия носит генерализованный характер, то запрещаются водные процедуры, в том числе и мытье. Контакт с водой крайне не желателен, особенно в острой фазе заболевания.
Кожу вокруг пораженного участка обрабатывают спиртовыми растворами анилиновых красителей и дезинфектантами, хороший эффект оказывает салициловая кислота и раствор перманганата калия. Несмотря на то, что контакт с водой запрещен, ежедневно нужно тщательно мыть руки и обрабатывать ногти 2% раствором йода, чтобы предотвратить распространение инфекции, а также протирать здоровую кожу влажной губкой.
Питание в период лечения должно быть сбалансированным, лучше перейти на молочно-растительную диету, полностью исключить из меню экстрактивные вещества и алкоголь, ограничить употребление соли и простых углеводов. Если пациент ослаблен, имеет сопутствующие заболевания или пиодермия принимает затяжной или хронический характер течения, при присоединении симптомов интоксикации, медикаментозное лечение пиодермии целесообразно проводить антибактериальными препаратами. Перед назначением антибиотика проводят бакпосев отделяемого или соскоба, определяют возбудителя и его чувствительность к препаратам. Антибиотики пенициллинового ряда практически не назначают из-за их низкой эффективности, макролиды и тетрациклины дают хороший терапевтический эффект, но эритромицин и тетрациклин нежелательно применять для лечения детей и беременных.
Лечение комбинированными антибактериальными препаратами и цефалоспоринами (цефотаксим и др) назначают при инфицировании смешанной микрофлорой, так как эти препараты обладают широким спектром действия и устойчивы к изменчивости бактерий. Курс и дозировка препаратов назначаются индивидуально, исходя из тяжести течения пиодермий, обычно прием антибиотиков не должен быть меньше недели. Сульфаниламидные препараты менее эффективны при пиодермиях, но если у пациента непереносимость антибиотиков, то назначают сульфаметоксазол+триметоприм, сульфомонометоксин в нужных дозировках.
Активная специфическая иммунотерапия в сочетании с антибиотикотерапией и местным лечением дает хорошие результаты, особенно при хронических и вялотекущих процессах. Подкожное введение анатоксинов, специфических антигенов, стафилопротектинов два раза в неделю проводят в условиях поликлиники или в стационаре, если пациент находится на госпитальном лечении.
Для стимуляции неспецифического иммунитета прибегают к аутогемотрансфузии, переливанию компонентов крови, ультрафиолетовому облучению крови (УФОК); такие препараты как метилурацил, настойка лимонника и экстракт элеутерококка тоже стимулируют иммунную систему. Если имеются иммунные нарушения, то лечение пиодермий целесообразно проводить с назначением иммуностимуляторов группы препаратов тимуса; препаратов гамма-глобулинов и стимуляторов выработки интерферона. Витаминотерапия показана при всех видах пиодермий.
Профилактика пиодермий
Профилактика как для лиц, у которых нет в анамнезе гнойничковых заболеваний, так и для лиц с рецидивами пиодермий в анамнезе, заключается в соблюдении правил личной гигиены, в организации предупреждающих мер в быту и на производстве. Соблюдение санитарно-технических и санитарно-гигиенических норм на производстве существенно снижают заболеваемость пиодермиями в отдельно взятом учреждении. Кроме того своевременная обработка травм и микротравм позволяет исключить дальнейшее инфицирование ран и развитие пиодермий.
Регулярные профилактические медицинские осмотры с целью выявления хронических заболеваний пищеварительной системы, ЛОР-органов позволяют назначить лечение и не допустить развитие вторичных пиодермий. Для больных сахарным диабетом профилактика пиодермий заключается в более тщательном уходе за кожей, в своевременном ее увлажнении, чтобы не допускать мацерации и образования микротравм, так как при сахарном диабете даже небольшая царапина зачастую становится причиной обширных и глубоких пиодермий.
Глубокая пиодермия – группа гнойно-воспалительных поражений кожи (преимущественно ее глубоких слоев – дермы), обусловленных инфицированием тканей стафилококками, стрептококками или смешанной микрофлорой. Симптомы заболевания различаются в зависимости от выраженности воспаления и характера возбудителя, но обязательно включают в себя отек, болезненность, покраснение и образование гноя. Диагностика глубокой пиодермии основывается на внешних кожных проявлениях и микробиологических исследованиях для идентификации возбудителя. В лечении широко применяются хирургические приемы для обеспечения оттока гноя, местные и общие антибиотики, противомикробные и антисептические средства.
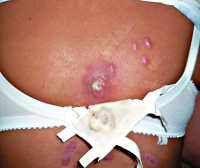
Общие сведения
Глубокая пиодермия – гнойное заболевание кожных покровов, особенностью которого является поражение дермы, подкожной клетчатки, глубоко расположенных волосяных фолликулов, потовых и сальных желез. Это состояние является одной из наиболее распространенных патологий в дерматологии – по разным данным, на нее приходится от 30 до 40% всех дерматологических заболеваний. Практически каждый человек минимум несколько раз в жизни страдал от проявлений различных форм глубокой пиодермии. Это объясняется высокой распространенностью возбудителей (стафилококков и стрептококков), их вирулентностью, огромным разнообразием штаммов. В большинстве случаев глубокая пиодермия не угрожает жизни человека и даже излечивается самостоятельно без специальной терапии, но иногда она может быть причиной интоксикации, источником метастатических гнойных очагов и даже причиной сепсиса.

Причины глубокой пиодермии
В широком плане, глубокая пиодермия – поражение кожи, обусловленное гноеродной микрофлорой, к которой относят стафилококков, стрептококков, синегнойную палочку и некоторые другие микроорганизмы. Однако более 95% случаев заболевания вызываются именно кокковой флорой, так как она широко распространена в окружающей среде и отчасти представлена даже на поверхности кожи здорового человека. При проникновении в ткани кожи через микротрещины, повреждения эпидермиса, вдоль волосяных стержней и по протокам кожных желез микроорганизмы начинают бурно размножаться. Выделяемые ими в процессе жизнедеятельности ферменты и различные токсины вызывают деструкцию клеток кожи. В результате этих процессов формируется первичный очаг, расположенный в дерме – симптомов глубокой пиодермии на этом этапе не наблюдается.
Сами микроорганизмы и выделяемые ими ферменты обладают сильными иммуногенными свойствами, поэтому практически сразу после формирования первичного очага происходит незамедлительная реакция иммунной системы. Традиционно первыми на инфицирование реагируют тканевые макрофаги, затем путем хемотаксиса в будущий очаг глубокой пиодермии попадают нейтрофилы, а затем и другие иммунокомпетентные клетки. Выделяемые ими биологически активные вещества приводят к местному отеку, покраснению, появлению болезненных ощущений. Клинически это соответствует первой стадии глубокой пиодермии – образованию воспалительного очага, который может иметь тенденцию к расширению.
На определенном этапе иммунитету удается локализовать воспаление, и его распространение в тканях останавливается. Нейтрофилы атакуют патогенные микроорганизмы и отчасти собственные ткани (вторичная альтерация) в очаге с формированием гноя – субстанции, состоящей из «осколков» возбудителей, разрушенных собственных клеток и погибших нейтрофилов. Развитие глубокой пиодермии облегчается при ряде обстоятельств – пониженном иммунитете, сахарном диабете, истощении, гиповитаминозах и других ослабляющих организм состояниях. Немаловажную роль играет пренебрежение правилами личной гигиены, избыточная продукция кожного сала, местное переохлаждение кожи. Для лиц с пониженным иммунитетом глубокая пиодермия опасна тем, что способна вызывать сильные поражения, стать причиной различных осложнений, некоторые из которых могут напрямую угрожать жизни человека.
Симптомы глубокой пиодермии
Существует несколько клинических разновидностей глубокой пиодермии, которые характеризуется разными возбудителями, выраженностью симптомов и типом поражаемых тканей. Все формы этого заболевания по характеру микрофлоры, вызвавшей воспаление, делят на стафилодермии, стрептодермии и смешанные разновидности, которые иногда называют стрептостафилодермиями. К глубоким пиодермиям, вызванным стафилококками, относят фурункулы, карбункулы, гидрадениты и глубокий фолликулит. Глубокие стрептодермии представлены вульгарной эктимой, а воспаления из-за смешанной микрофлоры – хронической язвенно-вегетирующей пиодермией.
Фурункул – разновидность глубокой пиодермии, особенностью которой является поражение волосяного фолликула гнойно-некротического характера с переходом на окружающие ткани. Его развитию может предшествовать поверхностное гнойное воспаление (фолликулит), однако возможно и первичное развитие глубокого процесса. На участке кожи, окружающей волос, формируется сначала очаг багрового цвета размером от нескольких миллиметров до 1-2 сантиметров, болезненный и плотный, его температура заметно выше окружающих кожных покровов. Затем глубокая пиодермия такого типа сопровождается появлением гноя, в центре которого будет стержень из некротизированной ткани. Гнойно-некротическое содержимое отторгается через 3-10 дней, на месте поражения кожи формируется небольшая язва, которая быстро рубцуется.
Карбункул – более тяжелая разновидность глубокой пиодермии, вызываемая стафилококковой флорой и характеризующаяся поражением глубоких слоев дермы и подкожной жировой клетчатки. В глубине кожи возникает плотный инфильтрат, кожные покровы над ним приобретают синюшно-багровый оттенок, становятся горячими и болезненными. Через несколько дней в очаге глубокой пиодермии начинают формироваться пустулы, происходит выделение гноя и некротических стержней, на месте поражения образуется язва. Все это сопровождается выраженными общими симптомами – интоксикацией, лихорадкой, болями стреляющего характера в месте карбункула. Отмечается регионарный лимфаденит и лимфангит. После разрешения этой формы глубокой пиодермии на месте поражения остается заметный рубец.
Гидраденит – форма глубокой пиодермии, при которой поражаются апокриновые потовые железы с развитием гнойного воспаления. Из-за этого характерная локализация патологических очагов – подмышечные впадины, околососковая и аногенитальная области. Гидраденит начинается с развития болезненного узла синюшного цвета, который за несколько дней значительно увеличивается в размерах и самопроизвольно вскрываются с выделением обильного количества гноя. Затем происходит постепенное заживление, рубцы образуются в крайне редких случаях. При этой форме глубокой пиодермии также отмечается регионарный лимфаденит и лимфангит, но общие симптомы выражены слабо. Гидрадениты, особенно в области подмышечных впадин, склонны к частым рецидивам.
Глубокий фолликулит – одна из наиболее легких форм глубокой пиодермии, которая отличается от обычного фолликулита более выраженным поражением волосяных луковиц. Симптоматика в целом сходна с фурункулом, однако проявления менее выраженные, общих симптомов практически никогда не наблюдается. Главный диагностический критерий, позволяющий дерматологу отличить фурункул от глубокого фолликулита – отсутствие гнойно-некротического воспаления, так как не образуется характерный некротический стержень.
Вульгарная эктима – форма глубокой пиодермии, вызываемая стрептококковой микрофлорой. Чаще всего поражает кожу голени у ослабленных больных, в крайне редких случаях возникает у здоровых людей. Эктима начинается с образования на поверхности кожных покровов пустулы с мутным содержимым серозного, иногда геморрагического характера. Затем пустула исчезает и на ее месте формируется типичный очаг глубокой пиодермии – болезненная язва с выраженным воспалительным ободком вокруг, дно образования покрыто слоем гноя. Через 2-3 недели после появления язвы начинается ее постепенное рубцевание с развитием заметного шрама.
Хроническая язвенно-вегетирующая пиодермия – кожное заболевание, возбудителями которого является смешанная микрофлора, наибольшую роль в развитии патологии играет золотистый стафилококк и стрептококки группы А. Глубокая пиодермия такого типа чаще всего развивается у ослабленных больных – истощенных лиц, страдающих алкоголизмом, пожилых людей. Характеризуется образованием на нижних конечностях эрозий неправильной формы с рваными краями, окруженных воспаленной кожей. Дно язвенных образований покрыто гноем, часто возникают выделения с неприятным зловонным запахом. Эрозии длительное время не заживают и склонны к частым рецидивам или поражению других участков кожных покровов.
Осложнениями любой разновидности глубокой пиодермии могут быть метастатические гнойные поражения регионарных лимфатических узлов и отдаленных органов. Особенно опасны в этом отношении глубокие фолликулиты и фурункулы, возникающие в пределах носогубного треугольника – имеющиеся там анастомозы кровеносных сосудов способствуют заносу инфекции в головной мозг и его оболочки. У ослабленных больных на фоне глубокой пиодермии могут возникать флегмоны и сепсис, являющиеся жизнеугрожающими состояниями. В редких случаях возможно развитие токсического шока.
Диагностика глубокой пиодермии
Диагностика различных форм глубокой пиодермии осуществляется посредством осмотра дерматолога (иногда может потребоваться консультация хирурга). Из дополнительных методов исследования наиболее часто применяют посев гноя для определения характера возбудителя и для выяснения его чувствительности к антибактериальным средствам. При развитии общих симптомов также в ряде случаев необходимо проведение общего анализа крови, в самых тяжелых случаях – бакпосев крови для диагностики сепсиса. Результаты осмотра зависят от формы глубокой пиодермии и стадии ее развития – это может быть просто воспалительный очаг, сформировавшийся гнойник, ранка или язва с гнойным отделяемым. При посеве определяются стафилококки или стрептококки, может обнаруживаться смешанная микрофлора. Микробиологические исследования посевов могут определить вид и штамм возбудителя, а также его чувствительность к антибиотикам.
Если имеется повышение температуры, головная боль, слабость то необходимо проведение общего анализа крови. Обычно при глубокой пиодермии определяются легкие неспецифические признаки воспаления – повышение скорости оседания эритроцитов, небольшой лейкоцитоз. В более тяжелых случаях наблюдаются уже выраженные изменения – значительный рост СОЭ, выраженный лейкоцитоз, выявляются изменения в распределении нейтрофилов. В крови появляется множество юных форм этой фракции лейкоцитов, что носит название нейтрофильного сдвига влево. Если есть подозрения, что глубокая пиодермия стала причиной сепсиса, производят посев крови на питательные среды – в норме кровь человека абсолютно стерильна, рост культур говорит о наличии возбудителя в крови. Для диагностики таких осложнений, как метастатические гнойные очаги могут применяться ультразвуковые, рентгенологические и другие методы клинических исследований.
Лечение глубокой пиодермии
При незначительных по выраженности гнойных поражениях без общих проявлений интоксикации рекомендуется ждать самопроизвольного разрешения глубокой пиодермии. Лечебные мероприятия сводятся к недопущению осложнений. При наличии волос вокруг гнойного очага их нужно аккуратно состричь – использование бритвы может привести к распространению инфекции. Мыть участок с очагом глубокой пиодермии не рекомендуется, допустимо только протирать кожу вокруг него дезинфицирующими растворами (хлоргексидином, раствором салициловой кислоты). Строго запрещается без участия дерматолога или хирурга самостоятельно вскрывать гнойник или каким-либо способом ускорять отделение гноя – это может привести к диссеминации возбудителя.
Если глубокая пиодермия характеризуется развитием крупных очагов с появлением общих симптомов (лихорадка, слабость, головные боли), то необходимо назначение антибактериальных средств, таких как эритромицин, тетрациклин, линкомицин – предварительно желательно сделать бактериальный посев и определить препарат, к которому наиболее чувствителен данный микроорганизм. Также при глубокой пиодермии применяют и противомикробные средства из группы сульфаниламидов – например, сульфаметоксазол+триметоприм. В последние годы в тяжелых случаях гнойных поражений кожи используют и иммунологические препараты – стафилококковый анатоксин, антистафилококковую гипериммунную плазму и ряд других.
При глубоком расположении значительного по размерам очага пиодермии прибегают к хирургическому вскрытию полости гнойника для формирования дренажа и оттока гноя. Кроме того, это позволяет доставлять антисептические и антибактериальные препараты непосредственно в область поражения, что ускоряет лечение. Вскрытие очага глубокой пиодермии должно происходить в стерильном помещении и осуществляться квалифицированным гнойным хирургом.
Прогноз и профилактика глубокой пиодермии
В большинстве случаев прогноз при развитии различных форм глубокой пиодермии благоприятный – после отделения гноя происходит заживление очага, довольно часто с образованием рубцов. Однако у ослабленных больных с низким уровнем иммунитета возможно развитие осложнений, некоторые из которых могут угрожать жизни и требуют лечения в условиях стационара. Для профилактики развития глубокой пиодермии необходимо придерживаться правил личной гигиены, своевременно обрабатывать кожные повреждения (ссадины, порезы) антисептиками. Кроме того, важно устранять возможные источники инфекции в организме – кариозные зубы, хронические инфекции ЛОР-органов.
Хроническая язвенно-вегетирующая пиодермия — это глубокое гнойно-воспалительное заболевание кожи, обусловленное стафило-стрептококковой инфекцией и проявляющееся образованием длительно существующих язвенных дефектов с вегетационными разрастаниями по периферии. Диагностика хронической язвенно-вегетирующей пиодермии заключается в проведении осмотра, исследовании отделяемого язв с определением возбудителя заболевания, выявлении сопутствующих заболеваний и нарушений иммунитета. Лечение включает антибиотикотерапию, иммунокоррекцию, терапию сопутствующих заболеваний, местную антибактериальную, протеолитическую и заживляющую терапию, лечение лазером и УВЧ.
МКБ-10
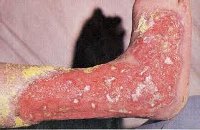
Общие сведения
Наиболее часто хроническая язвенно-вегетирующая пиодермия встречается в возрасте от 40 до 60 лет. Мужчины более подвержены заболеваемости, чем женщины. Хроническая язвенно-вегетирующая пиодермия относится к глубоким формам пиодермии со смешанным характером вызвавших ее возбудителей. Как правило, это стрептококковая инфекция и золотистый стафилококк. Заболевание может возникнуть как осложнение длительно текущего фолликулита или запущенного стрептококкового импетиго.

Причины
Развитие хронической язвенно-вегетирующей пиодермии связано с одной стороны с особой вирулентностью вызывающих ее бактерий, а с другой — с ослабленным состоянием организма. Последнее может быть обусловлено:
- сахарным диабетом;
- ВИЧ-инфекцией;
- истощением в результате анорексии;
- алкоголизмом;
- заболеваниями ЖКТ (язвенная болезнь 12п. кишки, хронический гастрит, панкреатит, гепатит, язвенный колит и пр.);
- витаминной недостаточностью;
- снижением иммунитета;
- сосудистой патологией (атеросклероз, варикоз, лимфедема).
Симптомы
Хроническая язвенно-вегетирующая пиодермия начинается с образования глубокого инфильтрата или фурункула, который быстро трансформируется в большую язву. Процесс носит множественный характер и локализуется чаще всего на нижних конечностях. Для него типично длительное течение, которое может затягиваться на несколько лет.
Язвенные дефекты при хронической язвенно-вегетирующей пиодермии выстланы вялыми грануляциями и характеризуются большим количеством гнойного отделяемого, что сопровождается неприятным запахом. Типичными являются разрастания тканей по периферии язвы — вегетации. Вокруг очага поражения наблюдается отечность и краснота кожи, происходит высыпание глубоких пустул. Язвенные дефекты склонны увеличиваться в диаметре и распространяться в глубь тканей, затрагивая не только дерму и подкожную клетчатку, но и мышцы. Вовлечение в гнойный процесс подлежащей кости приводит к развитию остеомиелита.
Хроническая язвенно-вегетирующая пиодермия сопровождается общими симптомами: недомоганием, выраженной болезненностью, нарушением сна, развитием анемии. Заживление язвенных дефектов происходит с образованием грубых рубцов. Отдельно выделяют шанкриформную пиодермию, имеющую сходство с твердым шанкром, и серпигинозную пиодермию, для которой характерно сочетание процессов заживления в центре язвы с продолжающимся воспалением на ее периферии.
Диагностика
Диагностику осуществляет врач-дерматолог на основании осмотра, анамнестических данных, результатов бакпосева отделяемого язв. Гистологическое исследование при хронической язвенно-вегетирующей пиодермии выявляет признаки хронического воспаления дермы с некротическими и гранулематозными очагами, дистрофические изменения в эпидермисе. В анализе крови часто отмечается анемия. По показаниям проводится копрограмма, анализ кала на дисбактериоз, исследование сахара крови и панкреатических ферментов, УЗИ брюшной полости, иммунограмма. При шанкриформной пиодермии требуется микроскопия отделяемого язв на бледную трепонему, ПЦР-диагностика и RPR-тест.
Для диагностики сопутствующих соматических заболеваний назначается консультация гастроэнтеролога и иммунолога, при необходимости — сосудистого хирурга. Дифдиагностика хронической язвенно-вегетирующей пиодермии проводится с:
- вегетирующей пузырчаткой;
- глубокими формами грибковых заболеваний;
- третичным сифилисом;
- язвенно-вегетирующими проявлениями туберкулеза.
Лечение
Хроническая язвенно-вегетирующая пиодермия является показанием для проведения системной антибиотикотерапии. Антибиотики применяются в соответствии с данными антибиотикограммы и сочетаются с иммуностимулирующей терапией (гамма-глобулин, антистафилококковая плазма). По результатам иммунограммы назначаются иммуномодуляторы. Хороший эффект дает использование в комплексной терапии препарата с флавоноидами диких злаков, стимулирующего выработку интерферона в организме. Одновременно следует проводить коррекцию имеющихся соматических нарушений.
В местом лечении хронической язвенно-вегетирующей пиодермии применяют мази с глюкокортикостероидами и антибиотиками, протеолитические ферменты, мазь Вишневского, нитрат серебра, дерматоловую мазь, средства для ускоренной эпителизации. Проводится лазеротерапия, УВЧ, местная УФО-терапия.
ГУ "МОНИКИ им М.Ф. Владимирского", Москва
Комплексное лечение длительно незаживающих ран разной этиологии
Журнал: Клиническая дерматология и венерология. 2013;11(3): 101‑106
Третьякова Е.И. Комплексное лечение длительно незаживающих ран разной этиологии. Клиническая дерматология и венерология. 2013;11(3):101‑106.
Tret'iakova EI. Combination treatment for persistent wounds of various etiologies. Klinicheskaya Dermatologiya i Venerologiya. 2013;11(3):101‑106. (In Russ.).
ГУ "МОНИКИ им М.Ф. Владимирского", Москва
Представлены результаты наружного лечения 2% кремом Аргосульфан 47 больных с длительно не заживающими ранами разной этиологии. В результате комплексного лечения полная эпителизация трофических язв у больных с хронической венозной недостаточностью, облитерирующим эндоартериитом и липоидным некробиозом наступила у 10 (41,7%) пациентов, частичный регресс - у 14 (58,3%). Явления пиодермии разрешились у 7 (87,5%) больных, значительно уменьшились - у 1 (12,5%). Трещины в области ладоней и подошв на фоне разрешения тилотической экземы заэпителизировались у всех 15 (100%) пациентов. Крем Аргосульфан в комплексной терапии больных с длительно не заживающими ранами оказался высокоэффективным, отличался хорошей переносимостью, удобством в применении.
ГУ "МОНИКИ им М.Ф. Владимирского", Москва
Важнейшей медико-социальной проблемой является лечение длительно не заживающих ран разной этиологии. Трофические язвы и глубокие трещины кожи в области нижних конечностей, а также хронические язвенные пиодермии резко снижают качество жизни и надолго ограничивают активность больных. Особое место в лечении и профилактике этих заболеваний, предупреждающей развитие инфекционного процесса в ране и являющейся барьером на пути распространения инфекции, занимает местная терапия.
Современные высокоэффективные средства для местного лечения длительно не заживающих ран имеют ряд лечебных качеств, которые позволяют применять их с учетом фаз раневого процесса. Они должны обладать противовоспалительным и протеолитическим действием, иметь широкий антибактериальный спектр воздействия, сохранять активность в кислой среде, не вызывать явлений гипергрануляции и пигментации, иметь гипоаллергенные качества, быть нетоксичными и удобными в применении.
Существует много комбинированных препаратов для местного лечения, содержащих антибиотики или сульфаниламиды в сочетании друг с другом и/или разными антисептиками. Для таких препаратов характерно более медленное развитие микробной резистентности и более широкий охват бактериальных агентов — возбудителей инфекций.
Присутствующие в составе крема ионы серебра усиливают антибактериальное действие сульфаниламида — тормозят рост и деление бактерий путем связывания с дезоксирибонуклеиновой кислотой микробной клетки [1]. Постепенное высвобождение ионов серебра подавляет рост патогенной микрофлоры на протяжении длительного периода нахождения повязки на ране, что важно при высоком риске реинфекции госпитальными штаммами и является постоянным барьером на пути распространения инфекции.
Кроме того, ионы серебра ослабляют сенсибилизирующие свойства сульфаниламида. Существует мнение, согласно которому аппликация на кожу и слизистые оболочки сульфаниламидов нежелательна в связи с невысокой активностью и риском возникновения аллергической реакции. При нанесении такой мази на ожоговую или инфицированную поверхность могут наблюдаться жжение и боль [1]. Гидрофильная основа крема Аргосульфан, имеющая оптимальный рН и содержащая большое количество воды, обеспечивает его увлажняющее и аналгезирующее действие и приводит к уменьшению сроков заживления ран.
Благодаря минимальной резорбции Аргосульфан-крем, нанесенный даже на обширные раневые поверхности, не оказывает токсического действия, так как сульфатиазол серебра обладает небольшой растворимостью, благодаря чему концентрация лекарственного средства в ране длительно поддерживается на одинаковом уровне. Незначительное количество сульфатиазола серебра, оказавшегося в кровотоке, в печени подвергается ацетилированию и в моче находится в виде неактивных метаболитов и частично в неизмененном виде [1]. В связи с отсутствием системной абсорбции препарата можно использовать крем Аргосульфан в сочетании с другими препаратами. Повязки с кремом Аргосульфан, содержащие ионы серебра, безболезненны при наложении на раневую поверхность, не присыхают к ране и легко удаляются с ее поверхности, обладают мягким подсушивающим эффектом, хорошо проникают в некротизированную ткань и экссудат. Тканевый детрит, пропитанный препаратом, образует «защитную подушку», под которой идет форсированное образование грануляций и эпителизация.
Мы применяли крем Аргосульфан при длительно не заживающих ранах у больных с трофическими язвами разной этиологии, липоидном некробиозе, хронической язвенной и язвенно-вегетирующей пиодермиях, глубоких трещинах, осложняющих течение тилотической экземы.
Появление трофических язв может осложнить течение многих заболеваний – от болезней системы кровообращения до нарушений обмена веществ, причем развитие язвенного дефекта сопровождается как нарушением нормального кровообращения, так и изменением иннервации. Именно поэтому процесс выздоровления может потребовать применения комплексного воздействия и достаточно продолжительного лечения.
Различают варикозные, ишемические и нейротрофические язвы [2—5]. Наибольшую группу (1—2% взрослого населения) составляют больные с хронической венозной недостаточностью (ХВН) нижних конечностей, развивающейся при нарушении венозного оттока и повышении давления внутри капилляров. Основные причины ХВН — варикозное расширение вен и посттромбофлебитический синдром. При повреждении клапанов глубоких вен голени нарушается функция мышечно-венозной помпы и возникает ретроградный ток крови. Повреждение прободающих вен, которые соединяют поверхностные вены с глубокими, усугубляет венозную недостаточность. Из-за отложения фибрина в периваскулярном пространстве и угнетения тканевого фибринолиза развиваются склероз и облитерация лимфатических и мелких кровеносных сосудов. Периваскулярный фиброз нарушает доставку питательных веществ к эпидермису, что приводит к образованию варикозных трофических язв [2—5].
Ишемические язвы формируются при заболеваниях периферических артерий, в частности при облитерирующем атеросклерозе (ОАС). ОАС всегда сопровождается поражением кожи — от постепенно нарастающей ишемии до инфаркта, т.е. некроза, развивающегося при внезапном нарушении кровоснабжения в результате атероэмболии — закупорки мелких артерий фрагментами атеросклеротических бляшек. Ишемические язвы локализуются на часто травмируемых участках и местах сдавления, сопровождаются выраженными болевыми ощущениями. Смешанные язвы развиваются у больных, страдающих и ХВН, и ОАС, у которых клинически присутствуют черты обоих заболеваний [4, 5].
Причиной нейротрофических язв являются поражение чувствительных и двигательных нервов, нарушения кровообращения и атеросклероз при сахарном диабете и его осложнениях, вторичном гиперпаратиреозе, гранулематозном воспалении в ответ на дегенерацию коллагена при липоидном некробиозе [6, 7].
Липоидный некробиоз — редкий хронический дерматоз сосудисто-обменного характера, который обычно относят к группе локализованных липоидозов кожи. Провоцирующими факторами при липоидном некробиозе в 1 /3 случаев является сахарный диабет, еще у 1 /3 — нарушение толерантности к глюкозе, поэтому необходимы семейный анамнез и исследования для выявления скрытых форм сахарного диабета. Началу заболевания нередко предшествует травма. Дегенерация коллагена приводит к усиленной агрегации тромбоцитов, микроангиопатиям, поражению артериол, склерозированию и облитерации сосудов в очагах некробиоза. Сосудистые нарушения приводят к нарушению трофики и некробиотическим изменениям дермы с последующим отложением в ней липидов. Заболевание часто имеет длительное рецидивирующее течение, его выраженность не зависит от тяжести сахарного диабета, формирующиеся трофические язвы сопровождаются выраженными болевыми ощущениями и заживают, как правило, с формированием грубого рубца [6, 7].
Без специального лечения трофические язвы характеризуются низкой тенденцией к заживлению и длительным рецидивирующим течением [8, 9]. Общепризнано, что оперативное лечение ХВН и ОАС лучше выполнять после заживления трофической язвы или тщательной санации ее поверхности. Однако консервативное лечение с применением устаревших малоэффективных местных медикаментозных средств часто осложняется дерматитом, экземой, рожистым воспалением, что отодвигает сроки выполнения сосудистой операции. На выбор лекарственного препарата влияют фаза течения заболевания и выраженность воспалительной реакции (I фаза — предъязвенное состояние; II фаза — дистрофические изменения, некроз, воспаление кожи и прилежащих тканей; III фаза — очищение язвы и регенерация; IV фаза — эпителизация и рубцевание), осложнения (микозы, экзема, пиодермии, рожистое воспаление, рецидивирующий тромбофлебит, малигнизация и др.), видовой состав микрофлоры язвы. В многочисленных бактериологических исследованиях качественного состава микрофлоры поверхности трофических язв выявлена полирезистентная грампозитивная и грамнегативная микрофлора. Содержание микроорганизмов в индуративно измененных тканях, окружающих язву, иногда достигает 10 7 -10 9 микробных тел на 1 г ткани раны, что указывает на высокий риск генерализации инфекционного процесса [10]. Как правило, выделяемые микроорганизмы высокорезистентны не только к традиционным антибактериальным препаратам, но и к наиболее часто используемым в таких случаях местным средствам — растворам фурацилина, хлоргексидина, синтомициновой эмульсии, мазям с антибиотиками (тетрациклином, гентамицином) и др. На стадиях грануляции и эпителизации, для их ускорения, а также при осложнении ран дерматитом, экземой или другими проявлениями аллергии на традиционные препараты, средством выбора могут стать соли серебра, учитывая их высокую эффективность в подавлении как грампозитивной, так и грамнегативной микрофлоры, лучшую переносимость и редкость аллергических реакций даже у пациентов с отягощенным аллергоанамнезом.
Пиодермии (гнойничковые заболевания кожи) представляют собой группу дерматозов, в основе которых лежит гнойное воспаление кожи и ее придатков, а также подкожно-жировой клетчатки. На долю пиодермий приходится 1 /3 всех случаев заболеваний кожи [4, 5]. Развитию пиодермий способствуют микротравмы, мацерация и загрязнение эпидермиса, повышенное потоотделение, переохлаждение, перегревание, эндокринопатии (сахарный диабет), гипогаммаглобулинемия, недостаточное поступление белков, гиповитаминоз, нарушения иммунитета и тяжелые соматические заболевания, переутомление, хронические интоксикации, персистирующие очаги стафилококковой инфекции. Наиболее частыми возбудителями пиодермий являются золотистый и эпидермальный стафилококк (80—90% больных), в 10—15% случаев выявляется смешанная инфекция (стафилококк в сочетании со стрептококком, синегнойной палочкой, протеем, кишечной палочкой и др.) [1, 4, 10].
Хронические язвенная и язвенно-вегетирующая пиодермии относятся к глубоким стрептостафилококковым пиодермиям, характеризуются образованием плохо заживающих язвенных гнойных поражений кожи и подлежащих тканей. Нередко заболевание сопровождается ухудшением общего состояния, повышением температуры тела, слабостью, явлениями интоксикации, лимфангиитами и лимфаденитом. Язвенная пиодермия (стрептостафилококковое импетиго) проявляется фликтенами, эктимами, располагающимися на фоне эритемы. Высыпания, как правило, диссеминированные, захватывают обширные участки кожного покрова. Под корками характерно образование глубоких язв с вялыми грануляциями на дне и воспаленными мягкими краями. Стрептостафилококковое импетиго нередко является осложнением зудящих дерматозов (экземы, чесотки, атопического дерматита и др.). Хроническая язвенно-вегетирующая пиодермия характеризуется язвенными образованиями неправильной формы с выраженными вегетациями в области краев и дна. Нередко вокруг язвы присутствует застойно-розовый венчик гиперемии. Характерно хроническое течение с периодическими обострениями с появлением новых язв или серпигенизации основного язвенного образования.
Терапия пиодермий должна быть этиопатогенетической. При лечении хронических, рецидивирующих и глубоких форм пиодермий используют антибиотики (местно и системно), антисептические растворы, по показаниям глюкокортикостероиды, иммуномодуляторы, витамины, проводят вскрытие пустул и абсцессов, при необходимости — удаляют и выскабливают вегетации и некротические ткани.
Тилотическая (роговая) экзема — хроническое упорно рецидивирующее аллергическое заболевание кожи, разновидность истинной экземы. Тилотическая экзема проявляется гиперкератозом ладоней и подошв с образованием грубых роговых и корковых наслоений, сухостью кожи, а также глубокими болезненными длительно не заживающими, нередко кровоточащими трещинами. Данное заболевание характеризуется поливалентной сенсибилизацией и аутосенсибилизацией, протекает на фоне нейроэндокринных сдвигов, сопровождается изменениями в центральной и вегетативной нервной системе, нарушениями обменных процессов и трофики тканей [4, 5]. Поражение подошв и ладоней, как правило, симметричное, трещины формируются на фоне эритемы, шелушения, особенно на участках наибольшего давления и нагрузки, в том числе и на боковых поверхностях пальцев. Воспаление может быть выражено на ограниченном участке или занимать всю подошву и/или ладонь, боль в области трещин может быть более интенсивной, чем зуд. Тенденция к углублению трещин связана с возрастом пациента, длительностью болезни, холодным временем года и наличием фоновых заболеваний.
В трещины на подошвах легко может проникать пиогенная инфекция, развиваться рожистое воспаление или пиодермии. Тилотическая экзема резистентна к лечению, склонна к рецидивированию, к улучшению состояния приводят частое и сильное увлажнение кожи и немедленное прекращение ношения влажной обуви [11].
Под нашим наблюдением находились 47 больных (13 мужчин, 34 женщины) в возрасте 44—75 лет с трофическими язвами, развившимися на фоне ХВН и облитерирующего эндартериита, нарушениях кровоснабжения и трофики при липоидном некробиозе, а также с пиодермиями и тилотической экземой. Длительность заболевания составляла от 2 мес до 4 лет. Все больные в составе комплексной терапии наружно применяли крем Аргосульфан.
У 11 (23,4%) больных имелись варикозные, у 5 (10,6%) — смешанные трофические язвы, у 8 (17%) — трофические язвы при липоидном некробиозе; у 8 (17%) — хроническая язвенная и хроническая язвенно-вегетирующая пиодермии, у 15 (32%) — тилотическая экзема с глубокими трещинами на ладонях и подошвах.
У 22 (46,8%) больных дерматозы протекали на фоне эндокринных заболеваний: у 4 (8,4%) — сахарного диабета, у 2 (4,2%) — нарушений толерантности к глюкозе, у 5 (10,6%) — узлового зоба, у 1 (2,1%) — гипотиреоза, у 1 (2,1%) — патологии надпочечников. У 2 (4,2%) больных был выявлен хронический бронхит, у 3 (6,3%) — хронический гастрит, у 5 (10,6%) — хронический панкреатит, у 2 (4,2%) — вирусный гепатит С, у 10 (21,3%) — гипертоническая болезнь, у 9 (1%) — ишемическая болезнь сердца, у 2 (4,2%) — миома матки.
При бактериологических исследованиях качественного состава микрофлоры с поверхности очагов (язв, трещин) у 29 (61,7%) больных выявлен золотистый и эпидермальный стафилококк, у 18 (38,3%) — смешанная инфекция (стафилококки в сочетании со стрептококком, кишечной палочкой, бактероидами, протеем, дрожжевыми грибами) в количестве 104—105 микробных тел на 1 г ткани раны.
Всем пациентам назначался охранительный режим. Предлагалось ограничить пребывание в вертикальном положении с целью уменьшения статической нагрузки, размещать пораженную конечность в возвышенном положении. Рекомендовалось уменьшить потребление с пищей соли и экстрактивных продуктов, больным с тилотической экземой назначалась гипоаллергенная диета, пациентам с липоидным некробиозом — диета с ограничением углеводно-жировой нагрузки.
В составе комплексной терапии все больные получали сосудистые препараты и венопротекторы (пентоксифиллин, детралекс, эскузан), антиагреганты (курантил), десенсибилизирующие средства (глюконат кальция, тиосульфат натрия), улучшающие трофику (солкосерил, актовегин) и антигистаминные (супрастин, тавегил, лоратадин) препараты. Пациентам с трофическими язвами, липоидным некробиозом, пиодермиями проводилось лечение антибиотиками цефалоспоринового ряда, иммуномодуляторами (метилурацил, виферон, циклоферон), витаминами (мильгамма), с тилотической экземой — препаратами витамина А (аевит, ретинола пальмитат), с липоидным некробиозом — препаратами липоевой кислоты (берлитион).
В качестве наружного средства все больные использовали 2% крем Аргосульфан. После очищения 0,1% водным раствором хлоргексидина и/или хирургической обработки раневых поверхностей препарат слоем 2—3 мм ежедневно 2 раза в сутки наносили на очаги поражения на трещины или язвы с середины к краям до полного впитывания. На очаги, имеющие большую площадь, крем Аргосульфан наносили ежедневно под окклюзионную повязку на ночь. Рана во время лечения покрывалась препаратом полностью, если ее часть открывалась, крем наносили дополнительно. Курс комплексного лечения составлял 25—30 сут.
Болевых ощущений, а также местных и общих аллергических реакций при использовании крема Аргосульфан не наблюдалось.
Крем Аргосульфан при местном лечении длительно не заживающих ран позволил добиться улучшения у всех больных. В результате комплексной терапии полная эпителизация трофических язв у больных с ХВН, ОАС и липоидным некробиозом наступила в 10 (41,7%) случаях, частичный регресс (уменьшение размеров, воспалительных и дистрофических изменений кожи, появление зрелых грануляций и краевой эпителизации с минимально выраженной пигментацией) — в 14 (58,3%). Явления пиодермии разрешились у 7 (87,5%) пациентов, значительно уменьшились (с резким замедлением роста микрофлоры до 102 микробных тел на 1 г ткани раны) — у 1 (12,5%). Отсутствие под повязкой с кремом Аргосульфан гипергрануляций в ране способствовало формированию негрубых подвижных слабопигментированных рубцов. Трещины в области ладоней и подошв на фоне разрешения тилотической экземы эпителизировались у всех 15 (100%) пациентов.
Поскольку крем Аргосульфан — препарат длительного применения, что обусловлено медленным восстановлением физиологических процессов в эпидермисе и дерме, больным с трофическими язвами и пиодермией мы рекомендовали использовать его по ранее применяемой схеме амбулаторно в течение 1—2 мес после окончания курса лечения в стационаре (до полного заживления или пересадки кожи).
Таким образом, 2% крем Аргосульфан в комплексной терапии больных с длительно не заживающими ранами оказался высокоэффективным как на стадии формирования трофических язв, так и в период заполнения глубоких ран грануляционной тканью, что во многих случаях привело к самостоятельному заживлению их под повязкой. Препарат отличался хорошей переносимостью, удобством в применении, позволил значительно снизить стоимость лечения больного в стационаре и успешно продолжить лечение амбулаторно.
Читайте также:

