Передается ли ихтиоз от отца к ребенку
Обновлено: 18.04.2024
Бестактные вопросы, брезгливость, глупые советы — это лишь часть того, с чем сталкиваются родители детей-«рыбок». Что важно знать об этой болезни?
В феврале 2020 года американская модель Джейза Гэри появилась на обложке британского Glamour. Дело в том, что у Джейзы ламеллярный ихтиоз — редкое генетическое заболевание кожи. С раннего детства Джейза подвергалась буллингу и испытывала комплексы, но не переставала верить в то, что однажды ее жизнь изменится.
Не каждый день встретишь человека с редким заболеванием кожи, но такие люди живут среди нас. Каково им приходится, рассказывает ведущий врач-дерматолог фонда «Дети-бабочки» Маргарита Гехт.
Что такое ихтиоз?
Ихтиоз — это группа генетических заболеваний кожи. Отличительная особенность ихтиоза — усиленная сухость кожи и шелушение. Такая кожа нуждается в постоянном очищении, увлажнении и заживлении с помощью специальных средств.
Предоставлено фондом «Дети-бабочки»
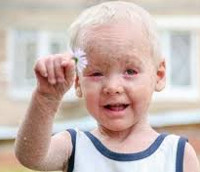
Из-за сильного шелушения кожи детей с ихтиозом называют «рыбками».
Почему ихтиоз — это группа заболеваний?
Ихтиоз имеет три основные формы, и каждая форма делится на типы течения заболевания. Всего таких типов около 40. Заболевание может протекать и выглядеть совершенно по-разному в зависимости от формы и типа ихтиоза.
Существует врожденный ихтиоз. Он проявляется с первых минут жизни новорожденного. В этом случае очень важно правильно и вовремя поставить диагноз, а также своевременно оказать помощь, обеспечивая правильный уход за больным.
Также есть приобретенный ихтиоз. Его сложнее диагностировать, так как он не проявляется сразу. По этой причине врачи часто ставят диагноз неверно, путая ихтиоз с другими дерматозами. В итоге назначается неверная терапия, что ухудшает состояние кожи.
Как возникает заболевание и возможно ли его вылечить?
Всего причин возникновения ихтиоза две: передача «сломанного» гена по наследству (врожденный ихтиоз) и спонтанная «поломка» гена (приобретенный ихтиоз).
Родители могут быть носителями «сломанного» гена или сами быть больными ихтиозом.

Следствием мутации некоторых групп генов становится тяжелая болезнь – ихтиоз. Так называют патологическую трансформацию эпидермиса, в результате которой поверхность кожи покрывается твердыми чешуйками. Степени и формы ороговения варьируют от легкой шероховатости до образования плотного слоя ороговевшего эпидермиса.
Почему развивается заболевание
Патология носит наследственный характер, а главной причиной ихтиоза является мутация некоторых групп генов, которая передается детям от родителей. В редких случаях заболевание является приобретенным и становится следствием недостатка витаминов, проявлением некоторых болезней крови и др.
У больных отмечается нарушение метаболизма белков и аминокислот, в эпидермисе усиливается активность окислительных ферментов, понижается концентрация иммуноглобулинов. Этиология и патогенез до сих пор недостаточно изучены, но многие исследователи отмечают важную роль недостаточности витамина А и функции некоторых желез – щитовидной, надпочечников.
У пациентов с генетической формой ихтиоза, как правило, замедляются обменные процессы, нарушается терморегуляция, плохо работают потовые железы. Высокий уровень ферментов приводит к существенному усилению кожного дыхания. Клеточный и гуморальный иммунитет часто понижен. Нередко гиперкератоз сопровождается эндокринными заболеваниями, болезнями надпочечников и репродуктивной сферы, глазными заболеваниями. Часто у больных усиливается ломкость волос и ногтей, зубы легко поражаются кариесом.
В кожных покровах присутствует чрезмерное количество структурно измененного кератина. Из-за замедления метаболических процессов старые клетки кожи отторгаются недостаточно быстро, что приводит к образованию на поверхности кожи твердых чешуек. Между слоями клеток кожи скапливаются аминокислотные комплексы, ускоряющие процесс затвердения и ороговения, а также скрепляющие чешуйки между собой.
Клинические проявления

Основной симптом ихтиоза – характерные твердые чешуевидные образования на сухой коже – проявляется уже на первом году жизни, гораздо реже – в течение нескольких последующих лет. Кожа ребенка становится шершавой, на ней появляются прозрачные, белесые или сероватые чешуйки, прилегающие друг к другу. Чистыми остаются только локтевые сгибы, впадины под коленями и подмышечные зоны, а также область паха. Ладони и стопы шелушатся, на них ярко выделяется рисунок кожи. В наиболее легких случаях болезнь проявляется лишь небольшим шелушением и сухостью кожи.
В настоящее время насчитывается более пятидесяти клинико-морфологических форм заболевания, однако во всех случаях присутствуют следующие проявления:
- роговой слой эпидермиса утолщен, на нем формируются чешуйчатые образования и зоны ороговения;
- кожа сухая и шелушащаяся, сальные железы практически не работают;
- ногтевые пластины расслаиваются или ломаются, в ряде случаев деформированы и напоминают птичьи когти, отслаиваются от мягких тканей;
- кожный рисунок становится более глубоким и выразительным;
- присутствуют высыпания разной формы и окраски.
Ихтиоз кожи, как правило, обостряется с наступлением холодов. В теплое время обычно наступает ремиссия. Во время полового созревания у подростков болезненные проявления уменьшаются, чтобы вновь вернуться во взрослом возрасте.
Разновидности патологии
Более чем у 90% пациентов развивается вульгарный ихтиоз – заболевание, которое впервые проявляется уже на втором или третьем месяце жизни. В зависимости от характера поражения кожи выделяют следующие клинические формы:
- ксеродермию, или абортивную форму – наиболее легкий вариант болезни, при котором кожа становится сухой и шершавой, но чешуйчатые наслоения отсутствуют;
- простую форму с небольшими чешуйками, тонкими по краям и с уплотненным центром, которыми покрывается все тело вплоть до волосистой части головы;
- блестящую форму с прозрачными чешуйками, расположенными в виде мозаики преимущественно на ногах;
- белую форму с белыми либо слегка желтоватыми чешуйками, внешне похожими на асбестовые волокна;
- змеевидную форму с грубыми ороговениями коричневого, бурого или серого цвета, напоминающими змеиную чешую.
Намного реже встречается ламеллярная форма заболевания (коллодийный плод), фетальная (плод Арлекина), линеарная и т. д. Некоторые из них несовместимы с жизнью – так, фетальный ихтиоз формируется еще во втором триместре внутриутробного развития, и ребенок гибнет в первые дни жизни либо рождается уже мертвым.
Как определяют заболевание
Для первичной диагностики ихтиоза, как правило, бывает достаточно внешних проявлений заболевания. Чтобы отличить его от других кожных заболеваний, назначают гистологическое исследование эпидермиса.
При наличии случаев заболевания в семье проводится пренатальная диагностика: между 19 и 21 неделями развития у плода забирают биопсию эпидермиса.
Можно ли излечить?

На текущем этапе развития медицина еще не умеет справляться с генетическими заболеваниями, поэтому современное лечение ихтиоза направлено на уменьшение клинических проявлений и облегчение состояния пациента. Для этого назначают:
- витаминные комплексы, железосодержащие составы, иммуноглобулин;
- переливания плазмы крови;
- гормонотерапию (в сложных случаях);
- ванны с добавлением различных препаратов, смягчающие мази и кремы;
- физиопроцедуры, курортное лечение по показаниям.
Выбор лечебных методик зависит от степени поражения кожи и особенностей протекания болезни.
Часто возникающие вопросы
Как наследуется ихтиоз от больных родителей?
Заболеванию одинаково подвержены как мужчины, так и женщины, но некоторые формы развиваются преимущественно у детей одного пола. Генная мутация наследуется в 97% случаев, если хотя бы один из родителей болен ихтиозом.
Передается ли ихтиоз при контактах с больным?
Ихтиоз – заболевание генетического характера, поэтому люди, которые им болеют, абсолютно не заразны и не могут передавать свою патологию иначе, чем наследственным способом, т.е. собственным детям.
Как живется людям с ихтиозом?
При ихтиозе показано пребывание в теплом и влажном климате, здоровое разнообразное питание с большим количеством витаминов. Чтобы уменьшить проявления болезни и продлить ремиссию, необходимо:
Что такое синдром Жильбера? Причины возникновения, диагностику и методы лечения разберем в статье доктора Васильева Романа Владимировича, гастроэнтеролога со стажем в 15 лет.
Над статьей доктора Васильева Романа Владимировича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Синдром Жильбера — это генетический пигментный гепатоз с аутосомно-доминантным типом наследования, протекающий с повышением уровня неконъюгированного (свободного) билирубина, чаще проявляющееся в период полового созревания и характеризующийся доброкачественным течением [1] .
Краткое содержание статьи — в видео:
Синонимы названия болезни: простая семейная холемия, конституциональная или идиопатическая неконъюгированная гипербилирубинемия, негемолитическая семейная желтуха.
По распространённости данное заболевание встречается не менее, чем у 5 % населения, в соотношении мужчин и женщин — 4:1. Впервые заболевание описал французский терапевт Августин Жильбер в 1901 году.
Чаще синдром Жильбера проявляется в период полового созревания и характеризуется доброкачественным течением. Основным проявлением этого синдрома является желтуха.
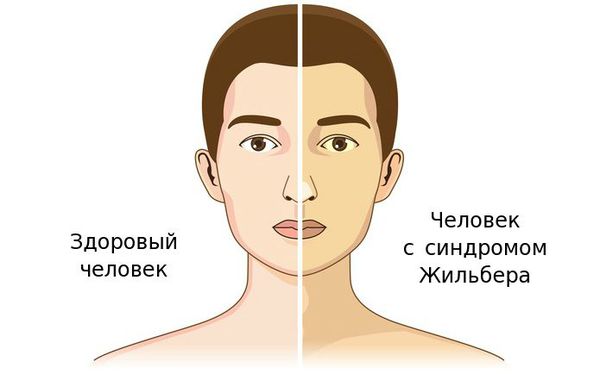
К провоцирующим факторам проявления синдрома можно отнести:
- голодание или переедание;
- жирную пищу;
- некоторые лекарственные средства;
- алкоголь;
- инфекции (грипп, ОРЗ, вирусный гепатит);
- физические и психические перегрузки;
- травмы и оперативные вмешательства.
Причина заболевания — генетический дефект фермента УДФГТ1*1, который возникает в результате его мутации. В связи с этим дефектом функциональная активность данного фермента снижается, а внутриклеточный транспорт билирубина в клетках печени к месту соединения свободного (несвязанного) билирубина с глюкуроновой кислотой нарушается. Это и приводит к увеличению свободного билирубина.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы синдрома Жильбера
Некоторые специалисты трактуют синдром Жильбера не как болезнь, а как физиологическую особенность организма.
До периода полового созревания данный синдром может протекать бессимптомно. Позже (после 11 лет) возникает характерная триада признаков:
- желтуха различной степени выраженности;
- ксантелазмы век (жёлтые папулы);
- периодичность появления симптомов [1] .
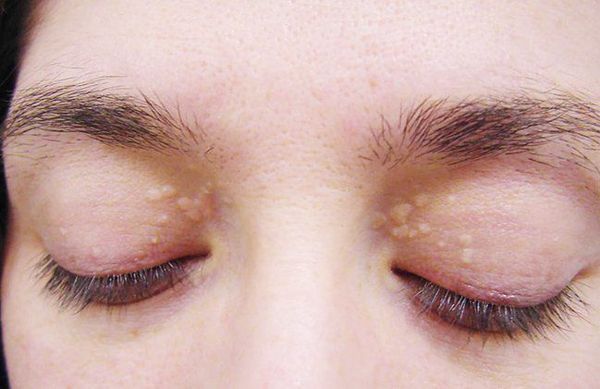
Желтуха чаще всего проявляется иктеричностью (желтушностью) склер, матовой желтушностью кожных покровов (особенно лица), иногда частичным поражением стоп, ладоней, подмышечных впадин и носогубного треугольника.
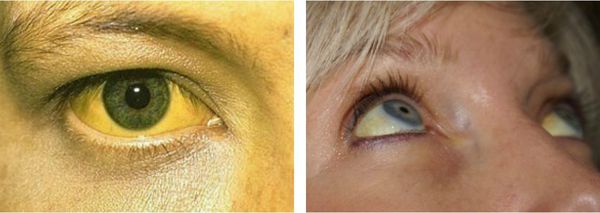
Заболевание нередко сочетается с генерализованной дисплазией (неправильным развитием) соединительной ткани.
Усиление желтухи может наблюдаться после перенесения инфекций, эмоциональной и физической нагрузки, приёма ряда лекарственных препаратов (в частности, антибиотиков), голодания и рвоты.
Клиническими проявлениями заболевания общего характера могут быть:
- слабость;
- недомогание;
- подавленность;
- плохой сон;
- снижение концентрации внимания.
В отношении ЖКТ синдром Жильбера проявляется снижением аппетита, изменением привкуса во рту (горечь, металлический привкус), реже возникает отрыжка, тяжесть в области правого подреберья, иногда наблюдается боль ноющего характера и плохая переносимость лекарственных препаратов.
При ухудшении течения синдрома Жильбера и существенном повышении токсичной (свободной) фракции билирубина может появляться скрытый гемолиз, усиливая при этом гипербилирубинемию и добавляя в клиническую картину системный зуд.
Патогенез синдрома Жильбера
В норме свободный билирубин появляется в крови преимущественно (в 80-85 % случаев) при разрушении эритроцитов, в частности комплекса ГЕМ, входящего в структуру гемоглобина. Это происходит в клетках макрофагической системы, особенно активно в селезёнке и купферовских клетках печени. Остальная часть билирубина образуется из разрушения других гемсодержащих белков (к примеру, цитохрома P-450).
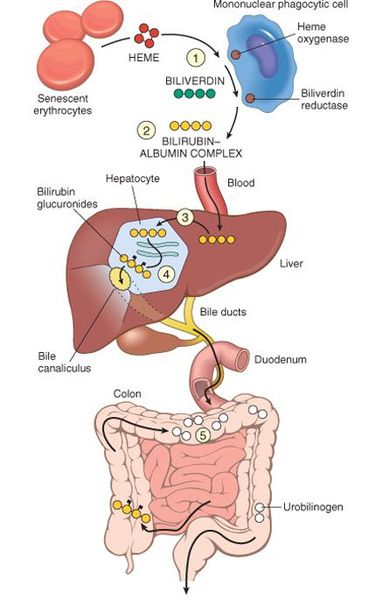
У взрослого человека в сутки образуется приблизительно от 200 мг до 350 мг свободного билирубина. Такой билирубин слаборастворим в воде, но при этом хорошо растворяется в жирах, поэтому он может взаимодействовать с фосфолипидами ("жирами") клеточных мембран, особенно головного мозга, чем можно объяснить его высокую токсичность, в частности токсичное влияние на нервную систему.
Первично после разрушения комплекса ГЕМ в плазме билирубин появляется в неконъюгированной (свободной или несвязанной) форме и транспортируется с кровью при помощи белков альбуминов. Свободный билирубин не может проникнуть через почечный барьер за счёт сцепления с белком альбумином, поэтому сохраняется в крови.
В печени несвязанный билирубин переходит на поверхность гепатоцитов. С целью снижения токсичности и выведения в клетках печени свободного билирубина при помощи фермента УДФГТ1*1 он связывается с глюкуроновой кислотой и превращается в конъюгированный (прямой или связанный) билирубин. Конъюгированный билирубин хорошо растворим в воде, он является менее токсичным для организма и в дальнейшем легко выводится через кишечник с желчью.
При синдроме Жильбера связывание свободного билирубина с глюкуроновой кислотой снижается до 30% от нормы, тогда как концентрация прямого билирубина в желчи увеличивается.
В основе синдрома Жильбера лежит генетический дефект — наличие на промонторном участке A(TA)6TAA гена, кодирующего фермент УДФГТ1*1, дополнительного динуклеотида ТА. Это становится причиной образования дефектного участка А(ТА)7ТАА. Удлинение промонторной последовательности нарушает связывание фактора транскрипции IID, в связи с чем уменьшается количество и качество синтезируемого фермента УДФГТ1, который участвует в процессе связывания свободного билирубина с глюкуроновой кислотой, преобразуя токсичный свободный билирубин в нетоксичный связанный.
Вторым механизмом развития синдрома Жильбера является нарушение захвата билирубина микросомами сосудистого полюса клетки печени и его транспорта глутатион-S-трансферазой, которая доставляет свободный билирубин к микросомам клеток печени.
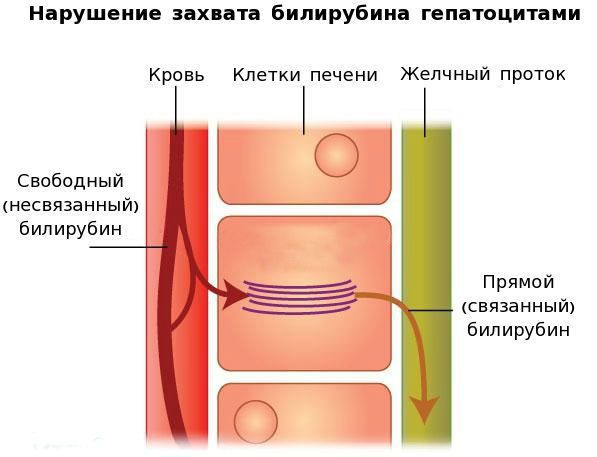
В конечном итоге вышеперечисленные патологические процессы приводят к увеличению содержания свободного (несвязанного) билирубина в плазме, что обуславливает клинические проявления заболевания [6] .
Классификация и стадии развития синдрома Жильбера
Общепринятой классификации синдрома Жильбера не существует, однако условно можно разделить генотипы синдрома по полиморфизму.
Врожденный ихтиоз – гетерогенная группа наследственных заболеваний, для которых характерны мутации генов, отвечающих за правильное развитие кожи, следствием чего являются специфические поражения дермы и другие системные патологии. Основные симптомы – очаги усиленного шелушения кожи, образование плотных чешуек с болезненными бороздками между ними, склонность к гиперпирексии, системное поражение внутренних органов, дефекты лица. Врожденный ихтиоз диагностируется клинически, подтверждается результатами биопсии кожи. В лечении используются препараты ретиноидов и кератолитики, также проводится неспецифическая терапия.
МКБ-10
Общие сведения
Врожденный ихтиоз – наследственный дерматоз, характеризующийся нарушением процессов ороговения. Точное описание болезни дал Роберт Виллан в 1808 году, термин «ихтиоз» предложен В. Вилсоном в 1852 году и используется в настоящее время. Частота встречаемости врожденного ихтиоза варьирует в зависимости от формы заболевания и составляет в среднем 1:2000 для простого ихтиоза, 1:4000 для Х-сцепленного ихтиоза, 1:100000 для эпидермолитического ихтиоза, 1:300000 для ламеллярного ихтиоза. Половых различий не выявлено, кроме Х-сцепленной формы врожденного ихтиоза, которая диагностируется только у мальчиков. Актуальность проблемы в педиатрии связана с часто запоздалой диагностикой и временным эффектом от лечения. Врожденный ихтиоз – одна из причин детской инвалидности.

Причины врожденного ихтиоза
Врожденный ихтиоз всегда является следствием мутаций в генах, отвечающих за правильное развитие эпителия. Мутировавшие гены передаются из поколения в поколение, то есть заболевание наследуется. Первичные причины самих мутаций достоверно неизвестны, но могут быть связаны с тератогенными факторами и факторами внешней среды. Простой и эпидермолитический ихтиоз наследуются по аутосомно-доминантному типу, ламеллярный – по аутосомно-рецессивному типу. При Х-сцепленном ихтиозе мутация происходит в гене, сцепленном с половой хромосомой, механизм наследования рецессивный.
В случае простого ихтиоза нарушен синтез филаггрина – белка, отвечающего за соединение нитей кератина между собой. Именно кератин способствует удержанию влаги кожей, и в данном случае нарушается эта его функция. Х-сцепленный врожденный ихтиоз характеризуется недостаточностью стеролсульфатазы, вследствие чего кератиноциты оказываются прочно связанными с подлежащими слоями кожи, ввиду чего нарушается их своевременное отторжение. Ламеллярный ихтиоз связан с недостаточностью трансглутаминазы-1, которая принимает участие в ороговении оболочек клеток кожи, и ускоренным продвижением кератиноцитов к поверхности кожи, то есть быстрой их сменой. Следствием являются обширные воспалительные процессы, нарушения терморегуляции и высокий риск вторичных инфекций.
В основе эпидермолитического ихтиоза – нарушение синтеза кератина, из-за чего клетки кожи становятся нестабильными. Это способствует образованию буллезных пузырей, характерных для этого типа врожденного ихтиоза. Редко встречающийся ихтиоз плода развивается внутриутробно и обусловлен нарушением транспорта липидов, вследствие чего нарушается барьерная функция кожи.
Классификация врожденного ихтиоза
Существует несколько классификаций заболевания по различным признакам. В зависимости от типа наследования врожденный ихтиоз может быть:
- Аутосомно-доминантным (простой и эпидермолитический ихтиоз);
- Аутосомно-рецессивным (ламеллярный ихтиоз, ихтиоз плода);
- Х-сцепленным (Х-сцепленный ихтиоз).
Различаются условия, необходимые для проявления заболевания. Первые два типа не связаны с полом, мутировавший ген должен быть представлен в доминантной и рецессивной форме соответственно. Х-сцепленный ихтиоз наследуется рецессивно, проявляется у мальчиков, в то время как девочки являются носителями мутации.
Клинически выделяют следующие типы врожденного ихтиоза: простой (вульгарный), ламеллярный, Х-сцепленный, эпидермолитический, ихтиоз плода. В зависимости от тяжести клинических проявлений ихтиоз может быть тяжелым, средней тяжести и поздним (проявляется не сразу после рождения). Врожденный ихтиоз может быть не только самостоятельным заболеванием, также он присутствует в структуре некоторых синдромов, таких как синдром Нетерсона, синдром Рефсума, синдром Руда, синдром Шегрена-Ларссона и некоторые другие. Также существуют ихтиозиформные заболевания, например, гиповитаминоз А, сенильный ихтиоз и др. В этих случаях клиника схожа, но причины другие.
Симптомы врожденного ихтиоза
Симптоматика напрямую зависит от формы заболевания. В клинике простого ихтиоза всегда имеет место выраженная сухость кожи и шелушение. Зоны поражения располагаются на разгибательных поверхностях суставов, особенно ног. Лицо остается нетронутым, за редким исключением, когда в процесс вовлекается кожа лба и щек. Также характерен фолликулярный гиперкератоз – скопление кератина в фолликулах волос. Возникает почти на всей поверхности кожи, где растут волосы. Обнаруживается при пальпации в виде так называемого симптома «тёрки». Кожа на ладонях и подошвах утолщена, усилен кожный рисунок, выделяются бороздки между участками утолщенной кожи. У больных отмечается снижение потоотделения, что является причиной частой гипертермии.
Основные симптомы врожденного ихтиоза проявляются с 3-12 месяцев жизни ребенка. Шелушение кожи часто практически нивелируется к 20-25 годам. При этом остаются характерные для этой формы заболевания изменения ладоней и подошв. Часто врожденный ихтиоз данного типа сопровождается аллергическими заболеваниями в виде ринита, крапивницы, бронхиальной астмы. В большинстве случаев характерно поражение желудочно-кишечного тракта: гастрит, колит, дискинезия желчных путей, гепатоспленомегалия. На клеточном уровне изменения идентичны таковым в клетках кожи.
Х-сцепленный врожденный ихтиоз проявляется в первые месяцы жизни и только у мальчиков. Характерное поражение кожи – крупные, грязно-коричневого цвета чешуйки без шелушения. Локализация подобных участков может быть практически любой, кроме области ладоней и стоп. Такой цвет чешуек обусловлен высокой концентрацией меланина в нижних слоях эпидермиса. Из других признаков часто обнаруживается специфическое помутнение роговицы в форме цветка без влияния на остроту зрения. У пятой части пациентов диагностируется крипторхизм. В отличие от простого ихтиоза, поражения кожи при данном типе заболевания практически не уменьшаются с возрастом.
Ламеллярный ихтиоз проявляется с рождения. Кожа новорожденного покрыта тонкой, но плотной пленкой - это патогномоничный симптом врожденного ихтиоза данного типа. Постепенно пленка трансформируется в крупные толстые чешуйки от светлого до коричневого цвета. Вследствие закупорки потовых желез нарушено потоотделение, поэтому часто наблюдается гиперпирексия. На ладонях и подошвах – глубокие трещины и кератодермия. Бороздки между чешуйками болезненны и являются воротами для вторичной бактериальной инфекции, включая сепсис. Ламеллярный врожденный ихтиоз сопровождается дефектами развития: часто отмечается выворот век (эктропион) и губ (экслабион), деформация или отсутствие ушных раковин, деформация хрящей носа, сращение фаланг пальцев либо отсутствие концевых фаланг и др.
Эпидермолитический врожденный ихтиоз проявляется обширной влажной эритродермией с формированием буллезных пузырей. На месте вскрытия пузырей остаются эрозии, которые бесследно проходят. Со временем присоединяется грубое ороговение, часто образуются бородавки. Ороговевшие чешуйки темные, с неприятным запахом (следствие вторичной инфекции). Слизистые оболочки при данном типе врожденного ихтиоза не поражаются, потоотделение также не нарушено. Тем не менее, эта форма заболевания очень опасна и может сопровождаться смертельным исходом.
Врожденный ихтиоз плода – самая редкая форма заболевания, развивается внутриутробно на 16-20 неделе беременности. Дети рождаются недоношенными, кожа их напоминает панцирь, который вскоре трескается с образованием крупных пластинчатых чешуек, чаще темных. Характерно почти полное отсутствие волос на голове, кератодермия ладоней и подошв. Из-за сильного ороговения кожи лица рот постоянно открыт, выражены эктропион и экслабион, ушные раковины деформированы. При врожденном ихтиозе плода часто диагностируется нейросенсорная тугоухость. Сниженный иммунитет способствует развитию бактериальных инфекций уже в первые дни жизни; часто встречаются отиты, пневмония, подкожные абсцессы. Высока смертность в первые дни и недели жизни.
Диагностика врожденного ихтиоза
Во время беременности с целью диагностики можно использовать амниоцентез с последующим анализом амниотической жидкости, а также биопсию ворсин хориона. Однако инвазивные методы повышают риск самопроизвольного прерывания беременности, поэтому на практике используются крайне редко. Показанием для пренатальной биопсии является отягощенный анамнез по врожденному ихтиозу. УЗИ в III триместре позволяет диагностировать ихтиоз плода. Заметно фиксированное положение рук и открытый рот, можно увидеть гипоплазию носовых хрящей и неспецифические признаки в виде многоводия и повышенной эхогенности амниотической жидкости. Остальные формы врожденного ихтиоза можно лишь заподозрить.
После рождения ребенка диагноз ставится педиатром, в первую очередь, на основании клинических симптомов, характерных для врожденного ихтиоза. Это специфическое шелушение кожи, локализация пораженных участков, симптом «тёрки» при простом ихтиозе, выраженная эритродермия при эпидермолитическом ихтиозе и др. Изменения в анализах неспецифичны, но могут выявить аллергические процессы (часто сопутствуют ихтиозу), высокий уровень холестерола и одновременно сниженный уровень эстриола в крови (при Х-сцепленном ихтиозе). Имеет значение анамнез родителей: выявленные прежде случаи врожденного ихтиоза, в том числе его синдромные формы.
Часто клиническая картина заболевания неспецифична, поэтому обязательно проведение дифференциальной диагностики. Необходимо исключать приобретенные формы ихтиоза, дерматозы (псориаз, экзема, контактный дерматит, врожденный сифилис и др.), атопический дерматит. Так, для дерматитов характерно наличие воспалительного процесса, зуда, экземы и др. Однако часто врожденный ихтиоз также сопровождается дерматитом. Дерматозы имеют свои патогномоничные симптомы, отсутствующие при ихтиозе, например, зубы Гетчинсона при врожденном сифилисе, специфические папулы с излюбленной локализацией при псориазе и т. д. Приобретенные формы ихтиоза развиваются вследствие аутоиммунных, инфекционных заболеваний, опухолей и др., в этом случае нужно искать причину, способную вызвать патологию уже после рождения.
Лечение врожденного ихтиоза
Лечение заболевания проводится в стационаре, в случае тяжелых форм врожденного ихтиоза – в отделении реанимации. В помещении должна поддерживаться высокая влажность и пониженная температура воздуха. Обычно показана гипоаллергенная диета, в тяжелых случаях – питание через зонд. Рекомендуется принимать ванны от 2 раз в день. Это позволяет увлажнить кожу, уменьшить шелушение и провести профилактику вторичных инфекций. В случае эпидермолитического врожденного ихтиоза во время купания часто используются антисептики. После купания, как правило, проводят механическое отшелушивание с последующим нанесением увлажняющего крема.
Применяется системная терапия врожденного ихтиоза препаратами витамина А и ретиноидами, которые облегчают отшелушивание ороговевших клеток и снижают скорость пролиферации клеток, иными словами, тормозят их усиленный рост. Кроме того, ретиноиды оказывают противовоспалительное и иммуномодулирующее действие. В педиатрической практике в настоящее время используется тигазон, неотигазон. Очевидна высокая клиническая эффективность данных препаратов, однако эффект от лечения временный, а терапия проводится курсами ввиду множества побочных эффектов: сухость и кровоточивость слизистых, гиперостоз, нарушений функций печени, фотосенсибилизация кожи и высокая чувствительность к свету и др.
К современным препаратам относятся блокаторы метаболизма ретиноевой кислоты, например, лиарозол. При лечении отмечается тот же клинический эффект, но безопасность намного выше. Основу наружной терапии врожденного ихтиоза составляют кератолитики: растворы хлорида натрия и мочевины, декспантенол, салициловая кислота, топические ретиноиды. Средства наносятся на пораженные участки кожи и оказывают местное действие, способствуя отшелушиванию, смягчению кожи, уменьшению воспаления и др. При назначении кератолитиков необходимо учитывать возраст ребенка, поскольку некоторые из них (мочевина, салициловая кислота) токсичны для детей первого года жизни.
В лечении тяжелых форм врожденного ихтиоза применяются системные кортикостероиды, иммуноглобулины, а также антибиотики в случае необходимости. Обязательна консультация детского офтальмолога при диагностике эктропиона, детского оториноларинголога – при деформации и отсутствии ушной раковины, а также для диагностики и лечения нарушений слуха, в частности нейросенсорной тугоухости. При синдромальных формах врожденному ихтиозу часто сопутствуют неврологические нарушения, в этих случаях обязательна консультация детского невролога. Также к лечению подключается генетик для планирования последующих беременностей и расчета вероятности заболевания у будущих поколений.
Прогноз и профилактика врожденного ихтиоза
Прогноз зависит от формы заболевания. Клинические проявления простого ихтиоза минимизируются после 20-25 лет, однако качество жизни все равно снижается из-за наличия системных патологий желудочно-кишечного тракта. Тяжелые формы врожденного ихтиоза часто являются причиной смерти и детской инвалидности.
Генетическое консультирование – единственный способ профилактики врожденного ихтиоза. Необходимо планировать беременность в случае отягощенного анамнеза по данному заболеванию, то есть, если один и тем более оба родителя больны, либо кто-то из них является носителем мутации. В этом случае рекомендуется отказ от беременности, но в любом случае окончательно решение принимает семья. Как вариант, парам предлагается ЭКО и усыновление.
Х-сцепленный ихтиоз — это распространенный генодерматоз, который проявляется избыточным ороговением кожного покрова, образованием чешуек. Заболевание обусловлено мутацией гена стеролсульфатазы в женской половой хромосоме. Основные симптомы: плотные темные чешуйки на коже, поражение шеи, туловища, разгибательных поверхностей конечностей, начало болезни в младенческом возрасте. Диагностика базируется на дерматологическом осмотре и сборе семейного анамнеза, для уточнения проводятся биохимические, молекулярно-генетические, инструментальные методы. Больным назначается специальный уход за кожными покровами с применением кератолитиков, смягчающих компонентов, AHA/BHA кислот.
МКБ-10

Общие сведения
Ихтиоз рецессивный Х-сцепленный (ИРХС) относится к группе менделирующих (наследуемых по законам Менделя) нарушений кератинизации. Болезнь выделена в отдельную форму в 1960 году, занимает второе место в структуре всех видов ихтиоза, уступая только ichthyosis vulgaris, и регистрируется с частотой 1:2000-1:6000. Учитывая тип наследования, болеют преимущественно мужчины, а большинство женщин являются бессимптомными носителями пораженного гена. Патология не является опасной или смертельной, однако отличается высокой распространенностью, требует правильного поддерживающего лечения, что обуславливает ее актуальность в современной дерматологии.

Причины
Заболевание вызвано точечной мутацией в гене стероидной сульфатазы (STS), который расположен на коротком плече Х-хромосомы в локусе Xp22.3. Моногенная аномалия наследуется с помощью Х-сцепленного рецессивного механизма передачи: в браке матери, которая является здоровым носителем мутантного гена, со здоровым мужчиной в соответствии с законами Менделя 25% сыновей имеют вероятность родиться больными, 25% — здоровыми, 25% дочерей, вероятно, окажутся здоровыми, 25% — носителями мутантного гена.
Дети от брака здоровой женщины с больным мужчиной будут клинически здоровыми, однако все дочери окажутся носительницами сцепленного наследственного заболевания. Все сыновья женщины, больной наследственным гиперкератозом, и здорового мужчины родятся больными, а дочери — носительницами болезни. И, наконец, в крайне редких случаях, когда оба родителя страдают от ихтиоза, сцепленного с Х-хромосомой, все дети также будут больными.
Патогенез
Патологические кожные изменения вызваны нарушениями метаболизма липидов в эпидермальном слое. В норме в роговом слое присутствует фермент гидролаза (стеролсульфатаза), которая контролирует выработку стероидных сульфатов — холестерина сульфата CSO4, сульфатированных стероидных гормонов. Достаточный уровень этих веществ необходим для регулярного отшелушивания кератинизированных клеток, самообновления кожных покровов.
Для ихтиоза Х-сцепленного моногенного типа характерна недостаточность этого фермента, в результате чего в эпидермисе повышается уровень CSO4, угнетается активность эпидермальных стериновых протеаз. Такие изменения провоцируют ретенционный гиперкератоз: связи между ороговевшими клетками укрепляются, нарушается нормальный процесс десквамации кератиноцитов. Однако пролиферация кератиноцитов не нарушена.
Симптомы X-сцепленного ихтиоза
Клинические проявления ихтиоза возникают в первые месяцы жизни ребенка. На теле ребенка становятся заметными тонкие непигментированные чешуйки неправильной формы, которые слабо прилегают к коже, довольно легко удаляются при механическом воздействии. Спустя 3-4 месяца они приобретают сероватый или коричневый цвет, становясь похожими на грязь. При этом чешуйки прочно связываются с кожей, их не удается удалить во время гигиенических процедур.
Типичная локализация гиперкератоза: задняя поверхность шеи (симптом «грязной шеи»), локтевые суставы, наружная поверхность предплечий. Реже элементы генодерматоза наблюдаются на туловище, в подколенных ямках. Ладони, подошвы, лицо остаются неповрежденными. Кожа напоминает змеиный покров из-за трещин, неравномерной окраски чешуек. Активность Х-сцепленного ихтиоза зависит от сезона: заболевание обостряется в холодное время года, при повышенной влажности воздуха.
Осложнения
Изолированные кожные проявления гиперкератоза дают негативные последствия в виде косметического дефекта. Ряд пациентов испытывают психологический дискомфорт, трудности с социализацией. Более серьезными являются внекожные осложнения Х-сцепленного ихтиоза: помутнение роговицы, СДВГ — синдром дефицита внимания и гиперактивности (40% больных), расстройства аутистического спектра (25%), крипторхизм (20%). Редко патология сопровождается аносмией, односторонней аплазией почек.
Диагностика
Обследование пациента у врача-дерматолога начинается со стандартного осмотра кожной поверхности для обнаружения типичных элементов ретенционного гиперкератоза. Заподозрить заболевание можно по наличию «грязной кожи шеи», чистой поверхности кожи подошв и ладоней, выявлению подобных изменений у других членов семьи. Чтобы подтвердить диагноз, используются лабораторно-инструментальные методики:
- Биохимические исследования. Чтобы дифференцировать Х-сцепленный вариант от вульгарного ихтиоза, проводится электрофорез сывороточных протеинов, исследование активности STS в лейкоцитах или клетках кожи.
- Генетическое тестирование. При затруднениях в диагностике рекомендовано ПЦР-исследование, флуоресцентная гибридизация, чтобы выявить мутацию гена на Х-хромосоме.
- Визуализация структуры кожи. Гистология и электронная микроскопия пораженных участков кожного покрова необходимы для дифференциальной диагностики наследственных дерматозов.
В семьях с отягощенной наследственностью возможно пренатальное обследование для исключения Х-сцепленного ихтиоза. Заподозрить патологию удается по снижению уровня материнского эстрадиола. Для верификации диагноза назначаются инвазивные диагностические методы (амниоцентез, биопсия ворсин хориона). Полученный биоматериал исследуется в лаборатории для подтверждения недостаточности стеролсульфатазы.
Лечение Х-сцепленного ихтиоза
Этиотропная терапия Х-сцепленного гиперкератоза отсутствует. Основная задача — подбор правильных средств по уходу за кожей, которые уменьшают интенсивность субъективной симптоматики, угнетают процессы ороговения, улучшают внешний вид кожного покрова. В комплексной терапии ихтиоза применяются средства со следующими активными компонентами:
- Кератолитики. Зачастую назначаются пропиленгликоль и мочевина в разных лекарственных формах, которые удаляют избыток ороговевших чешуек, делают кожные покровы более гладкими.
- КислотыAHA иBHA. Уходовая косметика с кислотами (салициловой, молочной, гликолевой) регулирует уровень кератинизации, усиливает отшелушивание ороговевших частиц, поддерживает нормальный уровень гидратации кожных покровов.
- Глицерин. Компонент должен постоянно присутствовать в косметике для пациентов с ихтиозом, поскольку он смягчает кожу после кератолитиков и кислотных агентов, устраняет ощущения сухости и дискомфорта.
- Ретиноиды. Препараты наружного применения рекомендуются по показаниям взрослым больным в зимние месяцы, чтобы предупредить обострение ихтиоза, нормализовать процессы регенерации кожи.
- Средства, содержащиеSPF. Фильтры, блокирующие УФ-лучи, являются обязательными составляющими при использовании кислот, ретиноидов. Солнцезащитные средства предупреждают появление гиперпигментации, препятствуют фотостарению кожи.
Прогноз и профилактика
Для Х-сцепленного типа болезни характерно доброкачественное течение, хотя с возрастом, в отличие от простого ихтиоза, число элементов дерматоза не уменьшается. Прогноз благоприятный при правильном подборе ухода, соблюдении больным всех рекомендаций дерматолога. При наличии внекожных симптомов заболевания прогноз определяется их степенью тяжести. Основу профилактики гиперкератоза, сцепленного с женской половой хромосомой, обеспечивается медико-генетическое консультирование пар, в семейной истории которых были случаи ихтиоза.
1. Х-сцепленный ихтиоз (клинический случай)/ М.В. Яндутова, А.Ю. Епифанова, А.В. Каракаева, А.А. Моисеев// Саратовский научно-медицинский журнал. — 2020. — №3.
2. Рецессивный Х-сцепленный ихтиоз/ Ф.Б. Бассе, В.Н. Гребенюк, Н.Ф. Заторская, С.О. Пилявская// Клиническая дерматология и венерология. — 2019. - №1.
3. Х-сцепленный ихтиоз/ В.Н. Терещенко, Н.Е. Карпылаева, М.В. Рябкова, О.Ю. Шевелева// Российский журнал кожных и венерических болезней. — 2013. - №1.
Читайте также:

