Паста лассара при розацеа
Обновлено: 24.04.2024
Розацеа – хроническое воспалительное заболевание с распространенностью от 0,5% до 18%. Розацеа чаще встречается у лиц северного и западноевропейского происхождения, реже в других этнических группах. По некоторым данным, около 4% пациентов с розацеа имеют
Abstract. Rosacea is a chronic inflammatory disease with a prevalence of 0.5% to 18%. Rosacea is more common in people of northern and Western European origin, less common in other ethnic groups. According to some data, about 4% of rosacea patients are of African, Latin American or Asian origin. Women are found on average a third more than men. Rosacea usually manifests in patients aged 30-50 years. However, it can occur in childhood with a family history of rosacea, persist and progress into adulthood. Rosacea is chronic, can develop from erythema, telangiectasia to rhinophyma, and also cause eye damage. The classification of rosacea includes four subtypes and a variant of granulomatous rosacea. Adverse trigger factors of rosacea are endocrinological, pharmacological, immunological, infectious, climatic, thermal and alimentary factors. Skin with rosacea is most sensitive to temperature changes, especially to heat. Clinical trigger factors that contribute to rosacea outbreaks or disease progression are associated with increased stress of the endoplasmic reticulum, which indicates a birth defect predisposed rosacea patients to increased stress of the endoplasmic reticulum and pathologies associated with it. Numerous factors are involved in the pathogenesis of rosacea, such as impaired barrier function of the epidermis, inflammation mediated by cathelicidin antimicrobial peptide, vascular reactivity disorders, increased innate immunity, neurogenic inflammation, angiogenesis, fibrosis and hypercolonization of demodex mites. Rosacea requires an interdisciplinary approach consisting of adequate general measures, local and/or systemic therapy, physical methods for the targeted treatment of various symptoms. The choice of treatment method depends primarily on the severity of the disease and varies from avoiding factors that can provoke an exacerbation of the disease to the use of surgical intervention to correct hypertrophied soft tissues of the nose (rhinophymes). Prevention of factors provoking rosacea and proper skin care such as sunscreens and moisturizers are important steps in the treatment and prevention of rosacea patients. For citation: Ayupova K. R., Yusupova L. A. The current state of the rosacea problem // Lechaschi Vrach. 2022; 5-6 (25): 30-33. DOI: 10.51793/OS.2022.25.6.005
Резюме. Розацеа – хроническое воспалительное заболевание с распространенностью от 0,5% до 18%. Розацеа чаще встречается у лиц северного и западноевропейского происхождения, реже в других этнических группах. По некоторым данным, около 4% пациентов с розацеа имеют африканское, латиноамериканское или азиатское происхождение. Женщин встречается в среднем на треть больше, чем мужчин. Розацеа обычно возникает у пациентов в возрасте 30-50 лет, однако может встречаться у детей с семейным анамнезом розацеа, сохраняясь и прогрессируя во взрослом возрасте. Розацеа протекает хронически, может развиваться в разных формах – от эритемы и телеангиэктазии до ринофимы, а также вызывать поражение глаз. Классификация розацеа включает четыре подтипа и вариант гранулематозной розацеа. Неблагоприятными тригерными факторами розацеа являются эндокринологические, фармакологические, иммунологические, инфекционные, климатические, термические и алиментарные. Кожа с проявлениями розацеа наиболее чувствительна к перепадам температуры, особенно к жаре. Клинические триггерные факторы, которые способствуют вспышкам розацеа или прогрессированию заболевания, связаны с усиленным стрессом эндоплазматического ретикулума, что указывает на врожденный дефект у пациентов, предрасположенных к розацеа, к повышенному стрессу эндоплазматического ретикулума и патологиям, связанных с ним. В патогенезе розацеа участвуют многочисленные факторы, такие как нарушение барьерной функции эпидермиса, воспаление, опосредованное кателицидиновым антимикробным пептидом, нарушения сосудистой реактивности, усиление врожденного иммунитета, нейрогенное воспаление, ангиогенез, фиброз и гиперколонизация клещами демодекса. Розацеа требует междисциплинарного подхода, состоящего из адекватных общих мер, местной и/или системной терапии, физиотерапевтических методов для целенаправленного лечения различных симптомов. Выбор метода лечения зависит в первую очередь от тяжести заболевания и варьирует от избегания факторов, способных спровоцировать обострение заболевания, до применения хирургического вмешательства с целью коррекции гипертрофированных мягких тканей носа (ринофимы). Предотвращение факторов, провоцирующих розацеа, и надлежащий уход за кожей (солнцезащитные кремы и увлажняющие средства) являются важными этапами лечения и профилактики пациентов розацеа.
Розацеа является наиболее распространенным хроническим воспалительным дерматозом, развивающимся под влиянием генетических и средовых факторов, характеризующимся выраженным поражением центральной части лица с преходящей или персистирующей эритемой, воспалительными папулами, пустулами, телеангиэктазиями и гиперплазией соединительной ткани [1, 2]. Распространенность заболеваемости во всем мире достигает 18%, особенно в популяциях с преобладающим кельтским типом, как, например, в Ирландии [3]. Женщины и мужчины страдают в равной степени. В то же время имеются данные о том, что женщины страдают этим заболеванием чаще, чем мужчины, однако у последних в большей степени наблюдаются фиматозные изменения, особенно ринофима [4, 5]. В более молодом возрасте часто первыми признаками заболевания являются гиперемия и эритема, а телеангиэктазии в качестве начальных очагов розацеа наблюдаются в более старшем возрасте [6]. У ряда пациентов розацеа усиливается инвазией демодекса, эрадикация которого облегчает симптомы розацеа, вероятно, предотвращая образование провоспалительных цитокинов [7]. Нередко может осложняться вторичной инфекцией. Пиодермия считается самым часто встречаемым дерматозом среди всех кожных болезней [8]. При центрально-лицевой локализации розацеа часто встречающимся тяжелые психосоциальные симптомы, включая снижение самооценки и проблемы в общении. Недавние эпидемиологические исследования подтверждают эти клинические наблюдения и свидетельствуют о значительном психологическом бремени и снижении качества жизни пациентов с розацеа [9, 10].
Факторы, участвующие в патофизиологии розацеа, включают повышенную активность сальных желез на лице, а также нарушения нервной и сосудистой реакции на раздражители. Многочисленные триггеры (ультрафиолетовые лучи, жара, острая пища и алкоголь) инициируют или усугубляют клинические проявления розацеа [7]. Светлокожие люди кельтского или североевропейского происхождения генетически предрасположены к розацеа. У пациентов с генетической предрасположенностью имеется рецептор, опосредующий неоваскулярную регуляцию. При воздействии триггеров происходит высвобождение нейропептидов, что приводит к рекрутированию провоспалительных клеток в кожу с развитием гиперемии и отека [7].
Розацеа может быть инициирована или усугублена различными эндогенными и экзогенными триггерными факторами, включая жару, сильный холод, ультрафиолетовое облучение. Развивается гелиодермический статус, который включает все варианты изменений кожи, связанных с инсоляцией (клинические, гистологические и функциональные проявления хронического облучения кожи) [4, 11]. Нередко к неблагоприятным факторам относится сухость кожи, сопровождающаяся гиперчувствительностью и повышенной раздражительностью к воздействию экзогенных факторов [12]. В целом на индивидуальные клинические проявления розацеа влияют особая триггерная констелляция и восприимчивость пациента.
Классификация розацеа учитывает важность каждого проявления заболевания и позволяет дифференцировать основные и вторичные симптомы. Фиматозные изменения и стойкая центрально-лицевая эритема признаны единственными диагностическими признаками розацеа, тогда как покраснение, телеангиэктазии и воспалительные папулы/пустулы считаются основными симптомами и только в сочетании заставляют предполагать диагноз розацеа. Жгучая боль, отек и сухость определяются как вторичные признаки розацеа. Кожа при этой патологии характеризуется дисрегуляцией воспалительных, сосудистых, лимфатических, железистых и фиброзных процессов, что отражает многофакторный патогенез кожного заболевания [4]. Сухость кожи визуализируется у женщин, сопровождаясь повышенной чувствительностью к внешним воздействиям, постоянным присутствием нестойкой эритемы и других проявлений розацеа [13].
Адаптивная иммунная система наряду с врожденной может играть центральную роль в патофизиологии розацеа. В инфильтрате циркулируют CD4+ лифоциты, превалируют Т-хелперы 1-го и 17-го типа [14].
Генетические признаки, лежащие в основе розацеа, выражаются в семейном анамнезе. Несколько общегеномных ассоциативных исследований предлагают генетические локусы риска развития розацеа. В одной из этих работ, включавшей лиц европейского происхождения, выявлены однонуклеотидные полиморфизмы в генах бутирофилиноподобного 2 (BTNL2) и человеческого лейкоцитарного антигена (DRA). Оба гена связаны с основным комплексом гистосовместимости приобретенного иммунитета, что указывает на центральную роль дисрегуляций иммунной системы в патогенезе розацеа. В другом исследовании обнаружен нулевой мутационный полиморфизм в гене глутатион S-трансферазы (GST), который кодирует фермент, участвующий в клеточном окислительном стрессе. В клиническом исследовании пациента с гранулематозной розацеа зафиксирован полиморфизм в гене белка 2, содержащего домен олигомеризации, связывающий нуклеотиды (NOD2), который функционирует как белок рекрутирования каспазы (CARD15) и связан с функцией рецепторов врожденного иммунитета, таких как толл-подобные рецепторы 2 (TLR2), и последующими воспалительными процессами. Недавнее популяционное исследование показало, что розацеа имеет общие генетические локусы риска с различными аутоиммунными заболеваниями (рассеянный склероз, сахарный диабет 1 типа, целиакия и ревматоидный артрит). Это наблюдение подчеркивает важность тщательной оценки риска для отдельного пациента с розацеа, подверженного опасности развития аутоиммунного расстройства [4, 15].
Розацеа диагностируется на основании сооответствующего анамнеза и физического обследования, а также наличия симптомов со стороны центральной части лица (нестойкая эритема лица, телеангиэктазии или папулы/пустулы) [16].
Розацеа следует дифференцировать от вульгарных акне у взрослых, себорейного, контактного и фотодерматита. Следует также отличать ее от эксфолиативного дерматита, при котором эритематозная кожа повсеместно утолщена. Эритродермия может возникать спонтанно или развиться в течение нескольких месяцев. Быстрое развитие эксфолиативного дерматита в качестве более вероятной причины может требовать более активной лекарственной терапии [17]. Менее распространенные заболевания, с которыми нужно проводить дифференциальную диагностику, включают системную красную волчанку, атопический дерматит, фолликулит, бромодермию и мастоцитоз.
Последующее соблюдение рекомендаций по адекватному нераздражающему уходу за кожей может в значительной степени предотвратить обострение розацеа и улучшить качество жизни пациента. Рекомендации по уходу за кожей состоят главным образом в избегании триггерных факторов (включая управление стрессом), использовании солнцезащитного крема (с фактором защиты от солнца 30+), применении увлажняющих средств для сухой кожи и сушащих – для жирной, а также нежном очищении всего лица. Пациентам следует избегать вяжущих и тонизирующих средств, сенсорных стимуляторов и потенциально раздражающих ингредиентов [5, 18].
Поскольку симптомы розацеа развиваются из различных патофизиологических причин, терапевтический режим в большинстве случаев будет состоять из комбинаций топических препаратов с системной или физиотерапией или из того и другого [19, 20].
При эритематозной розацеа некоторые виды лазерной терапии могут быть использованы, но их следует избегать у пациентов, чувствительных к боли. Применение бета-блокаторов, таких как карведилол или модуляторы адренергических рецепторов (например, бримонидин), может облегчить симптомы. При наличии боли может быть полезна анальгетическая терапия.
Существует лишь несколько вариантов лечения телеангиэктазии, среди которых наиболее часто используются физическая лазерная терапия и внутрисосудистые инъекции Этоксисклерола (0,5-1%).
Пациенты с папулами легкой и средней степени тяжести получают местное лечение ивермектином (1%), метронидазолом (1%), азелаиновой кислотой (15%) или сульфацетамидом натрия. Терапия с использованием местного эритромицина (2%), изотретиноина, клиндамицина, перметрина, доксициклина, миноциклина и перорального эритромицина также показала хорошие результаты. Комбинированная терапия часто помогает продлить периоды без симптомов. В тяжелых или рефрактерных к терапии случаях может проводиться системное лечение метронидазолом, кларитромицином и азитромицином. При обнаружении демодекса перметрин или крем ивермектина и пероральный ивермектин могут улучшить терапевтический результат [21].
Фиматозная розацеа, как правило, трудно поддается лечению. Наилучшие результаты достигаются при его раннем начале. Пероральный изотретиноин может быть эффективен в уменьшении объема носа на ранних стадиях заболевания; однако после прекращения приема препарата вероятен рецидив, а муцинозные и фиброзные изменения не реагируют на прием ретинодов. Хирургические методы, включая лазерную или световую терапию (импульсный красящий лазер, интенсивный импульсный свет, лазер на углекислом газе), электрохирургию, дермабразию, тангенциальное иссечение, электроскальпель, петлевую каутеризацию, эффективны в коррекции или минимизации физиологических изменений и могут повысить качество жизни пациентов. Криотерапия оказывает противовоспалительное, сосудосуживающее, антидемодекозное действие и показана пациентам независимо от стадии заболевания [22, 23].
Таким образом, розацеа является распространенным хроническим заболеванием кожи лица. Достижения последних лет меняют понимание розацеа как с точки зрения патофизиологии, так и с точки зрения клинического подхода к терапии, позволяя применять новые препараты, которые улучшают результаты лечения пациентов и снижают заболеваемость. Комбинированная терапия может обеспечить удовлетворительные результаты при лечении пациентов с розацеа, а систематические профилактические мероприятия позволяют достичь стойкой ремисии и улучшить качество жизни больных.
КОНФЛИКТ ИНТЕРЕСОВ. Авторы статьи подтвердили отсутствие конфликта интересов, о котором необходимо сообщить.
CONFLICT OF INTERESTS. Not declared.
Литература/References
Казанская государственная медицинская академия – филиал федерального государственного бюджетного образовательного учреждения дополнительного профессионального образования Российская медицинская академия непрерывного профессионального образования Министерства здравоохранения Российской Федерации; 420012, Россия, Казань, ул. Толстого, 4 А
Сведения об авторах:
Information about the authors:
Современное состояние проблемы розацеа/ К. Р. Аюпова, Л. А. Юсупова
Для цитирования: Аюпова К. Р., Юсупова Л. А. Современное состояние проблемы розацеа // Лечащий Врач. 2022; 5-6 (25): 30-33. DOI: 10.51793/OS.2022.25.6.005
Теги: кожа, дерматоз, эритема, ринофима
Сайт предоставляет справочную информацию исключительно для ознакомления. Диагностику и лечение заболеваний нужно проходить под наблюдением специалиста. У всех препаратов имеются противопоказания. Консультация специалиста обязательна!
Для чего нужна салицилово-цинковая паста (салицило-цинковая мазь, паста Лассара): применение, инструкция, цена, отзывы
Состав препарата
Салицилово-цинковая паста, которую нередко неправильно называют салицило-цинковой мазью, представляет собой сочетание цинковой пасты с салициловой кислотой. Таким образом, препарат содержит 25% оксида цинка, 25% крахмала (сухое вещество цинковой пасты), 2% салициловой кислоты и 48% вазелина.
Препарат имеет вид густой белой однородной массы и выпускается в плотно закупоренных пластиковыми крышками стеклянных банках темного стекла.
Салициловая кислота значительно усиливает противовоспалительные свойства цинковой пасты. Поэтому салицилово-цинковая паста более эффективна при поражениях кожи, протекающих с выраженной воспалительной реакцией.
Показания и противопоказания
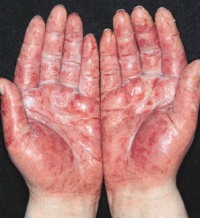
В целом, сфера применения салицилово-цинковой пасты такая же как и цинковой пасты. В частности, данный препарат с успехом используют при дерматитах (себорейном, атопическом, контактном и др.), экземе, псориазе.
- язвенная болезнь желудка и двенадцатиперстной кишки;
- нарушения выделительной функции почек;
- заболевания, протекающие со снижением свертываемости крови;
- геморрагический диатез и другие состояния, характеризующиеся повышенной ломкостью капилляров;
- выраженное малокровие.
Применение при беременности
В отличие от цинковой мази и пасты, препарат салицилово-цинковая паста при беременности использовать нельзя.
Можно ли применять препарат салицилово-цинковая паста (мазь) для лечения детей и новорожденных
Поскольку в состав препарата салицилово-цинковая паста входит салициловая кислота, данное лекарственное средство имеет ограничения по возрасту.
Пасту Лассара не используют для лечения новорожденных и детей в возрасте до двенадцати лет.
Как пользоваться салицилово-цинковой пастой
Салицилово-цинковую пасту наносят тонким слоем на поврежденные участки кожи 1-2 раза в сутки.
Следует соблюдать осторожность, поскольку при смазывании обширных участков мокнущей поверхности салициловая кислота может попадать в общий кровоток и оказывать системное действие.
Побочные эффекты
При длительном бесконтрольном использовании саилицилово цинковой пасты возможно развитие таких побочных эффектов как потливость, головокружение, нарушение работы слухового анализатора (шум в ушах, снижение слуха).
В случае передозировки, которая чаще всего происходит при смазывании обширных поверхностей поврежденного кожного покрова, могут возникнуть такие тяжелые осложнения, как нарушение деятельности печени и почек, судороги, появление геморрагической сыпи на теле в результате повышения ломкости капилляров.
Где купить?
Препарат салицилово-цинковая паста можно приобрести практически в любой аптеке. Данное лекарственное средство разрешено отпускать без рецепта врача.
Цена салицилово-цинковой пасты невысока (стоимость препарата в аптеках Москвы в среднем около 25 рублей).
Салицилово-цинковая паста (мазь) от прыщей и черных точек (отзывы пациентов и рекомендации врачей)
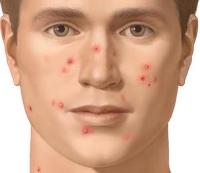
Как свидетельствуют многочисленные отзывы, пациенты с проблемной кожей используют салицилово-цинковую пасту против прыщей (угрей) и так называемых "черных точек".
Врачи-дерматологи утверждают, что данный препарат действительно весьма эффективен в борьбе с себорейным дерматитом, поскольку оказывает выраженное противовоспалительное, обезболивающее, подсушивающее и обеззараживающее действие.
Однако в основе развития себорейного дерматита лежат глубокие нарушения обмена веществ, вызванные нарушением гормонального фона (именно поэтому заболевание чаще всего развивается в переходном возрасте).
Поэтому местного лечения нередко бывает недостаточно для избавления от патологии. При среднетяжелой и тяжелой форме показана коррекция гормонального фона при помощи специальных препаратов, которые может назначить только врач-специалист.
Кроме того, даже в случае легкого течения себорейного дерматита возможно присоединение бактериальной инфекции. В таких случаях необходимо дополтнительное использование антибактериальных средств, поскольку антисептического действия салицилово-цинковой пасты недостаточно для подавления острого инфекционного процесса.
Косметологи не рекомендуют пациентам практиковать самостоятельное удаление "черных точек", которые представляют собой закупоренные протоки сальных желез – комедоны. Такого рода действия могут значительно усугубить течение заболевания.
Так что для лечения проблемной кожи лучше всего обратиться к специалисту – дерматологу или косметологу.
Салицилово-цинковая паста (мазь) при псориазе (отзывы пациентов и рекомендации врачей)
На форумах, посвященных проблемам лечения такого тяжелого кожного заболевания, как псориаз, можно встретить позитивные отзывы об использовании салицилово-цинковой пасты для борьбы с патологическими высыпаниями.
И это неудивительно, поскольку базовыми препаратами для местного лечения псориаза являются лекарственные средства, содержащие 2% концентрацию салициловой кислоты.
Псориаз – хронически протекающее поражение кожи, характеризующееся появлением специфических высыпаний, в основе развития которых лежит повышенная пролиферация эпителиальных клеток в сочетании с нарушением процесса их ороговения и возникновение выраженной воспалительной реакции.
Однако выбор медикаментов осуществляется врачом в зависимости от активности процесса. При этом могут понадобиться более сильные противовоспалительные препараты, сочетающие салициловую кислоту и глюкокортикоиды (гормональные противовоспалительные средства).
Кроме того, следует учитывать, что псориаз является заболеванием всего организма, а ведущую роль в развитии патологии играет нарушение функции иммунной системы. Поэтому лечение псориаза требует комплексного подхода.
Так что любая местная терапия, в том числе и применение салицилово-цинковой пасты, должна проводиться по рекомендации и под наблюдением врача-дерматолога в сочетании с другими оздоравливающими мероприятиями.
Подробнее о псориазе
Салицилово-цинковая паста (мазь): способ применения от герпеса на губах (отзывы пациентов и рекомендации врачей)
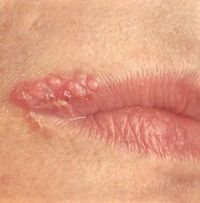
Как свидетельствуют многочисленные отзывы, пациенты с успехом используют салицилово-цинковую мазь против герпетических высыпаний на губах.
Действительно, входящая в состав препарата салициловая кислота обладает мощным противовоспалительным и обезболивающим действием, так что салицилово-цинковая паста по эффективности намного превосходит обычную цинковую пасту или мазь.
Однако следует учитывать, что нежность кожи и обилие сосудов губной каймы способствуют всасыванию компонентов салицилово-цинковой пасты в кровь. Так что данный препарат может оказывать системное действие и привести к развитию неблагоприятных побочных эффектов.
Вместе с тем, салицилово-цинковая паста не влияет на продолжительность периода высыпаний, поскольку не оказывает влияния на вирус герпеса как причину заболевания. Поэтому прежде чем использовать данный препарат, следует подумать, стоит ли подвергать свое здоровье излишнему риску.
Кроме того, салицилово-цинковая паста имеет сильно выраженные адсорбирующие свойства и может сильно пересушивать нежную кожу губ. Так что для скорейшего исчезновения патологических элементов герпеса лучше использовать обычную цинковую мазь, а для лечения герпеса – противовирусные препараты (Зовиракс и др.).
Применение препарата салицилово-цинковая паста (мазь) в косметологии от пота и пигментных пятен (отзывы пациентов и рекомендации врачей)
Поскольку салицилово-цинковая паста является дешевым препаратом, который можно купить в любой аптеке без рецепта врача, многие пациенты считают ее абсолютно безвредной и экспериментируют в свое удовольствие.
Примером такого рода экспериментов является использование салицилово-цинковой пасты в косметологии в качестве отбеливающего средства и против излишней потливости.
Сразу следует отметить, что салицилово-цинковая паста действительно может помочь в подобных ситуациях. Однако ее действие в этом отношении будет значительно слабее действия препаратов, которые предлагает современная косметология.
Даже самое, казалось бы, безобидное лекарственное средство может принести весьма ощутимый вред здоровью, если вы будете использовать его не по назначению.
Между тем салицилово-цинковая паста имеет свои противопоказания по возрасту (запрещена к применению детям до 12 лет), по физиологическому статусу (не рекомендуется для беременных женщин) и по состоянию здоровья (противопоказана пациентам с язвенной болезнью желудочно-кишечного тракта, при повышенной ломкости сосудов и склонности к кровоточивости и др.).
Иными словами, салицилово-цинковая паста является достаточно серьезным лечебным препаратом, который следует использовать по назначению, а для уничтожения пигментных пятен и против повышенной потливости целесообразнее применять специально предназначенные для этого средства.
Серная салициловая цинковая (салицилово-серно-цинковая) паста (мазь) от подкожных прыщей (розацеа)
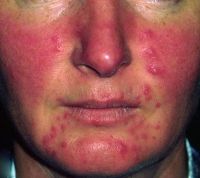
Розацеа или розовые угри (подкожные прыщи) – хронически рецидивирующее поражение кожи, которое вызывается клещом рода демодекс у подверженных к развитию данного заболевания пациентов.
В отличие от обыкновенных или вульгарных угрей, розовые угри чаще всего появляются у женщин в возрасте около 40 лет. При этом угревидные высыпания характеризуются отсутствием черных точек (комедоны) и визуально более глубоким расположением прыщей на воспаленной утолщенной коже.
Для лечения розовых угрей используют медикаменты, сочетающие противопаразитарное (уничтожающее клеща демодекс), антисептическое (обеззараживающее), противовоспалительное и подсушивающее действие.
К такого рода препаратам относится салицилово-серно-цинковая паста, которую нередко неправильно называют мазью. Данное лекарственное средство продается во флаконах темного стекла по 50 и 100 г. В состав пасты входят 0.6 г салициловой кислоты и 5 г серы на каждые 20 г цинковой пасты.
При розацеа подкожные прыщи смазывают салицилово-серно-цинковой пастой один раз в сутки (как правило, на ночь). Сера уничтожает клещей рода демодекс и, вступая в реакцию с органическими веществами, образует сульфиды, обладающие противомикробным и противовоспалительным действием.
Салициловая кислота снимает зуд, боль и воспалительную реакцию, а оксид цинка подсушивает высыпания, способствуя их скорейшему заживлению.
Необходимо учитывать, что розацеа склонно к упорно рецидивирующему течению, поэтому лечение должно быть комплексным и включать диету (отказ от спиртных напитков, горячих и острых блюд), терапию сопутствующих заболеваний, которые могут провоцировать появление розовых угрей (нарушение гормонального фона, хеликобактериоз, патология печени и мочеполовой системы), общеоздоравливающие процедуры.
Для полного исцеления от розацеа, как правило, необходим достаточно продолжительный период лечения (месяцы или даже годы), во время которого пациенты успевают сменить несколько препаратов. Для повышения эффективности терапии и исключения неприятных побочных эффектов лучше всего проводить лечение под наблюдением врача-дерматолога.
Следует отметить, что салицилово-серно-цинковая паста также рекомендована к использованию при обычных угрях (себорейный дерматит) и псориазе. Беременность и детский возраст (до 12 лет), язвенные поражения желудочно-кишечного тракта, повышенная ломкость сосудов и склонность к кровоточивости являются противопоказаниями к назначению препарата.
Подробнее о розацеа
Что лечит цинково-ихтиоловая (цинковая ихтиоловая, цинко-ихтиоловая) паста (мазь)
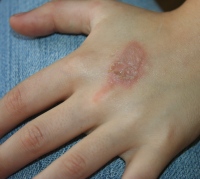
Цинко-ихтиоловая паста, которую "в народе" нередко неправильно называют цинково-ихтиоловой или цинковой ихтиоловой мазью, представляет собой комбинированный препарат, в 100 г которого содержится 24.4 г окиси цинка, 2.5 г ихтиола и основа пасты, состоящая из крахмала (24.4 г) и вазелина (48.8 г).
Таким образом, по сути, цинко-ихтиловая паста – это цинковая паста с добавлением ихтиола. Последней компонент является аммониевой солью сульфокислот сланцевого масла и содержит около 10.5% серы, связанной с органическими веществами.
Ихтиол обладает противовоспалительным, местноанестезирующим (снимает боль и зуд в пораженной области) и слабым обеззараживающим эффектом.
Сфера применения цинко-ихтиоловой пасты такая же, как цинковой пасты без ихтиола – ожоги, рожистое воспаление, экзема, дерматиты различного происхождения (в том числе, себорейный, контактный и аллергический).
В сети есть отзывы об успешном использовании цинково-ихтиоловой пасты при псориазе. Однако по эффективности данный препарат значительно уступает пастам, содержащим салициловую кислоту (салицилово-цинковая паста и препараты, содержащие салициловую кислоту в комбинации с гормональными противовоспалительными лекарственными средствами).
Некоторые пациентки используют цинково-ихтиоловую пасту против розовых угрей (розацеа), однако по эффективности данный препарат уступает другим медикаментам местного действия, оказывающим более выраженный акарицидный (противоклещевой) эффект, таким как салицилово-серно-цинковая паста, паста Ям, бензилбензоат и другие.
Преимуществами цинково-ихтиоловой пасты является ее абсолютная безвредность – побочные эффекты в виде непереносимости отдельных компонентов препарата встречаются крайне редко.
К негативным особенностям препарата следует отнести сильный специфичный запах, который придает пасте содержащийся в ней ихитол.
Для чего применяется борно-серная цинковая мазь
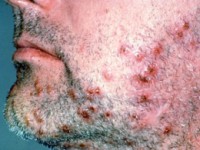
Борно-серная цинковая мазь представляет собой смесь трех лекарственных средств, зафиксированных в ее названии. Препарат содержит по 15 грамм цинковой и серной мази на каждые 0.6 грамма борной кислоты.
В отличие от других препаратов на цинковой основе, борно-серная цинковая мазь отличается более выраженным обеззараживающим эффектом за счет содержания антисептика – борной кислоты.
Поэтому данное лекарственное средство с успехом используют при поверхностных поражениях кожи осложненных инфекционным процессом, в том числе при сикозе (вызванном стафилококком хронически протекающем воспалении волосяных фолликулов).
Сера усиливает как обеззараживающие, так и противовоспалительные свойства препарата, так что борно-серная цинковая мазь может оказаться более эффективной при экземе, дерматитах (контактном, аллергическом, себорейном), потертостях и других легких поражениях кожи.
Вместе с тем, наличие в составе препарата борной кислоты ограничивает ее использование. Борно-серная цинковая мазь противопоказана при беременности и кормлении грудью, ее также не назначают детям и пациентам с тяжелой патологией мочевыделительной системы.
При использовании данного препарата необходимо соблюдать осторожность, не рекомендуется применять мазь для обработки обширных поверхностей кожи и слизистых оболочек, поскольку борная кислота может попасть в системный кровоток и вызвать симптомы отравления, такие как: тошнота, рвота, понос, головокружение, а в тяжелых случаях – нарушение сознания, судороги, почечная недостаточность, и даже шок.
Кроме того, при длительном бесконтрольном использовании борно-серная цинковая мазь может вызвать десквамацию эпителия (отторжение поверхностного слоя кожи). Поэтому мазь следует накладывать на небольшие поверхности один раз в сутки, а лечение проводить по рекомендации и под наблюдением врача.
Описаны подходы к лечению розацеа с использованием различных лекарственных средств и методов терапии, эффективность которых находится в прямой зависимости от длительности терапии и степени выраженности побочных эффектов. В этой связи лазеры и устройства с
Approaches to rosacea treatment were described, using different medications and therapeutic methods, whose efficiency directly depends on the therapy duration and degree of side effects intensity. In this connection lasers and devices with sources of light is the best choice.
.jpg)
Многочисленные способы лечения розацеа определяются разнообразием этиологических и патогенетических факторов, стадией, многообразием клинических форм заболевания. Терапия больных розацеа представляет трудную задачу, так как использование любого из предлагаемых в настоящее время методов лечения в виде монотерапии не приводит к полному выздоровлению, а оказывает лишь временный эффект. Наличие неясных до настоящего времени многих сторон этиологии и патогенеза розацеа, отсутствие надежных методов лечения делают проблему разработки новых подходов к терапии данной патологии крайне актуальной для современной дерматологии.
Терапевтическое действие одних средств направлено на редукцию воспалительных явлений, других — на коррекцию различных соматических нарушений со стороны пищеварительного тракта, центральной нервной системы, сосудистых реакций и т. д. [1]. Основное лечение предполагает устранение предрасполагающих и провоцирующих факторов, соблюдение диеты, фотопротекцию [2].
Классическая общая терапия розацеа включает антибиотики, метронидазол и наружную терапию. В период выраженного обострения присоединяют антигистаминные препараты. Однако до сих пор базисной терапией розацеа являются антибиотики, при этом тетрациклины остаются самыми эффективными антибактериальными препаратами в терапии данного дерматоза [3–6]. Лечение тетрациклинами, как правило, длительное — до 12 недель [3], что, несомненно, влечет за собой формирование побочных эффектов, таких как развитие кандидоза, нарушения пигментации кожи и зубов. В настоящее время используют антибиотики из группы макролидов — эритромицин, кларитромицин, джозамицин и т. д. [3, 7, 8].
Несмотря на спорный вопрос об этиологической роли Demodex folliculorum в патогенезе розацеа, прием метронидазола внутрь является неотъемлемой частью терапии розацеа [9]. Пероральное лечение метронидазолом составляет 4–6 недель, у некоторых больных до 8 недель, что также провоцирует побочные явления: тошноту, головные боли, сухость во рту, рвоту, крапивницу и т. д. Эффективной альтернативой является метронидазол в виде 1% геля, применяемого наружно [3, 4, 7, 10]. Хотя в отечественной дерматологии эти препараты широко назначаются в терапии розацеа, Управление по контролю качества пищевых продуктов и лекарственных средств (FDA, the Food and Drug Administration) в США их применение не санкционировало. Считается, что Demodex spp. выживают в условиях даже высоких концентраций метронидазола [11].
Развитие устойчивости бактериально-паразитарной флоры к препаратам имидазольной группы и антибиотикам тетрациклинового ряда приводит к необходимости совершенствования методов лечения и поиска новых лекарственных средств. В последнее время для лечения тяжелых форм розацеа применяют синтетические ретиноиды. Высокая терапевтическая эффективность препарата связана с влиянием на процессы дифференцировки и кератинизации клеток эпидермиса и сальных желез. Длительность лечения изотретиноином в среднем составляет 4–6 месяцев [12]. Данный препарат обладает побочными эффектами, главный из которых — тератогенное действие. Местное использование синтетических ретиноидов исключает развитие их системных побочных явлений, однако также вызывает сухость кожного покрова, шелушение, зуд [3–7, 11, 13]. Последние исследования указали на увеличение длительности ремиссии на 20% у пациентов с розацеа, принимавших изотретиноин, по сравнению с пациентами, получавших комплексное лечение (метронидазол и доксициклин) [14].
Традиционно местная терапия розацеа состоит из холодных примочек с антисептическими растворами (1–2% раствор борной кислоты, 1–2% раствор резорцина, отвар ромашки и т. д.), мазей, паст или кремов с противодемодекозным эффектом [1, 3].
Современные топические препараты используются в основном в виде кремов, содержащих азелаиновую кислоту, метронидазол 0,75% и 1%, адапален 0,1% и гель с метронидазолом 1% [1, 3, 4]. Некоторые авторы настаивают на особой эффективности азалаиновой кислоты в лечении розацеа [10]. Однако данное заявление также оспаривается. По мнению A. Parodi et al. (2011) и B. A. Yentzer et al. (2010), монотерапия азелаиновой кислотой без применения пероральных антибиотиков ведет к хронизации процесса и отсутствию видимого эффекта [8, 15]. Наиболее оптимальным является комплексное применение азелаиновой кислоты, доксициклина (или клиндамицина) и метронидазола [8, 11, 16].
Как показывают различные исследования отечественных и зарубежных ученых, значительного повышения эффективности терапии можно ожидать при использовании комбинированных методов терапии, сочетающих медикаментозные и физиотерапевтические методы лечения.
Физиотерапевтическими методами, используемыми в терапии розацеа, являются криотерапия, электрофорез, деструктивные методики.
Криотерапию проводят через день или ежедневно до глубокого отшелушивания. Метод показан больным независимо от стадии заболевания. Криотерапия оказывает противовоспалительное, сосудосуживающее, антипаразитарное действие [4, 7]. Клинические рекомендации также включают электрофорез (10–30% раствором ихтиола 2–3 раза в неделю, с лидазой 2–3 раза в неделю, 10–15 сеансов) [4].
В лечении папулопустулезной, кистозной и узловатой форм розацеа показаны деструктивные методики, такие как электрокоагуляция, дермабразия. Данные методы, к сожалению, имеют ряд недостатков: послеоперационное инфицирование, лейкодерма, формирование эпидермальных кист и рубцов [3, 4, 7].
В последние годы наиболее успешными считаются комбинированные методы лечения. Например, некоторые исследователи с успехом применили сочетание изотретиноина и дермабразии с хорошим результатом [5]. Эффективным является совмещение различных наружных препаратов, таких как азалаиновой кислоты, метронидазола и клиндамицина [11].
Однако все эти методы постепенно теряют свою актуальность не только в связи с имеющимися побочными эффектами, но с низкой эффективностью по сравнению с лазерным излучением [19].
Одним из наиболее значимых научных достижений практической медицины ХХ века стало образование самостоятельного направления — лазерной медицины. Первые исследования по практическому применению лазерного излучения посвящены различным областям хирургии, где лазерные устройства использовались как универсальные деструкторы и коагулянты. Открытие биохемилюминесценции дало предпосылку для развития нового направления лазерной медицины — терапевтического влияния низко- и высокоэнергетического лазерного излучения на клеточные и внутриклеточные процессы. Достижения науки позволили обосновать не только симптоматическое, но и патогенетическое применение лазера в терапии кожных заболеваний [2]. До появления лазерной терапии возможность улучшить состояние кожи лица у больных с розацеа была весьма ограничена. Так, для лечения телеангиэктазий лица применялись в основном электрокоагуляция и криотерапия. Однако эти методы характеризуются риском развития различных осложнений (гиперпигментаций, атрофий) и высокой частотой рецидивов [10, 19, 20]. Поэтому на сегодняшний день, по мнению большинства авторов, лазеротерапия — метод, обеспечивающий наиболее эффективный и продолжительный результат лечения розацеа [2–5, 7, 11, 19, 20].
В зависимости от энергетических характеристик лазера выделяют низкоэнергетические с плотностью мощности менее 100 мВт/см 2 и высокоэнергетические лазеры с плотностью мощности более 10 Вт/см 2 . От мощности лазера напрямую зависят фотобиологические эффекты, которые он вызывает. Низкоинтенсивное лазерное излучение (НЛИ) сопряжено с фотохимическими реакциями.
Фототермические эффекты высокоинтенсивного лазерного излучения (ВЛИ) вызывают локальную деструкцию ткани в виде фотодинамического действия, фотокоагуляции или фотоабляции [2].
Избирательное фототермическое или фотоакустическое действие ВЛИ объясняется теорией селективного фототермолиза (СФТ), согласно которой для повреждения или разрушения целевого хромофора необходимо, чтобы коэффициент поглощения мишени и окружающей ткани максимально различался, а продолжительность импульса была меньше или равна времени термической релаксации [2].
Открытие СФТ обосновало воздействие на специфические хромофоры кожи без повреждения окружающих структур путем подбора соответствующей длины волны, длительности импульса и плотности энергии. Таким образом, параметры лазерного излучения могут быть оптимизированы таким образом, чтобы точно воздействовать на ткань-мишень с минимальным сопутствующим повреждением других тканей. Хромофором, на который направлено воздействие при лечении сосудистых образований, является оксигемоглобин [19]. Наибольшее поглощение излучения оксигемоглобином происходит при длине волны 18, 542, 577 нм. В результате поглощения оксигемоглобином лазерного излучения сосуд подвергается воздействию энергии и коагулируется [19].
Для лечения сосудистой патологии кожи применялись с той или иной степенью эффективности и безопасности различные виды лазеров. Первым большим достижением лазеротерапии сосудистых образований было создание в 1970 году аргонового лазера с длиной волны 488 и 514 нм. К сожалению, использование лазерной установки, генерирующей непрерывное излучение, вызывало коагуляционный некроз поверхностных слоев кожи, что часто вело к последующему образованию рубцов и депигментации [19].
Современные авторы для лечения телеангиэктазий лица предлагают использовать в основном длинноволновые (577 и 585 нм) лучи [3, 4, 7] и импульсный лазер на красителях (ИЛК) (585 нм) с низкой плотностью энергии 1,5 Дж/см 2 или 3,0 Дж/см 2 . За один сеанс осуществляют один проход, процедуры проводят один раз в неделю, на курс 3–4 сеанса [2, 5, 21]. Несмотря на то, что длина волны 595 нм лучше проникает в ткани по сравнению с 585 нм, степень поглощения излучения оксигемоглобином уменьшается после 585 нм. Поэтому для увеличения глубины проникновения ИЛК с длиной волны 595–600 нм требуется дополнительное повышение плотности потока излучения на 20–50% по сравнению с ИЛК с длиной волны 585 нм [19]. Улучшение очищения кожи лица от телеангиэктазий и уменьшение выраженности эритемы могут быть достигнуты наложением импульсов с меньшей плотностью светового потока, но с большей длительностью, что позволяет также избежать появления пурпуры после лечения. По данным Голдберга Дж. (2010) степень очищения кожи после одного сеанса лечения увеличилась с 67% при использовании неперекрывающихся импульсов до 87% после применения методики наложения импульсов [19]. Осложнения после лечения ИЛК, такие как гиперпигментация, атрофия, гипертрофический рубец, экзематозный дерматит, встречаются крайне редко [19]. Последние исследования доказали терапевтическую результативность ВЛИ с длиной волны 578 нм, которая составляет при эритематозно-телеангиэктатической форме 88%, при папулезной — 83,7%, при пустулезной — 76,3%, при инфильтративно-пролиферативной — 62,7%. Отдаленные результаты данного исследования показали, что спустя три года достигнутый эффект в среднем сохраняется у 21% пациентов [22].
Однако, как считают Потекаев Н. Н. и Круглова Л. С. (2012), при преобладании в клинической картине телеангиэктазий показан метод лазерной бесконтактной коагуляции с помощью диодного или неодимового лазера [2, 23]. По мнению авторов, в лечении розацеа также эффективны генераторы интенсивного импульсного света (Intense Pulsed Light, IPL) c длиной волны 500–1200 нм и максимумом эмиссии в диапазоне 530–700 нм. При поверхностных телеангиэктазиях диаметром до 0,3 см действенный эффект отмечен при длине волны 530–600 нм (желто-зеленый спектр) [2, 21]. Имея широкий диапазон длины волны, излучение способно достигать сосуды-мишени, расположенные на различной глубине от поверхности кожи. Несмотря на то, что излучение с большой длиной волны проникает глубже, уровень поглощения энергии оксигемоглобином уменьшается. Поэтому для компенсации снижения абсорбции энергии требуется увеличение плотности потока излучения, что и применяется в данном типе устройств. Таким образом, эффективно нагреваются как поверхностные, так и глубоко расположенные сосуды, размер пятна, образуемого излучением, также достаточно велик. Другим вероятным преимуществом IPL является то, что энергия лазерного излучения доставляется к ткани-мишени с помощью импульса большей длительности. Это ведет к более равномерному нагреванию, коагуляции всего патологически измененного сосуда [19, 21, 23].
Лазеры на парах тяжелых металлов также успешно использовались для лечения телеангиэктазий, однако в данном случае энергия лазерного излучения поглощается не только оксигемоглобином, но и меланином, содержащимся в эпидермисе и дерме. Поэтому лазеры на парах металлов применяются для лечения пациентов только со светлой кожей (тип I и II по Фитцпатрику). У пациентов с темной кожей высок риск нарушений пигментации, появляющихся вслед за воспалительной реакцией, как правило, это образование пузырей и струпа [19, 23].
Другие системы, использующиеся для лечения сосудистых образований, это калий-титанил-фосфатный (КТФ) лазер, длинноимпульсный лазер на алюмоиттриевом гранате с неодимом (Nd: YAG), длинноимпульсные лазеры на александрите (755 нм) и диодные лазеры (800, 810, 930 нм). КТФ-лазер — это Nd: YAG-лазер с удвоением частоты, генерирующей излучение в диапазоне 532 нм (зеленый свет). Длина волны 532 нм приближается к одному из пиков поглощения излучения гемоглобином, поэтому хорошо подходит для лечения поверхностно расположенных кровеносных сосудов [19, 21]. На длине волны 1064 нм Nd: YAG-лазер позволяет намного глубже проникнуть в дерму. При этом может быть достигнута коагуляция кровеносных сосудов на глубине 2–3 мм от дермоэпидермального соединения. Это позволяет иметь в качестве цели более глубокую сосудистую сеть, которую ИЛК может быть не в состоянии достигнуть. Эти глубокие крупные кровеносные сосуды обычно требуют продолжительности импульса между 3 и 15 мс. Так как абсолютное поглощение гемоглобина на 1064 нм ниже, чем на 585 нм, с этой длиной волны должны использоваться значительно более высокие плотности потока. Вследствие этого для данного лазера охлаждение стоит на первом месте [20, 23].
Длинноимпульсные лазеры на александрите (755 нм) и диодные лазеры (800, 810, 930 нм) генерируют излучение с большей длиной волны, которое соответствует области минимального поглощения гемоглобином, что делает их теоретически более подходящими для лечения крупных, глубоко расположенных сосудов диаметром 0,4 мм [19].
По мнению Дж. Голдберг (2010) в терапии лазером розацеа определенные трудности представляют сосудистые образования крыльев носа. Для удаления телеангиэктазий в этой области необходимо многократное проведение лечебных сеансов и, возможно, повторного курса лечения в будущем [19]. Эритема лица поддается лечению одинаково хорошо как с использованием ИЛК, так и c IPL [10, 20].
Современная лазерная терапия стоит на пороге комбинаций различных лазерных методов в лечении дерматозов. Оптимизировать клинический результат и уменьшить риск побочных эффектов возможно при сочетанном применении фракционного неселективного лазера и IPL; углекислотного (СО2) лазера и радиочастотной (Radio Frequency, RF) технологии, лазера и фотодинамической терапии (ФДТ) [24, 25].
На сегодняшний день одним из самых дискутируемых вопросов является применение лазерной ФДТ. Прежде всего это обусловлено ограниченным числом исследований с достаточной доказательной базой эффективности ФДТ в лечении злокачественных и доброкачественных новообразований кожи. Терапевтическое действие ФДТ основывается на фотохимических реакциях, происходящих при взаимодействии порфиринов, лазерного излучения и кислорода. В данном случае лазер является активатором фотохимических процессов в клетках и не вызывает фототермического повреждения. Для ФДТ может применяться любой лазер с длиной волны 400–800 нм [2]. Однако данный метод тоже не лишен недостатков. Побочные эффекты проявляются в виде фототоксических реакций в виде эритемы, отека, корочек, эрозий, везикул, что, как правило, наблюдается у большинства пациентов и носит проходящий характер. Из отдаленных последствий терапии отмечают возможное возникновение гиперпигментаций на месте проведения ФДТ [2].
При инфильтративно-продуктивной стадии розацеа показаны деструктивные методы, поскольку имеющиеся ультраструктурные изменения в системе микроциркуляторного русла кожи лица носят необратимый характер. В этой ситуации назначают лазерную абляцию с целью удаления гипертрофированной ткани, например при ринофиме [5]. Абляцию проводят до достижения уровня сальных желез. При этом возможно использование импульсного СО2-лазера или фракционного эрбиевого (Er: YAG) лазера с модулированным импульсным режимом [2]. Применение данных типов лазеров остается «золотым» стандартом аблятивных процедур, являясь альтернативой традиционному хирургическому подходу к этой проблеме [5, 7]. Однако при лечении СО2- или Er: YAG-лазером наблюдается длительное заживление раневого дефекта и повышается риск развития таких явлений, как замедленная реэпитализация, стойкая эритема, гипопигментация кожи, а в некоторых случаях — формирование гипертрофических и келоидных рубцов [26].
При всех формах розацеа показаны курсы низкоэнергетического лазерного воздействия, которое проводят через день (6 процедур), среднее время воздействия составляет 25 минут [2].
Таким образом, несмотря на некоторые ограничения, лазеры и устройства с источниками света остаются наилучшим выбором в лечении сосудистых поражений кожи [10, 20].
Несмотря на то, что в настоящее время существует обширный арсенал лекарственных средств и методов терапии розацеа, эффективность лечения находится в прямой зависимости от длительности терапии и степени выраженности побочных эффектов. Постоянный поиск оптимального подхода к терапии данного дерматоза привел к достижениям в области лазерных технологий, позволивших сделать огромный шаг в этом направлении.
Литература
И. Я. Пинсон*, доктор медицинских наук, профессор
И. В. Верхогляд**, доктор медицинских наук, доцент
А. В. Семочкин***
*ГБОУ ВПО Первый МГМУ им. И. М. Сеченова Минздравсоцразвития России,
**ГБОУ ДПО РМАПО Минздравсоцразвития России,
***Клиника «Президентмед», Москва
Паста д/наружн. прим. 20 мг+250 мг/1 г: 25 г или 50 г тубы, 25 г, 50 г или 100 г банки, 50 г или 100 г флаконы.
Форма выпуска, упаковка и состав препарата Салицилово-цинковая паста
Паста для наружного применения белого цвета с желтоватым или сероватым оттенком.
| 1 г | |
| салициловая кислота | 20 мг |
| цинка оксид | 250 мг |
Вспомогательные вещества: крахмал кукурузный 25 мг, вазелин 48 мг.
25 г - тубы (1) - пачки картонные.
50 г - тубы (1) - пачки картонные.
25 г - банки (1) - пачки картонные.
50 г - банки (1) - пачки картонные.
100 г - банки (1) - пачки картонные.
50 г - флаконы полимерные (1) - пачки картонные.
100 г - флаконы полимерные (1) - пачки картонные.
Фармакологическое действие
Комбинированный препарат для местного применения. Салициловая кислота оказывает противовоспалительное, антисептическое и кератолитическое действие. Zn 2+ оказывает подсушивающее действие.
Показания препарата Салицилово-цинковая паста
- подострая экзема различного генеза;
- гипергидроз стоп.
Режим дозирования
Наружно. Наносят на пораженные участки кожи 1-2 раза/сут. Курс лечения не должен превышать 2-х недель. Если симптомы заболевания не исчезают, необходимо проконсультироваться с врачом.
Особенности действия лекарственного препарата при первом его приеме или при его отмене отсутствуют.
Побочное действие
Противопоказания к применению
- детский возраст (до 12 лет);
- поышенная чувствительность.
Применение при беременности и кормлении грудью
Применение у детей
Противопоказан детям до 1 2лет.
Особые указания
Салициловая кислота, входящая в состав пасты, может проникать через кожу в кровь.
Не наносить пасту в очаги мокнующих ран.
Влияние на способность к управлению транспортными средствами и механизмами
Передозировка
Лекарственное взаимодействие
Условия хранения препарата Салицилово-цинковая паста
Хранить в сухом защищенном от света месте при температуре не выше 25°С. Хранить в недоступном для детей месте.
Срок годности препарата Салицилово-цинковая паста
Условия реализации
Салицилово-цинковая . (ЯРОСЛАВСКАЯ ФАРМАЦЕВТИЧЕСКАЯ ФАБРИКА, Россия)
Салицилово-цинковая . (ТУЛЬСКАЯ ФАРМАЦЕВТИЧЕСКАЯ ФАБРИКА, Россия)
Салицилово-цинковая . (ТВЕРСКАЯ ФАРМАЦЕВТИЧЕСКАЯ ФАБРИКА, Россия)
Салицилово-цинковая . (МОСКОВСКАЯ ФАРМАЦЕВТИЧЕСКАЯ ФАБРИКА, Россия)
Информация о препаратах, отпускаемых по рецепту, размещенная на сайте, предназначена только для специалистов. Информация, содержащаяся на сайте, не должна использоваться пациентами для принятия самостоятельного решения о применении представленных лекарственных препаратов и не может служить заменой очной консультации врача.
Свидетельство о регистрации средства массовой информации Эл № ФС77-79153 выдано Федеральной службой по надзору в сфере связи, информационных технологий и массовых коммуникаций (Роскомнадзор) 15 сентября 2020 года.

Читайте также:

