Ожог мозга у человека что такое
Обновлено: 04.05.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Бляшки на коже: причины появления, при каких заболеваниях возникают, диагностика и способы лечения.
Определение
Бляшка – это патологический элемент с четкими краями, который возвышается над поверхностью кожи или сливается с ней, размером более 5 мм.
В дерматологии выделяют множество разновидностей бляшек - около 70 болезней протекают с образованием этих элементов, что делает бляшку одним из самых часто встречающихся высыпаний.
Разновидности бляшек
По форме бляшки бывают круглыми, овальными и неправильной формы. Со временем форма, поверхность и внешний вид этого элемента могут изменяться.
По причине возникновения бляшки могут быть как проявлением заболеваний кожи, так и симптомом болезней внутренних органов и систем (аутоиммунные реакции, болезни печени, онкологические процессы, аллергические реакции).
Бляшки бывают сухими, гладкими, красными, коричневыми, серо-белыми и пр.
Возможные причины появления бляшек
Сухие бляшки на коже у взрослых могут быть проявлением следующих заболеваний:
- Грибковое поражение кожи, сопровождающееся бляшками с выраженным зудом.
- Аллергические реакции характеризуются появлением на коже гладких сухих бляшек, пятен розового цвета, волдырей, которые сильно зудят и доставляют выраженный дискомфорт. Могут развиваться как при контакте кожи с аллергеном, так и при попадании его на слизистые (например, при крапивнице, поллинозе, пищевой и контактной аллергии).
- Псориаз – хроническое неинфекционное заболевание кожи, при котором образуются шелушащиеся сухие бляшки на локтях, коленях, волосистой части головы, склонные к слиянию и сопровождающиеся слабовыраженным зудом.
- Сухие бляшки формируются на коже, если она длительное время подвергается стрессовым воздействиям с потерей своих защитных функций.
- Заболевания пищеварительного тракта, сопровождающиеся синдромом мальабсорбции (нарушением всасывания витаминов и микроэлементов в тонкой кишке), хронические заболевания печени и других органов, при которых в дерме накапливаются вещества, в норме в ней не присутствующие, также ведут к появлению сухих бляшек.
- Солнечная кератома – предраковое состояние, для которого характерно наличие на коже множества светло-сероватых бляшек.
- Лекарственная токсидермия – аллергическая реакция, сопровождающаяся появлением на коже элементов в виде бляшек. В тяжелых случаях может развиться синдром Лайелла или Стивенса–Джонсона - токсического эпидермального некролиза.
- Дерматит Дюринга (герпетиформный) – хроническое заболевание кожи без установленной этиологии, для которого характерно рецидивирующее появление на коже сыпи различной морфологии, сопровождающейся сильным кожным зудом и жжением.
- Грибовидный микоз – первичная Т-клеточная лимфома кожи, злокачественное лимфоидное поражение, в первую очередь кожи. На коже появляются чешущиеся красные бляшки, напоминающие экзему. На начальных стадиях хорошо поддаются лечению гормональными мазями, однако само заболевание требует более сложной терапии.
- У детей появление красных пятен и бляшек на коже чаще всего связано с аллергической реакцией на пищевые продукты.
- Невус Беккера – аномалия развития дермы, когда на коже появляются темные бляшки с неровной поверхностью, на которых со временем могут начать расти волосы.
- Пигментный невус – «родимое пятно», может возвышаться над кожей, имеет коричневую или темную окраску.
- Меланома – самая злокачественная опухоль кожи, характеризующаяся стремительным метастазированием. Развивается преимущественно из невусов и родинок. При изменении характера поверхности, границ родинки, увеличении ее размеров, появлении кровоточивости необходимо незамедлительно обратиться к дерматологу или онкологу для исключения развития меланомы.
- Базальноклеточный рак кожи чаще локализуется на голове, лице, шее, не метастазирует, характеризуется медленным ростом.
- Сенильная кератома встречается у людей пожилого возраста, развивается, вероятнее всего, из-за недостатка витаминов, обилия потребляемых животных жиров, чувствительности кожи к ультрафиолету вследствие нарушения ее защитных функций. Типичная локализация – лицо, шея, открытые участки тела.
- Себорейная кератома – желтоватая бляшка на коже, которая со временем трансформируется в темно-коричневый нарост, который склонен шелушиться, сильно зудеть, покрываться трещинами, кровоточить и может служить входными воротами для инфекции.
При образовании на коже бляшек необходимо обратиться к дерматологу для установления причин появления данного элемента сыпи.
Диагностика и обследования при появлении бляшек
Для диагностики грибкового поражения кожи используется соскоб с пораженного участка для последующего микроскопического изучения.
Развитие аллергической реакции требует обращения за медицинской помощью для выявления аллергена, назначения антигистаминных, иногда – гормональных препаратов. В клинических случаях аллергии наряду с кожными пробами проводят анализы с использованием различных наборов распространенных аллергенов и триггеров: панель на респираторные аллергены, на пищевые аллергены и на их сочетание.
Синонимы: Комплексная панель тестов на респираторные аллергены; Respiratory allergens panel, Allergen respiratory profile, Allergy testing. Краткое описание исследования «Панель респираторные аллергены» Панель респираторные аллергены домашняя пыль (кле.
© С.Е. Хрулев, А.Н.Белова, И.Д.Булюбаш,
С.В.Евстигнеев, А.Л. Борисевич, М.В.Растеряева, 2002 г.
УДК 616.831—001.17
Поступила 29.11.2001 г.
С.Е.Хрулев, А.Н.Белова, И.Д.Булюбаш, С.В.Евстигнеев, А.Л.Борисевич, М.В.Растеряева
Научно-исследовательский институт травматологии и ортопедии, Нижний Новгород
Профилактика и лечение поражений головного мозга при ожоговой болезни
К числу наименее изученных вопросов комбустиологии относится проблема поражения нервной системы при термической травме. Ожоговая болезнь — яркий пример полиорганной недостаточности. Одним из проявлений этой недостаточности является поражение головного мозга, которое наиболее часто манифестирует острой ожоговой энцефалопатией [1]. Помимо энцефалопатии церебральная патология при ожоговой болезни может проявляться в форме делирия и мозгового инсульта. Все эти патологические состояния до настоящего времени изучены недостаточно полно. Существующие публикации по лечению неврологических осложнений термической травмы в основном касаются коррекции эмоционально-волевых расстройств и нарушений когнитивных функций в поздних периодах ожоговой болезни [2, 3]. Таким образом, адресная специфическая профилактика и терапия различных вариантов поражения головного мозга, проводимая с учетом риска их развития при ожоговой травме, является весьма актуальной проблемой.
Цель исследования — выявление факторов риска развития энцефалопатии, делирия и острого нарушения мозгового кровообращения у обожженных и разработка мер профилактики и лечения данных состояний.
Материалы и методы.
Исследование проводилось в клинике Российского ожогового центра (РОЦ) на базе Нижегородского НИИ травматологии и ортопедии. Работа осуществлялась в два этапа: 1) выявление факторов риска развития энцефалопатии, делирия и острого нарушения мозгового кровообращения у обожженных; 2) разработка схем профилактики и лечения данных состояний и оценка их эффективности.
На первом этапе обследовано 160 ожоговых больных, прошедших лечение в РОЦ в 1999—2000 гг., в возрасте от 16 до 75 лет, с площадью поражения от 5 до 75% поверхности тела. Среди них у 68 человек выявлена клиника энцефалопатии (средний возраст 51±8 лет, средняя площадь поражения 38±15%), у 3 человек отмечено развитие инсульта (средний возраст 59±8 лет, средняя площадь поражения 30±17% поверхности тела); у 10 больных развился делирий (средний возраст 43±14 лет, средняя площадь поражения 46±16% поверхности тела). Кроме того, взяты из архива и обработаны данные 18 историй болезни пациентов, перенесших в период термической травмы мозговой инсульт (с 1985 по 1998 гг.).
Для определения факторов, игравших решающую роль в развитии той или иной формы церебральной патологии, был проведен дисперсионный анализ 16 параметров, отражавших пол, возраст, характер и тяжесть ожоговой травмы, данные анамнеза жизни, лабораторные показатели. Определение критических значений выявленных факторов и достоверность их влияния на развитие патологии головного мозга проводились с помощью точного критерия Фишера.
На втором этапе работы обследовано 148 больных, проходивших лечение в РОЦ в 2000—2001 гг., из них профилактические и специализированные лечебные мероприятия проведены 75 больным, имевшим высокий риск развития различной церебральной патологии (основная группа). В данной группе 60 пострадавших имели высокий риск развития энцефалопатии разной степени тяжести (средний возраст 52±7 лет, площадь ожога 42±4% поверхности тела), 10 человек (средний возраст 57±7 лет, площадь ожога 25±13% поверхности тела) — мозгового инсульта и 8 человек (средний возраст 49±17 лет, площадь ожога 37±13% поверхности тела) — делирия.
Оценка эффективности мер профилактики и лечения проводилась путем сравнения результатов, достигнутых в основной группе, и у 80 больных, сопоставимых с пациентами основной группы по возрасту, тяжести ожоговой травмы и по степени риска развития церебральной патологии, но не получавших соответствующих профилактических и лечебных воздействий (группа сравнения).
Результаты и обсуждение.
Выявленным в результате исследования факторам риска развития энцефалопатии, делирия и инсульта у обожженных методом экспертной оценки был придан индекс значимости, выраженный в баллах (1, 2 и 3 балла). Чем больше индекс значимости, тем важнее фактор в прогностическом отношении (см. таблицу).
| Факторы риска развития энцефалопатии, делирия и инсульта у обожженных |
Для определения вероятности развития ожоговой энцефалопатии необходимо при поступлении больного в отделение оценить наличие и выраженность у него ожоговой болезни, величину индекса тяжести поражения*, наличие в анамнезе черепно-мозговых травм, сопутствующей гипертонической болезни, хронического алкоголизма, а также учесть возраст пациента. Далее производится суммирование баллов. Если тот или иной фактор отсутствует, проставляется балл «0». Оценка выявленных факторов риска в баллах при поступлении может варьировать от
0 до 10. Результаты проведенных исследований позволили установить следующую закономерность: при сумме баллов от 0 до 2 риск развития энцефалопатии достаточно низкий (11%), при сумме от 3 до 5 он повышается до 66%; при сумме, равной 6 баллам и выше, вероятность развития энцефалопатии равна 98% (p 4 .
Для определения вероятности развития делирия выявляют данные анамнеза о злоупотреблениях алкоголем в виде эпизодов запойного пьянства, вычисляют индекс тяжести поражения и уровень аланинаминотрансферазы крови. Процедура суммирования баллов аналогична вышеописанной. Оценка выявленных факторов риска в баллах при поступлении может варьировать от
0 до 3. Больной, набравший в сумме 3 балла, имеет 100%-ный риск развития делирия; при сумме
2 балла вероятность возникновения делирия — 32%; при оценке в 0—1 балл вероятность присоединения делирия крайне низкая (p 5 .
Для определения вероятности развития инсульта необходимо при поступлении больного в отделение оценить величину индекса тяжести поражения, наличие в анамнезе данных о перенесенных нарушениях мозгового кровообращения, алкоголизме, сопутствующих гипертонической болезни и ишемической болезни сердца, а также учесть возраст пациента. Оценка факторов риска инсульта в баллах при поступлении может варьировать от 0 до 10 баллов. При оценке в 3—4 балла вероятность развития инсульта равна 33,3%; при 5—6 баллах — 62,5%, при сумме 7—8 баллов она увеличивается до 80% и при 9—10 баллах достигает 100% (p 6 .
Итогом первого этапа работы стало выделение групп риска по развитию у больных с ожогами различных клинических вариантов поражения головного мозга.
На втором этапе исследования разработаны и апробированы дифференцированные схемы профилактики и лечения церебральных осложнений у обожженных.
Больным с риском развития церебральной патологии, превышающим 70%, профилактически (начиная со стадии шока) назначались препараты, улучшающие метаболизм головного мозга, микроциркуляцию и церебральное кровообращение, направленные на борьбу с отеком головного мозга при наличии внутричерепной гипертензии. Из всего многообразия препаратов, улучшающих церебральный метаболизм, нами выбраны ноотропил, церебролизин и актовегин как наиболее эффективные и имеющие минимальное количество осложнений 7 . Церебролизин обладает нейромодулирующим, нейропротекторным и нейротрофическим действием. Ноотропил повышает энергетический обмен клеток головного мозга, улучшает интегративную деятельность мозга, способствует консолидации памяти. Актовегин, помимо положительного воздействия на метаболизм и кровообращение головного мозга, оказывает выраженное антиоксидантное действие и способствует репаративным процессам, что представляется крайне важным при ожоговой травме.
Из препаратов, улучшающих кровообращение головного мозга, был выбран инстенон как эффективный препарат, обладающий минимальной кардиотоксичностью (в отличие, например, от кавинтона). Инстенон является единственным кобинированным ноотропным препаратом, сочетающим к себе истинно ноотропный, сосудистый и нейростимулирующий компоненты, что дает возможность комплексного воздействия на различные звенья патогенеза ишемии и гипоксии головного мозга 7 . Ограничением к назначению инстенона у обожженных служила клиника выраженного повышения внутричерепного давления, препарат не использовался также при эпилептическом синдроме, подозрении на внутримозговое кровоизлияние.
Кроме того, при высоком риске инсульта для улучшения микроциркуляции головного мозга нами использовался тиклид, который тормозит агрегацию и адгезию тромбоцитов, а также снижает оседание тромбоцитов на атеросклеротической бляшке у пациентов с цереброваскулярными заболеваниями. Из препаратов, уменьшающих отек головного мозга, отдано предпочтение диакарбу (фонуриту), который помимо мочегонного действия, обладает противосудорожной активностью.
Для профилактики и лечения делирия использовался нейролептик тиапридал, который наряду с антипсихотическим и анксиолитическим действием способствует ясности мышления и имеет выраженный анальгезирующий эффект.
При ожоговой травме в течение многих лет успешно используется магния сульфат в качестве дегидратационного средства, который обладает еще и дезинтоксикационным, противосудорожным и седативным эффектом. Подбор наиболее эффективных неврологических препаратов с учетом не только их основного действия, но и сопутствующих эффектов позволил избежать полипрагмазии, что крайне важно при полиорганной недостаточности.
С целью профилактики поражений головного мозга использовались следующие схемы приема препаратов.
Для профилактики энцефалопатии ноотропил применяли в дозе 5 мл внутривенно струйно 1 раз в сутки в течение 10 дней; актовегин — в дозе 2 мл (80 мг) внутривенно 1 раз в сутки в течение 10 дней.
Профилактика развития делирия заключалась в назначении седативной, психотропной терапии, витаминов, препаратов, улучшающих церебральный метаболизм и кровообращение. Использовалась следующая схема: реланиум — 2 мл 2 раза в сутки в течение 2—3 дней, тиапридал — внутримышечно 2 мл 2 раза в сутки; магния сульфат 25% — 10 мл 1 раз в сутки в течение 5—7 дней; ноотропил, актовегин в вышеуказанных дозировках; витамины В1 6% — 3 мл 2 раза в сутки, В6 5% — по 3 мл 2 раза в сутки в течение 7—10 дней, аскорбиновая кислота 5% — 0,3—1 мл 3 раза в сутки в течение 5 дней. Лечение осуществлялось на фоне усиления дезинтоксикационной терапии, проведения плазмафереза с частотой 2—3 раза в неделю.
Мероприятия по профилактике острых нарушений мозгового кровообращения зависели от наличия или отсутствия признаков внутричерепной гипертензии. Если клинические данные о повышении внутричерепного давления отсутствовали, то назначались ноотропил — 5 мл внутривенно струйно 2 раза в сутки в течение 15 дней; актовегин — 5 мл (200 мг) внутривенно 2 раза в сутки в течение 10 дней, либо актовегин 5 мл (200 мг) внутривенно 1 раз в сутки в течение 10 дней и инстенон — 2 мл на 0,9% физрастворе внутривенно медленно (в течение 2—3 ч) 1 раз в сутки в течение 7 дней; тиклид — 250 мг 2 раза в сутки в течение 15 дней. Затем переходили на пероральный прием препаратов в течение 1—2 мес. Если у больного имелись клинические проявления внутричерепной гипертензии (головная боль, нарушение сознания, изменения психики, менингеальные симптомы), то в первую очередь добивались снижения внутричерепного давления. Для этого головному концу кровати придавали возвышенное положение на 10—15%, ограничивали объем вводимой жидкости (разница между объемом потребляемой и выделяемой жидкости не должна была превышать 1,5 л в сутки); назначали диакарб — 250 мг утром через день в течение 2—3 нед под контролем содержания калия в сыворотке крови (не ниже 3,3 ммоль/л). Применяли препараты: тиклид — 250 мг 2 раза в сутки в течение 15 дней, церебролизин — 5 мл внутривенно 2 раза в сутки в течение 15 дней или ноотропил — 5 мл внутривенно струйно 2 раза в сутки в течение 15 дней, актовегин — 5 мл внутривенно капельно 2 раза в сутки в течение 10 дней, затем переходили на пероральный прием этих же препаратов в течение 1—2 мес. При необходимости курсы ноотропов и сосудистых препаратов повторяли.
Несмотря на проводимые профилактические мероприятия, полностью предотвратить развитие церебральных нарушений при ожоговой болезни очень сложно. Нами разработаны комплексы лечебных воздействий при развитии различных форм поражений головного мозга. Лечение церебральной патологии проводилось на фоне стандартной инфузионно-трансфузионной терапии, применяемой при ожоговой болезни.
При развитии проявлений энцефалопатии легкой степени у обожженных назначались ноотропил в дозе 5 мл внутривенно струйно 2 раза в сутки в течение 10 дней; актовегин — 4 мл
(160 мг) внутривенно один раз в сутки в течение 10 дней. У больных с тяжелой энцефалопатией лечение различалось в зависимости от наличия внутричерепной гипертензии. При отсутствии признаков повышения внутричерепного давления: ноотропил — 10 мл внутривенно струйно 2 раза в сутки в течение 15 дней; актовегин — 6 мл (240 мг) внутривенно 2 раза в сутки в течение 15 дней либо актовегин — 6 мл (240 мг) внутривенно 1 раз в сутки на 0,9% физрастворе в течение 15 дней в комбинации с инстеноном — 2 мл внутривенно капельно медленно (в течение 2—3 ч) 1 раз в сутки в течение 7 дней; тиклид — 250 мг 2 раза в сутки в течение 25 дней. Затем переходили на пероральный прием препаратов в течение 1 мес. При наличии явлений внутричерепной гипертензии больным устанавливали возвышенное положение головного конца кровати на 10—15°, ограничивали объем вводимой жидкости; назначали диакарб — 250 мг утром через день в течение месяца; тиклид — 250 мг 2 раза в сутки на протяжении 25 дней; церебролизин — 10 мл внутривенно 2 раза в сутки в течение 15 дней. Затем переходили на пероральный прием этих препаратов в течение 1 мес. При необходимости курсы ноотропов и сосудистых препаратов повторяли.
У больных с делирием, развившимся на фоне ожоговой травмы, применялась следующая терапия: реланиум — 2 мл 2—3 раза в сутки в течение 2—3 дней, при продолжающихся приступах психомоторного возбуждения — ГОМК — 6 мл в сутки; тиапридал — внутримышечно 2 мл 3—4 раза в сутки; магния сульфат 25% — 10 мл 2 раза в сутки в течение 5—7 дней, витамины: В1 6% — 3 мл 2 раза в сутки, В6 5% — 3 мл 2 раза в сутки в течение 7—10 дней, 5% аскорбиновая кислота — 1 мл 3 раза в день в течение 5 дней; сосудистые препараты, ноотропы (по предложенным выше схемам); усиление дезинтоксикационных мероприятий (проведение ежедневного плазмафереза).
Для лечения инсульта схемы воздействий различаются в зависимости от наличия симптомов повышения внутричерепного давления. При отсутствии клиники внутричерепной гипертензии терапия заключалась в назначении ноотропила — 10 мл внутривенно струйно 2 раза в сутки в течение 15 дней; актовегина — 8—10 мл (360—400 мг) внутривенно 2 раза в сутки в течение 15 дней либо актовегина — 8—10 мл (360—400 мг) внутривенно один раз в сутки в течение 15 дней и инстенона — 2 мл внутривенно капельно медленно (в течение 2—3 ч) один раз в сутки на протяжении 7 дней; тиклида — 250 мг 2 раза в сутки в течение 25 дней. Затем продолжали пероральный прием препаратов в течение 1—2 мес. У больных с явлением внутричерепной гипертензии устанавливали возвышенное положение головного конца кровати на 10—15°; производилось ограничение объема вводимой жидкости, назначались диакарб — 250 мг утром через день в течение месяца, тиклид — 250 мг 2 раза в сутки на протяжении 25 дней, церебролизин — 10 мл внутривенно 2 раза в сутки в течение 15 дней; актовегин — 8—10 мл (360—400 мг) внутривенно капельно 2 раза в сутки в течение 15 дней. Затем переходили на пероральный прием этих же препаратов в течение 1—2 мес. При необходимости курсы ноотропов и сосудистых препаратов повторяли.
По результатам исследований была определена эффективность проводимых профилактических и лечебных воздействий. Частота развития энцефалопатии в основной группе составила 35,1%, тогда как в группе сравнения — 42,5% (p Литература
Лейдерман И.Н. Синдром полиорганной недостаточности, метаболические основы. Вестник интенсивной терапии 1999; 2: 5—10.
Волошин П.В. Патология нервной системы при ожоговой болезни. Киев: Здоровье; 1982.
Гельфанд В.Б., Николаев Г.В. Нервно-психические расстройства при термических повреждениях. Сов мед 1985; 2: 74—78.
Хрулев С.Е., Белова А.Н., Евстигнеев С.В. и др. Реабилитация обожженных с позиций невролога. В кн.: Материалы I Межрегиональной конференции «Проблемы восстановительной медицины». Воронеж; 2001.
Хрулев С.Е., Белова А.Н., Стручков А.А. и др. Ожоговая энцефалопатия: степени тяжести и факторы риска. В кн.: Материалы юбил. научн. конф., посвященной 140-летию кафедры душевных и нервных болезней военно-медицинской академии. СПб; 2000.
Хрулев С.Е., Белова А.Н., Стручков А.А. и др. Делирий как проявление ожоговой энцефалопатии. В кн.: Материалы VIII Всерос. съезда неврологов. Казань; 2001.
Бурцев С.В. Нейрометаболическая фармакотерапия. М; 2000.
"Медикум"
новый научно-практический медицинский журнал, который будет издаваться на 2-х языках: русском и английском, в трех формах выпуска: печатная, интернет-версия, CD-версия.
Что такое пограничное расстройство личности? Причины возникновения, диагностику и методы лечения разберем в статье доктора Рахманова Владимира Александровича, психиатра со стажем в 18 лет.
Над статьей доктора Рахманова Владимира Александровича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Пограничное расстройство личности (ПРЛ, Borderline personality disorder (BPD), emotionally unstable personality disorder (EUPD)) — расстройство личности, характеризующееся продолжительным аномальным поведением: нестабильностью в отношениях с другими людьми, нестабильным представлением о себе и нестабильной эмоциональной сферой. Часто встречается рискованное поведение и самоповреждение (например, самостоятельно нанесённые порезы). Люди с ПРЛ также могут страдать от чувства эмоциональной опустошённости и панического страха перед одиночеством.
Краткое содержание статьи — в видео:
Важно отметить, что указанные симптомы могут быть спровоцированы на вид нормальными жизненными событиями. Проявление расстройства начинается в период полового созревания. Химические зависимости, депрессия и пищевые расстройства обычно поддерживаются ПРЛ или развиваются в связи с ним. Приблизительно 10% пациентов погибают в результате суицида. [1]

В международной классификации болезней 10-го пересмотра ПРЛ названо «Эмоционально неустойчивым расстройством личности (F60.3)». [2] Именно это наименование распространено на территории России. Также такое расстройство называют пограничным типом расстройства.
Причины ПРЛ до конца не ясны, однако становится всё более очевидным, что появление данного расстройства обусловлено генетическими, мозговыми, и социальными факторами. Пограничное расстройство встречается в 5 раз чаще у лиц с нарушенными отношениями в семье (заброшенность родителями, активная критика и непринятие со стороны близких). У женщин ПРЛ наблюдается в 3 раза чаще, чем у мужчин. [3]
Неблагоприятные факторы жизни (например, физическое или эмоциональное насилие) также играют немаловажную роль в появлении этого отклонения. В ряде нейрофизиологических исследований показано, что проявления расстройства связаны с фронтально-лимбическими группами нейронов. [4] [5] [6]
Распространённость
По данным исследования 2008 года распространённость нарушения в популяции составляет 5,9%. Около 20% госпитализаций в психиатрический стационар приходится на пациентов с ПРЛ. [7]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы пограничного расстройства личности
Согласно утверждению американского психолога Марши Лайнен, ПРЛ можно сравнить с ожогом третьей степени. «У таких людей попросту нет «эмоциональной кожи». Даже малейшее прикосновение или движение может вызвать тяжелейшее страдание». [8]
Заподозрить пограничный тип расстройства можно при обнаружении четырёх или более симптомов (черт характера), представленных на схеме ниже. При этом важно, чтобы одной из проявленных черт была импульсивность, рискованность или враждебность. Симптомы должны иметь устойчивый характер (не изменяться в течение долгого времени) и проявляться практически ежедневно.
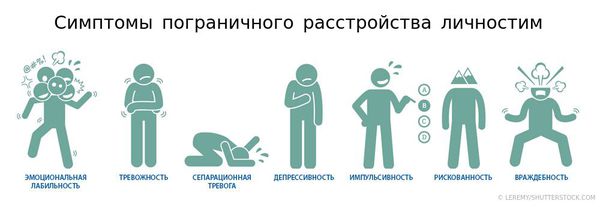
Под эмоциональной лабильностью понимаются резкие скачки настроения: паника или грусть могут сменяться приступами агрессии, затем может возникнуть жгучее чувство вины и т. д.
Сепарационной тревогой называется тревога, которую испытывает личность по причине разлуки с домом и близкими людьми.
Патогенез пограничного расстройства личности
Как и в случае других психических расстройств, патогенез ПРЛ является многофакторным и не до конца изученным. По данным некоторых исследований, пограничное расстройство имеет общие черты и причины с посттравматическим стрессовым расстройством (ПТСР). Кроме того, возможна их патогенетическая взаимосвязь.
Большинство исследователей согласны с тем, что присутствие в анамнезе детской хронической эмоциональной травмы способствует развитию ПРЛ. Однако стоит отметить, что уделяется недостаточное внимание исследованию роли других патогенетических факторов: врождённым дисфункциям головного мозга, генетике, нейробиологическим факторам и факторам социального окружения.
Под социальными факторами подразумевается взаимодействие людей в процессе роста и взросления в своих семьях, в окружении друзей и других личностей.
Психологические факторы включают в себя личностные особенности и темперамент, адаптацию к окружению, а также сформированные навыки, позволяющие справляться со стрессом.
Генетика
Наследуемость ПРЛ составляет примерно 40%. В действительности, добиться объективной оценки генетических факторов достаточно сложно. Так, например, близнецовый метод может дать переоценённые показатели в связи с наличием травмирующих факторов в общей семье сиблингов (родных братьев-сестёр). [9] Тем не менее одно из исследований показало, что ПРЛ находится на третьем месте из десяти по наследуемости среди личностных расстройств. Исследование в Нидерландах (Trull & colleagues) выявило, что генетический материал в девятой хромосоме связан с симптомами ПРЛ. Исходя из этого учёные сделали вывод, что генетические факторы играют ключевую роль в индивидуальных особенностях расстройства у каждого отдельно взятого пациента. Эти же исследователи ранее установили, что 42% симптоматики ПРЛ определено генетикой и 58% — влиянием среды. [10]
Особенности головного мозга
Целый ряд исследований в области нейровизуализации при ПРЛ показал наличие редукции (уменьшения) вещества мозга в конкретных отделах. Эти отделы в норме вовлечены в регуляцию ответа на стресс и регуляцию эмоциональной сферы. Речь идёт о гиппокампе, глазнично-лобных участках коры головного мозга (префронтальная кора), миндалевидном теле. [11]
- Миндалевидное тело меньше в абсолютном объёме и более активно у людей с ПРЛ. Уменьшенный объём миндалины так же был обнаружен у пациентов с обсессивно–компульсивным расстройством. Одно из исследований показало аномально высокую активность в левой миндалине у людей с ПРЛ в момент, когда они рассматривали карточки с изображением людей в негативных эмоциях. В связи с тем, что миндалина генерирует все эмоции, в том числе и негативные, это необычно высокая активность может объяснять сильные и продолжительные эмоциональные проявления страха, горя, злости и стыда, испытываемые людьми с ПРЛ. Этим же фактом трактуется и их способность тонко распознавать эмоции других людей. [12]
- Префронтальная кора имеет тенденцию к меньшей активности у лиц с ПРЛ, особенно в момент оживления воспоминаний об их «эмоциональной заброшенности». Это относительное снижение активности более всего определяется в правой передней извилине. Отдавая должное роли префронтальной коры в регуляции эмоционального возбуждения, относительная неактивность названых участков может объяснять сложности у людей с ПРЛ в регуляции их эмоций и реакции на стресс. [13]
- Гипоталамо-гипофизарно-надпочечниковая (ГГН) ось регулирует продукцию кортизола, который высвобождается в ответ на стресс. Уровень этого гормона надпочечников у людей с ПРЛ фактически более высок, чем в популяции. Это является признаком гиперреактивности ГГН оси. Гиперреактивность может объяснять более высокую биологическую реакцию на стресс и большую уязвимость к тревожащим факторам. Так же высокий уровень кортизола ассоциирован с высоким риском суицидального поведения. [12]
Нейробиологические факторы (эстрогены)
Контролируемое исследование в 2003 году показало, что симптомы ПРЛ у женщин предсказуемо связаны с уровнем эстрогена (женского полового гормона) в течение менструального цикла. [14]
Факторы личностного развития (детская травма)
Существует прочная взаимосвязь между насилием над детьми, особенно детского сексуального насилия, и развитием ПРЛ.
Предполагается, что дети, которые в раннем возрасте испытали хроническое плохое обращение по отношению к себе и трудности с формированием привязанностей, встают на путь формирования ПРЛ. [15]
Классификация и стадии развития пограничного расстройства личности
Американский психолог Теодор Миллон выделил 4 подтипа ПРЛ: [16]
1. Унылое пограничное расстройство (включает избегающие или зависимые личностные особенности).
- Характерные черты: уступчивость, покорность, верность, скромность; чувство уязвимости и постоянной опасности; личность испытывает чувство безнадёжности, подавленности, беспомощности и бессилия.
2. Обидчивое пограничное расстройство (включает пассивно-агрессивные личностные особенности).
- Характерные черты: негативизма (противодействие всему), нетерпеливость, беспокойство, а также упрямость, вызывающее поведение, угрюмость, пессимистичность; человек легко обижается и быстро разочаровывается.
3. Импульсивное пограничное расстройство (включает истерические и антисоциальные личностные особенности).
- Характерные черты: капризность, поверхностность, ветреность, лихорадочное и соблазняющее поведение; боясь потери, личность легко впадает в ажитацию (волнение); мрачность и раздражительность; потенциально суицидальное намерение.
4. Самоповреждающее пограничное расстройство (включает депрессивные и мазохистические, а также саморазрушающие личностные особенности).
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Ожоги: причины появления, симптомы, диагностика и способы лечения.
Определение
Ожоги - это травмы, возникающие в результате высокотемпературного, химического, электрического или радиационного воздействия, которое повреждает кожу и подлежащие ткани. Ингаляционной травмой называют повреждение слизистой оболочки дыхательных путей и/или легочной ткани за счет воздействия термических и/или токсикохимических факторов.
Причины появления ожогов
К наиболее частым относят термические ожоги, которые связаны с воздействием высоких температур. Обычно это ожоги горячими жидкостями и паром, реже – открытым пламенем. Контактные термические ожоги развиваются при контакте с горячими предметами или веществами, например, раскаленным металлом, горячей смолой, битумом, асфальтом и т.д.
Химические ожоги возникают вследствие агрессивного воздействия на кожу или слизистые оболочки химических веществ. Кроме ожогов эти вещества вызывают и другие поражения кожи - контактные дерматиты и экземы.
Электротравма (травма в результате действия на организм электрического тока) также может привести к ожогу и сопровождаться местной и общей реакцией. У взрослых электротравмы, как правило, связаны с профессиональной деятельностью, у детей - с использованием домашних электроприборов.
Поражения молнией встречаются с одинаковой частотой у лиц всех возрастных групп, чаще это происходит за городом у жителей сельской местности.
Лучевые ожоги вызывает ультрафиолетовое, инфракрасное и ионизирующее излучение. Солнечные ожоги кожи знакомы многим, они обусловленные чрезмерным воздействием на нее солнечных лучей. Ионизирующее излучение приводит как к местным, так и к общим изменениям в организме, получившим название «лучевая болезнь».
Ингаляционные травмы происходят при вдыхании горячего воздуха, пара и/или под действием токсичных химических соединений (продуктов горения), попадающих в дыхательные пути вместе с дымом.
Классификация ожогов
По этиологии (причинам) формирования:
- Термические ожоги (пламенем, кипятком, контактные).
- Электрические ожоги.
- Химические ожоги.
- Лучевые ожоги.
- Смешанные ожоги.
- Ингаляционные травмы:
- термические (термоингаляционное поражение дыхательных путей);
- токсикохимические (острые ингаляционные отравления продуктами горения);
- термохимические (смешанные).
- I степень – ожоги на уровне верхних слоев эпидермиса.
- II степень – поражение на всю глубину эпидермиса.
- III степень – некроз (омертвление) поверхностных и/или глубоких слоев кожи, включая дерму.
- IV степень – некроз всех слоев тканей (обугливание).
По площади повреждения ожоги делятся на ограниченные (локальные) и обширные.
![Степени ожогов.jpg]()
Симптомы ожогов
Клиническая картина ожоговых состояний зависит от глубины и площади поражения и включает местные и общие проявления. Для поверхностных ожогов, площадь которых составляет менее 10% поверхности тела, характерны только местные проявления. Ожоги I степени проявляются отечностью, гиперемией (покраснением) кожи, выраженной болезненностью. При II степени образуются пузыри, заполненные прозрачной жидкостью. Для ожогов III и IV степени характерно появление пузырей с геморрагическим (кровянистым) содержимым, обугливание кожи, подкожной жировой клетчатки и подлежащих тканей вплоть до костей; болевая и тактильная чувствительность отсутствуют.
При поражении органов зрения больной жалуется на сильную резь в глазах, светобоязнь, отек и покраснение век и конъюнктивы.
При ингаляционных ожогах отмечается осиплость голоса, кашель со скудной вязкой, возможно, черной мокротой (копотью). Часто сопровождаются ожогами лица, шеи, передней поверхности грудной клетки.
Распространенные поверхностные ожоги (более 30% поверхности тела у взрослых) и глубокие ожоги (более 10% поверхности тела у взрослых), а также ожоги меньшей площади и глубины у детей и пожилых людей или у лиц с хроническими заболеваниями сопровождаются развитием ожоговой болезни.
Выделяют несколько стадий этого состояния.
Ожоговый шок продолжается от 12 до 72 часов и связан с нарушением кровообращения и водно-солевого баланса. Сразу после травмы пострадавший возбужден, у него может повышаться давление, учащаться пульс и дыхание, через 1-2 часа возбуждение сменяется заторможенностью, наблюдаются озноб, мышечная дрожь, повторяющаяся рвота, температура тела может как повышаться, так и снижаться. Отмечается уменьшение количества мочи, при этом моча приобретает темный цвет.
Следующая стадия – острая токсемия, которая развивается вследствие всасывания в кровь продуктов распада поврежденных тканей и длится до 10-15 дней. Эта стадия проявляется самыми разнообразными нарушениями психики (возбуждением, спутанностью сознания, галлюцинациями, нарушениями сна), а также поражением внутренних органов (сердца, легких, органов желудочно-кишечного тракта), поэтому у пациента наблюдаются перебои в работе сердца, кашель, одышка, боль в животе. Третий период – септикотоксемия, продолжающаяся от 2-3 недель до 2-3 месяцев. Проявления связаны с гнойными осложнениями (обильным гнойным отделяемым из раны, плохо заживающей раной), пациент испытывает вялость, отсутствие аппетита, снижается вес.
Прогноз в каждом конкретном случае определяется распространенностью поражения, исходным состоянием здоровья пострадавшего и адекватностью проводимого лечения.
Диагностика ожогов
Постановка диагноза, как правило, затруднений не вызывает. Для определения тактики лечения врач оценивает выраженность болевого синдрома, площадь и глубину ожогов, наличие признаков сочетанной травмы, поражения дыхательных путей, ожогового шока.Поскольку при обширных, глубоких ожогах в той или иной степени страдают все органы и системы организма, проводится расширенная лабораторная и инструментальная диагностика.
Лабораторная диагностика может включать самый разнообразный спектр анализов.
-
Клинический анализ крови.
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Отек мозга: причины появления, при каких заболеваниях возникает, диагностика и способы лечения.
Определение
Отек мозга – это состояние, характеризующееся накоплением жидкости в клетках и межклеточном пространстве мозга с увеличением объема содержимого черепа и повышением внутричерепного давления (ВЧД).
Содержимое полости черепа условно можно разделить на три части: паренхима мозга, ликвор и кровь. На вещество мозга приходится 80–85% объема (около 1200 мл), на ликвор и кровь 5-15% и 3-6% соответственно. Внутри- и внеклеточная жидкость в мозге составляет 60-70% всего внутричерепного объема. В течение суток у здорового человека вырабатывается и поглощается до 500-600 мл ликвора.
Ткань мозга – это гетерогенная (неоднородная) среда с переменными свойствами, практически несжимаемая. Увеличение объема одного из компонентов черепа приводит к уменьшению других.
Гидростатическое давление цереброспинальной жидкости в системе желудочков мозга и в субарахноидальном пространстве, оказываемое на полушария мозга, называется внутричерепным давлением (ВЧД), которое в норме составляет 7-15 мм рт. ст.
Выделяют следующие степени внутричерепной гипертензии:
- 1-я степень (умеренно повышенное ВЧД) – 15–20 мм рт. ст.;
- 2-я степень (повышенное ВЧД) - 20–40 мм рт. ст.;
- 3-я степень (значительно повышенное) – свыше 40 мм рт. ст.
Разновидности отека мозга
По распространенности отека головного мозга (ОГМ) различают:
- локальный отек,
- трифокальный отек,
- долевой полушарный отек,
- диффузный отек.
При отеке головного мозга выделяют три клинических синдрома:
- Общемозговой синдром, возникающий вследствие повышения внутричерепного давления.
- глазодвигательные расстройства (III и VI пары),
- менингеальные симптомы,
- гиперрефлексия,
- заторможенность, снижение памяти.
- Синдром диффузного рострокаудального нарастания неврологической симптоматики (очаговых и стволовых синдромов), возникающий в результате постепенного вовлечения в процесс корковых, затем подкорковых и в конечном итоге стволовых структур мозга.
- Синдром дислокации мозговых структур, возникающий как следствие смещения больших полушарий мозга и/или полушарий мозжечка и приводящий к компрессии ствола мозга, характеризуется последующим нарушением жизненно важных функций дыхания и кровообращения. Поражаются глазодвигательные нервы, сужаются поля зрения, повышается тонус мышц, урежается пульс, нарушается функция глотания, появляется ригидность мышц затылка, может быть остановка дыхания.
- окклюзионный – при блокаде ликворопроводящих путей,
- арезорбтивный – вследствие нарушения всасывания ликвора.
- КТ головного мозга и черепа и МРТ головного мозга позволяют выявить у больного опухоли, кисты, сосудистые мальформации, аневризмы, отек. По результатам повторных исследований можно следить за изменениями объема головного мозга и выявляемой в ней зоны отека, за сопутствующими деформациями мозговых структур и изменением формы и размера желудочков мозга.
Отек средних отделов ствола мозга (мост) вызывает периодическое дыхание, двустороннее максимальное сужение зрачков (миоз). Распространение отека на продолговатый мозг приводит к нарастанию нарушений жизненно-важных функций: дыхания и сердечно-сосудистой деятельности.
У пациентов отмечается распространенная мышечная гипотония, арефлексия глубоких рефлексов, расширение обоих зрачков с отсутствием их реакции на свет, глазные яблоки неподвижны.
Возможными причинами развития ОГМ могут быть травмы, нарушение мозгового кровообращения, гипертонический криз, геморрагический и ишемический инсульт, опухоли мозга, энцефалит или менингоэнцефалит, гипоксическая энцефалопатия, токсическая энцефалопатия, облучение мозга, эпилептический статус.
В развитии отека мозга преобладающими могут быть сосудистые (вазогенные) причины, тканевые факторы, цитотоксические и осмотические процессы. Форма отека мозга зависит от характера обусловившего его патологического процесса и возраста больного.
В настоящее время принято деление ОГМ на несколько основных видов.
-
Цитотоксический отек мозга характеризуется перераспределением воды из межклеточного во внутриклеточный сектор мозговой ткани и сохранностью проницаемости гематоэнцефалического барьера (ГЭБ) для белка в результате нарушения функции клеточных мембран.
Обычно имеет место сочетание нескольких видов отека мозга или определенная последовательность их развития.
Так, при черепно-мозговой травме в первые часы преобладают явления вазогенного отека, к которому в дальнейшем присоединяется цитотоксический. При ишемии головного мозга сначала развивается цитотоксический, а затем вазогенный отек.
Жидкость при отеке накапливается в ткани головного мозга неравномерно: в белом веществе она располагается преимущественно во внеклеточных пространствах, в сером – внутри клеток.
К каким врачам обращаться при отеке мозга
Диагностикой и лечением отека головного мозга занимается врач-реаниматолог в условиях отделения интенсивной терапии совместно с врачом-невропатологом .
Осмотр окулиста позволяет выявлять застойные диски зрительных нервов глазного дна.
Диагностика и обследования при появлении запаха аммиака
Диагноз ОГМ основывается на клинических данных и данных дополнительных методов исследования.
Для определения степени угнетения сознания используют шкалу Глазго:
15 баллов – ясное сознание;
13–14 баллов – умеренное оглушение;
10–12 баллов – глубокое оглушение;
8–9 баллов – сопор;
6–7 баллов – умеренная кома;
4–5 баллов – глубокая кома;
3 балла – терминальная (запредельная) кома.К методам, подтверждающим диагноз ОГМ, относят данные МРТ, компьютерной томографии (КТ) и нейросонографии (у новорожденных и детей до года), электроэнцефалографии (ЭЭГ), Эхо-ЭС, нейрофтальмоскопии, церебральной ангиографии, сканирования мозга с применением радиоактивных изотопов, ангиографии, сонографии зрительного нерва и люмбальной пункции.
Применение комплекса исследований у больных, находящихся в критических состояниях, позволяет провести раннюю диагностику отека и осуществить динамический контроль над течением процесса.
Сканирование головного мозга, черепа и окружающих их тканей, позволяющее диагностировать различные патологии.
Читайте также: