Ожог легких у новорожденных при родах
Обновлено: 25.04.2024
Ателектаз легких у новорожденных – это нерасправление легочных альвеол или их спадение после периода функционирования в течение первых двух суток жизни, связанное с особенностями строения дыхательных путей у новорожденных, а также с несовершенством центральной регуляции дыхания. Проявляется одышкой различной степени, цианозом, в тяжелых случаях – сердечной недостаточностью и признаками шока. Диагностируется клинически, подтверждается при помощи рентгенографии легких и бронхоскопии. Лечение ателектаза легких у новорожденных включает респираторную поддержку, стимуляцию синтеза сурфактанта, бронходилататоры, устранение причины патологии.
МКБ-10



Общие сведения
Ателектаз в дословном переводе означает «неполное расправление», что в целом отражает анатомическую основу состояния. Ателектаз легких у новорожденных входит в понятие «синдром дыхательных расстройств». Общая частота последнего составляет около 1% среди всех новорожденных, а у недоношенных детей с массой тела менее 2 500 г встречается в 14% случаев. Актуальность проблемы для современной педиатрии связана с большим количеством причин спадения легочной ткани в первый месяц жизни ребенка. Практически единственным способом терапии остается ИВЛ, которая часто проводится в течение длительного времени. Если ателектаз легких у новорожденных не купируется в течение нескольких дней, с большой долей вероятности присоединяется пневмония, что значительно ухудшает прогноз для жизни ребенка.

Причины
После рождения малыша воздух впервые попадает в легкие и расправляет их. Движения диафрагмы создают отрицательное давление в грудной полости, а легочно-альвеолярный секрет (сурфактант) препятствует спадению ткани альвеол за счет поверхностного натяжения. К моменту рождения количество выделяемого сурфактанта невелико, особенно у недоношенных детей. Вне зависимости от срока гестации центральные механизмы регуляции дыхания также продолжают закрепляться. Таким образом, причиной развития ателектаза легких у новорожденных является возрастная незрелость легких и нервной регуляции акта дыхания.
Нерасправлению легких могут способствовать многие патологические состояния.
- При муковисцидозе накапливающаяся в бронхах вязкая слизь механически закрывает просвет дыхательных путей, приводя к развитию ателектаза легких у новорожденных.
- Обструкцию бронхов вызывают также опухоли и частицы пищи, хотя это случается намного реже. Аспирация обычно происходит при наличии врожденных свищей между пищеварительным трактом и трахеей.
- Плевральный выпот сдавливает легкое снаружи, что также может привести к его спадению, однако в данном случае многие специалисты говорят о коллапсе.
- Кроме того, ателектаз легких у новорожденных формируется при параличе нервов, например, диафрагмы.
Классификация
Выделяют рассеянный и обширный ателектаз. В первом случае участки безвоздушной легочной ткани мелких размеров располагаются по всей поверхности легких. Обширный ателектаз бывает сегментарным и полисегментарным, затрагивая, соответственно, один или несколько сегментов легкого. Редко встречается тотальный ателектаз легких у новорожденных, когда выключенным из акта дыхания оказывает одно или оба легких (в последнем случае быстро наступает летальный исход). Сегментарная форма чаще встречается у детей, рожденных в срок. Для недоношенных малышей больше характерно диссеминированное расположение участков ателектаза.

Симптомы
Если причиной образования безвоздушных участков является обструкция дыхательных путей, симптомы отмечаются с момента рождения. Ребенок не кричит, кожные покровы быстро приобретают цианотичный оттенок. В большинстве случаев первые признаки появляются через несколько часов после родов. Обширный ателектаз легких у новорожденных проявляется одышкой, втяжением уступчивых мест грудной клетки, в том числе грудины, положение которой напоминает воронкообразную деформацию. Возможно некоторое западение грудной клетки с пораженной стороны. Быстро присоединяется сердечная недостаточность. Рассеянный ателектаз отличается отсутствием дыхательных движений на стороне спадения легкого. Дыхание часто стонущее («дыхание трубача»).
Диагностика
Дыхательная недостаточность у недоношенного ребенка позволяет заподозрить ателектаз, поскольку это состояние часто встречается при родах раньше срока. Клинически диагностировать спадение ткани легких педиатр может по втяжению межреберных промежутков и грудины и отсутствию дыхательных движений с одной стороны. Физикальный осмотр обнаруживает равномерно ослабленное дыхание, крепитацию по всей поверхности легких и коробочный звук при наличии рассеянного ателектаза легких у новорожденных. Сегментарная форма характеризуется отсутствием дыхательных шумов в безвоздушной области.
Диагноз подтверждается рентгенологически. Рассеянный ателектаз легких у новорожденных на рентгеновском снимке представлен множественными участками затемнения небольших размеров. Характерно преимущественно паравертебральное расположение безвоздушных областей. Сегментарный ателектаз легких у новорожденных выглядит, как обширный участок затемнения. При высокой разрешающей способности аппаратуры можно заметить сморщенный участок легочной ткани возле корня легкого. Часто отмечается смещение сердца в пораженную сторону и более высокое стояние диафрагмы со стороны ателектаза. Для подтверждения диагноза, особенно при подозрении на обструкцию дыхательных путей, показана бронхоскопия.

Лечение ателектаза легких у новорожденных
Лечение проводится в отделении интенсивной терапии. Показан кувезный режим. Основа терапии – вентиляция легких (вспомогательная или искусственная) с положительным давлением на вдохе для механического расправления легочной ткани. Стимуляторы синтеза сурфактанта особенно показаны недоношенным детям, возможно также эндотрахеальное введение препаратов. Проводится инфузионная терапия, осуществляется коррекция метаболического ацидоза, связанного с дыхательной недостаточностью. Для расширения бронхов применяются метилксантины. По показаниям используются препараты для лечения сердечной недостаточности.
Прогноз и профилактика
Прогноз ателектаза легких у новорожденных зависит от срока гестации, размеров участка легкого, выключенного из дыхания, и состояния, послужившего причиной развития данной патологии. Рассеянные ателектазы у недоношенных детей обычно исчезают в течение первого месяца жизни. Сегментарные ателектазы при адекватной терапии расправляются в течение примерно одной недели. Наиболее тяжелое течение отмечается в случае присоединения пневмонии, хотя воспаление легких часто само по себе является причиной ателектаза легких у новорожденных. В данном случае нагрузка на легкие возрастает за счет воспалительного процесса и интоксикации. Кроме того, продлевается срок нахождения на ИВЛ, что также повышает риск развития осложнений.
1. Судебно-медицинское значение первичного ателектаза легких и синдрома дыхательного расстройства у новорожденных/ Недугов Г.В., Ардашкин А.П.// Проблемы экспертизы в медицине. - 2005.
2. Особенности рентгенологических изменений в легких у недоношенных новорожденных с дыхательной недостаточностью/ Перепелица С.А., Голубев А.М., Мороз В.В.// Общая реаниматология. - 2011.
3. Возможности ультразвукового исследования в комплексной диагностике заболеваний легких в неонатальном периоде/ Колтунов И.Е., Дягтерева М.В.// Трудный пациент. - 2017. и др.
Синдром аспирации мекония – состояние острой дыхательной недостаточности вследствие внутриутробного попадания в легкие ребенка мекониальных масс с закупоркой просвета бронхов. Характерен синюшный оттенок кожи с рождения, тяжелое шумное дыхание с западением уступчивых мест груди. Состояние расценивается как тяжелое. Синдром аспирации мекония диагностируется на основании внешних признаков дыхательной недостаточности, физикального осмотра и рентгенографической картины. Лечение комплексное, направлено на механическое очищение бронхиального дерева, усиленную оксигенацию и борьбу с инфекционными осложнениями.
Общие сведения
Синдром аспирации мекония – поражение легких новорожденного с высокой вероятностью летального исхода. Смертность достигает 10%, связана с массивной аспирацией мекониальных масс и развитием септического состояния. Частицы первородного кала определяются в амниотической жидкости у 5-20% рожениц, однако заболевание возникает не всегда. Синдром аспирации мекония встречается с частотой около 2-4%. Обычно развивается у доношенных и переношенных детей, у недоношенных встречается реже в связи с особенностями нервной системы, практически исключающими пассаж мекония в околоплодные воды. Является одной из важнейших проблем современной педиатрии в связи с многофакторностью развития и трудностями терапии. В частности, нередко необходимо длительное нахождение ребенка на ИВЛ, что может служить дополнительной причиной развития резистентных к лечению пневмоний.

Причины синдрома аспирации мекония
Хотя этиология состояния продолжает изучаться, большинство исследователей склоняются к гипоксической природе синдрома аспирации мекония. Недостаток кислорода, который возник внутриутробно или в процессе родов, рефлекторно повышает тонус парасимпатической нервной системы. Одновременно происходит централизация кровоснабжения, то есть перераспределение крови с преимущественной циркуляцией в жизненно важных органах (сердце, легкие, мозг) в ущерб всем остальным органам и системам, в том числе кишечнику. Эти два фактора в сумме приводят к гипоксии сосудов брыжейки и рефлекторному расслаблению гладкой мускулатуры кишечника. Как следствие, происходит пассаж первородного кала в околоплодные воды с дальнейшим попаданием в легкие.
Существует большое количество возможных причин гипоксии. Чаще всего дефицит поступления кислорода связан с патологией плаценты, поскольку именно плацентарный кровоток является источником кислорода во внутриутробном периоде развития. Как правило, речь идет о хронической фетоплацентарной недостаточности, обусловленной соматическими заболеваниями матери (в частности, сахарным диабетом и артериальной гипертензией), патологией сосудов плаценты и т. д. Второй вариант – это патологии пуповины или механическое сдавление дыхательных путей (обвитие), что также запускает описанные выше механизмы, приводящие к появлению мекония в околоплодных водах. Определенную роль играет большой вес плода и малое количество амниотической жидкости.
Симптомы и диагностика синдрома аспирации мекония
Синдром аспирации мекония может развиваться с первых минут жизни или спустя несколько часов и даже дней после периода мнимого благополучия. Во многом это зависит от того, как долго малыш испытывал гипоксию, находясь в утробе матери. При раннем появлении симптомов ребенок начинает испытывать трудности с дыханием сразу после рождения. Малыш тяжело и шумно дышит, заметно западение надключичных ямок, межреберных промежутков и других уступчивых мест грудной клетки. Внешне ребенок цианотичный, беспокойный, в тяжелых случаях нервная система, наоборот, угнетена, и пациент выглядит заторможенным. При отсроченном начале синдрома аспирации мекония наблюдаются те же симптомы, но время их возникновения приходится на более поздний период.
Первичная диагностика возможна еще в процессе планового обследования во время беременности. Кардиотокография плода отчетливо показывает затруднение дыхания малыша, в подобных случаях необходимо дальнейшее обследование и поиск причин гипоксии, в частности – анализ амниотической жидкости для выявления в ней частиц мекония. Возможно решение вопроса о досрочном родоразрешении. В процессе интранатальной диагностики синдрома аспирации мекония обращает на себя внимание зеленоватый цвет околоплодных вод, иногда частицы мекония удается визуализировать. Также часто наблюдается зеленоватый цвет ногтей, кожи и пуповины малыша, что, как правило, свидетельствует в пользу длительной внутриутробной гипоксии и тяжелого течения синдрома аспирации мекония.
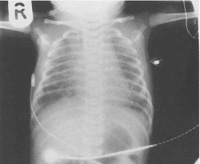
Аускультативно педиатр прослушивает разнокалиберные хрипы, при перкуссии легких участки приглушения чередуются с участками с коробочным звуком. Данные физикального осмотра подтверждаются рентгенографически. На снимке определяются участки ателектаза (спадания альвеол) и эмфиземы (патологического расширения дистальных отделов легких). Такая картина является следствием механической закупорки частицами мекония просвета мелких бронхов, а также вторичного воспалительного процесса, обусловленного токсичностью мекониальных масс. В тяжелых случаях на рентгенограмме обнаруживается так называемая «снежная буря», когда почти вся поверхность альвеол спадается, и остается множество эмфизематозно расширенных участков, неспособных обеспечить циркуляцию воздуха.
Лечение синдрома аспирации мекония
Если синдром аспирации мекония диагностируется еще до родов, то уже в процессе родоразрешения, когда рождается головка, необходимо произвести отсасывание специальным катетером Де Ли. Одна только эта манипуляция, выполненная как можно раньше, позволяет частично освободить верхние дыхательные пути и значительно улучшить оксигенацию. После рождения пациентам с синдромом аспирации мекония проводится лаваж (введение физиологического раствора в трахею с последующим отсасыванием до чистого отделяемого). При наличии выраженной дыхательной недостаточности показано подключение новорожденного к системе ИВЛ.
Важно учитывать, что к моменту подключения ИВЛ легкие должны быть очищены, поскольку в противном случае возможно продвижение оставшихся частиц мекония в дистальные отделы с последующим усугублением дыхательной недостаточности. С целью более быстрого расправления участков ателектаза назначается сурфактант, иногда – оксид азота. Обязательно применение антибиотиков, поскольку частым осложнением синдрома аспирации мекония является аспирационная пневмония. В наиболее тяжелых случаях выполняется экстракорпоральная мембранная оксигенация. Все манипуляции проводятся в отделении реанимации.
Прогноз и профилактика синдрома аспирации мекония
Основным фактором, провоцирующим развитие синдрома аспирации мекония, является внутриутробная гипоксия, поэтому все профилактические мероприятия проводятся в период беременности. Необходима своевременная диагностика и лечение фетоплацентарной недостаточности и соматических заболеваний матери. Стоит избегать перенашивания, которое также повышает риск синдрома аспирации мекония. Прогноз заболевания неблагоприятный. Летальность составляет 10%, выжившие дети в дальнейшем часто имеют хронические легочные патологии. Возможно отставание в развитии вследствие длительной гипоксии.
Родовая травма новорожденных – различные повреждения плода, возникающие в процессе родового акта. Среди родовых травм новорожденных встречаются повреждения мягких тканей (кожи, подкожной клетчатки, мышц), костной системы, внутренних органов, центральной и периферической нервной системы. Родовая травма новорожденных диагностируется с учетом акушерско-гинекологического анамнеза матери, особенностей течения родов, данных осмотра новорожденного и дополнительных исследований (ЭЭГ, УЗИ, рентгенографии, офтальмоскопии и др.). Лечение родовых травм новорожденных проводится дифференцированно с учетом вида и тяжести повреждения.
Общие сведения

Классификация родовых травм новорожденных
В зависимости от локализации повреждения и преимущественного нарушения функций выделяют следующие виды родовой травмы новорожденных:
1. Родовые травмы мягких тканей (кожи, подкожной клетчатки, мышц, родовая опухоль, кефалогематома).
2. Родовые травмы костно-суставной системы (трещины и переломы ключицы, плечевых и бедренных костей; травматический эпифизеолиз плечевой кости, подвывих суставов С1 и С2, повреждение костей черепа и др.).
3. Родовые травмы внутренних органов (кровоизлияния во внутренние органы: печень, селезенку, надпочечники).
4. Родовые травмы центральной и периферической нервной системы у новорожденных:
- внутричерепная родовая травма (эпидуральные, субдуральные, субарахноидальные, интравентрикулярные кровоизлияния)
- родовая травма спинного мозга (кровоизлияния в спинной мозг и его оболочки)
- родовая травма периферической нервной системы (повреждение плечевого сплетения - парез/паралич Дюшена-Эрба или паралич Дежерин-Клюмпке, тотальный паралич, парез диафрагмы, повреждение лицевого нерва и др.).
Причины
Анализ причин родовой травмы новорожденных позволяет выделить три группы факторов, повышающих вероятность ее возникновения: относящихся к матери, к плоду, а также к течению и ведению родов.
Предрасполагающими «материнскими» факторами могут выступать ранний или поздний репродуктивный возраст, гестозы, узкий таз, гипоплазия или гиперантефлексия матки, заболевания беременной (сердечно-сосудистые, эндокринные, гинекологические и др.), переношенная беременность, профессиональные вредности и т. д.
Наиболее обширную группу причин, приводящих к родовой травме новорожденных, составляют обстоятельства, связанные с плодом. Провоцировать родовую травму может тазовое предлежание плода, маловодие, неправильное (асинклитическое или разгибательное вставление головки), недоношенность, крупные размеры плода, аномалии развития плода, внутриутробная гипоксия и асфиксия и др.
К возникновению родовой травмы новорожденного могут приводить аномалии родовой деятельности: затяжные или быстрые роды, родостимуляция при слабой родовой деятельности, дискоординированная или чрезмерно сильная родовая деятельность. Серьезную группу причин родовых травм новорожденных составляет неправильное или необоснованное применение акушерских пособий (поворота плода на ножку, наложение акушерских щипцов, использование вакуум-экстрактора, проведение кесарева сечения и др.).
Как правило, при возникновении родовых травм новорожденных имеет место сочетание ряда неблагоприятных факторов, нарушающих нормальную биомеханику родов.
Различные виды травм новорожденных
Родовые травмы мягких тканей
Самыми частыми проявлениями родового травматизма новорожденных являются повреждения кожи и подкожной клетчатки. К ним относятся царапины, ссадины, петехии, экхимозы на различных участках тела. Такие повреждения выявляются при визуальном осмотре новорожденного неонатологом; обычно они не опасны и требуют лишь местной антисептической обработки и наложения асептической повязки. Незначительные родовые травмы мягких тканей исчезают к исходу первой недели жизни новорожденного.
Разновидностью родовой травмы новорожденных является родовая опухоль, которая характеризуется локальной припухлостью мягких тканей головы. Родовая опухоль имеет мягкоэластическую консистенцию, синюшный цвет с множественными петехиями и экхимозами. Ее возникновение обычно связано с затяжными родами в головном предлежании или наложением акушерских щипцов. Родовая опухоль лечения не требует, исчезает самостоятельно через 1-3 суток.
Более тяжелым видом родовой травмы новорожденных служит повреждение (кровоизлияние, разрыв) грудино-ключично-сосцевидной мышцы, обычно ее нижней трети. В этом случае в месте повреждения определяется небольшая опухоль умеренно плотной или тестоватой консистенции. Повреждение грудино-ключично-сосцевидной мышцы может быть выявлено не сразу, а примерно через неделю, когда у ребенка развивается кривошея. В лечении родовой травмы грудино-ключично-сосцевидной мышцы у новорожденных используется корригирующее положение головы с помощью валиков, сухое тепло, электрофорез йодистого калия, массаж; при неэффективности – хирургическая коррекция.
Кефалогематома, как разновидность родовой травмы новорожденных, характеризуется кровоизлиянием под надкостницу теменных или затылочной костей черепа. Типичными признаками кефалогематомы служат упругая консистенция, отсутствие пульсации, безболезненность, флюктуация, наличие валика по периферии. В дальнейшем у новорожденных с кефалогематомой может отмечаться желтуха, вызванная повышенным внесосудистым образованием билирубина. Кефалогематома уменьшается в размерах к 2-3 неделе жизни, а полностью рассасывается к исходу 6-8 недели. К осложнениям поднадкостничной родовой травмы новорожденных относится анемия, обызвествление и нагноение кефалогематомы. Дети с большими (более 6 см в диаметре) кефалогематомами нуждаются в проведении рентгенографии черепа для исключения трещин костей. Поскольку у недоношенных детей кефалогематомы часто ассоциированы с внутриутробным микоплазмозом, требуется проведение ПЦР или ИФА диагностики.
В большинстве случаев родовые травмы мягких тканей у новорожденных проходят без последствий.
Родовые травмы костной системы
Среди родовых травм костно-суставной системы у новорожденных чаще встречаются повреждения ключицы и костей конечностей. Они всегда относятся к чисто акушерским видам повреждений. Поднадкостничные переломы ключицы без смещения обычно обнаруживаются через 3-4 дня после родов по наличию веретенообразной плотной припухлости - формирующейся костной мозоли. Перелом ключиц со смещением сопровождается невозможностью выполнения активных движений, болью, плачем при пассивном движении руки, припухлостью и крепитацией над местом перелома.
При переломе плечевой или бедренной кости отсутствуют активные движения в конечностях, возникает болевая реакция на пассивные движения, имеется отек, деформация и укорочение поврежденной конечности. При любых видах переломов новорожденные нуждаются в консультации детского травматолога, проведении рентгенологической диагностики (рентгенографии ключицы, рентгенографии трубчатых костей). При переломе ключицы проводится кратковременная иммобилизация руки путем наложения повязки Дезо или плотного пеленания. При переломах плечевой и бедренной костей выполняется репозиция костей верхней или нижней конечности и наложение гипсовой повязки (при необходимости – вытяжение).
Разновидностью родовой травмы костной системы новорожденных является травматический эпифизеолиз плечевой кости. Его проявлениями служат болезненность, припухлость и крепитация в области плечевого или локтевого суставов, ограничение объема движений в пораженной руке. Исходом подобной травмы может являться парез лучевого нерва, формирование сгибательной контрактуры в суставах. Лечение состоит в иммобилизации конечности, проведении физиотерапевтических процедур, массажа.
Родовые травмы внутренних органов
Повреждения внутренних органов возникают вследствие механического воздействия на плод при аномальном течении родов. Наиболее часто встречаются кровоизлияния в печень, селезенку и надпочечники. Клинические проявления родовой травмы внутренних органов у новорожденных развиваются на 3-5 сутки в связи с внутренним кровотечением. При разрыве гематомы возникает вздутие живота, развивается парез кишечника, мышечная гипотония (или атония), угнетение физиологических рефлексов, артериальная гипотония, упорные срыгивания и рвота.
При подозрении на родовую травму внутренних органов новорожденным производится обзорная рентгенография брюшной полости, УЗИ органов брюшной полости и УЗИ надпочечников. Лечение заключается в проведении гемостатической и симптоматической терапии; при необходимости – лапароскопии или лапаротомии с ревизией внутренних органов.
При кровоизлиянии в надпочечники у ребенка может развиться острая или хроническая надпочечниковая недостаточность. Прогноз при родовой травме внутренних органов у новорожденных определяется объемом и тяжестью поражения, своевременностью выявления повреждения.
Родовые травмы центральной и периферической нервной системы
Повреждения нервной системы у новорожденных составляют наиболее обширную группу родовых травм. В рамках данного обзора остановимся на родовой травме спинного мозга и периферической нервной системы; подробная характеристика внутричерепных родовых травм новорожденных будет дана в соответствующей статье.
Родовые травмы спинного мозга у новорожденных могут включать кровоизлияние, растяжение, сдавление или разрыв спинного мозга на различном уровне, связанные с переломом позвоночника или возникающие без него. Тяжелые повреждения характеризуются клиникой спинального шока: вялостью, мышечной гипотонией, арефлексией, слабым криком, диафрагмальным дыханием. Гибель детей может наступить от дыхательной недостаточности. В более благоприятных случаях происходит постепенный регресс явлений спинального шока; на смену гипотонии приходит спастика; развиваются вегетативные нарушения (вазомоторные реакции, потливость), трофические изменения в мышечной и костной ткани. Родовые травмы легкой степени у новорожденных сопровождаются преходящей неврологической симптоматикой: изменением тонуса мышц, рефлекторных и двигательных реакций.
Постановке диагноза способствует осмотр ребенка детским неврологом, проведение рентгенографии или МРТ позвоночника, электромиографии, люмбальной пункции и исследования цереброспинальной жидкости. Лечение родовой травмы спинного мозга у новорожденных включает иммобилизацию области повреждения, проведение дегидратационной и противогеморрагической терапии, восстановительных мероприятий (ортопедического массажа, ЛФК, электростимуляции, физиотерапии).
Родовые травмы периферической нервной системы у новорожденных объединяют повреждения корешков, сплетений, периферических и черепных нервов.
С учетом локализации парез плечевого сплетения (акушерский парез) может быть верхним (проксимальным), нижним (дистальным) или тотальным. Верхний парез Дюшенна–Эрба связан с повреждением сплетений и корешков, берущих начало в сегментах С5-С6, что сопровождается нарушением функции проксимального отдела верхней конечности. В этом случае ребенок принимает характерное положение с рукой, приведенной к туловищу, разогнутой в локтевом суставе, повернутой внутрь в плече и пронированной в предплечье; согнутой в ладони кистью и головой, наклоненной к больному плечу.
При нижнем акушерском парезе Дежерина-Клюмпке поражаются сплетения или корешки, берущие начало от С7-Т1, следствием чего служит нарушение функции дистального отдела руки. Проявления включают мышечную гипотонию, гипестезии, ограничение движений в лучезапястном и локтевом суставах, пальцах руки, симптом «когтистой лапы». При тотальном типе акушерского пареза рука полностью бездействует, резко выражена мышечная гипотония, рано развивается атрофия мышц.
Диагноз и локализация повреждения уточняется с помощью электромиографии. Лечение родовой травмы плечевого сплетения у новорожденных состоит в иммобилизации руки с помощью лонгеты, проведении массажа, ЛФК, физиопроцедур (аппликаций озокерита, парафина, электростимуляции, электрофореза), лекарственной терапии.
При парезе диафрагмы у новорожденного развивается одышка, парадоксальное дыхание, цианоз, выбухание грудной клети на пораженной стороне. Выявлению пареза способствует рентгеноскопия и рентгенография грудной клетки, при которых определяется высокое стояние и малоподвижность купола диафрагмы. На этом фоне у детей может развиться застойная пневмония. Лечение родовой травмы заключается в чрескожной стимуляции диафрагмального нерва; при необходимости – ИВЛ до восстановления адекватного самостоятельного дыхания.
Парез лицевого нерва связан с повреждение ствола или ветвей лицевого нерва. В этом случае у ребенка отмечается асимметрия лица, лагофтальм, смещение глазного яблока вверх при крике, асимметрия рта, затруднение сосания. Родовая травма у новорожденных диагностируется на основании клинических признаков, электронейрографии, регистрации вызванных потенциалов. Нередко парез лицевого нерва проходит без специального лечения; в других случаях проводится теплолечение, медикаментозная терапия.
К более редким видам родовых травм новорожденных относятся травмы глоточного, срединного, лучевого, седалищного, перонеального нерва, пояснично-крестцового сплетения.
Профилактика
Профилактика родовых травм у новорожденных предполагает оценку степени риска их возникновения еще на этапе ведения беременности, максимально бережное отношение к ребенку в процессе родов, отказ от необоснованного использования пособий по извлечению плода и оперативного родоразрешения.
Ожоги у новорожденных детей - причины
Инфильтрация мягких тканей внутривенными жидкостями часто вызывает воспаление кожи и некроз. Гипертонические жидкости, такие как глюкоза и кальций, могут привести к полнослойному некрозу кожи и контрактурам.
Очаги обычно заживают в течение недель и месяцев, и могут потребоваться наложение шины, физиотерапия и хирургическая коррекция, особенно если такие очаги расположены над суставами.
Удаление пластырей, применяющихся для закрепления повязок, эндотрахеальных и назотрахеальных трубок, а также проводов от мониторов, может привести к обширной травме кожи. Хотя полнослойный некроз кожи развивается редко, типична поствоспалительная гипо- или гиперпигментация.
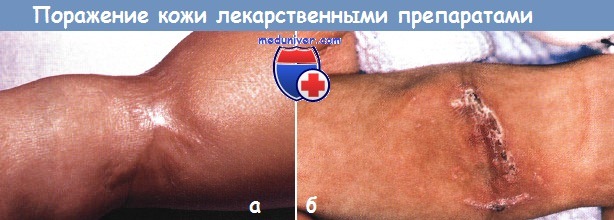
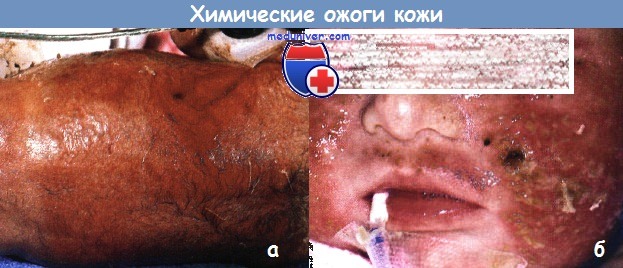
а - инфильтрация кожи на внутренней поверхности локтевого сустава 20% раствором глюкозы привела к язве, которая зажила с тяжелым рубцеванием. Хирургическая коррекция рубца была проведена в возрасте 4 лет.
б - инфильтрация тканей препаратом кальция привела к появлению болезненного красного пятна, после заживления которого осталась кольцевидная красная кальцифицированная бляшка.
Изменения пигментации сохраняются годами, особенно у детей с темным цветом кожи, но обычно заметно ослабляются в первый год жизни. Местное применение различных веществ, таких как соединения йода, мыла, детергенты и растворители, может вызвать тяжелую реакцию раздражения, особенно у недоношенных детей или детей с предшествующей кожной травмой.
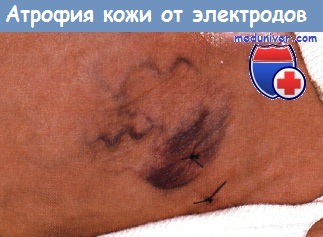
Многократная травма при снятии проводков монитора привела к появлению круглого атрофического пятна на нижней стенке брюшной полости у этого 29-недельного недоношенного ребенка.
Обратите внимание на морщинистость кожи, выступающие сосуды и пурпуру (которая присутствовала до взятия биопсии).
Случайные термические ожоги регистрировались после помещения ребенка в кроватку с водяным подогревом, инфракрасными обогревателями, в результате контакта с чрескожным анализатором кислорода и с увлажненным нагретым воздухом.
Поскольку переохлаждения недоношенного ребенка с малым весом нельзя допускать, необходим строгий контроль работы всех подобных приборов с целью предотвратить обширные ожоги с поражением кожи и дыхательных путей.
Тяжелые реакции раздражения:
а - местное применение раствора йодоформа вызвало эрозивный дерматит раздражения на боковой части туловища у недоношенного ребенка в детском отделении интенсивной терапии.
К счастью, заживление на этом участке привело лишь к минимальному рубцеванию.
б - химический ожог, вызванный растворителем, который применили на лице ребенка для удаления клейкой ленты.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Синдром аспирации мекония (САМ) – дыхательное расстройство, обусловленное попаданием мекония вместе с околоплодными водами в дыхательные пути ребенка до родов или в момент рождения [1].

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 800 RUB / 4500 KZT / 27 BYN - 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место - 800 RUB / 4500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
- Легкое течение – кислородная зависимость сохраняется менее 48 часов, новорожденный нуждается в менее чем 40% кислороде.
- Средняя степень тяжести – новорожденный нуждается в более чем 40% кислороде в течение более 48 часов, отсутствуют признаки синдрома утечки воздуха.
- Тяжелое течение – необходимость в проведении вспомогательной вентиляции легких в течение более чем 48 часов. Частым осложнением при тяжелом течении является ПЛГН.
- может встречаться вследствие обструкции дыхательных путей, воспалительного процесса, присоединения инфекционных заболеваний либо формирования шунтов.
- может развиваться практически на любой стадии, поскольку синдром мекониальной аспирации относится к заболеваниям, которые сопровождаются формированием воздушных ловушек. Эту особенность необходимо постоянно принимать во внимание при проведении реанимационных мероприятий и интенсивной терапии. Наиболее важно помнить об этом в тех ситуациях, когда внезапно происходит ухудшение состояния ребенка, либо изначально имеет место тяжелое течение заболевания.
- ранняя диагностика, исключение гипоксемии, гипотермии, гипогликемии и соблюдение лечебно-охранительного режима – наиболее важные профилактические мероприятия для предотвращения ПЛГН.
- за исключением сепсиса все остальные варианты инфекционных процессов, как правило, не провоцируют отхождение мекония;
- меконий представляет собой благоприятную среду для роста микроорганизмов, поэтому возможно развитие вторичных инфекционных процессов.
Этиология и патогенез
САМ чаще наблюдается у переношенных или доношенных новорожденных. Аспирация содержащих меконий околоплодных вод может возникнуть до родов или в момент рождения. Редко наблюдается выход мекония в околоплодные воды до полных 34 недель [2]. Появление мекония в околоплодных водах – результат стимуляции созревающего кишечника вследствие гипоксического стресса. У почти доношенного плода кишечник достаточно зрелый и вагусная стимуляция от головного мозга при компрессии пуповины или других состояниях, сопровождающихся гипоксией, может вызвать перистальтику и релаксацию ректального сфинктера, приводя к пассажу мекония. Меконий, попадая в околоплодные воды, уменьшает их антибактериальную активность и, впоследствии, увеличивает риск перинатальной бактериальной инфекции. Однако, самое тяжелое осложнение пассажа мекония, возникшего внутриутробно - аспирация загрязненных меконием околоплодных вод. Аспирация мекониальными водами может возникнуть, если у плода на фоне прогрессирующей гипоксии развивается дистресс, приводящий к возникновению паттерна «гаспинг-дыхания». Аспирация вызывает гипоксию после рождения за счет четырех легочных эффектов: обструкция дыхательных путей, дисфункция сурфактанта, химический пневмонит, легочная гипертензия [3].
1. Обструкция дыхательных путей. Полная обструкция дыхательных путей меконием приводит к ателектазам. Частичная обструкция вызывает задержку газа (воздушные ловушки) и перерастяжение альвеол. Это часто называют «клапанным эффектом». Газ «воздушных ловушек» (перерастягивая легкое) может вызывать повреждение легкого с выходом в плевральную полость (пневмоторакс), средостение (пневмомедиастинум) или перикард (пневмоперикард) [4].
2. Вторичный дефицит сурфактанта. Меконий деактивирует сурфактант и может угнетать синтез сурфактанта [5, 6]. Некоторые компоненты мекония, особенно свободные жирные кислоты (пальмовая, стеариновая, олеиновая), имеют минимальное поверхностное натяжение выше сурфактанта, в результате чего уменьшается альвеолярная поверхность, вызывая диффузные ателектазы [7].
3. Аспирационный пневмонит. Энзимы, желчные соли и свободные жирные кислоты мекония раздражают дыхательные пути и паренхиму, способствуя выбросу цитокинов, которые вызывают диффузный пневмонит. Развитие асептического воспалительного процесса в респираторном отделе легких возможно через несколько часов после аспирации.
Все эти легочные эффекты могут вызвать серьезные нарушения перфузионно-вентиляционных отношений и привести к развитию персистирующей легочной гипертензии новорожденного (ПЛГН).
Эпидемиология
Диагностика
Диагностика
- острая гипоксия плода (обвитие пуповиной вокруг шеи ребенка, преждевременная отслойка плаценты и др.);
- хроническая гипоксия плода (обусловленная плацентарной недостаточностью, вызванной резус-конфликтом, сахарным диабетом у матери, артериальной гипертензией у матери, преэклампсией и эклампсией);
- курение, наркомания (особенно, кокаин) [2].
- Рекомендуется на этапе постановки диагноза оценить симптомы дыхательных расстройств у новорожденного по шкале Доунс (Приложение Г1) [16].
Комментарии: Клинически развернутый синдром мекониальной аспирации, как правило, развивается в первые 48 часов после рождения. Ребенок, родившийся в мекониальных околоплодных водах, требует интенсивного наблюдения динамики состояния с целью мониторинга развития дыхательных нарушений. Первая оценка степени дыхательной недостаточности должна быть произведена в возрасте 1 часа после рождения [15]. Клинически развернутый САМ включает в себя: наличие мекония в амниотической жидкости, респираторный дистресс в возрасте первых нескольких часов жизни (одышка, стон, участие вспомогательной мускулатуры, цианоз), необходимость в респираторной поддержке, исключены другие причины респираторного дистресса [1, 2, 17, 18, 19].
- Рекомендуется провести перкуссию, аускультацию легких, подсчет частоты сердечных сокращений (ЧСС) и частоты дыхания (ЧД) и измерить транскутанную сатурацию [4].
Комментарии: Вследствие образования воздушных ловушек и чрезмерного растяжения альвеол грудная клетка постепенно принимает бочкообразную форму, поэтому при перкуссии может определяться коробочный звук, чередующийся с участками притупления в связи с образованием ателектазов. При аускультации выслушивается ослабленное или жёсткое дыхание, обилие разнокалиберных хрипов.
- Рекомендуется для оценки степени тяжести дыхательной недостаточности провести анализ кислотно-основного состояния (КОС) и газов крови [20].
Комментарии: В зависимости от выраженности мекониальной аспирации может отмечаться развитие респираторного либо метаболического ацидоза вследствие гипоксемии и гиперкарбии. Ацидоз любого генеза в свою очередь увеличивает риск развития, либо потенцирует формирование персистирующей легочной гипертензии [4].
- Рекомендуется у ребенка из группы риска по развитию САМ в случае развития дыхательных расстройств выполнить бактериологическое исследование содержимого трахеи и крови на стерильность [1].
Комментарии: Выбор тактики антибактериальной терапии у новорожденных с САМ желательно проводить с учетом результатов бактериологического исследования.
- Рекомендуется выполнить общий (клинический) анализ крови развернутый с определением нейтрофильного индекса [1].
Комментарии: Необходимо проводить дифференциальный диагноз с врожденной пневмонией.
- Рекомендуется провести рентгенографию органов грудной клетки [20].
Комментарии: Мекониальная аспирация приводит к формированию характерных изменений, обнаруживаемых при рентгенографии органов грудной полости: появление диффузных, полиморфных, неоднородных по структуре узелковых инфильтратов, локальных либо генерализованных, расположенных асимметрично либо симметрично; увеличение воздушности неизмененной легочной ткани; признаки утечки воздуха; плевральный выпот; кардиомегалия. Полная окклюзия дыхательных путей приводит к формированию ателектазов. Ателектазы могут быть двусторонними, диффузными/распространенными, неоднородными по структуре и полиморфными по форме и размерам или более четкими в виде отдельных узелков. Наличие ателектазов является наиболее значимым прогностическим признаком в отношении тяжести дыхательной недостаточности и смертности. Вследствие повреждения альвеолярного эндотелия в дыхательных путях накапливается жидкость, развивается альвеолярный отек легких и появляется плевральный выпот. Частичное перекрытие просвета дыхательных путей и альвеол мекониальным детритом приводит к формированию воздушных ловушек, а также сопровождается гипервентиляцией отдельных участков легких, что рентгенологически проявляется более легким/усиленным прохождением через данную зону рентгеновских лучей, а также более низким стоянием диафрагмы на стороне поражения. Чрезмерное растяжение дыхательных путей и альвеол может приводить к разрыву альвеол с последующим выходом воздуха в интерстициальное пространство, расширением интерстициальных лимфатических сосудов и распространения по ним далее вышедшего воздуха, а также выходом его в плевральную полость и средостение. Кардиомегалия может быть следствием перенесенной асфиксии, либо отсроченным проявлением персистирующей легочной гипертензии новорожденного [4].
Дифференциальный диагноз
- Транзиторным тахипноэ новорождённых и другими состояниями, сопровождающимися развитием дыхательной недостаточности в раннем неонатальном периоде.
При диагностике РДС при рентгенологическом исследовании характерными признаками являются: диффузное снижение прозрачности легочных полей (симптом «матового стекла»), контрастирование воздухом бронхов (воздушная бронхограмма). Важно отметить, что при наличии болезни гиалиновых мембран отмечается тенденция к тому, что легкие выглядят пропорционально, диффузно уменьшенными в размерах вследствие дефицита сурфактанта, в то время как при наличии САМ определяется повышенная воздушность задействованных в процессе дыхания участков легочной ткани.
Диагностика раннего неонатального сепсиса, врожденной пневмонии. Характерны положительные маркеры воспаления, определяемые в динамике в первые 72 часа жизни. Рентгенологические симптомы врожденной пневмонии неспецифичны. В большинстве случаев отмечается двустороннее поражение легочной ткани, как правило, в виде пятнистой картины легких — сочетание участков уплотнения легочной ткани и компенсаторного повышения воздушности. Может обнаруживаться выпот в плевральных полостях [21, 22, 23]. При наличии пневмонии, вызванной стрептококками группы В, на рентгенограммах отмечается усиление рисунка за счет сетчатых/зернистых структур, особенно в случае сочетания с дефицитом сурфактанта [24]. При наличии очагов уплотнения легочной ткани, они, как правило, затрагивают несколько долей. Выраженное уплотнение, ограниченное одной, отдельно взятой долей, сравнительно редко встречается у новорожденных [25].
Лечение
Рекомендуется дифференцированный подход к оказанию помощи в родильном зале новорожденным с околоплодными водами, содержащими меконий [26]. Акушеры должны заранее предупредить врачей-неонатологов, если околоплодные воды окрашены меконием и имеются признаки дистресса плода. Санация ротоглотки после рождения головки плода не снижает вероятности развития респираторного дистресс-синдрома или клинически выраженного синдрома мекониальной аспирации, включая подгруппы, где имело место наличие густого мекония, отмечались признаки дистресса у плода или родоразрешение выполнялось абдоминальным путем [19].
- Не рекомендуется рутинная интубация и санация трахеи через интубационную трубку, если на момент рождения у новорожденного ЧСС более 100 ударов в минуту, спонтанное дыхание эффективное, хороший мышечный тонус [27, 28].
Комментарии: Интубация и санация трахеи в родильном зале выполняются в соответствии с Методическим письмом №15-4/10/2-3204 от 21.04.2010 г. «Первичная и реанимационная помощь новорожденным детям». Если у ребенка сразу после рождения отмечается хороший мышечный тонус, активное самостоятельное дыхание или громкий крик, то санация трахеи не показана. Если околоплодные воды содержат меконий и у ребенка отмечается сниженный мышечный тонус, неэффективное или ослабленное самостоятельное дыхание, сразу после рождения необходимо провести интубацию трахеи с последующей санацией через эндотрахеальную трубку.
- Не рекомендуется проведение лаважа желудка при наличии окрашенных меконием околоплодных вод [29, 30].
- Рекомендуется начать респираторную поддержку в родильном зале по показаниям [26].
- Рекомендуется создать оптимальный температурный режим для уменьшения потребления кислорода и энергии [34].
Комментарии: Создание оптимального температурного режима осуществляется при помощи специального медицинского оборудования, позволяющего обеспечивать термонейтральный климат (кувез, открытая реанимационная система, матрасик с подогревом, источник лучистого тепла). Под термонейтральным климатом следует понимать температуру окружающей среды, при которой температура тела ребенка поддерживается в пределах 36,5-37,50С.
- Рекомендуется обеспечить минимизацию прикосновений к ребенку и манипуляций, особенно в случае развития ПЛГН [34].
Комментарии: Соблюдение лечебно-охранительного режима важно, поскольку беспокойство может увеличивать проявления ПЛГН и право-левое шунтирование крови, приводя к дополнительной гипоксемии и ацидозу. Может возникнуть необходимость в проведении седативной терапии для уменьшения беспокойства ребенка [35]. Санация эндотрахеальной трубки не должна быть рутинной. Проводится только по показаниям. Желательно использовать закрытые санационные системы, поскольку они позволяют наиболее оптимально уменьшить эпизоды гипоксемии, связанные с санацией, а также снизить риск инфицирования [28].
- Рекомендуется при наличии показаний начать ИВЛ [36].
Комментарии: Необходимо избегать гипоксемии и гиперкапнии, поддерживая сатурацию гемоглобина кислородом (SpO2) более 95%. Следует помнить, что доказательства эффективности применения СРАР у новорождённых с САМ отсутствуют. Кроме того, СРАР при САМ может увеличивать риск развития пневмоторакса [37].
При подтверждении САМ можно рассмотреть вопрос о проведении сурфактантной терапии [45]. Терапия сурфактантом может быть представлена в виде болюсного введения препарата или в виде лаважа трахеобронхиального дерева разведенным препаратом. При проведении лаважа жидкость вводится в легкие через дыхательные пути с последующей попыткой удаления ее посредством активного отсасывания [46, 47]. Учитывая то, что рекомендуемая при САМ методика введения сурфактанта относится к OFF-label, необходимо проведение врачебного консилиума и взятие согласия на применение методики по жизненным показаниям у законных представителей ребенка.
В тяжелых случаях проявления ПЛГН может потребоваться проведение ЭКМО при наличии технической и организационной возможности.
- Рекомендуется проведение медикаментозной синхронизации с аппаратом ИВЛ при наличии показаний [1].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2a)
Комментарии: Медикаментозная синхронизация с аппаратом ИВЛ проводится для уменьшения потребления кислорода и исключения работы дыхания в отделении реанимации и интенсивной терапии новорожденных по показаниям (особенно при развитии ПЛГН) с учетом индивидуальных особенностей. Показания: одышка более 80 вдохов в минуту, выраженное участие дыхательной мускулатуры в акте дыхания, сопротивление аппарату, при котором происходит снижение оксигенации. Используются опиоидные аналгетики и бензодиазепины [35]. Применение мышечных релаксантов может быть использовано в период стабилизации состояния у пациентов со стойкой рефрактерностью к опиоидным аналгетикам и бензодиазепинам и сопутствующей легочной гипертензией. Медикаментозные средства, которые могут быть использованы у новорожденных с целью синхронизации с аппаратом ИВЛ, представлены в Приложении Г5.
- Рекомендуется назначить стартовую антибактериальную терапию до исключения инфекционного процесса и получения результатов бактериологического исследования [20].
Комментарии: Антибактериальная терапия при аспирации мекония проводится в связи с высоким риском развития инфекционного процесса, так как меконий способствует росту бактерий. Стартовая антибактериальная терапия включает в себя комбинацию ампициллина с аминогликозидом. Важно отметить, что отбор крови на бактериологическое исследование необходимо произвести перед первым введением антибактериального препарата. Дальнейшая тактика антибактериальной терапии выбирается согласно результатам бактериологического исследования. При получении отрицательного результата культуры крови антибактериальную терапию можно отменить.
Читайте также:

