Отеки и синяки при сахарном диабете
Обновлено: 19.04.2024
Сегодня мы познакомим вас с признаками сахарного диабета. Это важная информация, ведь сахарный диабет — серьезное и тяжелое заболевание, ранняя диагностика которого позволит избежать страшных осложнений, среди которых: инсульт и ишемическая болезнь сердца.
Если вы обнаружили у себя несколько из перечисленных признаков — это повод незамедлительно обратиться к врачу.
Частые позывы к мочеиспусканию могут быть связаны с сахарным диабетом, так как из-за повышенного содержания глюкозы в крови возникает повышенная нагрузка на почки.
Второй признак вытекает из первого. Частые мочеиспускания обезвоживают организм, поэтому он испытывает постоянную жажду. Если чувство голода не покидает вас даже после приема пищи — это серьезный сигнал. При наличие излишков глюкозы в крови организм запускает повышенную выработку инсулина, благодаря чему уровень глюкозы после еды падает, а вам хочется снова поесть, особенно выпечки и сладостей.
Ещё один признак — сухость во рту, который наблюдается в результате всего того же обезвоживания организма.
Идем дальше — головная боль. Реакцией организма на скачки уровня глюкозы станет головная боль, так как возникает дополнительная нагрузка на кровеносные сосуды мозга.
Двоение в глазах также может стать признаком сахарного диабета, ведь глюкоза накапливается в хрусталике глазного яблока, что сопровождается нечетким зрением или двоением в глазах.
Повышенный сахар в крови создает отличные условия для размножения грибков, поэтому молочница и грибок на ногах могут стать признаками диабета.
Если повреждение кожи в виде синяков, порезов, царапин очень долго заживают и не проходят, то это может говорить о том, что сосуды сужены и кровь с кислородом не могут в достаточном объеме достигнуть пораженный участок для заживления.
Судороги, слабость, ночная боль в мышцах, нарушение координации — признаки диабетической невропатии, которые требуют безотлагательного обращения к врачу.
Поскольку при сахарном диабете повреждаются кровеносные сосуды и страдает нервная система, в большом количестве случаев это вызывает эректильную дисфункцию мужчин и неприятные ощущения при половом акте у женщин из-за повреждений слизистой стенок влагалища.
Неожиданное снижение веса у больных сахарным диабетом происходит по причине выведения большого количества жидкости из организма, а тело получает энергию за счет сжигания подкожного жира и мышечной массы, поскольку глюкозу из крови уже получать не может.
Обнаруженные черные пятна на теле, шее, локтях, под коленным суставом, под мышками — результат активного размножения клеток из-за высокого уровня инсулина в организме.
Специфический признак диабета — сладкий фруктовый запах изо рта. Наличие даже одного этого признака — повод сходить к врачу.
Люди, страдающие сахарным диабетом, испытывают одышку при даже небольших физических нагрузках.
Повышенное давление — также один из спутников сахарного диабета.
Постоянное состояние усталости у диабетиков — следствие того, что клетки не получают глюкозу и не могут выработать энергию, ведь когда мы принимаем пищу с помощью инсулина, она преобразуется в глюкозу, а инсулина из-за болезни стало мало либо организм приобрел устойчивость к нему.
Глюкоза — это топливо для головного мозга в том числе. Частые и необъяснимые перепады настроения могут быть обусловлены излишком либо недостатком глюкозы. Если вы обнаружили у себя такой тревожный симптом, нужно сдать анализы на уровень глюкозы в крови.
Сахарный диабет — достаточно часто встречающееся заболевание, и чем ранее оно будет выявлено, тем ниже риск возникновения осложнений и перехода диабета в более тяжелую форму.
Поэтому каждый должен знать все эти признаки наличия сахарного диабета и иметь их на вооружении.
Острые осложнения сахарного диабета — это угрожающие жизни состояния, обусловленные значительными изменениями уровня сахара в крови и сопутствующими метаболическими нарушениями. Острые осложнения сахарного диабета: гипергликемические комы - кетоацидот
Острые осложнения сахарного диабета — это угрожающие жизни состояния, обусловленные значительными изменениями уровня сахара в крови и сопутствующими метаболическими нарушениями.
Острые осложнения сахарного диабета:
- гипергликемические комы - кетоацидотическая, гиперосмолярная;
- гипогликемическая кома.
Диабетический кетоацидоз и некетоновая гиперосмолярная кома характеризуются разными степенями инсулиновой недостаточности, избыточной продукцией контринсулиновых гормонов и обезвоживанием. В некоторых случаях признаки диабетического кетоацидоза и гиперосмолярной комы могут развиваться одновременно.
Гипогликемия связана с нарушением равновесия между лекарственным средством, применяемым для лечения диабета (инсулин или таблетированные сахороснижающие средства), и приемом пищи или физической нагрузкой.
Быстрота и своевременность оказания помощи больным в коматозном состоянии во многом определяют прогноз. Поэтому правильное ведение пациентов на догоспитальном этапе представляется весьма важным.
В структуре ком на догоспитальном этапе гипогликемическая кома занимает третье место (5,4%), а диабетическая (3%) — пятое (данные ННПОСМП).
Диабетическая кетоацидотическая кома (ДКА)
ДКА представляет собой очень серьезное осложнение сахарного диабета, характеризующееся метаболическим ацидозом (рН меньше 7,35 или концентрация бикарбоната меньше 15 ммоль/л), увеличением анионной разницы, гипергликемией выше 14 ммоль/л, кетонемией. Чаще развивается при СД 1 типа. На ДКА приходится от 5 до 20 случаев на 1000 больных в год (2/100). Смертность при этом составляет 5—15%, для больных старше 60 лет — 20%. От кетоацидотической комы погибают более 16% пациентов с СД 1 типа. Причина развития ДКА — абсолютный или резко выраженный относительный дефицит инсулина вследствие неадекватной инсулиновой терапии или повышения потребности в инсулине.
Провоцирующие факторы: недостаточная доза инсулина или пропуск инъекции инсулина (либо приема таблетированных сахароснижающих средств), самовольная отмена сахароснижающей терапии, нарушение техники введения инсулина, присоединение других заболеваний (инфекции, травма, операции, беременность, инфаркт миокарда, инсульт, стресс и др.), нарушения диеты (слишком большое количество углеводов), физическая нагрузка при высокой гликемии, злоупотребление алкоголем, недостаточное проведение самоконтроля обмена веществ, прием некоторых лекарственных препаратов (кортикостероиды, кальцитонин, салуретики, ацетазоламид, β-блокаторы, дилтиазем, изониазид, дифенин и др.).
Часто этиология ДКА остается неизвестной. Следует помнить, что примерно в 25% случаев ДКА отмечается у пациентов со вновь выявленным сахарным диабетом.
Различают три стадии диабетического кетоацидоза: умеренный кетоацидоз, прекома, или декомпенсированный кетоацидоз, кома.
К осложнениям кетоацидотической комы относят тромбозы глубоких вен, легочную эмболию, артериальные тромбозы (инфаркт миокарда, инфаркт мозга, некрозы), аспирационную пневмонию, отек мозга, отек легких, инфекции, редко — ЖКК и ишемический колит, эрозивный гастрит, позднюю гипогликемию. Отмечаются тяжелая дыхательная недостаточность, олигурия и почечная недостаточность. Осложнения терапии — отек мозга и легких, гипогликемия, гипокалиемия, гипонатриемия, гипофосфатемия.
Диагностические критерии ДКА
- Особенность ДКА - постепенное развитие, обычно на протяжении нескольких суток.
- Наличие симптомов кетоацидоза (запах ацетона в выдыхаемом воздухе, дыхание Куссмауля, тошнота, рвота, анорексия, боли в животе).
- Наличие симптомов дегидратации (снижение тургора тканей, тонуса глазных яблок, мышечного тонуса, сухожильных рефлексов, температуры тела и АД).
При диагностике ДКА на догоспитальном этапе нужно выяснить, страдает ли пациент сахарным диабетом, была ли ДКА в анамнезе, получает ли пациент сахароснижающую терапию, и если да, то какую, когда последний прием препарата, время последнего приема пищи, отмечались ли чрезмерная физическая нагрузка либо прием алкоголя, какие недавно перенесенные заболевания предшествовали коме, были ли полиурия, полидипсия и слабость.
Терапия ДКА на догоспитальном этапе (см. таблицу 1) требует особого внимания во избежание ошибок.
Возможные ошибки терапии и диагностики на догоспитальном этапе
- Инсулинотерапия на догоспитальном этапе без контроля гликемии.
- Акцент в лечении на интенсивную инсулинотерапию при отсутствии эффективной регидратации.
- Введение недостаточного объема жидкостей.
- Введение гипотонических растворов, особенно в начале лечения.
- Применение форсированного диуреза вместо регидратации. Применение диуретиков одновременно с введением жидкостей только замедлит восстановление водного баланса, а при гиперосмолярной коме назначение мочегонных средств категорически противопоказано.
- Начало терапии с введения бикарбоната натрия может привести к летальному исходу. Доказано, что адекватная инсулинотерапия в большинстве случаев помогает устранить ацидоз. Коррекция ацидоза бикарбонатом натрия сопряжена с исключительно большим риском осложнений. Введение щелочей усиливает гипокалиемию, нарушает диссоциацию оксигемоглобина; углекислота, образующаяся при введении бикарбоната натрия, усиливает внутриклеточный ацидоз (хотя рН крови при этом может повышаться); парадоксальный ацидоз наблюдается и в спинно-мозговой жидкости, что может способствовать отеку мозга; не исключено развитие "рикошетного" алкалоза. Быстрое введение бикарбоната натрия (струйное) может вызвать смерть в результате скоротечного развития гипокалиемии.
- Введение раствора бикарбоната натрия без дополнительного назначения препаратов калия.
- Отмена или неназначение инсулина при ДКА больному, который не в состоянии принимать пищу.
- Внутривенное струйное введение инсулина. Лишь первые 15-20 мин концентрация его в крови поддерживается на достаточном уровне, поэтому такой путь введения неэффективен.
- Трех-четырехкратное назначение инсулина короткого действия (ИКД) подкожно. ИКД эффективен в течение 4-5 ч, особенно в условиях кетоацидоза, поэтому его надо назначать не менее пяти-шести раз в сутки без ночного перерыва.
- Применение для борьбы с коллапсом симпатотонических препаратов, которые, во-первых, являются контринсулиновыми гормонами, и, во-вторых, у больных диабетом их стимулирующее влияние на секрецию глюкагона выражено значительно сильнее, чем у здоровых лиц.
- Неправильная диагностика ДКА. При ДКА нередко встречается так называемый "диабетический псевдоперитонит", который симулирует симптомы "острого живота" - напряжение и болезненность брюшной стенки, уменьшение или исчезновение перистальтических шумов, иногда повышение сывороточной амилазы. Одновременное обнаружение лейкоцитоза может привести к ошибке в диагностике, вследствие чего больной попадает в инфекционное ("кишечная инфекция") или хирургическое ("острый живот") отделение. Во всех случаях "острого живота" или диспепсических явлений у больного сахарным диабетом необходимо определение гликемии и кетотонурии.
- Не проводимое измерение гликемии любому больному, находящемуся в бессознательном состоянии, что нередко влечет постановку ошибочных диагнозов - "нарушение мозгового кровообращения", "кома неясной этиологии", в то время как у пациента наблюдается острая диабетическая декомпенсация обмена веществ.
Гиперосмолярная некетоацидотическая кома
Гиперосмолярная некетоацидотическая кома характеризуется выраженной дегидратацией, значительной гипергликемией (часто выше 33 ммоль/л), гиперосмолярностью (более 340 мОсм/л), гипернатриемией выше 150 ммоль/л, отсутствием кетоацидоза (максимальная кетонурия (+)). Чаще развивается у пожилых больных СД 2 типа. Встречается в 10 раз реже, чем ДКА. Характеризуется более высокой летальностью (15—60%). Причины развития гиперосмолярной комы — относительный дефицит инсулина и факторы, провоцирующие возникновение дегидратации.
Провоцирующие факторы: недостаточная доза инсулина или пропуск инъекции инсулина (либо приема таблетированных сахароснижающих средств), самовольная отмена сахароснижающей терапии, нарушение техники введения инсулина, присоединение других заболеваний (инфекции, острый панкреатит, травма, операции, беременность, инфаркт миокарда, инсульт, стресс и др.), нарушения диеты (слишком большое количество углеводов), прием некоторых лекарственных препаратов (диуретики, кортикостероиды, бета-блокаторы и др.),охлаждение, невозможность утолить жажду, ожоги, рвота или диарея, гемодиализ или перитонеальный диализ.
Следует помнить, что у трети пациентов с гиперосмолярной комой не имеется предшествующего диагноза сахарного диабета.
Клиническая картина
Нарастающие в течение нескольких дней или недель сильная жажда, полиурия, выраженная дегидратация, артериальная гипотония, тахикардия, фокальные или генерализованные судороги. Если при ДКА расстройства функции ЦНС и периферической нервной системы протекают по типу постепенного угасания сознания и угнетения сухожильных рефлексов, то гиперосмолярная кома сопровождается разнообразными психическими и неврологическими нарушениями. Кроме сопорозного состояния, также нередко отмечающегося при гиперосмолярной коме, психические нарушения часто протекают по типу делирия, острого галлюцинаторного психоза, катотонического синдрома. Неврологические нарушения проявляются очаговой неврологической симптоматикой (афазией, гемипарезом, тетрапарезом, полиморфными сенсорными нарушениями, патологическими сухожильными рефлексами и т. д.).
Диагностические критерии
- Гиперосмолярная некетоацидозная кома развивается медленнее (в течение 5-14 дней), чем ДКА. Более выражена дегидратация (снижение тургора тканей, тонуса глазных яблок, мышечного тонуса, сухожильных рефлексов, температуры тела и АД) с неврологической симптоматикой, отсутствуют кетоацидоза, кетонурия, чаще возникают анурия и азотемия, в пожилом и старческом возрасте.
Среди возможных ошибок в терапии (см. таблицу 2) и диагностике принято выделять введение гипотонических растворов на догоспитальном этапе, длительное введение гипотонических растворов.
Гипогликемическая кома
Гипогликемическая кома развивается вследствие резкого снижения уровня глюкозы в крови (ниже 3-3,5 ммоль/л) и выраженного энергетического дефицита в головном мозге.
Провоцирующие факторы: передозировка инсулина и ТСС, пропуск или неадекватный прием пищи, повышенная физическая нагрузка, избыточный прием алкоголя, прием лекарственных средств (β-блокаторы, салицилаты, сульфаниламиды и др.).
Клиническая картина
Симптомы гипогликемии делятся на ранние (холодный пот, особенно на лбу, бледность кожи, сильный приступообразный голод, дрожь в руках, раздражительность, слабость, головная боль, головокружение, онемение губ), промежуточные (неадекватное поведение, агрессивность, сердцебиение, плохая координация движений, двоение в глазах, спутанность сознания) и поздние (потеря сознания, судороги).
Диагностические критерии
- Внезапное развитие симптомов, обычно на протяжении нескольких минут, реже часов.
- Наличие характерных симптомов гипогликемии.
- Гликемия ниже 3-3,5 ммоль/л.
На догоспитальном этапе нужно выяснить: на протяжении какого времени пациент страдает сахарным диабетом, получает ли больной сахароснижающую терапию, и если да, то какую, когда был последний прием препарата, имели ли место нарушение диеты, отмечались ли какие-нибудь эпизоды гипогликемии в прошлом, допускалась ли чрезмерная физическая нагрузка и алкогольная интоксикация.
Терапия гипогликемической комы на догоспитальном этапе (см. таблицу 3) включает применение тиамина, преднизолона, глюкозы, раствора адреналина, магния сульфата.
После выведения больного из гипогликемической комы рекомендуется применять средства, улучшающие микроциркуляцию и метаболизм в клетках головного мозга (глютаминовая кислота, аминолон, стугерон, кавинтон) в течение трех—шести недель.
Повторные гипогликемии могут привести к поражению головного мозга.
Возможные диагностические и терапевтические ошибки
- Попытка ввести углеводсодержащие продукты (сахар и т. п.) в ротовую полость пациенту, находящемуся без сознания. Это часто приводит к аспирации и асфиксии.
- Применение для купирования гипогликемии непригодных для этого продуктов (хлеб, шоколад и т. п.). Эти продукты не обладают достаточным сахароповышающим действием или повышают уровень сахара в крови, но слишком медленно.
- Неправильная диагностика гипогликемии. Некоторые симптомы гипогликемии могут ошибочно расцениваться как эпилептический припадок, инсульт, "вегетативный криз" и др. У больного, получающего сахароснижающую терапию, при обоснованном подозрении на гипогликемию ее купирование следует начинать сразу же, еще до получения ответа лаборатории.
- После выведения пациента из состояния тяжелой гипогликемии часто не учитывается опасность рецидива.
У пациентов, находящихся в коматозном состоянии неизвестного генеза, всегда необходимо предполагать наличие гликемии. Если достоверно известно, что у пациента сахарный диабет и в то же время трудно дифференцировать гипо- или гипергликемический генез коматозного состояния, рекомендуется внутривенное струйное введение глюкозы в дозе 20–40—60 мл 40% раствора в целях дифференциальной диагностики и оказания экстренной помощи при гипогликемической коме. В случае гипогликемии это значительно снижает выраженность симптоматики и, таким образом, позволит дифференцировать эти два состояния. При гипергликемической коме такое количество глюкозы на состоянии пациента практически не скажется.
Во всех случаях, когда невозможно измерение гликемии немедленно, эмпирически следует ввести высококонцентрированную глюкозу. Если гипогликемию не купировать в экстренном порядке, она может быть смертельной.
Базовыми препаратами для пациентов, находящихся в коме, при отсутствии возможности уточнения диагноза и скорой госпитализации, считаются тиамин 100 мг в/в, глюкоза 40% 60 мл и налоксон 0,4—2 мг в/в. Эффективность и безопасность этой комбинации неоднократно находили подтверждение на практике.
Х. М. Торшхоева, кандидат медицинских наук
А. Л. Верткин, доктор медицинских наук, профессор
В. В. Городецкий, кандидат медицинских наук, доцент
ННПО скорой медицинской помощи, МГМСУ
Сахарный диабет вызывает опасные осложнения со стороны глаз, сердца, почек и структур нижних конечностей. Одно из распространенных проявлений патологии – отеки ног. Они не только вызывают дискомфорт и ухудшают качество жизни, но и могут стать причиной угрожающих состояний – тромбоза вен нижних конечностей и диабетической стопы. Поэтому требуют врачебного вмешательства.
Почему отекают ноги при сахарном диабете
Повышенный уровень глюкозы в крови вызывает поражения сосудов, суставов и нервных волокон, а также поражения почек. При поражении структур нижних конечностей измененные стенки сосудов ног пропускают в межклеточное пространство плазму крови. Там она скапливается и образует отеки. Из-за диабетического поражения нервных окончаний человек может долго этого не ощущать. В результате массивные отеки затрудняют циркуляцию крови в ножных венах, в связи с чем они могут тромбироваться.
В свою очередь кожа и мягкие ткани из-за недостаточного кровоснабжения плохо заживают даже после незначительных травм, а в ранах легко размножается инфекция. Так развиваются гнойные некрозы и язвы костей и суставов – вплоть до флегмон, абсцессов и гангрены.
Сосуды ножных вен также могут изменяться из-за атеросклероза – распространенного осложнения диабета 2-го типа. В этом случае на стенках нарастают атеросклеротические бляшки, просвет сосудов сужается, движение крови замедляется и ее скопление вызывает отек.
При диабетической нефропатии фильтрация крови в почечных структурах нарушается. Организм перестает справляться с отводом жидкости. Ее задержка провоцирует отеки, особенно в стопах и голенях – отделах тела, максимально удаленных от сердечного «насоса».
При сахарном диабете нередки отеки не только в нижних конечностях, но также в области лица, рук, живота, макулярный отек глаз, а также внутренних органов – почек и сердца. При диабете первого типа отечность часто бывает неравномерной – на левой стороне больше чем на правой. При диабете второго типа к отеку может присоединяться сдавливающая боль.
Факторы риска, которые повышают риск развития отеков при диабете:
- плохой гликемический контроль;
- высокое артериальное давление;
- сердечная недостаточность, ИБС;
- повышенный уровень холестерина;
- курение или употребление алкоголя;
- лишний вес;
- регулярные переедания;
- избыток соли в рационе;
- недостаточная физическая активность;
- варикоз;
- ношение тесной обуви;
- нарушения гормонального баланса, в том числе во время беременности;
- недостаток сна;
- хронический стресс.
На практике у большинства больных диабетом выявляют одновременно и несколько причин отекания, и несколько факторов повышения риска.
Сопутствующие признаки
Процесс отекания тканей ног трудно заметить на начальной стадии. Но даже на начальной стадии его можно заподозрить по сопутствующим симптомам. Незамедлительно проконсультируйтесь с врачом, если у больного появились вторичные признаки отека:
- дискомфорт во время стояния;
- изменение цвета кожи ступней и лодыжек – бледность, посинение или покраснение (особенно покраснение от синтетики);
- водянистые волдыри;
- снижение чувствительности к механическим воздействиям (например, не почувствовал камешка в ботинке);
- чувство жжения в пальцах;
- покалывания, пощипывания, ощущение пульсации в конечностях;
- сухость кожи стоп, трещины пяток, мозоли;
- выпадение волос на ногах;
- синдром беспокойных ног СБН – потребность двигать ногами из-за неприятных ощущений;
- онемение пальцев ног;
- натирание привычной обувью.
Чем опасны отеки ног при сахарном диабете
Помимо диабетической стопы, тромбозов и трофических язв, отеки конечностей при диабете могут стать причиной вывихов и подвывихов, переломов, деформации пальцев ног. Они могут провоцировать боль и врастание ногтей.Если их оставить без внимания, состояние может закончиться ампутацией нижних конечностей.
Лечение отеков ног при сахарном диабете 1 и 2 типов
При отеках на фоне диабета нужна консультация эндокринолога и/или сосудистого хирурга. Чтобы подобрать работающую лечебную схему, помимо осмотра, проверки пульсации ножных вен и рефлексов врач может назначить УЗИ и электронейромиографию.
Основные цели лечения:
- нормализовать уровень глюкозы – это поможет восстановить нормальную работу почек, функции нервных окончаний, состояние сосудистых стенок и суставов.
- подобрать диету, которая поможет поддерживать показатели сахара крови в норме – таким образом добиваются устойчивой ремиссии;
- при необходимости – устранить нефропатический синдром и нормализовать функции мочевыделительной системы;
- помочь организму вывести скопившуюся жидкость (с помощью системных или местных лекарственных средств, фиточаев или ванночек).
При диабете I типа уровень сахара снижают путем введения инсулина – гормона поджелудочной железы, который у больных этой группы не вырабатывается. При диабете II типа стараются обойтись сахароснижающими препаратами (если они оказывают эффект, а уровень глюкозы в крови не слишком высокий).
Если есть болевой синдром, назначают обезболивающие НПВП-препараты. Кроме этого, корректируют влияние провоцирующих факторов:
- нормализуют давление с помощью препаратов-ингибиторов, блокаторов рецепторов или диуретиков (в зависимости от причины гипертонии);
- купируют процессы формирования атеросклеротических бляшек с помощью статинов;
- нормализуют гормональный фон;
- помогают пациенту отказаться от курения путем подбора подходящей методики;
- консультируют по подбору подходящей обуви;
- поддерживают работу сердца с помощью сердечных гликозидов;
- назначают диету и лечебную физкультуру;
- корректируют режим дня и ночного отдыха;
- учат преодолевать стресс;
- при варикозе опционально прописывают флеботоники и компрессионный трикотаж.
Для общего укрепления организма врач может порекомендовать витаминно-минеральные комплексы для диабетиков и БАДы. После устранения острой фазы нередко назначают поддерживающую терапию. Помимо медикаментозных средств и коррекции образа жизни в нее включают физиотерапию – чтобы улучшить кровоснабжение в конечностях.
Что нельзя делать, когда отекают ноги при диабете
Крайне опасно самостоятельно принимать мочегонные средства.Неправильный подбор, некорректная доза или длительность курса могут резко уменьшить объем циркулирующей крови, спровоцировать острую почечную недостаточность,критическое снижение артериального давления и уровня калия(он необходим для работы сердца).
Также учитывайте, что в остром периоде болезни противопоказан противоотечный массаж. Его назначают только после устранения симптомов,на этапе реабилитации и профилактики.
Профилактика отеков:
- Носить компрессионный трикотаж (не лечебного, а профилактического класса).
- Если есть симптомы диабетической стопы – ухаживать за ней в точности как назначил врач и использовать специальные средства для диабетиков.
- Соблюдать подобранную диету –с минимумом соли и простых углеводов.
- Выпивать 1,5-2 литра воды в день (не на ночь).
- Поддерживать рекомендованную врачом нормальную двигательную активность – даже небольшие физические нагрузки снижают риск развития отеков в 2 раза.
- Не допускать переохлаждения и перегрева ног.
- Носить удобную обувь – устойчивую, на низком каблуке и из качественных материалов.
- Выполнять все врачебные назначения, чтобы достичь компенсации диабета и сопутствующих заболеваний.
Отеки при диабете сигнализируют о проблеме декомпенсации. Их игнорирование или самолечение могут катастрофически ухудшить ситуацию. И напротив – своевременное обращение к специалисту позволяет компенсировать диабетические процессы, нормализовать нарушенные функции и добиться устойчивой ремиссии.
Что такое стопа Шарко? В чем трудность диагностики диабетической остеоартропатии? Диабетическая остеоартропатия (ОАП, стопа Шарко, сустав Шарко) — редкое, но крайне тяжелое осложнение сахарного диабета, при неадекватном лечении приводящее к необратимо
Что такое стопа Шарко?
В чем трудность диагностики диабетической остеоартропатии?
Диабетическая остеоартропатия (ОАП, стопа Шарко, сустав Шарко) — редкое, но крайне тяжелое осложнение сахарного диабета, при неадекватном лечении приводящее к необратимой инвалидизации. Это осложнение можно назвать одной из самых загадочных форм синдрома диабетической стопы, так как предсказать развитие ОАП и выделить группы риска среди пациентов с сахарным диабетом крайне трудно. С этим осложнением диабета встречаются врачи разных специальностей — хирурги, эндокринологи, ортопеды, но далеко не всегда оно вовремя распознается.
Современное определение диабетической остеоартропатии — «деструкция кости и сустава неинфекционного характера, вызванная диабетической нейропатией» [1].
Деструктивная остеоартропатия была описана в ХIХ веке французским неврологом Шарко [2], но не при сахарном диабете (в доинсулиновую эру поздние осложнения диабета практически не встречались), а при сифилитическом поражении проводящих путей спинного мозга (tаbеs dоrsаlis). Впоследствии было установлено, что подобные изменения суставов стоп также встречаются при различных заболеваниях, приводящих к нарушению иннервации нижних конечностей (сирингомиелии, диабетической полинейропатии и др.). В настоящее время наиболее частой формой остеоартропатии является диабетическая.
Распространенность данного осложнения среди больных сахарным диабетом составляет менее 1% [3], хотя в литературе встречаются данные о поражении костной ткани стоп у 0,1-55% больных [4]. Такая противоречивость сведений, очевидно, связана с различиями в методике обследования и разными критериями диагностики остеоартропатии.
Локализация поражений
В подавляющем большинстве случаев ОАП поражает кости и суставы стоп. В 1991 году была предложена классификация ОАП [3] в зависимости от локализации процесса (рис. 1). У 20-25% пациентов ОАП поражает обе стопы, но обычно не одновременно. Встречаются случаи ОАП с поражением других суставов: коленного и даже локтевого.
Этиология, патогенез и естественное течение ОАП
Остеоартропатия — это по сути поражение костной ткани в отличие от типичных форм остеопороза, имеющих исключительно локальный характер. Причиной такого поражения кости является нарушение иннервации нижних конечностей вследствие диабетической нейропатии.
Длительное время развитие ОАП рассматривалось в основном с позиций нейротравматической и нейроваскулярной [5]. Согласно первой, моторная и сенсорная (посредством утраты проприоцептивных рефлексов) формы нейропатии приводят к нарушениям биомеханики стопы. Результатом этого является аномальная нагрузка на отдельные суставы стопы при ходьбе, приводящая через некоторое время к их деструкции. Альтернативная теория основана на обнаружении при ОАП признаков артериовенозного шунтирования крови через сосудистое русло костной ткани, в связи с чем было сделано заключение о ведущей роли аномального усиления кровотока в костной ткани в развитии локальной остеопении [6]. В 1989 году ученые выдвинули предположение о том, что в развитии ОАП определенную роль играют как рецидивирующая травма стоп, так и усиление кровотока в костной ткани. Таким образом оба этих патологических процесса нашли отражение в «синтетической» теории [7].
Известно, что ОАП не развивается у пациентов с нарушениями кровоснабжения нижних конечностей. Это объясняется тем, что при ишемической и нейроишемической формах синдрома диабетической стопы невозможно аномальное усиление кровотока в костной ткани.
Несмотря на то что факт развития ОАП лишь при тяжелой диабетической нейропатии хорошо известен, предсказать развитие ОАП практически невозможно, так как это осложнение возникает далеко не у всех больных даже с выраженной нейропатией. В связи с этим было высказано предположение, что ОАП вызывает не любая форма, а лишь определенные «подвиды» нейропатии. В 1992 году британские исследователи выдвинули гипотезу (впоследствии подтвержденную в ряде работ), что к ОАП приводит особая форма диабетической нейропатии с преимущественным поражением миелиновых нервных волокон и относительной сохранностью безмиелиновых, что вызывает нарушение тонуса микрососудов, которое влечет за собой усиление кровотока в костной ткани [8].
Эти патологические процессы служат предпосылкой, своего рода фоном для манифестации ОАП — остеопороза дистальных отделов нижних конечностей, снижающего устойчивость кости к повреждающим воздействиям. В этой ситуации провоцирующий фактор (минимальная травма при ходьбе или хирургическое вмешательство на стопе) приводит к повреждению кости или усилению в ней кровотока, активации остеокластов и «запускает» бурный и безостановочный процесс остеолиза, в отсутствие лечения приводящий к разрушению скелета стопы.
После манифестации ОАП процесс проходит четыре стадии [4].
Первая (острая) стадия характеризуется отеком стопы, умеренной гиперемией и местной гипертермией (рис. 2). Боли и лихорадка нехарактерны. Рентгенография может не выявлять деструктивных изменений (на этой стадии они представлены лишь микропереломами); обнаруживается остеопороз костей стоп.
Вторая (подострая): фрагментация костей и начало деформации стопы. В типичных случаях происходит уплощение свода стопы на пораженной стороне (рис. 3). Отек и воспалительные явления в этой стадии уменьшаются. Рентгенологически определяются фрагментации костных структур.
Третья (хроническая): выраженная деформация стопы, наличие спонтанных переломов и вывихов. Вид деформации зависит от локализации поражения. В типичных случаях нагрузки на стопу при ходьбе приводят к деформации по типу «пресс-папье» или «стопы-качалки» (рис. 4). Это сопровождается вальгусной деформацией внутреннего края стопы в области предплюсны, клювовидной деформацией пальцев. Рентгенологически — фрагментация костей, выраженная деформация скелета, периостальное и параоссальное обызвествление (рис. 6). Функция скелета стопы полностью нарушается, в тяжелых случаях стопу можно образно сравнить с «мешком с костями».
Четвертая (стадия осложнений): перегрузка отдельных участков деформированной стопы приводит к образованию язвенных дефектов (рис. 5); при их инфицировании возможно развитие флегмоны стопы, остеомиелита, гангрены.
Диагностика
Из-за сложности лечения ОАП, а также в связи с тем, что в популяции это состояние встречается достаточно редко, пациентов с подозрением на ОАП для диагностики и лечения следует направлять в специализированные отделения (центры) «Диабетическая стопа».
ОАП диагностируется на основании клинической картины, анамнеза (небольшая травма, хирургическое вмешательство) и рентгенологических признаков, соответствующих той или иной стадии. Очень часто из-за недостаточной информированности врачей общей практики об ОАП это осложнение ошибочно диагностируется как лимфостаз, тромбофлебит, флегмона стопы и др.
Наиболее затруднен дифференциальный диагноз в острой стадии, когда несвоевременное начало адекватного лечения приводит к необратимой инвалидизации.
Дифференциальная диагностика ОАП в острой фазе включает два основных вопроса:
- Являются ли воспалительные изменения следствием поражения костных структур или их следует рассматривать как проявление другого заболевания (флегмоны стопы, острого тромбофлебита, подагрического артрита, ревматических поражений суставов и др.)?
- При наличии рентгенографических признаков деструкции кости имеет она неинфекционную (ОАП) или инфекционную (остеомиелит) природу?
Для решения первого вопроса необходимы данные рентгенографии стоп (хотя в острой фазе могут присутствовать лишь неспецифические изменения в виде остеопороза). Магнитно-резонансная томография и сцинтиграфия скелета стопы выявляют микропереломы, воспалительные изменения, усиление кровотока в пораженных костях.
Возможна оценка биохимических маркеров распада костной ткани (гидроксипролина, дезоксипиридинолина, фрагментов коллагена и др.). С аналогичной целью могут использоваться и маркеры перестройки костной ткани, отражающие активность остеобластов (то есть остеосинтеза), — костный изофермент щелочной фосфатазы и др. Но уровень этих веществ во многом зависит от активности процессов распада костной ткани в скелете в целом.
Очевидно, что изменения, характерные для других заболеваний: признаки острого тромбофлебита при УЗДГ венозной системы, типичная клиника подагрического артрита (с болевым синдромом и лихорадкой, соответствующей рентгенологической и биохимической картиной) и прочие — делают диагноз ОАП менее вероятным.
Для остальных случаев наиболее приемлемым на сегодняшний день алгоритмом диагностики ОАП в острой фазе можно считать следующий [9]:
При возникновении у больного сахарным диабетом одностороннего отека стопы (особенно при неповрежденной коже) следует обязательно исключить возможность ОАП. При подозрении на ОАП и при повышенном риске ее развития (длительное течение сахарного диабета, выраженная диабетическая нейропатия) целесообразнее назначить лечение сразу, чем через несколько месяцев наблюдать необратимую деформацию стопы.
Второй вопрос чаще возникает при наличии трофической язвы стопы или в послеоперационном периоде после ампутации в пределах стопы или другого оперативного вмешательства. Это связано с тем, что остеомиелит при синдроме диабетической стопы чаще всего вторичный, являющийся осложнением трофической язвы или раневого процесса. В решении этого вопроса помогают данные анализа крови: нейтрофильный лейкоцитоз характерен (хотя и необязателен) для остеомиелита, но не для ОАП. Об остеомиелите свидетельствуют также некоторые рентгенологические признаки (реакция надкостницы), а также наличие свища, зондирование костных структур в дне раны. Эффективный, но малодоступный метод исследования — сцинтиграфия скелета с введением лейкоцитов с радиоактивной меткой. «Золотым стандартом» в определении природы деструкции костной ткани является биопсия кости.
Лечение ОАП
В острой фазе цель лечения — остановка процессов остеолиза, предотвращение патологических переломов или их консолидация.
Наиболее частая ошибка — назначение вазоактивных препаратов. Эти средства показаны далеко не при всех формах синдрома диабетической стопы (только при ишемической и нейроишемической), а при ОАП способны усилить и без того избыточный кровоток в костной ткани.
Основой лечения ОАП в острой стадии является полная разгрузка конечности до исчезновения признаков воспаления (отека, локальной гипертермии). Адекватная разгрузка обеспечивает консолидацию костных отломков и более важна, чем медикаментозное лечение [3]. Если разгрузка не проводится, наиболее вероятны смещение костных отломков и развитие прогрессирующей деформации стопы, представленной на рис. 2-5. В первые дни и недели заболевания показан строгий постельный режим. В дальнейшем возможна ходьба, но только в специально изготовленном ортезе, переносящем значительную часть нагрузки со стопы на голень. Временная разгрузка в период изготовления ортеза может выполняться с помощью тутора, который отличается от ортеза стандартной формой (продается в готовом виде) и менее плотной фиксацией конечности.
После разрешения отека (обычно через 4 месяца) от ношения ортеза постепенно отказываются, а пациенту разрешают ходить в индивидуально изготовленной ортопедической обуви (рис. 7).
Стандартным методом разгрузки конечности при ОАП в большинстве зарубежных стран, особенно англоязычных (США, Великобритания, Австралия и др.), является применение фиксирующих повязок из полимерных материалов, по свойствам аналогичных гипсу (Тоtаl Соntасt Саst). Но даже при наличии высококвалифицированного персонала, проводящего эту процедуру, метод чреват развитием повреждений кожи (пролежней) под иммобилизирующей повязкой в 10% случаев.
В острой фазе ОАП применяются лекарственные препараты, влияющие на метаболизм костной ткани.
Тормозят процесс резорбции костной ткани бифосфонаты и кальцитонин.
Кальцитонин (миакальцик) применяется подкожно или внутримышечно по 100 МЕ один раз в день (обычно 1-2 недели), далее — в виде назального аэрозоля по 200 МЕ ежедневно.
Образование костной ткани стимулируют активные метаболиты витамина Д3 (альфа Д3-Тева и др.) и анаболические стероиды.
Альфа Д3-Тева применяется по 0,5-1 мкг/сут (2-4 капсулы) после еды. Альфа Д3-Тева способствует улучшению абсорбции кальция в кишечнике и активации процессов костного ремоделирования, обладает способностью подавлять повышенный уровень паратиреоидного гормона, усиливать нервно-мышечную проводимость, уменьшая проявления миопатии. Длительная терапия Альфа Д3-Тева способствует уменьшению болевого синдрома, повышению мышечной силы, координации движений, снижению риска падений и переломов костей. Частота побочных реакций на фоне длительной терапии Альфа Д3-Тева остается низкой.
Анаболические стероиды (ретаболил, неробол) назначают в виде инъекций один раз в неделю в течение 3-4 недель.
Препараты кальция самостоятельного действия на метаболизм костной ткани не оказывают, поскольку включение кальция в состав костной ткани регулируется соответствующими гормонами. Эти препараты применяются как вспомогательные для обеспечения достаточного потребления кальция при лечении патологии костной ткани (которое должно составлять с учетом всех пищевых продуктов 1000-1500 мг/сут). Наибольшей биодоступностью обладают лактат и карбонат кальция. Они входят в состав препаратов кальций-Сандоз форте, витрум-кальциум и кальций-Д3-Никомед, которые можно назначать по одной таблетке в день (около 500 мг элементарного кальция). Последний из названных препаратов содержит также витамин Д3, но в профилактических дозах, поэтому это средство следует рассматривать в первую очередь как источник кальция. Препараты кальция принимают во второй половине дня, так как именно в это время происходит их максимальное усвоение. Глюконат кальция (таблетки по 100 мг) стоит недорого, но отличается низкой биодоступностью, из-за чего необходимая суточная доза препарата составляет 10 таблеток.
Кальцитонин и бифосфонаты способны вызывать гипокальциемию, витамин Д3 и препараты кальция — повышать уровень кальция в крови. Поэтому необходимо определение уровня ионизированного кальция до начала лечения и ежемесячно на его фоне (в современных лабораториях этот показатель определяется в капиллярной крови). Обычно применяется комбинация какого-либо из ингибиторов резорбции, витамина Д3 и препаратов кальция. В зависимости от уровня ионизированного кальция дозы тех или иных препаратов увеличиваются или уменьшаются. Продолжительность лечения составляет 4-6 месяцев.
Вспомогательные средства (НПВС, эластичное бинтование конечности, иногда диуретики) применяются в целях устранения отека.
Рентгенотерапия пораженных суставов позволяет достаточно быстро купировать воспалительные явления. Однако, по данным ряда плацебо-контролируемых исследований, факт улучшения прогноза течения ОАП после рентгеновского облучения не подтвердился. Поэтому рентгенотерапию следует применять только в сочетании с адекватной разгрузкой конечности.
Оптимальным результатом лечения, начатого в острой фазе, является предотвращение переломов или консолидация отломков. О результатах лечения позволяют судить изменения клинической картины и контрольная рентгенография через 4-6 месяцев от манифестации заболевания.
После стихания воспалительных явлений сохраняется повышенный риск ОАП (в этой же или других зонах). Помимо общих профилактических мер (см. ниже) целесообразно носить ортопедическую обувь, уменьшающую нагрузку на суставы стопы (в первую очередь, предплюсны) при ходьбе.
В том случае, если процесс находится на второй или третьей стадии, основной целью лечения становится предотвращение осложнений ОАП. При наличии деформаций стопы необходима сложная ортопедическая обувь с внутренним рельефом, повторяющим аномальную форму стопы. Ригидная подошва с так называемым перекатом — приподнятой передней частью — препятствует дальнейшему смещению костных отломков при ходьбе. Постоянное ношение качественной ортопедической обуви предотвращает развитие трофических язв в местах повышенного давления. Попытки ортопедической коррекции деформаций при ОАП (супинаторы и т. п.) бесперспективны и чреваты быстрым развитием язв.
Методы хирургического восстановления скелета стопы при ОАП
Предложен ряд методов оперативного вмешательства, направленных на коррекцию деформации стопы при ОАП (артродез, резекция костных структур, создающих повышенное давление на подошвенную поверхность и приводящих к образованию незаживающей язвы), но в России опыт их применения невелик. Несомненным условием использования этих методов является полное стихание воспалительного процесса и остеолиза (так как в противном случае оперативное вмешательство может способствовать появлению новых очагов деструкции). Вероятно, лечение препаратами, укрепляющими костную ткань, создает более благоприятные условия для проведения операции. Однако вопрос о показаниях к хирургическому лечению и его безопасности при ОАП по-прежнему остается спорным. Чаще всего показанием к такому лечению служит тяжелая деформация стопы, делающая невозможным изготовление адекватной ортопедической обуви. В любом случае после оперативного вмешательства необходимо обеспечить полную 3-месячную разгрузку пораженной конечности (постельный режим, далее — Total Contact Cast или его аналог) [3].
Профилактика ОАП
Вопрос о методах профилактики в группах риска окончательно не решен. Своевременное выявление остеопении в дистальных отделах конечностей позволило бы восстанавливать костную плотность с помощью соответствующих препаратов. Однако остеопороз скелета стоп при рентгенографии у больных диабетом встречается в десятки раз чаще, чем ОАП, в связи с чем группа пациентов, имеющих показания для профилактического лечения, становится неоправданно большой. Кроме того, недостаточно разработаны методы количественной оценки костной плотности (денситометрии) скелета стоп, без которых невозможно составить представление об изменениях плотности костной ткани на фоне лечения, а также выбрать наиболее эффективные препараты и т. п.
Следовательно, основой профилактики ОАП остается адекватное лечение сахарного диабета, подобранное с учетом современных рекомендаций: обучение больных методам самоконтроля, поддержание гликемии на уровне, близком к «недиабетическому», и своевременное назначение инсулина при СД 2-го типа.
Что такое диабетическая стопа? Причины возникновения, диагностику и методы лечения разберем в статье доктора Есипенко И. А., сосудистого хирурга со стажем в 37 лет.
Над статьей доктора Есипенко И. А. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Диабетическая стопа (синдром диабетической стопы, СДС) — это тяжёлое осложнение сахарного диабета в виде инфекции, язв или разрушения глубоких тканей, которое возникает в связи с нарушением макроструктуры стопы и микроциркуляции крови, по причине разрушения нервных окончаний и нервных волокон. [10]
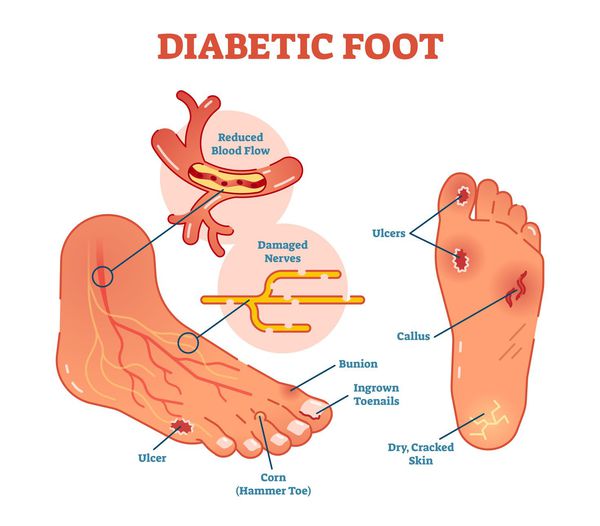
Главная причина ДС — это сахарный диабет (СД). И хотя синдром диабетической стопы не развивается с первого дня увеличения уровня глюкозы в крови более 7,0-8,0 ммоль/л, каждый пациент с диагнозом «сахарный диабет» должен помнить о таком грозном возможном осложнении.
Хронические раны на ногах у людей с сахарным диабетом встречаются в 4-15 % случаев. В некоторых случаях они становятся первым признаком развившегося диабета [10] .
Основные «пусковые механизмы» развития язв при СДС:
1. Ношение неудобной обуви. К изменению нагрузки на суставы стопы, сдавливанию или потёртости кожи, локальной микроишемии, инфильтрату, или некрозу могу привести любые дефекты обуви:
- несоответствующий размер обуви (меньше или больше, чем нужно);
- стоптанные и/или высокие каблуки;
- рубец на стельке;
- дефект подошвы;
- мокрая обувь;
- несоответствие обуви времени года.
2. Увеличенный вес тела. Учитывая площадь стоп, при увеличении веса тела (даже на 1 кг) увеличивается и нагрузка на каждый сустав стопы. Самая уязвимая область — подошвенная поверхность.
3. Разрастание эпидермиса (поверхности) кожи. Этот процесс происходит из-за нарушенных обменных процессов в коже на фоне СД (под утолщённым эпидермисом-"мозолью" в слоях кожи нарушается микроциркуляция, что приводит к микроишемии и некрозу).
4. Микротравмы:
- укусы животных;
- уколы шипами растений;
- порезы при педикюре и т. п.
5. Стенозы (сужение) и окклюзии (закупорка) магистральных артерий. В результате отсутствия кровоснабжения в стопах и голенях к микроишемии присоединяется макроишемия и развитие гангрены конечности.
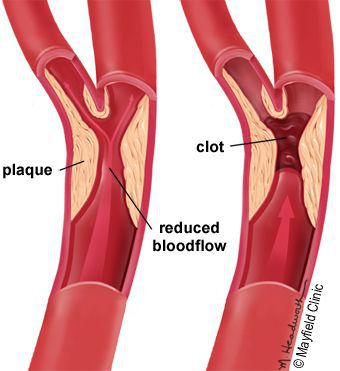
6. Условно патогенная или патогенная микрофлора. Активизация флоры (микробов и других микроорганизмов) на поверхности кожи в условиях СД приводит к воспалению кожного покрова, а в условия ишемии или микротравмы значительно ускоряется развитие гангрены.
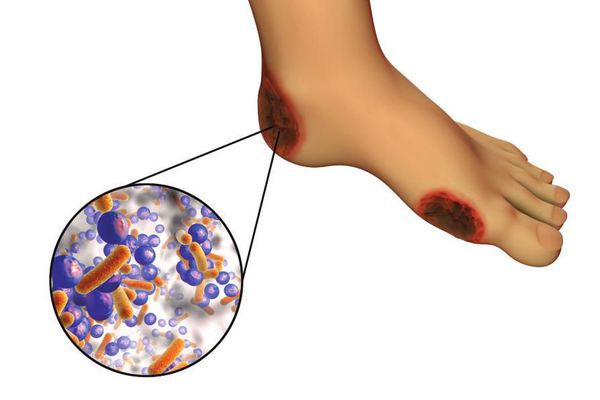
Часто наблюдается сочетание нескольких причин возникновения язв при СДС.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы диабетической стопы
Отправной точкой развития СДС считается не дата установления диагноза «Сахарный диабет», а время, когда были выявлены первые симптомы СД (однократные подъёмы глюкозы крови, сухость во рту и другие).
Симптомы СДС:
- онемение, зябкость, жжение, отёки в стопах и другие неприятные ощущения;
- выпадение волос на на стопах и голенях, потливость стоп;
- изменение окраски кожи (гиперемия, гиперпигментация, цианоз);
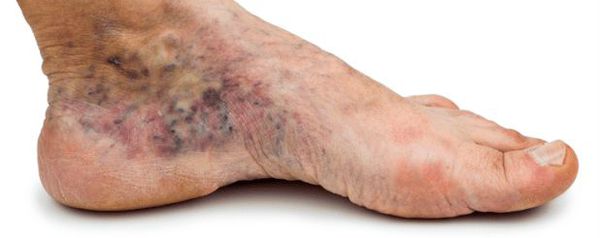
- утолщение, расслаивание, изменение формы и цвета ногтевых пластинок;
- кровоизлияния под ногтевой пластинкой в виде «синяков» под ногтями;
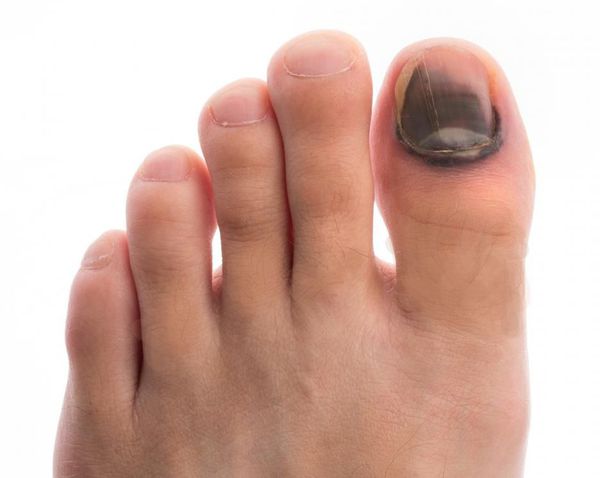
- деформация стоп;
- снижение чувствительности стоп — вибрационного, температурного, болевого и тактильного восприятия;
- боль в области стопы и язвы, возникающая как в покое или ночью, так и при ходьбе на определённые расстояния;
- истончение кожи, шелушение;
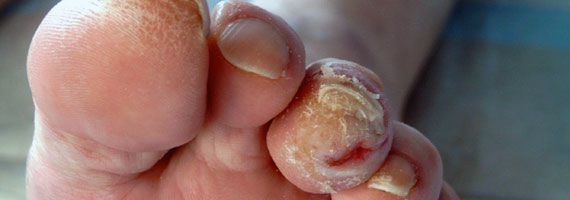
- понижение или увеличение температуры стоп и голеней;
- длительная эпителизация (заживление) микротравм — до двух месяцев, при этом остаются коричневые рубцы;
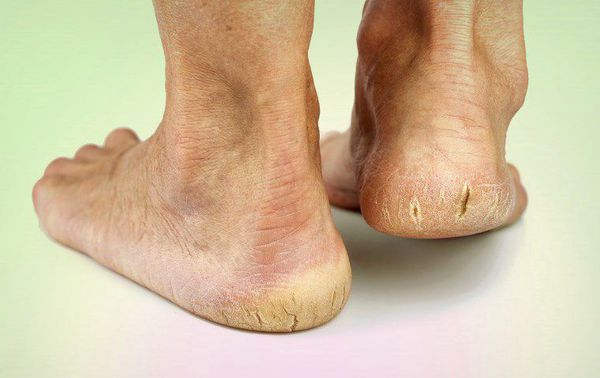
- трофические язвы, длительно не заживающие на стопах.
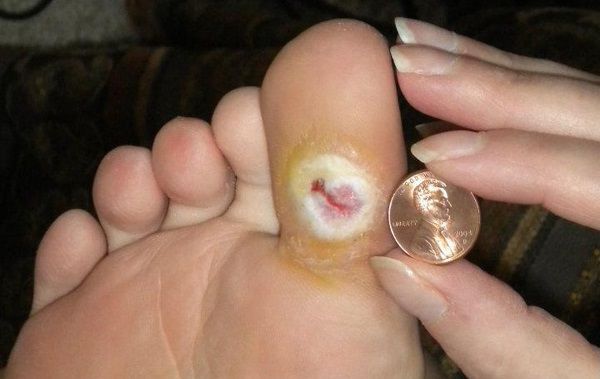
Чаще всего трофическим изменениям подвержены дистальные отделы конечности: пальцы и подошвенная поверхность стопы в проекции головок плюсневых костей. Зона образования трофической язвы зависит от причины её возникновения.
Патогенез диабетической стопы
Механизм развития СДС представляет собой следующую последовательность нарушений:
- Снижается выработка гормона инсулина.
- Увеличивается уровеь глюкозы в крови — развивается гипергликемия.
- Блокируется кровоток в мелких сосудах, через сосудистую стенку перестаёт поступать кислород и другие микроэлементы.
- Разрушаются нервные волокна и рецепторы.
- Наступает микро- и макроишемия тканей стопы.
- Образуются трофические язвы.
Таким образом, при СДС происходит повреждение всех тканей ноги.
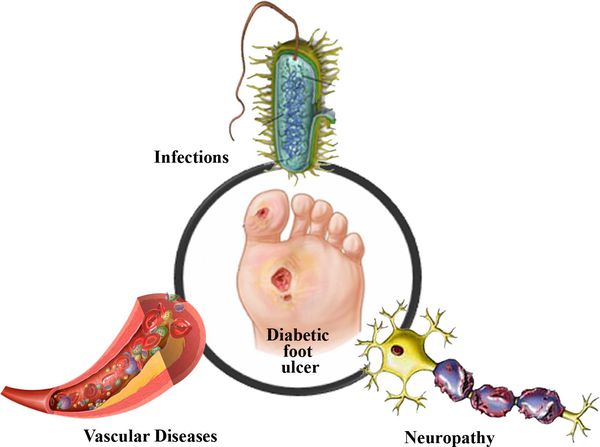
В результате дефицита инсулина в организме диабетика количество глюкозы в крови увеличивается. Это в свою очередь негативно сказывается на состоянии как мелких, так и крупных сосудов:
- на стенках сосудов скапливаются иммунологические вещества;
- мембраны становятся отёчными;
- просвет сосудов сужается.
В результате этих изменений кровообращение нарушается и образуются небольшие тромбы. Эти изменения в организме препятствуют поступлению достаточного количества микроэлементов и кислорода в клетки и тем самым приводят к нарушениям обменного процесса. Кислородное голодание тканей замедляет процесс деления клеток и провоцирует их распад.
Увеличение уровня глюкозы в крови также становятся причиной поражения нервных волокон — снижается чувствительность.
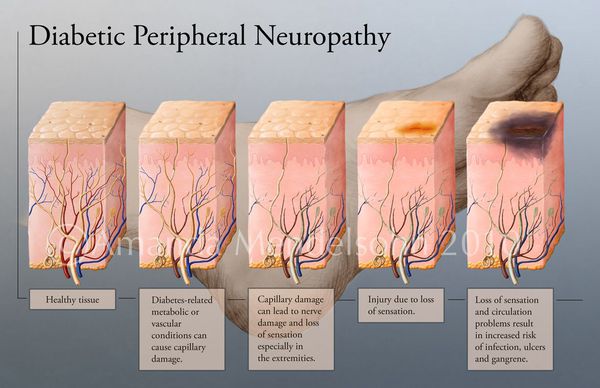
Все деструктивные процессы, происходящие в тканях стопы приводят к тому, что любое повреждение кожи становится лёгким процессом, а заживление — длительным. Усугубить состояние стопы могут присоединившиеся инфекции, которые способны привести к образованию гангрены — некрозу тканей. [9]
Классификация и стадии развития диабетической стопы
Классификация I Международного симпозиума по диабетической стопе
В 1991 году в Нидерландах на I Международном симпозиуме была принята классификация СДС, которая является наиболее распространённой. [1] Она предполагает разделение заболевания на три типа в зависимости от преобладающего патологического процесса:
- нейропатическая инфицированная стопа:
- длительное течение сахарного диабета;
- позднее возникновение осложнений;
- отсутствие болевого синдрома;
- цвет и температура кожи не изменены;
- уменьшение всех видов периферической чувствительности;
- наличие периферического пульса.
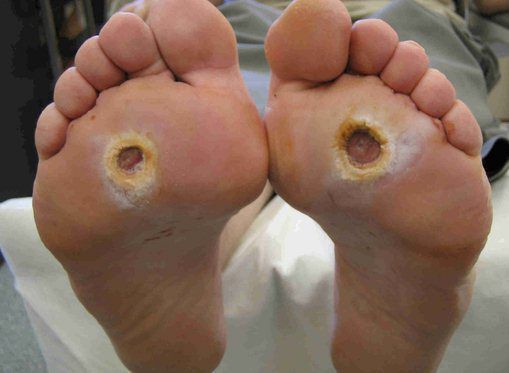
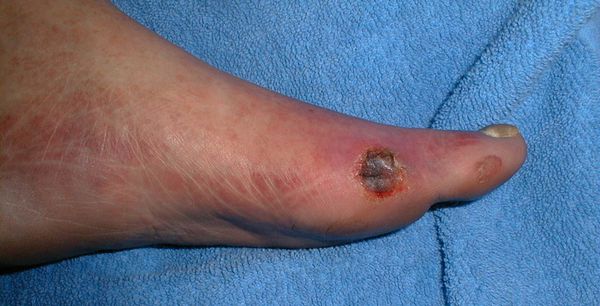
Классификация Вагнера
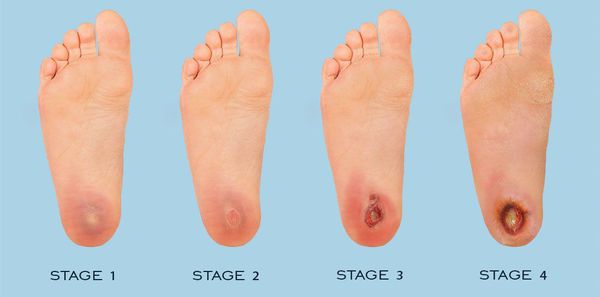
По степени выраженности поражений тканей стопы выделяют следующие стадии СДС: [6] [7]
- Стадия 0 — изменение костной структуры стопы — артропатия;
- Стадия 1 — изъязвление (язвы) кожи;
- Стадия 2 — изъязвление всех мягких тканей, дном язвы являются кости и сухожилия;
- Стадия 3 — абсцедирование и остеомиелит (воспаление костной ткани);
- Стадия 4 — образование гангрены дистальных отделов стопы (пальцев);
- Стадия 5 — образование гангрены стопы и отделов голени.
Классификация Техасского университета
Данная классификация была разработана в 1996-1998 годах. [8] В её основе лежит оценка язвы по глубине, наличию инфицирования и ишемии — риска ампутации конечности.
Читайте также:

