От чего печет кожа при сахарном диабете
Обновлено: 19.04.2024
Для цитирования: Бурова С.А. Системный и локализованный кандидоз у больных сахарным диабетом. РМЖ. 2003;17:969.
Национальная академия микологии, Центр глубоких микозов, ГКБ № 81, Москва
О собенности обменных процессов в организме больного сахарным диабетом (СД) требуют индивидуального подхода к лечению инфекционных и неинфекционных заболеваний у этих пациентов. Общей чертой разнообразных состояний при СД является гипергликемия, возникающая вследствие либо нарушения способности поджелудочной железы вырабатывать необходимое количество инсулина, либо изменения чувствительности периферических тканей к инсулину, либо сочетания того и другого.
По типу выделяют: СД 1 типа и СД 2 типа; по тяжести течения: легкой, средней и тяжелой степени.
У больных СД отмечаются гормональный дисбаланс, гиперкалиемия, нарушение липидного обмена, ожирение, снижение функции гранулоцитов, гликолиз различных белков, тканевая гипоксия, расстройство системы гемостаза, иммунные нарушения (в том числе аутоиммунные процессы), а также макрососудистые и микрососудистые осложнения, такие, как атеросклероз, ишемическая болезнь сердца, артериальная гипертония, гангрена нижних конечностей и др. [2,3].
В связи с этими факторами СД нередко осложняется присоединением различных инфекций, которые имеют свои особенности. Наиболее часто у этих пациентов поражаются мочевыводящие пути, при этом в моче выделяют грамотрицательные бактерии, стафилококки, энтерококки и, наконец, грибы, которые в структуре возбудителей у больных СД составляют, по нашим данным, 32,5%. Это объясняется также и тем, что в условиях гиперкалиемии грибы активно используют глюкозу для своих метаболических процессов и усиленно размножаются, вызывая болезнь. В большинстве случаев возбудителем являются дрожжеподобные грибы Candida аlbicans.
Клинические формы грибкового поражения мочевыводящих путей у больных СД от бессимптомной кандидурии до кандидозных уретрита, цистита, пиелонефрита, простатита, эпидидимита и баланопостита, проявляются различными по степени дизурическими явлениями, болями в поясничной и области мочевого пузыря, положительным симптомом Пастернацкого, жжением в уретре, раздражением и покраснением головки полового члена, синдромом нейрогенного мочевого пузыря, недержанием мочи и др.
На 2–м месте среди грибковых осложнений у больных СД стоят орофарингеальный кандидоз и кандидозный вульвовагинит [9]. Грибковые поражения зева и верхних дыхательных путей проявляются характерными симптомами: гиперемией, покашливанием, «раздражением» слизистой и др. Вульвовагинит встречается у женщин как в репродуктивном, так в климактерическом возрасте и проявляется характерными творожистыми выделениями из половых путей, зудом и жжением. Нередко присоединяется раздражение в области наружных гениталий и ануса.
Кандидозный бронхит и пневмония часто осложняют течение СД. Они приобретают, как правило, хроническое рецидивирующее течение, трудно поддаются излечению и характеризуются одышкой, продуктивным кашлем, болями в грудной клетке, изменением на рентгенограмме и др. симптомами [1].
Кандидозные эзофагит, синусит, ангина встречаются редко. Кандидозные и криптококковые перитонит, остеомиелит, сепсис и менингит при СД описаны в литературе недостаточно, но следует помнить об этих осложнениях у больных СД, особенно в отделениях реанимации и палатах интенсивной терапии [4,5,6].
Известно также, что при СД нарушение микроциркуляции в сосудах нижних конечностей наблюдается в 20 раз чаще, чем у лиц без эндокринной патологии. Это способствует развитию синдрома диабетической стопы, трофических язв, присоединению кандидозной инфекции [3].
В 81–й Городской клинической больнице за последние 3 года в стационаре и амбулаторно наблюдали 76 больных с системными и локализованными микозами на фоне СД, верифицированными по данным микробиологических исследований (табл. 1). Из них 27 мужчин и 49 женщин.
Кандидозный (к) стоматит выявлен у 5 больных, к. глоссит – у 4, к. фарингит – у 5, к. эзофагит – у 3, к. бронхит – у 4, к. бронхопневмония – у 2, к. пневмония – у 1, к. цистит – у 19, к. уретрит – у 11, к. острый вульвовагинит – у 18, к. баланопостит – у 2. У всех больных диагноз микоза был впервые установлен в нашей клинике.
Лечение было комплексным: соблюдение строгой диеты, применение сахароснижающих препаратов, лечение сопутствующих заболеваний, прием общеукрепляющих средств, физиотерапевтических процедур, и наконец, проведение противогрибковой этиотропной терапии.
Лечение кандидозной инфекции у больных СД имеет некоторые особенности:
- при нарушении обменных процессов, осложнениях СД и наличии многочисленных сопутствующих заболеваний у большинства больных, особенно у лиц пожилого возраста, предпочтителен толерантный противогрибковый препарат, высокоэффективный и без токсических побочных действий;
- при длительном хроническом течении заболевания и, как правило, вялотекущем процессе, требуется применять продолжительную схему лечения в адекватных разовых и курсовых дозах;
- после проведения основного курса лечения больной должен оставаться на диспансерном учете, при этом не исключаются профилактические курсы лечения системными и местными антимикотиками.
В многочисленных научных исследованиях и в практике доказано, что для лечения микозов у описанной категории больных, как впрочем, и для всех больных кандидозом, оптимальным является системный противогрибковый препарат, современный триазол – флуконазол [1,7,8].
Есть исследования, доказывающие, что именно у больных СД флуконазол резко уменьшает продукцию фосфолипазы грибами Candida albicans, тем самым уменьшая адгезивную способность этих инфектантов [9].
Приводим схемы лечения кандидоза на фоне СД системным антимикотиком флуконазолом (Медофлюконом) (табл. 2).
Применяли различный режим приема Медофлюкона в капсулах по 200 мг – 1 раз в день, 2 раза в день или через день.
Эффективность лечения определяли по исчезновению клинических симптомов болезни, рентгенологической и эндоскопической динамике и эрадикации возбудителя (табл. 3).
Таким образом, течение системных и локализованных микозов у больных СД имеет определенные особенности, что требует комплексной терапии и эффективного, нетоксичного антимикотика, более длительных курсов лечения и последующего диспансерного наблюдения. Применение Медофлюкона, как этиотропного противогрибкового средства, показало высокую эффективность: выздоровление в 67,1% случаев, улучшение в 30,3% случаев. Низкий процент побочных действий, даже у больных СД, еще раз подтвердил превосходство флуконазола (Медофлюкона) перед другими препаратами при лечении кандидоза.
1. Бурова С.А. Проблемы грибковых заболеваний человека. // Российский журнал кожных и венерологических болезней –1998–№1–с.39–41.
2. Бурова С.А., Талалаева С.М. Отдаленные результаты лечения онихомикозов у больных сахарным диабетом. // Российский журнал кожных и венерических болезней. – 2000 – №5. – с.31–33.
3. Руководство по клинической эндокринологии. /Под ред. В.Г.Баранова. – Л., 1977.
5. Magee L.T. et al. Pyrolesis typing of isolates from a recurrence of systemic cryptococcosis.// J.Med. Microbiol. – 1994 – №40(3).–p.165–169.
6. Morris B.A. et al. Cryptococcal peritonitis in CAPD patient. // J. Med. Vet. Mycal. –1992–№30(4)–p.309–315.
7. Penk A., Pittrow L. Therapeutic experience with fluconazole in the treatment of fungal infections in diabetic patients.// Mycoses. –1999–№42 Suppl.2–p.97–100.
8. Sobel J.D., et al. Candiduria a randomized d.–b. study of treatment with fluconazole and placebo.// Clin. Infect. Dis. –2000 –№30.–p.19–24.
9. Willis A.M., et al. The influence of antifungal drugs on virulence properties of Candida alb. in patient with diabetes mellitus.// Oral Surg. Med. –2001–№91(3).–p.317–321.
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Нарастание частоты заболеваемости инсулинзависимым сахарным диабетом (ИЗСД) у детей и подростков требует расширения исследований по профилактическому и раннему выявлению как доклинических стадий сахарного диабета (СД), так и его осложнений, своевременное
Ряд авторов не только признают, что поражение кожи при ИЗСД является наиболее доступным признаком для клинической оценки врачом, но и прослеживают связь между поражением кожи при ИЗСД и такими осложнениями этого заболевания, как нефропатия, нейропатия, ретинопатия, развитие ограничения подвижности суставов (ОПС) — артропатия (хайропатия)
В настоящее время поражение кожи при ИЗСД у детей может быть классифицировано следующим образом: первичное, вторичное и смешанное (сочетанное) поражения кожи; метаболические нарушения кожи; поражение кожи, связанное с лечением ИЗСД
Нарастание частоты заболеваемости инсулинзависимым сахарным диабетом (ИЗСД) у детей и подростков требует расширения исследований по профилактическому и раннему выявлению как доклинических стадий сахарного диабета (СД), так и его осложнений, своевременное обнаружение и лечение которых являются основными факторами, позволяющими предотвратить инвалидизацию и сократить смертность больных. При ИЗСД поражаются все органы и ткани организма, наиболее общим механизмом поражения является формирование диабетической микроангиопатии. Ряд авторов не только признают, что поражение кожи при ИЗСД является наиболее доступным признаком для клинической оценки врачом, но и прослеживают связь между поражением кожи при ИЗСД и такими осложнениями этого заболевания, как нефропатия, нейропатия, ретинопатия, развитие ограничения подвижности суставов (ОПС) — артропатия (хайропатия). Большинство исследований, проведенных в основном у взрослых больных, страдающих как инсулиннезависимым сахарным диабетом (ИНСД), так и ИЗСД, статистически достоверно показывают, что частота встречаемости симптомокомплекса поражения кожи, чаще всего описываемого как «диабетическая дермопатия», возрастает с повышением частоты других специфических осложнений СД. Все исследователи отмечают, что своевременная диагностика и лечение, включающее повышение уровня гликемического контроля, уменьшают проявления осложнений, а на ранних стадиях делают возможным их обратное развитие.
Особенностью кожных покровов ребенка, обусловливающей их повышенную чувствительность к патологическим изменениям, является более тонкий, чем у взрослых, и более рыхлый слой эпидермиса за счет большего содержания воды. Граница между эпидермисом и дермой неровная, связь между ними слабее, чем у взрослых. Дерма имеет преимущественно клеточную структуру, особенно у детей до шести лет; коллагеновые волокна очень тонкие, эластические, слабо развиты, тогда как волокнистая структура у взрослых имеет малое количество клеточных элементов. За счет этих особенностей защитная функция кожи у детей ослаблена — кожа более ранима, склонна к инфицированию (недостаточная кератинизация рогового слоя, его тонкость, незрелость местного иммунитета), эпидермолизу (легкое отделение эпидермиса от дермы), особенно у детей до трех лет. Поверхность детской кожи суше, чем у взрослых, имеет более выраженную склонность к шелушению вследствие физиологического паракератоза и более слабого функционирования железистого аппарата кожи.
Большинство исследователей считают, что поражения кожи при СД встречаются довольно часто, и, учитывая микроскопические изменения, они могут достигать даже 100% при манифестации заболевания. С помощью гистологических и электронно-микроскопических исследований доказано сходство морфологического строения кожи больных СД в возрасте моложе 40 лет и практически здоровых людей старше 60 лет. У них исчезают эластические волокна и активируются фибробласты, отмечаются разрывы коллагеновых пучков, снижение синтеза эластина и полимеризации коллагена при повышении количества коллагеновых белков, глюкозоаминогликанов, структурных гликопротеинов. При этом установлено, что снижение количества эластических волокон на всех стадиях старения кожи обычно предшествует изменениям коллагена.
У детей, в отличие от взрослых, практически не встречаются такие разнообразные, распространенные при СД первичные формы поражения кожи микроангиопатического и макроангиопатического генеза (в связи с резистентностью к инсулину), как генерализованная кольцевидная гранулема (granuloma annulare), папуллезно-роговой дерматоз Карле (hyperkeratosis follicularis et parafollicularis in cutem penetrans), папиллярно-пигментная дистрофия кожи (acanthosis nigricans), эруптивные ксантомы (xantoma papuloeruptivum), склередема (scleredema), кальцифилаксия (calcifilaxia), а также исчезающие гранулемы, резипелоидоподобная эритема, пигментный пурпурный дерматоз, периунгвальные телеангиоэктазии. Также крайне редки у детей и такие вторичные инфекционные поражения, в том числе кожи, как злокачественный наружный отит — тяжелая инфекция, вызываемая Pseudomonas; неклостридиальная газовая гангрена, как правило вызываемая Proteus, Klebsiella, E. coli, Pseudomonas; некротизирующий фасциит — смертельная инфекция, поражающая поверхностную фасцию. Из метаболических нарушений кожи, сопровождающих СД, практически не встречаются у детей гемохроматоз и порфирия.
- классическая — единичные крупные очаги поражения, чаще встречаемые на коже голеней, нередко с изъязвлениями;
- атипичная — с двумя вариантами течения — склеродермоподобным и поверхностно-бляшечным.
Никакое современное лечение, направленное либо на коррекцию углеводного обмена и метаболических нарушений, либо на улучшение микроциркуляции и тканевой резистентности (лазеротерапия, рентгенотерапия, криодеструкция и др.), не позволяет добиться стойких радикальных результатов. В настоящее время большинство исследователей все же рассматривают ЛН как самостоятельное заболевание — хронический дерматоз.
Таким образом, в настоящее время поражения кожи при ИЗСД у детей может быть классифицированы следующим образом:
- первичное, вторичное и смешанное (сочетанное) поражение кожи;
- метаболические нарушения кожи;
- поражение кожи, связанное с лечением ИЗСД.
Первичное поражение кожи — это сосудистые поражения (осложнения) микроангиопатического генеза — структурные и функциональные нарушения в мелких кровеносных сосудах (артериолы, венулы, капилляры). Клинически проявляются эритемой конечностей, внешне напоминающей рожу, иногда с изъязвлениями. Микроскопически характерны утолщение базальных мембран сосудов и пролиферация эндотелиальных клеток. К ним относится диабетическая дермопатия и рубеоз. Собственно диабетическая дермопатия — одна из самых распространенных форм поражения кожи — выражается в образовании множественных бессимптомных двухсторонних атрофических гиперпигментированных пятен, чаще всего на голенях. Их присутствие свидетельствует о возможности микрососудистых изменений в других тканях. Специфическое лечение дермопатии не проводится. Также имеет место рубеоз — розовый оттенок кожи лица у больных ИЗСД, обусловленный функциональной микроангиопатией или повышенным сродством гликированного гемоглобина к кислороду.
Вторичное поражение кожи включает: кожные инфекции — бактериальные и грибковые; неврологические нарушения — сенсорные, моторные и автономные.
Больные СД склонны к развитию инфекционно-воспалительных заболеваний, особенно при неудовлетворительном контроле гликемии. На поверхности кожи больных СД выявляется в 2,5 раза больше микроорганизмов, чем у здоровых лиц, а бактерицидная активность кожи у больных СД ниже, чем у здоровых, в среднем на 20%, и это снижение прямо коррелирует с тяжестью течения СД, в связи с чем при СД, в том числе ИЗСД, часто наблюдаются различные инфекционно-воспалительные и инфекционно-грибковые заболевания кожи. Прежде всего они развиваются на коже нижних конечностей, пораженных нейропатией и ишемией. Это обычно полимикробные инфекции: золотистый стафилококк, гемолитический стрептококк, грамотрицательные аэробные бактерии и множество анаэробов. На ногах, в области мозолей или в других местах трения и нарушения целостности кожи, в области ногтевых лож образуются язвы или нагноения. Инфекция может распространиться на окружающие ткани, вызывая некротизирующий целлюлит, лимфангит, гнойный миозит, некротизирующий фасциит, остеомиелит или даже газовую гангрену (такие исходы распространения инфекции у детей практически не встречаются). Пиодермии, фурункулы, карбункулы, флегмоны, рожа, дерматиты, эпидермофития, кандидомикоз, хронические паронихии и панариции, инфицированная гангрена встречаются у больных СД значительно чаще, чем в популяции. По принятой нами классификации ИЗСД у детей и подростков инфекционно-воспалительные и инфекционно-грибковые заболевания, в том числе кожи, отнесены не к сопутствующим ИЗСД заболеваниям, а к неспецифическим осложнениям ИЗСД, что правомерно, так как распространенность, тяжесть этих поражений, сложность их лечения у детей обусловлена именно наличием ИЗСД. Фурункулез у больных СД протекает тяжело и длительно, а подкожные абсцессы головы могут привести даже к тяжелым поражениям мозга. У взрослых больных СД встречается и гангрена Фурнье, для которой характерно поражение подкожных тканей в области полового члена, мошонки и промежности, реже — стенки живота. Возбудителем этого поражения является смешанная аэробная и анаэробная микрофлора. Микробно-воспалительные процессы при СД могут привести к сепсису. Присоединение инфекционно-воспалительных и грибковых заболеваний кожи, как правило, приводит к тяжелым и длительным декомпенсациям СД и увеличивает потребность организма в инсулине. У лиц с хорошим контролем СД фурункулез и карбункулы встречаются не чаще, чем в популяции здоровых. Из грибковых поражений у детей с ИЗСД наиболее распространены кандидозы, чаще всего вызывающие ангулярные стоматиты, паронихии, вульвовагиниты или баланиты.
Эпидермофитии у детей с ИЗСД довольно редки, но часто осложняются вторичной бактериальной инфекцией. Крайне редки у детей трудно поддающиеся терапии фикомикоз, мукормикоз, при которых в процесс могут вовлекаться мозговые оболочки. У детей с ИЗСД довольно распространены дерматомикозы, особенно стоп и ладоней, кожа которых становится сухой и чешуйчатой.
Широко распространены вторичные нарушения кожи, связанные с неврологической патологией при СД. Среди них: сенсорные нарушения — онемение пальцев ног, постепенно распространяющееся выше, захватывающее стопы, способствующее развитию травматических язвенных поражений, вторичных инфекций и гангрены, особенно при наличии сосудистых изменений; моторные нарушения — слабость межкостных мышц вызывает уплощение стоп с потерей смягчающей функции подошвы стоп; автономные (вегетативные) нарушения — гипергидроз верхней половины тела и сухость кожи нижней части туловища. Эти проявления относятся к диабетической нейропатии, поражающей 5-50% больных СД. У детей с ИЗСД наиболее часто встречается дистальная симметричная сенсорно-моторная полинейропатия с минимальными кожными проявлениями (сухость кожи, гиперкератоз, мозоли, вторичное инфицирование пораженных участков кожи, нарушения роста ногтей), обратимая в фазе начальных проявлений. Именно нейропатия — один из ведущих патогенетических факторов развития в дальнейшем синдрома «диабетической стопы» (ДС). Среди больных СД, осложненным синдромом ДС, частота ампутации нижних конечностей в 15 раз выше, чем у остального населения. При преобладании нейропатических изменений над изменениями периферического кровотока развивается нейропатическая форма ДС, одним из вариантов течения которой является поражение кожи — нейропатическая язва. Она чаще возникает на участках стопы, испытывающих давление, — плантарной поверхности и межпальцевых промежутках. Длительно протекающая сенсорно-моторная нейропатия приводит к деформации стопы с перераспределением и повышением давления на ее отдельные участки. В этих местах отмечается утолщение кожи, гиперкератоз с высокой плотностью. В дальнейшем развивается аутолиз подлежащих мягких тканей с формированием язвенного дефекта, при этом больной может ничего не замечать из-за снижения болевой чувствительности. Язвенный дефект может вторично инфицироваться, в том числе анаэробной микрофлорой, с развитием гипертермии, лейкоцитоза, требующих срочного хирургического лечения с некроэктомией, антибактериальной терапией, улучшением гликемического контроля. У детей все формы ДС встречаются крайне редко, но начальные проявления имеют место в детском возрасте, что требует адекватного обучения, обследования и лечения больных, в том числе прицельного осмотра состояния кожи при ИЗСД.
К смешанному (сочетанному) поражению кожи при СД относятся: утолщение кожи (синдром «диабетической руки» — ОПС с утолщением кожи и склеродермоподобным синдромом), желтый цвет кожи и ногтей, синдром «диабетических пузырей», пруригус и повреждения волос. К нему же следует отнести склеродермоподобные изменения кожи пальцев и тыльной части кистей рук, снижающие их подвижность. Кожа утолщается в области пальцевых суставов и периунгвально. Эти изменения, иногда в сочетании с артропатией (ОПС), описываются некоторыми исследователями как синдром «диабетической руки». Часто с утолщением кожи ассоциируется гиперкератоз. Желтый цвет кожи и ногтей (ксантохромия) ранее связывался с гиперкаротинемией, но сейчас доказано, что при СД в крови сохраняется нормальный уровень каротина. В настоящее время этиология и патогенез не выяснены. Синдром «диабетических пузырей» возникает редко, как правило на коже конечностей. Выявляются одиночные или множественные пузыри, заживающие без рубцевания через две—пять недель. Возможна симптоматическая терапия. Пруригус — поражение кожи в аногенитальной области на фоне кандидоза (гиперемия, трещины, шелушения, вторичное инфицирование). Иногда при плохо контролируемом СД может быть диффузное выпадение, а у больных пониженного питания — избыточный рост волос (лануго) на коже рук и спины. Редко, обычно при плохом уровне гликемического контроля, наблюдаются повышенное шелушение кожи, себорейный дерматит, ихтиозоподобный синдром, особенно в области голеней.
К метаболическим нарушениям кожи при СД относится ксантоматоз, редко встречающийся в детском возрасте и являющийся следствием гиперлипидемии. Клинически ксантоматоз проявляется в виде плотных желтых папул с эритематозным ободком, чаще на кистях, стопах, ягодицах, разгибательных поверхностях верхних и нижних конечностей. Купируется адекватной инсулинотерапией.
Специфическими кожными осложнениями лечения ИЗСД являются липодистрофии, образующиеся в местах инъекций инсулина. Встречаются в виде липом или липогипертрофий (плюс-ткань) и липоатрофий (минус-ткань). В связи с широким применением в настоящее время хорошо очищенных биосинтетических человеческих инсулинов липоатрофии встречаются крайне редко. В настоящее время именно липогипертрофии, или липомы, представляют собой наиболее распространенную проблему для больных ИЗСД, даже при небольшом сроке заболевания. Они возникают в результате некорректной техники введения инсулина (нарушения схем ротаций мест инъекций инсулина, несоблюдение техники и правил введения препаратов), а иногда и без видимых причин; затрудняют абсорбцию и метаболизм инсулина, ухудшают компенсацию заболевания, увеличивают потребность в инсулине, создают косметические дефекты на коже. Кроме вышеописанных правил профилактики липодистрофий, в случае их появления дополнительно и с хорошим эффектом применяется массаж липом, физиотерапия. Также у некоторых больных периодически возникают кровоподтеки в местах инъекций инсулина. Эти места, как правило, теплее на ощупь, чем окружающая кожа.
Обобщая вышеизложенное, можно сказать, что исследование кожи, представляющей собой наиболее доступную неинвазивному клиническому осмотру систему организма, имеет огромное клиническое значение. Знание особенностей поражения кожи у детей при ИЗСД не только помогает в оценке фазы течения заболевания, но и имеет непреходящее значение для решения вопросов о направлении диагностического поиска, коррекции лечения и прогнозе течения ИЗСД.
Что такое диабетическая стопа? Причины возникновения, диагностику и методы лечения разберем в статье доктора Есипенко И. А., сосудистого хирурга со стажем в 37 лет.
Над статьей доктора Есипенко И. А. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Диабетическая стопа (синдром диабетической стопы, СДС) — это тяжёлое осложнение сахарного диабета в виде инфекции, язв или разрушения глубоких тканей, которое возникает в связи с нарушением макроструктуры стопы и микроциркуляции крови, по причине разрушения нервных окончаний и нервных волокон. [10]
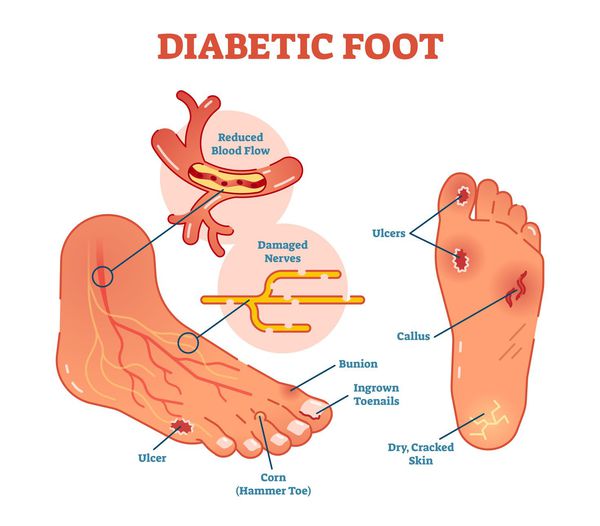
Главная причина ДС — это сахарный диабет (СД). И хотя синдром диабетической стопы не развивается с первого дня увеличения уровня глюкозы в крови более 7,0-8,0 ммоль/л, каждый пациент с диагнозом «сахарный диабет» должен помнить о таком грозном возможном осложнении.
Хронические раны на ногах у людей с сахарным диабетом встречаются в 4-15 % случаев. В некоторых случаях они становятся первым признаком развившегося диабета [10] .
Основные «пусковые механизмы» развития язв при СДС:
1. Ношение неудобной обуви. К изменению нагрузки на суставы стопы, сдавливанию или потёртости кожи, локальной микроишемии, инфильтрату, или некрозу могу привести любые дефекты обуви:
- несоответствующий размер обуви (меньше или больше, чем нужно);
- стоптанные и/или высокие каблуки;
- рубец на стельке;
- дефект подошвы;
- мокрая обувь;
- несоответствие обуви времени года.
2. Увеличенный вес тела. Учитывая площадь стоп, при увеличении веса тела (даже на 1 кг) увеличивается и нагрузка на каждый сустав стопы. Самая уязвимая область — подошвенная поверхность.
3. Разрастание эпидермиса (поверхности) кожи. Этот процесс происходит из-за нарушенных обменных процессов в коже на фоне СД (под утолщённым эпидермисом-"мозолью" в слоях кожи нарушается микроциркуляция, что приводит к микроишемии и некрозу).
4. Микротравмы:
- укусы животных;
- уколы шипами растений;
- порезы при педикюре и т. п.
5. Стенозы (сужение) и окклюзии (закупорка) магистральных артерий. В результате отсутствия кровоснабжения в стопах и голенях к микроишемии присоединяется макроишемия и развитие гангрены конечности.
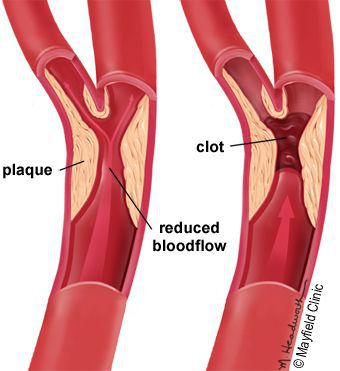
6. Условно патогенная или патогенная микрофлора. Активизация флоры (микробов и других микроорганизмов) на поверхности кожи в условиях СД приводит к воспалению кожного покрова, а в условия ишемии или микротравмы значительно ускоряется развитие гангрены.
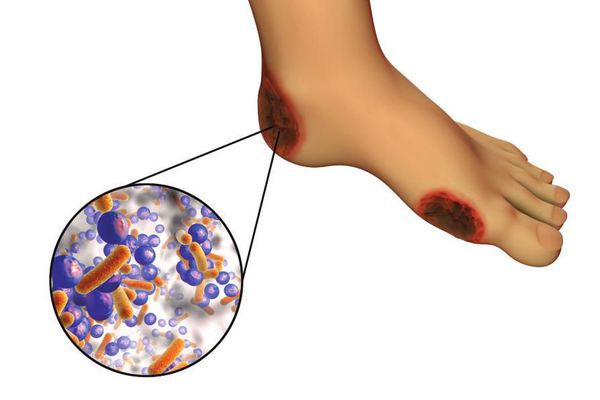
Часто наблюдается сочетание нескольких причин возникновения язв при СДС.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы диабетической стопы
Отправной точкой развития СДС считается не дата установления диагноза «Сахарный диабет», а время, когда были выявлены первые симптомы СД (однократные подъёмы глюкозы крови, сухость во рту и другие).
Симптомы СДС:
- онемение, зябкость, жжение, отёки в стопах и другие неприятные ощущения;
- выпадение волос на на стопах и голенях, потливость стоп;
- изменение окраски кожи (гиперемия, гиперпигментация, цианоз);
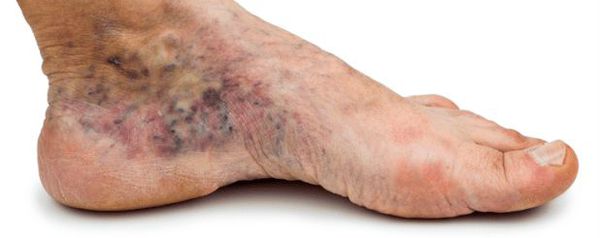
- утолщение, расслаивание, изменение формы и цвета ногтевых пластинок;
- кровоизлияния под ногтевой пластинкой в виде «синяков» под ногтями;
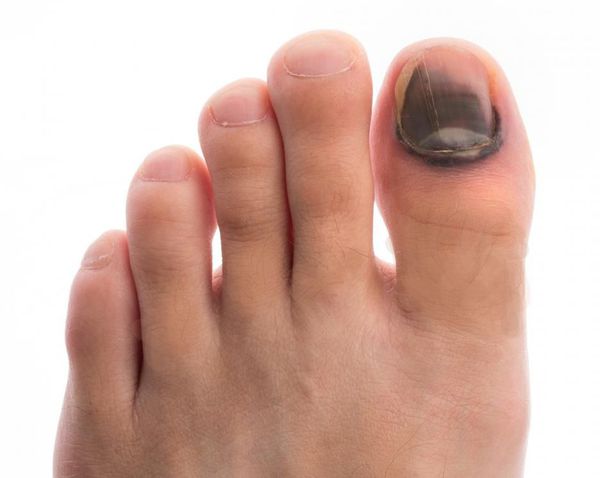
- деформация стоп;
- снижение чувствительности стоп — вибрационного, температурного, болевого и тактильного восприятия;
- боль в области стопы и язвы, возникающая как в покое или ночью, так и при ходьбе на определённые расстояния;
- истончение кожи, шелушение;
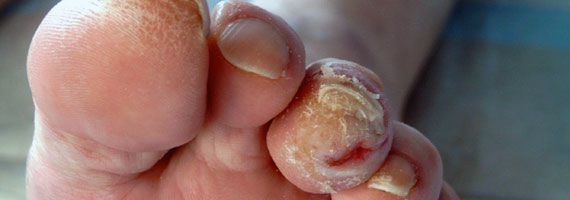
- понижение или увеличение температуры стоп и голеней;
- длительная эпителизация (заживление) микротравм — до двух месяцев, при этом остаются коричневые рубцы;
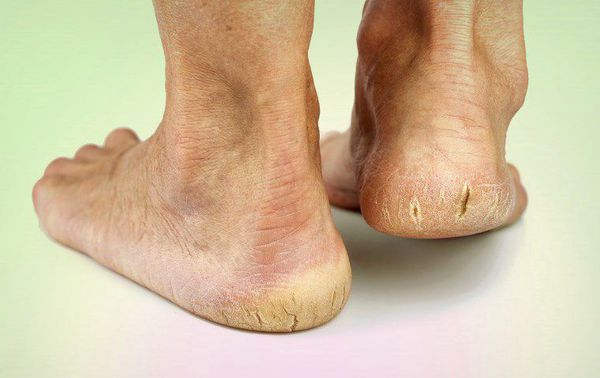
- трофические язвы, длительно не заживающие на стопах.
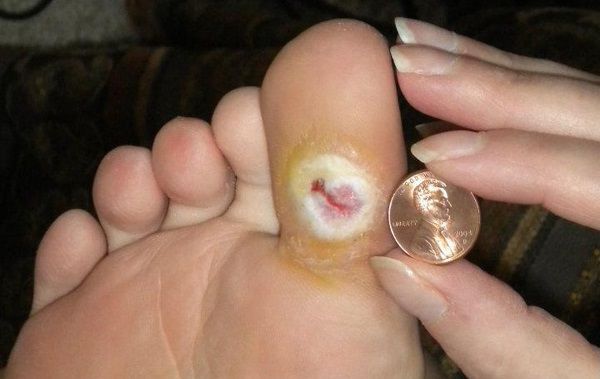
Чаще всего трофическим изменениям подвержены дистальные отделы конечности: пальцы и подошвенная поверхность стопы в проекции головок плюсневых костей. Зона образования трофической язвы зависит от причины её возникновения.
Патогенез диабетической стопы
Механизм развития СДС представляет собой следующую последовательность нарушений:
- Снижается выработка гормона инсулина.
- Увеличивается уровеь глюкозы в крови — развивается гипергликемия.
- Блокируется кровоток в мелких сосудах, через сосудистую стенку перестаёт поступать кислород и другие микроэлементы.
- Разрушаются нервные волокна и рецепторы.
- Наступает микро- и макроишемия тканей стопы.
- Образуются трофические язвы.
Таким образом, при СДС происходит повреждение всех тканей ноги.
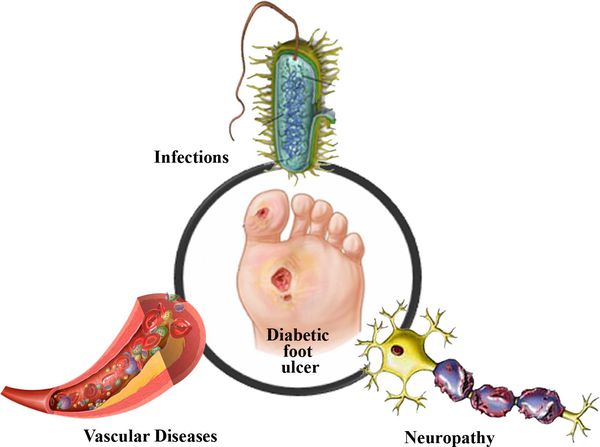
В результате дефицита инсулина в организме диабетика количество глюкозы в крови увеличивается. Это в свою очередь негативно сказывается на состоянии как мелких, так и крупных сосудов:
- на стенках сосудов скапливаются иммунологические вещества;
- мембраны становятся отёчными;
- просвет сосудов сужается.
В результате этих изменений кровообращение нарушается и образуются небольшие тромбы. Эти изменения в организме препятствуют поступлению достаточного количества микроэлементов и кислорода в клетки и тем самым приводят к нарушениям обменного процесса. Кислородное голодание тканей замедляет процесс деления клеток и провоцирует их распад.
Увеличение уровня глюкозы в крови также становятся причиной поражения нервных волокон — снижается чувствительность.
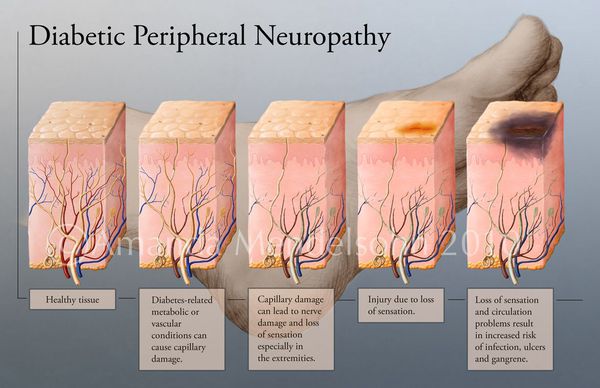
Все деструктивные процессы, происходящие в тканях стопы приводят к тому, что любое повреждение кожи становится лёгким процессом, а заживление — длительным. Усугубить состояние стопы могут присоединившиеся инфекции, которые способны привести к образованию гангрены — некрозу тканей. [9]
Классификация и стадии развития диабетической стопы
Классификация I Международного симпозиума по диабетической стопе
В 1991 году в Нидерландах на I Международном симпозиуме была принята классификация СДС, которая является наиболее распространённой. [1] Она предполагает разделение заболевания на три типа в зависимости от преобладающего патологического процесса:
- нейропатическая инфицированная стопа:
- длительное течение сахарного диабета;
- позднее возникновение осложнений;
- отсутствие болевого синдрома;
- цвет и температура кожи не изменены;
- уменьшение всех видов периферической чувствительности;
- наличие периферического пульса.
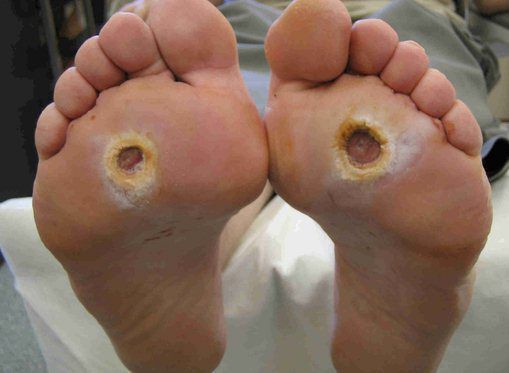
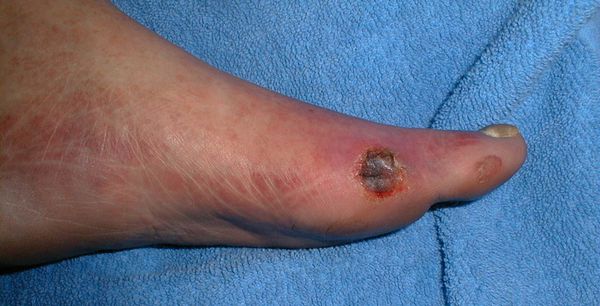
Классификация Вагнера
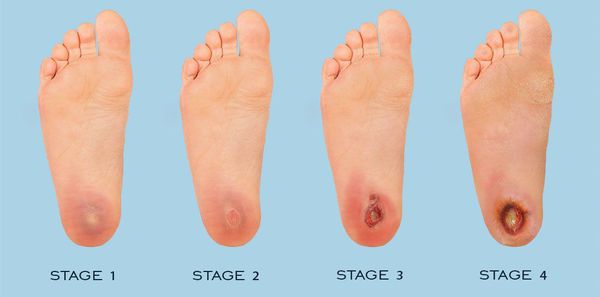
По степени выраженности поражений тканей стопы выделяют следующие стадии СДС: [6] [7]
- Стадия 0 — изменение костной структуры стопы — артропатия;
- Стадия 1 — изъязвление (язвы) кожи;
- Стадия 2 — изъязвление всех мягких тканей, дном язвы являются кости и сухожилия;
- Стадия 3 — абсцедирование и остеомиелит (воспаление костной ткани);
- Стадия 4 — образование гангрены дистальных отделов стопы (пальцев);
- Стадия 5 — образование гангрены стопы и отделов голени.
Классификация Техасского университета
Данная классификация была разработана в 1996-1998 годах. [8] В её основе лежит оценка язвы по глубине, наличию инфицирования и ишемии — риска ампутации конечности.
Очень часто пациенты с диабетом, особенно с суб- или декомпенсированным диабетом, испытывают серьезные проблемы с кожей. Часто возникает вопрос: а как нарушение углеводного обмена – сахарный диабет – связан с сухостью кожи и кожными инфекциями, которым они подвержены? Ведь всё это свидетельствует о нарушении барьерной, защитной функции кожи, вернее, состояния эпидермиса и даже – его верхнего, рогового, слоя. И почему при высоком уровне сахара в крови страдает кожа?
При сахарном диабете кожа становится более уязвимой и требует особого и ежедневного ухода. Сухость, трещины, натоптыши, утолщение кожного покрова, и как следствие повышенный риск инфицирования – все эти проблемы поможет решить специализированная линейка косметических средств.
Как происходит снижение защитных свойств кожи при диабете
Нарушение защитной, барьерной функции кожи напрямую связано с ее сухостью, с нехваткой воды в верхнем, роговом, слое кожи.
Причин такого серьезного нарушения гидратации рогового слоя при диабете несколько:
- Нарушение микроциркуляции крови в капиллярах, которыми пронизана дерма – внутренний слой кожи. Это состояние называется «микроангиопатией». В норме часть воды попадает в роговой слой из нижних слоев кожи, которые пронизаны сетью мелких кровеносных сосудов. Вода из капилляров дермы поднимается вверх и задерживается в роговом слое особыми молекулами – компонентами Натурального Увлажняющего Фактора. При диабете кровоснабжение дермы нарушается, воды становится меньше, роговой слой ее не получает изнутри.
- На поверхности кожи всегда есть естественная водно-жировая пленка, которая состоит из воды, кожного сала и компонентов пота. Она снижает испарение воды из эпидермиса. Но при диабете нарушается ее состав из-за изменения кислотности: поверхность кожи, которая в норме должна быть слабокислой, становится слабощелочной (рН 7.0 и выше). Соотношение жира и воды в пленке меняется, и она уже не может удерживать воду. И к тому же изменение среды ухудшает микрофлору кожи (состав и количество живущих на нашей коже бактерий): начинают быстро размножаться болезнетворные микроорганизмы, возрастет риск инфекции.
- Очень специфическим изменением кожи при диабете является следствие гликирования коллагена (связывания глюкозы с коллагеном и эластаном). Если глюкозы в крови много, то она вступает в химические реакции с белками кожи, в первую очередь с коллагеном. А если коллаген оказывается связанным, он не может поддерживать упругость кожи, и она становится жесткой или, наоборот, дряблой, внешний вид ухудшается.
Ксероз и гиперкератоз
Научное название сухости кожи – ксероз или ксеродермия. При этом состоянии кожа вялая, ее упругость снижена, она шелушится, что часто сопровождается зудом. Такая кожа тонкая, как пергамент, и ухаживать за ней следует с осторожностью. Желательно использовать только специализированные косметические кремы с небольшим процентом мочевины (3-5%). Этот ингредиент проникает в роговой слой и удерживает вокруг себя молекулы воды, не давая им испаряться. Высокое содержание питательных масел (авокадо, кокосовое) в таких кремах помогает смягчать сухость и насыщает кожу необходимыми липидами.

Гиперкератоз, наоборот, - это избыточное ороговение, утолщение кожи. Роговой слой разрастается, потому что нарушается процесс отшелушивания корнеоцитов («кирпичиков» рогового слоя). Чаще всего это происходит на конечностях. Такие ороговевшие, потрескавшиеся пятки знакомы практически всем взрослым людям, а не только диабетикам. Но при диабете это нарушение состояния кожи встречается гораздо чаще и гораздо опаснее: под толстым слоем кожи, под сухой мозолью может образоваться внутренняя язва, что приведет к синдрому диабетической стопы. Этому грозному осложнению диабета подвержены 6% людей с нарушением углеводного обмена, поэтому уход за проблемной кожей стоп является важной частью профилактики этого синдрома. Для избавления от гиперкератоза нужны уже кремы с более высоким содержанием мочевины: 10% и даже выше.
Мочевина в кремах при диабете: зачем, сколько и когда?
Эффективность таких кремов значительно повышается, если в их состав помимо мочевины входит молочная кислота, усиливающая их кератолитическое (отшелушивающее) действие. Схема действий проста и понятна: чистые пяточки обрабатываются мелкой пемзой или мягкой пилочкой, а потом на кожу наносится крем. Желательно делать это сразу после водных процедур, пока кожа еще влажная.

Микротравмы кожи при диабете

И в заключение приведем общие правила ухода за сухой кожей, которые помогут восстановить ее защитную функцию и улучшить качество жизни пациента:
- Для купания и умывания не использовать щелочное натуральное мыло (твердое, кусковое), у которого кислотность (рН) составляет 7.0-12.0, а использовать жидкие средства для с кислотностью (рН) 4.5-5.7.
- Избегать частого и продолжительного мытья, особенно в горячей воде.
- Для ухода за сухой кожей использовать эмоленты (смягчающие и увлажняющие косметические средства) на основе глицерина, мочевины, ниацинамида (витамин В3).
- Наносить на кожу эмоленты не реже 2 раз в день.
- Для ухода за раздраженной кожей использовать кремы, содержащие 2.5-5% пантенола.
Источники
- Demirseren D. D. et al. Relationship between skin diseases and extracutaneous complications of diabetes mellitus: clinical analysis of 750 patients //American journal of clinical dermatology. – 2014. – Т. 15. – №. 1. – С. 65-70.
- Macedo G. M. C., Nunes S., Barreto T. Skin disorders in diabetes mellitus: an epidemiology and physiopathology review //Diabetology & metabolic syndrome. – 2016. – Т. 8. – №. 1. – С. 63.
- Zhang P. et al. Global epidemiology of diabetic foot ulceration: a systematic review and meta-analysis //Annals of medicine. – 2017. – Т. 49. – №. 2. – С. 106-116.
- Lichterfeld A. et al. Evidence-based skin care //Journal of Wound, Ostomy and Continence Nursing. – 2015. – Т. 42. – №. 5. – С. 501-524.
- Shakya S., Wang Y., Mack JA., Maytin EV. Hyperglycemia-Induced Changes in Hyaluronan Contribute to Impaired Skin Wound Healing in Diabetes: Review and Perspective. //Int J Cell Biol - 2015 - Vol.2015 - p.701738.
Редакция благодарит специалистов компании АВАНТА за помощь в подготовке материала.
Для цитирования: Волковой А.К., Комелягина Е.Ю., Анциферов М.Б. Поражения нижних конечностей у больных сахарным диабетом. РМЖ. 2006;13:972.
Сахарный диабет (СД) является одним из наиболее распространенных хронических заболеваний и носит характер неинфекционной эпидемии. В настоящее время около 200 млн. человек в мире страдают СД, при этом количество больных ежегодно увеличивается на 5–7% и каждые 15 лет удваивается. По прогнозам экспертов ВОЗ, их число к 2025 году достигнет 325 млн. человек, а у 410 млн. человек будет определяться нарушенная толерантность к глюкозе (НТГ). СД характеризуется ранней инвалидизацией и высокой смертностью больных вследствие развития поздних сосудистых осложнений. Это обстоятельство ставит СД в ряд социально значимых заболеваний.
Поражения нижних конечностей у больных сахарным диабетом являются одной из основных причин инвалидизации, так как риск выполнения нетравматических ампутаций нижних конечностей у больного СД в 22 раза выше по сравнению с аналогичной вероятностью при отсутствии диабета [1]. Вышеуказанный факт явился одной из основных причин, по которой в Сент–Винсентской декларации (1989 г.) провозглашено снижение в мире к 2000 году на 50% количества высоких ампутаций среди больных сахарным диабетом [2].
К поражениям нижних конечностей у больных сахарным диабетом относятся: диабетическая нейропатия (ДН), поражения магистрального кровотока нижних конечностей (макроангиопатия), синдром диабетической стопы (СДС).
Диабетическая нейропатия
Диабетическая нейропатия – наличие симптомов и/или объективных признаков нейрональной дисфункции у больного сахарным диабетом, при условии исключения других причин [3]. Распространенность осложнения достаточно высока, в зависимости от различных методов обследования варьирует в пределах 30–50% [4]. А если к числу пациентов, имеющих явные клинические признаки диабетической нейропатии, прибавить пациентов с субклиническими формами, то частота нейропатии может достичь 90% [5].
Существуют различные классификации диабетической полинейропатии, одна из которых приводится ниже.
Классификация диабетической полинейропатии [6]:
• Гипергликемическая нейропатия
• Генерализованные нейропатии:
– сенсо–моторная
– острая болевая
– автономная
– острая моторная
• Фокальные и мультифокальные нейропатии
• Гипогликемичекая нейропатия.
В аспекте поражения нижних конечностей в клинической практике чаще всего встречается сенсо–моторная нейропатия, о которой и пойдет речь далее.
Ключевая роль в патогенезе диабетической нейропатии принадлежит хронической гипергликемии [7]. Длительно существующий повышенный уровень сахара в крови приводит к активации полиолового пути обмена глюкозы, вызывает оксидативный стресс, снижает образование оксида азота, уменьшает кровоток в нервном волокне, нарушает образование факторов роста. Все вышеуказанные механизмы являются причиной гибели нервной клетки и приводят к замедлению проведения импульса по нервному волокну.
Клинические проявления ДН значительно снижают качество жизни больных и являются важнейшим патогенетическим и прогностически значимым фактором риска развития ряда осложнений сахарного диабета, в частности, синдрома диабетической стопы.
Клиническая симптоматика ДН может быть положительной (продуктивной), когда пациент предъявляет определенные жалобы, и отрицательной, когда активные жалобы отсутствуют, но уже имеются нарушения чувствительности. В основном выделяют болевые и безболевые варианты поражений [8]. При отсутствии активных жалоб больного диагноз нейропатии можно поставить только на основании результатов осмотра и диагностического исследования. Среди болевых форм нейропатий выделяют острую и хроническую [9].
Продолжительность острой болевой формы составляет 6 месяцев. Появляются колющие, стреляющие, ноющие боли в стопах и голенях; чувство жжения, онемения, стягивания стоп. Интенсивность болевого синдрома может усиливаться в вечернее и ночное время.
Для хронической нейропатии характерно наличие болевой симптоматики более полугода. Клиническая картина болевого синдрома разнообразна по интенсивности и частоте. Компенсация СД может приводить к регрессу субъективных симптомов, в то время как ненадлежащий контроль уровня глюкозы в крови, напротив, ухудшает чувствительность и усиливает чувство онемения, жжение, покалывание, парестезии.
В таблице 1 приведены основные клинические проявления нейропатии в зависимости от стадии развития патологического процесса [10].
Диагноз ДН устанавливается на основании характерных жалоб, анамнеза (давность симптоматики, наличие сопутствующей патологии), данных объективного осмотра. В клинической практике при помощи специальных инструментов определяются нарушения различных видов чувствительности. Для оценки наличия изменений тактильной чувствительности применяется монофиламент весом 10 г (5,07 Semmens–Weinstein), болевой – укол тыльной поверхности большого пальца специальной иглой с притупленным концом, температурной – при помощи определения разницы в ощущениях тепла и холода инструментом «tip therm», вибрационной – с использованием камертона либо биотезиометра. Ахилловы и коленные рефлексы применяются для оценки нарушений моторной функции. С целью раннего выявления и углубленного исследования ДН выполняется электромиография с определением скорости проведения импульса по нервному волокну. К наиболее точным методам диагностики можно отнести биопсию нерва с последующим морфологическим исследованием.
Для дифференциального диагноза с нарушением магистрального кровотока нижних конечностей проводится ультразвуковая допплерография (УЗДГ) артерий голеней и стоп.
Лечение диабетической полинейропатии
Лечение ДН отличает комплексный подход и во многом зависит от стадии развития патологического процесса. В таблице 2 приведены принципы ведения больных сахарным диабетом с наличием диабетической полинейропатии.
Как видно, на начальной стадии лечения обязательным условием является достижение компенсации углеводного обмена. Кроме того, нормализация гликемии часто приводит к устранению нейропатических болей, в то время как лекарственная терапия на фоне декомпенсации углеводного обмена может быть малоэффективной.
Назначение средств симптоматической терапии направлено прежде всего на устранение симптомов периферической нейропатии (боли, судороги, жжение, парестезии). Могут назначаться:
• трициклические антидепрессанты (имипрамин, амитриптиллин)
• противосудорожные препараты (габапентин, карбамазепин)
• анальгетики
• местно раздражающие средства
К препаратам патогенетической направленности относятся:
• ингибиторы альдозоредуктазы
• g–линоленовая кислота
• ингибиторы конечных продуктов гликирования структурных белков
• препараты a–липоевой кислоты
• факторы роста нерва
• миоинозитол
В настоящее время из всех вышеуказанных методов патогенетического воздействия, на основании ряда международных плацебо–контролируемых исследований, свою эффективность доказали препараты a–липоевой кислоты.
Необходимо отметить, что одной из основных задач ведения больных с диабетической периферической полинейропатией является предупреждение развития язвенных дефектов стоп. В данном аспекте основная роль принадлежит обучению больных правилам ухода за ногами, подбору ортопедической обуви.
Диабетическая ангиопатия
нижних конечностей
Под диабетической ангиопатией нижних конечностей понимают «наличие таких клинических признаков, как отсутствие пульса на артериях стоп, перемежающаяся хромота в анамнезе, наличие болей покоя и/или изменений, выявляемых при неинвазивном сосудистом обследовании, указывающих на нарушение кровообращения» [3].
Снижение кровотока является ведущим фактором, нарушающим процессы репарации тканей и в сочетании с инфекцией – основным фактором ампутаций нижних конечностей [11].
Развитию диабетической макроангиопатии способствуют: курение, артериальная гипертензия, хроническая гипергликемия, гиперлипидемия, возраст, генетическая предрасположенность, длительность СД [12].
К проявлениям макроангиопатии при сахарном диабете относятся: медиакальциноз (склероз Менкеберга) и атеросклероз. Склероз Менкеберга – кальцификация средней оболочки артериальной стенки. Как правило, медиакальциноз в изолированном виде не является причиной ишемии конечности, так как не сопровождается уменьшением просвета сосуда. Есть мнение, что склероз Менкеберга ассоциируется с автономной полинейропатией [13].
Течение атеросклероза при сахарном диабете имеет некоторые отличия по сравнению с атеросклерозом при его отсутствии [14]. Морфологически атеросклеротическое поражение сосудов характеризуется циркулярным расположением бляшек, системностью, склонностью к осложненным поражениям с казеозным распадом, образованием аневризм, а клинически – поражением больных более молодого возраста, одинаковой частотой встречаемости у мужчин и женщин, более быстрым прогрессированием, частым поражением подколенных и берцовых артерий.
Клинически ангиопатия нижних конечностей проявляется болями в области голеней при ходьбе – «синдромом перемежающейся хромоты», зябкостью стоп. При осмотре – ослабление или отсутствие пульсации магистральных сосудов нижних конечностей; мраморная окраска кожи, алопеция в области голеней, гипотермия стоп. В запущенных случаях развивается критическая ишемия конечности. Она характеризуется наличием ишемической боли в покое более чем в течение 2–х недель, и/или наличием язв или гангрены в области стопы или пальцев при систолическом давлении в области тибиальных артерий 1,15).
К углубленным методам диагностики поражений магистрального кровотока нижних конечностей относится дуплексное сканирование артерий. «Золотым стандартом» исследования сосудистого русла считается ангиография. Показанием к выполнению ангиографии или аорто–артериографии является выявление стеноза или окклюзии по УЗДГ для определения возможности выполнения реконструктивной операции.
Для оценки степени выраженности ишемии тканей все более широкое распространение приобретает метод определения транскутанного напряжения кислорода на нижних конечностях. Посредством чрескожного газоанализа удается измерить локальную оксигенацию (ТсрО2) кожи и, таким образом, оценить прогноз заживления раневого дефекта. Критическим показателем считается уровень ТсрО2 1,2 ммоль/л, триглицериды
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Читайте также:

