Очаговый акантоз многослойного плоского эпителия что это
Обновлено: 26.04.2024
Опухолеподобные поражения шейки матки. Классификация опухолей шейки матки.
В шейке матки возникают разнообразные процессы, захватывающие как ее влагалищную часть, так и слизистую оболочку цервикального канала (канала шейки матки).
При морфологической диагностике следует учитывать функциональный характер изменений эпителия и стромы, возникающих в связи со сменой фаз менструального цикла. В пролиферативной фазе менструального цикла многослойный плоский эпителий эктоцервикса достигает наибольшей толщины, клетки промежуточного и функционального слоев богаты гликогеном. Призматический эпителий эндоцервикса высокий, с базальным расположением ядер, в цитоплазме определяют слизь. Резервные клетки единичны, находятся в состоянии покоя.
В секреторной фазе менструального цикла начинается отторжение поверхностных клеток функционального слоя многослойного плоского эпителия, особенно над высокими соединительнотканными сосочками подэпителиальной ткани. В базальном слое отмечают повышенную митотическую активность. В эпителии эндоцервикса обнаруживают большое количество пролиферирующих резервных клеток с образованием 2— 3-рядных и многослойных пластов, внутриэиителиальных железистых структур. Со стороны призматического эпителия отмечают миграцию ядер в центр клеток и повышение слизеобразования.
В строме слизистой оболочки экто- и эндоцервикса имеются скопления лимфоидных клеток, гистиоцитов, встречаются «тучные» клетки. В десквамативной и регенераторной фазах менструального цикла наблюдают слущивание большей части клеток функционального и промежуточного слоев многослойного плоского эпителия; разрыхление базальной мембраны; инфильтрацию межуточной ткани лимфоидными и гистиоцитарными элементами. В призматическом эпителии эндоцервикса снижается количество слизи, клетки уменьшаются в размерах, ядра расположены базально. Гиперплазия резервных клеток отсутствует.
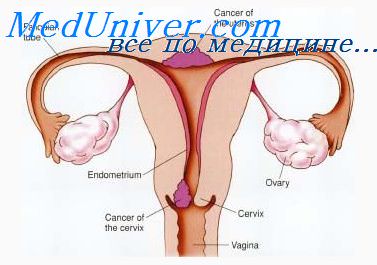
Граница многослойного плоского эпителия влагалищной части и призматического эпителия эндоцервикса чаще всего находится у наружного маточного зева, однако она может быть сдвшгута как в сторону влагалищной части, так и эндоцервикса. Судят о границе но так называемой последней цервикальной железе [Burghardt, 1984], которая является как бы ее маркером. Обнаруживающийся в области эктопий и эндоцервикозов многослойный плоский эпителий, по данным Burghardt, всегда метапластический.
Камбиальными элементами многослойного плоского эпителия эктоцервикса, за счет которых происходит его регенерация, являются базальные клетки призматического эпителия — резервные клетки. Резервные клетки плюрипотентны и могут в процессе пролиферации образовывать как железистые структуры, так и метаплазированный многослойный плоский эпителий. Последний на ультраструктурном уровне по характеру межклеточных контактов и цитоскелету отличается от истинного многослойного плоского эпителия. Резерв ные клетки в призматическом эпителии эндоцервикса обнаруживают непостоянно, их много в шейке матки новорожденных и грудных детей.
У женщин пубертатного периода они появляются в значительном количестве в секреторной фазе менструального цикла, в первой половине беременности и при различных дисгормональных нарушениях. Все это необходимо учитывать при интерпретации того или иного патологического процесса.
В классификации отсутствует четкое подразделение на фоновые, пред-опухолевые и опухолевые процессы. Выделенная рубрика «Опухолеподобные изменения» по существу включает фоновые процессы. Причем в ней представлены как нозологические формы» так и фрагменты патологических изменений, встречающиеся при различных фоновых заболеваниях и в норме. Например, метаплазия в многослойный плоский эпителий может наблюдаться в области эндоцервикозов, полипов, и она же возникает в канале шейки матки в период беременности, при гормональных нарушениях и гормонотерапии. Таким образом, самостоятельного значения этот процесс не имеет, он всегда связан с чем-то, являясь выражением либо нормы, либо частью патологического процесса.
Возникающие в шейке матки поражения неоднозначны в отношении перехода в злокачественные новообразования, поэтому их следует подразделять на фоновые процессы, предопухолевые изменения и опухоли.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.

Врач гинеколог-эндокринолог. Стаж 19+ лет. Принимает в Университетской клинике в Санкт-Петербурге. Стоимость приема 1700 руб.
- Запись опубликована: 03.12.2019
- Reading time: 2 минут чтения
Паракератозом называются патологические изменения в слизистой шейки матки, сопровождающиеся появлением на ней плотных участков. Патология относится к дискератозам – нарушениям, при которых происходит уплотнение (ороговение) слизистой. Такие очаги опасны переходом в рак.
Механизм развития паракератоза шейки
Здоровая слизистая шейки покрыта многослойным плоским эпителием. Его клетки постоянно обновляются – старые отшелушиваются, а на их месте появляются новые.
При нарушении этого процесса отжившие свой срок клетки не отторгаются, а формируют плотные участки, которые называют частично ороговевшими – паракератическими. Это состояние опасно с точки зрения онкологии.
Причины паракератоза шейки
- Хроническое воспаление шейки матки – цервицит, ее слизистой – эктоцервицит, цервикального канала – эндоцервицит.
- Хронический воспалительный процесс слизистой влагалища – кольпит – и матки (эндометрит, метрит).
- Инфекции половой сферы. Изменения в тканях часто возникают на фоне хламидиоза, уреаплазмоза, микоплазмоза, трихомониаза, генитального герпеса.
- Инфицирование папилломавирусом. Возбудитель проникает в слизистую шейки, вызывая образование неправильно развитых (атипичных) клеток.
- Травмы шейки матки, вызванные абортами и родами.
- Неправильное лечение патологий шейки матки. Паракератоз обнаруживается у женщин, прижигавших эрозии электрическим током. Патология может возникнуть при применении сомнительных «народных методов» лечения эрозии – спринцеваний, использования тампонов, пропитанных маслами и отварами. Шейка матки от такого «лечения» воспаляется, что приводит к нарушению развития клеток и их частичному ороговению.
- Гормональные сбои. Заболевание возникает при дисбалансе женских половых гормонов – прогестерона и эстрогена. Поэтому паракератоз многослойного плоского эпителия шейки матки часто сочетается с нарушением менструальной функции.
Развитию заболевания способствуют снижение иммунитета, беспорядочные незащищенные половые контакты, частые спринцевания.
Симптомы паракератоза шейки
Заболевание может очень долго себя не проявлять, обнаруживаясь случайно при осмотре шейки матки. Иногда женщины жалуются на слизистые выделения из половых путей, контактные кровотечения, возникающие после интимной близости, нарушения менструальной функции.
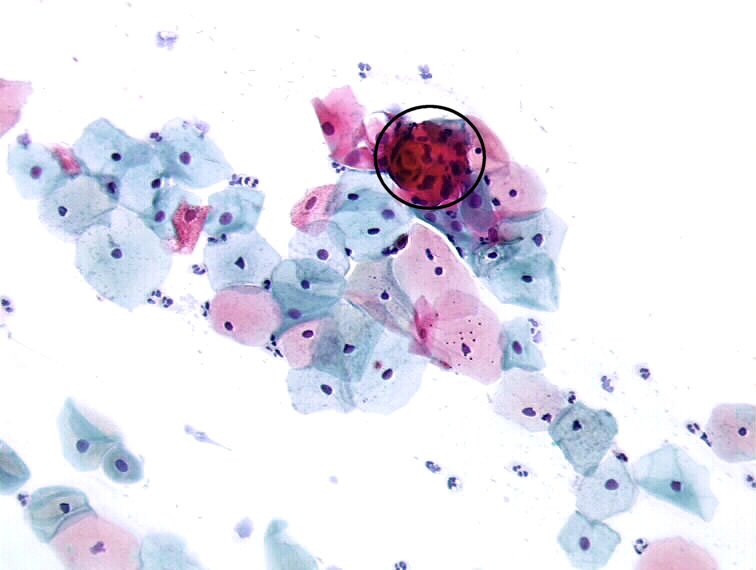
Паракератоз шейки матки
Диагностика паракератоза шейки
Патология выявляется при осмотре шейки матки на зеркалах. Признак паракератоза – наличие плотных бляшек, которые выглядят как светлые, белые и красноватые пятна на слизистой. Изменённые участки располагаются вокруг выхода из цервикального канала, соединяющего маточную полость и половые пути женщины. Иногда отдельные патологические участки наблюдаются на всей поверхности шейки.
Паракератоз может сочетаться с более тяжелыми поражениями слизистой, сопровождающимися образованием плотных ороговевших очагов – гиперкератозом и акантозом.
Заболевание протекает в нескольких формах:
- Очаговой, при которой обнаруживаются ярко выраженные очерченные очаги паракератоза. Эта форма распространяется вглубь тканей.
- Диффузной, при которой патологические очаги не имеют определенных границ.
- Поверхностной – этот тип патологии распространяется по поверхности шейки, долго не проникая внутрь. В рак перерождается редко.
Для уточнения формы патологии и размера ороговевших очагов проводится кольпоскопия. Во время процедуры поверхность шейки матки осматривают с помощью оптического прибора кольпоскопа, снабженного камерой и источником света. Изображение, получаемое с помощью оптики, передаётся на экран компьютера. Врач может детально рассмотреть исследуемую область и выбрать, как лечить паракератоз шейки матки в конкретном случае.
Выполняется расширенная кольпоскопия, позволяющая выявить все имеющиеся патологические очаги. Для этого проводятся пробы:
- Уксусная – с раствором уксуса, который растворяет слизь и делает ороговевшие участки более заметными. Очаги уплотненной слизистой окрашиваются в белый цвет. , при которой поверхность шейки смазывают йодным раствором. Йод взаимодействует с гликогеном – веществом, содержащимся в здоровых тканях шейки матки. Поэтому неизмененная слизистая окрашивается в коричневатый или желтоватый цвет. При гипер- и паракератозе клетки шейки матки полностью или частично теряют гликоген и во время проведения пробы остаются белыми или окрашиваются очень слабо.
У женщины берутся мазки:
-
– клеточный анализ на рак и предрак. В образцах биоматериала обнаруживаются клетки с разной степенью отклонения от нормы. Они не являются раковыми, но считаются признаком предраковой патологии. , выявляющие инфекционные поражения половых путей, которые часто провоцируют возникновение уплотнений слизистой.
При необходимости назначаются дополнительные исследования:
- Диагностическое выскабливание цервикального канала, которое проводится при подозрении на наличие патологических очагов внутри шейки матки.
- Биопсия шейки матки – взятие небольшого фрагмента с подозрительных участков для последующего клеточного анализа.
- Анализ на папилломавирус позволяет выявить заражение этим возбудителем. Исследование выявляет не только наличие инфекции, но и тип (штамм) вируса.
Лечение паракератоза шейки
Патологические очаги удаляют лазерным, радиоволновым или фотодинамическим (световым) методом. Такое лечение не оставляет следов на поверхности шейки и предотвращает рецидив заболевания.
При глубоких поражениях слизистой, расположении патологических очагов внутри канала шейки матки применяют конизацию. В этом случае удаляется конусообразный участок ткани, захватывающий цервикальный канал. Удаленные фрагменты исследуются в лаборатории на раковые и предраковые клетки.
Для лечения паракератоза плоского эпителия шейки матки, возникшего на фоне инфекции половых путей, назначают антибактериальные препараты внутрь и местно. Большое распространение получили вагинальные свечи, содержащие антибиотики, противогрибковые и противовоспалительные компоненты.
Профилактика
Профилактикой служат своевременное лечение половых инфекций, вакцинация от папилломавируса, защищенные половые контакты и прерывание беременности на ранних сроках без применения хирургического инструмента.
Чтобы не пропустить развитие паракератоза шейки, женщине нужно записаться на прием к врачу-гинекологу Университетской клиники. Специалист проведет осмотр, возьмет необходимые анализы и при обнаружении патологии осуществит её лечение с помощью современных методик.
Что такое дисплазия шейки матки? Причины возникновения, диагностику и методы лечения разберем в статье доктора Игнатенко Татьяны Алексеевны, гинеколога со стажем в 14 лет.
Над статьей доктора Игнатенко Татьяны Алексеевны работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
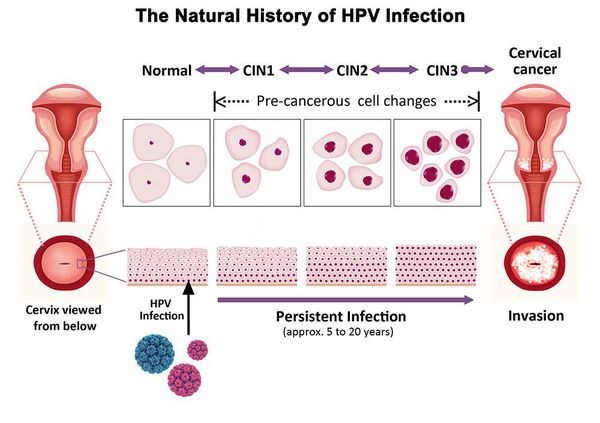
Дисплазия шейки матки, или цервикальная интраэпителиальная неоплазия (ЦИН), или Cervical Intraepithelial neoplasia (CIN) — это патологический процесс, при котором в толще клеток, покрывающих шейку матки, появляются клетки с различной степенью атипии (неправильного строения, размера, формы).
Причины дисплазии шейки матки
Папилломавирусная инфекция (ВПЧ) — основная причина дисплазии и рака шейки матки. К болезни приводит длительное персистирование именно ВПЧ высокого канцерогенного риска. У женщин с риском развития цервикальной неоплазии распространенность онкогенных типов ВПЧ чрезвычайно велика. ВПЧ становится причиной CIN 2-3 и рака шейки матки в 91,8% и 94,5% случаев соответственно. [1]
К факторам риска дисплазии шейки матки относится длительный приём контрацептивов и курение. Выявлена связь между пассивным курением среди некурящих и повышенным риском возникновения CIN 1. [3]
Другие факторы риска — раннее начало половой жизни, большое число и частая смена половых партнеров, употребление алкоголя, сопутствующие половые инфекции, много беременностей и родов. Риск цервикальной CIN 2 особенно высок у женщин, которые до этого имели опыт пересадки органов, у них выявлена ВИЧ-инфекция или они принимают иммунодепрессанты. [2]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы дисплазии шейки матки
Дисплазия шейки матки, как правило, имеет бессимптомное течение, поэтому пациентки не предъявляют никаких специфических жалоб.
Патогенез дисплазии шейки матки
Критический фактор развития цервикальной интраэпителиальной неоплазии — инфицирование вирусом папилломы человека. Во многих случаях цервикальная интраэпителиальная неоплазия легкой степени отражает временную реакцию организма на папиломавирусную инфекцию и без лечения исчезает в течение полугода-года наблюдения. При цервикальной интраэпителиальной неоплазии умеренной и тяжелой степени высока вероятность встраивания вируса папилломы человека в клеточный геном. Инфицированные клетки начинают продуцировать вирусные белки E6 и Е7, которые продлевают жизнь клетки, сохраняя ее способность к неограниченному делению. Неизбежно формирующиеся на этом фоне мутации клеток ведут к формированию предрака (дисплазии) и рака шейки матки, влагалища и вульвы.
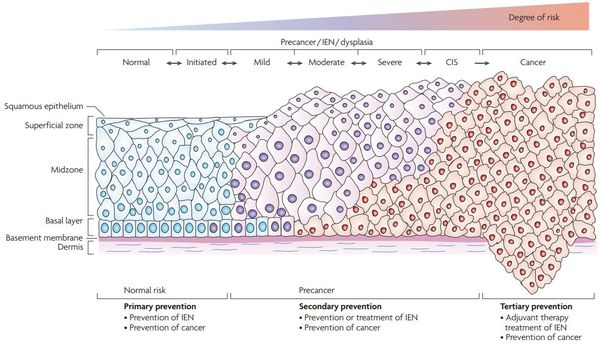
Онкогенные белки ВПЧ (Е6, Е7) взаимодействуют с регуляторными белками клеток шейки матки, приводя к повышению активности онкомаркера p16INK4A, что свидетельствует о неконтролируемом размножении клеток шейки матки. Таким образом, сверхэкспрессия p16INK4A, определяемая в материале шейки матки, который получают при биопсии, является биомаркером интеграции вируса папилломы человека высокого риска в геном и трансформации эпителиальных клеток под действием вируса, что делает эту информацию полезной при оценке прогноза развития предраковых и злокачественных поражений, связанных с инфицированием генитального тракта вирусом папилломы человека. [5]
Классификация и стадии развития дисплазии шейки матки
Для постановки цитологического диагноза (по результатам цитологического исследования соскобов шейки матки и цервикального канала с окрашиванием по Папаниколау (Рар-тест) или жидкостной цитологии) используется классификация Бетесда (The Bethesda System, 2014), основанная на термине SIL (Squamous Intraepithelial Lesion) – плоскоклеточное интраэпителиальное поражение. [10]
Выделяют три вида результатов соскобов с поверхности шейки матки (экзоцервикса):
- нормальные мазки, без изменений клеток шейки матки (NILM, Negative for intraepithelial lesion or malignancy);
- «непонятные» мазки без определенного значения, по которым нельзя определить характер поражения, однако они при этом не являются нормой (ASC-US, Atypical Squamous Cells of Undetermined Significance) или, что хуже, ASC-H, Atypical squamous cells cannot exclude HSIL, обнаружение атипичных клеток плоского эпителия, не исключающее SIL высокой степени);
- предраки низкой (LSIL, Low Grade Squamous Intraepithelial Lesion) и высокой (HSIL, High Grade Squamous Intraepithelial Lesion) степени.
Классификация Папаниколау
- 1-й класс — нормальная цитологическая картина (отрицательный результат);
- 2-й класс — изменение морфологии клеток, которое обусловлено воспалением во влагалище и (или) шейке матки;
- 3-й класс — единичные клетки с аномалией ядер и цитоплазмы (подозрение на злокачественное новообразование);
- 4-й класс — отдельные клетки с явными признаками озлокачествления;
- 5-й класс — много типично раковых клеток (злокачественное новообразование).
Существуют также гистологические классификации для оценки материала, полученного при биопсии.
По классификации R. M. Richart (1968) в зависимости от глубины поражения поверхностного клеточного слоя выделяют три степени дисплазии шейки матки:
- ЦИН 1 (дисплазия слабой степени) — признаки папилломавирусной инфекции (койлоцитоз и дискератоз). Поражение до 1/3 толщины клеточного пласта;
- ЦИН 2 (дисплазия средней степени) — поражена 1/2 толщины клеточного слоя;
- ЦИН 3 (дисплазия тяжелой степени) — поражение более 2/3 клеточного слоя. [8]
В приведенной ниже таблице даны соотношения классификаций предраковых поражений шейки матки. [9]
| Система Папаниколау | Описательная система ВОЗ | CIN | Терминологи- ческая система Бетесда (ТСБ) |
|---|---|---|---|
| Класс 1 (норма) | Отсутствие злокачественных клеток | Отсутствие неопластических изменений | Норма |
| Класс 2 (метаплазия эпителия, воспалительный тип) | Атипия, связанная с воспалением | Реактивные изменения клеток ASC: ASC - US, ASC - H | |
| Класс 3 ("дискариоз") | Слабая дисплазия | CIN 1 койлоцитоз | LSIL |
| Умеренная дисплазия | CIN 2 | HSIL | |
| Тяжелая дисплазия | CIN 3 | ||
| Класс 4 (клетки, подозрительные на рак или карцинома in situ | Карцинома in situ | ||
| Класс 5 (рак) | Инвазивная карцинома | Карцинома | Карцинома |
Осложнения дисплазии шейки матки
Последствия дисплазии шейки матки
Основное и самое опасное осложнение цервикальной интраэпителиальной неоплазии заключается в развитии рака шейки матки, любой случай развития которого — результат упущенных возможностей диагностики и лечения дисплазии шейки матки. [7]
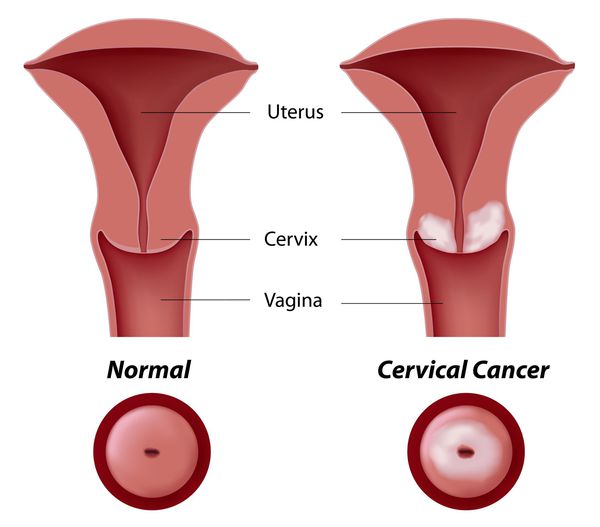
Проводились длительные, систематические исследования риска рака шейки матки у женщин с диагнозом цервикальной интраэпителиальной неоплазии 3 степени (CIN3) по сравнению с женщинами, у которых были нормальные цитологические результаты. Согласно полученным данным, долгосрочный относительный риск развития рака шейки матки зависит от различных гистологических типов CIN3 и выше всего он для аденокарциномы in situ. Даже через 25 и более лет после конизации (хирургического иссечения патологических тканей шейки матки) риск злокачественного перерождения клеток был значительным. [4]
Диагностика дисплазии шейки матки
Для ранней диагностики предраковых поражений шейки матки во многих странах мира существует система цервикального скрининга.
Методы диагностики дисплазии шейки матки
В России система цервикального скрининга включает последовательность действий:
- Цитологическое исследование: РАР-тест;
- ВПЧ-тестирование: в США и странах Евросоюза ВПЧ-тест применяется для первичного скрининга рака шейки матки (РШМ). В России его использование вариативно: при первичном скрининге в сочетании с РАР-тестом, в качестве самостоятельного теста, при ведении пациенток с неясными результатами РАР-теста (ASCUS) и для наблюдения паценток после лечения HSIL;
- Кольпоскопия: показаниями к исследованию являются положительные результаты РАР-теста (класс 2-5). Метод основан на осмотре шейки матки при помощи увеличивающих оптических систем и проведения диагностических проб с растворами уксусной кислоты и йода (Люголя). С помощью кольпоскопии определяют локализацию поражения, его размер, выбирают участок для проведения биопсии, определяют тактику лечения.
При кольпоскопии должна быть тщательно оценена зона трансформации (переходная зона стыка двух видов покровного эпителия шейки матки).
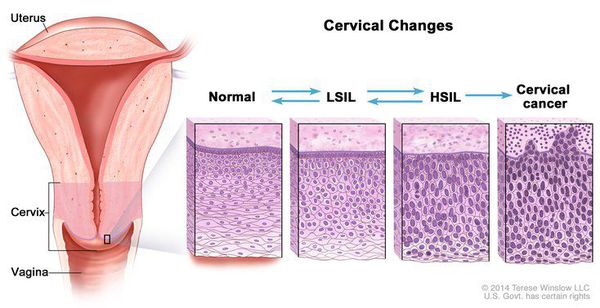
Влагалищная часть шейки матки (экзоцервикс) покрыта многослойным плоским эпителием. В канале шейки матки (цервикальном канале, эндоцервиксе) — цилиндрический эпителий. Место перехода цилиндрического эпителия цервикального канала в многослойный плоский эпителий поверхности шейки матки носит название зоны трансформации. Эта область имеет большое клиническое значение, поскольку именно в ней возникает более 80% случаев дисплазии и рака шейки матки.
- Зона трансформации 1 типа — переходная зона видна полностью. Это самый оптимальный и прогностически «благоприятный» вариант кольпоскопического заключения.
- Зона трансформации 2 типа — переходная зона частично скрыта в канале шейки матки. Адекватно оценить такую картину сложно, так как наиболее измененные участки могут быть не видны и пропущены.
- Зона трансформации 3 типа — переходная зона находится глубоко в канале шейки матки и оценить её кольпоскопически невозможно. Кольпоскопия в этом случае считается неинформативной, поскольку глубина залегания патологического очага остается неизвестной.
- Биопсия: прицельная или расширенная биопсия (конизация) всегда должна выполняться под контролем кольпоскопии. Выбор метода биопсии зависит от типа поражения, возраста пациентки и зоны трансформации. Важной информацией, которую дает биопсия, является возможность иммуногистохимического определения маркера ранней диагностики дисплазии с высокой степенью риска озлокачествления: p16INK4a.
Лечение дисплазии шейки матки
Динамическому наблюдению подлежат молодые пациентки (до 35 лет) с LSIL (ВПЧ, ЦИН 1, ЦИН 2, если при биопсии не обнаружен белок р16, являющийся признаком проникновения ВПЧ высокого риска в геном и трансформации опухолевых клеток под действием вируса). Наблюдать возможно пациенток только с 1 и 2 кольпоскопическим типом зоны трансформации.
Контрольные осмотры, цитологическое и ВПЧ-тестирование показаны через 6 и 12 месяцев после первичного обнаружения патологии.
Хирургическое лечение дисплазии
При выявлении HSIL (ЦИН 2 c обнаружением белка р16 при биопсии, ЦИН 3) неизбежно хирургическое лечение в виде абляции («прижигания») или эксцизии (удаления) поврежденной ткани. Для абляции используют электро-/радио-, крио- и лазерные воздействия. Эксцизия возможна электро-/радиоволновая или ножевая.
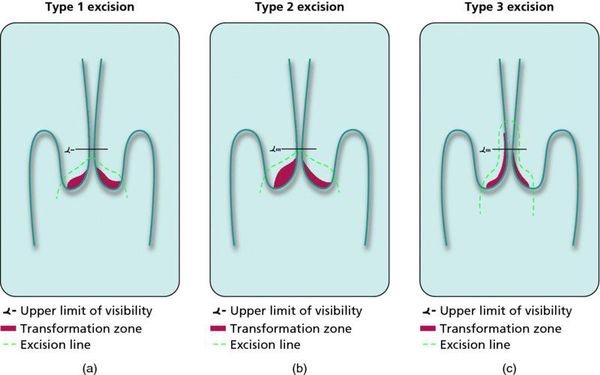
Немаловажно, что при выявлении по кольпоскопии 3 типа зоны трансформации на фоне положительного РАР-теста гинеколог обязан провести выскабливание слизистой канала шейки матки и/или широкую эксцизионную биопсию (конизацию шейки матки) для исключения опухолевого процесса, потенциально располагающегося вне зоны кольпоскопического обзора. Немаловажно наблюдение после операции через 6 и 12 месяцев с выполнением цитологического соскоба и ВПЧ-теста.
Следует отметить, что процедура хирургического иссечения патологических тканей на шейке матки увеличивает риск преждевременных родов. А сама по себе цервикальная интраэпителиальная неоплазия первой степени на течении беременности и родов никак не отражается и зачастую опасности не представляет. [12]
Средний возраст женщин, когда может потребоваться хирургическая коррекция цервикальной внутриэпителиальной неоплазии — около 30 лет. Хирургическое лечение нередко ассоциировано с неблагоприятным течением последующей беременности. Частота и тяжесть неблагоприятных осложнений возрастают с увеличением глубины иссекаемых тканей. [13]
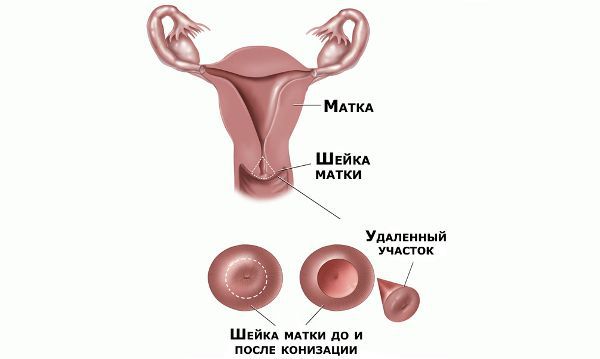
Реабилитация после хирургического лечения
В течение месяца после операции следует воздержаться от спринцеваний, половых контактов и не пользоваться тампонами. На 2–3 недели исключают тяжёлые физические нагрузки и тепловые процедуры. Незначительные сукровичные выделения, усиливающиеся иногда до менструальноподобных, в течение 10–20 дней после операции — это нормальное явление.
При реабилитации после хирургического лечения шейки матки эффективны препараты, содержащие антисептик и стимулятор регенерации эпителия.
После лечения возможен рецидив, поэтому необходимо пожизненное наблюдение: цитологический мазок через 6 и 12 месяцев после операции, затем раз в год в течение 10 лет, далее раз в 3 года.
Планировать беременность после операции на шейке матки можно не ранее, чем через 3–6 месяцев. Эти сроки будут зависеть от глубины эксцизии или конизации и длины шейки матки [9] .
Лечение дисплазии при беременности
В большинстве случаев лечение должно быть отложено на послеродовый период. При беременности на фоне дисплазии шейки матки каждые три месяца проводится кольпоскопический и цитологический контроль. При выявлении рака шейки матки пациентку консультирует онкогинеколог. Доктор подбирает тактику лечения, может потребоваться прервать беременность по онкологическим показаниям [9] .
Прогноз. Профилактика
Дополнительными факторами риска прогрессирования ПВИ с формированием предраковой патологии являются:
- курение;
- длительное использование гормональных контрацептивов;
- многократные травматичные роды;
- ВИЧ-инфекция.
- У пациенток с ЦИН часто обнаруживают вирус простого герпеса 2 типа, цитомегаловирусную инфекцию, хламидийную урогенитальную инфекцию, бактериальный вагиноз, ассоциированный с резким снижением или отсутствием вагинальной лактофлоры, повышенным ростом во влагалище Gardnerella vaginalis и Atopobium vaginae, повышение концентрации в бакпосеве грибов рода Candida, Mycoplasma hominis.
Устранение и профилактика данных факторов способны снизить вероятность развития предраковой патологии шейки матки.
Рак шейки матки поражает преимущественно женщин репродуктивного возраста. Скрининг является важной стратегией вторичной профилактики. Длительный процесс канцерогенной трансформации от появления в организме вируса папилломы человека (ВПЧ) до инвазивного рака дает широкие возможности для выявления заболевания на стадии, когда лечение высокоэффективно. Подходящими скрининговыми тестами в мире признаны цитологическое исследование, визуальный осмотр после применения уксусной кислоты и тесты на выявление ВПЧ. Всемирная организация здравоохранения рекомендует проводить скрининг женщин по крайней мере один раз в жизни в возрасте от 30 до 49 лет. [14]
Согласно приказу Министерства здравоохранения РФ от 03.02.2015. N36ан "Об утверждении порядка проведения диспансеризации определенных групп взрослого населения", осмотр со взятием мазка (соскоба) с поверхности шейки матки и цервикального канала на цитологическое исследование производится 1 раза в 3 года для женщин в возрасте от 21 года до 69 лет включительно.
Что такое эктопия шейки матки? Причины возникновения, диагностику и методы лечения разберем в статье доктора Пенкиной Анны Евгеньевны, гинеколога со стажем в 26 лет.
Над статьей доктора Пенкиной Анны Евгеньевны работали литературный редактор Юлия Липовская , научный редактор Сергей Федосов
Определение болезни. Причины заболевания
Эктопия шейки матки — состояние шейки матки, которое характеризуется смещением кнаружи границы между цилиндрическим и многослойным плоским эпителием.
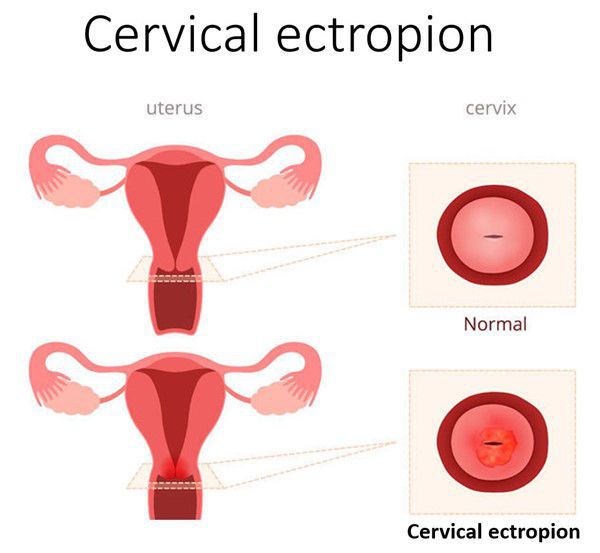
В норме цилиндрический эпителий выстилает канал шейки матки изнутри, а многослойный плоский должен покрывать видимую часть шейки матки. При эктопии цилиндрический эпителий в той или иной степени выходит на поверхность влагалищной части шейки матки. Такое расположение для него нетипично. Цилиндрический эпителий плохо приспособлен к кислой вагинальной среде, что вызывает ряд проблем. Данное состояние иногда называют ложной, железистой или псевдоэрозией, а также эндоцервикозом или железисто-мышечной гиперплазией [3] [9] [13] .
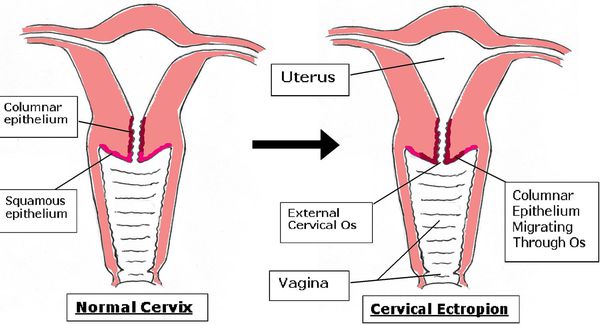
У молодых нерожавших девушек до 25 лет эта патология встречается более чем в 50 % случаев [8] . Женщины старше 40 с ней практически не сталкиваются. Сейчас считается, что неосложнённая эктопия у девочек-подростков, женщин раннего репродуктивного возраста, а также у беременных является вариантом физиологической нормы.
В иных случаях приобретённую эктопию расценивают как фоновое заболевание половой сферы, имеющее мультифакторную природу и потенциально способное при определённых предрасполагающих условиях спровоцировать развитие злокачественноного новообразования (рака шейки матки) [6] .
Факторы, способствующие развитию эктопии.
- наследственная предрасположенность;
- раннее начало менструаций (в возрасте моложе 12 лет);
- сбои менструального цикла;
- неправильное половое развитие;
- хронические болезни, в том числе воспалительные заболевания репродуктивной сферы;
- эндокринная патология [17] ;
- нарушения функции иммунной системы.
- инфекции, передающиеся половым путём, особенно вирус папилломы человека, а также хламидийная, микоплазменная, герпесвирусная инфекции и др. [2][12] ;
- травматизация шейки матки (аборты, осложнённые роды, частое и длительное применение химических методов контрацепции);
- нерациональное использование гормональных противозачаточных средств;
- профессиональные вредности, неблагоприятные экологические факторы, вредные привычки.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы эктопии шейки матки
Неосложнённая эктопия не даёт каких-либо субъективных симптомов и обычно обнаруживается гинекологом в ходе профилактического осмотра в зеркалах. Выглядит она как бледно-розовое или ярко-красное пятно неправильной формы с зернистой поверхностью, располагающееся вокруг наружного зева шейки матки [3] .
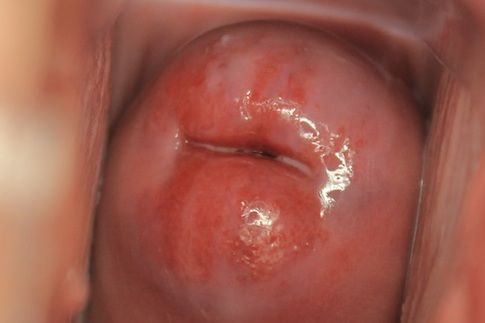
Характерным симптомом при кольпоскопическом осмотре также является особая реакция участка эктопии на пробы с уксусной кислотой и раствором Люголя (5 % водный раствор йода). Эктопированный участок бледнеет и раствором Люголя не окрашивается.
Осложнённые формы [10] нередко сочетаются с воспалительными проявлениями в половых путях и могут сопровождаться обильными белями, ощущением зуда в области вульвы, болезненностью при половых актах, иногда — кровянистыми выделениями после полового акта [15] .
Зачастую эктопию обнаруживают при обращении пациентки к гинекологу по поводу нарушений менструального цикла и/или проблем с зачатием. Однако до сих пор не удалось выяснить, является ли эктопия причиной данных нарушений либо имеет с ними общие предпосылки.
Патогенез эктопии шейки матки
Патогенез эктопии шейки матки продолжает изучаться. Выдвигается целый ряд теорий развития данного состояния [15] .
Врождённая эктопия формируется во внутриутробном периоде, когда смещение границ эпителия считается нормальным этапом развития. Это физиологическое состояние, не требующее лечения и не представляющее опасности в плане озлокачествления. Причины сохранения смещения в подростковом и молодом возрасте до конца не выяснены [3] .
Место стыка двух видов эпителия, в которой происходят изменения, называется зоной трансформации. Она особенно уязвима в плане развития злокачественных новообразований. Около 90 % случаев рака шейки матки развивается именно здесь.
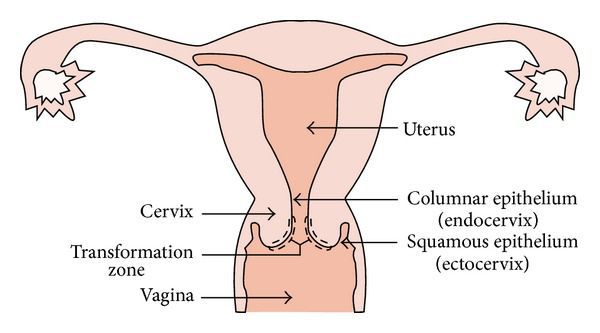
Атипично расположенный цилиндрический эпителий более подвержен внешним влияниям, хуже защищён от инфекций. Интенсивное деление клеток зоны трансформации повышает вероятность возникновения нежелательных мутаций, которые в итоге могут стать причиной развития опухолей [6] .
Воспалительная теория развития приобретённой эктопии подтверждается тем, что это состояние довольно часто сочетается с хроническими воспалительными процессами в органах репродуктивной сферы, инфекциями, передающимися половым путём. Согласно воспалительной теории, участок эктопии представляет собой своеобразный резервуар патологической микрофлоры, поддерживающей хроническое воспаление.
Иммунологическая теория связывает формирование эктопии с нарушениями местного гуморального и клеточного иммунитета, в частности, с понижением активности Т-лимфоцитов и повышением синтеза отдельных классов иммуноглобулинов. Шейка матки обеспечивает иммунный барьер на пути внешних неблагоприятных факторов. С этой целью вырабатывается особый слизистый секрет, имеющий сложный состав, который может нарушаться вследствие воздействия тех же гормональных колебаний и других факторов. Выраженность эктопии, как правило, положительно взаимосвязана с выраженностью иммунологических нарушений.
Согласно дисгормональной теории [17] появление цилиндрического эпителия за пределами наружного зева спровоцировано нарушением баланса между эстрогенами и прогестероном, к которым особенно чувствительны клетки зоны трансформации. У женщин с проблемами менструального цикла эктопия диагностируется в несколько раз чаще.
Травматическая теория отводит решающую роль в развитии цервикальной эктопии различным повреждениям шейки матки: разрывы при осложнённых родах, аборты, гинекологические операции и другие вмешательства могут нарушать кровоснабжение и иннервацию (связь с центральной нервной системой), что, в свою очередь, ведёт к изменениям.
В целом единая теория до сих пор не сформулирована. Вероятнее всего, истинный механизм развития эктопии представляет собой сочетание компонентов разных теорий.
Классификация и стадии развития эктопии шейки матки
Существует Международная классификация болезней (МКБ-10), Международная гистологическая классификация опухолей, Международная классификация кольпоскопических терминов, в которых представлены основные виды поражений шейки матки. Эти классификации используются исключительно специалистами — врачами-гинекологами — они малопонятны для людей без медицинского образования. А для общего представления можно представить следующую классификацию.
По времени возникновения выделяют врождённую и приобретённую эктопию [13] .
- Врождённая эктопия обнаруживается у женщины, которая недавно начала половую жизнь, при первом визите к гинекологу.
- Приобретённая эктопия диагностируется на ранее неизменённой шейке матки в том случае, если предыдущие гинекологические осмотры не обнаруживали признаков эктопии.
По признаку наличия осложнений различают осложнённые [10] и неосложнённые клинические формы.
По характеру течения эктопия шейки матки может быть ранней рецидивирующей, если после проведённого лечения она вновь обнаруживается через 2-3 месяца, и поздней рецидивирующей, если до рецидива прошло 6 месяцев или более.
По морфологическим признакам эктопия шейки матки подразделяется на следующие варианты и их сочетания:
- поверхностная;
- железистая (фолликулярная) — характеризуется воспалительными признаками, скоплением желёз, разветвленными железистыми ходами;
- папиллярная (гистологически выявляются сосочковые структуры);
- кистозная;
- эпидермизирующаяся.
По течению цервикальная эктопия может быть прогрессирующей (пролиферирующей), стационарной (простой) и заживающей (находящейся в фазе обратного развития).
Осложнения эктопии шейки матки
К числу патологий, осложняющих течение цервикальной эктопии [10] , относят:
- различные проявления воспаления: вагинит (кольпит), эндоцервицит, эндометрит;
- образование истинной эрозии;
- эктропион — выворот шейки матки; — уплотнение и ороговение многослойного плоского эпителия (предраковое заболевание);
- прогрессирующая дисплазия различной степени тяжести;
- плоскоклеточный рак [6] .
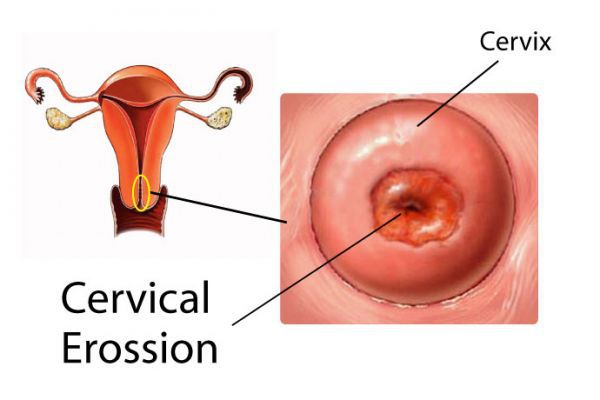
Согласно отдельным исследованиям, эктопия может способствовать различным осложнениям в ходе беременности, вплоть до спонтанных абортов, а также повышать риск травматизации половых путей при родах. Есть данные о том, что эктопия может быть повинна в 2,7 % случаев репродуктивных потерь (невынашивания, замерших беременностей и др.) [18] . Например, осложняющий эктопию эндоцервицит способен спровоцировать восходящее инфицирование плодного яйца и преждевременный разрыв его оболочек.
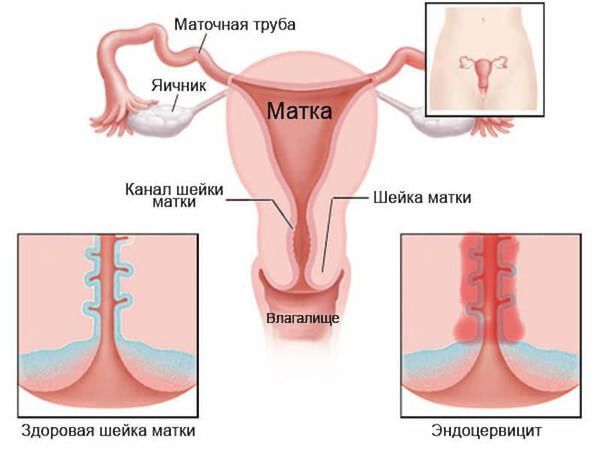
Инфекционно-воспалительные явления в половых путях могут не только ухудшать течение беременности, осложнять родовой процесс, но и затягивать восстановление женщины в послеродовом периоде, иногда приводя к серьёзным проблемам, например:
- несостоятельность швов;
- лохиометра — задержка отделяемого секрета (лохий) в полости матки;
- субинволюция матки — замедленное восстановление дородовых размеров матки;
- эндометрит — воспалительное заболевание внутреннего слоя матки.
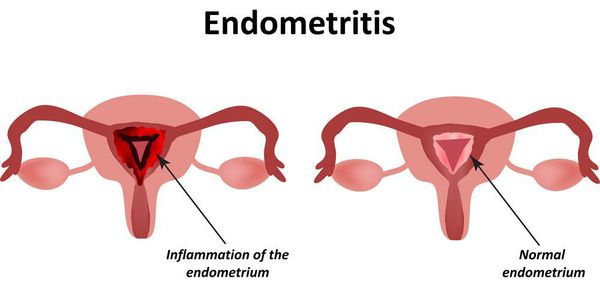
Пациентке, страдающей эктопией, трудно самостоятельно заподозрить у себя развивающиеся осложнения, например, злокачественный процесс. Ведь до некоторых пор они не дают явных симптомов. Именно поэтому так важно своевременно проходить профилактические гинекологические обследования. Тем не менее, когда в качестве осложнений выступают воспалительные процессы, женщину могут беспокоить:
- зуд и жжение в области вульвы;
- тянущие боли и дискомфорт внизу живота;
- общее недомогание, повышение температуры тела;
- обильные белые выделения, иногда с неприятным запахом;
- болезненность при половых контактах и появление после них кровянистых выделений.
Диагностика эктопии шейки матки
Для полноценной диагностики необходимо пройти комплексное обследование. Оно включает следующие методы:
- анализ жалоб, анамнеза жизни, наследственных особенностей, сексуальной активности, применяемых методов контрацепции, выявление отклонений менструальной функции, уточнение акушерско-гинекологического анамнеза;
- гинекологический осмотр в зеркалах (эктопия имеет характерные визуальные признаки, которые затем уточняются в ходе кольпоскопии);
- онкоцитологическое исследование соскоба с влагалищной части шейки матки и из цервикального канала (метод Папаниколау) [16][20] ;
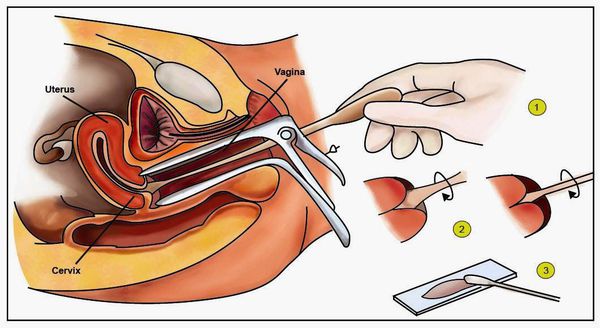
- расширенная кольпоскопия (пробы с уксусной кислотой и раствором Люголя), видеокольпоскопия [19] ;
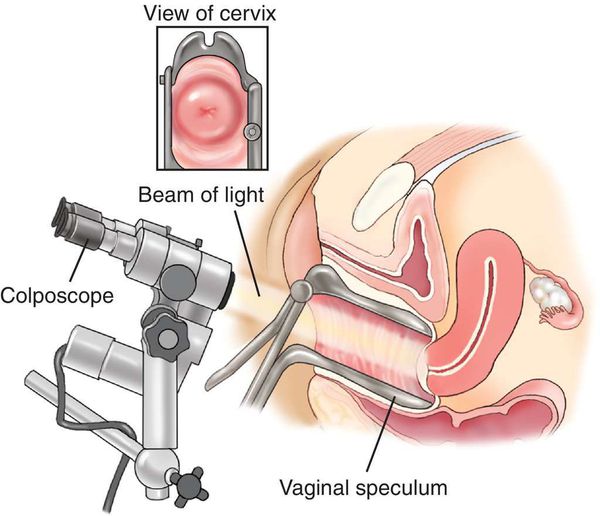
- гистологическое исследование материала, полученного в результате прицельной биопсии под кольпоскопическим контролем [16] ;
- исследования на предмет наличия инфекций, передаваемых половым путём (бактериоскопическое, бактериологическое, ПЦР) [2][12] ;
- при обнаружении папилломавирусной инфекции (штаммы высокого онкогенного риска) необходимо определить степень вирусной нагрузки;
- изучение гормонального профиля;
- определение иммунного статуса (иммунограмма).
Диагностикой обычно занимается гинеколог. При гормональных нарушениях может потребоваться консультация гинеколога-эндокринолога, при высокой степени дисплазии, подозрении на злокачественный процесс — онкогинеколога.
Лечение эктопии шейки матки
Неосложнённая цервикальная эктопия не требует лечения. Однако такая пациентка находится в группе риска, поэтому ей показано диспансерное наблюдение: ежегодное прохождение плановых профилактических осмотров с кольпоцитологическим и бактериоскопическим исследованием.
Случаи цервикальной эктопии, осложнённые дисплазией высокой степени, должны лечиться онкогинекологом.
В остальных случаях выделяют следующие основные цели лечения [10] [13] :
- купирование воспалительного процесса;
- коррекция гормональных отклонений;
- иммунокоррекция;
- нормализация вагинальной микрофлоры [14] ;
- деструкция изменённых участков тканей;
- стимуляция восстановления многослойного плоского эпителия;
- предупреждение рецидивов.
Медикаментозная терапия включает следующие группы лекарственных средств:
- противовоспалительные препараты;
- средства для антимикробной и противовирусной терапии [12] ;
- препараты, способствующие нормализации микробиоценоза влагалища [14] ;
- иммуномодуляторы;
- средства для коррекции выявленных гормональных нарушений.
Немедикаментозное лечение
Довольно широко применяются деструктивные методы лечения, являющиеся менее травматичными, нежели полномасштабное хирургическое вмешательство. К ним относятся:
- электрокоагуляция;
- химическая, фармакологическая коагуляция;
- криодеструкция;
- лазерная коагуляция [4][5] ;
- радиоволновая хирургия [1][11] .
Наиболее прогрессивными из деструктивных методов являются лазерная коагуляция и радиоволновая хирургия. Обе методики малотравматичны, отличаются быстрым заживлением, не приводят к обильным кровотечениям, имеют крайне низкий риск других осложнений. Лечебные манипуляции выполняются амбулаторно, практически не влияют на трудоспособность пациентки, имеют минимальные ограничения в периоде реабилитации.
Метод лазерной коагуляции основан на применении высокоэнергетического лазерного луча, под действием которого происходит мгновенное выпаривание тканей на заданную глубину. Наиболее приемлемым и эффективным аппаратом для устранения патологии шейки матки является СО2-лазер [4] [5] . Метод показан для применения у молодых нерожавших пациенток [7] , так как не затрагивает менструальную и репродуктивную функцию.
Радиоволновая хирургия (аппарат "Сургитрон") также используется для коагуляции (прижигания) патологических тканей [1] [11] . Метод основан на воздействии высокочастотного электромагнитного поля. Его преимущество заключается в том, что он позволяет при необходимости получить неповреждённый фрагмент патологической ткани с целью исключения онкопатологии.
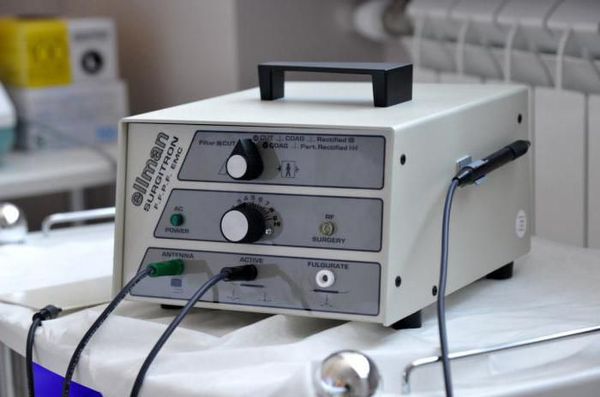
Хирургическое лечение
К хирургическому вмешательству (реконструктивно-пластическим операциям) прибегают в случаях сочетания цервикальной эктопии с высокой степенью дисплазии, а также при выраженных деформациях шейки матки.
Поскольку цервикальная эктопия представляет собой проблему преимущественно молодых женщин [7] , важно, чтобы лечение было не только эффективным, но и максимально бережным, чтобы обеспечить анатомо-функциональную полноценность шейки матки и сохранить репродуктивную функцию. Выбор тактики лечения зависит от возраста пациентки, выраженности и стадии процесса, имеющихся осложнений, особенностей микрофлоры, гормонального и иммунного статуса, сопутствующей патологии и многого другого.
Как правило, обнадёживающие результаты даёт комплексное лечение с применением разных методов. Так, например, при сочетании цервикальной эктопии и папилломавирусной инфекции с высокой вирусной нагрузкой лазерную вапоризацию (выпаривание патологического эпителия) предваряют противовирусной терапией, иммунокоррекцией.
Прогноз. Профилактика
В подавляющем большинстве случаев эктопии шейки матки прогноз для жизни и здоровья остаётся благоприятным.
Специфических мер профилактики данного вида патологии пока не разработано. В целом для понижения вероятности развития цервикальной эктопиии и её осложнений следует придерживаться следующих рекомендаций [15] :
- регулярно проходить профилактическое гинекологическое обследование с целью своевременного выявления воспалительных заболеваний половой сферы, а также их эффективного лечения;
- в случае выявления гормонального дисбаланса проводить его полноценную коррекцию под руководством специалиста;
- осуществлять подбор методов контрацепции исключительно в содружестве с врачом, не злоупотреблять химическими методами контрацепции;
- не заниматься самолечением, не злоупотреблять антибиотиками, спринцеваниями, оберегать нормальную вагинальную микрофлору [14] ;
- практиковать ответственное сексуальное поведение (предохраняться не только от нежелательной беременности, но и от инфекций, передающихся половым путём [12] , не допускать случайных половых контактов);
- своевременно вакцинироваться против высокоонкогенных штаммов папилломавирусной инфекции;
- избегать абортов;
- укреплять иммунную систему;
- вести здоровый образ жизни (отказаться от вредных привычек, питаться рационально, закаляться).
В плане вторичной профилактики у пациенток с папилломавирусной инфекцией после успешно проведённого лечения цервикальной эктопии рекомендуется регулярное наблюдение (не менее четырёх раз в течение первого года) с обязательным определением вирусной нагрузки и экспрессии онкопротеина Е7.
Опухоли пищевода. Доброкачественные и злокачественные опухоли пищевода.
В дистальном отделе пищевода изредка наблюдают аденому, имеющую такое же строение, что и аденомы желудка. Она может развиваться из слизистой оболочки при так называемом пищеводе Баррета, когда в результате хронического рефлюкс-эзофагита и гегеротопяи (что менее вероятно) многослойный плоский эпителий нижней части пищевода замещается цилиндрическим эпителием с формированием структур, соответствующих слизистой оболочке фундального или кардиального отделов желудка, нередко с явлениями кишечной метаплазии.
Рак — наиболее часто встречающаяся злокачественная опухоль пищевода. Чаще наблюдают у мужчин? возраст большинства которых 50—70 лет. К предрасполагающим факторам относятся особенности питания — употребление очень горячей и грубой пищи; недостаток витаминов, особенно В2, А; железа, меди, цинка; вредные привычки (курение, алкоголь и др.); некоторые географические особенности местности; аномалии и посттравматические рубцовые изменения пищевода, грыжа пищеводного отверстия диафрагмы, тилоз (гиперкератоз ладоней и подошв), синдром Пламмера—Винсона (железодефицитная анемия, гипохлоргидрия, дисфагия), наблюдающийся преимущественно у жительниц стран Скандинавского полуострова в возрасте 40 -45 лет и др.
Заболеваемость раком пищевода колеблется в очень широких пределах, достигая наиболее высоких показателей в некоторых районах Ирана, Китая, Туркменской, Казахской, Узбекской ССР и др. Эпидемиологические исследования показали, что в этих районах среди населения чрезвычайно широко распространен хронический эзофагит (60—80% населения и более), который, очевидно, имеет значение в развитии рака пищевода. При гистологическом исследовании на фоне хронического эзофагита обнаруживают очаговые и диффузные атрофические и гиперпластические изменения многослойного плоского эпителия, пролиферацию базальных клеток, очаги дисплазии, внутриэпителиальный и ранний инвазивный рак.
Такие же изменения часто можно обнаружить при раке пищевода, исследуя слизистую оболочку на различном расстоянии от опухоли. Эти изменения, по-видимому, являются основными этапами морфогенеза рака пищевода, что подтверждается динамическими наблюдениями, проведенными в районах Китая с повышенной заболеваемостью раком пищевода.
Предраковые изменения в многослойном плоском эпителии пищевода принципиально не отличаются от аналогичных изменений в шейке матки. Гистологическими критериями дисплазии являются усиление пролиферации и нарушение дифференцировки клеток. Количество базальных клеток, которые в норме занимают не более 15% толщины эпителиального пласта, при дисплазии увеличивается, клетки становятся более крупными, полиморфными, увеличивается число митозов. В зависимости от выраженности клеточных изменений и степени их распространения в эпителиальном пласте различают слабую» умеренную и тяжелую дисплазию. Выраженные полиморфизм и атипия клеток, большое количество митозов, утрата полярности расположения клеток и деления на слои при сохранении базальной мембраны характерны для внутриэпителиального рака.
В тех случаях, когда базальная мембрана не прослеживается, имеется тенденция к погружному росту и отшнуровка эпителиальных комплексов, изменения должны расцениваться как начало инвазивного рака.
При гистологическом исследовании, особенно по материалу эндоскопической биопсии, бывает трудно дифференцировать диспластические (предраковые) изменения и реактивную гиперплазию базальных клеток, которая может наблюдаться, например, при рефлюкс-эзофагите.
Трудности возникают также при дифференциальной диагностике тяжелой дисплазии, карциномы in situ и инвазивного рака. Для уточнения характера процесса необходимы динамическое наблюдение за такими больными и повторные биопсии.
Основная масса форм плоскоклеточного рака пищевода, видимо, развивается из покровного эпителия. Другим источником развития рака пищевода могут быть слизистые железы, в которых при хроническом гастрите также наблюдают атрофические и гиперпластические изменения, образование кист, пролиферацию резервных клеток, плоскоклеточную метаплазию и дисплазию эпителия. Из них могут возникать плоскоклеточный рак, аденокарцинома, железисто-плоскоклеточный рак, а также мукоэлидермоидная опухоль и аденокистозный рак (цилиндрома), аналогичные соответствующим опухолям слюнных желез. Аденокарциномы в пищеводе могут развиваться также от остатков цилиндрического эпителия, выстилающего пищевод на ранних стадиях эмбриогенеза, участков гетеротопии слизистой оболочки желудка.
Аденокарциномы дистальной части пищевода могут развиваться также на фоне так называемого пищевода Баррета. Во многих случаях труден или невозможен дифференциальный диагноз такой аденокарциномы и рака кардиального отдела желудка, прорастающего в пищевод.
Рак пищевода наиболее часто локализуется в средней его трети, затем следует нижняя треть пищевода; верхняя его треть поражается редко. Исключение составляет рак пищевода при синдроме Пламмера—Винсона, который наблюдается преимущественно у женщин 40—45 лет и поражает самый верхний отрезок пищевода.
Макроскопически большинство форм рака пищевода представляет собой изъязвленные блюдцеобразные или эндофитные опухоли, часто циркулярно охватывающие стенку, нередко на значительном протяжении. Экзофитные опухоли встречаются редко. Рак пищевода может распространяться по подслизистому слою далеко за пределы видимого очага опухоли, а также прорастать в прилежащие к пищеводу ткани и органы. Для суждения о степени распространенности процесса и радикальности оперативного вмешательства при исследовании удаленного отрезка пищевода необходимо изучение линий операционных разрезов и глубины прорастания стенки пищевода.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

