Облепиховое масло при фурункулезе
Обновлено: 24.04.2024
Маслянистая жидкость оранжево-красного цвета с характерным запахом. Допускается образование незначительного осадка растворимого при нагревании до 40 °С.
Состав
1 флакон содержит
Действующее вещество: облепихового масла - 45 мл (содержание суммы каротиноидов, в пересчете на β-каротин, не менее 0.2%);
Вспомогательное вещество: масла подсолнечного до 50 мл.
Фармакотерапевтическая группа
Прочие терапевтические продукты. Код ATX V03AX.
Показания к применению
В комплексной терапии в качестве ранозаживляющего средства при поражении кожи и слизистых оболочек.
- атрофический кольпит, постлучевой кольпит;
- наружный геморрой, трещины заднего прохода, эрозивно-язвенные поражения прямой кишки, лучевое поражение слизистой оболочки нижних отделов прямой кишки.
- лучевые поражения кожи, ожоги;
- для стимуляции репаративных процессов послеоперационных ран в хирургии.
- язвенная болезнь желудка, двенадцатиперстной кишки.
Данные контролируемых клинических исследований в поддержку заявленных показаний отсутствуют.
Использование основано на многолетнем практическом опыте.
Способ применения и дозировка
В комплексной терапии в качестве ранозаживляющего средства при поражении кожи и слизистых оболочек.
Местно: при гинекологических заболеваниях - атрофическом кольпите, постлучевом кольпите - ватными тампонами, смоченными маслом, смазывают стенки влагалища, влагалищную часть и канал шейки матки (после их предварительной обработки). Курс лечения составляет 10-15 процедур. В случае необходимости курс лечения повторить через 4-6 недель. При проктологических заболеваниях - наружном геморрое, трещинах заднего прохода ватными тампонами, просоленными препаратом, смазывают анус и геморроидальные узлы; при проктологических процессах прямой кишки масло вводят в ее просвет с помощью микроклизмы (предварительно сделав очистительную клизму). Курс лечения - 10-12 процедур. В случае необходимости куре лечения можно повторить через 4-6 недель.
Наружно: при патологических процессах кожи препарат используют наружно, через день, в виде масляных повязок после очищения пораженной поверхности кожи от некротических тканей до появления участков тканевой регенерации.
Внутрь: при язвенной болезни желудка и двенадцатиперстной кишки препарат принимают внутрь, по 1 чайной ложке, 2-3 раза в день. Курс лечения указанных заболеваний составляет 3-4 недели. При необходимости курс лечения можно повторить через 4-6 недель.
Побочное действие
Возможна индивидуальная повышенная чувствительность к препарату, со стороны желудочно-кишечного тракта возможны горечь во рту (при приеме внутрь), диарея, со стороны иммунной системы возможны аллергические реакции, зуд, гиперемия, отек кожи, кожные высыпания, ощущения жжения (при наружном применении); при ингаляционном способе применения возможны нарушения дыхания вследствие спазма бронхов, чрезмерное выделение слюны.
Противопоказания
Повышенная чувствительность к препарату; при применении внутрь: холецистит, холангит, панкреатит, холелитиаз, гепатит, детский возраст до 12 лет (в связи с ограниченностью данных); при ректальном введении - диарея: при наружном и местном применении - профузное кровотечение, обильное гнойное отделяемое из раны.
Передозировка
При передозировке возможно появление тошноты, рвоты, головной боли, спутанности сознания, судорог, диареи, кожных высыпаний, десквамации эпителия. Может развиваться олигурия. В отдельных случаях возникают шоковые состояния. В таком случае необходимо промывание желудка, назначение активированного угля и других видов адсорбентов и соответствующая симптоматическая терапия.
Меры предосторожности
Препарат следует с осторожностью применять больным, склонным к аллергическим реакциям. Перед применением взболтать.
Применение у пациентов с нарушением функции печени и почек. Данные касающиеся особенностей дозирования у пациентов с нарушением функции печени и почек отсутствуют.
Применение у пациентов пожилого возраста. Данные касающиеся особенностей дозирования у пожилых пациентов отсутствуют.
Дети. Детям препарат применять после оценки врачом соотношения польза/риск.
Применение в период беременности или кормления грудью
В период беременности и кормлении грудью препарат применяется по назначению врача только тогда, когда ожидаемая польза для матери превышает потенциальный риск для плода или ребенка.
Форма выпуска, упаковка и состав препарата Облепиховое масло
| Масло для приема внутрь и местного применения | 1 фл. |
| масло облепиховое | 100 мл |
50 мл - флаконы оранжевого стекла (1) - пачки картонные.
100 мл - флаконы оранжевого стекла (1) - пачки картонные.
100 мл - флаконы темного стекла (1) - пачки картонные.
100 мл - флаконы полиэтилентерефталатные (1) коричневого цвета - пачки картонные.
Фармакологическое действие
Стимулирует репаративные процессы при поражениях кожи и слизистых оболочек различной этиологии (раневые, лучевые, ожоговые, язвенные). Оказывает общеукрепляющее действие, обладает антиоксидантным и цитопротекторным действием. Уменьшает интенсивность свободно-радикальных процессов и защищает от повреждения клеточные и субклеточные мембраны. Фармакологическое действие обусловлено наличием в препарате каротина (провитамина А), токоферолов (витамина Е) и других липофильных веществ.
Фармакокинетика
Показания препарата Облепиховое масло
В комплексной терапии в качестве ранозаживляющего средства при поражениях кожи и слизистых оболочек:
- язвенная болезнь желудка и двенадцатиперстной кишки;
- кольпит;
- эндоцервицит;
- эрозия шейки матки;
- послеоперационные раны с целью ускорения заживления;
- наружный геморрой;
- трещины прямой кишки;
- для стимуляции репаративных процессов при раневых повреждениях кожи, лучевых поражениях, ожогах.
| Код МКБ-10 | Показание |
| K25 | Язва желудка |
| K26 | Язва двенадцатиперстной кишки |
| K60 | Трещина и свищ области заднего прохода и прямой кишки |
| K64 | Геморрой и перианальный венозный тромбоз |
| L58 | Радиационный дерматит лучевой |
| N72 | Воспалительная болезнь шейки матки (в т.ч. цервицит, эндоцервицит, экзоцервицит) |
| N76 | Другие воспалительные болезни влагалища и вульвы |
| N86 | Эрозия и эктропион шейки матки |
| T14.0 | Поверхностная травма неуточненной области тела (в т.ч. ссадина, кровоподтек, ушиб, гематома, укус неядовитого насекомого) |
| T14.1 | Открытая рана неуточненной области тела |
| T30 | Термические и химические ожоги неуточненной локализации |
Режим дозирования
Внутрь, местно, наружно.
Внутрь: при язвенной болезни желудка и двенадцатиперстной кишки препарат принимают по 1 чайной ложке 2-3 раза в день. Курс лечения 3-4 недели.
Наружно: при поражениях кожи применяют в виде масляных повязок. На предварительно очищенный от некротических тканей участок кожи наносят облепиховое масло, а затем накладывают ватно-марлевую повязку, которую меняют через день. Лечение проводят до появления грануляций.
В оториноларингологии - при тимпанопластике, после обработки раны антибиотиками или гидрокортизоном, тампонами, обильно пропитанными облепиховым маслом, тампонируют раневую поверхность. Курс лечения -7-10 процедур.
Побочное действие
Возможны аллергические реакции; при приеме препарата внутрь - ощущение горечи во рту, диарея, желчная колика; при местном и наружном применении возможно ощущение жжения.
Если любые из указанных в инструкции побочных эффектов усугубляются, или Вы заметили любые другие побочные эффекты, не указанные в инструкции, сообщите об этом врачу.
Противопоказания к применению
- повышенная чувствительность к препарату;
- детский возраст до 12 лет;
при применении внутрь:
- холецистит;
- холангит;
- панкреатит;
- холелитиаз;
- гепатит;
при ректальном введении:
при наружном и местном применении:
- профузное кровотечение;
- обильное гнойное отделяемое из раны.
С осторожностью: при приеме внутрь - беременность, детский возраст старше 12 лет.
Применение при беременности и кормлении грудью
Применение препарата при беременности и в период грудного вскармливания возможно, если ожидаемая польза для матери превышает потенциальный риск для плода или ребенка. Необходимо проконсультироваться с врачом.
Применение у детей
Особые указания
Лечение проводится под наблюдением врача.
Влияние на способность к управлению транспортными средствами и механизмами
Применение препарата не влияет на выполнение потенциально опасных видов деятельности, требующих повышенной концентрации внимания и быстроты психомоторных реакций (управление транспортными средствами, работа с движущимися механизмами, работа диспетчера, оператора).
Фурункулы – это болезненные, воспаленные, заполненные гноем полости в коже. Размер фурункула может быть от горошинки до грецкого ореха. Хотя фурункулы могут возникать на любом участке тела, чаще всего они возникают в тех областях, где есть волосяной покров и где происходит трение, например: шея, подмышки, пах, лицо, грудь, ягодицы и т.д.
Карбункулы – это особенно крупные фурункулы или несколько рядом расположенных фурункулов, которые обычно более глубокие и болезненные. При подозрении на карбункул обязательно проконсультируйтесь с врачом, т.к. воспаление может проникнуть в кровоток, и тогда вам могут понадобиться антибиотики.
Причины возникновения фурункула
Фурункулы возникают, когда бактерии проникают в волосяной фолликул. Кожная ткань вздувается и появляется красная, наполненная гноем, болезненная припухлость. Пока фурункул не вскроется и не опорожнится (содержащийся в нем гной не выйдет), фурункул будет болеть, и к нему будет неприятно прикасаться.
Cимптомы
Если у фурункула не формируется головка или не наблюдается улучшения в течение трех дней, или если фурункул очень болезненный, с большим количеством гноя, если возникающая боль мешает движению, или если фурункул возник в области лица, позвоночника или в ректальной зоне, если при этом повышается температура или видны красные полоски, расходящиеся от фурункула (лимфангит), а также при частом появлении (фурункулез) даже небольших фурункулов следует обязательно обратиться к врачу
Осложнения
- распространение фурункулов на другие части тела;
- септицемия (заражение крови).
Что можете сделать Вы
Мойте руки с антибактериальным мылом, прежде чем прикасаться к фурункулу и после контакта с фурункулом (неважно, с ранкой или гнойной головкой).
Мягко нанести на пораженную область антибактериальное средство 3-4 раза в день. Наложите теплый компресс на 15 минут 3-4 раза в день для облегчения боли и ускорения созревания гнойной головки. Затем следует закрыть фурункул толстым слоем марли и держать повязку сухой. Ни в коем случае не царапайте и не ковыряйте фурункул, не выдавливайте и не вскрывайте фурункул самостоятельно, т.к. это может разнести инфекцию. Если фурункул открылся сам, осторожно удалите гной, затем тщательно обработайте это место перекисью водорода. Потом наложите сухую повязку. Повторяйте процедуры каждый день до полного заживления. Примите обезболивающее, чтобы облегчить боль и уменьшить воспаление. Не используйте безрецептурные препараты (кремы, мази), содержащие антибиотики без консультации врача. Никогда не пытайтесь сами вскрыть фурункул без разрешения врача.
Тщательно мойте руки перед приготовлением пищи, т.к. бактерии из фурункула могут вызвать заражение пищи. Диабетикам при возникновении фурункула следует немедленно обратиться к врачу.
Что может сделать врач для лечения фурункула
Ваш врач может вскрыть фурункул, сделав небольшой надрез хирургическим лезвием, так, чтобы гной мог выйти, удалить гной и наложить сухую повязку. При необходимости выписать подходящие антибиотики (в т.ч. и мази). При частых фурункулах (фурункулез) назначить анализы (в т.ч. чтобы убедиться, что у вас нет сахарного диабета).
Профилактические меры
Принимайте ванну или душ хотя бы раз в день. Не царапайте зудящее место на коже, т.к. это может спровоцировать попадание инфекции в поврежденное место.
Наносите антисептический лосьон, чтобы не допустить попадания инфекции.
Р-р д/местн. и наружн. прим. масляный 20%: 5 мл, 10 мл, 15 мл, 20 мл, 30 мл или 50 мл фл., 15 мл, 20 мл или 25 мл фл.-капельн.
В настоящее время существует тенденция к росту хронических бактериальных и вирусных заболеваний, для которых характерны непрерывно рецидивирующее течение и малая эффективность антибактериальной и симптоматической терапии. Одним из таких заболеваний яв
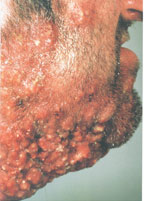
В настоящее время существует тенденция к росту хронических бактериальных и вирусных заболеваний, для которых характерны непрерывно рецидивирующее течение и малая эффективность антибактериальной и симптоматической терапии. Одним из таких заболеваний является хронический рецидивирующий фурункулез (ХРФ). Фурункул развивается в результате острого гнойно-некротического воспаления волосяного фолликула и окружающих его тканей. Как правило, фурункул является осложнением остеофолликулита стафилококковой этиологии. Фурункулы могут возникать как одиночно, так и множественно (так называемый фурункулез).
В случае рецидивирования фурункулеза диагностируется хронический рецидивирующий фурункулез. Как правило, он характеризуется частыми рецидивами, длительными, вялотекущими обострениями, толерантными к проводимой антибактериальной терапии. В зависимости от количества фурункулов, распространенности и выраженности воспалительного процесса ХРФ классифицируется по степени тяжести (Л. Н. Савицкая, 1987).
Тяжелая степень: диссеминированные, множественные, непрерывно рецидивирующие небольшие очаги со слабой местной воспалительной реакцией, не пальпируемыми или слегка определяющимися регионарными лимфатическими узлами. Тяжелое течение фурункулеза сопровождается симптомами общей интоксикации: слабостью, головной болью, снижением работоспособности, повышением температуры тела, потливостью.
Средняя степень тяжести — одиночные или множественные фурункулы больших размеров, протекающие с бурной воспалительной реакцией, с рецидивами от 1 до 3 раз в год. Иногда сопровождается увеличением регионарных лимфатических узлов, лимфангоитом, кратковременным повышением температуры тела и незначительными признаками интоксикации.
Легкая степень тяжести — одиночные фурункулы, сопровождающиеся умеренной воспалительной реакцией, с рецидивами от 1 до 2 раз в год, хорошо пальпируемыми регионарными лимфатическими узлами, без явлений интоксикации.
Чаще всего пациенты, страдающие фурункулезом, получают лечение у хирургов, в лучшем случае на амбулаторном этапе им проводится исследование крови на сахар, аутогемотерапия, некоторым назначают и иммуномодулирующие препараты без предварительно проведенного обследования, и в большинстве случаев они не получают положительного результата от проведенной терапии. Цель нашей статьи — поделиться опытом ведения больных с ХРФ.
Основным этиологическим фактором ХРФ считается золотистый стафилококк, который встречается, по разным данным, в 60–97% случаев. Реже ХРФ вызывается другими микроорганизмами — эпидермальным стафилококком (ранее считавшимся апатогенным), стрептококками групп А и В и другими видами бактерий. Описана вспышка заболеваемости фурункулезом нижних конечностей у 110 пациентов, являвшихся пациентами одного и того же педикюрного салона. Возбудителем данной вспышки являлся Mycobacterium fortuitium, причем этот микроорганизм был выявлен в ванночках для ног, используемых в салоне. В большинстве случаев ХРФ из гнойных очагов высеваются антибиотикорезистентные штаммы золотистого стафилококка. По данным Н. М. Калининой, St. aureus в 89,5% случаев резистентен к пенициллину и ампициллину, в 18,7% — резистентен к эритромицину и в 93% случаев чувствителен к клоксациллину, цефалексину и котримоксазолу. В последние годы отмечается достаточно широкое распространение метициллин-резистентных штаммов этого микроорганизма (до 25% пациентов). По данным зарубежной литературы, наличие на коже или на слизистой оболочке носа патогенного штамма St. aureus считается важным фактором развития заболевания.
ХРФ имеет сложный и до сих пор недостаточно изученный патогенез. Установлено, что дебют и дальнейшее рецидивирование заболевания обусловлены целым рядом эндо- и экзогенных факторов, среди которых наиболее значимыми считаются нарушение барьерной функции кожных покровов, патология ЖКТ, эндокринной и мочевыделительной систем, наличие очагов хронической инфекции различной локализации. По данным проведенных нами исследований, очаги хронической инфекции различной локализации выявляются у 75–99,7% пациентов, страдающих ХРФ. Наиболее часто встречаются очаги хронической инфекции ЛОР-органов (хронический тонзиллит, хронический гайморит, хронический фарингит), дисбактериоз кишечника с увеличением содержания кокковых форм. У больных хроническим фурункулезом патология ЖКТ (хронический гастродуоденит, эрозивный бульбит, хронический холецистит) определяется в 48–91,7% случаев. У 39,7% пациентов диагностируется патология эндокринной системы, представленная нарушениями обмена углеводов, гормонпродуцирующей функции щитовидной и половых желез. У 39,2% больных с упорно текущим фурункулезом имеется латентная сенсибилизация, у 4,2% — клинические проявления сенсибилизации к аллергенам домашней пыли, пыльцы деревьев и злаковых трав, у 11,1% — повышенная концентрация сывороточного IgE.
Таким образом, для большинства больных ХРФ характерны непрерывно рецидивирующее течение заболевания (41,3%) при тяжелой и средней тяжести течения фурункулеза (88%) и длительные обострения (от 14 до 21 дня — 39,3%). У 99,7% пациентов выявлены хронические очаги инфекции различной локализации. В 39,2% случаев определялась латентная сенсибилизация к различным аллергенам. Основным возбудителем является St. aureus.
В возникновении и развитии хронического фурункулеза, наряду с особенностями возбудителя, его патогенными, вирулентными и инвазивными свойствами, наличием сопутствующей патологии, большая роль отводится нарушениям нормального функционирования и взаимодействия различных звеньев иммунной системы. Иммунная система, призванная обеспечить биологическую индивидуальность организма и, как следствие, выполняющая защитную функцию при контакте с инфекционными, генетически чужеродными агентами, в силу разных причин может давать сбой, что ведет к нарушению защиты организма от микробов и проявляется в повышенной инфекционной заболеваемости.
Иммунная защита от бактерий-патогенов включает два взаимосвязанных компонента — врожденный (носящий преимущественно неспецифический характер) и адаптивный (характеризующийся высокой специфичностью к чужеродным антигенам) иммунитет. Возбудитель ХРФ при попадании в кожу вызывает «каскад» защитных реакций.
У 26–35% больных, страдающих хроническим фурункулезом, снижается количество В-лимфоцитов. При оценке компонентов гуморального иммунитета у больных фурункулезом выявляются различные дисиммуноглобулинемии. Наиболее часто встречаются снижение уровней IgG и IgM. Отмечено снижение аффинности иммуноглобулинов у больных ХРФ, причем выявлена корреляция между частотой встречаемости этого дефекта, стадией и тяжестью заболевания. Тяжесть нарушений лабораторных показателей коррелирует с тяжестью клинических проявлений фурункулеза.
Из вышесказанного следует, что изменения показателей иммунного статуса у больных ХРФ носят разноплановый характер: у 42,9% отмечено изменение субпопуляционного состава лимфоцитов, у 71,1% — фагоцитарного и у 59,5% — гуморального звена иммунной системы. В зависимости от выраженности изменений в показателях иммунного статуса больных ХРФ можно разделить на три группы: легкой тяжести, средней и тяжелого течения, что коррелирует с клиническим течением заболевания. При легком течении фурункулеза у большинства больных (70%) показатели иммунного статуса находятся в пределах нормы. При средней и тяжелой степени преимущественно выявляются изменения фагоцитарного и гуморального звеньев иммунной системы.
Диагностика и лечение ХРФ
Исходя из вышеуказанных патогенетических особенностей ХРФ алгоритм диагностики должен включать в себя выявление очагов хронической инфекции, диагностику сопутствующих заболеваний, оценку лабораторных параметров состояния иммунной системы (рис.).
В нашем институте был разработан план обследования больных ХРФ.
- Обязательное лабораторное исследование:
- клинический анализ крови;
- общий анализ мочи;
- биохимический анализ крови (общий белок, белковые фракции, общий билирубин, мочевина, креатинин, трансаминазы - АСТ, АЛТ);
- RW, ВИЧ;
- анализ крови на наличие гепатита В и С;
- посев содержимого фурункула на флору и чувствительность к антибиотикам;
- гликемический профиль;
- иммунологическое обследование (фагоцитарный индекс, спонтанная и индуцированная хемилюминесценция (ХЛ), индекс стимуляции (ИС) люминолзависимой хемилюминесценции ЛЗХЛ), бактерицидность нейтрофилов, иммуноглобулины A, M, G, аффинность иммуноглобулинов);
- бактериологическое исследование фекалий;
- анализ кала на яйца глистов;
- посев из зева на флору и грибы.
- Дополнительное лабораторное исследование:
- определение уровня гормонов щитовидной железы (Т3,Т4, ТТГ, АТ к ТГ);
- определение уровня половых гормонов (эстрадиол, пролактин, прогестерон);
- посев крови на стерильность трехкратно;
- посев мочи (по показаниям);
- посев желчи (по показаниям);
- определение базальной секреции;
- иммунологическое обследование (субпопуляции Т-лимфоцитов, В-лимфоциты);
- общий IgE.
- Инструментальные методы обследования:
- гастроскопия с определением базальной секреции;
- УЗИ органов брюшной полости;
- УЗИ щитовидной железы (по показаниям);
- УЗИ женских половых органов (по показаниям);
- дуоденальное зондирование;
- функции внешнего дыхания;
- ЭКГ;
- рентгенография органов грудной клетки;
- рентгенография придаточных пазух носа.
- Консультации специалистов: отоларинголога, гинеколога, эндокринолога, хирурга, уролога.
Тактика лечения больных ХРФ определяется стадией заболевания, сопутствующей патологией и иммунологическими нарушениями. В стадии обострения ХРФ требуется проведение местной терапии в виде обработки фурункулов антисептическими растворами, антибактериальными мазями, гипертоническим раствором; в случае локализации фурункулов в области головы и шеи или наличия множественных фурункулов — проведение антибактериальной терапии с учетом чувствительности возбудителя. В любой стадии заболевания необходима коррекция выявленной патологии (санация очагов хронической инфекции, лечение патологии ЖКТ, эндокринной патологии и т. д.). При выявлении у больных ХРФ латентной сенсибилизации или при наличии клинических проявлений аллергии необходимо в период поллинации добавлять к лечению антигистаминные препараты, назначать гипоаллергенную диету, проводить хирургическое вмешательство с премедикацией гормональными и антигистаминными препаратами.
В последнее время в комплексной терапии больных ХРФ все чаще используют препараты, оказывающие корригирующее действие на иммунную систему.
Разработаны показания к назначению иммуномодуляторов в зависимости от доминирующего типа нарушений иммунного статуса и степени заболевания. Так, в стадии обострения ХРФ рекомендовано применение следующих иммуномодуляторов.
- При наличии изменений фагоцитарного звена иммунитета целесообразно назначение полиоксидония по 6-12 мг внутримышечно в течение 6-12 дней.
- При снижении аффинности иммуноглобулинов - галавит 100 мг № 15 внутримышечно.
- При снижении уровня В-лимфоцитов, нарушении соотношения CD4/CD8 в сторону уменьшения показано применение миелопида по 3 мг в течение 5 дней внутримышечно.
- При снижении уровня IgG на фоне тяжелого обострения ХРФ при клинической неэффективности применения галавита используются препараты иммуноглобулина для внутривенного введения (октагам, габриглобин, интраглобин).
В период ремиссии возможно назначение следующих иммуномодуляторов.
- Полиоксидоний 6-12 мг внутримышечно в течение 6-12 дней - при наличии изменений фагоцитарного звена иммунитета.
- Ликопид 10 мг в течение 10 дней перорально - при наличии дефектов образования активных форм кислорода.
- Галавит 100 мг № 15 внутримышечно - при снижении аффинности иммуноглобулинов.
Применение ликопида целесообразно также при вялотекущем, непрерывно рецидивирующем фурункулезе. При упорном рецидивировании ХРФ на фоне изменений гуморального звена иммунитета показано назначение препаратов иммуноглобулина для внутривенного введения (октагам, габриглобин, интраглобин). В некоторых случаях целесообразно комбинированное применение иммуномодулирующих препаратов (например, при обострении фурункулеза возможно назначение полиоксидония, в дальнейшем, при выявлении дефекта аффинности иммуноглобулинов, добавляется галавит и т. д.).
Несмотря на значительные успехи, достигнутые в области клинической иммунологии, эффективное лечение ХРФ остается достаточно сложной задачей. В связи с этим требуется дальнейшее изучение патогенетических особенностей этого заболевания, а также разработка новых подходов к терапии ХРФ.
Неоген является синтетическим трипептидом, состоящим из L-аминокислотных остатков изолецитина, глютамина и триптофана. Неоген применялся в составе комплексной терапии, проводимой больным хроническим фурункулезом. Внутримышечные инъекции препарата неогена проводились по 1 мл 0,01% раствора 1 раз в сутки ежедневно, курс — 10 инъекций. Применение неогена в комплексной терапии больных хроническим фурункулезом на стадии ремиссии заболевания вызывает достоверную нормализацию изначально измененных иммунологических показателей (относительного и абсолютного количества лимфоцитов, относительного количества CD3 + , CD8 + , CD19 + , CD16 + -лимфоцитов, поглотительной способности моноцитов по отношению к St. aureus) и увеличение показателей спонтанной ХЛ и аффинности анти-ОАД-антител, количества HLA-DR+-лимфоцитов, а следовательно, позволяет продлить период ремиссии заболевания по сравнению с группой контроля.
Таким образом, из вышеизложенного следует, что ХРФ протекает под воздействием сложного комплекса этиологических и патогенетических факторов и его нельзя рассматривать только как местное воспаление. Больным с ХРФ необходимо проводить всестороннее обследование с целью выявления возможных очагов хронической инфекции, которые являются источником септицемии и при нарушении элиминации микробов в крови в результате снижения иммунологической реактивности организма приводят к возникновению фурункулов. Так как назначение иммунокорригирующих препаратов может вызвать обострение основного заболевания, мы считаем, что лечение больных необходимо начинать с санации выявленных очагов инфекции.
Вопрос о назначении иммунокорригирующих препаратов должен решаться индивидуально, с учетом стадии заболевания, наличия сопутствующей патологии и типа иммунологического дефекта. При выявлении у больного сенсибилизации к различным аллергенам лечение фурункулеза необходимо проводить на фоне противоаллергенной терапии.
Н. Х. Сетдикова, доктор медицинских наук
К. С. Манько
Т. В. Латышева, доктор медицинских наук, профессор
Обеспечение эффективного контроля над желудочной секрецией — одно из главных условий успешной терапии так называемых «кислотозависимых» заболеваний верхних отделов желудочно-кишечного тракта. В клинической и поликлинической практике в настоящее время для
Обеспечение эффективного контроля над желудочной секрецией — одно из главных условий успешной терапии так называемых «кислотозависимых» заболеваний верхних отделов желудочно-кишечного тракта. В клинической и поликлинической практике в настоящее время для ингибирования соляной кислоты париетальными клетками слизистой оболочки желудка чаще всего используются блокаторы Н2-рецепторов гистамина второго (ранитидин) и третьего (фамотидин) поколений, несколько реже — ингибиторы протонного насоса (омепразол, рабепразол), а для нейтрализации уже выделенной в полость желудка соляной кислоты — антацидные препараты. Антацидные препараты иногда применяются в лечении больных, страдающих так называемыми «кислотозависимыми» заболеваниями, в сочетании с Н2-блокаторами рецепторов гистамина; иногда в качестве терапии по «требованию» в сочетании с ингибиторами протонного насоса. Одна или две «разжеванные» антацидные таблетки не оказывают значительного эффекта [10] на фармакокинетику и фармакодинамику фамотидина, применяемого в дозе 20 мг.
Между этими медикаментозными препаратами существуют определенные различия, перечислим основные из них: различные механизмы действия; скорость наступления терапевтического эффекта; продолжительность действия; разная степень эффективности их терапевтического действия в зависимости от времени приема препарата и приема пищи; стоимость медикаментозных препаратов [1]. Вышеперечисленные факторы не всегда учитываются врачами при лечении больных.
В последние годы в литературе все чаще обсуждаются вопросы фармакоэкономической эффективности использования в терапии «кислотозависимых» заболеваний различных медикаментозных препаратов, применяющихся по той или иной схеме [2, 7]. Стоимость обследования и лечения больных особенно важно учитывать в тех случаях, когда больные в силу особенностей заболевания нуждаются в продолжительном лечении [4, 6], например при гастроэзофагеальной рефлюксной болезни (ГЭРБ). Это весьма распространенное заболевание, обследование и лечение таких пациентов требуют значительных расходов.
Как известно, у большей части больных ГЭРБ отсутствуют эндоскопические признаки рефлюкс-эзофагита. Однако по мере прогрессирования ГЭРБ появляются патологические изменения слизистой оболочки пищевода. Симптомы этого заболевания оказывают на качество жизни такое же воздействие, что и симптомы других заболеваний, включая и ишемическую болезнь сердца [5]. Замечено [8] отрицательное воздействие ГЭРБ на качество жизни, особенно на показатели боли, психическое здоровье и социальную функцию. У больных, страдающих ГЭРБ, высок риск появления пищевода Барретта, а затем и аденокарциномы пищевода. Поэтому при первых же клинических симптомах ГЭРБ, особенно при возникновении эндоскопических признаков эзофагита, необходимо уделять достаточное внимание своевременному обследованию и лечению таких больных.
В настоящее время лечение больных ГЭРБ проводится, в частности, препаратом фамотидин (гастросидин) в обычных терапевтических дозировках (по 20 мг или по 40 мг в сутки). Этот препарат обладает рядом достоинств: удобство применения (1-2 раза в сутки), высокая эффективность в терапии «кислотозависимых» заболеваний, в том числе и по сравнению с антацидными препаратами [9], а также большая безопасность по сравнению с циметидином. Однако наблюдения показали [1], что в ряде случаев для повышения эффективности терапии целесообразно увеличение суточной дозы гастросидина, что, по некоторым наблюдениям [1], снижает вероятность появления побочных эффектов по сравнению с использованием в повышенных дозах блокаторов Н2-рецепторов гистамина первого (циметидин) и второго (ранитидин) поколений. Преимущество фамотидина [11] перед циметидином и ранитидином заключается в более продолжительном ингибирующем эффекте на секрецию соляной кислоты обкладочными клетками слизистой оболочки желудка.
Существуют и другие преимущества блокаторов Н2-рецепторов гистамина (ранитидина или фамотидина) перед ингибиторами протонного насоса; в частности, назначение этих препаратов на ночь позволяет эффективно использовать их в лечении больных из-за отсутствия необходимости соблюдать определенную «временную» связь между приемом этих препаратов и пищи. Назначение некоторых ингибиторов протонного насоса на ночь не позволяет использовать их на полную мощность: эффективность ингибиторов протонного насоса снижается, даже если эти препараты приняты больными вечером и за час до приема пищи. Однако суточное мониторирование рН, проведенное у больных, лечившихся омезом (20 мг) или фамотидином (40 мг), свидетельствует [3] о том, что продолжительность действия этих препаратов (соответственно 10,5 ч и 9,4 ч) не перекрывает период ночной секреции, и в утренние часы у значительной части больных вновь наблюдается «закисление» желудка. В связи с этим необходим и утренний прием этих препаратов.
Определенный научно-практический интерес вызывает изучение эффективности и безопасности использования фамотидина и омеза (омепразола) в более высоких дозировках при лечении больных, страдающих «кислотозависимыми» заболеваниями верхних отделов желудочно-кишечного тракта.
Нами изучены результаты клинико-лабораторного и эндоскопического обследования и лечения 30 больных (10 мужчин и 20 женщин), страдающих ГЭРБ в стадии рефлюкс-эзофагита. Возраст больных — от 18 до 65 лет. При поступлении в ЦНИИГ у 30 пациентов выявлены основные клинические симптомы ГЭРБ (изжога, боль за грудиной и/или в эпигастральной области, отрыжка), у 25 больных наблюдались клинические симптомы, в основном ассоциируемые с нарушением моторики верхних отделов желудочно-кишечного тракта (чувство быстрого насыщения, переполнения и растяжения желудка, тяжесть в подложечной области), обычно возникающие во время или после приема пищи. Сочетание тех или иных клинических симптомов, частота и время их возникновения, а также интенсивность и продолжительность у разных больных были различными. Каких-либо существенных отклонений в показателях крови (общий и биохимический анализы), в анализах мочи и кала до начала терапии не отмечено.
При проведении эзофагогастродуоденоскопии (ЭГДС) у 21 больного выявлен рефлюкс-эзофагит (при отсутствии эрозий), в том числе у 4 больных обнаружена рубцово-язвенная деформация луковицы двенадцатиперстной кишки и у одного больного — щелевидная язва луковицы двенадцатиперстной кишки (5 больных страдали язвенной болезнью двенадцатиперстной кишки, сочетающейся с рефлюкс-эзофагитом). Кроме того, у одной больной обнаружена пептическая язва пищевода на фоне рефлюкс-эзофагита и у 8 больных — эрозивный рефлюкс-эзофагит. У всех больных, по данным ЭГДС, обнаружена недостаточность кардии (в сочетании с аксиальной грыжей пищеводного отверстия диафрагмы или без нее).
В лечении таких пациентов использовался гастросидин (фамотидин) в дозировке 40-80 мг в сутки в течение 4 недель (первые 2-2,5 недели лечение проводилось в стационаре ЦНИИГ, в последующие 2 недели пациенты принимали гастросидин в амбулаторно-поликлинических условиях). Терапию гастросидином всегда начинали и продолжали при отсутствии выраженных побочных эффектов, пациентам назначали по 40 мг 2 раза в сутки в течение 4 недель; лишь при появлении диареи и крапивницы дозировку гастросидина уменьшали до 40 мг в сутки.
Исследование было выполнено с учетом критериев включения и исключения больных из исследования согласно правилам клинической практики.
При проведении ЭГДС определяли НР, используя быстрый уреазный тест (один фрагмент антрального отдела желудка в пределах 2-3 см проксимальнее привратника) и гистологическое исследование биопсийного материала (два фрагмента антрального отдела в пределах 2-3 см проксимальнее привратника и один фрагмент тела желудка в пределах 4-5 см проксимальнее угла желудка). При обследовании больных при необходимости проводили УЗИ органов брюшной полости и рентгенологическое исследование желудочно-кишечного тракта. Полученные данные, включая и выявленные побочные эффекты, регистрировали в истории болезни.
В период проведения исследования больные дополнительно не принимали ингибиторы протонного насоса, блокаторы Н2-рецепторов гистамина или другие так называемые «противоульцерогенные» препараты, включая антацидные препараты и средства, содержащие висмут. 25 из 30 пациентов (84%) из-за наличия клинических симптомов, ассоциируемых чаще всего с нарушением моторики верхних отделов пищеварительного тракта, дополнительно получали прокинетики: домперидон (мотилиум) в течение 4 недель или метоклопрамид (церукал) в течение 3-4 недель.
Лечение больных ГЭРБ в стадии рефлюкс-эзофагита всегда начинали с назначения им гастросидина по 40 мг 2 раза в сутки (предполагалось, что в случае появления существенных побочных эффектов доза гастросидина будет уменьшена до 40 мг в сутки). Через 4 недели от начала лечения (с учетом состояния больных) при наличии клинических признаков ГЭРБ и (или) эндоскопических признаков эзофагита терапию продолжали еще в течение 4 недель. Через 4-8 недель по результатам клинико-лабораторного и эндоскопического обследования предполагалось подвести итоги лечения больных ГЭРБ.
При лечении больных гастросидином (фамотидином) учитывались следующие факторы: эффективность гастросидина в подавлении как базальной и ночной, так и стимулированной пищей и пентагастрином секреции соляной кислоты, отсутствие изменений концентрации пролактина в сыворотке крови и антиандрогенных эффектов, отсутствие влияния препарата на метаболизм в печени других лекарственных средств.
Двое из 30 больных (6,6%) через 2-3 дня от начала лечения отказались от приема гастросидина, с их слов, из-за усиления болей в эпигастральной области и появления тупых болей в левом подреберье, хотя объективно состояние их было вполне удовлетворительным. Эти больные были исключены из исследования.
По данным ЭГДС, через 4 недели лечения у 17 пациентов из 28 (60,7%) исчезли эндоскопические признаки рефлюкс-эзофагита, у 11 — отмечена положительная динамика — уменьшение выраженности эзофагита. Поэтому в дальнейшем этих больных лечили гастросидином в амбулаторно-поликлинических условиях в течение еще 4 недель по 40 мг 2 раза в сутки (7 больных) и по 40 мг 1 раз в сутки (4 больных, у которых ранее была снижена дозировка гастросидина).
Весьма спорным остается вопрос — рассматривать ли рефлюкс-эзофагит, нередко наблюдаемый при язвенной болезни (чаще всего при язвенной болезни двенадцатиперстной кишки), как осложнение этого заболевания или же считать его самостоятельным, сопутствующим язвенной болезни заболеванием? Наш многолетний опыт наблюдений показывает, что, несмотря на некоторую связь ГЭРБ и язвенной болезни (их относительно частое сочетание и даже появление или обострение рефлюкс-эзофагита в результате проведения антихеликобактерной терапии), все же язвенную болезнь и ГЭРБ (в том числе и в стадии рефлюкс-эзофагита) следует считать самостоятельными заболеваниями. Мы неоднократно наблюдали больных с частыми обострениями ГЭРБ в стадии рефлюкс-эзофагита (при наличии у них рубцово-язвенной деформации луковицы двенадцатиперстной кишки). Последнее обострение язвенной болезни (с образованием язвы в луковице двенадцатиперстной кишки) у этих больных отмечалось 6-7 и более лет назад (значительно реже, чем рецидивы ГЭРБ в стадии рефлюкс-эзофагита), однако при очередном обострении язвенной болезни с образованием язвы в луковице двенадцатиперстной кишки всегда при эндоскопическом исследовании выявляли и рефлюкс-эзофагит. Мы уверены, что при наличии современных медикаментозных препаратов лечить неосложненную язвенную болезнь значительно легче, чем ГЭРБ: период терапии при обострении язвенной болезни двенадцатиперстной кишки занимает значительно меньше времени по сравнению с терапией ГЭРБ; да и в период ремиссии этих заболеваний пациенты с язвенной болезнью двенадцатиперстной кишки чувствуют себя более комфортно, в то время как больные ГЭРБ вынуждены для улучшения качества жизни отказываться от приема значительно большего количества продуктов и напитков.
При обследовании (через 8 недель лечения) трое из 11 больных по-прежнему предъявляли жалобы, ассоциированные с нарушением моторики верхних отделов желудочно-кишечного тракта. Трое больных при хорошем самочувствии отказались от проведения контрольной ЭГДС через 8 недель. По данным ЭГДС, у 7 из 8 больных отмечено исчезновение эндоскопических признаков эзофагита (в том числе у одной больной — заживление пептической язвы пищевода).
Определение НР проводилось у всех 30 больных: в 11 случаях выявлена обсемененность НР слизистой оболочки желудка (по данным быстрого уреазного теста и гистологического исследования материалов прицельных гастробиопсий). Антихеликобактерная терапия в период лечения больным ГЭРБ в стадии рефлюкс-эзофагита не проводилась.
При оценке безопасности проведенного лечения каких-либо значимых отклонений в лабораторных показателях крови, мочи и кала отмечено не было. У 4 больных (13,3%), у которых ранее наблюдался «нормальный» (регулярный) стул, на 3-й день лечения гастросидином (в дозе 40 мг 2 раза в сутки) был отмечен, с их слов, «жидкий» стул (кашицеобразный, без патологических примесей), в связи с чем доза гастросидина была уменьшена до 40 мг в сутки. Через 10-12 дней после снижения дозы стул нормализовался без какой-либо дополнительной терапии. Интересно отметить, что еще у 4 больных, которые ранее страдали запорами, на фоне проводимого лечения стул нормализовался на 7-й день. У 3 из 30 больных (10%) на 3-4-й день приема гастросидина появились высыпания на коже туловища и конечностей (крапивница). После уменьшения дозировки гастросидина до 40 мг в сутки и проведения дополнительного лечения диазолином (по 0,1 г 3 раза в день) высыпания на коже исчезли.
Проведенные исследования показали целесообразность и эффективность терапии ГЭРБ в стадии рефлюкс-эзофагита гастросидином по 40 мг 2 раза в сутки, особенно при лечении больных с выраженными болевым синдромом и изжогой. Такое лечение может успешно проводиться в стационарных и амбулаторно-поликлинических условиях. Изучение отдаленных результатов проведенного лечения позволит определить продолжительность периода ремиссии этого заболевания и целесообразность лечения гастросидином в качестве «поддерживающей» терапии или же терапии «по требованию».
Читайте также:

