Неврит это волчанка это
Обновлено: 19.04.2024
Ревматические болезни относятся к группе заболеваний, которые характеризуются развитием аутоиммунных процессов против антигенов почти всех органов и тканей организма, что сочетается с образованием аутоантител с органонеспецифическими с
Ревматические болезни относятся к группе заболеваний, которые характеризуются развитием аутоиммунных процессов против антигенов почти всех органов и тканей организма, что сочетается с образованием аутоантител с органонеспецифическими свойствами.
Аутоиммунные процессы осуществляют информационный обмен между нейроэндокринной и иммунной системами, при этом главную роль играют аутоантитела к гормонам, медиаторам и их рецепторам. Продемонстрирован синтез нейропептидов в иммунокомпетентных клетках, а в клетках нейроэндокринной системы доказана возможность синтеза лимфокинов и монокинов.
Получены данные о нейрогенной регуляции функций иммунитета и их нарушений, в то же время иммунокомпетентные клетки и их медиаторы могут влиять на функцию центральной нервной системы (ЦНС) по принципу нейроиммуномодуляции. Показано, что свойством нейросекреции обладает вся центральная и периферическая нервная система. Влияние иммунной и нервной систем друг на друга реализуется через рецепторные структуры клеток, взаимодействие которых создает связи «рецептор-рецептор» и таким образом организует молекулярный механизм совместной работы обеих систем.
Функционирование клеток и сигнальная информация обеспечиваются медиаторами и нейротрансмиттерами в обеих системах, между нервной и иммунной системой происходит взаимообмен информацией с помощью цитокинов, стероидов и нейропептидов [1, 2].
Таким образом, доказана общность и взаимосвязь нервной и иммунной систем, сходство между их структурами и функциями и развитие нового направления современной иммунологии — нейроиммунологии [3, 4]. Широкий диапазон неврологических синдромов при аутоиммунных системных заболеваниях позволяет рассматривать их как модельные системы для изучения патогенетической роли иммунных механизмов поражения центральной и периферической нервной системы [5].
Потенциальными мишенями для аутоиммунной агрессии могут быть различные антигены нервной ткани, включая миелин, в том числе ассоциированный с гликопротеином, и его основной белок, ганглиозиды, белок ядер нейрональных клеток и другие [6]. Так, мишеневидные антигены при нейролюпусе представлены антигенами нейрональной ткани, рибосомальным Р-белком, рДНК, малым ядерным рибонуклеопротеидом, а также анионными фосфолипидами при антифосфолипидном синдроме, что обуславливает широкий спектр неврологической симптоматики при данной патологии [7, 8].
По данным различных авторов, частота поражений нервной системы при ревматических заболеваниях (РЗ) колеблется от 40% до 70% и выше, если учитывать психические синдромы и головную боль. Неврологические синдромы включены в классификационные критерии системных васкулитов, опубликованные Американской коллегией ревматологии в 1990 году, в диагностические критерии и критерии активности системной красной волчанки (СКВ), а также в ряд других диагностических критериев, в частности узелкового полиартериита у детей. Неврологические нарушения при РЗ требуют проведения дифференциальной диагностики и назначения адекватного лечения совместно ревматологом и неврологом.
При СКВ в диагностические критерии неврологических поражений включены судороги или психозы. Поражение ЦНС обусловлено в основном сосудистой патологией, к которой относят васкулопатию, тромбозы, истинные васкулиты, инфаркты и геморрагии [7]. В цереброспинальной жидкости обнаруживаются антинейрональные антитела, определяется повышение уровня белка, увеличение клеточного состава. Описаны разные виды судорожных припадков: большие, малые, по типу височной эпилепсии, а также гиперкинезы. При ЦНС-люпусе имеет место головная боль типа мигрени, устойчивая к анальгетикам, но отвечающая на лечение глюкокортикостероидами. Параличи черепных нервов обычно сопровождаются офтальмоплегией, мозжечковыми и пирамидными симптомами и нистагмом. Имеют место зрительные нарушения, преходящие нарушения мозгового кровообращения. Острый поперечный миелит встречается редко и имеет неблагоприятный прогноз. Психические синдромы разнообразны и характеризуются аффективными, органическими мозговыми или шизофреноподобными проявлениями [9, 10].
В рамках СКВ был описан и антифосфолипидный синдром. Этот синдром включает: рецидивирующие артериальные или венозные тромбозы, привычное невынашивание беременности и тромбоцитопению и дополнительные признаки: сетчатое ливедо, неврологические проявления: хорею, эпилепсию, мигренеподобную головную боль, нарушения мозгового кровообращения и деменцию вследствие множественных инфарктов, хронические язвы голеней, Кумбс-положительную гемолитическую анемию, клапанные поражения сердца и серологические маркеры — антифосфолипидные антитела, к которым относятся антикардиолипиновые антитела IgG и IgM и волчаночный антикоагулянт [11].
При системной склеродермии (ССД) неврологический синдром представлен в основном полиневритическими проявлениями, связанными с сосудистыми изменениями и фиброзными процессами в соединительной ткани. Для узелкового полиартериита характерны множественные мононевриты, для гранулематоза Вегенера — асимметричная полинейропатия, для неспецифического аортоартериита — дисциркуляторная энцефалопатия и нарушения мозгового кровообращения.
Собственные данные включали обследование 229 больных различными формами РЗ, среди которых 110 больных страдали системными заболеваниями соединительной ткани: 88 больных СКВ, 22 — ССД и 119 больных — системными васкулитами: облитерирующий тромбангиит (ОТ) — 21, узелковый полиартериит (УП) — 27, неспецифический аортоартериит — (НАА) — 32, геморрагический васкулит (ГВ) — 15 и гранулематоз Вегенера (ГрВ) — 2, другие формы — 22. Проведено детальное неврологическое исследование, ультразвуковая транскраниальная допплерография сосудов мозга, реоэнцефалография, компьютерная (КТ) и магнитно-резонансная томография (МРТ) головного мозга, электроэнцефалография, исследование иммунного статуса.
У большинства больных заболевания дебютировали кожным (50,6%), суставно-мышечным (35,4%) и сосудистым (27,1%) синдромом. Органные поражения в дебюте регистрировались с частотой 7%, синдром артериальной гипертензии — у 5,2%, лихорадка — у 7,0%, гематологические нарушения — 7,9%. Неврологические расстройства в дебюте заболевания отмечены у 12,2% и проявлялись моно- и полиневропатией и синдромом энцефаломиелополирадикулоневрита (ЭМПРН). Поражение периферической нервной системы в дебюте заболевания было особенно характерно для УП и наблюдалось у 30% больных. Основными синдромами дебюта со стороны ЦНС был цефалгический (10,5%) и вестибулярный (6,3%), чаще они наблюдались при НАА. Вовлечение ЦНС имело место у 96 (41,9%) больных, являясь наиболее выраженным при СКВ, НАА, УП.
Цереброваскулярная патология была доминирующей в клинической картине болезни у 34,7% больных, а иногда разнообразные симптомы поражения ЦНС развивались задолго до появления полисиндромной картины заболевания. Основные клинические проявления цереброваскулярной патологии включали: цефалгический (82%), астенический (76%), вестибулярно-атактический (80%), пирамидный (74%) синдромы, синдром вегетативно-сосудистой недостаточности (69%), диссомнический (79%) и базально-оболочечный (37%), гипопоталамической дисфункции (34,7%).
Описанная неврологическая симптоматика часто сочеталась с симптомами сосудистой недостаточности головного мозга, которые объединялись синдромом дисциркуляторной энцефалопатии 1 (11%), 2 (26,4%) или 3 (8%) степени. У 7,8% больных имели место преходящие нарушения мозгового кровообращения.
Гипоталамическая дисфункция у больных РЗ проявлялась полиморфными нейроэндокринными расстройствами, нарушением терморегуляции, преимущественно по типу пароксизмальной центральной гипертермии, инсомнией, патологией психоэмоциональной сферы.
Установлено достоверное преобладание у больных пирамидной недостаточности слева (41%). Преобладание пирамидной недостаточности справа регистрировалось реже (23,7%). Дистонические феномены в форме вестибулярно-мозжечковой установки кисти и диссоциированная мышечная гипотония в ногах также были более выражены слева. Полученные данные свидетельствуют о преобладающем поражении пирамидной и сенсорной систем, а также неспецифических структур правого полушария, которое тесно связано с гипоталамической областью и обеспечивает адаптацию организма к воздействующим факторам внешней среды. Обнаруженная функциональная асимметрия свидетельствует о срыве адаптационных механизмов нервной системы и указывает на роль дисфункции правополушарно-гипоталамической системы.
При использовании методов МРТ и/или КТ было выявлено изменение желудочковой системы в виде ее расширения или деформации и/или расширения субарахноидального пространства, а также очаговые поражения различных структур головного мозга, атрофия вещества мозга и краниовертебральные аномалии. Признаки наружной, внутренней или сочетанной гидроцефалии отмечались при всех нозологических формах. Очаговые изменения вещества мозга включали гиперденситивные зоны, гиподенситивные зоны с отеком или без него, единичные или множественные.
При исследовании сосудистой системы и мозгового кровообращения достоверно наблюдалось повышение тонуса сосудов, гипертонический и дисциркуляторный тип кровообращения по данным реоэнцефалографии (РЭГ) и увеличение линейной скорости кровотока по средней мозговой артерии. Больные с вовлечением ЦНС отличались по электроэнцефалографии: им были свойственны диффузные патологические изменения, наличие дезорганизации альфа-ритма, дизритмий и пароксизмальной активности.
Корреляционный анализ цереброваскулярной патологии и результатов инструментальных исследований сосудов головного мозга показал, что при всех нозологических формах у пациентов имело место нарушение венозной гемоциркуляции. В последующем происходило сужение церебральных артерий, ликвородинамические нарушения с формированием внутричерепной гипертензии, нарушением системы микроциркуляции в головном мозге. Очаговые поражения головного мозга отличались локализацией процесса в зависимости от нозологической формы. В табл. представлены основные неврологические проявления РЗ.
У 39% больных СКВ молодого возраста с поражением ЦНС имели место нарушения мозгового кровообращения, причем у половины из них инсульт развился в начале заболевания. Одновременно с инсультом в дебюте СКВ у больных чаще выявлялась «сосудистая бабочка» и/или вазоспастический синдром, повышение артериального давления, чаще диастолического. У этих больных отмечались умеренные или высокие титры кардиолипинов IgG, антител к нативной ДНК и ревматоидного фактора (РФ) IgM, что могло свидетельствовать о наличии текущего церебрального васкулита. Эти данные подтверждались выявлением гипертонуса резистивных интракраниальных сосудов и патологией микроциркуляторного русла в виде увеличения количества функционирующих капилляров, их выраженной извитостью с замедлением кровотока в артериолах. Изменения в свертывающей системе характеризовались синдромом гиперкоагуляции. Выявлены основные факторы риска развития инсульта у больных РЗ: артериальная гипертензия, поражения сердца, гиперкоагуляция, иммунное воспаление сосудистой стенки, асимметрия мозгового кровотока.
Среди больных РЗ цереброваскулиты (ЦВ) имели место у 28,3% больных. Диагноз ЦВ ставился при обнаружении очаговой неврологической симптоматики, изменений на глазном дне, снижения зрения, наличии признаков нарушения мозгового кровообращения, а также по результатам КТ и ядерно-магнитно-резонансной томографии (ЯМРТ), при которых выявлялись наружная и внутренняя гидроцефалия, очаговые изменения в коре и субкортикальном веществе. При этом с течением времени число очагов любой локализации в головном мозге нарастало. При магнитно-резонансном ангиографическом (МРА) исследовании отмечались множественные сегментарные неровности сосудистой стенки, циркулярные или эксцентричные стенозы и дилятация мелких и средних интракраниальных артерий с формированием аневризм, нарушения кровотока. Выявленное снижение интенсивности МРА-сигнала на фоне повышения активности ревматического процесса свидетельствовало о наличии ЦВ.
Иммунологическими маркерами ЦВ считали антитела к нативной ДНК, IgG-антитела к кардиолипину (аКЛ) и IgM аКЛ, антинейтрофильные цитоплазматические антитела (АНЦА), в меньшей степени — РФ и волчаночный антикоагулянт (ВА). Имели место клинико-иммунологические корреляции с неврологическими проявлениями.
Изолированный (первичный) ЦВ характеризовался обнаружением симптомов вовлечения ЦНС и такими признаками, как головная боль, судороги, менингеальный синдром, острая прогрессирующая энцефалопатия без признаков экстракраниального или системного васкулита, психические синдромы, деменция, прогрессирующее снижение интеллекта, инсульты, нарушения зрения, нистагм. Чаще перивентрикулярные очаги выявлялись в первый год заболевания.
Ряд больных обращались на консультацию к окулисту в связи с ухудшением зрения, вплоть до амавроза, наличием увеита, ишемического неврита. Ангиопатия сетчатки имела место у 41% этих больных, флебопатия — у 14%, ретиноваскулит — у 6%, ангиоспазм — у 13%, ангиосклероз — у 18%.
Полиневритический синдром встречался у подавляющего большинства больных (96,7%) в виде сенсорной, чувствительно-двигательной полиневропатии или в сочетании с поражениями ЦНС, с синдромом ЭПН и ЭМПРН. При ССД, ОТ и ГВ преобладали формы в виде чувствительной или чувствительно-двигательной полиневропатии, а при СКВ и НАА — формы с сочетанным поражением периферической НС (ПНС) и ЦНС — синдромы ЭПН и ЭМПРН. При ОТ и НАА отмечалась отчетливая диссоциация степени выраженности полиневропатии по оси тела, причем при ОТ симптоматика была более отчетливой в ногах, при НАА — в руках. В целом асимметричная полиневропатия имела место у 19,2% больных, достигая максимума при УП (59,3%).
Патология НС при РЗ нередко определяет прогноз, клиническую картину заболевания и качество жизни больных, а также требует обязательного сочетанного применения базисной противовоспалительной терапии, ангио- и нейропротекторов. К группе нейропротекторов относят Актовегин, Инстенон. Используются препараты, улучшающие мозговое кровообращение, — Винпоцетин, Кавинтон, метаболические средства с антигипоксантным действием — Ноотропил, Пирацетам, Церебролизин, по показаниям седативные и противосудорожные средства, антидепрессанты.
При РЗ терапия включает глюкокортикостероиды, иммуносупрессанты, иммуноглобулин, плазмаферез, иммуномодуляторы, дезагреганты, нестероидные противовоспалительные препараты и симптоматические средства.
Лечение состоит из нескольких этапов: быстрое подавление иммунного ответа в дебюте заболевания и при его обострениях (индукция ремиссии); длительная поддерживающая терапия иммуносупрессантами, в дозах, достаточных для достижения клинической и лабораторной ремиссии заболевания; определение степени повреждения органов или систем организма и их коррекция, проведение последующих реабилитационных мероприятий.
Первый этап включает эффективное подавление иммунного воспаления на ранних стадиях болезни и предполагает использование глюкокортикостероидов, иммуносупрессантов цитостатического действия типа Циклофосфана и антиметаболитного действия типа Метотрексата, цитокинсупрессивного препарата Циклоспорина А, внутривенного иммуноглобулина, назначение повторных курсов пульс-терапии метилпреднизолоном и Циклофосфаном, в сочетании с экстракорпоральными методами лечения.
При острых церебральных нарушениях при высокой активности СКВ используется схема пульс-терапии с введением Метипреда 1 г внутривенно 1 раз в день в течение 3 дней и с добавлением 800 мг Циклофосфана во 2-й день. При хроническом течении СКВ суточная доза преднизолона составляла 15–20 мг с последующим постепенным снижением, Циклофосфан применяется внутримышечно в дозе 400 мг в неделю до 1600–2000 мг на курс, затем по 200 мг в неделю в течение года и более. Апробируются препараты мофетила микофенолат и лефлуномид.
При патологии органа зрения назначают нестероидные противовоспалительные препараты в виде инъекций диклофенака, а затем пероральные препараты этой группы, дезагреганты, при наличии признаков воспалительной активности добавляют умеренные дозы глюкокортикостероидов, а при резком снижении зрения и выраженных признаках активности используют пульс-терапию.
Проводится определение наиболее эффективных и менее токсичных схем применения иммуносупрессивных препаратов, путей их введения, и включение в комплексное лечение больных препаратов, улучшающих микроциркуляцию и/или влияющих на реологические свойства крови (Гепарин, Фраксипарин, Трентал, Ралофект, Тиклид).
В ряде случаев назначают препараты типа Реаферона, а при наличии инфицированных язв, некрозов кожи или конечностей применяют антибиотики. Ввиду многообразия нозологических форм на выбор лекарственных средств в дебюте заболевания оказывает влияние распространенность патологического процесса и наличие интеркуррентной инфекции. Показано назначение ангиопротекторов и посиндромная терапия.
Учитывая высокий удельный вес неврологической патологии, больные РЗ должны проходить комплексное клинико-инструментальное неврологическое исследование уже на ранней стадии патологического процесса. Постановка диагноза РЗ и комплексная терапия глюкокортикостероидами и иммуносупрессантами способствуют коррекции нарушений ЦНС и ПНС.
Литература
Stenberg E. M. Neuroendocrine regulation of autoimmune / inflammatory diseases // J. Endocrinol. 2001; 169 (3): 429–435.
Насонова В. А., Иванова М. М., Калашникова Е. А. и др. Актуальные проблемы нейроиммунологии // Вестн. РАМН. 1994;1: 4–7.
Сrofford L. J. The hypothalamic-pituitary-adrenal axis in the pathogenesis of rheumatic diseases // Endocrinol. Metab. Clin. North. Am. 2002; 31 (1): 1–13.
Мотовилов А. А., Травина И. В., Проказова Н. В. и др. Антитела к нейтральным гликосфинголипидам и ганглиозидам у больных системной красной волчанкой с поражением центральной нервной системы // Клин. ревматол. 1995; 1: 36–38.
Иванова М. М. ЦНС-люпус: проблемы и достижения (результаты 10-летнего клинико-инструментального исследования) // Тер. арх. 2001; 5: 25–29.
Лисицина Т. А., Вельтищев Д. Ю., Серавина О. Ф. и др. Варианты психических нарушений у больных системной красной волчанкой // Научно-практ. ревматол. 2008; 4: 21–27.
Nived O., Sturfelt G., Liang M. H., De Pablo P. The ACR nomenclature for CNS lupus revisited // Lupus. 2003; 12: 872–876.
Н. П. Шилкина, доктор медицинских наук, профессор Н. Н. Спирин, доктор медицинских наук, профессор И. В. Дряженкова, кандидат медицинских наук ЯГМА, НУЗ «ДКБ на станции Ярославль «ОАО «РЖД», Ярославль
Что такое невропатия (нейропатия)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Алексеевича Григория Васильевича, невролога со стажем в 16 лет.
Над статьей доктора Алексеевича Григория Васильевича работали литературный редактор Вера Васина , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Невропатия, или нейропатия (Neuropathy) — повреждение одного или нескольких нервов периферической нервной системы. К ней относятся черепные и спинальные нервы, а также нервы и сплетения вегетативной нервной системы [2] [3] . Невропатия проявляется нарушением чувствительности, болью в поражённом участке, судорогами, мышечной слабостью и затруднением движений. Выделяют две основные группы невропатий:
- мононевропатия — повреждение отдельного нерва, например срединного.
- полинейропатия — множественные повреждения нервов при диабетической полинейропатии, диффузной нейропатии, полирадикулопатии, плексопатии.
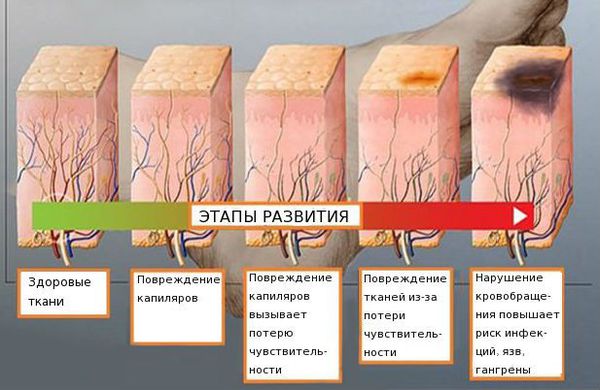
Распространённость нейропатии среди населения составляет 2-7 %. Риск развития заболевания увеличивается с возрастом: в 40 лет патология встречается в 15 % случаев [4] [5] [6] .
Повреждение периферических нервов может вызывать множество причин. Даже после комплексного обследования выявить их удаётся не всегда. К основным факторам, приводящим к заболеванию, относят:
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы невропатии
Несмотря на то, что нейропатию вызывают различные причины, основные симптомы заболевания схожи [9] [14] [15] [16] [17] :
- Двигательные нарушения, слабость мышц. Пациент с трудом выполняет действия, связанные с мелкой моторикой, например застёгивание пуговиц. Возникают проблемы с ходьбой — больной может упасть из-за слабости мышц стопы.
- Сенсорные нарушения — онемение, повышенная тактильная чувствительность, резкая стреляющая боль, подобная удару электрическим током.
- Снижение и выпадение сухожильных рефлексов. Появляются трудности при выполнении повседневных действий, таких как надевание одежды, перемещение предметов.
- Расстройства сердечно-сосудистой системы. Выражается в нестабильности артериального давления и его снижении при резком вставании, проявляется головокружением и потемнением в глазах .
- Расстройства желудочно-кишечного тракта — запоры и кишечная непроходимость, вызванные ухудшением тонуса мышц кишечника.
- Боли в кистях и стопах.
- Нарушение равновесия и координации движений.
- Повышенная потливость.
- Задержка мочеиспускания.
- Сексуальная дисфункция.
При нейропатии могут поражаться не только нервы конечностей, но и черепно-мозговые нервы:
- невропатия зрительного нерва (оптическая нейропатия) приводит к нечёткости, затуманенности зрения, нарушению цветового восприятия, слепоте;
- поражение глазодвигательного нерва проявляется опущением верхнего века и параличом глазных мышц;
- патология отводящего нерва вызывает сходящееся косоглазие, опущение верхнего века, двоение в глазах;
- лицевого нерва — паралич мимических мышц;
- преддверно-улиткового (слухового нерва) — потерю слуха;
- языкоглоточного нерва — нарушение подвижности языка;
- гортанного нерва — дыхательную недостаточность [15] .
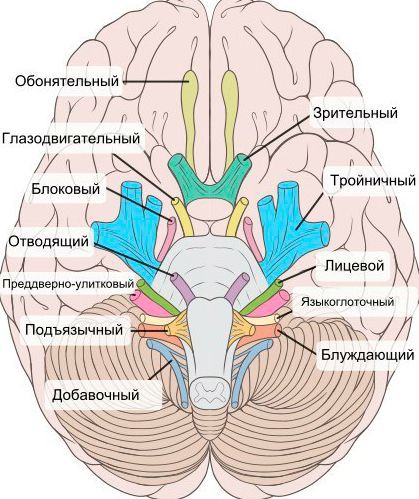
На начальных стадиях двигательные расстройства могут не проявляться. Но в дальнейшем нейропатия значительно ограничивает физическую активность пациента [5] [7] [16] [17] .
Для повреждения периферической нервной системы характерны основные синдромы:
- Поражение переднего корешка спинного мозга — приводит к ослаблению или параличу мышц. Возможны судороги и подёргивания.
- Поражение заднего корешка спинного мозга — проявляется повышенной тактильной чувствительностью, жжением, нарушением спинальных рефлексов, болью в области поражения.
- Поражение межпозвоночного узла — вызывает жжение, покалывание, снижение болевого порога, интенсивные жгучие боли, обострение герпесвирусной инфекции.
- Поражение спинального нерва — приводит к расстройствам чувствительности и двигательным нарушениям.
- Поражение сплетения периферических нервов — вызывает боль, но менее интенсивную, чем при повреждении корешков [16] .
Патогенез невропатии
К нейропатии могут приводить нарушения обмена веществ и иммунной системы, генетические факторы, инфекционное и токсическое воздействие [1] .
Развитие заболевания при обменных нарушениях, например при сахарном диабете, вызвано чрезмерным накоплением глюкозы в клетке. Гипергликемия приводит к отложению в нервных клетках продукта обмена — сорбитола. Избыток сорбитола нарушает функции клеток периферических нервов. При этом уменьшается выработка мио-инозитола — соединения, влияющего на передачу сигналов в мозге и защиту нервных клеток от повреждения. Всё это приводит к ухудшению регенеративных способностей нервной ткани и снижению её проводимости [9] .
В развитии нейропатии важная роль принадлежит митохондриям (органеллам, обеспечивающих клетку энергией) . Они повреждаются при гипергликемии и приёме противоопухолевых препаратов: паклитаксела, бортезомиба, оксалиплатина. Эти лекарства влияют и на другие внутриклеточные структуры (например микротрубочки, поддерживающие форму клетки ), негативно воздействуют на клеточные процессы и в результате активируют запрограммированную гибель нейронов [9] [15] [18] . Схожие нарушения возникают и у ВИЧ-инфицированных пациентов, принимающих антиретровирусные препараты [9] [15] .
Классификация и стадии развития невропатии
Попытки систематизировать различные виды нейропатии предпринимались многократно как отечественными, так и зарубежными авторами. Но ни одна из классификаций не удовлетворяет всем потребностям клиницистов. Это связано с тем, что к развитию заболевания приводит множество сложных и до конца не изученных факторов [16] .
По одной из классификаций, нейропатии разделяют на следующие группы: [19]
I. Мононевропатии (поражение одного нерва).
- Травматические мононевропатии — возникают при травмах, ранениях, электротравмах, химических повреждениях.
- Туннельные синдромы — это ущемление нерва при длительном сдавлении и травматизации в костно-мышечных каналах. К ним относятся: синдром карпального канала (сдавление нерва в области запястья), пронаторный синдром (поражение нерва в плече), синдром кубитального канала (в локте), синдром тарзального канала (сдавление большеберцового нерва), синдром ложа Гийона (сдавление глубокой ветви локтевого нерва) и др.
II. Множественные нейропатии (поражение нескольких отдельных нервов).
- Моторная мультифокальная нейропатия с блоками проведения — аутоиммунное заболевание, проявляющееся слабостью мышц стоп и кистей.
- Моторно-сенсорная невропатия с блоками проведения — вызывает поражение не только моторных, но и сенсорных волокон.
- Множественная невропатия при васкулитах.
III. Полиневропатии (множественные поражения нервной ткани).
1. Наследственные полиневропатии: Шарко — Мари — Тута, синдром Руси — Леви, Дежерина — Сотта и др.
2. Приобретённые полиневропатии.
2.1. Аутоиммунные полиневропатии — возникают при сбое в работе иммунной системы (синдром Гийена — Барре, синдром Миллера — Фишера, хроническая воспалительная демиелинизирующая полинейропатия, парапротеинемические полиневропатии, паранеопластические полинейропатии).
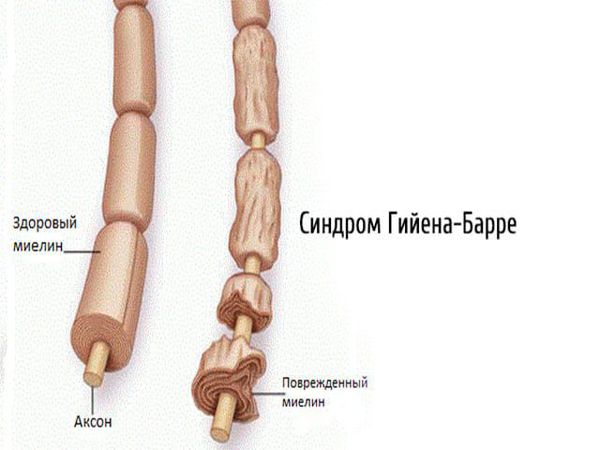
2.2. Метаболические полинейропатии — диабетическая, уремическая, печёночная, при системных заболеваниях. Наиболее часто встречается диабетическая нейропатия.
2.2 Вызванные дефицитом витаминов В1, В6, В12.
2.3 Токсические полинейропатии — вызванная алкоголем, лекарствами, отравлением тяжёлыми металлами. Препараты, способные приводить к нейропатии:
-
— крайне нейротоксичное средство. Развитие острой нейропатии возникает в 90 % случаев, а хронической — в 50 %. Приём оксалиплатина приводит к жжению, покалыванию, онемению рук, ног и области вокруг рта.
- Таксен (Палитаксел,Доцетаксел) — вызывает нарушение чувствительности, слабость и боль в мышцах, возможны редкие вегетативные симптомы.
- Препараты на основе алкалоидов барвинка (Винбластин, Винорелбин, Виндезин, Винкристин) — нарушают функции мочевого пузыря и кишечника, влияют на чувствительность в руках и ногах, ухудшают мелкую моторику, приводят к мышечной слабости и резкому снижению артериального давления.
- Бортезомиб — нарушает чувствительность, приводит к боли и вегетативным симптомам.
- Иммуномодулирующие препараты (Талидомид) — провоцирует сенсорные нарушения, преимущественно в нижних конечностях, лёгкие двигательные, желудочно-кишечные и сердечно-сосудистые расстройства [15][16][18] .
2.4 Инфекционно-токсические — после гриппа, кори, дифтерии, мононуклеоза, поствакцинальные, при ВИЧ-инфекции, лепре.
IV. Поражения сплетений (шейного, верхнего плечевого, нижнего плечевого, пояснично-крестцового).
V. Вертеброгенные поражения нервных корешков (радикулиты).
Несмотря на многообразие причин, вызывающих полинейропатии, по участкам поражения их можно разделить на два вида:
- Аксональные — вовлечены нервы с наиболее длинными отростками (аксонами), к ним относится большинство токсических полинейропатий, аксональный тип наследственной моторно-сенсорной полинейропатии. Характеризуются мышечными атрофиями.
- Демиелинизирующие — вызваны разрушением миелиновой оболочки, окружающей отростки нервных клеток. Проявляются выпадением сухожильных рефлексов, развитием мышечной слабости без мышечных атрофий [19] .
Осложнения невропатии
Зачастую нейропатия уже является осложнением какого-либо заболевания, например сахарного диабета. У некоторых пациентов, страдающих диабетом, может развиваться диабетическая амиотрофия — асимметричное поражение проксимальных (близких к туловищу) отделов ног с развитием болей и слабости в мышцах [16] [17] [19] .
Если лечение не начато вовремя, нейропатия стремительно прогрессирует. В результате снижается тонус мускулатуры, наступает атрофия мышц и инвалидность. На фоне мышечной слабости случаются падения и травмы. Пациенты утрачивают способность ходить и обслуживать себя. Иногда последствиями полинейропатии становятся полный паралич конечностей или дыхательная недостаточность.
Диагностика невропатии
Неврологи используют различные шкалы для оценки тяжести нейропатии. Универсального опросника, соответствующего всем потребностям клиницистов, не существует. Это связано с различным прогнозом, проявлениями и причинами нейропатии [21] .
Во время обследования оценивают проводимость нерва, учитывая временную динамику [17] . Для диагностики применяют следующие методы:
- Электромиография (ЭМГ) — регистрация электрической активности в мышце при её сокращении. Позволяет определить характер двигательных расстройств, уточняет степень разрушения нерва и выявляет заболевание до появления симптомов. ЭМГ позволяет провести дифференциальную диагностику невропатии с миастенией, миотонией, миоплегией, полимиозитом [16][17] .
- Электронейромиография (ЭНМГ) — оценивает прохождение импульса по нервному волокну. ЭНМГ поможет не только выявить расположение поражённых участков, но и определить момент начала патологического процесса [17] .
- УЗИ — распространённый метод визуализации периферических нервов. Ультразвук поможет выявить нарушения, которые незаметны при электродиагностике. Оценивается изменение диаметра нерва, непрерывность и ухудшение звукопроводимости. УЗИ позволяет обнаружить опухоли периферических нервов, травматические невромы, разрывы, воспаление, демиелинизирующие процессы.
- МРТ — визуализирует нервы и структуру мягких тканей, выявляет злокачественные опухоли и предоставляет информацию о мышечной атрофии и поражении нервов. МРТ выявляет повреждение нерва в областях, которые трудно исследовать при помощи электродиагностики или ультразвука.
Согласно статистике, УЗИ выявляет мононевропатии или плечевые плексопатии чаще, чем МРТ [20] .
Лечение невропатии
Выбор методов лечения нейропатии зависит от вызвавших её причин:
- Метаболические нейропатии, в частности диабетическую нейропатию лечат препаратами альфа-липоевой кислоты. Перспективный препарат для терапии диабетических невропатий — канитин. Однако основное лечение при сахарном диабете заключается в контроле уровня глюкозы [6] .
- При комплексной терапии применяют препараты с витаминами. Высокие дозы принимают не более месяца.
- При возникновении болевого синдрома используют противосудорожные препараты, трициклические антидепрессанты. Их противоболевое действие связано с блокированием болевого импульса в головном мозге и устранением болевой «памяти». К физическим методам воздействия относят магнитотерапию, лазеротерапию, электрофорез с прозерином, элетростимуляцию ослабленных мышц, иглотерапию [17][16] .
- Для лечения хронической демиелинизирующей полирадикулониейропатии применяют иммуносупрессивные препараты. Иногда при терапии на первый план выходит уменьшение боли.
- При синдроме Гийена — Барре необходима госпитализация в многопрофильную больницу с отделением реанимации и интенсивной терапии, в тяжёлых случаях — вентиляция лёгких, мониторинг ЭКГ и артериального давления, введение гепарина для предупреждения тромбоза глубоких вен и лёгочной эмболии. При выраженных болях вводят опиоидные анальгетики, антиконвульсанты, проводят лечебную физкультуру, организуют рациональное (зондовое) питание. Патогенетическая терапия включает использование плазмафереза, введение иммуноглобулинов, кортикостероидную терапию. При синдроме Гийена — Барре иммунотерапия ускоряет выздоровление, но не влияет на окончательный прогноз [16][17] .
- Для достижения долгосрочной ремиссии при системном васкулите, не связанном с вирусами, применяют кортикостероиды и циклофосфамид. Продолжительность терапии кортикостероидами может быть более двух лет [1][17] .
- Лечение нейропатий, вызванных приёмом противоопухолевых препаратов, является сложной задачей. Общепризнанной профилактической или лечебной стратегии до сих пор не существует [15][18] .
Прогноз. Профилактика
Невропатия зачастую развивается достаточно медленно. Пациенты сообщают о неврологических проявлениях врачу спустя годы после её формирования. О симптомах симметричной полинейропатии лечащий врач узнаёт в среднем через 39 месяцев. В таком случае лечение может быть запоздалым, а повреждение нерва необратимым [5] .
При синдроме Гийена — Барре прогноз ухудшают пожилой возраст, быстрое развитие заболевания, потеря аксонов. Восстановление может занять несколько месяцев и быть неполным. Приблизительно у 15 % пациентов с синдромом Гийена — Барре сохраняются остаточные параличи [16] [17] .
Васкулитная нейропатия развивается с разной скоростью. Заболевание может протекать как в прогрессирующей хронической форме, так и в рецидивирующей с длительными периодами ремиссии.
Прогноз при сахарном диабете зависит от поддержания оптимального уровня сахара в крови. Приверженность лечению позволяют замедлить развитие нейропатии.
Прогноз после травмы периферической нервной системы плохой. При повреждении эндоневральной трубки (внешнего слоя соединительной ткани, окружающей периферические нервы) пациенты редко восстанавливаются полностью [17] .
После терапии противоопухолевыми средствами нейропатия может сохраняться несколько лет [18] . Обратимость патологии остаётся под вопросом, особенно при приёме противораковых препаратов на основе платины и таксанов. Для уменьшения тяжести симптомов онкологи могут снизить дозировку или прекратить применение нейротоксических противоопухолевых препаратов [15] [18] .
Не все нейропатии можно предотвратить. Однако часть нарушений возможно избежать или отсрочить их появление на несколько лет. Это в первую очередь относится к эндокринным нейропатиям, например диабетической, и нейропатии, вызванной дефицитом витаминов в организме.
Что такое неврит зрительного нерва? Причины возникновения, диагностику и методы лечения разберем в статье доктора Зубковой Екатерины Андреевны, офтальмолога со стажем в 12 лет.
Над статьей доктора Зубковой Екатерины Андреевны работали литературный редактор Вера Васина , научный редактор Сергей Цыганок и шеф-редактор Маргарита Тихонова

Определение болезни. Причины заболевания
Неврит зрительного нерва (Optic neuritis) — это воспаление зрительного нерва. При заболевании резко снижается зрение, сужается его поле и нарушается восприятие цветов. Перед глазами появляются пятна и мерцания, в глазничной области возникает боль, которая усиливается при движениях глаза [2] .
Среди всех глазных болезней поражения зрительного нерва встречаются в 3,2 % случаев [6] .
Зрительный нерв — это нетипичный черепно-мозговой нерв, который содержит около 1 млн нервных волокон. Он представляет собой белое вещество головного мозга, вынесенное на периферию. Его длина составляет 35–55 мм [1] . По нему зрительная информация, воспринятая клетками сетчатки, передаётся в головной мозг.
Отростки нервных клеток собираются со всей сетчатки и образуют диск зрительного нерва. Затем они направляются к головному мозгу, перекрещиваются с нервными волокнами второго глаза и формируют зрительный перекрёст. От него начинается зрительный тракт, который заканчивается в первичных подкорковых зрительных центрах.
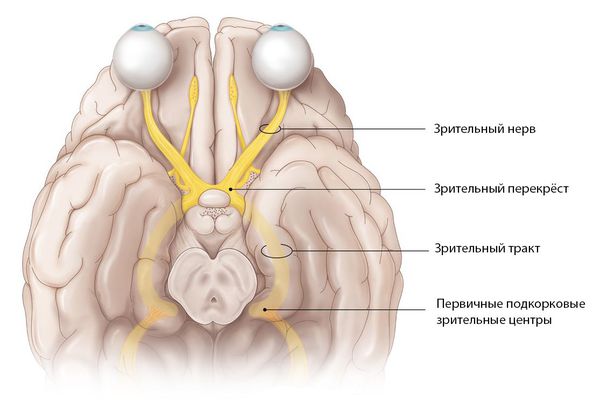
Зрительный нерв подразделяется на несколько частей:
- внутриглазная часть и головка зрительного нерва;
- ретробульбарная часть (за глазом), или орбитальная;
- внутриканальцевая;
- внутричерепная.
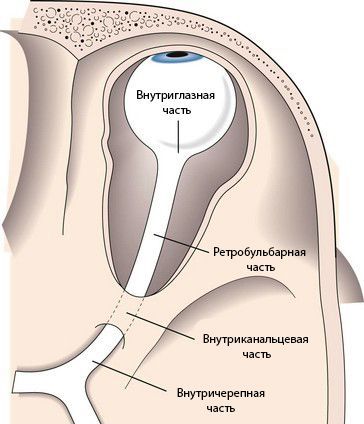
Длина внутриглазной части зрительного нерва составляет 25–35 мм. В горизонтальной плоскости нерв S-образно изгибается, благодаря чему при движениях глазного яблока он не натягивается.
К внутриглазной части относится диск зрительного нерва. В нём соединяются оптические волокна сетчатки, а из центра выходят сосуды: узкие светло-красные артерии и более тёмные толстые вены.
Ретробульбарная или орбитальная часть — это участок зрительного нерва длиной 25–35 мм. Начинается от области, где нерв выходит из глазного яблока, и продолжается до входа в зрительный канал.
Внутриканальцевая часть зрительного нерва заключена в зрительный канал. Её длина составляет около 6 мм, нерв здесь фиксирован к стенке канала.
Внутричерепная часть зрительного нерва переходит в перекрёст зрительных нервов. Длина этого участка в среднем составляет 10 мм. Внутричерепной отдел особо уязвим при патологиях прилежащих структур, например аденоме гипофиза или аневризме. При таких нарушениях зрительный перекрёст может сдавливаться, из-за чего сужаются поля зрения и атрофируется зрительный нерв. Если повреждается сосуд зрительного нерва, то пациент перестаёт видеть одним глазом [2] . Также встречается гемианопсия — слепота обоих глаз в половине поля зрения.
При неврите воспаляются ствол и оболочки зрительного нерва в различных его отделах. Если процесс распространяется на диск зрительного нерва, то такое воспаление называют внутриглазным невритом или папиллитом. Когда процесс протекает за глазом, то это ретробульбарный неврит зрительного нерва [3] .
Причины неврита зрительного нерва
Точную причину заболевания выяснить удаётся не всегда, но чаще всего к воспалению зрительного нерва приводят:
-
— это самая распространённая причина неврита зрительного нерва;
- другие аутоиммунные заболевания, такие как синдром Шегрена, системная красная волчанка;
- нейромиелит зрительного нерва — демиелинизирующее заболевание, которое поражает преимущественно глаза и спинной мозг;
- демиелинизирующие заболевания, связанные с сывороточными иммуноглобулинами G к миелин-олигодендроцитарному гликопротеину (MOG-IgG) — например, острый рассеянный энцефаломиелит ;
- гранулематозные болезни — саркоидоз, гранулематоз с полиангиитом[13] ;
- воспалительные заболевания головного мозга — энцефалит, арахноидит, менингит , абсцесс мозга и др.;
- острые и хронические общие инфекции — туберкулёз, болезнь Лайма, сифилис, бруцеллёз, тиф, рожа, грипп, оспа и др.;
- воспалительные заболевания глаз и орбиты;
- интоксикации свинцом или метиловым спиртом, у детей возможна глистная интоксикация;
- проникающие ранения глаза и орбиты;
- черепно-мозговые травмы.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы неврита зрительного нерва
Основные жалобы пациентов при неврите:
- резко снижается зрение и сужаются его поля;
- нарушается способность воспринимать цвета и различать тона;
- перед глазами постоянно или периодически появляются пятна или мерцания;
- в глазничной области возникает боль, которая усиливается при движениях глаза [2] ;
- нарушается зрачковая реакция на поражённом глазу.
Внутриглазной неврит (папиллит) — это воспаление внутриглазной части зрительного нерва. Заболевание, как правило, начинается остро: зрение ухудшается за пару часов (чаще всего одного глаза), реже за нескольких суток. Потеря зрения сопровождается умеренной головной болью и болью при движении глаз, но этих симптомов может и не быть. Обычно зрение перестаёт ухудшаться через 7–10 дней, а через 2–3 недели восстанавливается. Но если пациент не выздоравливает, то длительный отёк приводит к атрофии нервных волокон и потере зрения [4] .
Папиллит — это самый распространённый вид неврита у детей, но может встречаться и у взрослых [7] .
Ретробульбарный неврит — это воспаление участка зрительного нерва, расположенного между глазным яблоком и зрительным перекрёстом.
Чаще всего ретробульбарный неврит развивается при демиелинизирующих заболеваниях, в 80 % случаев он является первым признаком рассеянного склероза. Но может возникать при инфекционных заболеваниях и отравлениях, например метиловым спиртом.
Ретробульбарный неврит может протекать в острой форме (чаще при инфекциях) и в хронической (при отравлениях токсинами). Одностороннее поражение обычно протекает в острой форме, двустороннее — в хронической. При надавливании на глаз и его движениях 90 % пациентов чувствуют боль за глазным яблоком. Часто нарушается цветовое зрение и быстро возникает цветовое утомление, т. е. чувствительность глаза к цветам снижается, оттенки быстро тускнеют. Сильно падает острота зрения: пациент перестаёт различать предметы и видит только свет. В поле зрения появляются скотомы различных размеров — участки полного или частичного выпадения зрения, которые не связаны с периферическими границами.

При аксиальном неврите возникает центральная скотома размером 2–10 ° и более. Она может объединяться с частичными выпадениями полей зрения, которые примыкают к точке фиксации взора. Также в поле зрения могут возникать периферические дефекты.
При периферической форме неврита поле зрения имеет концентрический характер, т. е. сужается по всему периметру.
При трансверсальной форме неврита зрение снижается очень сильно, вплоть до слепоты. Скотомы сливаются с периферическими выпадениями поля зрения. Характерная особенность такого неврита — отсутствие изменений при смотре глазного дна в начале заболевания [4] .
Патогенез неврита зрительного нерва
Зрительный нерв состоит из миллиона нервных волокон. Снаружи они покрыты специальным веществом — миелином, который облегчает проведение нервного импульса к мозгу. Наиболее частой причиной неврита являются демиелинизирующие заболевания, при которых зрительный нерв разрушается клетками иммунной системы.
Иммунитет уничтожает вирусы и бактерии, которые вызывают инфекционные болезни. При аутоиммунных заболеваниях наша иммунная система принимает собственные ткани организма за чужеродные и разрушает их. При неврите иммунная система атакует миелиновую оболочку, которая покрывает зрительный нерв.

Острый неврит зрительного нерва может развиться из-за вирусной инфекции, которой пациент болел несколько лет назад или больше. До конца неизвестно, что именно в таких случаях приводит к поражению зрительного нерва. Вероятно, заболевание развивается у людей с определённым типом иммунной системы.
Воспаление при неврите протекает на стволе и оболочках зрительного нерва и ощущается пациентом как дискомфорт, особенно при движениях глаз. Из-за воспаления возникает отёк и инфильтрация — накопление в тканях клеточных элементов и жидкости. В результате этого зрительные волокна сдавливаются, их клетки разрушаются и зрение ухудшается.
Когда воспаление проходит, часть нервных волокон восстанавливается, поэтому зрение улучшается. Если болезнь протекает тяжело, то нервные волокна распадаются, зрительный нерв атрофируется и зрение утрачивается необратимо [4] . В редких случаях в патологический процесс может вовлекаться зрительный нерв другого глаза, место перекрёста зрительных нервов или другие ткани мозга [5] .
Классификация и стадии развития неврита зрительного нерва
Код неврита зрительного нерва по МКБ-10 (Международной классификации болезней): H46.
Выделяют следующие виды неврита:
- внутриглазной неврит (папиллит) — это воспаление диска зрительного нерва;
- ретробульбарный неврит — это воспаление зрительного нерва на участке между глазным яблоком и перекрёстом .
В зависимости от того, где расположено воспаление, выделяют три формы ретробульбарного неврита:
- трансверсальный неврит — поражены все группы волокон зрительного нерва;
- периферический — страдают волокна нервного ствола, воспаление обычно начинается в мягкой мозговой оболочке и переходит на периферические волокна;
- аксиальный — воспаление осевого пучка зрительного нерва [4] .
Осложнения неврита зрительного нерва
Заболевания, связанные с воспалением нервной системы, могут вызвать необратимые изменения в организме. Чем дольше продолжается воспалительный процесс, тем они тяжелее.
Возможные осложнения при неврите зрительного нерва: атрофия тканей, ухудшение зрения или его полная потеря. У многих пациентов через некоторое время зрение полностью восстанавливается. Но при тяжёлом течении миелиновая оболочка разрушается, что приводит к необратимой потере зрения [2] [3] .
Диагностика неврита зрительного нерва
Сбор анамнеза
Диагностика начинается с опроса пациентов. К типичным жалобам относятся:
- перед глазом появился « туман » , « пятно » или « сетка » , которые со временем темнеют;
- зрение ухудшалось постепенно, чаще за 1–3 дня, реже в течение недели;
- выпадают отдельные участки поля зрения, или ограничено периферическое зрение;
- ухудшилось восприятие цветов;
- появилась боль при движениях глаз, что характерно для периферической формы ретробульбарного неврита.
Врач уточняет у пациента:
- поражены оба глаза или только один;
- когда появились симптомы и сколько длятся;
- признаки болезни возникли впервые или появляются периодически;
- имеются ли общие или локальные заболевания.
Внешний осмотр и пальпация
При наружном осмотре зачастую изменения не выявляются. При ретробульбарном неврите глазное яблоко может быть смещено вперёд, движения глаза ограничены и вызывают боль.
Инструментальные методы исследования
- Определение остроты зрения: центральное зрение не нарушается при периферической форме ретробульбарного неврита, но резко ухудшается при аксиальной. При трансверсальной форме зрение снижается до сотых долей, т. е. от 0,09 и меньше, вплоть до слепоты.
- Исследование цветоощущения проводится по полихроматическимтаблицам Рабкина , на которых изображены фигуры, цифры или буквы. Они составлены из кружков одного тона, но разной насыщенности и располагаются на фоне, состоящем из кругов других близких цветов.

- Биомикроскопия — осмотр переднего отрезка глаза. Проводится, чтобы исключить патологию этого участка.
- Измерение внутриглазного давления — оно повышается при заболеваниях, которые могут послужить причиной неврита, или при сопутствующей глаукоме .
- Офтальмоскопия под мидриазом — осмотр глазного дна, перед которым в глаза закапывают специальные капли, расширяющие зрачки. Обследование проводится в зелёном свете, чтобы точнее выявить отёк диска зрительного нерва и кровоизлияния на нём. В начале болезни изменений может не быть, первые признаки появятся только через несколько недель. Время их появления зависит от удалённости инфекционного очага и воспаления глазного яблока. В этот период врачу следует быть особенно внимательным, чтобы избежать ошибочного диагноза, так изменений на диске зрительного нерва нет. Как и в норме, диск имеет форму правильного круга диаметром 1,5–2 мм, цвет бледно-розовый, границы в норме чётко очерчены. Только спустя время, когда воспаление достигнет глазного яблока и распространится по нервному волокну, можно заметить покраснение диска, его границы становятся размытыми, диаметр сосудов изменяется, появляются кровоизлияния [8] .
- Исследование зрачковой реакции на свет.
- Компьютерное исследование полей зрения по 120 точкам.
- Исследование полей зрения методом кинетической периметрии.
Дополнительные методы диагностики для уточнения диагноза
- электрофизиологические методы — исследование зрительных вызванных потенциалов (позволяет понять , как головной мозг реагирует на различные зрительные стимулы ) и порога электрической чувствительности сетчатки ( чем больше площадь дефектов поля зрения, тем ниже электрическая возбудимость сетчатки);

- УЗИ глаз;
- когерентная томография зрительного нерва;
- МРТ орбиты и головного мозга;
- флюоресцентная ангиография сетчатки.
Лабораторные исследования
Гистологические, иммунологические и биохимические методы позволяют уточнить диагноз при туберкулёзе, ревматоидном артрите , сифилисе и других заболеваниях. К таким анализам также относятся тест на ВИЧ, анализ на ревматоидный фактор и др. [4] [8]
Лечение неврита зрительного нерва
Если диагноз подтверждён, то пациента срочно госпитализируют. Лечение консервативное, его цель — подавить инфекции, уменьшить воспалительный отёк и аллергические реакции, улучшить обмен веществ в тканях центральной нервной системы.
Для лечения неврита применяются:
- Антибиотики широкого спектра действия. Их назначают, если причиной неврита являются бактериальные инфекции.
- Глюкокортикоиды уменьшают аллергические реакции, воспаление, отёк и усиливают иммунный ответ клеток. Может применяться Дексаметазон, но важно знать, что местное применение глюкокортикоидов без внутривенного и перорального введения не работает [11] . При неврите, который вызван аутоиммунными заболеваниями, применяют метод пульс-терапии: внутривенно каждые 6 часов в течение 3–5 дней вводят большие дозы Метилпреднизолона. Затем глюкокортикоиды применяют внутрь в дозе 1 мг/кг. В РФ доза глюкокортикоидов, применяемых перорально, часто занижена, в результате побочных эффектов больше, чем пользы. Вместе с глюкокортикоидами назначаются ингибиторы протонной помпы.
Хорошие результаты показывает лечение внутривенным иммуноглобулином (IVIg) и плазмаферез (PLEX), но широко эти методы пока не применяются [14] .
В РФ иногда назначают противоаллергические препараты, мочегонные средства, физиотерапию и нестероидные противовоспалительные препараты (НПВС), но в зарубежных руководствах таких рекомендаций нет. Более того, описаны случаи, когда приём НПВС становился причиной неврита зрительного нерва [12] .
Одновременно с лечением неврита выясняют его причины. После уточнения диагноза проводится специфическое лечение основного заболевания, например операция при синусите, специфическая терапия туберкулёза или противовирусная терапия герпеса [9] .
Прогноз. Профилактика
При инфекционно-токсическом неврите зрительного нерва прогноз благоприятный: в 75–90 % случаев зрение полностью восстанавливается [4] .
При воспалении диска зрительного нерва (папиллите) пациент нетрудоспособен примерно 15–28 дней. При правильном лечении зрение значительно или полностью восстанавливается.
Прогноз хуже при неврите, вызванном аутоиммунными болезнями, а также коллагенозами, саркоидозом, специфическими инфекциями и демиелинизирующими заболеваниями. Зрительные нарушения прогрессируют в течение 7–10 дней. Зрение редко восстанавливается полностью, часто случаются рецидивы, может частично атрофироваться зрительный нерв.
Профилактика неврита зрительного нерва
Чтобы избежать воспаления зрительного нерва, нужно предупреждать и вовремя лечить инфекционные заболевания. При хронических болезнях необходимо регулярно посещать офтальмолога, невролога, отоларинголога, терапевта и других профильных врачей [2] [4] .
Читайте также:

