Мумие при красной волчанке
Обновлено: 24.04.2024
За последние два десятилетия благодаря рациональному использованию кортикостероидных гормонов (КГ) и цитотоксических иммунодепрессантов (ЦИ) удалось значительно улучшить жизненный прогноз больных системной красной волчанкой (СКВ). Проведение пульс-терапи
За последние два десятилетия благодаря рациональному использованию кортикостероидных гормонов (КГ) и цитотоксических иммунодепрессантов (ЦИ) удалось значительно улучшить жизненный прогноз больных системной красной волчанкой (СКВ). Проведение пульс-терапии метилпреднизолоном (МП) и циклофосфаном (ЦФ) у больных с волчаночным нефритом, поражением центральной нервной системы (ЦНС) и цитопеническим кризом способствует ускорению сроков достижения клинического улучшения. Патофизиологическим обоснованием для применения ударных доз метилпреднизолона является его способность активно влиять на систему иммунитета и подавлять воспалительные реакции. Один из важнейших эффектов ударных доз КГ — подавление активности нейтрофилов и моноцитов и способность вызывать транзиторную перераспределительную лимфопению. Угнетающее воздействие мегадоз кортикостероидов на функцию В-лимфоцитов приводит к стойкому снижению продукции иммуноглобулинов, а следовательно, и аутоантител, а также к уменьшению образования патологических иммунных комплексов. Из других важных компонентов механизма действия ударных доз КГ заслуживают внимания воздействие на систему цитокинов-интерлейкинов-1,6, фактора некроза опухоли, металлопротеиназ и липокортина, ингибиция экспрессии и функциональной активности Fc и СЗ рецепторов мононуклеарных фагоцитов.
Однако далеко не во всех случаях классическая ПТ позволяет быстро и надежно решать сложнейшие вопросы лечения в критических ситуациях и прогностически неблагоприятных вариантах течения СКВ. В настоящее время достаточно четко выявляется особая группа риска. В эту группу в первую очередь включаются пациенты с развитием СКВ в подростковом возрасте, быстропрогрессирующим волчаночным нефритом с диффузным поражением клубочкового аппарата и «полулуниями», стойкой артериальной гипертензией и азотемией, быстрым развитием нефротического синдрома в молодом возрасте, церебропатией с судорожным синдромом и комой, поперечным миелитом, геморрагическим пневмонитом, тромбоцитопенией, генерализованным поражением кожи и слизистых оболочек с развитием некрозов, сопровождающихся криоглобулинемией, гипокомплементемией и высоким уровнем антиядерных антител. Огромное значение в оценке жизненного прогноза у этой группы пациентов имеет своевременное назначение патогенетической терапии.
Консервативная терапия с использованием подавляющих доз преднизолона и цитостатиков, назначаемых внутрь, у некоторых больных улучшает клиническую картину, но почти не влияет на жизненный прогноз, особенно в случаях прогрессирующего волчаночного нефрита, церебрального криза и геморрагического пневмонита. Однократное трехдневное применение ПТ МП может за сравнительно короткое время уменьшить клиническую и лабораторную активность при нефротическом синдроме. Однако 5-летняя выживаемость пациентов, как правило, не превышает 60%. Другими словами, ударные дозы МП прекрасно зарекомендовали себя в качестве фактически ургентной терапии, с успехом применяющейся в ситуациях, непосредственно угрожающих жизни пациента, при нарастании симптоматики и в случаях неэффективности или невозможности использования консервативной схемы лечения.
Практически при всех прогрессирующих хронических заболеваниях, в том числе и аутоиммунных, жизненный и социальный прогноз в огромной степени зависит от системного, программного подхода к терапии.
Различные схемы и программы интенсивной терапии у больных СКВ стали появляться уже с середины 80-х годов и сводились к назначению ПТ в ежемесячном режиме в течение полугода. Несколько позже появилась схема программного назначения ПТ в комбинации с циклофосфаном: 1 г циклофосфана может быть добавлен к стандартной пульс-терапии обычно на 2-3-й день лечения или дополнительно к метипреду при ежемесячном режиме. Показанием для комбинированного использования циклофосфана и метипреда является манифестная высокоактивная СКВ с выраженными иммунологическими нарушениями. Программное применение пульс-терапии ЦФ у больных быстро прогрессирующим люпус-нефритом впервые в стране предложила группа исследователей во главе с профессором И. Е. Тареевой. Согласно этой методике, ЦФ вводится внутривенно из расчета 1 г на 1 м 2 поверхности тела 1-2 раза в месяц в течение года. По сравнению с пероральным назначением ЦФ эта программа позволяет добиться хороших и стабильных результатов более чем у 70% больных с прогрессирующим нефритом. Особенно важным представляется то, что внутривенное введение мегадоз ЦФ оказывает значительно меньшее токсическое воздействие на эпителий мочевого пузыря и костный мозг, практически не вызывая геморрагических циститов и агранулоцитоза.
Другое направление интенсивной терапии ревматических заболеваний — экстракорпоральные методы лечения: плазмаферез (ПФ) и практически все сорбционные технологии, гемо- и плазмосорбция. В современном исполнении ПФ осуществляется с помощью центрифужной или мебранной технологии с удалением 40-60 мл плазмы на 1 кг веса больного. Для замещения потери белка используется альбумин или свежезамороженная плазма. Стандартные курсы ПФ состоят из 3-6 процедур, проводимых последовательно или с короткими интервалами, с суммарной эксфузией плазмы до 15 л.
Интерес к ПФ у ревматологов возник на рубеже 60-80-х годов после фундаментальных исследований, посвященных иммунокомплексной природе СКВ, изучению механизмов иммунокомплексного поражения органов и тканей и патогенетической роли антител к нативной ДНК. Представлялось вполне рациональным уменьшить степень тканевых повреждений за счет удаления из циркуляции иммунных комплексов (ЦИК), антител к ДНК (а-ДНК), криоглобулинов и цитокинов.
Первые попытки применения терапевтического ПФ у больных СКВ продемонстрировали возможности этого метода в первую очередь в ситуациях, когда кортикостероидная и иммуносупрессивная терапия оказывается неэффективной, при наличии высокого уровня ЦИК, а-ДНК, криоглобулинемии, цитопениях. Выявлена прямая зависимость между адекватным удалением из циркуляции патологических белковых структур и клиническим эффектом, изучены механизмы деблокирования РЭС и повышения естественного клиренса.
Эффективность плазмафереза (от нескольких процедур до многократно повторяемых серий при неблагоприятном течении СКВ) хорошо известна и доказана в ходе многочисленных, в основном зарубежных, исследований 80-90-х годов. Пока не получено убедительных данных об эффективности ПФ у больных люпус-нефритом. Результаты проведенных в США и Канаде открытых и контролируемых испытаний весьма противоречивы.
Изолированное применение ПФ при СКВ в большинстве случаев существенно ограничено развитием так называемого синдрома рикошета, возникающего непосредственно после удаления достаточно большого объема плазмы. Резкое повышение уровня аутоантител в ближайшие дни после процедуры — «рикошет» — связывается со стимуляцией лимфоцитов, продуцирующих аутоантитела по принципу обратной связи. Обычно лабораторный «рикошет» сопровождается обострением клинической картины, что в целом производит впечатление терапевтической неудачи. Логичными представляются два выхода из этой ситуации. Первый — сокращение времени между процедурами и проведение длительных серий ПФ в течение нескольких месяцев или даже лет. Второй, по-видимому, более рациональный и эффективный способ достижения стойкого клинического эффекта при назначении ПФ у больных СКВ — комбинирование экстракорпоральных методов и пульс-терапии МП и ЦФ в синхронном режиме.
Идея синхронной ИТ материализовалась уже в 80-х годах и является практически неотъемлемой частью лечения некоторых системных васкулитов, синдрома Гудпасчера, Вегенера, Хаммана-Ричи, криоглобулинемической пурпуры и поражения центральной и периферической нервной системы при болезни Шегрена. Первые успешные попытки применения синхронной ИТ у больных СКВ были предприняты в 1984 году в Японии, России и Германии: за рубежом — плазмаферез в комбинации с ЦФ, в России — ПФ в комбинации с пульс-терапией МП и ЦФ.
В Институте ревматологии начиная с середины 80-х изучалась эффективность синхронного применения ПФ и пульс-терапии МП и ЦФ у 56 больных СКВ с неблагоприятным жизненным прогнозом. Методика проведения синхронной интенсивной терапии (СИТ) заключалась в следующем: в течение первого месяца больным проводились три процедуры ПФ с удалением не менее 1500 мл плазмы за сеанс, интервалы между процедурами составляли 5-6 дней. После каждой процедуры назначался внутривенно 1 г метипреда, а после второй процедуры к МП добавлялся 1 г ЦФ. Далее в течение года через каждые 3 месяца проводилась одна процедура ПФ с последующим введением 1 г МП и 1 г ЦФ. Основу группы составляли молодые женщины, в подавляющем большинстве с небольшим сроком заболевания, с развернутой клиникой СКВ. Почти у каждого пациента наблюдался прогрессирующий волчаночный нефрит, более чем у половины — нефротический синдром, церебропатия, у трети больных на фоне криоглобулинемии наблюдался распространенный генерализованный васкулит кожи и слизистых оболочек. Высокая клиническая активность сопровождалась значительным повышением уровня антител к ДНК, ЦИК и гипокомплементемией.
Особо следует подчеркнуть, что у половины больных этой группы стандартная терапия, включавшая в себя массивные дозы кортикостероидов и иммунодепрессантов, была неэффективной, а почти трети пациентов адекватная терапия вообще не проводилась.
Многолетнее наблюдение за этой группой больных по окончании 12-месячной СИТ позволило сделать заключение о ее высокой эффективности. Среди этих пациентов 5-летняя выживаемость составила 81%. Наиболее показательными оказались результаты применения СИТ в группе из 12 подростков, у которых течение волчанки, как правило, приобретает фатальный характер. За весь период наблюдения состояние, близкое к клинико-лабораторной ремиссии, было отмечено у 8 из 12 больных, у 2 пациентов эпизодически наблюдались кратковременные обострения СКВ. Ежедневная доза преднизолона составляла от 2,5 до 15 мг, у одной пациентки кортикостероиды были полностью отменены. Большинству больных удалось вернуться к нормальной жизни, учебе, посильной работе, некоторые пациентки вышли замуж и имеют здоровых детей.
Таким образом, программа синхронной интенсивной многомесячной терапии оказывает значительное влияние на клинико-лабораторные проявления и существенно улучшает жизненный и социальный прогноз у больных СКВ с прогностически неблагоприятным вариантом течения. Синхронное назначение ПФ и внутривенное введение ударных доз МП и ЦФ могут использоваться по жизненным показаниям в случаях так называемого волчаночного криза — при тромбоцитопенической пурпуре, церебральной коме, развитии тромбозов, инфарктов и инсультов у больных с антифосфолипидным синдромом и геморрагическим пневмонитом. В этих ситуациях проведение СИТ обычно ограничивается 3-4 последовательными процедурами — вплоть до купирования ургентной ситуации. В случаях с заведомо неблагоприятным долгосрочным жизненным прогнозом — прогрессирующий гломерулонефрит или поражение ЦНС, язвенно-некротический васкулит, острое начало болезни у подростка — требуется проведение длительных программ СИТ.
Нам представляется, что возможности программной СИТ далеко не исчерпаны. Перспективным может оказаться добавление в схему внутривенного иммуноглобулина, моноклональных антител и интерферонов, применение которых способно блокировать образование аутоантител и патологических ЦИК. Весьма актуальным остается индивидуальный подбор программы с более частым (ежемесячным, еженедельным) назначением плазмафереза и ПТ. Особенно важным аспектом, обеспечивающим возможность проведения более длительных и полноценных курсов экстракорпоральных процедур, является внедрение новых технологий обработки плазмы, таких, как каскадная фильтрация и иммуносорбция, применение которых позволяет сводить к минимуму потерю альбумина и селективно удалять из циркуляции патологические аутоантитела и иммунные комплексы.
Системную красную волчанку лечит ревматолог. На фоне терапии антималярийными (гидроксихлорохин, хлорохин) препаратами необходимо наблюдение офтальмолога. При подозрении на развитие плоскоклеточного рака кожи на фоне дискоидной формы красной волчанки необходима консультация онколога.
Высыпания красной волчанки на коже и/или слизистых могут быть самостоятельным заболеванием или проявлением системной красной волчанки — хронического заболевания, связанного с формированием антител к компонентам ядер клеток. Антитела вызывают повреждение и воспаление разных тканей, в том числе и кожи.
Формы и осложнения
Кожные проявления красной волчанки включают три группы, в каждую входят специфические кожные проявления:
- острая кожная красная волчанка (локализованная, генерализованная и подобная токсическому эпидермальному некролизу);
- подострая кожная красная волчанка (кольцевидная, папулосквамозная, лекарственно индуцированная, эритродермическая, пойкилодермическая, везиклобулезная, синдром Роуэлл);
- хроническая кожная красная волчанка (дискоидная, отечная, панникулит, перниоподобная, лихеноидная).
Выделение этих форм обусловлено не только продолжительностью течения кожного заболевания, но также отражает связь с системной красной волчанкой.
Чаще всего проявлением системного заболевания являются острые формы, тогда как дискоидная форма наблюдается только в 5-15% всех случаев. Чем дольше кожные проявления существуют изолированно, тем меньше риск формирования системной формы заболевания. Риск системного заболевания при наличии кожных проявлений выше у женщин и детей.
Высыпания красной волчанки могут возникать у детей (антитела передаются плоду) от матерей с системной красной волчанкой. Такая форма называется неонатальной волчанкой, возникает в течение первых двух месяцев жизни ребенка и может быть первым признаком системной красной волчанки у мамы.
В комплекс системной красной волчанки могут входить и другие, неспецифичные исключительно для этого заболевания, изменения кожи и ее придатков.
Причины возникновения
Причины развития заболевания не ясны, но предполагается значение следующих факторов:
- ультрафиолетовое излучение (почти 50% людей, страдающих волчанкой, светочувствительны);
- некоторые лекарства;
- вирусы;
- наследственность;
- гормональные влияния;
- курение;
- переохлаждение.
Симптомы
Кожные проявления красной волчанки многообразны. Знаковым проявлением, почти всегда ассоциированным с системным заболеванием, являются высыпания на лице, по форме напоминающие бабочку: с крыльями — на скулах и щеках и туловищем — на переносице и спинке носа. Высыпания могут проявляться возвышающимися или залегающими в глубине тканей элементами розового и синюшно-красного цвета. Имеется тенденция к формированию кольцевидных очагов, покрытых очень плотными, болезненными при снимании чешуйками. В ряде случаев формируется так называемая ознобленная красная волчанка, при которой болезненные ярко-красные синюшные узелки возникают на пальцах ног, рук, носу, ушах в холодную погоду. Повреждение сосудов сопровождается появлением высыпаний, напоминающих синяки, расширенные сосуды могут просвечивать в ногтевых ложах. Некоторые пациенты с СКВ имеют симптомы, напоминающие красный плоский лишай.
Бывают и тяжелые поражения с формированием пузырей и отслаиванием кожи, что больше характерно для начала системного заболевания. Изменения могут затрагивать слизистые оболочки, особенно часто это слизистая губ, полости рта. Очаги волчанки на голове могут проявляться потерей волос. Возможно и диффузное выпадение, и разрежение волос.
Стадии протекания
Обострения чаще возникают в весенне-летнее время в период интенсивного солнечного излучения.
Лечение кожной красной волчанки
Основой лечения служат кортикостероидные гормоны. При этом заболевании они могут наноситься на очаги в виде мазей, вводиться с помощью инъекций непосредственно в очаг пораженной кожи. В тяжелых случаях возможно назначение системных кортикостероидов. В качестве альтернативы или для усиления терапии возможно нанесение на очаги препаратов ингибиторов кальциневрина.
В случаях тяжелого поражения кожи, недостаточном эффекте от наружного лечения проводится системная терапия с использованием антималярийных препаратов (хлорохин, гидроксихлорохин), противовоспалительных препаратов (метотрексат, микофенолат, дапсон, азатиоприн и др.).
Особенности методики лечения
Первой линией терапии является назначение наружных кортикостероидов и гидроксихлорохина.
Для уменьшения общей дозы и побочных эффектов наружных кортикостероидов в лечение включаются ингибиторы кальциневрина.
В период лечения гидроксихлорохином необходим регулярный контроль врача. Обязательно проводится контроль состояния сетчатки, так как препарат при длительном (более 5 лет) применении может нарушить зрение. Этот побочный эффект встречается нечасто, но появление признаков повреждения сетчатки может потребовать отмены препарата.
Внутриочаговое введение лекарственных средств (кортикостероидных гормонов) при помощи множества поверхностных уколов непосредственно в очаг пораженной кожи позволяет создать высокую концентрацию лекарства в очаге, уменьшив при этом риски системных побочных эффектов. Лекарство вводится врачом в условиях перевязочного кабинета на глубину 2-3 мм. Процедура является болезненной, но боль не резкая, во многом зависит от чувствительности рецепторов пациента. Для уменьшения боли используется тонкая игла, возможно использование мази с анестетиком.
Всем пациентам обязательно назначаются средства защиты кожи от ультрафиолета.
Как происходит лечение красной волчанки в клинике Рассвет
Дерматолог попросит рассказать о течении заболевания и лечении, которое проводилось ранее. Врач осмотрит кожу (в том числе волосистую часть головы), слизистые оболочки. Информативным может быть проведение дерматоскопии, трихоскопии. При этом заболевании для установления диагноза в большинстве случаев потребуется проведение биопсии кожи с дополнительным проведением реакции иммунофлуоресценции.
При подозрении на кожную красную волчанку необходимо будет обсудить возможность системных проявлений, оценить состояние других органов и систем организма. Могут потребоваться дополнительные исследования для выявления системного процесса (анализы крови, мочи и др.).
Рекомендации пациентам
Соблюдайте режим фотозащиты:
- избегайте прямых солнечных лучей, не находитесь на улице в период интенсивного солнечного излучения (примерно с 11 до 17 часов дня, в зависимости от региона и времени года часы могут отличаться);
- носите головные уборы с широкими полями, одежду с длинными рукавами и штанинами, закрытым декольте;
- используйте фотозащитные средства широкого спектра с SPF 30 и выше.
Если вы курите, желательно избавиться от этой привычки.
Если очаги находятся на открытых участках кожи, возможно использование средств медицинского камуфляжа.
Если вы планируете беременность, обсудите с лечащим врачом возможные риски. Желательно дождаться исчезновения симптомов — на протяжении не менее 6 месяцев.
Прогноз при кожных формах красной волчанки в большинстве случаев благоприятный! Помните о возможном риске развития на фоне очагов плоскоклеточного рака кожи и соблюдайте рекомендованный врачом график наблюдения.
Ларингофарингеальный рефлюкс (ЛФР) — это заброс желудочного содержимого (кислоты и таких ферментов, как пепсин) в гортань, приводящий к появлению охриплости, ощущению кома в горле, затруднению глотания, кашлю, ощущению слизи в гортаноглотке.
Рефлюкс, как причина вышеописанных симптомов без гастроэзофагеальной рефлюксной болезни (ГЭРБ), постоянно ставится под сомнение. Руководства, выпущенные специализированными обществами в области ларингологии и гастроэнтерологии, представляют разные точки зрения. Обе группы признают, что интерпретация существующих исследований затрудняется из-за неопределенных диагностических критериев ЛФР, различных показателей ответа на лечение и значительного эффекта плацебо при проводимом лечении.
Имеются относительно ограниченные данные о распространенности ЛФР: примерно у 30% здоровых людей могут фиксироваться эпизоды рефлюкса на суточной pH-метрии или обнаруживаться характерные изменения в гортани.
ЛФР может прямо или косвенно вызывать гортанные симптомы. Прямой механизм включает раздражение слизистой оболочки гортани едкими веществами — рефлюксатами (кислота, пепсин). Косвенный механизм включает раздражение пищевода, что приводит к гортанным рефлексам и появлению симптомов.
Инфекция Helicobacter pylori также может вносить свой вклад. Распространенность H. pylori среди пациентов с ЛФР составляет около 44%.
Ларингофангеальный рефлюкс и ГЭРБ
Хотя кислота желудка является общей как для ЛФР, так и для ГЭРБ, существует много различий, что делает ЛФР отдельным клиническим объектом.
- Обязательным условием ГЭРБ является изжога, которая достоверно наблюдается только у 40% пациентов с ЛФР.
- Большинство пациентов с ГЭРБ имеют признаки эзофагита при биопсии, в то время как пациенты с ЛФР только в 25% случаев.
- Считается, что ГЭРБ является проблемой нижнего сфинктера пищевода и возникает в основном в положении лежа. Напротив, ЛФР рассматривается в первую очередь как проблема верхнего сфинктера пищевода, и возникает в основном в вертикальном положении во время физических нагрузок.
- Для формирования ЛФР необходимо гораздо меньшее воздействие кислоты, чем при ГЭРБ.
Между слизистой оболочкой пищевода и гортани есть существенные различия.
- Верхним пределом нормы для кислотного рефлюкса в пищевод считается до 50 эпизодов в день, при этом 4 эпизода заброса рефлюксата в гортань уже не является вариантом нормы.
- В гортани, в отличие от пищевода, который при перистальтике устраняет кислоту, рефлюксат сохраняется намного дольше, вызывая дополнительное раздражение.
- Эпителий гортани тонкий и плохо приспособлен для борьбы с едкими химическими повреждениями от того же пепсина и кислоты.
Симптомы ларингофарингеального рефлюкса
- Дисфония или охриплость; ;
- ощущение кома в горле;
- дискомфорт и ощущение слизи в горле;
- дисфагия (нарушение глотания).
Некоторые исследователи считают, что хроническое раздражение гортани может приводить к развитию карциномы у пациентов, не употребляющих алкоголь или не курящих, хотя данных, подтверждающих это, нет.
Симптомы, характерные для ЛФР, также могут быть обусловлены следующими состояниями:
- постназальный синдром;
- аллергический ринит;
- вазомоторный ринит;
- инфекции верхних дыхательных путей;
- привычное покашливание;
- употребление табака или алкоголя;
- чрезмерное использование голоса;
- изменение температуры или климата;
- эмоциональные проблемы;
- раздражители окружающей среды;
- блуждающая нейропатия.
Диагностика
Существуют значительные разногласия по поводу подходящего способа диагностики ЛФР.
При ларингоскопии (осмотре гортани) отмечается отечность и гиперемия (краснота) различной степени. Однако относительно слабая корреляция между симптомами и эндоскопическими данными является аргументом против использования эндоскопических методов диагностики.
Шкала рефлюксных признаков и индекс рефлюксных симптомов хорошо подходят как для диагностики, так и для мониторинга ответа на терапию.
Суточная Ph-метрия зондом с двойным сенсором, несмотря на превосходную чувствительность и специфичность, ставится под сомнение, так как результаты этого диагностического метода зачастую не коррелируют с тяжестью симптомов.
Еще одним вариантом диагностики может быть эмпирическое назначение терапии ИПП.
Лечение ларингофарингеального рефлюкса
Изменение образа жизни и диета являются основным подходом при лечении ЛФР и ГЭРБ. Роль медикаментозной терапии более противоречива. Нуждаются ли в лечении пациенты без симптомов заболевания, со случайно выявленными признаками ЛФР, неизвестно. Существуют теоретические опасения, что ЛФР может увеличить риск злокачественных новообразований, но это пока не доказано. В любом случае, пациентам с бессимптомный ЛФР рекомендуется соблюдение диеты.
Пациентам рекомендуется отказаться от курения, алкоголя, исключить продукты и напитки, содержащие кофеин, шоколад, мяту. К запрещенным продуктам также относятся большинство фруктов (особенно цитрусовых), помидоры, джемы и желе, соусы для барбекю и большинство заправок для салатов, острая пища. Питание рекомендуется дробное.
Следует избегать физических упражнений в течение как минимум двух часов после еды, воздерживаться от еды и питья за три часа до сна.
Медикаментозная терапия обычно включает ингибиторы протонной помпы (ИПП), блокаторы H2 и антациды. ИПП рекомендуется принимать в течение шести месяцев для большинства пациентов с ЛФР. Данная цифра основана на результатах эндоскопических исследований (именно это время необходимо для уменьшения отека гортани), а также высоком проценте рецидива в случае трехмесячного курса терапии. Прекращение терапии следует проводить постепенно.
Если терапия ИПП и блокаторами Н2 оказалась безуспешна, следует рассмотреть вариант лечения трициклическими антидепрессантами, габапентином и прегабалином, так как один из возможных механизмов развития рефлюкса — повышенная чувствительность гортани.
Как проходит лечение ларингофарингеального рефлюкса в клинике Рассвет?
Все пациенты с жалобами на охриплость, ощущение кома в горле, затруднение глотания, кашель, ощущение слизи в гортаноглотке осматриваются оториноларингологом и гастроэнтерологом.
Проводится эндоскопическое исследование полости носа, носоглотки и гортани для исключения других заболеваний, которые, помимо ЛФР, могут провоцировать эти симптомы. Гастроэнтеролог также назначает весь необходимый спектр обследований, в том числе исключает инфекцию H. Pylori.
Залог успешной терапии — совместное ведение пациента оториноларингологом, гастроэнтерологом, в ряде случаев психиатром и психотерапевтом.
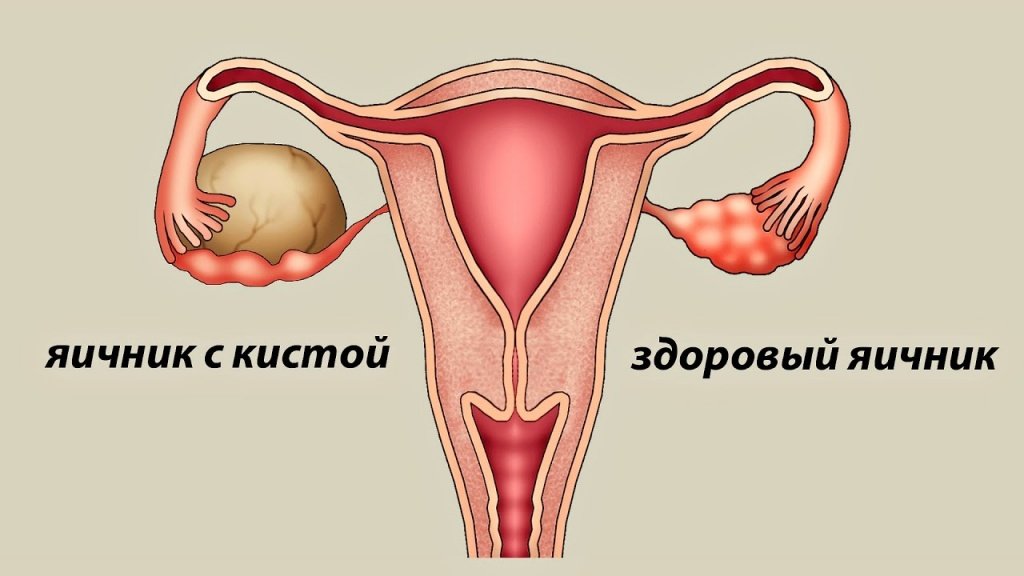
Киста яичника — это новообразование доброкачественной природы, которое относится к опухолевидным процессам и локализующееся непосредственно в тканях яичника. Слово «киста» происходит от греческого слова kystis — пузырь. Киста по сути представляет собой полость, заполненную жидкостным содержимым (секретом). Тонкий слой клеток, который продуцирует секрет, образует стенку кисты яичника.
array(6) < ["ID"]=>string(5) "29111" ["WIDTH"]=> int(1024) ["HEIGHT"]=> int(576) ["SRC"]=> string(86) "/upload/sprint.editor/eea/img-1653218344-5723-750-9f2de90151d4ea0eb799778a1ea9bf2d.jpg" ["ORIGIN_SRC"]=> string(86) "/upload/sprint.editor/eea/img-1653218344-5723-750-9f2de90151d4ea0eb799778a1ea9bf2d.jpg" ["DESCRIPTION"]=> string(0) "" >
Исходя из причин возникновения, можно выделить два основных вида – функциональные и патологические. А в зависимости от места возникновения новообразования, выделяют следующие подвиды:
- Фолликулярная – киста, которая образуется в результате нарушения нормальной овуляции (у яйцеклетки нет возможности покинуть фолликул, который впоследствии растягивается из-за накопления в нем жидкости);
- Лютеиновая киста (киста желтого тела) – образование ткани яичника на месте нерегрессировавшего желтого тела, в центральной зоне которого, образуется геморрагическая жидкость из-за нарушения кровообращения. Рассасываются самостоятельно через один-три менструальных циклов и не требуют хирургическое лечение при небольших размерах (до 6 сантиметров);
- Параовариальная – киста, которая представляет собой тонкостенное образование в брыжеечной области маточной трубы. Может достигать внушительных размеров (от 12 до 20 см);
- Дермоидная киста - толстостенная капсула, заполненная слизеобразным содержимым (ткани костей и зубов, волосы, хрящи, жировые клетки и прочее). Диаметр достигает до 15 см;
- Эндометриоидная – имеют размер от 5 до 20 см и образуются в результате разрастания яичниковой ткани эндометрия. Как правило, имеют двухсторонний характер поражения.
Очень часто кисты яичника протекают бессимптомно и случайно выявляются при посещении врача, однако выделяют основные клинические проявления:
- Нарушение менструального цикла;
- Болевой синдром;
- Ощущение инородного тела или внутреннего сдавления;
- Метеоризм.
При появлении первых симптомов пациентке требуется немедленная госпитализация независимо от того, какие размеры имеет киста - 3 см или 20. Затягивание с лечением влечет за собой последствие-развитие перитонита, из-за разрыва образования.
Специалисты онкологического центра Юсуповской больницы занимаются диагностикой и лечением различных видов новообразований репродуктивной системы. В распоряжении больницы имеется мощная база для диагностики и современное высокотехнологичное оборудование, а также работают ведущие специалисты. На базе онкологической клиники также может проводиться реабилитация пациентов.
В Юсуповской клинике лечение кисты яичника можно проводить медикаментозно при небольших размерах, однако если их размеры достигают 20 см и оказывают влияние на соседние органы, то применяется хирургическое лечение.
Остались вопросы? Мы вам перезвоним
Мы с радостью проконсультируем вас и ответим на все интересующие вопросы.
Когда актуально консервативное лечение кисты яичника?
Консервативное лечение приемлемо только при функциональных кистах яичника (фолликулярные или кисты желтого тела). Это так называемые гормональные кисты, которые поддаются лечению благодаря нормализации гормонального фона женщины.
В Юсуповской онкологической клинике при грамотно подобранном медикаментозном лечении, функциональные кисты исчезают уже спустя трех месяцев. На протяжении всего пребывания в клиники, врачи наблюдают за динамикой применяемого лечения.
В лучшей больнице Москвы занимаются консервативным лечением кист яичника, применяя комплексный подход к патологии. Квалифицированные врачи назначают противовоспалительные, противогрибковые, противомикробные и гормональные препараты. Антибиотики при кисте яичника используют с целью уничтожения патогенной микрофлоры, которая может быть основной причиной развития заболевания или фактором, который препятствует быстрому и эффективному лечению. Наряду с инъекциями и таблетками от кисты яичника используют свечи, которые бывают вагинальными и ректальными (вводятся в прямую кишку). Свечи применяют в связи с тем, что одним из факторов возникновения кист является воспалительный процесс в малом тазу. В своем составе они имеют ферменты, которые растворяют спайки, сгустки крови, тромбы и гной. Вводятся ректально, доза и продолжительность курса лечения определяется врачом индивидуально для каждого пациента.
При нарушении гормонального фона (избытке эстрогенов и недостатке прогестерона) применяют гормональные вагинальные свечи. Действующим веществом является прогестерон — вещество, нормализирующее гормональный фон, обеспечивает уменьшение кистозных образований, а также снижает риск осложнений.
Свечи с лактобактериями применяются для восстановления микрофлоры влагалища после лечения воспалений антибиотиками и свечами вагинального применения.
Иммуномодуляторы в виде ректальных свечей применяют в борьбе с нарушениями иммунной системы, которые могут привести к кистозным образованиям.
Какие выбрать свечи?
Ихтиоловые свечи в гинекологии при кисте яичника имеют противовоспалительный и антисептический эффект. Действующим веществом является ихтиол. Это вещество чёрного цвета, имеющее резкий запах. Применяется ректально после естественного очищения кишечника 1-2 раза в день, может применяться и вагинально. Положительный эффект достигается достаточно быстро за счет хорошего всасывания вещества. Ихтиоловые свечи при кисте яичника имеют хорошие отзывы в связи с отсутствием противопоказаний и побочных действий.
Индометацин при кисте яичника снижает болевые ощущения и отечность путем блокирования ферментов, вызывающих воспаления. Относится к нестероидным противовоспалительным средствам. Эффективность препарата достигается в 90%. Принимается вагинально по 1-2 свечи в сутки, быстро всасывается. Не рекомендуется принимать пациентам, имеющим заболевания желудочно-кишечного тракта, печени, аллергиях, беременным женщинам и кормящим матерям. Побочное действие заключается в головокружении, сонливости, боли в животе, тошноте и рвоте.
Дикловит - нестероидное противовоспалительное средство. Применяется как противовоспалительный препарат органов малого таза. Вводят ректально после дефекации или очистительной клизмы по 1-2 свечи в сутки. Нельзя назначать при аллергических реакциях, бронхоспазмах, индивидуальной непереносимости вещества, беременным и кормящим женщинам. Побочные эффекты: мигрень, шум в ушах, аллергическая реакция, в редких случаях — отёк ног. В случае передозировки может наблюдаться спутанность сознания, тошнота, рвота, кровотечение. Препарат следует очень аккуратно применять в сочетании с другими лекарственными средствами.
В гинекологии лонгидаза используется для лечения и профилактики спаек, образующихся на фоне воспалительного процесса. Обладает иммуномодулирующим, антиоксидантным и незначительным противовоспалительным действием. Имеет хорошую всасываемость. Применяется одна свеча через два дня перерыва. Вводится вагинально или ректально, после очищения кишечника. Противопоказан для пациентов с онкологическими заболеваниями, беременных, детей до 12 лет, болезнях почек. Побочные явления проявляются в виде аллергической реакции.
Свечи с прополисом используются как противовоспалительные, антибактериальные, антиоксидантные, иммуномодулирующие средства. Применяются вагинально или ректально, после очищения кишечника.
Эндометриоидная киста яичника
Эндометриоидная киста яичника – это патологическое полостное образование на поверхности яичника, которое состоит из скопившейся менструальной крови, окруженной оболочкой из клеток эндометрия. В отличие от функциональных кист, эндометриоидные кисты имеют совершенно другой механизм развития и, как правило, двухстороннее поражение. В гинекологии такая киста яичника относится к проявлениям генитальной формы эндометриоза.
В Юсуповской клиники широко применяют свечи при эндометриозе кисты яичников, которые оказывают обезболивающий эффект.
Чаще всего используются суппозитории, имеющие нестероидные противовоспалительные средства в своем составе (например, индометацин и диклофенак). При эндометриозе кишечника, который сопровождается спастическими болями, применяют свечи, в состав которых входит папаверин или белладонна.
При спаечном процессе в яичниках, с профилактической и рассасывающей целью, хорошо помогают суппозитории, состоящие из лонгидазы (они вводятся либо ректально, либо вагинально).

Фото: АстраЗенека
Главный герой одного из популярных «медицинских» сериалов при дифференциальном диагнозе именно системную красную волчанку (СКВ) подозревал у каждого трудного пациента. И хотя у кинематографических сценариев свои законы, авторы этого сценария четко уловили важную особенность СКВ — невероятную многоликость заболевания.

О многогранности проявлений сложной хронической патологии, при которой иммунная система организма атакует свои собственные клетки как чужеродные, о потенциальных причинах ее развития и о возможностях современных терапевтических стратегий корреспондент МВ узнал у Татьяны Решетняк, докт.мед.наук, врача высшей квалификационной категории, заведующей лабораторией тромбовоспаления ФГБНУ «Научно-исследовательского института ревматологии им. В.А. Насоновой».
— На самом деле, история этого заболевания значительно глубже. Первым, кто описал кожные язвы herpes esthiomenos, был еще Гиппократ (460-375 до н. э.). Название «красная волчанка» (Lupus erythematosus — лат.), происходит от латинских слов lupus — «волк» (из-за характерной, похожей по форме на бабочку сыпи на лице, напоминающей белые отметины на морде волка), и erythematosus — «красная», что указывает на цвет кожных высыпаний.
Выделяют несколько периодов изучения СКВ: классический, при котором описаны кожные проявления заболевания и их отличие от туберкулеза кожи; неоклассический — выделение диссеминированных или системных проявлений заболевания; современный, начало которого относится к описанию LE-клеточного феномена при СКВ, а продолжение характеризуется дальнейшими успехами в диагностике и терапии заболевания.
По определению ВОЗ и акад. В.А. Насоновой, «Системная красная волчанка (СКВ) — хроническое полисиндромное заболевание преимущественно молодых женщин и девушек, развивающееся на фоне генетически обусловленного несовершенства иммунорегуляторных процессов и приводящего к неконтролируемой продукции антител к собственным клеткам и их компонентам, с развитием аутоиммуного и иммунокомплексного хронического воспаления». Как следует из определения, контингент больных — в основном, молодые женщины трудоспособного и репродуктивного возраста, в связи с чем это заболевание остается актуальным как в мире, так и в России.
Теперь о распространенности. В учете истинной частоты и степени преобладания заболевания в различных этнических группах есть трудности. Связаны они с методологическими различиями в проведенных исследованиях.
Результаты исследования 2007 года, суммирующего данные 1950-2004 годов, приводят частоту заболевания от одного до 241 случая на 100 тыс. населения. При этом отмечается, что частота встречаемости СКВ возрастает с каждым десятилетием (с 1950 по 1979 год она составляла 1,51 на 100 тыс. населения, а с 1980 по 1992 год — 5,56 на 100 тыс.).
По данным российских исследований, распространенность данного заболевания колеблется в диапазоне от 4 до 250 случаев на 100 тыс. населения 1 .
К сожалению, в нашей стране отсутствует регистр по СКВ, но число новых случаев такое же, как и по Европе (например, по данным регистра Швеции — это 39-45 случаев на 100) 2 .
— Системная красная волчанка — сложное заболевание, этиология которого до конца не изучена. Расскажите, пожалуйста, что известно современной медицине о его патогенезе?
— Патогенез СКВ сложен и действительно до конца не изучен. Системная красная волчанка — заболевание с наследственной предрасположенностью, но не в полной мере наследственное заболевание. Выявлено достаточно много генов, которые вовлечены в механизм его развития (более 40). Однако сам ген волчанки до настоящего времени не найден, поэтому говорить о том, что это наследственное заболевание, мы пока не можем.
СКВ — аутоиммунная болезнь, возникающая в случае, когда иммунная система человека теряет способность отличать чужеродные агенты от собственных тканей и клеток. Иммунная система вырабатывает наряду с другими активными молекулами аутоантитела, которые расценивают собственные нормальные клетки организма как чужеродные и атакуют их.
Отмечается гиперактивность В-лимфоцитов и дефицит Т-супрессорной функции лимфоцитов, при этом отмечается продукция большого количества аутоантител (антиядерных, антител к двуспиральной, нативной ДНК, микросомам, лизосомам, митохондриям, форменным элементам крови и др.). Наибольшее патогенетическое значение имеют антитела к нативной ДНК (нДНК), которые, соединяясь с ней, образуют иммунные комплексы и активируют комплемент.
В патогенезе СКВ задействован как врожденный, так и приобретенный иммунитет, и важную роль в их дисрегуляции играет интерферон I типа (ИФН I типа). Недавние исследования обнаружили тесную взаимосвязь между ИФН I типа, особенно ИФН-α. С этим заболеванием более чем у половины пациентов с СКВ экспрессия генов «сигнатуры ИФН типа I» была выявлена в мононуклеарах периферической крови. ИФН-α может активировать лимфоциты, дендритные клетки и естественные киллерные клетки (NK), нарушая аутоиммунную толерантность. Результатом является аутоиммунная реакция, вызывающая воспаление определенных органов (суставов, почек, кожи и т. д.).
Также известно, что СКВ может быть спровоцирована гормональным дисбалансом в период полового созревания, стрессом, факторами окружающей среды (например, воздействием ультрафиолета), вирусной инфекцией, приемом лекарственных средств (таких, как изониазид, гидралазин, прокаины или противосудорожные препараты).
— Для волчанки характерно многообразие симптомов и проявлений. Врачам каких специальностей нужно иметь настороженность в отношении этого заболевания?
— Симптомы СКВ действительно многообразны и могут быть связаны с поражением любых систем и органов. Именно поэтому СКВ определяют как мультидисциплинарную проблему.
Врач любой специальности на практике имеет возможность «встретиться» с больным системной красной волчанкой. В первую очередь, это может быть терапевт, дерматолог, нефролог, невролог, гематолог, кардиолог, акушер-гинеколог, а также аллерголог и инфекционист.
— Татьяна Магомедалиевна, на что врачу следует обратить внимание, чтобы не пропустить такого пациента? Какие органы и системы поражаются при этом заболевании? Каковы наиболее часто встречающиеся симптомы при СКВ?
— Как правило, у пациента можно выделить какой-либо один пораженный орган-мишень, определяющий тяжесть состояния. При легкой степени активности СКВ наиболее часто вовлечены кожно-слизистая и костно-мышечная системы. Для тяжелой степени активности характерно поражение жизненно-важных органов.
Одинаковых случаев СКВ нет. У разных пациентов заболевание может проявляться по-разному. Это может быть, к примеру, лихорадка неясного генеза, боли в суставах, кратковременные, мигрирующие боли в области грудной клетки, которые могут быть связаны с дыханием или с переменой положения тела, адгезивный полисерозит. С такими проявлениями пациенты обращаются к терапевтам.
К неврологам попадают пациенты с эпилептическим статусом, хореиформными гиперкинезами, нарушением чувствительности, проблемами с мочеиспусканием или недержанием мочи у молодых пациентов. Встречаются также энцефаломиелопатии и радикулополинейропатии, которые обычно сочетаются с лихорадкой и другими проявлениями.
При поражении почек у больных СКВ болевых ощущений чаще всего нет. И врачи ориентируются на лабораторные анализы — появление белка в моче. Это в первую очередь требует исключения гломерулонефрита после ангины или простудного заболевания, на фоне приема лекарственных препаратов. О вовлечении почек зачастую говорит и появление отеков, преимущественно в области стоп, голеней, а также появление одутловатости лица и параорбитальных отеков.
При волчанке может наблюдаться феномен Рейно (изменение окраски кончиков пальцев или пальцев целиком в связи со стрессом или холодом). Поражения кожи при СКВ в 25-50% довольно типичны, поэтому дерматологи и терапевты сразу их замечают — высыпания эритематозного характера на скулах, спинке носа, подбородка, надбровных дуг. К проявлениям волчанки относятся и язвы во рту и носу — с такими жалобами пациент может попасть к отоларингологу или опять же к терапевту.
Системная красная волчанка иногда сопровождается так называемым сухим синдромом, или синдромом Шегрена, при котором отмечается сухость во рту, трудности с проглатыванием твердой пищи, снижение количества слез.
Кроме того, существует субтип волчанки с антифосфолипидным синдромом. Он вызывает рецидивирующие тромбозы любой локализации и акушерскую патологию, проявляющуюся рецидивирующими потерями беременности. Бывает, что первая беременность заканчивается самопроизвольным абортом, и при обследовании выявляется позитивная реакция Вассермана (реакция на сифилис), а при проверке эта реакция оказывается ложно-позитивной — это еще один признак волчанки.
— Очевидно, что и при СКВ важно как можно раньше поставить диагноз. Каким будет прогноз при запоздалой диагностике заболевания?
— Поздняя диагностика приводит к плохому прогнозу, как и запоздалое выявление повышения активности СКВ — это ведет к неконтролируемой выработке аутоантител и нарастанию функциональной недостаточности органов.
Самые серьезные из возможных поражений — поражения почек и центральной нервной системы. При волчаночном нефрите быстро наступает хроническая болезнь почек и уремия, что вызывает необходимость диализа, в перспективе трансплантации почек.
При поражении центральной нервной системы возможен поперечный миелит, приводящий пациентов с энцефаломиелопатией или радикулополинейропатией без своевременного лечения к инвалидизации. Наличие антифосфолипидного синдрома при СКВ ведет к возрастанию риска инсульта и нарушений когнитивных функций.
Как говорилось выше, антифосфолипидный синдром может также проявляться акушерской патологией с рецидивирующими случаями потери плода на разных сроках беременности. При этом фертильность у пациенток с СКВ не страдает, беременность наступает довольно легко. Поэтому при активной волчанке и при приеме иммуносупрессивных препаратов обязательно пользоваться средствами контрацепции.
Все перечисленные специалисты наблюдают пациента совместно с ревматологом.
— Какие современные терапевтические стратегии предлагает медицина для пациентов с этим сложным и мало предсказуемым заболеванием?
— Длительно существующее аутоиммунное воспаление, как это бывает при системной красной волчанке, может вызвать повреждение тканей и нарушить их нормальное функционирование, поэтому лечение СКВ направлено прежде всего на подавление аутоиммунных реакций.
В настоящее время выявлен ряд мишеней для создания лекарственных препаратов для лечения СКВ. Несмотря на большое число клинических исследований сегодня ревматологи располагают ограниченным набором высокотехнологичных лекарственных средств.
Генно-инженерная биологическая терапия — многообещающая опция в лечении СКВ. Она подразумевает разработку моноклональных антител, оказывающих селективное воздействие на основные звенья иммунопатогенеза СКВ. К сожалению, пока таких препаратов одобрено мало. Биологические препараты, рекомендуемые для терапии СКВ, влияют только на В-клеточное звено иммунитета.
Согласно последним научным данным, считается, что ведущий механизм развития СКВ связан с семейством интерферонов (ИФН) типа I, поэтому антитела к ИФН-α имеют большое будущее в лечении волчанки. В ближайшее время ожидается появление нового препарата — ингибитора ИФН типа I.
— Излечить волчанку пока нельзя, но этот диагноз уже не звучит фатально. Какова выживаемость пациентов с СКВ в наше время? Благодаря чему она достигнута?
— Да, сегодня 10-летняя выживаемость достигла 95%. Это результат и своевременной диагностики, и адекватного лечения. Появление новых биологических таргетных препаратов ведет к снижению дозы глюкокортикоидов и цитостатиков, что, в свою очередь, снижает нежелательные явления стандартной терапии, уменьшается повреждение органов, что способствует не только контролю активности заболевания, но и достижению еще одной важной цели в терапии СКВ — улучшению качества жизни пациентов.
Читайте также:

