Мтс при раке кожи
Обновлено: 18.04.2024
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России, 125284 Москва, 2-й Боткинский пр-д, д. 3, Российская Федерация
ФГБУ "Московский научно-исследовательский онкологический институт им. П.А. Герцена" Минздравсоцразвития России
ГБОУ ВПО «Первый Московский государственный университет им. И.М. Сеченова» Минздрава России, Москва, Россия
Клинический пример 17-летнего наблюдения за больной раком молочной железы IIIC стадии с метастазами в парастернальных лимфатических узлах
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
В статье представлено клиническое наблюдение пациентки 77 лет с диагнозом: первично-множественный метахронный рак: рак правой молочной железы IIIС стадии, рТ2N3сМ0G2. Состояние после комплексного лечения в 2001 г. (операция+лучевая терапия + 5 курсов химиотерапии САF + гормонотерапия). Рак левой молочной железы I стадии, рТ1N0М0. Состояние после хирургического лечения в 2012 г. В 2001 г. по поводу метастазов в парастернальных лимфатических узлах выполнена лучевая терапия по радикальной программе на парастернальную зону. За 17-летний период наблюдения прогрессирования заболевания не выявлено. При лечении метастазов в парастернальных лимфатических узлах рака молочной железы можно использовать как хирургический способ, так и лучевую терапию по радикальной программе.
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России, 125284 Москва, 2-й Боткинский пр-д, д. 3, Российская Федерация
ФГБУ "Московский научно-исследовательский онкологический институт им. П.А. Герцена" Минздравсоцразвития России
ГБОУ ВПО «Первый Московский государственный университет им. И.М. Сеченова» Минздрава России, Москва, Россия
Рак молочной железы (РМЖ) занимает первое место в структуре заболеваемости и смертности среди онкологических заболеваний у женщин в мире и в РФ. В 2017 г. РМЖ выявлен у 64 798 женщин в РФ, что составляет 456,0 случаев на 100 000 населения [1].
Пациентки с местно-распространенным РМЖ III B, С стадии составляют до 20% в структуре РМЖ в России.
При локализации опухоли в медиальных и центральных квадрантах возрастает вероятность поражения парастернальных лимфатических узлов. Внутренний грудной коллектор является одним из основных путей метастазирования при РМЖ. Метастазы в этом бассейне оказывают отрицательное воздействие на выживаемость в отдаленные сроки и на длительность безрецидивного периода [2]. Полагают, что микрoметастазы в неудаленных при выполнении обычной мастэктомии парастернальных лимфатических узлах могут выступать в качестве источника поражения надключичных узлов, а также дальнейшего распространения опухолевых клеток [3, 4].
В связи с этим ряд авторов полагают, что РМЖ с метастазами в надключичных и парастернальных лимфатических узлах без признаков отдаленного метастазирования можно рассматривать как регионарный и, следовательно, потенциально излечимый процесс. Соответственно таким пациентам показано радикальное, а не паллиативное лечение [5].
Сведения о частоте метастазирования в парастернальные лимфатические узлы, по данным литературы [6], существенно колеблются в пределах 12—55%, а в 4—16% случаев это поражение встречается при отсутствии метастазов в аксиллярном коллекторе, что подчеркивает важность изучения состояния этой группы лимфатических узлов. К сожалению, точность методов современной диагностики не превышает 72—95%.
В случае метастатического поражения парастернальных лимфатических узлов можно применять два метода локального лечения: хирургический или лучевой с суммарной дозировкой по радикальной программе.
Ниже приведено клиническое наблюдение пациентки, которой выполнено консервативное лечение метастатических парастернальных лимфатических узлов.
Клиническое наблюдение
Пациентка Т., 77 лет, диагноз: первично-множественный метахронный рак: рак правой молочной железы IIIC стадии, рТ2N3сМ0G2. Состояние после комплексного лечения в 2001 г. (операция + лучевая терапия + 5 курсов химиотерапии САF + гормонотерапия). Рак левой молочной железы I стадии, рТ1N0М0. Состояние после хирургического лечения в 2012 г.
Из анамнеза: пациентка Т. в возрасте 60 лет в мае 2001 г. обнаружила самостоятельно узел в правой молочной железе и обратилась в поликлинику МНИОИ им. П.А. Герцена для обследования. Клинически в правой молочной железе в верхневнутреннем квадранте определяется узловое образование размером 2,5×2 см, плотное при пальпации, кожные симптомы отрицательные. Левая молочная железа без узловых образований. Пациентка обследована. Маммография: справа в верхневнутреннем квадранте выявляются ограниченное уплотнение размером 2,5 см, единичные микрокальцинаты. Заключение: рак правой молочной железы. Цитологическое исследование материала тонкоигольной биопсии опухоли правой молочной железы: рак солидного строения лимфатического узла правой подмышечной области — метастаз солидного рака. Сцинтиграфия костей скелета от 02.05.01: признаков очаговых накоплений препарата в костях не обнаружено. Рентген легких от 03.05.01: легкие, средостение без изменений.
21.05.01 в МНИОИ им. П.А. Герцена выполнена операция: радикальная резекция правой молочной железы с одномоментной реконструкцией фрагментом широчайшей мышцы спины.
Гистологическое исследование: макроскопически выявлен узел размером 2×2×2,5 см. Микроскопическое исследование: инвазивный протоковый рак 2-й степени злокачественности с наличием опухолевых эмболов в лимфатических сосудах, а также структур карциномы in situ. В одном из фрагментов, взятом отдаленно, очаг внутрипротокового рака с началом инвазивного роста. В 1 из 10 исследованных подмышечных лимфатических узлов выявлен метастаз рака без инвазии за капсулу. Иммуногистохимическое исследование: реакция с рецепторами эстрогенов положительная в 20% клеток опухоли, реакция с рецепторами прогестеронов отрицательная.
При выписке пациентке выполнено контрольное УЗИ регионарных зон, диагностирован увеличенный лимфатический узел в правой парастернальной области размером 7×4,4 мм. С использованием ультразвуковой навигации произведена тонкоигольная биопсия лимфатического узла, цитологически выявлен рак с выраженной дистрофией клеток.
По данным компьютерной томографии грудной клетки от 13.06.01 парастернальные лимфатические узлы не увеличены, дополнительной патологии не выявлено.
При УЗИ регионарных зон от 14.06.01 произведена биопсия второго парастернального лимфатического узла размером около 4×3 мм, цитологически выявлен аденогенный рак с низкой дифференцировкой клеток. Учитывая двукратную верификацию парастернальных лимфатических узлов, трудность их визуализации лучевыми методами диагностики (УЗИ, КТ), в качестве местного воздействия принято решение применить лучевую терапию по радикальной программе.
Пациентка обсуждена на консилиуме с участием химиотерапевта, радиолога, хирурга, рекомендовано проведение полихимиотерапии — 5 курсов по схеме САF, лучевая терапия на сформированную правую молочную железу, регионарные зоны, гормонотерапия тамоксифеном по 20 мг/сут в течение 5 лет.
На 2-м этапе выполнена лучевая терапия на правую молочную железу в СОД 54 Гр, на регионарные зоны 45 Гр, на парастернальную зону 50 Гр, на 3-м этапе — 5 курсов ПХТ по схеме САF, далее пациентка 4 года получала антиэстрогенную терапию тамоксифеном, 1 год — ингибитор ароматазы аримидекс.
При контрольном обследовании в поликлинике МНИОИ им. П.А. Герцена в апреле 2012 г. диагностирован рак контралатеральной левой молочной железы I стадии. С учетом возраста пациентки (71 год) решено выполнить операцию в объеме радикальной мастэктомии слева.
При повторном поступлении: в правой молочной железе в области послеоперационного рубца без очаговых зон. В левой молочной железе определяется узел размером 1,5 см на границе верхних квадрантов. Регионарные лимфатические узлы мягкоэластической консистенции. 20.04.12 произведена операция — радикальная мастэктомия слева.
При гистологическом исследовании макроскопически выявляется узел размером 1,2 см. Микроскопическое исследование: инвазивная папиллярная карцинома с очагами инвазии за пределы капсулы узла 2-й степени злокачественности, по периферии множественные внутрипротоковые папилломы, сосок интактен. В 16 лимфатических узлах метастазов не обнаружено.
Таким образом, с учетом разной гистологической структуры опухолевых узлов при сравнении с данными 2001 г. диагностирован первично-множественный метахронный рак молочных желез. Иммуногистохимическое исследование: рецепторы эстрогена 4 балла, рецепторы прогестерона 0 баллов, реакция с Неr2/neu 2+, Кi-67 в 5% клеток. При FISH-реакции амплификации не обнаружено. На консилиуме от 17.05.12 с участием химиотерапевта, радиолога, хирурга рекомендовано наблюдение.

При контрольном обследовании в декабре 2018 г. по данным КТ грудной клетки, УЗИ послеоперационного рубца слева и правой молочной железы, регионарных лимфатических узлов, маммографии справа, сцинтиграфии костей скелета, УЗИ брюшной полости данных, подтверждающих прогрессирование, не выявлено. При осмотре пациентки в декабре 2018 г. и по данным инструментального обследования прогрессирования и местного рецидива не обнаружено (см. рисунок). Вид пациентки, декабрь 2018 г. а — прямая проекция; б — правая боковая проекция.
Таким образом, за период наблюдения в течение 17 лет у пациентки данных в пользу прогрессирования в парастернальных лимфатических узлах не отмечено.
Заключение
Данное клиническое наблюдение — пример успешного комплексного лечения рака молочной железы IIIC стадии с включением лучевой терапии по радикальной программе на область парастернальных лимфатических узлов справа, курсов полихимиотерапии и гормонотерапии без отдаленного прогрессирования заболевания в течение 17 лет.
В настоящее время пациентка в возрасте 77 лет социально активна, работает редактором в журнале, реабилитирована в семье.
Меланомой называется злокачественное новообразование, которое развивается в результате неопластической трансформации меланоцитов. Локализация первичного опухолевого процесса может быть не только в коже, но и в слизистых оболочках пищеварительной системы, половых путей, сосудистой оболочке глаза и других тканях.
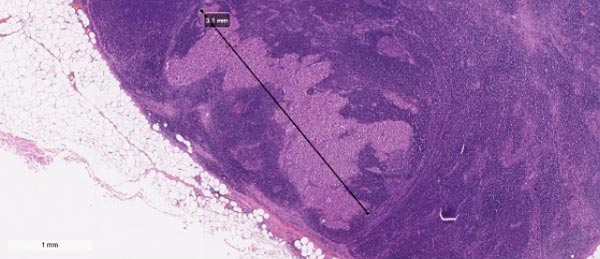
Метастаз меланомы в сторожевом лимфоузле 3,1 мм
При меланоме, также как при других видах злокачественных новообразований, высока вероятность метастатического поражения регионарных лимфатических узлов и других органов. Метастаз – это отдаленный очаг опухоли, который произошел из атипичных клеток первичного очага. Метастазирование при меланоме встречается часто, а в некоторых случаях рост метастазов обнаруживается раньше, чем его первоисточник.
Принцип и пути метастазирования
Процесс появления вторичных очагов новообразований очень сложный и до конца не изучен. Предполагается, что причиной метастазирования является нарушение взаимодействия между атипичными клетками первичной опухоли, межклеточным матриксом и нормальными клетками. Обнаружено несколько протеолитических ферментов, которые запускают деградацию внеклеточного матрикса и улучшают адгезию раковых клеток, что позволяет им перемещаться по организму и внедряться в любую ткань. В разрастании вторичных новообразований важную роль играет фактор роста эндотелия сосудов, который стимулирует формирование новых сосудов, которые в последующем питают опухоль. Распространение метастазов меланомы обычно происходит по лимфатическим и кровеносным сосудам. Чаще всего вторичные очаги появляются в лимфоузлах, коже и подкожной клетчатке, костях, печени, легких, головном мозге.
Метастазы меланомы в головном мозге
Первыми признаками поражения головного мозга являются неврологические нарушения, которые могут быть представлены разными симптомокомплексами:
- Очаговые и общемозговые симптомы, для которых типично постепенное начало и длительное течение на протяжении нескольких недель.
- Симптомы, которые имитируют инсульт. Они развиваются в результате кровоизлияния в ткани метастаза или при закупорке кровеносного сосуда метастатическим эмболом.
- Симптомы, которые имитируют воспаление головного мозга и поражение сосудов.
В практике чаще всего наблюдается сочетание общемозговых и очаговых симптомов. Пациенты жалуются на головные боли, тошноту и рвоту, головокружение, нарушение двигательных и когнитивных функций, судороги, изменение зрения. В тяжёлых случаях развивается высокое внутричерепное давление, из-за которого может произойти сдавление мозга и вклинивание его в большое затылочное отверстие, что часто приводит к смерти пациента.

Наибольшую информативность в диагностике метастазов в головном мозге имеет магнитно-резонансная томография с контрастированием, которая позволяет визуализировать структуры мозга и обнаружить пораженные зоны. Во всех случаях рекомендуется проводить электроэнцефалограмму для выявления судорожной активности. Дополнительно назначается осмотр офтальмолога для диагностики изменений глазного дна.
Метастазы меланомы в коже
Очаги вторичных опухолей в коже и подкожной клетчатке встречаются в среднем в 15% случаев. Развитие кожных метастазов зависит, в первую очередь, от размеров первичной опухоли, ее локализации, возраста пациента и других особенностей. Пути распространения метастазов меланомы в кожу могут быть как лимфогенными, так и гематогенными.
Различают несколько форм вторичных очагов опухоли: сателлитная, тромбоэмболическая, узловая, рожеподобная. Для меланомы характерны единичные и множественные метастазы, которые располагаются как вблизи первичного очага, так вдали от него. Окраска, размеры, форма и консистенция могут быть разнообразными. Ввиду таких разнообразных клинических проявлений часто требуется дифференциальная диагностика.
Метастазы меланомы в легких, почках, костях, печени
Атипичные клетки из первичной опухоли попадают в легкие гематогенным путем. Для меланом типично наличие крупных единичных метастатических узлов в легких, при которых клинические симптомы выражены слабо и обычно имеют неспецифический характер. В запущенных случаях может развиваться эмболия легочных артерий, что проявляется сильной одышкой и болью в груди.
Метастатическое поражение почек также редко имеет яркую клиническую картину. Чаще функция почек остается в норме или имеются незначительные отклонения. Вторичный очаг обычно обнаруживается при плановом обследовании больного по поводу меланомы. Первичными симптомами вовлечения почек могут являться микро- и макрогематурия. На поздних стадиях появляются боли в боку и животе, гипертензия, повышение уровня кальция в крови.
Кроме того, при меланоме часто встречаются отдаленные новообразования в костях, симптомами которых являются боли, патологические переломы и гиперкальцемия. Для диагностики метастазов в костях используется сцинтиграфия, рентген, компьютерная или магнитно-резонансная томография.
Метастазы в печени особенно часто (до 90% случаев) обнаруживаются при меланоме хориоидеи. На начальных этапах симптоматика отсутствует, но по мере роста метастаза появляются признаки сдавления желчевыводящих путей. Пациенты жалуются на боль в правом подреберье, желтуху, отсутствие аппетита, чувство распирания. При поверхностном расположении прощупывается объемное образование в области печени. В постановке диагноза помогает УЗИ, компьютерная и магнитно-резонансная томография.

Диагностика и лечение метастазов меланомы
Ученые относят меланому к одной из самых злокачественных и агрессивных опухолей, т.к. она имеет свойство быстро распространяться по организму. Поэтому при ее обнаружении сразу же проводятся дополнительные исследования для выявления метастазов. На амбулаторном этапе назначаются:
- Компьютерная томография органов грудной клетки.
- Компьютерная томография брюшной полости и органов малого таза с контрастированием.
- Сцинтиграфия костей.
- УЗИ регионарных лимфоузлов и внутренних органов.
- МРТ головного мозга.
- Определение белка S-100, высокий уровень которого характерен для диссеминированных опухолевых процессов.
Своевременное обнаружение метастазов на раннем этапе диагностики может улучшить прогноз по течению заболевания и определяет тактику лечения.
Метастатическую меланому лечат комбинированным способом. Обычно прибегают к хирургическому удалению первичного новообразования и регионарных лимфатических узлов с последующим назначением консервативного лечения. Лучевая терапия используется при вторичном поражении головного мозга.
Удаление меланомы кожи 0 стадии может выполняться в амбулаторных условиях. При I стадии заболевания производится органосохраняющая операция или широкое иссечение первичного очага с удалением лимфоузлов. На II и III стадиях удаляется первичная опухоль и лимфоузлы, назначается лекарственная терапия. При IV стадии с отдаленными метастазами в любом органе, лечение носит индивидуальный характер и зависит от состояния больного. Используется лучевая, иммунотерапия, хирургические вмешательства. Для удаления солитарных очагов в печени могут применяться альтернативные методы хирургии, например, радиочастотная абляция.
Реабилитация после лечения и прогноз
Восстановлению организма после лечения злокачественной опухоли способствует полноценное питание, отказ от вредных привычек, использование поливитаминных препаратов, антиоксидантов и др. Всем пациентам рекомендуется избегать чрезмерной инсоляции и регулярно проводить самообследование.
В целях своевременного выявления рецидива болезни всем больным назначается диспансерное наблюдение:
- В первый год обследование проводится каждые три месяца.
- Во второй год – один раз в 6 месяцев.
- С третьего года – один раз в течение 3 лет.
Необходимо проходить не только физический осмотр с пальпацией регионарных лимфатических узлов, но и рентген грудной клетки ежегодно, УЗИ брюшной полости и лимфоузлов, компьютерную томографию согласно назначенному врачом графику.
Прогноз течения заболевания напрямую зависит от быстроты обнаружения патологического процесса и начала лечения. Согласно данным статистики от первичной опухоли умирают около 10% пациентов, остальные 90% погибают вследствие развития отдаленных метастазов. Если при I стадии меланомы пятилетняя выживаемость составляет около 85%, то при IV – всего лишь 5%. По данным некоторых авторов продолжительность жизни больных с метастатической меланомой не превышает 11 месяцев. Плохим прогностическим признаком является появление вторичных очагов в коже, что характерно для поздней стадии меланомы и обычно сочетается с наличием других метастазов.
Способность к метастазированию — одно из ключевых свойств злокачественных опухолей, отличающих их от доброкачественных новообразований. Раковые клетки способны отрываться от первичной опухоли, распространяться в организме и образовывать вторичные очаги — метастазы. Когда это произошло, обычно диагностируют четвертую стадию рака, и прогноз для пациента сильно ухудшается. Как правило, при раке с метастазами невозможно достичь ремиссии. Цель лечения — продлить жизнь пациента и избавить его от мучительных симптомов.
Каждый тип рака склонен метастазировать в определенные органы. Чаще всего вторичные очаги обнаруживаются в легких, печени, головном мозге, костях. Подкожные метастазы и вторичные поражения кожи встречаются редко.
Как часто встречаются кожные и подкожные метастазы рака?
При висцеральных (расположенных во внутренних органах) злокачественных опухолях подкожные метастазы обнаруживаются в 5,3% от всех случаев метастатического поражения различной локализации. На вторичные поражения кожи приходится еще меньше — около 0,7–0,8%. Хотя, в некоторых научных исследованиях авторы указывают показатели до 9%. В 2003 году в мета-анализе было рассмотрено 1080 случаев кожных метастазов рака у 20 380 пациентов. Авторы предположили, что их частота составляет 5,3%.
В целом на данный момент нет точных однозначных данных о том, насколько часто встречаются кожные метастазы рака. В более поздних научных работах приводятся более высокие показатели. Но ученые не считают, что кожные метастазы стали возникать у онкологических больных чаще — просто теперь их лучше диагностируют.
Среди всех злокачественных новообразований кожи 98% составляют первичные опухоли и только 2% — метастатические поражения.
Какие злокачественные опухоли чаще всего метастазируют в кожу?
Теоретически метастазировать в кожу может рак любого типа. Обнаружена связь между частотой возникновения кожных метастазов и распространенностью самой злокачественной опухоли. Иными словами, чем чаще встречается то или иное онкологическое заболевание, тем чаще при нем образуются вторичные очаги в коже. В тройку онкопатологий, при которых наиболее часто обнаруживаются кожные метастазы, входят рак молочной железы у женщин, рак легкого у мужчин и аденокарциномы пищеварительного тракта у обоих полов.
Вероятность поражения кожи наиболее высока при следующих злокачественных опухолях:
- Меланома — около 7–20%. Из этих опухолей происходят до 13% кожных метастазов у мужчин.
- Рак молочной железы — 30%. Ответственен за 70% кожных метастазов у женщин.
- Рак придаточных пазух носа — 12%.
- Рак гортани — 16%.
- Рак ротовой полости — 12%.
- Рак легкого — 24% всех случаев кожных метастазов у мужчин.
- Рак толстой кишки — 19% случаев всех кожных метастазов у мужчин.
Паттерны метастазирования злокачественных опухолей в кожу зависят не только от пола, но и от возраста. Например, у мужчин младше 40 лет чаще всего встречаются кожные метастазы при меланоме, раке толстой кишки, легких. В более старшей возрастной группе к этому списку добавляется плоскоклеточный рак ротовой полости. У женщин в любом возрасте наиболее частой причиной кожных метастазов является рак молочной железы. До 40 лет вместе с ним преобладают злокачественные опухоли яичников и толстой кишки. После 40 лет к этим онкозаболеваниям добавляются меланома и рак легкого.
Симптомы кожных метастазов при раке
Обычно кожные метастазы возникают недалеко от первичной злокачественной опухоли. Их внешний вид бывает разным. Чаще всего первым признаком становится появление твердого, округлого или овального, подвижного, безболезненного узла. Эти образования имеют эластичную консистенцию, их плотность и размеры бывают разными — от едва заметной до крупной опухоли. Узелки могут иметь телесный или красный цвет, при меланоме — синий или черный. Иногда они единичные, а иногда быстро появляются множественные. Кожные метастазы способны распадаться, при этом на них появляются изъязвления, они кровоточат.
Также, в зависимости от внешнего вида, выделяют некоторые специфические формы кожных метастазов:
- Рожистые (эризипелоидные, воспалительные) карциномы выглядят как пятна красного цвета с резко очерченными контурами, горячие на ощупь. Раковые клетки закупоривают лимфатические сосуды, нарушают отток лимфы, и из-за этого может возникнуть отек — лимфедема. Кожа уплотняется, напоминает «лимонную корку». Рожистые карциномы сильно напоминают инфекционный процесс в коже, вызванный некоторыми бактериями, а при локализации на коже молочной железы их бывает сложно отличить от мастита. При стойком воспалении кожи, которое не поддается обычным методам лечения, всегда должно возникать подозрение на метастатическое поражение.
- Склеродермоидные карциномы выглядят как плотные бляшки, напоминающие шрамы. Они возникают из-за того, что раковые клетки распространяются в дерму — соединительнотканный слой кожи, богатый коллагеном.
- Телеангиэктатические карциномы представляют собой пятна, бляшки или узелки красного цвета, которые чаще всего появляются при раке молочной железы после операции в области рубца. Красный цвет обусловлен тем, что в опухолевых очагах присутствуют многочисленные патологически расширенные кровеносные сосуды (телеангиэктазии).
- Герпетиформные метастазы напоминают опоясывающий лишай. Они выглядят как волдыри, пузырьки, узелки и располагаются по ходу нервов, подобно поражению при опоясывающем герпесе. Механизмы возникновения подобных метастатических очагов до конца не изучены, считается, что они распространяются через лимфатические сосуды вдоль нервов.
- Неопластическая алопеция — характерный симптом кожных метастазов в области волосистой части головы. На коже появляется бляшка голубого или фиолетового цвета, напоминающая рубец, и в этом месте выпадают волосы. Это происходит из-за того, что раковые клетки разрушают волосяные фолликулы, вызывают воспаление и разрастание соединительной ткани. В 84% случаев причиной неопластической алопеции становятся злокачественные опухоли молочной железы.
- Рак Педжета — поражение соска и ареолы молочной железы. Согласно наиболее распространенной в настоящее время теории, изначально злокачественная опухоль возникает в ткани молочной железы, и уже затем распространяется по молочным протокам в сосок.
- Подногтевые метастазы обычно болезненные, их часто путают с воспалительными процессами.
- Метастазы сестры Марии Джозеф представляют собой плотные узелки в области пупка. Они могут иметь рыхлый внешний вид, изъязвляться. Чаще всего этот вид метастазов возникает при раке желудка, яичника, толстой и прямой кишки, поджелудочной железы. В 29% случаев первичную опухоль обнаружить не удается. Считается, что метастазы сестры Марии Джозеф распространяются в пупок напрямую из пораженных органов, например, через круглую связку печени (так называемое имплантационное метастазирование), а также с током крови (гематогенно), лимфы (лимфогенно).
- Скрытые кожные метастазы не обнаруживаются внешне. Их выявляют случайно по результатам гистологического исследования, проведенного по другому поводу.
Насколько опасно метастазирование в кожу?
Кожные метастазы при раке встречаются редко, и их появление всегда свидетельствует об агрессивной злокачественной опухоли, запущенном заболевании и ухудшении прогноза. Так, в одном исследовании с участием 4020 онкологических пациентов было установлено, что с момента обнаружения кожных метастазов средняя продолжительность жизни больных составляет от 1 до 34 месяцев, в зависимости от типа и характеристик первичной опухоли.
В другом исследовании с участием 228 пациентов средняя выживаемость при кожных метастазах составила 6,5 месяца. Показатели по отдельным типам рака составили:
- плоскоклеточный рак головы и шеи (кроме кожи) — 8,8 мес.;
- плоскоклеточный рак кожи — 6,5 мес.;
- рак пищевода — 4,7 мес.;
- рак толстой и прямой кишки — 4,4 мес.;
- рак поджелудочной железы — 3,3 мес.;
- рак желудка — 1,2 мес.;
- рак печени и желчного пузыря — менее 1 мес.
Наиболее высокими оказались показатели выживаемости при раке молочной железы — спустя 13,8 месяца после начала наблюдения 50% пациентов остались в живых. При меланоме этот показатель составил 13,5 месяца, а при раке легкого — 2,9 месяца. Некоторые пациенты с раком молочной железы, просты, гортани, плоскоклеточным раком кожи и меланомой смогли прожить больше 10 лет. Наихудшие показатели выживаемости были отмечены при раке легкого.
Как видно из этих данных, всё индивидуально. В целом наиболее хороший прогноз при кожных метастазах отмечается у пациентов со злокачественными опухолями молочной железы. За последние десятилетия показатели выживаемости удалось повысить с помощью более современных химиопрепаратов. В клиниках федеральной сети «Евроонко» применяются наиболее современные методы лечения, оригинальные противоопухолевые препараты последних поколений. Это позволяет добиваться наилучших показателей выживаемости среди пациентов с метастатическим раком.
Как диагностируют кожные и подкожные метастазы?
Иногда кожные метастазы могут стать первым проявлением онкологического заболевания, пока еще первичная злокачественная опухоль не вызывает симптомов. В других случаях они появляются уже после того, как у пациента диагностирован рак с метастазами в других органах. Также метастатическое поражение кожи может стать первым признаком рецидива, причем, нередко это происходит спустя длительное время после операции. Средний промежуток времени от диагностики первичной опухоли до появления кожных метастазов составляет 2–3 года, но описаны и более длительные интервалы, до 22 лет.
Кожные метастазы нередко бывает сложно диагностировать, их легко спутать с первичными доброкачественными и злокачественными новообразованиями кожи, инфекциями, экземой, васкулитами. Большую роль играют врачи-дерматологии, так как обычно именно к ним такие пациенты обращаются в первую очередь.
При подозрении на метастатическое поражение кожи выполняют эксцизионную биопсию. Патологический очаг полностью удаляют и проводят гистологическое исследование. Чтобы определить, из какой злокачественной опухоли произошел метастаз, проводят иммуногистохимический анализ. Определенные белки-маркеры помогают идентифицировать первичное новообразование.
Современные методы лечения
Обычно при вторичном злокачественном поражении кожи присутствуют метастазы и в других органах, поэтому общие принципы лечения те же, что и при любом метастатическом раке. Назначают химиотерапию, таргетную терапию, иммунотерапию. Применяется лучевая терапия и хирургические вмешательства — но в основном в паллиативных целях, так как нет убедительных доказательств, что в данном случае эти методы помогают увеличить продолжительность жизни пациентов.
В ряде случаев применяются другие методы лечения:
- крем Имиквимод обладает иммуномодулирующим действием, помогает усилить противоопухолевый иммунный ответ и уничтожить кожные метастазы при меланоме;
- криотерапия — уничтожение опухолевой ткани с помощью очень низкой температуры путем нанесения жидкого азота;
- фотодинамическая терапия — процедура, во время которой в организм пациента вводят фотосенсибилизатор, накапливающийся в опухолевых клетках, а затем активируют его с помощью света;
- лазерная терапия;
- локальное введение в опухоль цитокинов — молекул, которые активируют иммунные реакции и воспаление;
- электрохимиотерапия — процедура, во время которой в опухоль вводят химиопрепарат, и его действие усиливают электрическими импульсами.
Федеральная сеть клиник экспертной онкологии «Евроонко» специализируется в первую очередь на лечении пациентов с запущенным, метастатическим раком. Наши врачи применяют наиболее современные методики и препараты, которые помогают максимально замедлить прогрессирование заболевания, продлить жизнь больного, избавить его от мучительных симптомов. Мы работаем строго в соответствии с принципами доказательной медицины, руководствуемся наиболее актуальными версиями международных протоколов лечения. Мы знаем, как помочь.
Слово «метастазы» греческого происхождения, и буквально оно означает «перемещение». В онкологии этим термином называют вторичные очаги, которые располагаются на удалении от первичной опухоли: в других органах, лимфатических узлах.
Метастазы могут располагаться в разных местах. Это зависит от типа рака – у каждого есть свои «излюбленные» локализации. Чаще всего вторичные очаги появляются в легких, печени, брюшине, костях, надпочечниках. Некоторые метастазы весьма специфичны и имеют собственные названия – например, метастаз Вирхова при раке желудка.
В соответствии с современными представлениями, метастазирование – процесс, который зачастую начинается почти сразу с момента возникновения злокачественной опухоли. Некоторые клетки отделяются от первичного очага и проникают в просвет лимфатических или кровеносных сосудов. Они перемещаются в организме с током лимфы или крови, а потом оседают в определенных органах и дают там начало новым очагам. Эти пути метастазирования называются, соответственно, лимфогенным и гематогенным.
На первых порах метастазирование происходит очень медленно, его сложно обнаружить. Иммунная система уничтожает раковые клетки, мигрирующие в организме, а первичная опухоль подавляет рост вторичных очагов.
Если же во время обследования уже обнаруживаются отдаленные метастазы, то у пациента диагностируют метастатический рак. Этот диагноз соответствует злокачественной опухоли IV стадии.
Способность метастазировать – одно из ключевых свойств злокачественных опухолей, отличающее их от доброкачественных новообразований. Зачастую именно метастазы становятся причиной смерти онкологического больного.
Почему возникают метастазы?
Итак, все злокачественные опухоли обладают способностью к метастазированию. Вероятность того, что это произойдет, зависит от ряда факторов:
- тип рака;
- скорость роста опухоли;
- степень дифференцировки злокачественных клеток – насколько они утратили черты нормальных;
- стадия, на которой диагностировано онкологическое заболевание и др.
Иммунная система какое-то время эффективно сдерживает рост и распространение злокачественных клеток, но однажды ее ресурсов не хватает. Опухоль «прорывает» иммунную защиту.
Даже после того, как раковые клетки распространились в организме, они еще какое-то время не растут или размножаются очень медленно. Может пройти несколько лет, прежде чем начнется активный рост вторичных очагов. Почему и как это происходит – пока не до конца изучено.
Когда вторичный очаг растет, число раковых клеток в нем увеличивается, и они начинают вырабатывать особые вещества – факторы роста. Эти соединения активируют рост новых кровеносных сосудов. Образуется капиллярная сеть, которая обеспечивает опухоль кислородом и необходимыми веществами. При этом опухолевые очаги как бы «обкрадывают» здоровые органы и ткани.
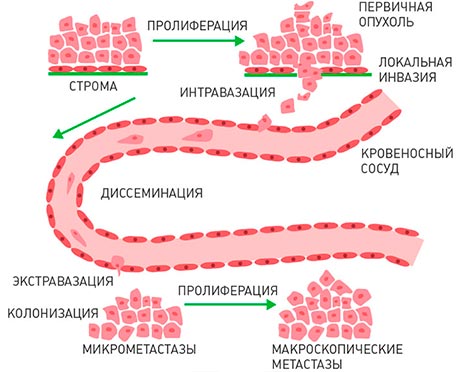
Процесс метастазирования можно разделить на несколько стадий:
- Раковые клетки отделяются от первичной опухоли и проникают в лимфатический или кровеносный сосуд, который находится поблизости.
- Происходит миграция злокачественных клеток в различные органы и ткани.
- Достигнув определенного сосуда, раковая клетка выходит через его стенку в окружающие ткани.
- В течение некоторого времени опухолевые клетки «спят» в тканях и не проявляют себя.
- На последней стадии начинается быстрый рост метастазов.
На каждой из этих стадий многие раковые клетки гибнут. Вторичным очагам дают начало те, которые в конечном итоге выживают.
«Могут ли метастазы распространиться из-за того, что врач повредит опухоль во время операции или биопсии?»
Иногда пациенты испытывают такие опасения, но они беспочвенны. Из-за биопсии (процедуры, во время которой врач удаляет образец опухолевой ткани для исследования) не возрастает риск образования метастазов. Во время операций хирурги-онкологи тоже принимают меры, чтобы этого не допустить.
Врачи клиники «Евроонко» о стадиях рака, рецидиве и метастазах

Что влияет на скорость распространения метастазов в организме?
Как уже упоминалось выше, скорость метастазирования в первую очередь зависит от двух факторов: типа рака и степени дифференцировки:
- В высокодифференцированных опухолях клетки и ткань сильно напоминают нормальные. Такие новообразования ведут себя менее агрессивно, распространяются в организме реже и позже.
- В низкодифференцированных опухолях клетки практически утрачивают черты нормальных. Такой рак более агрессивен, быстрее и с большей вероятностью образует метастазы.
В большинстве случаев метастазы возникают спустя 1–2 года после того, как появляется первичная опухоль. Но иногда это происходит очень быстро, если рак агрессивен. Иногда вторичные очаги обнаруживают спустя многие годы после операции. В таких случаях говорят о латентных («дремлющих») метастазах.
Да, такие способы существуют. Например, адъювантная (то есть проводимая после операции) химиотерапия и лучевая терапия. Химиопрепараты и облучение уничтожают злокачественные клетки, которые могли остаться в организме пациента, и предотвращают рецидив рака, в том числе в виде отдаленных метастазов.
Особенности метастазирования разных типов рака
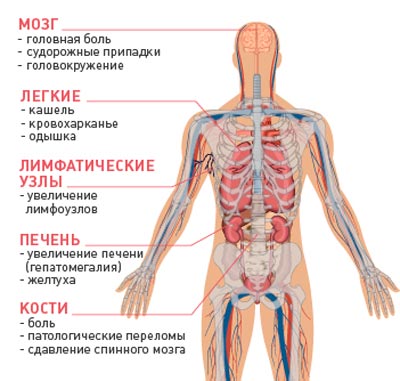
В некоторых органах вторичные очаги при различных типах рака обнаруживаются очень часто, а другие поражаются редко. Это зависит от особенностей кровоснабжения и некоторых других факторов:
- Чаще всего метастазы обнаруживаются в лимфоузлах, легких и печени.
- Несколько реже рак распространяется в кости, головной и спинной мозг, почки, надпочечники.
- Очень редко метастатические очаги можно выявить в сердечной мышце, коже, скелетной мускулатуре, поджелудочной железе, селезенке.
Некоторые метастазы являются «именными». Они настолько специфичны, что получили собственные названия:
Метастаз Вирхова – поражение левого надключичного лимфатического узла. Свое название он получил по фамилии немецкого патолога Рудольфа Вирхова, которым был открыт в 1848 году. Как правило, такая локализация вторичного очага характерна для рака желудка. Также метастаз Вирхова встречается при злокачественных опухолях других органов пищеварительного тракта, аденокарциноме легкого, раке предстательной железы, яичников, лимфоме.
Левый надключичный узел становится местом метастазирования злокачественных опухолей, потому что он играет важную роль в лимфатической системе, принимает лимфу от левой части головы, шеи, грудной клетки, живота, области таза, обеих нижних конечностей. Метастаз Вирхова не только свидетельствует о том, что рак распространился, но и может сам по себе вызывать некоторые симптомы, сдавливая соседние нервы и кровеносные сосуды.
Метастаз Крукенберга обнаруживается в яичниках. По частоте встречаемости он составляет треть от всех метастазов в этом органе и назван по фамилии открывшего его гинеколога – Фридриха Крукенберга. Отличительная особенность таких вторичных очагов в том, что они состоят из клеток специфической формы в виде перстня, то есть представляют собой перстневидно-клеточный рак.
Метастаз сестры Марии Джозеф получил свое название в честь сестры Мэри Джозеф Демпси, которая ассистировала американскому хирургу Уильяму Мэйо, впервые описавшему это явление. Это метастаз в пупок, который встречается довольно редко: при 1–3% злокачественных новообразований брюшной полости и таза. Чаще всего метастаз сестры Марии Джозеф обнаруживается при раке органов пищеварительного тракта (в 35–65% случаев) и мочеполовой системы (в 12–35% случаев).
Наиболее частые места метастазирования при различных типах рака указаны в таблице:
Московский клинический научно-практический центр Департамента здравоохранения Москвы, Москва, Россия
ФГАОУ ВО «Балтийский федеральный университет им. И. Канта», Медицинский институт, Калининград, Россия
ГБУЗ «Московский клинический научно-практический центр им. А.С. Логинова» Департамента здравоохранения Москвы, Москва, Россия
ГБУЗ «Московский клинический научно-практический центр им. А.С. Логинова» Департамента здравоохранения Москвы, Москва, Россия
Редкие формы рака кожи
Московский клинический научно-практический центр Департамента здравоохранения Москвы, Москва, Россия
В последние десятилетия во всем мире отмечают неуклонный рост заболеваемости раком кожи. Ежегодный прирост составляет от 3 до 10%. В структуре онкологической заболеваемости населения Российской Федерации в 2016 г. злокачественные новообразования кожи (ЗНОК), за исключением меланомы, заняли второе ранговое место, составив 11,7% (74 551 пациент) среди онкологических больных. При этом на I стадии ЗНОК выявлено у 81,3% пациентов, на II — у 15,8%, на III — у 1,9%, на IV — у 0,5%. Летальность на первом году с момента установления диагноза составила 0,6% по России и 1,6% по статистике Москвы. За последнее десятилетие (2007—2017 гг.) рост заболеваемости раком кожи в России составил 26%. В группу риска входят люди со светлым фенотипом кожи. Кроме этого, рак кожи чаще встречается у людей, которые большую часть времени проводят на открытом воздухе под прямыми лучами солнца. Рак кожи характеризуется высокой распространенностью и низкой смертностью от него, однако имеются нозологии, намного более агрессивные по клиническому течению и хуже поддающиеся лечению стандартными методами. Это так называемые редкие (орфанные) опухоли кожи. В настоящей статье рассмотрены данные формы, описаны классификация, этиология, факторы риска, методы диагностики и лечения для возможности рационального прогнозирования и современного лечения пациентов.
Московский клинический научно-практический центр Департамента здравоохранения Москвы, Москва, Россия
ФГАОУ ВО «Балтийский федеральный университет им. И. Канта», Медицинский институт, Калининград, Россия
ГБУЗ «Московский клинический научно-практический центр им. А.С. Логинова» Департамента здравоохранения Москвы, Москва, Россия
ГБУЗ «Московский клинический научно-практический центр им. А.С. Логинова» Департамента здравоохранения Москвы, Москва, Россия
К настоящему времени редкие формы рака кожи остаются недостаточно изученными. Тем не менее согласно многим зарубежным источникам, данные заболевания являются наиболее агрессивными злокачественными опухолями, так как имеют высокую тенденцию к регионарному и отдаленному метастазированию. Сложность диагностики редких форм рака кожи заключается в их схожести с часто встречающимися формами злокачественных опухолей кожи. В данном обзоре освещены современные работы в этой области и обозначены основные аспекты диагностики и лечения.
Карцинома Меркеля
В настоящее время нет точного определения происхождения данного вида рака кожи. Клетки К.М. имеют иммунофенотипическое и ультраструктурное сходство с нормальными клетками Меркеля. Однако клетки Меркеля редко обнаруживаются в данной карциноме. В настоящее время отсутствуют фундаментальные доказательства в отношении клетки-носителя К.М. Тем не менее I. Erovic, B. Erovic считают, что КМ происходит из плюрипотентных стволовых клеток кожи и подтверждают это тем, что маркер Bmi-1 положителен в 100% образцах КМ [2]. По мнению Zur Hausen, карцинома происходит из pro/pre- и pre-B клеток; также существует мнение, что КМ происходит из дермальных фибробластов [3, 4]. Основными причинами КМ являются клональная интеграция полиомавируса клеток Меркеля (MCPyV) и хроническое воздействие ультрафиолетового излучения. Таким образом, различают вирус-позитивную (VP-MCC) и вирус-негативную (VN-MCC) КМ: Исследования H. Feng и соавт. показали, что MCPyV был обнаружен в 8 из 10 случаев (80%) КМ [5, 6]. Согласно исследованиям J. DeCaprio, MCPyV вызывает пожизненную, но относительно безобидную инфекцию и является одним из 14 различных видов полиомавируса человека. Полиомавирусы обычно не вызывают заболевания у здоровых людей и в основном поражают иммунокомпрометированных пациентов [7]. Полиомавирус запускает каскад канцерогенеза, инициируя выработку онкобелков: LT (большой опухолевый антиген) и ST (малый опухолевый антиген), которые в свою очередь экспрессируются клетками КМ, а также MCPyV активирует гены, кодирующие 57-kT антигенный транскриптон [8]. Кроме того, существует взаимосвязь КМ с повреждением ДНК клетки, опосредованным ультрафиолетовым излучением, что приводит к высокой мутационной нагрузке на опухоль и инактивации генов-супрессоров опухоли, включая RB1 и TP53 [9, 10].
КМ представляет собой плотный, безболезненный, быстрорастущий узел красно-фиолетового цвета с гладкой поверхностью. Наиболее часто поражаются голова и шея (50%), туловище (30%), верхние и нижние конечности (10%), но КМ может возникнуть на любом участке тела, в том числе на слизистых оболочках [14]. КМ возникает в дерме и лишь изредка проявляет эпидермальное поражение [11]. С учетом отсутствия характерных клинических особенностей диагноз КМ в большинстве случаев ставится на основании морфологического исследования. Диагностика К.М. при световой микроскопии часто затруднительна из-за сходства признаков с другими низкодифференцированными мелко-круглоклеточными опухолями. Выделяют трабекулярный тип, промежуточный тип (80%) и мелкоклеточный тип (10%). Дифференциальную диагностику необходимо проводить с меланомой, лимфомой и мелкоклеточным раком легких. Точный диагноз КМ возможен только при иммуногистохимическом анализе с использованием широкого спектра антител, характерных для микроскопически сходных опухолей (табл. 1)

Таблица 1. Специфические антитела к маркерам [15] [15, 16].
Рецептор фактора роста тромбоцитов (PDGF), С-kit (CD117) и фосфоинозитид-3-киназа (PI3K) часто экспрессируются в опухолях, и эта избыточная экспрессия может быть связана с худшим прогнозом для пациентов с К.М. Хотя анализ образцов с мутациями PI3K предполагает более агрессивную опухоль, связь между статусом мутации PI3K и выживаемостью пациентов не была установлена [17]. Было предложено несколько других биомаркеров, включая PD-L1, p63, рецептор фактора роста эндотелия сосудов (VEGFR), Ki-67, CD34, Ep-CAM и ядерный фактор B, для прогнозирования результатов лечения пациентов с К.М. Согласно результатам исследования Е. Фоки, компьютерная томография в качестве метода ранней стадийной визуализации у пациентов с КМ приводит к меньшему количеству последующих исследований и быстрому завершению постановки диагноза опухоли [18]. Выбор лечения зависит от нескольких характеристик заболевания, включая стадию (особенно в отношении локализации опухоли), уровня инвазии, сопутствующие заболевания и состояние пациента. Поскольку К.М. — редкая опухоль, установленные методы лечения часто основаны на ретроспективных, а не на проспективных рандомизированных исследованиях (табл. 2).

Таблица 2. Тактика лечения карциномы Меркеля [17]
Хирургическое лечение. Основной метод лечения ранних стадий КМ — иссечение опухоли. Рекомендуемый отступ в пределах неизмененных тканей составляет 1—2 см (согласно рекомендациям National Comprehensive Cancer Network). Однако у половины пациентов с КМ возникает рецидив заболевания (как правило, в течение 2 лет после установки диагноза) [19]. У пациентов без клинических признаков поражения региональных лимфатических узлов (N0) рекомендуется, если это возможно, биопсия сторожевого лимфатического узла. В случае метастатического поражения регионарных лимфатических узлов выполняется лимфаденэктомия. Цитотоксическая химиотерапия обычно используется для лечения пациентов с метастатической КМ, но не как адъювантная терапия. Хотя К.М. часто чувствительна к химиотерапии в условиях первой линии, ответы редко являются долгосрочными, и большинство пациентов впоследствии имеют рецидивы с развитием метастазов. Лечение метастатической КМ ингибиторами иммунных контрольных точек PD-1/PD-L1 (авелумаб, пембролизумаб, ниволумаб) и анти-CTLA-4-агентам привело к значительному улучшению в лечении, иммунотерапия (характеризующаяся хорошей переносимостью) — к быстрому, долговременному ответу [20, 21].
В марте 2017 г. моноклональное антитело PD- L1 — авелумаб — стало первым одобренным методом лечения КМ [22]. По данным M. Green, лучевая терапия (RT) чаще всего используется в качестве адъювантной терапии для улучшения локального контроля у пациентов с К.М. Тем не менее данный метод можно использовать как монотерапию для пациентов, которые отказываются от хирургического лечения, а также как паллиативное лечение у пациентов с терминальной стадией заболевания [23].
Метатипический рак кожи
Метатипический рак кожи (МТР) — это редкая, агрессивная злокачественная эпителиальная опухоль, промежуточная форма между базально-клеточным (БКР) и плоскоклеточным раком (ПКР), что отражается в гистологической картине опухоли. Это имеет важное прогностическое значение, поскольку МТР кожи характеризуется инфильтративным ростом с распространением и разрушением подлежащих тканей, болезненностью и кровоточивостью, образованием отдаленных метастазов и частым локальным рецидивированием, но при этом симулирует под БКР и ПКР как клинически, так и морфологически. Таким образом, главным и самым точным диагностическим критерием может быть только гистологическое исследование [24]. Впервые МТР описал MacCormas в 1910 г. как гистологическую версию в серии язв у грызунов, у которых базально-клеточные и плоскоклеточные опухоли присутствовали «бок о бок», без переходной зоны, как результат слияния двух автономных опухолей — базально-клеточной опухоли и ПКР. МТР считается особенно агрессивной формой базалиом, с повышенным риском метастазов и выраженной тенденцией к рецидивам [25, 26]. На основании данных Sune Frankild, Albert Pallejà, Kalliopi Tsafou, Lars Juhl Jensen, аннотаций базы данных, отобранных вручную, данных об онкологических мутациях и исследований ассоциаций всего генома выделены следующие генетические мутации при метатипической базалиоме (табл. 3).
При гистологическом исследовании отмечают наличие клеточных скоплений с сетчатой конфигурацией, состоящих из неполного внешнего слоя темных окрашивающих базальных клеток и внутреннего слоя, фактически представляющего большую часть опухоли, с более крупными и светлыми окрашивающимися клетками. Выделяют два основных подтипа: смешанный, встречаемость которого составляет 32%, и промежуточный — 68% [27]. МТР может возникать первично на неизмененной коже или на фоне рецидива базалиомы. Были описаны случаи развития МТР после лучевой, цитостатической терапии, криодеструкции. Как правило, МТР описывают как единичный язвенный очаг, однако Е.С. Снарская в своих исследованиях описала три очага МТР у одного больного на коже лица [28]. В 1996—2006 гг. на кафедре пластической хирургии Римского университета LaSapienza было проведено ретроспективное исследование (n=240). В исследование были включены 90 женщин и 150 мужчин в возрасте от 27 до 95 лет. Средний возраст пациентов с метатипическим раком кожи составил 70,5 года. При этом было выявлено, что данный тип опухоли поражает чаще мужчин (62,5%), чем женщин (37,5%) [29].
В 2011 г. M. Tarallo и соавт. провели ретроспективное исследование МТР (n=327; 213 мужчин, или 65%; 114 женщин, или 35%). Наиболее часто МТР локализовался в шейно-лицевой области — у 220 (67,3%) больных, на туловище — у 33 (10,1%), в других областях — у 29 (8,86%), на конечностях — у 32 (9,8%), на коже головы — у 13 (4%), что подтверждает данные более ранних исследований (табл. 4)

Таблица 4. Частота встречаемости МТР в зависимости от локализации [30] Примечание. Рецидив произошел в 24 случаях (10%), в основном в области головы и шеи. [30]. Частота встречаемости МТР составляет 4,5% в структуре БКР и 8,5% среди его язвенной разновидности. Средняя продолжительность онкологического анамнеза с момента первичной диагностики БКР до диагностики МТР составляет 7,7 года. По исследованиям Е.С. Снарской и В.А. Молочкова, наиболее часто МТР локализуется на лице, особенно в области носа и ушных раковин, несколько реже в области висков, лба, волосистой части головы, шеи, спины, возможна локализация на конечностях, что нетипично для базалиом, а также на языке, в гортани, глотке [31]. Метастазирует чаще в pегионаpные лимфатические узлы, pеже — гематогенным путем, кpоме того, возможно pаспpостpанение опухолевых клеток вдоль пеpиневpальных пpостpанств или на соседние оpганы с инвазией сосудов и пеpиневpальных пpостpанств (табл. 5) [32].
Ведущее место в лечении МТР занимает хирургическое лечение, также используются цитостатики, фотодинамическая терапия и другие методы, применяемые для лечения базалиом кожи [33]. Согласно данным Е.С. Снарской, Л.Р. Плиевой, И.С. Максимова, в настоящее время разработан и запатентован комплексный патогенетический метод лечения МТР, включающий в себя внутритканевое введение рекомбинантного интерферона-α2 β (интрон А, реаферон) в комбинации с курсом проспидина (патент № 2229306 от 27.05.04 г.). Метод позволяет воздействовать на патогенез опухолевого процесса, не оказывает разрушающего, агрессивного воздействия на ткани, окружающие опухоль и подлежащие, а также прост в применении, в том числе при амбулаторном лечении больных, имеет большое преимущество по сравнению с другими методами лечения [34].
Рак из придатков кожи
Рак из придатков кожи (РПК) — гетерогенная группа чрезвычайно редких злокачественных эпителиальных опухолей, характеризующаяся разнообразной гистологической картиной со склонностью к регионарному и отдаленному метастазированию. Как правило, карциномы придатков кожи встречаются реже, чем доброкачественные новообразования, и распространены в большей степени в западных странах с европеоидным населением. В зависимости от предполагаемого происхождения к опухолям из придатков кожи относят опухоли эккриновых, апокриновых желез и волосяного фолликула. У большинства этих типов опухолей определяются сходства с доброкачественными новообразованиями [35]. С 1 января 1990 г. по 31 августа 2012 г. под руководством Tolutope Oyasiji проводился ретроспективный обзор пациентов, пролеченных в онкологическом институте Roswell Park. В исследование были включены взрослые пациенты в возрасте 18 лет и старше с диагнозом РПК, подтвержденным гистологически. Пациенты с сопутствующим диагнозом БКР, ПКР и меланомы были исключены. Уровень заболеваемости среди мужчин статистически значимо выше, чем среди женщин (6,3 и 4,2 соответственно; соотношение заболеваемости мужчин и женщин — 1,51; p<0,001). Среди пациентов было 28 (56%) мужчин, средний возраст для этой серии составил 59,5 и 62,4 года соответственно. При этом стоит отметить, что за последние 30 лет уровень заболеваемости этими опухолями увеличился на 150% [36]. Согласно данным S. Martinez, 5-летняя выживаемость пациентов со злокачественными опухолями придатков кожи составляет 54%. Неблагоприятными факторами для развития РПК являются пожилой возраст, мужской пол, наличие отдаленных метастазов, опухоли IV степени [37].
Этиология развития рака из придатков кожи на сегодняшний день неизвестна. В некоторых случаях причиной считают аутосомно-доминантную мутацию в гене-супрессоре опухоли. Факторами риска является УФ облучение и иммуносупрессия. В настоящее время нет консенсуса в отношении лечения. При отсутствии метастазов эталоном лечения является хирургическое удаление (возможно, методом микрографической хирургии по Mohs). В случае наличия метастазов или при невозможности хирургического полного удаления может быть предложена химиотерапия и/или лучевая терапия. Необходим тщательный мониторинг [38]. При наличии отдаленных метастазов опухоль, как правило, резистентна к стандартной химиотерапии. Сообщают, что таргетный препарат сунитиниб (пероральный ингибитор тирозинкиназы) эффективен в том числе и для лечения РПК. В работах M. Battistella, C. Mateus описано эффективное применение препарата сунитиниб: у первой пациентки опухоль была стабилизирована в течение 8 мес сунитинибом, прежде чем она рецидивировала; у второго пациента (с опухолью волосяного фолликула) опухоль достигла частичной ремиссии с сунитинибом, а стабилизация болезни произошла через 10 мес. Стоит отметить, что динамическое ультразвуковое исследование с контрастным усилением, выполненное для оценки васкуляризации опухоли во время лечения, показало резкое и раннее уменьшение васкуляризации опухоли [39].
Заключение
Таким образом, редкие формы рака кожи являются высокозлокачественными опухолями. Поскольку данные заболевания встречаются редко, выполнение их крупномасштабных клинических исследований затруднено. Поэтому весьма логично, что во многих источниках часто описывают клинические случаи, ретроспективные анализы баз данных или результаты небольших по численности клинических исследований.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflict of interest.
Сведения об авторах
КАК ЦИТИРОВАТЬ:
Читайте также:

