Можно ли кварцевать опоясывающий лишай
Обновлено: 22.04.2024
Вспомогательные вещества: лактозы моногидрат, кремния диоксид коллоидный (аэросил), повидон К-17 (поливинилпирролидон низкомолекулярный), крахмал картофельный, магния стеарат.
Описание
Фармакотерапевтическая группа
Код АТХ
Фармакодинамика:
Ацикловир - это синтетический аналог пуринового нуклеозида который обладает способностью ингибировать in vitro и in vivo вирусы герпеса человека включая вирус простого герпеса (ВПГ) 1 -го и 2-го типов вирус ветряной оспы и опоясывающего герпеса (варицелла-зостер вирус Varicella zoster virus (ВЗВ)) вирус Эпштейна-Барр (ЭБВ) и цитомегаловирус (ЦМВ). В культуре клеток ацикловир обладает наиболее выраженной противовирусной активностью в отношении ВПГ-1 далее в порядке убывания активности следуют: ВПГ-2 ВЗВ ЭБВ и ЦМВ.
Ингибирующее действие ацикловира на вирусы герпеса (ВПГ-1 ВПГ-2 ВЗВ ЭБВ и ЦМВ) имеет высокоизбирательный характер. Ацикловир не является субстратом для фермента тимидинкиназы неинфицированных клеток поэтому ацикловир малотоксичен для клеток млекопитающих. Тимидинкиназа клеток инфицированных вирусами ВПГ ВЗВ ЭБВ и ЦМВ превращает ацикловир в ацикловирмонофосфат - аналог нуклеозида который затем последовательно превращается в дифосфат и трифосфат под действием клеточных ферментов. Включение ацикловиртрифосфата в цепочку вирусной ДНК и последующий обрыв цепи блокируют дальнейшую репликацию вирусной ДНК.
У пациентов с выраженным иммунодефицитом длительные или повторные курсы терапии ацикловиром могут приводить к появлению резистентных штаммов поэтому дальнейшее лечение ацикловиром может быть неэффективным. У большинства выделенных штаммов со сниженной чувствительностью к ацикловиру отмечалось относительно низкое содержание вирусной тимидинкиназы нарушение структуры вирусной тимидинкиназы или ДНК-полимеразы.
Воздействие ацикловира на штаммы вируса простого герпеса (ВПГ) in vitro также может приводить к образованию менее чувствительных к нему штаммов. Не установлена корреляция между чувствительностью штаммов вируса простого герпеса (ВПГ) к ацикловиру in vitro и клинической эффективностью препарата.
Фармакокинетика:
Ацикловир только частично абсорбируется из кишечника. После приема 200 мг ацикловира каждые 4 часа средняя максимальная равновесная концентрация в плазме (Cssmax) составляла 31 мкМ (07 мкг/мг) а средняя равновесная минимальная концентрация в плазме (Cssmin) была 18 мкМ (04 мкг/мл). При приеме 400 мг и 800 мг ацикловира каждые 4 часа Cssmax составляла 53 мкМ (12 мкг/мл) и 8 мкМ (18 мкг/мл) соответственно a Cssmin 27 мкМ (06 мкг/мл) и 4 мкМ (09 мкг/мл) соответственно.
Концентрация ацикловира в спинномозговой жидкости составляет приблизительно 50% от его концентрации в плазме крови.
С белками плазмы крови ацикловир связывается в незначительной степени (9-33%) поэтому лекарственные взаимодействия вследствие вытеснения из участков связывания с белками плазмы крови маловероятны.
У взрослых после приема ацикловира внутрь период полувыведения из плазмы крови составляет около 3 ч. Большая часть препарата выводится почками в неизмененном виде. Почечный клиренс ацикловира значительно превышает клиренс креатинина что свидетельствует о выведении ацикловира посредством не только клубочковой фильтрации но и канальцевой секреции. Основным метаболитом ацикловира является 9-карбоксиметоксиметилгуанин на долю которого в моче приходится около 10-15% введенной дозы препарата.
При назначении ацикловира через 1 ч после приема 1 г пробенецида период полувыведения ацикловира и AUC (площадь под фармакокинетической кривой "концентрация - время") увеличивались на 18% и 40% соответственно.
Особые группы пациентов
У пациентов с хронической почечной недостаточностью период полувыведения ацикловира составлял в среднем 195 ч. При проведении гемодиализа средний период полувыведения ацикловира составлял 57 ч. Концентрация ацикловира в плазме крови во время диализа снижалась приблизительно на 60%.
У пожилых пациентов клиренс ацикловира с возрастом снижается параллельно со снижением клиренса креатинина однако период полувыведения ацикловира изменяется незначительно.
При одновременном введении ацикловира и зидовудина ВИЧ-инфицированным пациентам фармакокинетические характеристики обоих препаратов практически не изменялись.
Показания:
- Лечение инфекций кожи и слизистых оболочек вызванных вирусом простого герпеса включая первичный и рецидивирующий генитальный герпес;
- профилактика рецидивов инфекций вызванных вирусом простого герпеса у пациентов с нормальным иммунным статусом;
- профилактика инфекций вызванных вирусом простого герпеса у пациентов с иммунодефицитом;
- лечение ветряной оспы и опоясывающего герпеса (раннее лечение опоясывающего герпеса ацикловиром оказывает анальгезирующий эффект и может снизить частоту возникновения постгерпетической невралгии).
Противопоказания:
Повышенная чувствительность к ацикловиру валацикловиру или какому-либо вспомогательному веществу препарата дефицит лактазы непереносимость лактозы глюкозо-галактозная мальабсорбция.
Детский возраст до 3 лет (для данной лекарственной формы).
С осторожностью:
Беременность период грудного вскармливания пожилой возраст почечная недостаточность дегидратация одновременное применение с другими нефротоксичными препаратами.
Беременность и лактация:
Нет данных о влиянии ацикловира на женскую фертильность.
В исследовании с участием 20 пациентов мужского пола с нормальным количеством сперматозоидов было установлено что применение ацикловира внутрь в дозе до 1 г в сутки в течение 6 месяцев не имело клинически значимого влияния на количество подвижность или морфологию сперматозоидов.
В пострегистрационном реестре беременностей при лечении ацикловиром собраны данные об исходах беременности у женщин принимавших ацикловир в разных лекарственных формах. При анализе данных реестра не было отмечено увеличения количества врожденных дефектов у новорожденных матери которых принимали ацикловир во время беременности по сравнению с общей популяцией. Выявленные врожденные дефекты не отличались единообразием или закономерностью позволяющими предположить общую причину их возникновения.
Однако следует соблюдать осторожность при назначении препарата Ацикловир женщинам в период беременности и оценивать предполагаемую пользу для матери и возможный риск для плода.
Период грудного вскармливания
После приема препарата Ацикловир внутрь в дозе 200 мг 5 раз в сутки ацикловир определялся в грудном молоке в концентрации составляющей от 60 до 410% плазменной концентрации. При таких концентрациях в грудном молоке дети находящиеся на грудном вскармливании могут получать ацикловир в дозе до 03 мг/кг/сут. Учитывая это следует соблюдать осторожность при назначении препарата Ацикловир кормящим женщинам.
Способ применения и дозы:
Препарат Ацикловир таблетки можно принимать во время еды поскольку прием пищи не нарушает в значительной степени его абсорбцию. Таблетки следует запивать полным стаканом воды.
Взрослые
Лечение инфекций вызванных вирусом простого герпеса
Для лечения инфекций вызванных вирусом простого герпеса рекомендуемая доза препарата Ацикловир составляет 200 мг 5 раз в сутки (каждые 4 часа за исключением периода ночного сна). Обычно курс лечения составляет 5 дней но может быть продлен при тяжелых первичных инфекциях.
В случае выраженного иммунодефицита (например после трансплантации костного мозга) или при нарушении всасывания из кишечника доза препарата Ацикловир для приема внутрь может быть увеличена до 400 мг. В качестве альтернативы может быть рассмотрена возможность применения препарата Ацикловир в лекарственной форме лиофилизат для приготовления раствора для инфузий.
Лечение необходимо начинать как можно раньше после возникновения инфекции; при рецидивах препарат рекомендуется назначать уже в продромальном периоде или при появлении первых элементов сыпи.
Профилактика рецидивов инфекций вызванных вирусом простого герпеса у пациентов с нормальным иммунным статусом
Для профилактики рецидивов инфекций вызванных вирусом простого герпеса у пациентов с нормальным иммунным статусом рекомендуемая доза препарата Ацикловир составляет 200 мг 4 раза в сутки (каждые 6 часов).
Многим пациентам подходит более удобная схема терапии 400 мг 2 раза в сутки (каждые 12 часов).
В ряде случаев оказываются эффективными более низкие дозы препарата Ацикловир 200 мг 3 раза в сутки (каждые 8 часов) или 200 мг 2 раза в сутки (каждые 12 часов).
У некоторых пациентов может произойти обострение инфекции при приеме суммарной суточной дозы 800 мг.
Лечение препаратом Ацикловир следует периодически прерывать на 6-12 месяцев для выявления возможных изменений течения заболевания.
Профилактика инфекций вызванных вирусом простого герпеса у пациентов с иммунодефицитом
Для профилактики инфекций вызванных вирусом простого герпеса у пациентов с иммунодефицитом рекомендуемая доза препарата Ацикловир составляет 200 мг 4 раза в сутки (каждые 6 часов).
В случае выраженного иммунодефицита (например после трансплантации костного мозга) или при нарушении всасывания из кишечника доза препарата Ацикловир может быть увеличена до 400 мг внутрь. В качестве альтернативы может быть рассмотрена возможность применения препарата Ацикловир в лекарственной форме лиофилизат для приготовления раствора для инфузий. Продолжительность профилактического курса терапии определяется длительностью периода когда существует риск инфицирования.
Лечение ветряной оспы и опоясывающего герпеса
Для лечения ветряной оспы и опоясывающего герпеса рекомендуемая доза препарата Ацикловир составляет 800 мг 5 раз в сутки (каждые 4 часа за исключением периода ночного сна). Курс лечения составляет 7 дней.
У пациентов с тяжелым иммунодефицитом (например после трансплантации костного мозга) или при нарушении всасывания из кишечника необходимо рассмотреть возможность назначения препарата Ацикловир в лекарственной форме лиофилизат для приготовления раствора для инфузий.
Лечение опоясывающего герпеса следует начинать как можно раньше после появления высыпаний так как в этом случае лечение будет более эффективным.
Лечение ветряной оспы у пациентов с нормальным иммунным статусом следует начать в течение 24 часов с момента появления высыпаний.
Особые группы пациентов
Дети в возрасте от 3 лет и старше
Лечение инфекций вызванных вирусом простого герпеса; профилактика инфекций вызванных вирусом простого герпеса у пациентов с иммунодефицитом
- в возрасте от 3 лет и старше применяют такие же дозы как для взрослых.
Лечение ветряной оспы
- в возрасте от 6 лет и старше - 800 мг 4 раза в сутки;
- в возрасте от 3 до 6 лет - 400 мг 4 раза в сутки.
Более точно дозу можно определить из расчета 20 мг/кг массы тела (но не более 800 мг) 4 раза в сутки. Курс лечения составляет 5 дней.
Профилактика рецидивов инфекций вызванных вирусом простого герпеса у пациентов с нормальным иммунным статусом; лечение опоясывающего герпеса
Данные о режиме дозирования отсутствуют.
Пациенты пожилого возраста
Необходимо учитывать вероятность наличия почечной недостаточности у пациентов пожилого возраста дозы должны быть скорректированы в соответствии со степенью почечной недостаточности ( см. подраздел "Пациенты с нарушением функции почек").
Необходимо обеспечить поддержание адекватного водного баланса.
Пациенты с нарушением функции почек
Необходимо соблюдать осторожность при назначении препарата Ацикловир пациентам с нарушением функции почек.
Необходимо обеспечить поддержание адекватного водного баланса.
У пациентов с почечной недостаточностью прием ацикловира внутрь в рекомендуемых дозах с целью лечения и профилактики инфекций вызванных вирусом простого герпеса не приводит к кумуляции препарата до концентраций превышающих установленные безопасные уровни. Однако у пациентов с клиренсом креатинина менее 10 мл/мин дозу препарата Ацикловир рекомендуется снижать до 200 мг 2 раза в сутки (каждые 12 часов).
При лечении ветряной оспы и опоясывающего герпеса рекомендуемые дозы препарата Ацикловир таблетки составляют:
- при клиренсе креатинина менее 10 мл/мин - 800 мг 2 раза в сутки (каждые 12 часов);
- при клиренсе креатинина 10-25 мл/мин - 800 мг 3 раза в сутки (каждые 8 часов).
Побочные эффекты:
Использована следующая классификация нежелательных реакций в зависимости от частоты встречаемости: очень часто (≥1/10) часто (≥1/100 и
Со стороны кроветворения и лимфатической системы: очень редко - анемия лейкопения тромбоцитопения.
Со стороны иммунной системы:редко - анафилаксия.
Со стороны нервно-психического статуса: часто - головная боль головокружения; очень редко - возбуждение спутанность осознания тремор атаксия дизартрия галлюцинации психотические симптомы судороги сонливость энцефалопатия кома.
Обычно эти побочные эффекты наблюдались у пациентов с почечной недостаточностью или при наличии других провоцирующих факторов и были в основном обратимыми.
Со стороны дыхательной системы органов грудной клетки и средостения: редко - одышка.
Со стороны желудочно-кишечного тракта: часто - тошнота рвота диарея боль в животе.
Со стороны печени и желчевыводящих путей: редко - обратимое увеличение билирубина и печеночных ферментов в крови; очень редко - гепатит желтуха.
Со стороны кожи и подкожной клетчатки: часто - зуд сыпь в том числе фотосенсибилизация; нечасто - крапивница быстрое диффузное выпадение волос.
Поскольку такой тип алопеции наблюдается при различных заболеваниях и при терапии многими лекарственными средствами связь ее с приемом ацикловира не установлена; редко - ангионевротический отек; очень редко - токсический эпидермальный некролиз мультиформная экссудативная эритема.
Со стороны мочевыделительной системы: редко - повышение концентрации мочевины и креатинина в сыворотке крови; очень редко - острая почечная недостаточность почечная колика. Почечная колика может быть связана с почечной недостаточностью и кристаллурией.
Другие: часто - утомляемость лихорадка.
Передозировка:
Иногда могут наблюдаться такие неврологические эффекты как судорожные припадки кома.
Пациенты нуждаются в тщательном медицинском наблюдении с целью выявления возможных симптомов интоксикации. Ацикловир выводится из организма с помощью гемодиализа поэтому гемодиализ может быть использован для лечения передозировки.
Взаимодействие:
Никаких клинически значимых взаимодействий при применении препарата Ацикловир не отмечалось.
Ацикловир выводится в неизмененном виде с мочой путем активной канальцевой секреции. Все препараты с аналогичным путем выведения могут повышать плазменную концентрацию ацикловира.
Ацикловир повышает AUC теофиллина приблизительно на 50% при одновременном приеме поэтому рекомендуется измерять плазменные концентрации теофиллина при одновременном назначении ацикловира.
Пробенецид и циметидин увеличивают показатель AUC (площадь под кривой "концентрация - время") ацикловира и снижают его почечный клиренс.
Отмечалось увеличение показателя AUC в плазме крови для ацикловира и неактивного метаболита микофенолата мофетила иммунодепрессанта применяющегося в трансплантологии при одновременном применении обоих препаратов. Однако коррекции дозы не требуется вследствие широкого терапевтического индекса ацикловира.
Особые указания:
Доступных данных полученных в результате проведенных клинических исследований недостаточно чтобы сделать вывод о том что применение ацикловира снижает риск заболевания ветряной оспой у пациентов с нормальным иммунным статусом.
Риск развития почечной недостаточности увеличивается при одновременном применении с другими нефротоксическими препаратами.
Состояние гидратации
Пациенты принимающие высокие дозы препарата Ацикловир внутрь должны получать достаточное количество жидкости.
Пациенты пожилого возраста и пациенты с нарушением функции почек
Поскольку ацикловир выводится почками дозы должны быть уменьшены пациентам с почечной недостаточностью (см. раздел "Способ применения и дозы").
У пациентов пожилого возраста возможно снижение функции почек следовательно для данной группы пациентов также может потребоваться снижение дозы.
Как пожилые пациенты так и пациенты с нарушением функции почек находятся в группе повышенного риска развития побочных эффектов со стороны нервной системы (обычно такие реакции обратимы в ответ на отмену препарата) и соответственно должны находиться под пристальным медицинским наблюдением.
Пациенты с выраженным иммунодефицитом
Длительные или повторные курсы лечения ацикловиром у пациентов с выраженным иммунодефицитом могут привести к появлению штаммов вируса с пониженной чувствительностью к ацикловиру которые не ответят на продолжение терапии ацикловиром.
Передача инфекции
Всем пациентам особенно при наличии клинических проявлений следует соблюдать осторожность во избежание потенциальной возможности передачи вируса а также пациентов необходимо информировать о случаях бессимптомного вирусоносительства.
Влияние на способность управлять трансп. ср. и мех.:
Исследований влияния ацикловира на способность к управлению транспортными средствами или механизмами не проводилось. Спрогнозировать негативное воздействие ацикловира на эти виды деятельности на основании фармакологических свойств действующего вещества не представляется возможным но необходимо учитывать профиль побочного действия ацикловира.
Форма выпуска/дозировка:
Упаковка:
По 10 таблеток в контурную ячейковую упаковку из пленки поливинилхлоридной и фольги алюминиевой.
1 2 4 6 или 10 контурных ячейковых упаковок вместе с инструкцией по применению помещают в пачку из картона.
Условия хранения:
При температуре не выше 25 °С.
Хранить в недоступном для детей месте.
Срок годности:
Не применять по истечении срока годности.
Условия отпуска
Производитель
Акционерное общество "Татхимфармпрепараты" (АО "Татхимфармпрепараты" ), 420091, Республика Татарстан, г. Казань, ул. Беломорская, д. 260, Россия
Владелец регистрационного удостоверения/организация, принимающая претензии потребителей:
Ацикловир таблетки 400 - Татхимфармпрепараты - цена, наличие в аптеках
Указана цена, по которой можно купить Ацикловир таблетки 400 - Татхимфармпрепараты в Москве. Точную цену в Вашем городе Вы получите после перехода в службу онлайн заказа лекарств:
ОПЫТ КОМБИНИРОВАННОГО ЛЕЧЕНИЯ ОСТРОГО ПРОСТОГО ГЕРПЕСА – ПРОТИВОВИРУСНАЯ НАРУЖНАЯ ТЕРАПИЯ И КОРОТКОВОЛНОВОЕ УЛЬТРАФИОЛЕТОВОЕ ИЗЛУЧЕНИЕ. ПРАКТИЧЕСКОЕ НАБЛЮДЕНИЕ
Медицинский центр «Демос», Санкт-Петербург
При воздействии на организм человека электромагнитное поле оптического диапазона в большей степени оказывает свое влияние на его кожный покров. Ответные фотобиологические реакции возникают вследствие поглощения электромагнитной энергии теми тканями, на которые направлен источник излучения. Степень поглощения энергии определяется энергией световых квантов и возрастает с увеличением длины волны используемого излучения.
Ответная реакция биологических тканей проявляется в диапазоне от чисто теплового эффекта до разрушения тех структур, которые облучались. Например, коротковолновое ультрафиолетовое (КУФ) излучение длиной волны 180-280 нм вызывает ионизацию и разрушение ковалентных связей молекул в зоне непосредственного действия данного физического фактора. Это свойство широко применяется в лечебной физиотерапевтической практике.
КУФ-излучение с патогенетической точки зрения при воздействии на кожу и слизистые обладает бактерицидным и микоцидным, а также иммуностимулирующим и катаболическим лечебными эффектами. Благодаря этому одними из показаний для его применения в дерматологической практике являются:
-острые и подострые воспалительные заболевания кожи, в т.ч. инфекционной этиологии;
. раны с опасностью присоединения анаэробной инфекции;
Абсолютным противопоказанием является повышенная чувствительность кожи конкретного пациента к ультрафиолетовому излучению. С осторожностью КУФ-облучение назначается пациентам, принимающим лекарственные препараты, обладающие фотосенсибилизирующим действием.
Одним из заболеваний, часто встречающихся в практике врача-дерматолога, является острый простой герпес. Процесс носит инфекционный характер и проявляется типичным стадийным течением – продрома, стадия клинических проявлений различной степени выраженности, реконвалесценция, ремиссия (носительство).
Нами было пролечено 15 человек с диагнозом «острый простой герпес, экстрагенитальная форма» легкой степени тяжести; на стадии продромы – 4 человека и на стадии начальных клинических проявлений – 11 человек. Противовирусная терапия пероральными препаратами не проводилась.
Лечебная процедура проводилась следующим образом:
- обработка очага поражения (накожно) кожным антисептиком «Октенисепт»;
-местно КУФ-облучение очага поражения 1-1,5 биодозы (на нашем излучателе 1 биодоза составила 3 минуты), расстояние до излучателя 5 см, ежедневно, N 3-5;
-нанесение 5 % противовирусной мази «Ацикловир» или цинк-салициловой пасты в зависимости от стадии вирусного процесса.
В результате проводимого лечения у всех пациентов отмечалось укорочение сроков заболевания до 5-7 дней с полной регрессией клинических проявлений. У 13 человек после однократной процедуры уменьшались болевой синдром, отечность и дискомфортные ощущения в области очага поражения.
Таким образом, учитывая опыт данного практического наблюдения лечения острого простого герпеса комбинированием наружной терапии и лечебной физиотерапевтической методики, можно говорить об успешном их применении в повседневной практике врача-дерматолога с целью быстрого прерывания уже начавшегося инфекционного процесса.

Разработчик сайтов, журналист, редактор, дизайнер, программист, копирайтер. Стаж работы — 25 лет. Область интересов: новейшие технологии в медицине, медицинский web-контент, профессиональное фото, видео, web-дизайн. Цели: максимально амбициозные.
- Запись опубликована: 10.08.2020
- Reading time: 4 минут чтения
Опоясывающий лишай – острое инфекционное заболевание, вызываемое тем же вирусом, который вызывает ветряную оспу. Его течение варьируется в зависимости от состояния организма больного человека. Проявляется чаще всего очень сильной болью и изменениями кожи. Лечение проходит дома, и только в исключительных, крайних случаях необходимо лечение в стационаре.
С чего начинается заражение, как протекает и как с бороться с заболеванием?
Что такое опоясывающий лишай?
Опоясывающий лишай и герпес – самые распространенные вирусные кожные заболевания, вызываемые вирусом герпеса группы вирусов гоминиса. Это ДНК-вирусы, которые размножаются в ядре клетки. Этот же вирус вызывает ветряную оспу. Предполагается, что опоясывающий лишай возникает у тех, кто ранее был инфицирован ветряной оспой.
Подобно вирусам HSV1 и HSV2, вирус ветряной оспы может быть латентным в ганглиях. Когда организм ослаблен, у человека снижается иммунитет, и опоясывающий лишай становится активным. Воспаляются нерв и иннервируемая им кожа, что и вызывает жгучую боль. Боль ощущается по всему пораженному нерву.
Опоясывающий лишай заразен?
Опоясывающим лишаем страдают люди старше 50 лет, а дети среди пациентов встречаются крайне редко. Больной в активный период заболевания заражается напрямую при контакте с поражениями кожи, а иногда и капельно (у контактирующих людей может развиться ветряная оспа).
Тяжелая форма опоясывающего герпеса у молодых людей может быть признаком общего заболевания – лимфоцитарной гиперплазии, ВИЧ-положительного статуса, иммуносупрессии.
В случае опоясывающего лишая, вирус может передаваться главным образом при контакте с жидкостью в пузырьках на коже пациента.
Симптомы опоясывающего лишая
Возникновению кожных поражений при опоясывающем герпесе могут предшествовать продромальные симптомы в виде болезненности в разных областях тела – головная боль, боль в ухе, горле, плече, позвоночнике, животе, в сердце. Боль может предшествовать появлению кожных повреждений, похожих на везикулы при ветряной оспе, примерно в течение 5 дней.

Герпес опоясывающий
Из-за воспаления сенсорного нерва и кожи, которую он иннервирует, возникающая при опоясывающем лишае боль острая, жгучая и очень сильная. Это первые симптомы, указывающие на опоясывающий лишай.
Через несколько дней в том месте, где ранее была сильная боль, появляется сыпь с волдырями. Пятна красные и зудящие. Поражения чаще всего располагаются односторонне вдоль нервов вокруг лица и туловища (наиболее частое расположение также при ветряной оспе).
Примерно через четыре дня появляются новые пузырьки, свидетельствующие о развитии опоясывающего лишая . Со временем они превращаются в прыщики. Они, в свою очередь, через некоторое время, как в случае ветряной оспы, превращаются в струпья, которые постепенно отпадают.

Развитие опоясывающего лишая
Возникновение кожных высыпаний может сопровождаться повышением температуры тела, увеличением окружающих лимфатических узлов. В случае опоясывающего лишая лица, поражения также возможны на слизистой оболочке рта и могут поражать глазное яблоко.
Виды опоясывающего лишая
По течению и клинической картине можно выделить опоясывающий лишай:
Диссеминированная форма может быть признаком нарушения работы иммунной системы, течения общих заболеваний, таких как лимфоцитарная гиперплазия, рак, иммуносупрессия различной этиологии – аутоиммунные заболевания, иммуносупрессивное лечение, ВИЧ-инфекция. Поэтому пациенты с тяжелым или диссеминированным опоясывающим герпесом должны пройти общее обследование для выяснения причины обострения инфекции.
Расчесывать пораженные области нельзя – это вызовет дополнительное бактериальное инфицирование. Для снятия зуда рекомендуется принимать прохладные ванны и антигистаминные препараты.
Дополнительные симптомы, связанные с заболеванием, включают:
- головную боль;
- слабость;
- усталость.
Опоясывающий лишай или оспа?
Как уже упоминалось, и опоясывающий лишай, и ветряная оспа вызываются одним и тем же вирусом. Прежде всего, важно понимать, что эти два заболевания тесно связаны. Первичное заражение вирусом вызывает ветряную оспу . После лечения вирус не выводится из организма, а переходит в состояние покоя в ганглиях. При благоприятных обстоятельствах, когда организм ослаблен, он может активироваться, вызывая опоясывающий лишай.

Ветряная оспа
Как выглядит опоясывающий лишай?
На первый взгляд, опоясывающий лишай выглядит как кожное заболевание. Возникающие на теле везикулы очень напоминают пузырьки, образовавшиеся при ветрянке. Кожа пациента красная и раздраженная.
Обычно поражается одна половина тела, в основном туловище. В редких случаях опоясывающий лишай распространяется на руку, ногу или половину лица. В таких ситуациях, когда прыщики распространяются, они поражают конечность или лицо с той же стороны, что и туловище.
В некоторых, очень редких случаях опоясывающий лишай может пройти без изменений кожи. Тогда диагностировать патологию сложнее, потому что сыпь – самый однозначный признак.
Опоясывающий лишай – что делать, чтобы не заразиться?
Чтобы избежать заражения опоясывающим лишаем, в первую очередь следует избегать прямого контакта с больным ветряной оспой или опоясывающим лишаем. Поскольку вирус распространяется воздушно-капельным путем, достаточно чихать или кашлять, чтобы он проник в тело и начал действовать.
В случае людей, подверженных риску серьезных осложнений, также могут использоваться защитные маски, которые представляют собой своего рода барьер для вирусов. Детям и взрослым, которые до сих пор не болели ветрянкой, следует подумать о вакцинации от ветряной оспы .

Вакцинация от ветряной оспы
Лечение опоясывающего лишая
Лечение опоясывающего лишая должен назначать врач. Во время лечения рекомендуется оставаться дома и соблюдать правила гигиены, чтобы не допустить распространения болезни.
Врач обычно назначает обезболивающие и противовирусные препараты для облегчения симптомов и борьбы с причиной заболевания. Важно, чтобы лекарства давались как можно скорее после появления симптомов. Это значительно увеличивает их эффективность.
Вы не должны принимать какие-либо решения относительно лечения опоясывающего лишая самостоятельно. О любых тревожных симптомах следует сообщать и проконсультироваться с лечащим врачом. Следуя указаниям врача, пациент должен полностью выздороветь через две-три недели.
Врач назначает пероральные препараты : ацикловир, фамцикловир, валацикловир.
- Ацикловир (Зовиракс, Гевиран) следует вводить перорально или внутривенно 5 х 800 мг в течение 7-10 дней.
- Валацикловир 3 х 1000 мг перорально в течение 7 дней.
- Фамцикловир 3 х 500 мг перорально в течение 7 дней.
Внутривенное введение ацикловира более эффективно и должно применяться у пациентов с тяжелым течением опоясывающего лишая вокруг лица с поражением глазных яблок, у пациентов с ослабленным иммунитетом, у пациентов с диссеминированным опоясывающим герпесом.
При местном лечении используются подсушивающие препараты, предотвращающие бактериальные инфекции. Например, аэрозоль Неомицин. Нельзя использовать порошки, компрессы, мази с кортикостероидами.
Однако бывают случаи, когда боль не проходит, даже если сыпь зажила. Это состояние называется невралгией. Особенно это касается пожилых людей – боль может длиться несколько месяцев и даже лет. Заметив у себя такие симптомы, вы должны снова обратиться к врачу, который примет решение о необходимости дополнительной диагностики или лечения.
Применяемое противовирусное лечение не предотвращает развитие постгерпетической невралгии, но может снизить ее тяжесть. Общее лечение начинают в первые 3 дня от появления кожных симптомов или позже, если появляются новые везикулярные изменения.
Лечение постгерпетической невралгии большая проблема. Лекарств для предотвращения симптомов невралгии нет. Первоначально считалось, что введение средних доз кортикостероидов (40 мг) с ацикловиром снизит риск невралгии, но дальнейшие наблюдения не подтвердили это предположение. Лекарства и обезболивающие не уменьшают боль.
Были продемонстрированы благоприятные эффекты при приеме трициклических антидепрессантов (амитриптилин, дезипрамин) и использовании симпатических блокад.
Осложнения опоясывающего лишая
Как правило, опоясывающий лишай должен пройти бесследно. В исключительных случаях, например, могут остаться следы прыщиков в виде рубцов или изменения цвета кожи.
Если у пациента плохое общее состояние, может развиться ряд осложнений, таких как:
- невралгия, гипералгезия кожи – могут сохраняться до 8 месяцев после заживления инфекции;
- временный паралич периферических нервов – птоз, парез конечностей, асимметрия углов рта;
- офтальмологический опоясывающий лишай может развиться в серьезные осложнения, приводящие к тяжелым нарушениям зрения (кератит, склерит, увеит, неврит зрительного нерва);
- нарушение равновесия, слуха, потеря вкуса, светобоязнь.
К наиболее серьезным осложнениям относят офтальмологические изменения, невралгию. Редким, поздним осложнением опоясывающего герпеса может быть гранулематозный васкулит ЦНС, менингит.
Осложнения опоясывающего герпеса можно предотвратить путем вакцинации против оспы (если пациент еще не заразился) и тщательного соблюдения медицинских показаний и рекомендаций, а в крайних случаях – путем лечения пациентов в стационаре под постоянным наблюдением медицинского персонала.
В заключение стоит сказать, что опоясывающий лишай – это инфекционное заболевание. И это особая угроза для взрослых, у которых значительно снижен иммунитет. Дети также подвержены этому заболеванию, но с помощью грамотного лечения они преодолевают болезнь без серьезных осложнений.
У взрослых заболевание длится около четырех недель. Быстрое начало лечения облегчает течение болезни и снижает риск развития осложнений. К рекомендациям врача нельзя относиться легкомысленно, так как осложнения могут быть гораздо серьезнее, чем сам опоясывающий лишай.
Опоясывающий герпес или, как его еще называют, опоясывающий лишай, – одно из самых непонятных для обычного человека заболеваний вирусной природы. Его часто путают с другими видами лишая (розовый, стригущий, чешуйчатый), к которым приводят грибковые инфекции кожи, а также различные аутоиммунные процессы.
В случае опоясывающего лишая к появлению клинических симптомов и высыпаниям на коже приводит вирус герпеса 3 типа, Varicella zoster. Этот вирус также вызывает хорошо известную ветряную оспу. Выходит, что один и тот же вирус вызывает сразу два заболевания? Но как такое может быть? Давайте разбираться!
Когда организм человека встречается с вирусом Varicella zoster впервые, чаще всего развивается ветряная оспа. И обычно это происходит в детском возрасте, хотя в редких случаях заболевание может развиться и у взрослого человека. О том, что происходит, когда вирус дает о себе знать во второй раз, читайте далее. Также узнаете о том, как подобрать лекарство от опоясывающего герпеса.
Всем известно, что вирусы герпеса никогда не покидают организм, и Varicella zoster здесь не исключение. Проникая в скопления нервных клеток, он «впадает в спячку» и часто остается с нами навсегда, никак себя не проявляя. Однако, под воздействием внешних факторов вирус все-таки может «проснуться», вызывая при этом опоясывающий лишай. Также к развитию опоясывающего герпеса может привести контакт с больным ветряной оспой. Это происходит, когда человек, чаще пожилой, у которого снижены показатели иммунитета, контактирует с больным ребенком. Даже самое название вируса представляет интерес: «варицеллой» чаще называют именно ветряную оспу, а «зостер», что в переводе означает «ремень», ассоциируется с лишаем, так как характерная для этого заболевания сыпь появляется именно в области нижней части спины и живота.
Итак, мы выяснили, что опоясывающий герпес (опоясывающий лишай, герпес зостер, herpes zoster, ОГ) является вирусным заболеванием кожи и нервных тканей, которое возникает как результат реактивации вируса герпеса III типа (Human herpesvirus) подсемейства Alphaherpesviridae, семейства Herpesviridae. Встречается он примерно у 15 человек из 100 и проявляется у каждого четвертого взрослого из тех, кто ранее переболел ветряной оспой.
Важно помнить, что опоясывающий герпес у взрослых требует иного подхода к терапии: лекарства, которые педиатр рекомендует детям от ветряной оспы, не помогут. Терапию для лечения опоясывающего герпеса должен назначать врач-терапевт или врач-дерматолог после осмотра пациента и с учетом его анамнеза.
Как вирус герпеса зостер проникает в организм и как проявляется
Чаще всего первичное инфицирование вирусом, вызывающим ОГ, происходит в детском возрасте, когда ребенок заражается ветрянкой воздушно-капельным путем. После выздоровления вирус длительное время продолжает персистировать в области периферических нервных сплетений, спинальных ганглий (ограниченных скоплений нейронов) и ганглий мозга. К реактивации вируса могут привести иммунодефицитные состояния, когда естественная защита ослабевает и заболевание получает возможность «развернуться» в полную мощь.
Главные факторы, которые могут спровоцировать появление ОГ:
- возрастные изменения в организме – согласно данным статистики, это заболевание чаще всего встречается среди людей старше 50 лет;
- аутоиммунные и онкологические заболевания, в том числе сахарный диабет, лучевая и химиотерапия, состояние после тяжелых травм;
- беременность и вследствие этого повышенная нагрузка на организм;
- ВИЧ-инфекция – с ОГ сталкиваются почти 25% ВИЧ-инфицированных лиц, что в восемь раз превышает средний показатель заболеваемости пациентов среднего и старшего возраста;
- трансплантация органов, когда необходим прием иммуносупрессивных препаратов, предназначенных для искусственного угнетения иммунитета в целях предупреждения отторжения органа; i
- рецидив хронических заболеваний, затрагивающих сердечно-сосудистую систему, почки, печень и легкие;
- длительное лечение антибиотиками, цитостатиками, глюкокортикостероидами;
- частые стрессы, отсутствие достаточного отдыха, переутомление, переохлаждение или перегрев.
Опоясывающий герпес: симптомы и лечение
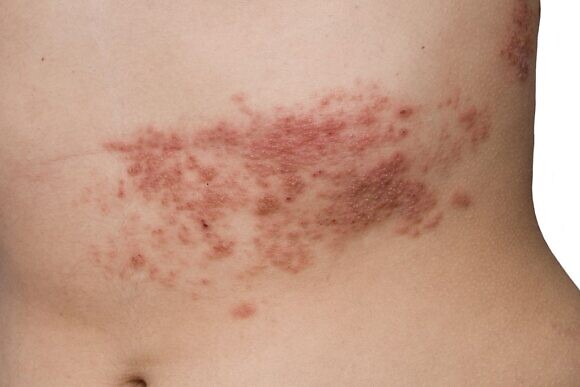
В отличие от ветряной оспы, при опоясывающем лишае не наблюдается резких вспышек заболеваемости, как в детских коллективах, также отсутствует и сезонная зависимость. Хотя некоторые ученые отмечают, что ОГ чаще встречается в теплое время года и поздней осенью. Тяжесть течения заболевания зависит от возраста. Дети, которые тоже болеют опоясывающим лишаем после перенесенной ветрянки, а также лица молодого возраста обычно переносят болезнь более благоприятно, чем пожилые люди.
Среди основных симптомов опоясывающего герпеса – кожные проявления и неврологические расстройства. Большинство инфицированных сталкивается с общеинфекционными клиническими признаками, которые проявляются в виде повышения температуры тела, головной и мышечной боли, тошноты, слабости, увеличения регионарных лимфатических узлов. Интенсивность проявления этих симптомов варьируется у каждого пациента. Продолжительность начального периода составляет примерно четыре-пять дней.
Клинические признаки ОГ могут быть похожими на плеврит, невралгию тройничного нерва и даже синдром острого живота, например, аппендицит, который требует немедленной помощи специалиста. Поэтому при общем плохом самочувствии и появлении на коже высыпаний любой природы необходимо сразу же обратиться к врачу.
В месте высыпаний перед появлением сыпи могут ощущаться легкие зуд и жжение. Потом на коже появляются розовые пятна круглой или неправильной формы, которые не склонны к слиянию, они отечные и немного приподнятые над поверхностью кожи. Затем на коже появляются везикулы с жидким серозным содержимым. Через несколько дней пузырьки подсыхают, на их месте появляются серозные корки, которые со временем отпадают и на их месте появляются пигментированные участки кожи. При правильном лечении снижается температура тела и исчезают симптомы общей интоксикации организма.
Как лечить опоясывающий герпес геморрагической, гангренозной абортивной и других форм
Кроме наиболее часто встречаемой формы опоясывающего лишая, о которой идет речь выше, также встречаются другие, которые могут выглядеть не совсем обычно и даже пугающе для неподготовленного человека. Например, при геморрагической форме везикулы заполняются кровянистым содержимым, поэтому на теле сыпь выглядит как пятна темно-коричневого цвета. Иногда везикулы не заживают бесследно, по разным причинам их дно некротизируется, после чего на коже остаются рубцы. Абортивная форма ОГ характеризуется появлением практически незаметных визуально папул (пузырьки не образуются), поэтому пациент не обращается к врачу.
При буллезной форме пузырьки на коже достаточно крупные, они могут сливаться в единый конгломерат с неровными краями. Их повреждение может приводить к инфицированию ранки, после чего может начаться гнойный процесс. В самых тяжелых случаях везикулы сливаются в обширные области, которые со временем некротизируются. В этом случае речь идет уже о гангренозной форме. Чаще эта форма развивается у пожилых людей, у лиц с язвенной болезнью и сахарным диабетом. В данном случае пациенту может быть необходима госпитализация и комплексное лечение.
Одна из главных целей лечения опоясывающего герпеса у взрослых, которые не требуют лечения в стационаре, – максимально быстрое купирование клинических симптомов заболевания (высыпаний и субъективных ощущений). Это обусловлено тем, что в зависимости от длительности цитопатического (приводящего к дегенеративным изменениям в клеточных структурах) действия вируса варицелла-зостер на клетки пораженных нервов значительно возрастает риск развития постгерпетической невралгии и других осложнений.
Возможные последствия отказа от лечения опоясывающего герпеса
ОГ приводит к многочисленным поражениям периферического и центрального отделов нервной системы. Чаще всего встречается такое осложнение, как постгерпетическая невралгия. Она проявляется в виде сильных болей, которые сохраняются или появляются через несколько недель и даже месяцев после появления первых высыпаний. Человек ощущает жгучие, резкие и приступообразные боли в области расположения сыпи. Этот симптом особенно усиливается по ночам. Особенно часто с таким осложнением болезни сталкиваются пожилые люди. Также встречаются случаи, когда вирус опоясывающего герпеса поражает брюшные мышцы и мочевой пузырь.
Кроме того, ОГ может поразить нервы, которые находятся в черепе. Подобное поражение может затронуть мозговые оболочки, что приводит к массе проблем со здоровьем. Одна из них – это поражение офтальмической ветви тройничного нерва, что неблагоприятно влияет на зрение.
Исследователи утверждают, что персистирующая, т.е. упорно протекающая и периодически вспыхивающая герпетическая инфекция может привести иммунную защиту организма к так называемой клеточной депрессии. Без поддержки в виде правильного лечения и возможности полноценно защитить себя организм может столкнуться с самыми разными осложнениями со стороны функционирования различных органов и систем.
Диагностика и правильное лечение опоясывающего герпеса у взрослых
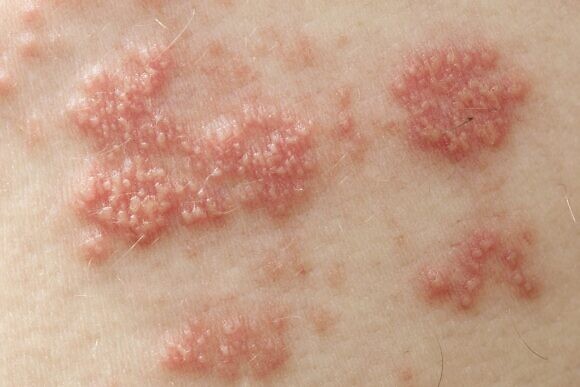
При подозрении на опоясывающий герпес необходимо обращаться к врачу-терапевту для осмотра и начала курса лечения. Также может понадобиться помочь врача-дерматолога и врача-иммунолога, а при выраженном болевом синдроме – врача-невролога.
Диагностика ОГ является преимущественно клинической, для подтверждения диагноза может потребоваться проведение лабораторных исследований. Также необходимо дифференцировать это заболевание от других похожих. Для этой цели широко применяется метод полимеразной цепной реакции (ПЦР), иммуноферментный анализ (ИФА) и иммунофлуоресцентный анализ, которые обычно не оставляют сомнений в диагнозе. Кроме того, могут потребоваться результаты общего и биохимического анализа крови, общего анализа мочи. При развитии генерализованной формы врач может дополнительно назначить анализ на ВИЧ.
Лечение ОГ чаще всего проводят амбулаторно, оно должно быть комплексным и включать как этиологические, так и патогенетические средства. Эффективность терапии во многом зависит от сроков начала лечения: чем раньше вы обратитесь к врачу и начнете лечение, тем быстрее наступит выздоровление и тем ниже будут риски развития осложнений.
Опоясывающий герпес: лечение народными средствами
Не стоит слепо доверять советам родственников и знакомых, не имеющих медицинского образования. Любые настойки, ванночки, растирания и аппликации на кожу могут принести вред, усилить зуд и расширить область появления высыпаний. Ведь во многих случаях народная медицина может не только не помочь избавиться от заболевания, но и быть небезопасной.
Опасность кроется и в том, что во время экспериментов с самолечением заболевание прогрессирует, у человека ухудшается самочувствие и могут развиться осложнения, что усложняет процесс лечения тогда, когда все же появляется решимость обратиться к врачу. Помните, что аргумент «даже если не поможет, то не навредит» в этом случае не работает. При подозрениях на опоясывающий лишай необходимо сразу же обратиться к врачу и начать лечение проверенными лекарственными препаратами.
Опоясывающий герпес: лечение, препараты и методы терапии
В настоящее время все методы лекарственного лечения и профилактики ОГ можно объединить в три основные группы, куда входят химиотерапия (прием ациклических нуклеозидов), иммунотерапия и комбинация этих двух групп, где пациент одновременно принимает химио- и иммуномодулирующие препараты.
Также применяют витамины B1, В6 и В12, аскорбиновую кислоту, рутин и при необходимости – антигистаминные препараты. При сильном болевом симптоме пациенту показан прием НПВП и анальгетиков.
Многие врачи придерживаются мнения, что приема только ациклических нуклеозидов в качестве основного лечения недостаточно, подобная монотерапия себя не оправдала. i Эти препараты наиболее эффективны только в первые 72 часа от начала развития болезни, они способны подавлять только вирусы герпеса в стадии активной репликации – процессе создания двух дочерних молекул ДНК на основе родительской молекулы ДНК. Они не оказывают влияния на те вирусы, которые уже существуют и находятся в латентном, т.е. «спящем» состоянии. Кроме того, ациклические нуклеозиды не помогают восстанавливать иммунитет.
Для лечения опоясывающего герпеса на теле пациентам необходима иммунокоррекция. Поэтому в этом случае будет уместной стратегия сочетания ациклических нуклеозидов и препаратов интерферона альфа-2b, которая признана врачами обоснованной и наиболее эффективной, что отражено в клинических и методических рекомендациях.
Интерфероны – «универсальные» бойцы, которые в отличие от антител не ориентированы на определенные патогены, а представляют неспецифический (врожденный) иммунитет и
способны бороться с любыми вирусными частицами. Интерфероны способны останавливать размножение и распространение вирусных частиц или бактерий.
Противовирусный препарат ВИФЕРОН в лечении опоясывающего герпеса
Одним из препаратов, применяемых для лечения герпеса, является ВИФЕРОН – противовирусный и иммуномодулирующий препарат, который обладает рядом уникальных фармакологических свойств.
ВИФЕРОН в своем составе сочетает рекомбинантный интерферон а-2b и комплекс антиоксидантов (витамины Е и С), в присутствии которых возрастает специфическая противовирусная активность главного действующего вещества, а также усиливается его иммуномодулирующее действие, что позволяет повысить эффективность собственного иммунного ответа организма на патогенные микроорганизмы. ii
Препарат представлен в виде ректальных суппозиториев (свечи), которые обеспечивают системное действие, то есть на весь организм в целом, а также в виде мази и геля, которые способны бороться с вирусами в «воротах» инфекции: в данном случае на поверхности кожи. Наличие как местных, так и системных форм позволяет применять препараты линейки ВИФЕРОН одновременно, усиливая тем самым эффекты проводимой терапии.
Препарат в форме свечей удобен в применении и для взрослых: он не перегружает желудочно-кишечный тракт (ЖКТ), что особенно актуально для людей, страдающих гастритом и другими заболеваниями ЖКТ, а также для тех, кто принимает большое количество таблетированных препаратов (пожилые пациенты и лица с сопутствующими заболеваниями).
Для лечения герпесвирусных инфекций у взрослых применяются свечи в дозировке 1 000 000 МЕ, у беременных женщин – 500 000 МЕ с последующими поддерживающими курсами с использованием дозировки 150 000 МЕ.

ВИФЕРОН Гель в виде полоски не более 0,5 см наносят на предварительно подсушенную пораженную поверхность 3-5 раз в день в течение 5-6 дней.
Сочетание ациклических нуклеозидов с препаратом ВИФЕРОН гарантированно сокращает сроки купирования ОГ и позволяет значительно снизить риск развития осложнений за счет комбинированного противовирусного действия (нарушение размножения вируса варицелла-зостер и препятствие прямому токсическому воздействию). iii
Как применять мазь при опоясывающем герпесе
Любая противогерпетическая мазь при опоясывающем герпесе может применяться в качестве дополнения к системной терапии, но не вместо нее.
Национальное научное общество инфекционистов и Московский научно-практический центр дерматовенерологии и косметологии рекомендуют включать препарат ВИФЕРОН в комплексную терапию опоясывающего герпеса у детей и взрослых, включая беременных женщин. iv
Справочно-информационный материал
Автор статьи
Врач общей практики
iii Халдин А.А., Васильев А.Н., Д.В. Баскаков Д.В. Виферон: опыт применения в дерматологической практике // Ремедиум Приволжье. – январь-февраль 2009. – С.20-22.
iv Потекаев Н.Н., Халдин А.А., Жукова О.В., Дмитриев Г.А. Методические рекомендации. Простой герпес. Опоясывающий герпес. Цитомегаловирусная инфекция. Московский научно-практический центр дерматовенерологии и косметологии ДЗМ. – 2019. – 32 с.
Вирус герпеса третьего типа varicella zoster (VZV) вызывает два клинически обособленных заболевания - ветряную оспу и опоясывающий герпес (Баринский И.Ф. и др., 1986; Haanpaa M., 2001). Оба заболевания, прежде всего, характеризуются везикулярной сыпью. Первичная инфекция манифестирует в форме ветряной оспы (ветрянки), а реактивация латентного VZV обусловливает появление локализованных высыпаний - опоясывающего лишая (Хахалин Н.Н., 2002). Мысль о связи между ветрянкой оспой и опоясывающим лишаем впервые была высказана в 1888 венским врачом Яношом Бокеем (von Bokay J., 1909).
Эпизод ветряной оспы в детстве способствует формированию специфической клеточной и гуморальной иммунной защиты. Считается, что рецидив инфекции у таких пациентов может развиться только на фоне недостаточности иммунной защиты, вследствие снижения активности специфических натуральных киллеров, Т-киллеров и системы интерферонов (Fleming D.M. et al., 2004). После первичной инфекции излюбленным местом персистенции VZV являются ганглий тройничного нерва и спинномозговые ганглии чувствительных корешков грудного отдела спинного мозга, где VZV находится в латентном состоянии. В течение этого времени вирус не размножается и не проявляет патогенных свойств. По-видимому, время латентного состояния вируса определяется уровнем специфических антител к VZV. Снижение их количества ведет к реактивации вируса, вирусной репликации (размножению), что на клиническом уровне и проявляется в виде опоясывающего лишая (Arvin A., 2005). Данный вывод подтверждается высокой корреляцией между вероятностью возникновения опоясывающего лишая у людей пожилого возраста и возрастным ослаблением активности клеточного звена иммунитета (Gilden et al., 2000)., На это также указывают данные, свидетельствующие о более высокой заболеваемости опоясывающим герпесом среди лиц, инфицированных вирусом иммунодефицита человека (Gilson I.H. et al., 1989), однако точные механизмы, лежащие в основе перехода вируса из латентного состояния в активное неизвестны.
В случае реактивации VZV ганглии чувствительных нервов становятся местами репликации вируса, именно в них обнаруживаются наиболее выраженные дегенеративные повреждения нейронов (Zerboni L. et al., 2005; Reichelt M. et al., 2008). В результате развивается ганглионит, сопровождаемый распространением инфекции вниз по нервным аксонам к коже. Каким образом происходит транспортировка вируса в поврежденных аксонах неизвестно. Инфекция также может распространяться центрально, приводя к воспалению оболочек в области передних и задних рогов спинного мозга (Gray F. et al. 1994). Отдельные патолого-анатомические наблюдения также свидетельствуют о наличии воспалительных изменений и в контралатеральных спинномозговых ганглиях (Miller S. E. et al., 1997), отмечается снижение количества нейронов и наличие воспалительных инфильтратов в ганглиях, периферических нервах, и спинномозговых корешках (Gowrishankar K. et al., 2007). В некоторых случаях отмечается выраженные некротические изменения в спинномозговых ганглиях. Большинство изменений в периферическом нерве протекает по типу Валлериановской дегенерации, имеющей место, как в толстых, так и в тонких волокнах. (Denny-Brown et al., 1944).
Доказано, что повреждение нейрональных структур начинается перед появлением кожной сыпи. При этом VZV по ходу чувствительных нервных волокон проникает в кожу, «ускользая» от факторов врожденного и приобретенного иммунитета, что в конечном итоге обусловливает возникновение односторонней везикулярной кожной сыпи, характерной для опоясывающего лишая.
Острая VZV инфекция клинически характеризуется стадией продрома и стадией везикулярных высыпаний (Arvin A., 2005).
Сыпь обычно локализуется в одном или нескольких смежных дерматомах и сопровождается развитием острой невропатической боли. У 50% больных сыпь встречается на туловище, у 20% - на голове, у 15% - на руках, и у 15% - на ногах (Arani R.B. et al., 2001).
Клинический диагноз опоясывающего лишая в типичных случаях достаточно прост. Однако иногда требуется проведение лабораторной диагностики с целью идентификации вируса. Наиболее быстрым и высокочувствительным методом является полимеразная цепная реакция.
В остром периоде болезни или после него возможно развитие осложнений, захватывающих различные системы организма. Наиболее серьезными считаются неврологические осложнения. В структуре неврологических расстройств ведущее место занимает поражение периферической нервной системы. При данном заболевании воспалительный процесс затрагивает региональные, чувствительные ганглии с развитием ганглиолитов. Наличие у больных корешковых болей, парастезий, сегментарных нарушений чувствительности отмечается практически у каждого больного (Stankus S. et al., 2000; Thyregod H. G. et al., 2007). Болевой синдром имеет выраженную вегетативную окраску в виде жгучих, приступообразных, резких болей, усиливающихся в ночное время. В головном мозге при опоясывающем герпесе могут быть обнаружены явления отека, выраженная диффузная инфильтрация подпаутинного пространства, геморрагии в белом веществе, базальных ганглиях (Sissoko D. et al., 1998). Следует заметить, что осложнения со стороны головного и спинного мозга в настоящее время встречаются редко. В случаях развития VZV-инфекции в области тройничного нерва часто наблюдаются осложнения со стороны глаз - кератит, ирит, ретинит, офтальмит. Ранее, при отсутствии специфической противогерпетической терапии, к частым осложнениям VZV-инфекции относились пневмонии, энцефалиты или гепатиты, иногда приводившие к летальному исходу.
Вместе с тем, из всех перечисленных осложнений VZV инфекции самым распространенным считается постгерпетическая невралгия (Dworkin R.H., Portenoy R.K., 1996).
Различают острую герпетическую невралгию (в течение 30 дней после начала заболевания) и постгерпетическую невралгию (Choo P. et al.,1997). К ПГН относят упорные боли в областях, затронутых герпесной инфекцией после заживления кожи (Dworkin R. et al. 2003). Наиболее хорошо установленными факторами риска для ПГН являются пожилой возраст, большая распространенность высыпаний на коже и выраженная боль перед везикулярной сыпью (Desmond R.A. et al., 2002; Fleming D.M. et al., 2004). Все эти факторы находятся во взаимосвязи, поэтому пациенты 50 лет и старше в большинстве случаев испытывают тяжелую, нестерпимую боль и значительные кожные высыпания, что гораздо чаще приводит к развитию ПГН. У пациентов со всеми этими факторами риск развития ПГН превышает 50-75 % (Gnann J., Whitley R. 2002; Jung B.F., 2004). Постгерпетическая невралгия может развиться в любом возрасте, однако для нее характерна прямая корреляция частоты встречаемости и длительности ПГН с возрастом. Более 50% всех пациентов с ПГН - старше 60 лет, 75% больных с указанной патологией приходится на возрастную группу старше 75 лет (Nurmikko T.J., 2001). Половина всех пациентов с ПГН старше 60 лет испытывает постоянную боль более 6 месяцев, в то время как в возрастной группе 30-50 лет ПГН более 6 месяцевь наблюдается у 10% больных (Whitley R. et al. 1996). В США ежегодно регистрируется 100-200 тыс. новых случаев ПГН (Nurmikko T.J., 2001). Однако, истинная распространенность ПГН не известна, не только потому, что эпидемиологические данные недостаточны, но также из-за отсутствия конценсусса по определению ПГН. Некоторые авторы относят к ПГН боли, возникающие в любой период герпесной инфекции, другие считают, что ПГН - это боль, сохраняющаяся спустя 3 месяца после заживления кожи. В первом случае определения ПГН ее распространенность составляет 8%, во втором - 4,5% (Choo P. et al. 1997). Постоянную боль в течение 1 мес после сыпи испытывают до 15% пациентов и около 4% пациентов от общего количества перенесших опоясывающий лишай отмечают сохранение боли в течение года (Lancaster T. et al. 1995).
Классическое проспективное исследование, проведенное Hope-Simpson (1975), продемонстрировало, что из 321 пациента с опоясывающим лишаем 10 % имеют выраженную боль спустя 3 месяца после острой герпетической инфекции, а 4 % - и через 12 месяцев. Подобные результаты были получены и в других проспективных исследованиях (Helgason S. et al. 1996; 2000; Scott F.T. et al., 2006), в которых также было показано, что наибольший риск пролонгации болевого синдрома после перенесенного опоясывающего лишая имеют пациенты в возрасте около 60 лет.
Постгерпетическая невралгия занимает третье место по частоте встречаемости среди различных типов невропатической боли и уступает только болям в нижней части спины и диабетической невропатии (Montero H.J. et al., 2005; Breivik H. et al, 2006; Torrance N. et al., 2006).
Локализация болевого синдрома практически всегда соответствует зоне кожных высыпаний. Интенсивность болевого синдрома как правило высокая. Кроме глубоких ноющих и стреляющих болей очень характерны поверхностные жгучие боли и наличие стимулозависимых болей - динамической гипералгезии и аллодинии (Baron R., 2004).
При клиническом осмотре в зоне болей выявляются нарушения поверхностной чувствительности. Качество боли в острый период опоясывающего лишая и при ПГН различно. Вместе с тем, несмотря на разный выбор дескрипторов из МакГилловского болевого вопросника, пациенты с опоясывающим лишаем и ПГН для описания своих болевых ощущений выбирают похожие по смыслу слова, например, горячая и жгучая боль или пронзающая и простреливающая боль (Bennett M., 2001).
Схожие проявления наблюдаются и при описании вызванной боли пациентами с опоясывающим лишаем и ПГН. И те, и другие отмечают наличие схожих типов гипералгезии и аллодинии (Haanpaa M. et al., 2000; Berry J.D., Rowbotham M.C., 2004).
У большинства пациентов боль, связанная с ПГН, уменьшается в течение первого года. Однако у части больных она может сохраняться годами и даже в течение всей оставшейся жизни, причиняя немалые страдания (Cunningham A.L., Dworkin R.H., 2000). Затяжной, тяжелый характер заболевания с длительным, выраженным болевым синдромом способствует формированию расстройств психики (Dworkin R.H., et al., 1992). У таких пациентов выявляются тревожно-депрессивные расстройства, когнитивные нарушения - снижение активного внимания, памяти, затруднения осмысления происходящего, отмечается некритичность, нетерпеливость, неряшливость, страх боли, неуверенность в завтрашнем дне, отмечается снижение социальной активности (Haythornthwaite J.A. et al., 2003). ПГН оказывает значительное отрицательное влияние на качество жизни и функциональный статус пациентов особенно пожилого возраста (Lydick E. et al., 1995). У пациентов с ПГН отмечается хроническая усталость, снижение массы тела, физической активности, нарушения сна (Morin C.M., Gibson D., Wade J., 1998).
В основе боли, связанной с ПГН, лежат воспалительные изменения или повреждения ганглиев задних корешков спинного мозга и периферических нервов в пораженных зонах тела. Такие боли относят к невропатическим болям, их выделяют в отдельную самостоятельную группу и определяют как боли, возникающие вследствие первичного повреждения соматосенсорной нервной системы (Treede R.D. et al., 2008).
Патофизиологической основой невропатических болевых синдромов являются нарушения генерации и проведения ноцицептивного сигнала в нервных волокнах, а также механизмов контроля возбудимости ноцицептивных нейронов в структурах спинного и головного мозга (Кукушкин М.Л., Хитров Н.К., 2004; Baron R. 2000).
Лечебная тактика при опоясывающем лишае включает два основных направления: противовирусная терапия и купирование невропатической боли, как в острый период заболевания, так и в стадии постгерпетической невралгии. Результаты нескольких рандомизированных контролируемых испытаний свидетельствуют о том, что раннее начало лечения простого герпеса может предотвратить развитие постгерпетической невралгии или способствовать ее скорейшему разрешению (Исаков В.А. и др., 2004; Helgason S. et al., 1996; Jackson J.L. et al., 1997 ; Volmink J. et al., 1996).
Наиболее широкое применение нашли такие специфические противогерпетические препараты, как ацикловир, фамцикловир и валацикловир, которые, являясь нуклеозидными аналогами, блокируют вирусную репликацию (Романцев М.Г., 1996; Beutner K. et al., 1995; Bruxelle J., 1995). Важно, что противовирусное лечение проявляет наивысшую активность, если назначено в течение 72 ч от начала герпетических высыпаний (Johnson R., 2001; Johnson R., Dworkin R.H., 2003). В ряде исследований доказана высокая эффективность ацикловира в уменьшении тяжести, продолжительности острой герпесной инфекции и профилактике ПГН, особенно при его раннем назначении. Оценка эффективности фамцикловира также продемонстрировала уменьшение времени до разрешения сыпи (Dworkin R.H. et al., 1998). В сравнительном исследовании ацикловира и валацикловира показана эквивалентная эффективность в сокращении продолжительности невропатической ПГН (Beutner K. et al. 1995). В другом клиническом испытании установлена терапевтическая эквивалентность фамцикловира и валацикловира для неосложненного герпеса (Tyring S. et al. 2000). Возможно также сочетанное использование противовирусной терапии и глюкокортикостероидов (Whitley R. et al. 1999). Выявлено, что такая комбинация эффективнее монотерапии противовирусными препаратами, особенно для лечения острой боли и коррекции различных аспектов качества жизни пациентов. Комбинация ацикловир+преднизолон значительно быстрее купирует острую невралгию и возвращает пациента к обычной жизнедеятельности, но существенно не влияет на течение ПГН, то есть она наиболее показана в остром периоде в старших возрастных группах для терапии острого болевого синдрома. Доказано, что хотя преднизолон является иммуносупрессором, его использование не увеличивает частоты развития ПГН и в этом смысле его действие сравнимо с влиянием плацебо, то есть данная комбинация может быть спокойно использована в старших возрастных группах. Для некупируемых тяжелых случаев ПГН некоторые исследователи рекомендуют интратекальное введение метилпреднизолона (Kost R., Straus S., 1996).
В настоящее время в США делается акцент на профилактику герпетической инфекции. С 1995 г. в США проводится всеобщая вакцинация от ветряной оспы, особенно пожилых лиц, и с 1999 г. отмечается резкое снижение заболеваемости (Hambleton S., Gershon A., 2005; Oxman M.N. et al., 2005).
При постгерпетической невралгии препаратами с доказанной эффективностью (класс А - терапия первой линии) являются: пластины с 5% лидокаином, габапентин, прегабалин, трициклические антидепрессанты, трамадол (Attal et al., 2006).
На сегодняшний день эффективность применения пластин с 5% лидокаином (Версатис, Grunenthal Gmbh) убедительно доказана при лечении ПГН. Так, в нескольких рандомизированных клинических исследованиях установлено, что применение пластин с 5% лидокаином статистически достоверно более значимо облегчает проявления болевого синдрома у пациентов с постгерпетической невралгией по сравнению с плацебо (Rowbotham M.C., 1996; Galer B.S., 1999, 2002). На основании полученных данных FDA одобрило применение данного препарата в качестве стартовой терапии у пациентов с постгерпетической невралгией. (Richard L. et al., 2004)
Версатис - это топический анальгетик, который действует непосредственно там, где болит. Он выпускается в виде мягких пластин размером 10х14 см, которые наклеиваются на неповрежденную кожу без признаков воспаления. Медленно высвобождающийся из пластины лидокаин создает более или менее значительную концентрацию лишь в поверхностных слоях кожи, где проходят тонкие волокна, обеспечивающие болевую и температурную чувствительность (Gammaitoni AR, Davis MW. 2002.). Лидокаин лишь в незначительной степени проникает в более глубокие слои кожи, где проходят кровеносные сосуды, поэтому его попадание в системный кровоток сведено к минимуму. У пациентов, использовавших пластины Версатис, не наблюдалось никаких известных системных эффектов лидокаина (влияние на деятельность ЦНС и сердечно-сосудистой системы). Таким образом, важнейшим преимуществом пластин Версатис служит отсутствие системного действия, что гарантирует безопасность лечения. Практически полное отсутствие системного эффекта позволяет назначать Версатис совместно с любыми другими препаратами для лечения нейропатической боли.
Механизм лечебного эффекта препарата Версатис не ограничивается только действием высвобождающегося из них лидокаина. Важное значение имеет также то, что пластина выполняет роль механического барьера, препятствуя раздражению участка кожи с измененной чувствительностью (аллодиния), а также оказывает не него легкое охлаждающее действие (Galer BS, Gammaitoni AR, Oleka N et al., 2004)
Пластины Версатис рекомендуется прикреплять на 12 ч в течение суток, затем следует 12-часовой перерыв. Обезболивающий эффект часто начинается в течение 30 мин после прикрепления пластины, но может проявляться и позже, нарастает в течение 4 ч и затем поддерживается в течение длительного времени, пока пластина прикреплена к коже. Более того, он может сохраняться и после ее удаления.
Для объективной оценки эффективности каждого из препаратов при лечении ПГН используется показатель NNT (number needed to treat - количество больных, которых нужно пролечить, чтобы получить у одного 50% снижение боли). Чем ниже NNT, тем более эффективен препарат при данной патологии. NNT для пластин с 5% лидокаином при лечении пациентов с ПГН составляет 2,0; для амитриптилина - 2,6; габапентина - 4,4; прегабалина - 4,6 (Wu C.L., Raja S.N., 2008); для трамадола - 3,9 (Kalso E., 2006).
Кроме того, в клинической практике очень важен показатель NNH (number needed to harm - число пациентов, которых необходимо пролечить данным препаратом, чтобы получить развитие 1 случая неблагоприятной побочной реакции, приводящей к отмене препарата). Он показывает, насколько безопасен данный препарат при его использовании. Величина NNH для трамадола, рассчитанная по результатам нескольких клинических исследований, составила 9.0, для ТЦА 14.7, для габапентина 26.1. Рассчитать показатель NNH для пластин с 5% лидокаином не представляется возможным в связи благоприятным профилем безопасности препарата, сравнимым с плацебо.
Таким образом, оценка препарата Версатис с позиций доказательной медицины делает его препаратом выбора при лечении постгерпетической невралгии, что подтверждено в соответствующих рекомендациях.
СПИСОК ЛИТЕРАТУРЫ
Читайте также:

