Можно ли детям рубец
Обновлено: 24.04.2024
Развитие грубых рубцов на коже — одно из частых осложнений при повреждениях мягких тканей лица и шеи у детей. Форма и характер рубцов чаще всего зависят от причин их возникновения: после ожогов, травм, воспалительных явлений, оперативных вмешательств. Рубцы не только вызывают обезображивание, но и приводят к функциональным нарушениям и деформациям различных органов лица и шеи, что особенно опасно в детском возрасте.
Послеоперационные стягивающие рубцы в полости носа приводят потом к стенозам и атрезиям, деформации крыльев носа, вызывая нарушение носового дыхания. При ожогах III—IV степени рубцы возникают не только на коже, но и в подлежащих тканях, что связано в первую очередь с потерей жирового слоя. Рубцы от ожогов следует выделить в отдельную группу в связи с тяжестью деформации, которую они вызывают. Они могут быть как келоидными, так и гипертрофическими. Послеожоговые рубцы часто характеризуются разнообразной и причудливой формой и вызывают тяжелые функциональные расстройства. Нередко они приводят к дефектам и деформации органов лица и шеи, ушных раковин, наружного носа, губ, бровей, век и т.д.
Наиболее серьезные функциональные нарушения, плохо поддающиеся коррекции, вызывают келоидные и гипертрофические рубцы. Они вызывают нарушение роста и развития лицевого скелета и с трудом поддаются лечению. Кроме того, внешний вид ребенка отталкивает от него сверстников, что приводит к психоэмоциональным расстройствам и нарушению социальной адаптации.
Не менее важной является и проблема реабилитации детей после реконструктивных операций по поводу врожденных пороков челюстно-лицевой области. Патологическое рубцевание в результате индивидуальных особенностей детского организма (гормональные сбои, нарушения обмена веществ и др.) и неадекватного лечения ребенка может значительно снизить эффект хирургического вмешательства.
Еще до недавнего времени не существовало четкого алгоритма лечения и профилактики рубцов из-за отсутствия общепринятой клинико-морфологической классификации, основанной на гистологическом морфологическом анализе. Однако сейчас нашими исследованиями доказано, что все рубцы лица и шеи, многообразные по форме и структуре, по клиническим и морфологическим признакам могут быть подразделены на: патологические, к которым относятся келоидные и гипертрофические, и простые, или нормотрофические, к которым относятся плоские (поверхностные) линейные и деформирующие, глубокие втянутые и эмбриональные.
К простым рубцам могут быть отнесены неглубокие плоские линейные и деформирующие рубцы и глубокие втянутые рубцы, захватывающие подлежащие ткани. Плоские рубцы являются окончательно сформированной тканью, отличительными признаками которой могут служить слабая васкуляризация, небольшое количество функционально неактивных клеток (фибробластов), продольная ориентация и плотная упаковка и немногочисленность коллагеновых волокон.
Глубокие втянутые рубцы по морфологическим признакам принципиально не отличаются от плоских, что позволяет отнести их к обычным (простым) рубцам. Статистически достоверные различия между ними обнаружены только в менее упорядоченной архитектонике коллагеновых волокон. Подобные изменения связаны, вероятно, с условиями биомеханических воздействий на рубцовую ткань. Таким образом, простой (нормотрофический) рубец является следствием неполной заместительной регенерации кожи (субституции) при полнослойном, но сравнительно необширном ее дефекте.
Глубокие втянутые рубцы вызывают деформацию не на поверхности кожи, а перпендикулярно ей, то есть подкожно-жировом слое и мышцах. Чаще всего такие рубцы формируются в результате нарушения техники ушивания раны или после осложненного течения раневого процесса. Они хорошо поддаются консервативному лечению (при ранних сроках заболевания). Старые, ранее не леченые глубокие рубцы требуют хирургической коррекции, с последующим профилактическим лечением.
Плоские деформирующие рубцы или рубцовые деформации образуются после обширных первичных пластических плановых или экстренных операций. Лечение их только хирургическое, с последующей профилактикой. По морфологическим признакам плоские деформирующие и глубокие втянутые рубцы отличаются от патологических рубцов преобладанием метаболически неактивных фибробластов, сниженной васкуляризацией, зрелостью соединительной ткани и инволютивными изменениями.
Патологические рубцы включают гипертрофические и келоидные рубцы. Они имеют различные этиологию, патогенез и морфологию. В обоих типах патологических рубцов отмечается сравнительная незрелость соединительной ткани, преобладание гиперпластических процессов (рост фибробластов) над инволютивными и продукции коллагена над его катаболизмом. Именно эти общие черты являются источником нечеткой дифференциальной диагностики, а также причиной того, что ряд исследователей, особенно зарубежных, не разделяют гипертрофические и келоидные рубцы, рассматривая их как варианты одного процесса.
Важнейшей отличительной особенностью гипертрофических рубцов от нормотрофических, в основном, является меньший диаметр коллагеновых волокон, увеличенное содержание кислых гликозаминогликанов (ГАГ), повышенная васкуляризация; увеличение количества фибробластов и содержания РНК в клетках, преобладание активных фибробластов над неактивными фиброцитами, наличие юных и делящихся клеток. Коллагеновые волокна имеют, в основном, продольную ориентацию, что в целом свидетельствует о влиянии биохимических условий на формирование рубца, о сохранении обычного векторного фибрилло- и фиброгенеза. В целом гипертрофический рубец по гистологической структуре близок к сравнительно незрелой соединительной ткани, возникающей после заживления раны.
Основными ультраструктурными особенностями гипертрофических рубцов являются:
1) выраженная биосинтетическая активность фибробластов,
2) наличие большого количества специфической сократительной формы фибробластов - миофибробластов, в цитоплазме которых обнаруживаются пучки миофиламентов. Эти клетки обусловливают контракцию рубцовой ткани.
Необходимо остановиться на некоторых клинических особенностях развития гипертрофических и келоидных рубцов. Гипертрофический рубец никогда не распространяется за пределы пораженной поверхности кожи, более того, в результате сморщивания он даже занимает меньший участок, чем первоначальная рана. Чаще всего он возникает на месте обширного полнослойного повреждения кожи и более глубоких слоев мягких тканей. Не имеет четких границ. Поверхность рубца матовая, неровная, часто отмечается гиперкератоз, изъязвления. Рубец довольно плотный на ощупь, но не упругий. Гипертрофические рубцы образуются сразу после заживления ран, т.е. значительно раньше, чем келоидные.
В отличие от гипертрофических, келоидный рубец может возникать как на месте полнослойного дефекта, так и на месте незначительного поверхностного повреждения кожи. Он характеризуется длительным распространяющимся ростом, значительно приподнят над поверхностью кожи, имеет четкие границы. Поверхность его гладкая, блестящая, цвет может варьировать от ярко-розового, багрово-цианотичного до коричнево-розового. Он плотный, упругий. Келоиды сопровождаются мучительным зудом, жжением, болью. При возникновении келоидов, между заживлением раны и видимым ростом рубца, проходит определенный период времени (период «покоя» рубца), составляющий 3–4 недели. Обычно через 1–1,5 года рост келоида замедляется и постепенно прекращается. Однако полного самостоятельного рассасывания рубца не происходит.
Келоидные рубцы по морфологическим критериям можно разделить на фибробластические (или активные, растущие) и фиброзные (или неактивные, стабильные, "старые") рубцы. Оба эти типа келоидов являются последовательными стадиями одного процесса и имеют ряд одинаковых морфологических признаков, достоверно отличающих их от гипертрофических рубцов: четкое отграничение от окружающей ткани и от эпидермиса; узелковая структура рубца; кольцевидная и аркадная структура коллагеновых волокон в узлах, наличие в рубце атипичных и гигантских форм фибробластов; наличие "зон роста", т.е. узлов незрелой ткани, полное отсутствие эластических волокон; усиление лимфогистиоцитарной и плазматической инфильтрации (хронического воспаления).
Однако в "старых" рубцах, в отличие от растущих: 1) уменьшены гиперпластические и усилены атрофические процессы в эпидермисе; 2) уменьшено содержание фибробластов, особенно юных и атипичных форм, снижены васкуляризация, метаболизм и пролиферативная активность ткани; 3) уменьшены в числе и размерах или отсутствуют "зоны роста", т.е. узлы незрелой растущей соединительной ткани; 4) зрелые и склерозированные узлы преобладают над незрелыми и созревающими; 5) уменьшается содержание тонких и увеличивается содержание толстых коллагеновых волокон; 6)уменьшается резорбция коллагена и цикличная перестройка рубца; 7) усиливается апоптоз фибробластов.
Лечение больных с гипертрофическими рубцами - одна из наиболее сложных задач. Никакие консервативные мероприятия к успеху не приводят. Лечение должно предусматривать иссечение рубцов с пластикой местными тканями. После хирургического лечения необходима профилактика образования грубых рубцов:
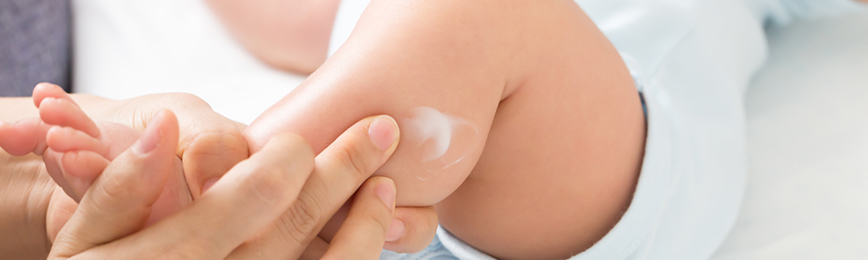
- обработка жирными увлажняющими питательными кремами,
- проведение давящего точечного массажа,
- лечебная мимическая гимнастика,
- лечение ультрамягкими рентгеновскими лучами (лучи Букки),
- использование препаратов KEPATАН.
Наружную мазевую терапию следует начинать сразу после полного заживления ран. Массаж и гимнастику - через 7 дней после снятия швов.
КЕРАТАН - высокоочищенная растворимая форма белка кератина. Порошок или присыпка КЕРАТАН применялись при лечении длительно незаживающих ран кожи и слизистой. Биоадекватность КЕРАТАНа к эпидермису рационализирует процесс моделирования репарации раны. Наблюдения показали, что сроки полного заживления ран сокращаются в среднем на 40 - 70%.
В последние 2 года все чаще используется NO-терапия. Это новая лечебная технология, основанная на свойствах открытого в конце XX века эндогенного NO (Нобелевская премия по медицине за 1998 г.). Экзогенный NO содержится в высоко- и низкотемпературных газовых потоках, генерируемых из атмосферного воздуха аппаратом Плазон 5. Лечебная эффективность экзогенного NO заключается в нормализации микроциркуляции за счет вазодилатации, в антиагрегантном и антикоагуляционном действии, бактерицидном действии, регуляции специфического и неспецифического иммунитета, прямой индукции пролиферации фибробластов, синтезе коллагена, регуляции апоптоза и предотвращении патологического рубцевания и др.
Следует отметить, что в некоторых случаях NO-терапия снижает напряжение рубцовой ткани, которая становится менее гиперемированной, уменьшаются ощущения зуда, болезненности, покалывания. В случаях пред- и послеоперационной подготовки рубцовой ткани с применением NO мы наблюдали отсутствие рецидивов. Иногда NO-терапию приходится дополнять апробированными ранее лечебными мероприятиями.
Таким образом, лечение келоидных и гипертрофических рубцов требует только комплексного подхода — сочетания профилактических и лечебных мер; при нарушении функции органа обязательна операция и продолжение лечения рубцов.
Лечение пациентов с келоидными рубцами далеко не всегда приводит к желаемому результату. Эффект зависит от своевременности и рациональности лечения. Метод лечения выбирают в зависимости от давности существования рубца, его локализации, распространенности, наличия функциональных нарушений.
Консервативная терапия проводится либо как подготовка к дальнейшему хирургическому лечению, либо с профилактической целью после оперативного лечения. Рассчитывать на успех консервативного лечения можно только при сроке существования рубца не более 9-12 месяцев.
Показанием к хирургическому лечению детей с "молодыми" келоидными рубцами служат выраженные функциональные нарушения, а также деформации окружающих мягких тканей. При небольших размерах «старых» неактивных келоидов лечение необходимо начинать с лазерного и криоиспарения с использованием С02 лазера - "Скальпель-1" или с хирургического лечения с обязательной последующей профилактикой келоидообразования.
В комплекс консервативных мероприятий, помимо Букки-терапии, давящего массажа и лечебной мимической гимнастики, входит применение крема КЕРАТАН с лидазой и силиконового пластыря. Данный комплекс консервативных мероприятий удобен в детской практике, так как он наименее инвазивен. Практически все мероприятия проводятся в домашних условиях.
Выбор метода хирургического лечения зависит от вида и размера рубца. При небольших размерах рубца дефект закрывается местными тканями, при обширных — необходима пересадка полнослойного лоскута с применением микрохирургической техники или на сосудистой ножке.

Клиника тесно сотрудничает с производителями и поставщиками (в том числе и зарубежными) лекарственных средств, поэтому в любое время у нас имеется большой выбор препаратов, что обеспечивает максимальную «индивидуализацию» лечения пациентов.

Резюме
Изучена клиническая эффективность ферментативного препарата Ферменкол при лечении послеожоговых рубцов у детей раннего возраста. В результате применения данного препарата отмечается снижение высоты и мобильности рубцовой ткани. Это биологически активное вещество является простым и легким в использовании. За все время наблюдения у детей раннего возраста не отмечалось аллергических реакций.
Ключевые слова: термический ожог, дети, ферментная терапия.
Abstract
The clinical efficacy of an enzyme drug Fermencol in post-burn scars treatment in infants was studied. The reduction of scar tissue height and mobility were observed as a result of this drug application. This biologically active substance is simple and easy to use. No allergic reactions were observed during study period in infants.
Keywords: thermal burns, children, enzyme therapy.
ВВЕДЕНИЕ
По данным Всемирной организации здравоохранения, ожоговая патология составляет около 30% всех травм и характеризуется высокими показателями летальности и инвалидности; 33% всех погибших составляют дети до 14 лет. В России за медицинской помощью по поводу ожогов ежегодно обращаются 75–77 тыс. детей [2], что составляет 33,5–38% от общего числа пострадавших от ожогов, а в Беларуси на долю детей приходится более 20% [4]. Однако отдаленные результаты лечения ожоговой раны напрямую зависят от своевременно начатого консервативного и хирургического лечения на этапе реабилитации [1], в которой нуждаются более 80% детей с последствиями ожоговой травмы.
Патологические рубцы – не только медицинская, но социальная проблема в современном мире, особенно в детском возрасте. У детей наиболее часто встречаются гипертрофические и келоидные рубцы.
Наиболее частой причиной возникновения данной патологии являются термические ожоги кожи. Особую группу риска ожоговых поражений составляют дети в возрасте от 2 до 4 лет [8]. Рост патологических рубцов у детей возможен до 1,5–2 лет от момента своего возникновения, но рост детского организма продолжается на протяжении длительного периода, что приводит и объясняет отставание рубцов в росте от нормальных тканей, часто вызывая развитие контрактур. Учитывая анатомо-физиологические особенности детского организма, такие как диспропорция роста рубцовой и неповрежденной кожи, а также рост детей, необходимо продолжительное динамическое наблюдение за формирующимся рубцом.
Для лечения рубцово-измененных тканей существует огромный арсенал лекарственных препаратов. В настоящее время применяются средства, обеспечивающие гидролиз коллагена и гликозаминогликанов в патологических тканях с последующим восстановлением нормального состава и структуры внеклеточного матрикса. Одним из препаратов, обладающим коллагенолитической активностью, является Ферменкол (Россия) [3]. Это природный комплекс из гепатопанкреаса камчатского краба, содержащий комплекс изоферментов коллагеназы с молекулярной массой от 23 до 36 кДа, а также гиалуроновую кислоту до отдельных фрагментов, вплоть до отдельных аминокислот. Применяется в 2 формах: гель и набор для электрофореза.

Оценить клиническую эффективность препарата Ферменкол в лечении послеожоговых рубцов у детей в возрасте до 3 лет.
МАТЕРИАЛЫ И МЕТОДЫ
В клинике детской хирургии на базе Гродненской областной детской клинической больницы было проведено обследование 25 пациентов в возрасте от 1 года до 2,5 лет. Пациенты были разделены на 2 группы:
- 1-я группа (контрольная, 10 человек) – основная, дети, которые не получали лечения после возникновения патологических рубцов;
- 2-я группа (15 человек) – дети, получавшие консервативное лечение препаратом Ферменкол (гель) 0,1 мг (0,01%) активного вещества (комплекс коллагенолитических протеаз) и один или два курса электрофореза с раствором Ферменкол на область гипертрофической ткани (спустя 1–1,5 мес. после ожоговой травмы).
Для лечения пациентов с гипертрофическими рубцами концентрация раствора составляла 0,1–0,2 мг/мл. Для растворения сухого вещества использовали специальное вещество солактин – прозрачную жидкость, содержащую хлориды калия и кальция, хлоргексидин и соляную кислоту. Эффективность консервативного лечения оценивали по субъективным критериям (зуд, нарушение сна) с использованием визуально-аналоговой шкалы от 0 до 10 баллов, объективно – с помощью Ванкуверской шкалы (Vancouver Scar Scale) [9], разработанной T. Sallivan и соавт. в 1990 г. (см. таблицу) для оценки рубца по следующим параметрам: пигментация, васкуляризация, эластичность, высота рубца над уровнем здоровой кожи. Также проводилась термометрия, фотографирование и измерение площади рубца с помощью компьютерной программы.
Ванкуверская шкала оценки рубцов
Цвет рубца (васкуляризация)
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В начале лечения у пациентов в обеих группах интенсивность зуда была 7–9 баллов, имелись нарушения сна, появление рубцов по Ванкуверской шкале оценивалось в 8–10 баллов. У пациентов 2-й группы после 3 мес. терапии субъективные и объективные показатели рубцового процесса были значительно лучше, чем в контрольной. Таким образом, интенсивность зуда у пациентов 1-й группы снизилась до 2–4 баллов, нормализация сна отмечалась у 12 пациентов, в то время как показатели во 2-й группе были 5–6 баллов и 3–4 балла соответственно. Объективно внешний вид рубцово-измененных тканей у пациентов 2-й группы, которые использовали препарат Ферменкол, составил 3–4 балла согласно Ванкуверской шкале, в то время в 1-й группе отмечалось 5–6 баллов. Особенно быстро во 2-й группе произошло снижение высоты и мобильности рубцовой ткани.
В развитии рубцов играют важную роль многие клетки (лейкоциты, макрофаги, фибробласты, клетки иммунной системы), ростовые факторы, гормоны и цитокины [5]. В результате различных вариантов течения раневого процесса исходом травмы является наличие фиброзноизмененной кожи. Необходимо отметить, что межклеточный органический матрикс соединительной ткани имеет сложный химический состав и состоит из следующих основных типов молекул: протеогликанов и белков, преимущественно структурных (эластин, коллаген), а также гликозаминогликанов. Встречаются также адгезивные белки (фибронектин, ламинин) [7].
КЛИНИЧЕСКИЙ ПРИМЕР
Ребенок Б. поступил в отделение экстренной хирургии с наличием ожоговой раны в области правой стопы S=2(1%)% 1–3 ст. Травма в быту, опрокинул на себя кружку с горячим чаем. Местное лечение: влажно-высыхающие повязки, повязки с мазями на серебре. На 14-е сутки выполнена аутодермопластика свободным расщепленным кожным лоскутом. Послеоперационный период без особенностей. Через 1,5 мес. после выписки контрольный осмотр. В области тыла стопы отмечается гипертрофический рубец, возвышающийся над кожей, гиперемированный, неровный, мать отмечает наличие у ребенка зуда (рис. 1).
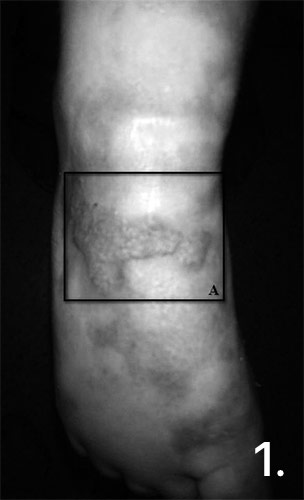
Рис. 1. Гипертрофический рубец в области тыла стопы через 2 мес. после получения ожога.
Ребенку назначена местная терапия: после очищения рубца легкими движениями, не втирая, наносить Ферменкол-гель 0,1 мг (0,01%) активного вещества (комплекс коллагенолитических протеаз) 3 недели.
Повторный осмотр через 1 мес. от начала терапии. Рубец возвышается над кожей, увеличен в толщине, но уменьшился зуд. Ребенку назначен курс электрофореза препаратом Ферменкол. Концентрация раствора составила 0,1 мг/мл, объем раствора – 0,3–0,5 мл на 1 см 2 рубцовой поверхности, длительность курса – 10 сеансов ежедневно. Через 1 мес. после выполнения электрофореза рубец уменьшился в толщине, стал более гладкий, но сохранялась его гиперемия (рис. 2).
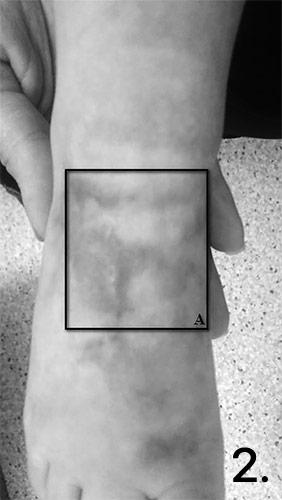
Рис. 2. Гипертрофический рубец в области тыла стопы через 4 мес. после получения ожога.
Ребенку назначено 2 курса геля Ферменкол. После последнего курса рубец не возвышается, бледнеет. Ферментативная терапия больше не применялась. Через 10 мес. от травмы контрольный осмотр, рубец нормотрофический, бледный (рис. 3). Родители отмечают, что при применении данной терапии аллергической реакции не выявлено.
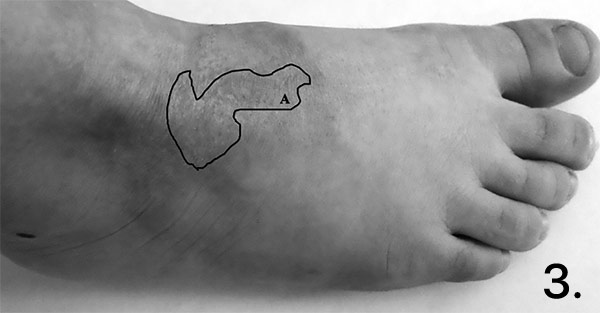
Рис. 3. Гипертрофический рубец в области тыла стопы через 10 мес. после получения ожога.
Известно, что рубцовые изменения являются непосредственным последствием глубоких ожогов, а при неадекватном местном лечении при обширных поражениях и некоторых особенностях иммунного статуса пациентов рубцы возникают и при поверхностных ожогах [6].
Установлено, что после курса электродного фармофореза с препаратом Ферменкол у пациентов с рубцовыми изменениями кожи отмечалось уменьшение толщины гиперэхогенного тяжа в глубоких отделах дермы с участками нормальной эхогенности [3].
Показано, что препараты гиалуронидазы действуют главным образом на полисахаридную составляющую внеклеточного матрикса, поэтому монотерапия гиалуронидазой имеет существенные ограничения. Фибробласты (миофибробласты), «населяющие» рубец, реагируют на изменение состава окружающего их внеклеточного матрикса (его полисахаридной составляющей) дополнительной продукцией гликозаминогликанов и белков, что и объясняет наличие в массиве рубца нетронутых волокон коллагена, в результате такая терапия в ряде случаев может спровоцировать рост рубца. В связи с эти препараты Ферменкол и Ферменкол-гель обладают выраженной амилолитической активностью, могут использоваться в виде монотерапии [7].
ЗАКЛЮЧЕНИЕ
Наши данные показывают эффективность применения препарата Ферменкол в лечении послеожоговых рубцов на коже у детей. Это биологически активное вещество является простым и легким в использовании. За все время наблюдения у детей раннего возраста не отмечалось аллергических реакций.

ЛИТЕРАТУРА
1. Baindurashvili A., Kaleva T., Afonichev K. (2012) Profilaktika posledstvij ozhogov u detej [Prophylactics of post-burn effects in children]. Russian Bulletin Pediatric Surgery, Anesthesiology and Intensive Care, Application. Proceedings of X All-Russian scientific-practical conference “Actual problems of pediatric surgery”, pp. 25–26.
2. Baindurashvili A., Solov’eva K., Zaletina A. (2012) Rasprostranennost’ ozhogov u detej, potrebnost’ v stacionarnom lechenii, invalidnost’ [The frequency of burns in children, the need of inpatients treatment, disability]. Russian Bulletin Pediatric Surgery, Anesthesiology and Intensive Care, Application. Proceedings of X All-Russian scientific-practical conference “Actual problems of pediatric surgery”, pp. 26–27.
3. Stenko A. (2014) Konservativnoe lechenie pacientov s rubcovymi izmeneniyami kozhi metod e’lektrodnogo farmaforeza [Conservative treatment of patients with scars by electrod pharmaphoresis]. Russian Journal of Skin and Venereal Diseases, no 1, pp. 58–61.
4. Koshel’kov Ya. (2008) Statistika ozhogovoj travmy v Respublike Belarus’ [Burn trauma statistics in Belarus]. Sbornik nauchnyh trudov: II s”ezd kombustiologov Rossii, Moskva, 2–5 iyunya 2008 g. [Collection of scientific papers: 2ND congress of Russian co mbustiologists, Moscow, 2–5 of June 2008]. Moscow: A. Vishnevsky Institute of Surgery Medical Technologies, pp. 24–25.
5. Kuzin M., Kostyuchenok B. (1990) Rany i ranevaya infekciya [Wounds and wound infections]. Moscow: Medicine, 592 p. (in Russian).
6. Fistal’ N. (2014) Osobennosti profilaktiki, lecheniya i rannej reabilitacii bol’nyh s posleozhogovymi rubcami [Details of prophylaxis, treatment and early rehabilitation of patients with post-burn scarring]. Bulletin of emergency and rehabilitation medicine, vol. 15, no 1, pp. 43–51.
7. Paramonov B., Turkovskij I., Antonov S. (2012) Fermentnaya terapiya patologicheskih rubcov kozhi Chast’ I. Sravnitel’naya ocenka sposobnosti fermentnyh preparatov razrushat’ komponenty vnekletochnogo matriksa [Enzyme therapy of pathologic scarring. Part 1. Comparison of enzyme drugs activity on extracellular matrix components breakdown]. Art beauty professionals, no 2, pp. 50–58.
8. Alekseev A. (2007) Profilaktika i lechenie posleozhogovyh rubcov gelem kontraktubeks [Prophylaxis and treatment of post-burn scars with Contractubex gel]. Recipe, no 1 (51), pp. 153–154.
9. Sullivan T. (1990) Rating the burn scar. J Burn Care Rehabil, vol. 11, no 3, pp. 256–260.
Глуткин Александр Викторович – к.м.н., ассистент кафедры детской хирургии Гродненского государственного медицинского университета
В статье рассмотрены клинические и гистологические особенности рубцовой ткани на различных стадиях ее созревания, описаны структурные изменения в рубцах, происходящие под влиянием компрессионной и коллагенолитической терапии. Показано истончение и разрыхление коллагеновых волокон при лечении препаратом коллагеназы, усиление противорубцового эффекта при сочетании коллагенолитической терапии с компрессионной за счет сдавления сосудов кожного сплетения.
Ключевые слова: гистология рубцов, динамика рубцового процесса, противорубцовая терапия.
Гипертрофические и келоидные рубцы являются медицинской и во многом хирургической проблемой, особенно у пациентов детского возраста. Детский скелет растет и развивается, патологические рубцы, которые всегда отстают в росте от нормальных тканей, нередко вызывают развитие вторичных деформаций опорно-двигательного аппарата [1, 2]. Эффект от реконструктивных операций не всегда бывает стойким и может быть частично утрачен в связи с ростом и естественным развитием ребенка [3, 4], поэтому значение профилактических мероприятий и консервативного лечения рубцов в детской практике трудно переоценить.
В настоящее время предложено значительное количество методов воздействия на рубцово-изме-ненные ткани, однако оценка эффективности разных способов лечения в большинстве случаев основывается на анализе клинических проявлений [5, 6]. Предложены разные шкалы оценки эффективности консервативного лечения, учитывающие ряд наиболее распространенных клинических симптомов: цвета, рельефа рубцов, консистенции и субъективных ощущений пациента [7—9].
Однако, как показывает практика, клинические признаки не всегда дают полное и адекватное представление о процессах, происходящих в рубцовой ткани, а эффект от разных методов воздействия на рубцовую ткань в ряде случаев бывает непредсказуемым и даже противоположным ожидаемому.
Наиболее информативными методами, позволяющими получить наиболее ценную и полную диагностическую информацию о рубцовом процессе, является изучение биоптатов рубцово-измененных тканей с использованием гистологических и биохимических методик [10—12].
Цель исследования — оценить клинические и гистоморфологические изменения в рубцовой ткани у детей на разных стадиях ее созревания и на фоне лечения препаратом коллагеназы Ферменколом.
Материал и методы
Были обследованы 32 пациента в возрасте 4-12 лет, получавшие оперативное и консервативное лечение по поводу послеожоговых рубцовых деформаций, обусловленных гипертрофическими рубцами.
Для реализации поставленной цели были использованы клинический и гистоморфологический методы исследования.
Клинический метод включал оценку жалоб и ощущений пациента, визуальную и мануальную оценку рубцовой ткани в динамике. Оценивали болезненность, окраску, плотность, эластичность, рельеф.
Для оценки структурных изменений рубца выполнялось гистоморфологическое исследование биоптатов рубцовой ткани на разных сроках ее формирования. В исследование включали пациентов, нуждающихся в многоэтапном хирургическом лечении. Биоптаты получали до и после курса консервативной противорубцовой терапии во время плановых реконструктивных операций. Биоптат представлял собой фрагмент рубцовой ткани размером 4×5 мм, взятый на всю толщину рубцовой ткани. Биопсийный материал погружали в 10% раствор Кайзерлинга на 1—2 сут, проводили по стандартной методике, окрашивали гематоксилином и эозином. Затем срезы толщиной 3 мкм изучали под световым микроскопом.

При микроскопическом исследовании гистологических препаратов оценивали особенности строения каждого слоя рубцово-изменен-ной кожи, толщину и расположение коллагеновых волокон, распределение сосудов и суммарную площадь микрососудистого русла, учитывали количество клеток, участвующих в воспалительной реакции и синтезе коллагеновых волокон. Кроме того, в ряде случаев на исследование отправляли незначительные излишки нормальной кожи, возникшие в результате перераспределения тканей в процессе выполнения местно-пластических операций.
Между этапами оперативного лечения пациентам проводили консервативную терапию с использованием коллагенолитического препарата Ферменкол в виде электрофореза и наружного нанесения в течение дня, в том числе и в виде аппликаций. Длительность курса консервативной терапии составляла не менее 14 сут.
Результаты исследования
В настоящее время выделяют три стадии формирования рубца:
- фибробластическую (до 30 сут), которая характеризуется эпителизацией раневого дефекта, обилием сосудов и пролиферацией юных фибробластов, образованием большого количества аморфного вещества и продукцией ретикулярных волокон;
- волокнистую (30—40 сут): характеризуется скоплением зрелых фибробластов, синтезирующих коллагеновые волокна;
- гиалиновую: характеризуется гиалинозом коллагеновых волокон рубцовой ткани, уменьшением количества фибробластов и сосудов.
Формирование нормотрофического рубца укладывается в среднем в 12 мес, тогда как при гипертрофическом рубцевании стадия активного синтеза коллагена (волокнистая) значительно растянута во времени, что отдаляет срок окончательной стабилизации рубца.
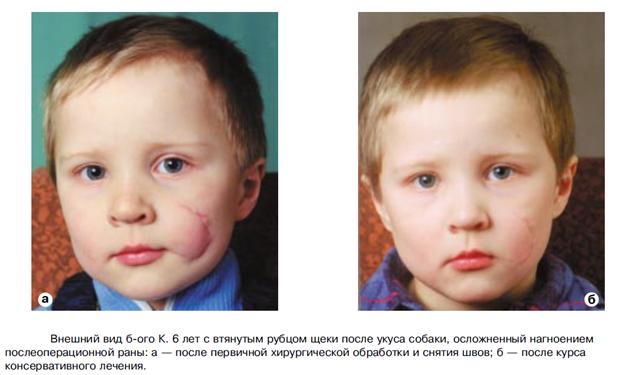
На разных сроках развития гипертрофической рубцовой ткани свойственны разные клинические проявления. Клиническая картина обычно наиболее яркая в волокнистую стадию рубцевания, в процессе активного синтеза коллагена. Признаки гипертрофии могут появляться уже через 4—6 нед после завершения эпителизации: прежде всего уплотнение рубцовой ткани и возвышение рубца над уровнем интактной кожи (рис. 1, а). До 11—12 мес рубец увеличивается в объеме, выступая над поверхностью кожи, имеет неравномерный, иногда бугристый рельеф (см. рис. 1, б).
Наиболее выступающие участки, как правило, располагаются в зонах локализации наиболее глубокого первичного повреждения кожи. Кроме того, больных беспокоят навязчивый зуд, шелушение, периодически возникающие пузыри на поверхности рубцовой ткани, на месте которых в дальнейшем появляются эрозии. Отмечено, что наиболее часто пузыри и эрозии возникают на грубых гипертрофических рубцах и в функционально активных зонах (см. рис. 1, в). Провоцирующим фактором является интенсивная или продолжительная физическая нагрузка. В этот период рубцы имеют наиболее интенсивную ярко-розовую или цианотичную окраску. Как показывает клиническая практика, при гипертрофических рубцах зуд и шелушение могут сохраняться до 1,5-2,0 лет, когда рубец бледнеет и уплощается.
В табл. 1 представлены усредненные морфоме-трические параметры рубцовой ткани у пациентов с разной давностью термической травмы и морфоме-трические параметры нормальной кожи.
Динамика структурных изменений в зависимости от возраста рубцовой ткани
| Морфометрические параметры | Норма | Гипертрофические рубцы | ||
| 1-6 мес | 7-12 мес | 12-24 мес | ||
| Общая толщина кожи (дермы с эпидермисом), мм | 1,519 | 7,198 | 2,506 | 2,22 |
| Общая толщина эпидермиса, мм | 0,135 | 0,144 | 0,185 | 0,153 |
| Толщина рогового слоя, мм | 0,018 | 0,036 | 0,08 | 0,048 |
| Толщина эпидермиса без рогового слоя, мм | 0,117 | 0,108 | 0,105 | 0,105 |
| Толщина дермы, мм | 1,384 | 7,054 | 2,321 | 2,067 |
| Толщина сосочкового слоя дермы, мм | 0,109 | 0,116 | 0,029 | 0,056 |
| Высота сосочков, мм | 0,01 | 0,015 | 0 | 0,051 |
| Толщина сетчатого слоя дермы, мм | 1,275 | 6,938 | 2,293 | 2,011 |
Полученные данные иллюстрируют динамику структурных изменений в зависимости от возраста рубца и отличия рубцовой ткани от нормальной кожи (см. табл. 1). Так, толщина рубцово-измененной кожи значительно превышает толщину нормальной кожи (в 2—3 раза), как правило, за счет сетчатого слоя дермы. Сетчатый слой рубца в первые 6 мес после травмы превышает толщину сетчатого слоя нормальной кожи в 5—6 раз и практически полностью представлен рубцовой тканью, сформированной разнонаправленными пучками толстых коллагеновых волокон. Сосочковый слой несколько утолщается в первые 3—4 мес после травмы, и уплощаясь в дальнейшем, становится тоньше нормального, сосочки плохо различимы.
Кроме того, на протяжении всего периода созревания рубца наблюдается утолщение в 2—4 раза рогового слоя на фоне некоторого истончения эпидермиса (рис. 2, а, б). У детей, перенесших тяжелую термическую травму, имелось значительное количество лимфоцитов и лейкоцитов как в рубце, так и в интактной коже еще на протяжении 4—6 мес с момента реконвалесценции (см. рис. 2, в, г). При обследовании таких пациентов в клинических анализах крови часто выявляются умеренный лейкоцитоз, лимфоцитоз, повышение скорости оседания эритроцитов.
Клинические проявления гипертрофических рубцов во многом обусловлены особенностями кровообращения в рубцовой ткани (табл. 2).
Динамика изменений в дермальной сосудистой сети
| Морфометрические параметры | Норма | Гипертрофические рубцы | ||
| 1-6 мес | 7-12 мес | 12-24 мес | ||
| Количество сосудов сосочкового слоя на 1 мм 2 | 120 | 95 | 90 | 44 |
| Количество сосудов сетчатого слоя на 1 мм 2 | 235 | 185 | 155 | 60 |
| Суммарная площадь сосудов в сосочковом слое, % на 1 мм 2 | 8,50 | 10,10 | 6,20 | 2,96 |
| Суммарная площадь сосудов в сетчатом слое, % на 1 мм 2 | 14,10 | 11,40 | 6,90 | 5,36 |
Имеются значительные различия в строении дермальной сосудистой сети рубцов на разных стадиях развития и по сравнению с интактной кожей (табл. 2). В первые месяцы после травмы количество сосудов в сетчатом слое дермы, где в этот период синтез коллагена протекает наиболее интенсивно, приближено к значениям в интактной коже, тогда как суммарная площадь их сечения превышает нормальные значения. В дальнейшем с 5—6-го месяца после травмы количество сосудов постепенно уменьшается и к окончанию формирования рубца становится в 2—3 раза ниже нормы. Увеличение площади сечения сосудистого русла связано с резким расширением сосудов на ранних сроках формирования рубца (см. рис. 2, д, е).
С 4—5-го месяца после эпителизации часто выявлялись сосуды, сдавленные пучками коллагеновых волокон и мозаично расположенные участки с паретически расширенными сосудами (см. рис. 2, ж). Сосуды расположены неравномерно по сравнению с нормальной кожей. В дальнейшем с 12-го месяца до 2 лет после травмы количество сосудов, сдавленных рубцовой тканью, увеличивалось, часто выявлялись спаявшиеся сосуды, практически не содержащие форменных элементов крови (см. рис. 2, з).
Сосудистая перестройка в гипертрофической рубцовой ткани, длящейся, согласно нашим наблюдениям, около 2 лет, клинически проявляется трофическими расстройствами в виде локального цианоза, шелушения, трещин, пузырей и эрозий с пе-рифокальной воспалительной реакцией. Перечисленные симптомы возникают на участках локальной гипоксии рубцовой ткани, что гистологически подтверждается мозаичным расположением зон со спаявшимися и паретически расширенными сосудами сетчатого слоя дермы.
Полученная гистологическая картина свидетельствует о тесной взаимосвязи между изменениями условий кровоснабжения покровных тканей и интенсивностью синтеза коллагеновых волокон, которые ухудшают трофику кожи, сдавливая сосуды дермального сплетения. Данное обстоятельство необходимо учитывать при выполнении реконструктивных кожно-пластических операций с использованием рубцово-измененных тканей. Как показывает клиническая практика, интраоперационное нарушение связей между дермальным сосудистым сплетением и лежащими глубже сосудами, нередко приводит к гибели вершин перемещенных лоскутов в лучшем случае до сетчатого слоя, даже при включении фасции в состав рубцово-измененного лоскута.
Синтез коллагена осуществляется клетками соединительной ткани — фибробластами, которые, по мере утраты своей синтетической активности, переходят в неактивную форму — фиброциты. Количество фибробластов и фиброцитов было выше в рубцах, чем в нормальной коже в течение всего периода наблюдения. Однако в ранние сроки после термической травмы этих фиброгенных клеток было больше не только в рубцовой, но и в нормальной коже. Это позволяет предположить, что после термической травмы появляется общая тенденция к гипертрофическому рубцеванию и на интактных участках кожи в случае их повреждения или хирургического вмешательства. С увеличением возраста рубца разница между содержанием фибробластов и фиброцитов в рубцово-измененной и нормальной коже возрастала: в рубце, хотя их количество и снижалось относительно первых месяцев после травмы, их было в 4-5 раз больше, чем в нормальной коже (рис. 3).
Основным структурным компонентом рубца, обусловливающим его рельеф и плотность, являются коллагеновые волокна. Применение препаратов, содержащих коллагеназу, разрушающую коллаген, патогенетически обоснованно. В рамках консервативной терапии с коллагенолитической целью мы применяли препарат Ферменкол, содержащий композицию коллагенолитических протеаз. Поскольку ряд пациентов нуждался в нескольких реконструктивных операциях, в перерывах между этапами оперативного лечения им проводили электрофорез и давящий массаж с гелем Ферменкол.

Консервативная терапия назначалась в волокнистую стадию рубцевания, при клинических признаках избыточного синтеза коллагена и в ряде случаев — на сформировавшиеся рубцы. Ферменкол применяли как изолированно, так и в сочетании с компрессионной терапией.
Клинически у всех обследуемых на фоне консервативного лечения наблюдались размягчение и визуальное выравнивание рельефа рубцовой ткани, уменьшалась интенсивность зуда.
В табл. 3 представлена динамика морфометрических параметров на фоне монотерапии Ферменколом и в сочетании с компрессией.
Динамика структурных изменений слоев кожи на фоне консервативной терапии в зависимости от возраста рубцовой ткани
| Морфометрические параметры | До лечения | После лечения | ||
| Ферменкол | Ферменкол + компрессия | |||
| Общая толщина кожи, мм | 3,131 | 2,668 | 2,287 | |
| Общая толщина эпидермиса, мм | 0,41 | 0,243 | 0,092 | |
| Толщина рогового слоя, мм | 0,18 | 0,103 | 0,027 | |
| Толщина эпидермиса без рогового слоя, мм | 0,229 | 0,139 | 0,065 | |
| Толщина дермы, мм | 2,721 | 2,426 | 2,195 | |
| Толщина сосочкового слоя дермы, мм | 0,08 | 0,175 | 0,067 | |
| Толщина сетчатого слоя дермы, мм | 2,641 | 2,251 | 2,128 | |
На фоне коллагенолитической терапии отмечалось заметное (в 2 раза) уменьшение толщины эпидермиса и рогового слоя (см. табл. 3). Уменьшалась общая толщина дермы, в том числе и за счет объема сетчатого слоя. Однако при монотерапии Ферменколом толщина сосочкового слоя дермы увеличивалась, чего не наблюдалось при использовании препарата в сочетании с компрессией. При применении Ферменкола в сочетании с компрессией уменьшалась толщина всех слоев рубцово-измененной кожи.
Утолщение сосочкового слоя при монотерапии Ферменколом может быть связано с расширением сосудов сосочкового слоя, на что указывает увеличение площади сосудистого сечения. При гистологическом исследовании после применения препарата мы наблюдали заметное разрыхление и уменьшение объема пучков коллагена. Давление коллагеновых волокон на дермальные сосуды ослабевало, что приводило к увеличению просвета сосудов и суммарной площади их сечения (рис. 4). Происходящая таким образом частичная реваскуляризация приводила к утолщению сосочкового слоя.
Возможно, именно этим процессом объясняется наблюдаемый в ряде случаев противоположный эффект от противорубцовой терапии на активно растущий гипертрофический рубец, проявляющийся гиперемией и некоторой отечностью рубца. Со стороны сформировавшегося рубца такого эффекта не наблюдалось, что, по-видимому, связано с необратимыми склеротическими изменениями сосудистой стенки сосудов из-за длительной компрессии пучками коллагена.
Учитывая полученные данные, мы дополняли коллагенолитическую терапию незрелых рубцов компрессионной терапией: в волокнистую фазу рубцового процесса Ферменкол назначали в сочетании с компрессионным бельем или эластичным бинтованием (рис. 5).
Выводы
Таким образом, ведущими факторами, обусловливающими клиническую картину и дальнейшее развитие рубца, являются изменение трофики кожи и синтез коллагеновых волокон, которые находятся в тесной взаимосвязи.
Измененные условия кровообращения делают рубцовую ткань рискованным пластическим материалом.
Увеличение фиброгенных клеток в покровных тканях носит системный характер, что необходимо учитывать при планировании реконструктивных операций.
В волокнистую стадию развития рубца мы рекомендуем сочетать коллагенолитическую терапию с компрессионной, поскольку изолированное применение коллагеназ на ранних стадиях развития рубца (до 8—10 мес) может улучшить трофику рубцовой ткани за счет истончения и разрушения коллагеновых волокон, сдавливающих сосуды кожного сплетения.
Удаление лазером шрамов у детей не рекомендуется проводить без особой надобности. Однако в редких случаях допускается осуществление такой процедуры. Но для этого следует учитывать возраст ребенка, сложность и характер рубцов, а также другие физиологические особенности малыша.
Особенности рубцов и шрамов у детей
Поскольку рост ребенка еще продолжается, это может приводить к различным неприятным ощущениям в области шрамов и рубцов. Многие дети жалуются на сильный зуд и жжение в местах заживших повреждений. Связано это с тем, что деформированные участки могут сильно стягивать кожу, так как рост соединительной ткани шрамов не успевает за ростом эпидермиса.
Помимо этого, существует и эстетический момент. Шрам приносит ребенку не только дискомфорт, но и может стать причиной развития психологических комплексов, особенно если находится на открытых участках тела – лице, руках, шее.
Можно ли удалять лазером рубцы в детском возрасте
Использовать лазерную шлифовку рубцов детям не рекомендуется. Однако в тяжелых случаях допускается применение такого способа терапии.
Перед использованием лазера требуется учитывать возраст ребенка. Не следует выполнять процедуры, если он не достиг 14 лет. При больших поражениях терапия может проводиться с 10-ти лет. Детям младшего школьного и дошкольного возраста лечение назначается при острой необходимости, в зависимости от места расположения рубца.
Новорожденным пациентам данный метод лечения противопоказан, поскольку шлифовка шрама лазером может привести к различным осложнениям.
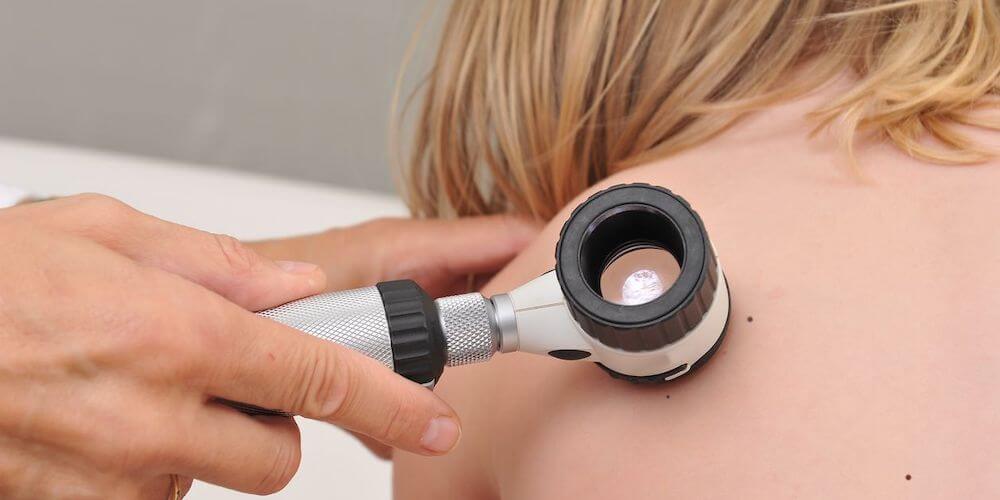
Показания и противопоказания к лазерному удалению рубцов у детей
Удаление лазером шрамов у детей может проводиться только при наличии определенных показаний:
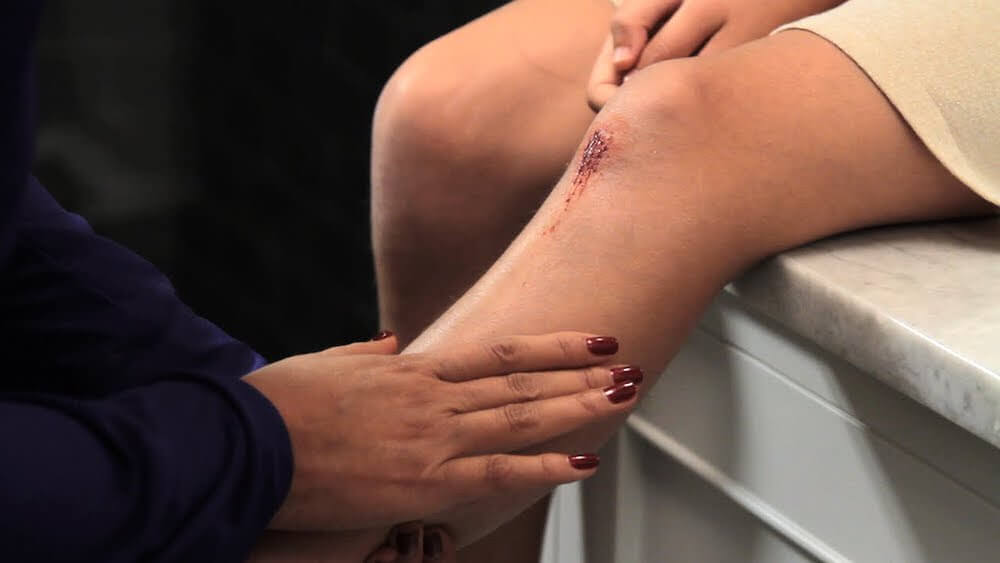
- незначительные травмы и повреждения кожных покровов – ссадины, порезы, царапины;
- небольшие ожоги;
- келоидные и гипертрофические рубцы.
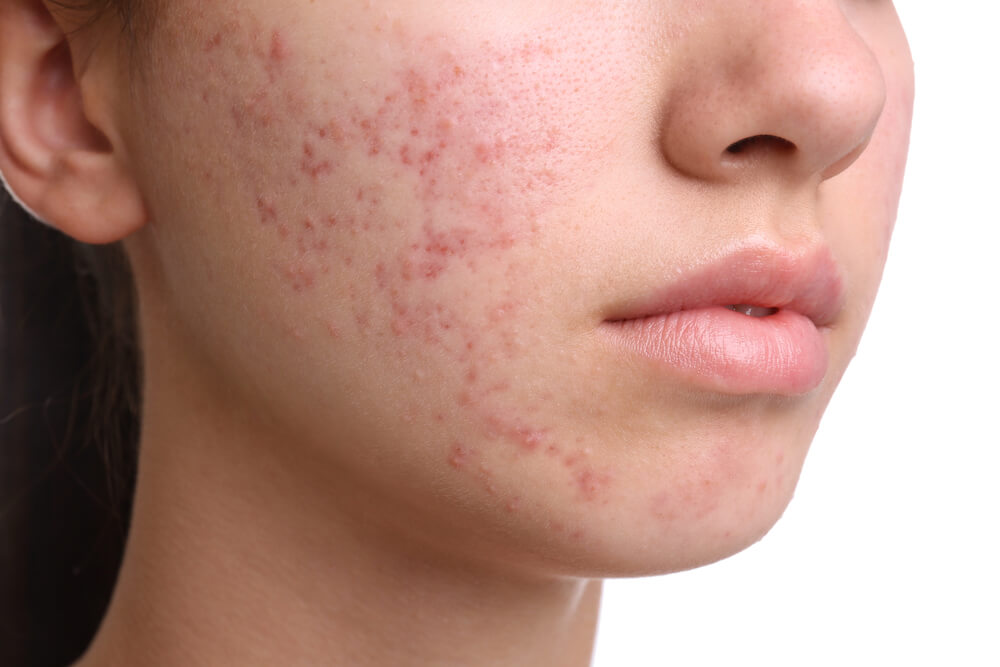
Также терапия может проводиться при постакне, шрамах от угревых высыпаний.
- новорожденный возраст;
- нарушение целостности кожных покровов в предполагаемых местах воздействия;
- сахарный диабет;
- врожденная почечная, печеночная или сердечная недостаточность;
- заболевания крови;
- инфекционные патологии;
- другие дерматологические болезни в фазе обострения;
- плохая свертываемость крови;
- развитие опухолевидных процессов.
Также удаление лазером шрамов у детей не рекомендуется проводить при длительном приеме различных препаратов, оказывающих влияние на процессы коагуляции.
Методы лазерной терапии у детей
Существует 2 способа удаления шрамов и рубцовой ткани в детском возрасте – лазерный пилинг и наноперфорация. Каждая процедура подбирается индивидуально согласно степени тяжести повреждения и области поражения.
Лазерная наноперфорация
Шлифовка рубца лазером ребенку может происходить с помощью инновационных методов. Одним из таких способов является наноперфорация.
Суть терапии заключается в воздействии на поврежденный участок лазерным лучом, который распадается на тысячи микроскопических пучков света. При попадании на кожные покровы они вызывают ее повреждение. В результате такого воздействия эпидермис начинает усиленно вырабатывать коллаген и эластин, что приводит к регенерации и обновлению клеток кожи.
Способ является самым щадящим, поскольку не вызывает термических повреждений и может применяться даже на деликатных участках тела.
Для того чтобы убрать шрам лазером ребенку, необходимо пройти 5 сеансов. В редких случаях результата можно достигнуть уже после одной-двух процедур.
После воздействия возможны небольшие покраснения, которые проходят самостоятельно в течение нескольких дней.
Продолжительность реабилитации после лечения рубцов лазером у детей составляет от 1 до 2-х недель.
Лазерный пилинг
Данный способ подразумевает воздействие лазерных пучков на эпидермис, в результате чего «счищаются» омертвевшие частички кожи и запускаются естественные процессы регенерации.
В зависимости от сложности проблемы, врач может изменять глубину воздействия.
Лазерная шлифовка рубцов и шрамов у детей может проводиться с помощью следующих методик:
- «Холодная» – поверхностное очищение кожи с маленькой глубиной проникновения луча. Используется при незначительных дефектах.
- «Горячая» – оказывает воздействие на более глубокие слои эпидермиса. Применяется в сложных ситуациях.
Длительность сеансов зависит от объема работ и составляет от 15 мин. до 1 часа. Количество процедур определяется индивидуально.
Полная реабилитация занимает от 3 до 5 суток.
Как еще можно убрать шрамы у ребенка
Удаление шрамов или рубцов может проводиться не только лазером, но и другими способами, которые безопасны для ребенка. Наиболее популярными методами являются:
- Микродермабразия – это аппаратное удаление верхнего слоя эпидермиса (омертвевших тканей). Данный тип лечения помогает справляться с различными шрамами и повреждениями кожных покровов, за исключением атрофических и келоидных рубцов. Помимо удаления омертвевших частичек, аппарат стимулирует здоровые клетки к дальнейшей регенерации. Микродермабразия может проводиться в качестве дополнения к лазерному удалению рубцов или шрамов не только у взрослых, но и детей.
- Пилинг Джесснера – процедура, при которой на область поражения наносится специальный состав, помогающий снимать верхний ороговевший слой кожи. При небольших шрамах результаты видны уже после первого сеанса.
- Инъекционное лечение. Данные процедуры особенно эффективны против атрофических рубцов. В состав растворов входит коллаген, который вводится в область дефекта. О том, можно ли убирать различные шрамы у ребенка уколами, следует заранее посоветоваться с врачом.
- Косметические средства (медицинские препараты). К этой группе относятся различные кремы, мази или гели. Все они эффективны только при незначительных повреждениях на начальной стадии заживления. С большими шрамами данные препараты не справятся. Для достижения более выраженного терапевтического эффекта рекомендуется применять составы совместно с электрофорезом или фракционными методами.
Также лечение рубцов лазером у детей может дополняться различными физиопроцедурами. Самыми эффективными являются фонофорез и электрофорез. Первый тип воздействия позволяет убрать повреждения с помощью ультразвуковых волн, что благоприятно сказывается и на состоянии всего организма.
При втором методе воздействие осуществляется с помощью различных лекарственных препаратов и небольших электрических импульсов.
Любой из методов шлифовки рубцов или шрамов при помощи лазерного луча в детском возрасте должен применяться только после предварительного осмотра и консультации врача.

После удаления родинок, ожогов и других травмирующих действий на кожу остаются некрасивые рубцы. Они разные по форме, внешнему виду и причинам появления, но сегодня мы поговорим о самом неприятном из них — о келоидном рубце.
Что такое келоидный рубец и как он выглядит
Келоидный рубец представляет собой разрастание соединительной ткани на травмированном месте кожи. Это грубый рельефный шрам красного цвета, который со временем увеличивается, зудит, чешется и значительно превышает размеры первоначальной раны.
Чаще всего келоидные рубцы образуются в зоне декольте, на спине, шее, лице и на мочках ушей.
Причины появления келоидных рубцов
Есть люди, генетически предрасположенные к рубцам: это связано с повышенным синтезом коллагена при травмировании кожи. В месте заживления раны коллагеновых волокон образуется слишком много, поэтому быстро растет выпуклый рубец. Замечено, что темнокожие люди и люди с азиатской внешностью чаще других имеют склонность к образованию келоидных рубцов.
Некоторые специалисты считают, что кожа, склонная к келоидным рубцам, чаще встречается у людей, имеющих определенные пищевые привычки. Потребление мяса большими порциями и протеина (спортивное питание) способствует активной выработке коллагена.
Чтобы уберечь себя от образования келоидного рубца, важно знать несколько важных правил.
Рассмотрим факторы, которые влияют на заживление раны, а значит, и на формирование шрама. Они бывают локальные и общие.
- Кровоснабжение. Чем лучше кровь поступает к поврежденным тканям, тем быстрее идет процесс заживления.
- Направление раны. Если разрез располагается параллельно частым движениям конечностей (например, рана на лодыжке неизбежно задевается при ходьбе), то риск образования келоида увеличивается.
- Попадание грязи или инфекции.
- Гематома.
- Количество и качество хирургической нити, с помощью которой накладывались швы.
- Возраст. В детстве и юности организм вырабатывает достаточно коллагена и эластина, чтобы раны затягивались быстро и практически без следов. В зрелые годы необходимые вещества вырабатываются с нарушениями в сторону дефицита либо переизбытка, последнее фактически означает склонность к образованию рубцов.
- Иммунитет. При травме иммунная система уничтожает инородные микроорганизмы. Слабая защита способствует инфицированию поврежденного участка.
- Истощение и дефицит витаминов приводят к нарушению обменных процессов и затрудняют нормальное заживление ран, так как организму требуются источники энергии и материал для формирования новых тканей. Кожа, склонная к образованию рубцов, как правило, заметно истощена либо отличается повышенной жирностью и угревыми высыпаниями.
- Ряд заболеваний, например, сахарный диабет и почечная недостаточность. При них нарушается углеводный обмен в тканях, снижается иммунитет, и вследствие этого появляется предрасположенность к келоидным рубцам.
- Онкологические заболевания, гормональные нарушения и необходимость проведения химиотерапии или лучевой терапии.
Виды келоидных рубцов
Келоиды — самые трудные в лечении шрамы. Они отличаются патологически высокой выработкой коллагена и способностью разрастаться со временем, поражая здоровые участки кожи.
Выделяют несколько типов келоидов:
- Истинные (спонтанные). Видимых причин для их возникновения, как правило, нет. Специалисты считают, что склонность к рубцам возникает из-за микротравм. Чаще всего истинные келоиды наблюдаются на лице и груди. Шрамы имеют причудливую форму с ветвящимися отростками, отходящими от основного шрама.
- Ложные (рубцовые). Ложный келоид образуется после операций, порезов, ожогов, фурункулеза и акне. Линейный, может появиться на любом участке тела. Такой рубец может образоваться после выдавливания воспалительного элемента (прыщика) и даже от небольшой царапины.
- Келоидные акне. Обычно встречаются у мужчин. Представляет собой фолликулярный дерматит волосистой части головы. Высыпания (папулы и пустулы) обычно располагаются на затылке.
Также по времени и развитию рубцы классифицируются на активные (растущие) и неактивные.
Активный келоид увеличивается и вызывает зуд, боль, онемение, гиперемию.
Неактивный не беспокоит и находится в стабильном состоянии.
Келоиды классифицируют и по возрасту. Молодым рубцам менее 5 лет, они имеют красный цвет и блестящую поверхность. Старые рубцы образовались более 5 лет назад, их окраска приближается к цвету кожи, а поверхность неровная.

Профилактика келоидных рубцов
Предсказать поведение рубца после травмы невозможно, но можно сократить риски появления келоидных рубцов. В этом помогут силиконовые гели и пластыри, за счет давления на поврежденную область они препятствуют росту рубцовой ткани. Данный метод эффективен только в начале формирования рубца (первые полгода). Силиконовые средства улучшают гидратацию в рубцово-измененной коже и создают кислородное голодание, благодаря которому сосуды в рубце уменьшаются.
Начинать профилактику образования рубца рекомендуется через 3 — 4 недели, когда от ранки полностью отойдут корочки. Заживающее место надо держать в чистоте, мыть с мылом и ни в коем случае не снимать ороговевший слой с ранки — так вы занесете инфекцию, а это верный путь к образованию келоидного рубца!
Возможные методы лечения келоидных рубцов
Несмотря на обилие советов в интернете, народными средствами не избавиться от келоидных рубцов, они могут применяться лишь в комплексе с медикаментами, физиотерапией или косметологией.

Самые популярные способы избавления от келоидных рубцов — это медикаментозное лечение, то есть использование гелей, мазей, кремов и инъекций в сочетании с физиотерапией, например, с ультрафонофорезом или электрофорезом и введение под кожу гормонов-кортикостероидов. Также эффективна мезотерапия — инъекции в ткань рубца витаминных комплексов и лечебных веществ, рассасывающих избыточный коллаген и избыточную гиалуроновую кислоту.
Если консервативные методы не дают ожидаемого результата, то прибегают к хирургии.
Медикаментозное лечение

Аптечные и косметические средства бывают разных направлений:
- содержат интерферон;
- кортикостероиды;
- ферменты или ферментосодержащие препараты.
Содержащие интерферон средства затормаживают выработку коллагена. Иными словами, рубец перестает расти в размерах, однако, он остается на той стадии, до которой дорос сейчас. К подобному способу лечения келоидного рубца прибегают после хирургического вмешательства в виде инъекций альфа- и бета-интерферона.
Уколы делают через сантиметр по всей длине рубца, продолжительность курса длится 4 месяца.
Кортикостероиды могут вводиться как сами по себе, так и комплексно с другими веществами и какой-либо терапией. Их вводят не в сам келоидный рубец, а ближайшее место рядом с ним. Это оберегает от дальнейшего уплотнения шрама, и, несмотря на курс лечения – 5 недель, у 20–30% пациентов наблюдаются рецидивы.
В качестве профилактики повторного образования рубца терапию дополняют лазерным или хирургическим удалением шрама. Данные методы являются очень болезненными и не исключают рецидив (повторное образование рубца). Лазерная шлифовка требует длительного периода восстановления.
Ферментосодержащие препараты расщепляют избыточный коллаген и избыточную гиалуроновую кислоту – основные составляющие рубцовой ткани. За счет этого восстанавливается рельеф и цвет кожи. Рубец становится эластичным, предотвращается его активный рост.
Прессотерапия

Способ, скорее близкий к профилактике, чем к лечению, но некоторые специалисты отмечают положительный эффект.
На проблемное место накладывают различные силиконовые повязки, бинты и пластины. Считается, что постоянно сдавливаемый рубец уменьшается в размерах. К средствам прессотерапии причисляют:
- хлопчатобумажное белье и специальные бандажи (рекомендовано носить полгода, делаются по индивидуальным меркам);
- силиконовые и гелевые давящие пластины;
- жидкости на основе геля — коллодий с полисиликоном или силиконом.
Все это можно найти в любом ортопедическом салоне или аптеке, но данный способ сам по себе не сможет полностью убрать келоидный рубец. Метод прессотерапии эффективен только в комплексном терапии в сочетании с другими способами коррекции рубца.
Микротоковая физиотерапия
Во время процедуры на организм ведется воздействие слабым током, из-за чего стимулируются обменные процессы в тканях эпидермиса, келоид уменьшается в размере и разглаживается.
Этапы проведения терапии:
- обработка шрама антисептиком;
- нанесение препарата, разрушающего рубец;
- подключение прибора, воздействие на рубец током;
- удаление оставшегося лекарства салфеткой.
Процедура не сложная по исполнению, однако, к ней есть противопоказания:
- обостренные вирусные заболевания;
- плохая свертываемость крови;
- патологии с сердцем;
- обострение хронических заболеваний;
- неврологические отклонения от нормы.
Эта процедура считается малоэффективной, по сравнению с другими видами физиотерапии. К тому же она стоит недешево.
Лучевое воздействие
Подразумевает регулируемое рентгеновское излучение, разрушающее фибробласты внутри рубцовых тканей. Интенсивность лучей назначается исходя из серьезности проблемы: ведь 90% от всего потока поглотит эпидермис, и только 10% достигнут глубинных слоев кожи.
Однако терапия проводится лишь в комплексе с другим лечением, иначе риск рецидива повышается на 50%.
Противопоказания к применению:
- шрамы на лице, шее и груди;
- онкология;
- заболевания почек;
- нарушенное кровообращение.
Обычная доза облучения 15–20 Гр. Процедуру повторяют раз в 2 месяца, но не более 6 раз.
Однако лучевое воздействие считается одним из самых эффективных методов в борьбе с рубцами, независимо от причины их появления.
Удаление келоида лазером
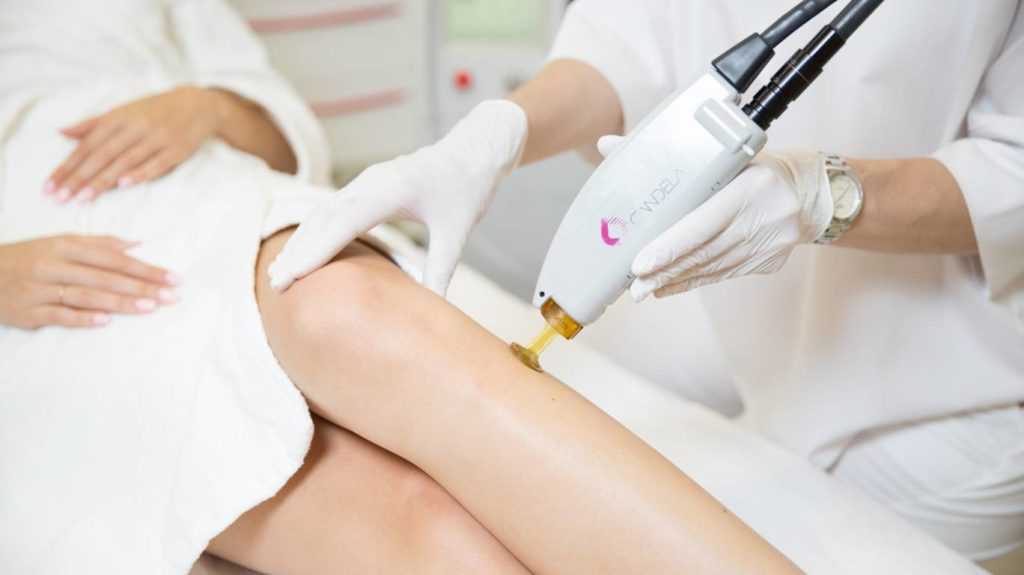
Бывает нескольких видов лизерной шлифовки: аргоновая, углеродная и дермабразия. Цель процедуры состоит в выпаривании жидкости из соединительных тканей шрама, из-за чего он высыхает и уменьшается в размере. Мертвые клетки убирают хирургическим путем, а сама лазерная процедура проводится под местной анестезией.
Достоинства лазерного удаления:
- во время первого сеанса исчезает до 70% шрама, что говорит о быстром видимом результате;
- длительность терапии от 20 минут до полутора часов, в зависимости от сложности проблемы.
Процедура достаточно болезненная и требует длительного периода реабилитации.
Чтобы избежать рецидива, врачи советуют сочетать лазер с другими видами лечения келоидных рубцов: применение противорубцовых гелей станет отличным помощником на пути к здоровой коже.
Криометодика
Влияние на келоид жидким азотом. Он выжигает клетки рубцовой ткани, на месте которых образуется здоровая кожа. Время соприкасания рубца с азотом 10–30 секунд, при передозировке возможна пигментация, также велик риск заработать атрофический рубец. Нужно быть крайне осторожным с данным методом коррекции!
Видимый эффект достигается за 1–3 сеанса, но для лучшего результата криотерапию совмещают с гормональными уколами с глюкокортикостероидами.
Однако при больших шрамах прижигание азотом лучше совместить с хирургией. Главным недостатком метода является болезненность.
Косметология

Сделать рубец менее заметным помогут косметические процедуры. Полностью избавиться от рубца с их помощью не получится, но в сочетанной терапии эти методы очень даже эффективны:
- дермабразия;
- пилинг;
- мезотерапия.
Пилинг. С помощью пилингов можно отшлифовать рубец, выровнять рельеф кожи и устранить пигментацию. В результате кожа становится более гладкой, а рубец более эластичным.
Глубокая дермабразия — отшелушивание рогового слоя эпидермиса. Процедура чувствительная, предполагает использование аппаратной техники. Как глубоко и долго проводить сеанс, решает косметолог.
Мезотерапия — инъекции гепарина, иммуномодулятора или витаминного комплекса в проблемный участок. Оказывает противовоспалительный и смягчающий эффект.
При небольшом шраме рекомендована дермабразия или мезотерапия, а большие и застарелые келоиды удаляются в комплексе с медикаментозной терапией.
Хирургия
Назначается в крайнем случае когда другие терапии недостаточно эффективны. Иссечение келоида проводят через пару лет после его образования и в несколько этапов:
- небольшой надрез скальпелем на шраме под местным наркозом;
- края рубца сшиваются косметическими стежками для лучшего срастания надреза;
- после рассасывания швов — гормональные инъекции и ферментативная терапия.
После операции показана профилактика против рецидива, ведь свежий рубец лучше поддается коррекции. Во время реабилитационного периода часто прописывают лучевую терапию, инъекции с иммуномодуляторами и гормонами, а также наружные средства в виде гелей и мазей.
Лечение с Ферменколом

Вся продукция линейки Ферменкол содержит комплекс из 9 ферментов коллагеназы — вещества, расщепляющего избыточный коллаген и избыточную гиалуроновую кислоту до простейших элементов.
Ферменкол используют в виде аппликаций (просто мазать), а также в сочетании с физиотерапией. Так, гель Ферменкол подходит для процедур фонофореза, а Ферменкол в виде раствора — для электрофореза.
Чем быстрее вы начнете лечение келоидного рубца, тем проще и дешевле от него будет избавиться! Не упускайте возможность вернуть красивую кожу, как можно скорее.
Получить бесплатную консультацию по своей проблеме можно, задав вопрос специалисту. Вам ответят в ближайшие два дня и подскажут оптимальный метод коррекции келоидного рубца.
Помните! Молодые рубцы быстрее и проще поддаются коррекции, чем застарелые. Не упускайте время, начните заботиться о себе уже сегодня!
Читайте также:

