Мезим при атопическом дерматите
Обновлено: 25.04.2024
Распространенность аллергических заболеваний у детей остается высокой. Это подтверждается многочисленными клиническими наблюдениями и результатами эпидемиологических исследований.
Распространенность аллергических заболеваний у детей остается высокой. Это подтверждается многочисленными клиническими наблюдениями и результатами эпидемиологических исследований. В структуре аллергических заболеваний атопический дерматит занимает ведущее место. Атопический дерматит — системное аллергическое заболевание со сложным патогенезом и характерной возрастной эволюцией клинических проявлений. Характеризуется упорным течением, частыми обострениями и недостаточной эффективностью существующих методов лечения.
На протяжении многих лет совершенствовались и углублялись знания о природе заболевания, появлялись новые концепции патогенеза, менялась терминология. Согласно современной концепции в основе развития атопического дерматита лежат иммунологические механизмы и нарушения (дисфункция) эпидермального барьера. Основные патоморфологические изменения, возникающие при атопическом дерматите, происходят в эпидермисе, затрагивая дерму при тяжелом, непрерывно-рецидивирующем течении болезни.
В настоящее время сформировалась научная точка зрения, что атопический дерматит развивается под влиянием генетических и внешнесредовых факторов. Антигенная нагрузка на организм факторов экзогенного и эндогенного происхождения играет одну из важнейших ролей в механизмах развития заболевания.
К экзогенным факторам относятся разнообразные аллергены (пищевые, бытовые, клещевые, пыльцевые, грибковые, эпидермальные, лекарственные) и неспецифические стимулы (климат, стресс, курение, холод). Эндогенные факторы составляют патологические состояния, ассоциирующиеся с атопическим дерматитом. У 80–90% детей с атопическим дерматитом наблюдаются патологические изменения в желудочно-кишечном тракте, у 20–30% — в дыхательной системе и у 15–18% — в почках. Нарушение барьерной функции внутренних органов способствует более быстрому поступлению в организм экзоаллергенов. При длительном, непрерывно-рецидивирующем течении болезни у подавляющего большинства больных нарушаются процессы их элиминации. Происходит накопление в тканях и биологических жидкостях продуктов нарушенного метаболизма, повышается содержание желчных кислот, концентрация биологически активных веществ (гистамина, серотонина, эйкозаноидов, цитокинов и т. д.), образующихся в организме в процессе значительной антигенной стимуляции. Развивается синдром эндогенной интоксикации. Клинически синдром эндогенной интоксикации проявляется в виде мраморности кожи, акроцианоза, сероватого оттенка кожи, сухости и шелушения.
С целью детоксикации используется эфферентная терапия, направленная на выведение из организма аллергенов и токсинов. Наиболее эффективными из них являются сорбционные методы. В педиатрической практике наиболее часто используется метод энтеросорбции — метод, основанный на связывании и выведении из организма аллергенов, различных экзогенных и эндогенных соединений, патогенных микроорганизмов и продуктов их жизнедеятельности.
Энтеросорбция — это метод лечения, основанный на способности энтеросорбентов связывать и выводить из организма различные экзогенные вещества, микроорганизмы и их токсины, промежуточные и конечные продукты обмена веществ. Эти вещества способны накапливаться или проникать в просвет ЖКТ.
На фоне энтеросорбции происходит повышение функциональной активности клеточного и гуморального иммунитета, увеличивается число Т-лимфоцитов, уменьшается выраженность эозинофилии, снижается уровень циркулирующих иммунных комплексов, уменьшается зуд кожных покровов и отек, снижается частота и тяжесть приступов бронхиальной астмы.
Энтеросорбенты (ЭСБ) — препараты медицинского назначения, обладающие высокой сорбционной емкостью, не разрушающиеся в ЖКТ и способные связывать экзо- и эндогенные вещества путем адсорбции, ионообмена или комплексообразования.
Существенным является то, что сорбенты позволяют уменьшить дозу гормонов, а в некоторых случаях даже отменить.
В клинической практике используется широкий ассортимент сорбционных средств. Лечебный эффект сорбента достигается за счет физико-химических свойств сорбирующего вещества, способного связывать и выводить из организма экзогенные и эндогенные соединения. Решающую роль играет пористость, характеризующая наличием пор между зернами, слоями, кристаллами. Сорбенты могут иметь микропоры, мезопоры, макропоры. Поэтому выбор сорбента с разной пористой структурой влияет на адсорбцию тех или иных токсинов, что определяет терапевтический эффект сорбента.
Энтеросорбенты подразделяются по таким характеристикам:
- По лекарственной форме — гранулы (угли), порошки (карболен, холестирамин), таблетки, пасты, пищевые добавки (пектины, хитин).
- По химической структуре — угли активированные, алюмосиликаты, алюмогель, сорбенты окисные, органоминеральные и композиционные, пищевые волокна.
- По механизмам сорбции — адсорбенты, абсорбенты, ионообменные материалы, сорбенты с катаболическими свойствами, сорбенты с сочетанными механизмами.
- По селективности — селективные, моно-, би-, полифункциональные, неселективные (угли активированные, природные препараты — лигнин, хитин, целлюлоза) [1].
К современным энтеросорбентам предъявляются следующие требования:
- не должны обладать токсическими свойствами;
- быть нетравматичными для слизистых оболочек;
- хорошо эвакуироваться из кишечника;
- иметь хорошие функциональные (сорбционные) свойства;
- не вызывать дисбактериоз;
- иметь удобную лекарственную форму.
Особый интерес представляют сорбенты, в состав которых входит пребиотик. К таким средствам относится Лактофильтрум. Препарат содержит пребиотик (лактулозу) и сорбент (лигнин).
Свойства Лактофильтрума обусловлены высокой сорбционной способностью природного энтеросорбента на основе лигнина. Лигнин гидролизный — сложное природное органическое соединение, продукт гидролизной переработки древесины, энтеросорбент. Обладает неспецифическим дезинтоксикационным действием. Связывает, удерживает и выводит из организма различную патогенную микрофлору, экзо- и эндотоксины, лекарственные препараты, соли тяжелых металлов, алкоголь, аллергены, избыток некоторых продуктов обмена веществ (билирубина, холестерина, гистамина, серотонина, мочевины, иных метаболитов, ответственных за развитие эндогенного токсикоза). За счет большой площади поверхности и развитой системы пор лигнин обладает высокой сорбционной емкостью. Лигнин не токсичен, не всасывается, полностью выводится из кишечника в течение 24 часов.
Второй компонент Лактофильтрума — лактулоза — синтетический дисахарид, состоящий из остатка галактозы и остатка фруктозы. В толстом кишечнике лактулоза ферментируется нормальной микрофлорой кишечника в качестве пищевого субстрата. Лактулоза стимулирует рост бифидобактерий и лактобактерий в толстом кишечнике, способствует нормализации обмена белков, жиров и углеводов, правильному всасыванию витаминов, макро- и микроэлементов, а также стимулирует неспецифический иммунитет. В результате гидролиза лактулозы образуются органические кислоты (молочная, уксусная и муравьиная), подавляющие рост патогенных микроорганизмов и уменьшающие вследствие этого продукцию азотсодержащих токсических веществ. Описанный процесс приводит к увеличению осмотического давления в просвете толстого кишечника и стимулированию перистальтики. Лактулоза не усваивается человеческим организмом.
Преимущество Лактофильтрума в его двойном действии: сорбент нейтрализует патогенные микроорганизмы и выводит кишечные токсины, а пребиотик стимулирует рост полезной микрофлоры (бифидо- и лактобактерий). Комплексное воздействие компонентов Лактофильтрума приводит к формированию мощного защитного фактора — нормальной микрофлоры кишечника, ликвидации клинических проявлений дисбактериоза, более быстрому исчезновению симптомов аллергических заболеваний и к эффективной детоксикации организма.
Способ применения и дозы
Ниже представлен опыт применения Лактофильтрума в комплексной терапии детей с атопическим дерматитом. Под наблюдением находилось 36 детей в возрасте от двух до пяти лет (n = 26 — основная группа, n = 10 — контрольная группа). Мальчиков было 20, девочек — 16. Длительность заболевания колебалась от одного года до 4,5 лет. По тяжести заболевания: у 16 детей наблюдалось среднетяжелое течение болезни (индекс SCORAD = 38,4 ± 1,8 балла), у 10 больных тяжелое течение атопического дерматита (индекс SCORAD = 56,5 ± 1,5 балла). Группу сравнения составили 10 детей со среднетяжелым течением атопического дерматита, получавших только традиционную терапию.
У детей со среднетяжелым течением атопического дерматита кожный процесс был локализован в области лица, шеи с переходом на кожу предплечий и локтевых сгибах, на сгибательной поверхности лучезапястных суставов, тыла кистей и в подколенных ямках. Патологический процесс носил островоспалительный характер и был представлен гиперемией, отеком, очагами экссудации, экскориациями, корочками, шелушением. Кожа вне очагов поражения была сухой, со сниженным тургором и эластичностью. Отмечался зуд кожных покровов умеренной интенсивности.
У детей с тяжелым течением атопического дерматита процесс был распространенным, отмечалась яркая гиперемия и отечность, выраженные и обширные очаги экссудации, папулезные элементы, сливающиеся в очаги стойкой инфильтрации. Лихенификация была ярко выраженной, наблюдались глубокие линейные трещины, экскориации, серозно-геморрагические корочки. У всех больных наблюдался выраженный зуд, нарушение сна.
Лактофильтрум назначали внутрь 3 раза в день между приемами пищи (за 1–1,5 часа до или после еды или приема других лекарственных средств).
Возрастные дозировки: детям от трех до пяти лет по 1 таблетке 3 раза в день; а детям от двух до трех лет по 1/2 таблетки 3 раза в день. Длительность курса приема 2 недели.
Включение в комплексную терапию атопического дерматита, сопровождающегося синдромом эндогенной интоксикации, энтеросорбента Лактофильтрум позволило существенно уменьшить выраженность кожного процесса, зуда и сухости кожных покровов. При этом индекс SCORAD у детей основной группы уменьшился до 14,6 ± 2,1 и 28,4 ± 1,4 балла соответственно (рис. 1), в то время как у детей из группы сравнения не наблюдалось столь выраженного регресса кожных высыпаний.
.jpg)
У пациентов основной группы на фоне применения Лактофильтрума отмечалась нормализация имеющихся нарушений со стороны стула. Курсовое использование Лактофильтрума позволило сократить период обострения (рис. 2), продлить ремиссию заболевания в среднем на 4,6 ± 2,3 месяца у детей в основной группе по сравнению с больными из группы сравнения (2,9 ± 1,8 месяца).
.jpg)
Таким образом, включение в состав комплексной терапии детей с атопическим дерматитом препарата Лактофильтрум в возрастной дозе в течение 14 дней повышало клиническую эффективность лечения, способствуя более быстрому разрешению кожного процесса, что показывает не только положительный краткосрочный эффект, но и позитивные долгосрочные результаты. Препарат удобен для приема, не токсичен, не вызывает развитие побочных эффектов.
Литература
В. А. Ревякина, доктор медицинских наук, профессор
Для цитирования: Хамаганова И.В., Никифорова Г.Д., Шекрота А.Г., Колибрина А.М. Применение гастроинтестинальных препаратов в комплексной терапии атопического дерматита. РМЖ. 2004;14:828.
Терапия атопического дерматита остается одной из актуальных задач дерматологии. Отсутствие эффективных десенсибилизирующих, противозудных средств предопределило интерес к необходимости воздействия на другие патогенетические механизмы. В настоящее время хорошо известно, что патологический процесс развивается на фоне функциональных нарушений центральной нервной системы, психических расстройств, изменений реактивности вегетативной нервной системы. Клинические поражения кожи варьируют в зависимости от возраста, нередко сочетаясь с поражением органов дыхания, почек, глаз, желудочно–кишечного тракта. Последнее обусловило необходимость включения в комплексную терапию препаратов, нормализующих моторику желудка и кишечника, состояние микрофлоры, желчеотделение, ферментативную активность [1]. В настоящей работе представлены результаты применения Дюфалака и Креона 10 000 в комплексном лечении атопического дерматита у взрослых и детей.
Дюфалак представляет собой раствор лактулозы (6–га – лактозид–фруктоза).100 мл сиропа содержит лактулозы 67 г; выпускается в полиэтиленовых флаконах по 200 и 500 мл, в комплекте с мерным стаканчиком. Препарат в неизмененном виде достигает уровня толстой кишки, оказывает осмотический «подсасывающий» эффект по типу «внутренней клизмы».Та часть лактулозы, которая успевает разложиться под влиянием кишечной флоры (в особенности при дисбактериозе) преобразуется в молочную и уксусную кислоту, частично – углекислоту. Указанные продукты закисляют содержимое толстой кишки, подавляя гнилостное брожение и всасывание аммиака (переводя его в аммоний). Последнее свойство препарата позволяет нормализовать кишечную флору при дисбактериозе, распространенном среди больных атопическим дерматитом, и уменьшить сопровождающую поражение кожи интоксикацию. Применение лактулозы приводит к изменению состояния кишечной микрофлоры, выражающемуся в повышении содержания бифидобактерий, лактобацилл и в снижении количества условно–патогенных микроорганизмов [3]. Обосновано применение лактулозы у больных язвенной болезнью, ассоциированной с Helicobacter pylori. Показана целесообразность назначения препарата больным, принимающим блокаторы Н 2 –рецепторов гистамина, так как последние активизируют антрагастральную бактериальную пролиферацию [4]. Препарат показан при хронических заболеваниях печени, желчно–каменной болезни [3,5]. Лактулоза является высокоэффективным средством для лечения печеночной энцефалопатии [5]. Ранее было показано, что гепато–билиарная патология распространена среди больных атопическим дерматитом [1,6–9].
Креон 10 000 (панкреатин) является препаратом, восполняющим дефицит ферментов поджелудочной железы.1 капсула с минимикросферами, покрытая кишечнорастворимой оболочкой, содержит 150 мг панкреатина, что соответствует 8000 МЕ амилазы, 10 000 МЕ липазы и 600 МЕ общих протеаз. Препарат применяется при нарушениях процессов пищеварения в качестве заместительной или симптоматической терапии. Многочисленные свидетельства дефицита ферментов поджелудочной железы при атопическом дерматите широко представлены в литературе [6–9], что является основанием к изучению применения Креона 10 000 в дерматологической практике. Под нашим наблюдением находилось 118 больных атопическим дерматитом в возрасте от 6 до 32 лет, в том числе 96 женщин, 22 мужчины (основная группа). Давность заболевания составляла от 2 до 29 лет (у всех пациентов заболевание началось до трехлетнего возраста). Все больные отмечали значительное улучшение состояния в летнее время года. Обострения были связаны с психоэмоциональными стрессами, погрешностями в диете, контактом с бытовыми аллергенами. Все пациенты ранее получали терапию, включающую десенсибилизирующие, седативные, антигистаминные средства, наружные противовоспалительные препараты (содержащие глюкокортикоиды, АСД, нафталан) с временным эффектом. К началу нашего обследования у всех пациентов процесс на коже носил распространенный характер и был представлен характерными для каждой возрастной группы очагами поражения на лице, шее, сгибательных поверхностях конечностей. Пациентов беспокоил зуд (разной степени выраженности, от умеренного до нестерпимого). Критериями исключения из данной (основной) группы были: повышеннаячувствительность к лактулозе, панкреатину, галактоземия, непроходимость кишечника, панкреатит. Ранее была показана целесообразность применения эбастина в сочетании с наружными нестероидными противовоспалительными средствами при атопическом дерматите [10]. Эти препараты использовались как в лечении больных основной, так и контрольной группы. Всем больным был назначен Дюфалак: детям в возрасте 6 лет по 5 мл, от 7 до 14 лет по 10 мл, взрослым по 15 мл утром натощак. Креон 10000 назначали: детям от 6 до 14 лет по 1 капсуле во время обеда, взрослым в течение первой недели лечения по 1 капсуле во время обеда, затем по 1 капсуле во время завтрака и обеда. Кроме того, все пациенты получали эбастин: дети в возрасте от 6 до 12 лет по 5 мг, от 12 лет по 10 мг 1 раз в сутки. Наружно применяли – противовоспалительные нестероидные средства. Контрольную группу составили 32 пациента с атопическим дерматитом в возрасте от 6 до 32 лет (28 женщин, 4 мужчин). Давность заболевания составляла от 2 до 29 лет. Клиническая картина была сопоставима по степени тяжести процесса и распространенности процесса у больных основной группы. Пациентам назначали эбастин в тех же дозировках, что и пациентам основной группы, аналогичные наружные нестероидные противовоспалительные средства. Продолжительность курса лечения в обеих группах составляла 20 дней. В основной группе некоторое уменьшение зуда, эритемы было отмечено на 2–3–й день лечения. В дальнейшем регресс высыпаний продолжался, и к окончанию курса лечения у 96 из 118 больных (81,36 %) сохранялась легкая гиперпигментация, частично – лихенизация, явления экссудации, инфильтрации, разрешились полностью, что было расценено нами, как значительное улучшение. У 22 отмечено улучшение состояния. В контрольной группе некоторое уменьшение зуда, эритемы отмечено на 2–3–й день. Значительное улучшение состояния достигнуто к окончанию терапии у 6 пациентов (27,27%), у 16 – улучшение состояния (72,73%). Как в основной, так и в контрольной группе пациентов нами не было отмечено отрицательной динамики лабораторных показателей периферической крови, мочи. Все больные в двух группах лечение переносили хорошо, побочных реакций и нежелательных явлений отмечено не было. Таким образом, результаты наших наблюдений свидетельствуют об обоснованности и целесообразности включения в комплексную терапию атопического дерматита средств, нормализующих кишечную флору, моторику желудка и кишечника, дезинтоксикационных, восполняющих дефицит ферментов поджелудочной железы.
Представленные данные свидетельствуют о высокой эффективности комплексной терапии атопического дерматита с применением таких препаратов, как Дюфалак, Креон 10 000, эбастин. Высокая эффективность, хорошая переносимость, отсутствие побочных эффектов позволяют рекомендовать их для использования в дерматологической практике.
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Для цитирования: Ревякина В.А. Современные аспекты терапии атопического дерматита у детей. РМЖ. 1999;11:516.
Среди аллергических заболеваний кожи у детей атопический дерматит (АД) занимает одно из ведущих мест. Распространенность этого заболевания, по данным эпидемиологических исследований, колеблется от 17-25% [1, 4]. Проблема АД чрезвычайно важна для педиатрии. Начинаясь в раннем детском возрасте, АД приобретает упорное, непрерывно-рецидивирующее течение, и наблюдается практически во всех возрастных периодах. Отмечена тенденция к формированию тяжелых, резистентных к терапии форм заболевания, снижению социальной адаптации и развитию инвалидизации ребенка [4].
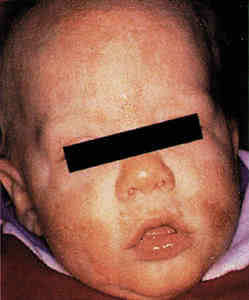
Дебют атопического дерматита.
Кожа является органом с многообразными функциями и сложными метаболическими процессами, обуславливающими связь внутренних органов с внешней средой, и выполняет важную роль в поддержании иммунного статуса организма. Согласно современным данным патогенетическую основу АД составляет аллергическое воспаление и гиперреактивность кожи, нарушающие естественную реакцию на воздействие различных внешних и внутренних факторов. Ключевую роль в механизмах развития АД играют IgE-опосредуемые реакции, обусловленные генетически детерминированной дисфункцией Т-лимфоцитов (хэлперов 2 типа) и рядом цитокинов, являющихся основными регуляторами синтеза иммуноглобулина Е [5, 6].
Развитие АД у детей тесно связано с воздействием различных аллергенов, причем у детей первых лет жизни ведущую роль играют пищевые аллергены (коровье молоко, яйцо, рыба, злаковые, овощи и фрукты оранжевой или красной окраски). С возрастом роль пищевой аллергии в развитии АД уменьшается и доминирующее значение приобретают такие ингаляционные аллергены, как домашняя пыль, пыльца растений, грибковые и эпидермальные аллергены.
Среди факторов, предрасполагающих к развитию АД у детей раннего возраста, следует отнести нарушение процессов пищеварения и всасывания из-за транзиторной ферментативной недостаточности, дискинезии билиарного и желудочно-кишечного тракта, перенесенного вирусного гепатита, нарушения микрофлоры кишечника, заражения гельминтами и простейшими (лямблиоз, энтеробиоз, описторхоз).
Современная терапия АД является патогенетической и включает проведение элиминационных мероприятий, медикаментозного лечения, наружной терапии, физиотерапии и санаторно-курортного лечения. Терапия должна быть строго индивидуальной, учитывать клиническую форму, стадию и период болезни, сопутствующие патологические состояния и осложнения.
Элиминационные мероприятия
Среди элиминационных мероприятий у детей раннего возраста ведущее место занимает исключение пищевых аллергенов с назначением специализированных диет, эффективность которых зависит от полноты выявления и исключения из рациона питания всех причинно-значимых продуктов [7]. Непременным условием является их замена равноценными по питательной ценности и калоражу пищевыми продуктами, обеспечивающими максимальное удовлетворение возрастных физиологических потребностей детей в основных пищевых веществах и энергии.
Специализированные диеты при АД обладают не только диагностическими и лечебными возможностями, но имеют определенную профилактическую направленность.
В начале обследования ребенка до получения результатов специфической диагностики используется эмпирическая диета. Она предусматривает исключение из питания подозреваемых (по данным анамнеза и клиническим проявлениям) пищевых аллергенов, а также продуктов, обладающих высокой аллергизирующей способностью (яйца, рыба, икра, морские продукты, грибы, орехи, мед, морковь, малина, клубника, черная и красная смородина, цитрусовые, шоколад, помидоры). Необходимым условием является также исключение мясных бульонов, острых и сильно соленых блюд, пряностей, маринадов, кофе, какао, консервированных продуктов. Затем устраняются из пищевого рациона вещества, выявленные в ходе специфического аллергологического обследования.
При развитии пищевой аллергии у ребенка, находящегося на естественном вскармливании, кормящей матери назначается специальная гипоаллергенная диета, предусматривающая исключение высокоаллергенных пищевых продуктов, а также продуктов, обладающих раздражающим действием на слизистую оболочку желудочно-кишечного тракта. Молочные продукты даются только в виде кисломолочных изделий, сметаны и неострого сыра. Гипоаллергенную диету кормящим матерям назначают на весь период кормления ребенка грудью [7]. Аналогичные диеты применяют у беременных женщин, страдающих аллергическими заболеваниями, особенно в течение последнего триместра беременности.
При аллергии к белкам коровьего молока назначают безмолочные диеты. У детей со слабо выраженной сенсибилизацией к этим белкам исключают цельное коровье молоко, пресные молочные смеси и творог. Таких детей переводят на такие адаптированные кисломолочные смеси, как (АГУ-1), (АГУ-2), ацидофильная смесь, (Бифилин) или гипоаллергенные смеси с частично гидролизованным белковым компонентом - (Хипп-ГА), (Хумана ГА), (Фрисопеп). У детей второго полугодия жизни можно назначать неадаптированные кисломолочные продукты - кефир, биокефир, (Биолакт), (Ацидолакт), а также продукты из сухого коровьего молока или молочных смесей, заквашенных специальными заквасками, содержащими бифидобактерии и ацидофильную палочку - (Наринэ), (Ацидофлора).
При выраженной аллергии к белкам коровьего молока (отсутствие положительной клинической динамики при использовании кисломолочных продуктов и выявленные высокие титры IgE или IgG антител к белкам коровьего молока) в качестве заменителя коровьего молока могут назначаться специализированные адаптированные смеси на основе изолята соевого белка, не содержащие молочного протеина и лактозы. К ним относятся - (Нутрилак-соя), (Хумана-СЛ), (Энфамил-соя), (Нутри-соя), (Бона-соя), (Фрисо-соя), (Хайнц-соевая смесь), (Туттели-соя).
Положительный эффект от применения соевых смесей наступает, как правило, через 3-4 нед от начала их использования и при обязательном исключении молочных, кисломолочных продуктов и творога.
При аллергии к белкам коровьего молока и сои, что наблюдается у 15-20% детей, назначают специализированные гипоаллергенные лечебные смеси, приготовленные на основе гидролизатов молочного белка с высокой степенью гидролиза - (Прегестимил), (Нутрамиген), (Алиментум, Пепти-Юниор), (Альфаре), (Пептиди-Туттели). Используют также гидролизаты белков молочной сыворотки с низкой степенью гидролиза белка - (Фрисо-пеп), (Хумна-ГА 1), (Хумана-ГА 2), (Хипп-ГА).
Элиминационные диеты не утрачивают своего значения и у детей старшего возраста. Успешное решение диетотерапии у детей старшего возраста во многом зависит от наличия специализированных продуктов, не уступающих элиминируемым [7]. Важным моментом при составлении диет у детей старшего возраста является исключение таких напитков, как газированные воды, жевательной резинки, которые нередко являются причиной обострения кожного процесса.
Среди других элиминационных мероприятий у детей с АД очень важное значение имеет уменьшение контакта с аллергенами жилищ, домашних животных, пыльцой растений.
Системная терапия
Полиорганность аллергических поражений при АД требует комплексного подхода к терапии этих детей, в связи с чем медикаментозное лечение предусматривает использование лекарственных средств, воздействующих на различные стороны патогенеза этого заболевания [8]. При назначении патогенетической и симптоматической терапии необходимо учитывать период заболевания: острый, подострый и ремиссию (см. схему).
Для купирования острых клинических проявлений АД назначают антигистаминные препараты. Они представлены группой медикаментозных средств, конкурирующих с гистамином на уровне Н1-рецепторов. Связываясь с Н1-рецепторами, эти препараты предупреждают или сводят к минимуму аллергические реакции, блокируя эффекты гистамина . К антигистаминным препаратам относятся средства первого (клемастин, хлоропирамин, ципрогептадин, диметинден, мебгидролин) и второго (терфенадин, астемизол, лоратадин, цетеризин, эбастин) поколения.
Эффективность антигистаминных препаратов первого поколения при лечении АД установлена давно. Их лечебное действие начинается быстро, в течение 15-20 мин, купируя острые проявления аллергии. Они обладают рядом побочных действий: седативным и холинергическим (сонливость, сухость слизистых оболочек, особенно в области глаз, задержка мочи, запоры, тахикардия).
Антигистаминные препараты второго поколения избирательно действуют на периферические Н1-рецепторы, обладают меньшей нейротоксичностью и седативным действием и в последние годы широко используются в терапии острого и подострого периодов АД.
В терапии АД применяются лекарственные средства, действие которых направлено на торможение секреции медиаторов аллергии - кетотифен и кромогликат натрия. Включение кетотифена в лечебный комплекс при АД уже с середины 2-й недели лечения приводит к улучшению общего состояния, аппетита, двигательной активности, уменьшению или исчезновению кожных высыпаний и ослаблению зуда. После 3-месячного применения положительный результат отмечается у большинства детей с экссудативным компонентом воспаления кожи. Длительное лечение кетотифеном - от 6 до 12 мес оправдано у детей с поливалентной аллергией и у больных с частыми обострениями болезни.
Кромогликат натрия - лекарственное средство, непосредственно и специфически воздействующее на слизистую оболочку желудочно-кишечного тракта, механизм действия которого направлен на стабилизацию мембран тучных клеток и предупреждение развития аллергических реакций на уровне слизистой оболочки пищеварительного тракта. Кромогликат натрия назначают прежде всего больным, имеющим гастроинтестинальные проявления пищевой аллергии, и тем, у которых не наблюдается положительного эффекта от проводимой диетотерапии и приема антигистаминных препаратов. Препарат используют, как правило, в подострый период заболевания и продолжают в фазе ремиссии болезни.
Интенсивный зуд, раздражительность, беспокойство, нарушение сна требуют применения препаратов, обладающих седативным эффектом. Некоторые антигистаминные (клемастин, хлоропирамин, диметинден, фенистил) и антисеротониновые (ципрогептадин) препараты обладают противозудным и седативным действием, в связи с чем они продолжают широко использоваться в терапии АД. В некоторых случаях показано применение транквилизаторов (оксазепам, диазепам) и нейролептиков (тиоридазин, хлорпромазин), антидепрессантов (имипрамин, амитриптилин), которые, снижая возбудимость и нормализуя сон, способствуют разрешению патологических изменений на коже. Однако их назначение требует строгих обоснований, учета прежде всего психического статуса больного.
Отчетливая связь между обострениями кожного процесса при АД и нарушениями функционального состояния органов пищеварения требует назначения препаратов, устраняющих гастроэнтерологические расстройства. С этой целью используют различные ферментные и желчегонные препараты, средства, нормализующие моторику желудочно-кишечного тракта. Дисбактериоз кишечника у детей первого года жизни является показанием для целенаправленного воздействия на микрофлору с селективным уничтожением патогенных бактерий и заселением кишечника недостающими представителями флоры (препаратами бифидумбактерий, лактобактерий, колибактерий). Весьма важно общее воздействие на микрофлору с целью создания таких условий в кишечнике, которые были бы неблагоприятны для нежелательных микроорганизмов и благоприятствовали заселению недостающими.
Оправдано использование в комплексной терапии АД витаминных препаратов (b-каротин, витамин А, Е, В6, аскорбиновая кислота), улучшающих межуточный обмен, способствующих повышению адаптационных возможностей организма. Однако применение комплексных поливитаминных препаратов может быть частой причиной обострений АД.
Одним из перспективных направлений терапии АД является фармакологическая коррекция нарушений иммунной системы с применением иммуномодулирующих препаратов, направленных на стимуляцию или угнетение функции клеток, участвующих в иммунном ответе.
Локальная терапия
Общую терапию АД следует проводить в сочетании с наружным лечением. Рациональное использование наружных лекарственных средств с учетом морфологии и стадии заболевания значительно повышает эффективность проводимого лечения и оказывает благоприятное влияние на регресс кожных проявлений аллергии. Используемые при этом лекарственные препараты оказывают не только местное, но и общее воздействие на организм через нервно-рецепторный аппарат, посредством всасывания их через кожу. Исчезновение или уменьшение с помощью местных лекарственных средств кожных проявлений аллергии, а также таких субъективных ощущений, как зуд, боль, жжение, положительно сказывается на общем и психоэмоциональном состоянии ребенка.
В острой стадии АД с явлениями гиперемии, отека, везикулезно-папулезных высыпаний, регионального лимфаденита следует назначать примочки из крепкого настоя чая, коры дуба, 1% раствора танина, 1-3% раствора резорцина, 1-2% водного раствора метиленовой сини, фукорцина (жидкости Кастеллани). Пиогенные высыпания целесообразно тушировать спиртовыми растворами анилиновых красок или с помощью аэрозолей с антибиотиками. На очаги поражения без явлений везикуляции и мокнутия используют кремы, пасты-мази, содержащие серу, деготь, нафталан, противозудные средства.
В настоящее время существует огромный арсенал кортикостероидных препаратов для наружной терапии АД [9, 10], различных по силе противовоспалительного действия. Среди них выделяют 4 класса препаратов (см. врезку). Несмотря на существующую (кортикофобию), местные кортикостероидные препараты продолжают занимать лидирующее положение в наружной терапии АД. В большинстве случаев их назначают тогда, когда традиционная наружная терапия не оказывает положительного эффекта.
Среди современных кортикостероидных препаратов наружного применения особого внимания заслуживают метилпреднизолона ацепонат и мометазон, обладающие выраженной активностью и высокой степенью безопасности. Данные препараты могут быть использованы у детей раннего возраста. Их применяют однократно в сутки, курс лечения составляет не более 14 дней. На современном этапе терапии АД местные кортикостероидные препараты назначают в острый период заболевания, длительностью 5-7 дней, как правило, 1 или 2 раза в сутки.
После купирования острых проявлений на коже применяют пасты или кремы на основе дегтя или нафталана. В ряде случаев для устранения кожного зуда используют мази или гели, содержащие антигистаминные средства (диметинден).
В период ремиссии заболевания применяют кремы, содержащие полиненасыщенные жирные кислоты, витамины, средства, блокирующие выделение медиаторов аллергии тучными клетками.
В комплексе лечебных мероприятий, направленных на оздоровление детей с АД, важное место принадлежит санаторно-курортному лечению. Для реабилитации детей с атопическим дерматитом показано пребывание как в санаториях местного климата, так и на морских курортах (Анапа, Сочи-Мацеста, Евпатория). У детей с хроническим течением АД, имеющих сопутствующую патологию со стороны органов пищеварения, показана реабилитация в санаториях гастроэнтерологического профиля (Пятигорск, Ессентуки, Минеральные Воды).
Залогом успешной терапии АД у детей является комплексное лечение, направленное на коррекцию различных звеньев этого заболевания, а также обеспечение систематического наблюдения у специалистов.
Литература
2. Dotterund L.K., Kvammen B., Boile R., Falk E.S. A survey of atopic diseases among school chidren in Sos-Varangar community: possible effects of subartic climate and industrial polution from Russia. Acta dermatol. Venerol. Scand. 1994; 74:124-8.
3.Neame R / Prevalence of atopic dermatitis in Leicester: a study of methodology and examination of possible ethnic variation. Br. J. of Dermatology 1995; 132: 772-7.
4. Балаболкин И.И. Современная концепция патогенеза и терапии атопического дерматита у детей. Сб. трудов Современные проблемы аллергологии, клинической иммунологии и иммунофармакологии. М., 1998; 113-9.
5. Олисова О.Ю. Значение иммунного статуса в диагностике атопического дерматита. Тез. докл. 7-го Рос. съезда дерматол. и венерол. Казань. 1996; ч.1: 57.
6. Chan S.C., Brown M.A., Willcox T.M., et al., Abnormal IL-4 gene expresion by atopic dermatitis T-lymphocytes is reflected in altered nuclear protein interactions with Il-4 transcriptional regulatory element, J.Invest. Dermatol. 1996; 106 (5): 1131-6.
7.Боровик Т.Э. Медико-биологические основы диетотерапии при пищевой непереносимости у детей раннего возраста: Автореф. дис. д-ра мед.наук. М. 1994.
8. Современные технологии реабилитации детей с аллергодерматозами (Практ. рук-во для врачей) / Под общ.ред. Л.Ф.Казначеевой. Новосибирск. 1999; 112 с.
10. Шахтмейстер И.Я., Шварц Г.Я. Новые лекарственные препараты в дерматологии. М., 1995; 5-21.
Гипоаллергенная питательная смесь на основе соевого белка:
Гипоаллергенная питательная смесь на основе соевого белка:
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.

Атопический дерматит — это хроническое воспалительное заболевание кожи, которое проявляется зудящими красными пятнами, сыпью, шелушением и сухостью. Это заболевание диагностируется у 30% детей и у 10% взрослых. Однако, зачастую атопическому дерматиту не уделяется должного внимания, и некорректное лечение этой болезни может замедлять наступление ремиссии и ухудшать общий уровень здоровья. О 5 самых распространенных ошибках в тактике лечения рассказывает дерматолог Анна Трушина.
Ошибка №1. Излишняя диагностика, направленная на выявление «некожных» причин.
Причины развития атопического дерматита кроются в генетически обусловленных особенностях:
1. Со стороны кожи — связаны с нарушением барьерной функции.
2. Со стороны иммунной системы. В ответ на проникновение раздражителей и аллергенов через нарушенный кожный барьер формируется воспаление.
Ошибка №2. Поиск причинного аллергена.
Атопический дерматит не является аллергическим заболеванием по своей природе. Однако, аллергические реакции могут сочетаться с атопическим дерматитом, как сопутствующее заболевание. Так происходит примерно у 20-30% пациентов.
Поэтому сам по себе атопический дерматит не является поводом для сдачи дорогостоящих панелей на специфические аллергены, а анализ должен сдаваться только при подозрении на конкретную аллергическую реакцию у части пациентов.
Ошибка №3. Соблюдение необоснованной диеты.
Часто атопический дерматит становится поводом для назначения строгой “гипоаллергенной” диеты. Детский рацион становится однообразным и скучным. Однако, такие пищевые ограничения не обоснованы с научной точки зрения и не приносят желаемого результата, даже если параллельно есть аллергия.
Помимо отсутствия эффекта, строгая диета способна нанести вред организму. Она приводит к дефициту важных нутриентов, минералов и витаминов, что может негативно сказаться на общем состоянии здоровья ребенка. Поэтому детям с атопическим дерматитом нужно питаться разнообразно и сбалансированно. Из рациона исключаются только те продукты, роль которых четко доказана с обострением патологического процесса. Аналогичные правила применимы и к питанию мамы, если малыш находится на грудном вскармливании.
Ошибка №4. Нерациональный уход за кожей.
Основа лечения атопического дерматита это восстановление барьерной функции кожи и устранение воспаления. Поэтому назначаются такие средства, которые помогают УВЛАЖНИТЬ и смягчить кожный покров и удержать влагу внутри него, и тем самым улучшить защитные свойства кожи. В комплексе используются также мероприятия, которые уменьшают вероятность развития воспалительного процесса, т.е. ограничивается контакт кожи с потенциальными агрессорами из внешней среды.
Чтобы реализовать перечисленные выше цели, требуется тщательный и бережный уход за кожей ребенка-атопика с использованием ЭМОЛЕНТОВ. Это специальные средства, лосьоны, кремы, бальзамы, которые при нанесении на кожу смягчают и увлажняют ее, способствуют заполнению межклеточных пространств в коже, восстанавливая ее барьерные свойства.
Важно понимать, что использования простых детских кремов 1-2 раза в день может быть недостаточно. Для правильного ухода требуется нанесение специальных эмолентов в достаточном объеме. Они распределяются толстым (!) слоем как на проблемные, так и на визуально неизмененные участки кожи. При этом, кратность нанесения напрямую зависит от состояния кожи. Требуется использовать эмоленты столько раз в течение дня, чтобы весь день наощупь кожа оставалось гладкой, мягкой и без шелушения.
Ошибка №5. Отказ от «гормонов».
При атопическом дерматите внутри кожи происходит воспалительный процесс (само слово “дерматит” в дословном переводе на русский означает воспаление кожи). Именно поэтому в период обострения используются противовоспалительные наружные средства, которые позволяют остановить воспаление. К таким средствам относят наружные глюкокортикостероиды. Однако многие родители отказываются от этих «гормонов» из-за стероидофобии (боязни использования стероидов).
Топические (т.е. используемые наружно: лосьоны, эмульсии, мази, кремы) кортикостероиды на протяжении не одного десятилетия используются в лечении атопического дерматита. За это время они продемонстрировали высокую эффективность и высокий профиль безопасности.
Если же родители не используют кортикостероиды в тех случаях, когда к этому есть показания, или делают это нерационально (назначают самостоятельно без учета степени и формы кожного воспаления, самостоятельно отменяют гормон раньше необходимого срока без контроля врача), то это может привести к ухудшению состояния кожи, формированию очагов хронического воспаления и другим местным осложнениям.
Заключение
Одной из частых причин кашля в детском возрасте является бронхит. Это воспалительный процесс слизистой оболочки бронхиального дерева, сопровождающийся отеком. Несмотря на кажущуюся простоту и якобы ясность представления об этом заболевании, многое родители все-таки не знают и совершают серьезные ошибки. Сегодня поговорим с детским пульмонологом о бронхите с позиций доказательной медицины.
Причины и механизмы
Термин «Бронхит» всего лишь подчеркивает локализацию патологического процесса (бронхи), но ничего не говорит о природе воспаления. Зачастую оно вызвано вирусами и намного реже бактериями. Причем определить этиологию всего лишь по цвету и характеру мокроты невозможно.
Для бронхита характерно увеличение объем секрета, который вырабатывают бронхи. Отсюда и появляется кашель. Это рефлекторный механизм, направленный на удаление из бронхов мокроты, пылевых частиц, вирусов и других посторонних веществ.
Симптомы бронхита
Типичные симптомы бронхита — кашель с мокротой. Последняя может иметь различный характер — прозрачная, желтая или зеленая.
При бронхите могут также быть и дополнительные проявления:
Обычно симптомы максимально выражены в первые 3-4 дня, затем постепенно стихают. При гладком течении примерно к 7-10-му дню наступает выздоровление. Кстати, остаточный кашель может длиться до 3-4 недель и в большинстве случаев он не требует терапии.
Лечение
Большим заблуждением является назначение антибиотиков при бронхите. Эти препараты показаны только в одном случае, когда доказано, что причиной воспаления стали бактерии.
Базовыми принципами лечения бронхита являются следующие мероприятия:
1. Увлажнение воздуха. Он должен быть также прохладным. Проветривайте комнату — это облегчает дыхание и улучшает откашливание.
2. Обильное питье комнатной температуры или слегка прохладное. Это улучшает отхождение мокроты.
3. Снижение высокой (!) температуры. Для этого могут применяться ибупрофен или парацетамол в соответствии с возрастными дозировками. Ибупрофен и парацетамол рассчитываем по весу ребенка. Нет однозначной цифры когда снижать температуру. Ориентируемся не на цифру на термометре, а на самочувствие ребенка. Но стоит помнить, что увлечение нестероидами может стереть истинную клиническую картину и помешает вовремя диагностировать пневмонию.
4. Выполнение дыхательной гимнастики и проведение вибрационного массажа грудной клетки. Эти упражнения улучшают дренаж бронхов и способствуют выведению из них мокроты. С этой же целью детям с бронхитом разрешается и даже рекомендуется бегать, прыгать, играть и веселиться.
Подводные камни в лечении
Отдельно стоит остановиться на муколитиках — препаратах, разжижающих мокроту. Эти лекарства противопоказаны при бронхите детям до 3 лет. Дело в том, что до этого возраста детские бронхи узкие, а в слизистой оболочке большое количество бокаловидных клеток, вырабатывающих слизь. И при всем этом кашлевой рефлекс до 3 лет минимально развит. Поэтому, применяя муколитики при бронхите до 3 летнего возраста, мы можем усугубить ситуацию — количество жидкой мокроты возрастает, но выводиться из бронхов полноценно она не может.
Отхаркивающие препараты растительного происхождения также требуют отдельного освещения. Эта группа лекарств не имеет достоверных доказательств эффективности. К тому же, существует риск развития аллергической реакции на любой из компонентов фитосборов.
И немного информации про использование небулайзера, он нужен только при обструкции. И нужны только бронхорасширяющие препараты в таком случае, не нужно дышать минералкой, физ.раствором и антибиотиками.
Заключение
Четкое понимание механизмов и причин развития бронхита помогают быстрее избавиться от этого заболевания. Важно, что не все лечится только медикаментами. Основное место в купировании воспаления в бронхах отводится общим мероприятиям, организация которых ложится на плечи родителей. Доказательная медицина на страже здоровья вашего ребенка!
Читайте также:

