Метилпреднизолон мазь при дерматите
Обновлено: 29.04.2024
Представлены результаты клинического мониторирования эффективности и безопасности терапии больных атопическим дерматитом взрослых с использованием различных лекарственных форм метилпреднизолона ацепоната. Показана рациональность дифференцированного назнач
Tactics of topical therapy of patients with atopic dermatitis using various dosage forms of topical glucocorticosteroid N. V. Kungurov, M. M. Kokhan, Yu. V. Keniksfest, E. I. Stukova, N. P. Toropova
The results of clinical monitoring of the effectiveness and safety of therapy in adult patients with atopic dermatitis using various dosage forms of methylprednisolone aceponate are presented. The rationality of differentiated prescription of dosage forms of methylprednisolone aceponate in the localization of skin manifestation in the problem areas, on the skin of the torso and limbs, and according to the clinical manifestations is shown. The safety of the drug methylprednisolone aceponate in the treatment of patients with atopic dermatitis, the absence of side effects in the treatment at the specified time was confirmed.
До настоящего времени широкая распространенность атопического дерматита (АтД) фиксируется в развитых странах, в том числе и в Российской Федерации, а проблема эффективной и безопасной наружной терапии заболевания находится в фокусе внимания практических специалистов дерматовенерологов [1–3]. АтД — это мультифакториальное воспалительное заболевание кожи, возникающее, как правило, в раннем детском возрасте у лиц с наследственной предрасположенностью к атопическим заболеваниям, имеющее хроническое рецидивирующее течение, возрастные особенности локализации и морфологии очагов воспаления, характеризующееся кожным зудом и обусловленное гиперчувствительностью как к аллергенам, так и к неспецифическим раздражителям [3–5].
Актуальные подходы к терапии больных АтД определены в отечественных [4] и зарубежных [5–7] клинических рекомендациях и включают следующие основные направления:
- профилактические стратегии (элиминационные меропрятия);
- гипоаллергенная диета;
- рациональный уход за кожей (умывание и купание, увлажнение);
- топическая, наружная терапия;
- противозудная терапия (топическая и системная);
- иммуносупрессивная терапия (системные глюкокортикостероиды (ГКС), иммунодепрессанты, в том числе генно-инженерные биологические препараты);
- противоинфекционная терапия (антибиотики, антимикотики, противовирусные препараты);
- фототерапия;
- аллерген-специфическая иммунотерапия;
- образовательные программы для детей, членов их семей и для взрослых пациентов.
Крайне важным из указанных направлений ведения больных АтД признается наружная противовоспалительная терапия, «первой линией» которой остаются топические глюкокортикостероидные (ТГКС) препараты, применяемые для купирования воспалительных проявлений АтД у детей и взрослых [4, 5, 8]. Среди современных ТГКС-препаратов последнего поколения присутствует метилпреднизолона ацепонат (МПА) (Адвантан®) — негалогенизированный топический глюкокортикостероид, относящийся к классу сильных ТГКС. Доказана высокая эффективность противовоспалительного действия МПА, особые механизмы которого заключаются в активации пролекарства в очаге воспаления за счет ферментов — эстераз; высокой скорости проникновения в кожу и быстром начале действия, благодаря высокой липофильности и сродству к рецепторам клеток — эффекторов воспаления. Активность МПА в составе Адвантана определяется количеством эстераз, таким образом кожа может сама регулировать необходимое количество МПП в зависисмости от выраженности воспаления. Важным фактором является, что механизм биоактивации, равно как и данные по безопасности и эффективности молекулы были исследованы только для МПА в составе Адвантана. Добавление дополнительных компонентов к молекуле Адвантана не изучалось с точки зрения эффективности препарата. МПА имеет дальнейшее минимизированное проникновение (0,27–2,5%) в кровь и полную быструю инактивацию за счет связывания с глюкуроновой кислотой, благодаря компактности молекулы [9, 10].
Особые фармакологические свойства МПА определяют высокую степень противовоспалительного действия препарата, что сочетается с минимальными нежелательными явлениями. Проведены исследования по сравнительному анализу комплекса клинических и лабораторных данных различных ТГКС: эффективности — по балльной оценке степени вазоконстрикции, сравнительной эффективности ТГКС при АтД; а также степени выраженности нежелательных явлений — по возможному развитию атрофии кожи, влиянию на системный баланс ГКС, аллергическому потенциалу. Соотношение указанных «про» и «контра» факторов исчисляется как «терапевтический индекс» (ТИ, Therapeutic index — TI) ТГКС. Установлено, что МПА имеет один из самых высоких терапевтических индексов (TI 2,0), в сравнении с ТГКС более ранних генераций [11, 12].
В работе, представленной Европейским дерматологическим форумом и посвященной применению топических глюкокортикостероидов у беременных, подтверждаются данные об эффективности и безопасности МПА 0,1%, подчеркивается целесообразность однократного в течение суток применения наружной гормональной терапии [13]. В недавнем обзоре А. Torrelo [14] анализируются данные нескольких клинических исследований МПА 0,1% при АтД, автор обоснованно указывает, что применение МПА 0,1% у младенцев и детей демонстрирует минимальные местные или системные побочные эффекты, даже при частых обострениях процесса и нанесении препарата на обширные участки кожи.
Уникальным для МПА (препарат Адвантан) является факт наличия четырех лекарственных форм препарата, содержащих 0,1% МПА, — эмульсии, крема, мази и жирной мази. В перечисленных лекарственных формах препарата Адвантан введено различное содержание воды: в эмульсии — 67,5%, в креме — 60% («масло в воде»), в мази — 30% («вода в масле»), а жирная мазь практически не содержит воды, при этом снижение содержания воды увеличивает липофильные свойства препарата и способствует скорости проникновения в эпидермис.
Отечественный опыт использования препарата Адвантан в клинической практике значителен и свидетельствует о высокой эффективности данного ТГКС, однако тактические вопросы дифференцированного назначения различных лекарственных форм МПА 0,1%, в зависимости от клинико-морфологических особенностей кожного процесса при АтД остаются до конца неизученными [15–17].
В клинике ГБУ СО «Уральский научно-исследовательский институт дерматовенерологии и иммунопатологии» осуществлена наблюдательная программа контроля эффективности и безопасности МПА 0,1% (эмульсия, крем, мазь, жирная мазь) в терапии больных АтД.
Все пациенты (n = 25) были проинформированы о необходимости соблюдения гипоаллергенного режима и диеты, получали стандартную системную терапию в соответствии с тяжестью кожного процесса, при этом исключалось введение системных глюкокортикостероидных гормонов, иммуносупрессивных средств, других ТГКС. Лечение проводилось в стационарном и амбулаторном режимах.
Определение тяжести процесса до начала и в динамике лечения проводилось с использованием индекса EASI (Eczema area and severity index) [18]. Индекс EASI определялся по общепринятой методике, где врачом проводилась оценка заболевания по основным его проявлениям (Е — эритема; I — инфильтрация; Ех — экскориации; L — лихенификация), то есть фиксировалась интенсивность объективных симптомов АтД отдельно в 4 локализациях: верхние конечности (A), нижние конечности (B), туловище (C), голова/шея (D) с применением балльной оценки выраженности симптомов от 0 до 3 баллов. Проводилась оценка площади поражения кожи (S), которая также оценивалась по балльной системе с применением градаций: 0 — нет высыпаний; 1 балл < 10% площади кожи; 2 балла = 10–29%; 3 балла = 30–49%; 4 балла = 50–69%; 5 баллов = 70–89%; 6 баллов = 90–100% площади кожи.
Общий индекс EASI исчислялся как сумма показателей всех локализаций (табл. 1). Подсчет индекса EASI проводился до начала лечения, в процессе лечения (еженедельно) и через 4 недели после окончания терапии.
Выраженность зуда оценивалась с использованием визуально-аналоговой шкалы (ВАШ зуда) от 0 до 10 баллов, лечащими врачами фиксировалось наличие пиогенных проявлений и возникновение побочных нежелательных явлений, переносимость терапии препаратом Адвантан.
В табл. 2 приведены характеристики наблюдаемых больных с АтД.
Назначение лекарственных форм МПА 0,1% и препаратов для ухода за кожей проводилось лечащими врачами дифференцированно в зависимости от клинико-морфологического характера проявлений и при различных локализациях процесса, при этом учитывались рекомендации, отражающие базовые принципы проведения наружной терапии дерматозов [4, 5].
До начала лечения средний показатель индекса EASI в группе больных АтД составил 16,6 ± 4,8 балла, при этом локальная составляющая индекса EASI, характеризующая тяжесть процесса на нижних конечностях (В), достигала 7,1 ± 2,2 балла, а в области головы/шеи (D) — 1,7 ± 0,6 балла (рис. 2). В процессе проведения терапии общий индекс EASI снижался при пропорциональном уменьшении всех его локальных составляющих: в области верхних и нижних конечностей, туловища, головы и шеи.
К окончанию срока терапии, продолжавшейся от 7 до 28 дней, отмечалось практически полное очищение кожи от высыпаний, общий среднегрупповой индекс EASI (EASI 4) составил менее 1,0 балла. При осмотре через месяц после прекращения лечения полный регресс высыпаний сохранялся у всех пациентов с АтД, а индекс EASI 5 также был менее 1,0 балла.
Анализ динамики регресса симптомов АтД при проведении топической терапии МПА 0,1% (Адвантан), исчисляемый по отношению к исходному показателю EASI, показал, что после первой недели лечения происходило снижение выраженности симптомов заболевания во всех локализациях: в области кожи головы/шеи на 41,2%, конечностей и туловища на 34,3–40,7% от исходного (табл. 3).
Достижение состояния клинической ремиссии с регрессом индекса EASI на 75% и более от исходного наблюдалось между 2-й и 3-й неделей лечения, а при последующих осмотрах (EASI 4) и через 4 недели после окончания терапии (EASI 5) снижение выраженности проявлений АтД достигало 88,2–94,0% от исходного, то есть сохранялось полное очищение кожи во всех локализациях.
До начала терапии выраженность зуда кожи у больных АтД по данным ВАШ зуда фиксировалась от 4 до 10 баллов, в среднем по группе 8,1 ± 1,9 балла. В динамике терапии уже после 1 недели лечения среднегрупповые показатели ВАШ оценки зуда снизились до 2,5 ± 0,7 балла, в последующие недели показатель зуда не превышал 2,0–2,2 балла.
Сопоставление динамики регресса выраженности зуда и индекса EASI (рис. 3) показало, что уменьшение чувства зуда происходило раньше, чем регресс других симптомов и площади поражения кожи, после 2 недели лечения эти показатели не отличались, через 4 недели и после окончания терапии — объективные симптомы регрессировали полностью (на 94% от исходного), а зуд носил минимальный остаточный характер.
Анализ показал, что для терапии проявлений АтД в области головы и шеи более половины специалистов (56%) рекомендовали использование лекарственной формы эмульсии Адвантана, а в 40% — крема (рис. 4). При локализации высыпаний в области кожи туловища врачи назначали практически с одинаковой частотой (40% и 48%) Адвантан в форме крема и мази, эмульсию использовали реже (8%). Терапия высыпаний на коже верхних конечностей проводилась преимущественно кремом и мазью Адвантан (48% и 32%), а у 8% больных АтД врачи использовали лекарственную форму жирной мази. Большинство дерматологов (52%) назначали для терапии высыпаний в области нижних конечностей мазь Адвантан и крем (24%), 16% специалистов проводили терапию АтД в данной локализации жирной мазью Адвантан.
Лечащие врачи отмечали, что с учетом многообразия проявлений АтД у взрослых, когда в одних локализациях преобладали гиперемия, отечность, очаги мокнутия, а в других — инфильтрация различной степени выраженности, лихенификация, фиссуризация, пациентам назначались дифференцированно несколько лекарственных форм препарата Адвантан: например, на кожу лица и шеи — эмульсия, на кожу конечностей — мазь или жирная мазь.
Результаты проведенной работы, клинический опыт позволили разработать алгоритм применения эмульсии, крема, мази и жирной мази Адвантан в зависимости от характера проявлений кожного процесса (острый, хронический), локализации поражений и основных, преобладающих симптомов заболевания (рис. 5).
В процессе терапии и в течение 4 недель после ее окончания больным АтД проводился уход за кожей с использованием эмолентов, что обеспечивало восстановление липидного состава эпидермиса, комплексное увлажнение кожи.
В процессе проведения наружного лечения препаратом МПА 0,1% (Адвантан) лечащими врачами фиксировалось возникновение нежелательных явлений и побочных эффектов терапии: усиление зуда, гиперемии на начальном этапе терапии у 2 больных, появление пиогенных, вирусных осложнений у 2 пациентов. Явлений атрофии кожи, гипертрихоза, сосудистых нарушений зафиксировано не было.
Заключение
Анализ фактических данных, полученных в ходе наблюдательной программы, свидетельствует о высокой клинической эффективности препарата МПА 0,1% (Адвантан) в терапии больных АтД, характеризовавшейся достижением клинической ремиссии у больных АтД после 3 недель лечения с регрессом индекса EASI на 88,6% от исходного уровня. Практически полное очищение кожи, минимальная выраженность зуда или его отсутствие сохранялись у всех больных в течение 4 недель после окончания лечения. Значимым, определяющим дополнительную результативность лечения, является дифференцированный подход к назначению различных лекарственных форм МПА 0,1% (Адвантан), когда эмульсия и крем применяются при локализации высыпаний в проблемных зонах в условиях преобладания симптомов гиперемии, отечности; мазь — в терапии высыпаний на коже туловища и конечностей при наличии очагов воспалительной инфильтрации, жирная мазь — в случае формирования стойких поражений кожи в области нижних конечностей, присутствия плотной инфильтрации, лихенификации, гиперкератоза. Клинические наблюдения показали, что редукция чувства зуда при топическом лечении МПА 0,1% (Адвантан) предшествует регрессу объективных симптомов в первые недели терапии.
Подтверждена безопасность использования препарата МПА 0,1% (Адвантан) в терапии больных АтД, отсутствие формирования побочных эффектов при лечении в указанные сроки. Представляется обоснованным широкое использование препарата МПА 0,1% (Адвантан) для топического применения у больных АтД, при этом достаточные сроки наружного лечения, обоснованное дифференцированное назначение эмульсии, крема, мази и жирной мази, а также адекватный уход за кожей обеспечивают высокую клиническую результативность терапии и сохранение ремиссии.
Литература
- Bieber T. Atopic Dermatitis // Ann. Dermatol. 2010; 22 (2): 125–137.
- Darsow U., Wollenberg A., Simon D., Ta?¨eb A., Werfel T., Oranje A. Gelmetti C., Svensson A., Deleuran M., Calza M., Giusti F., Ring J. ETFAD⁄EADV eczema task force 2009 position paper on diagnosis and treatment of atopic dermatitis // JEADV. 2010; 24: 317–328.
- Голдсмит Л. А., Кац С. И., Джилкрест Б. А. и др. Дерматология Фицпатрика в клинической практике / Пер. с англ. под общ. ред. Потекаева Н. Н., Львова А. Н. Изд. 2-е. Издательство Панфилова, 2015. Т. 1, с. 182–200.
- Федеральные клинические рекомендации. Дерматовенерология 2015: Болезни кожи. Инфекции, передаваемые половым путем. 5-е изд., перераб. и доп. М.: Деловой экспресс, 2016. 768 с.
- Wollenberg A., Barbarot S., Bieber T., Christen-Zaech S., Deleuran M. et al. GUIDELINES Consensus-based European guidelines for treatment of atopic eczema (atopic dermatitis) in adults and children: part I // JEADV. 2018, 32: 657–682.
- Calzavara Pinton P., Cristaudo A., Foti C., Canonica G. W., Balato N. et al. Diagnosis and management of moderate to severe adult atopic dermatitis: a Consensus by the italian Society of dermatology and Venereology (SidemaSt), the Italian association of Hospital dermatologists, the Italian Society of allergy, asthma and Clinical immunology (SiaaiC), and the italian Society of allergological, environmental and occupational dermatology (SidaPa) // Giornale italiano di dermatologia e Venereologia. 2018; 153 (2): 133–145.
- Ilgen Ertam, Özlem Su, Sibel Alper, Hayriye Saricaoglu, Ayse Serap Karadag et al. The Turkish guideline for the diagnosis and management of atopic dermatitis — 2018 // Turkderm-Turk Arch Dermatol Venereology. 2018; 52: 6–23.
- Кунгуров Н. В., Кохан М. М., Кениксфест Ю. В., Гришаева Е. В., Кащеева Я. В., Куклин И. А. Оптимизация наружной терапии стероидчувствительных дерматозов // Вестн. дерматол. и венерол. 2007; 4: 45–51.
- Haria M., Balfour J. A. Methylprednisolone aceponate. A review of its pharmacological properties and therapeutic potential in the topical treatment of eczema // Clin Immunother. 1995; 3: 241–253.
- Brazzini B., Pimpinelli N. New and established topical corticosteroids in dermatology: clinical pharmacology and therapeutic use // Am J. Clin. Dermatol. 2002; 3: 47–58.
- Luger T., Loske K., Elsner P. et al. Topical skin therapy with glucocorticosteroids — therapeutic index // J Deutsch Dermatol Ges. 2004; 7: 629–634.
- Luger T. A. Balancing efficacy and safety in the management of atopic dermatitis: the role of methylprednisolone aceponate // JEADV. 2011; 25: 251–258.
- Chi C. C., Kirtschig G., Aberer, Gabbud J.-P., Lipozencic J., Karp S. et al. Updated evidence-based (S2e) European Dermatology Forum guideline on topical corticosteroids in pregnancy // JEADV. 2017; 31: 761–773.
- Torrelo A. Methylprednisolone aceponate for atopic dermatitis // Int J Dermatol. 2017; 56 (6): 691–697.
- Кохан М. М., Кениксфест Ю. В., Новиков Г. М. Эффективность сочетанного применения наружных средств терапии и увлажнения кожи у больных атопическим дерматитом // Вестн. дерматологии и венерологии. 2007; 4: 55–60.
- Волкова Е. Н., Ланге Д. А., Родина Ю. А., Тарасова М. В. Метилпреднизолона ацепонат в комплексной терапии хронических дерматозов: анализ тактических ошибок применения // Клиническая дерматология и венерология. 2010; 5: 97–102.
- Дворянкова Е. В., Корсунская И. М., Сакания Л. Р., Невозинская З. А. К вопросу о рациональном выборе топической терапии при атопическом дерматите // Consilium medicum. Дерматология, 2015; 1: 70–74.
- Hanifin J. M., Thurston M., Omoto M., Cherill R., Tofte S. J., Graeber M. The eczema area and severity index (EASI): assessment of reliability in atopic dermatitis // EASI Evaluator Group. Exp Dermatol. 2001; 10 (1): 11–18.
Н. В. Кунгуров, доктор медицинских наук, профессор
М. М. Кохан 1 , доктор медицинских наук, профессор
Ю. В. Кениксфест, доктор медицинских наук
Е. И. Стукова
Н. П. Торопова, доктор медицинских наук, профессор
ГБУ СО УрНИИДВиИ, Екатеринбург
На основании собственных и литературных данных проведен анализ эффективности и безопасности применения нового топического глюкокортикостероидного препарата - Элоком (мометазона фуроат 0,1%-ный) для лечения различных нозологических форм аллергических болезней кожи (аллергодерматозов)у детей. При использовании Элокома у всех обследованных нами больных с аллергодерматозами не было выявлено ни местных, ни системных побочных эффектов.
Полученные данные свидетельствуют, что крем Элоком дает наилучший эффект при наличии экссудации, мокнутия и больших эрозивных поверхностей на коже. Мазь Элоком более эффективна при аллергодерматозах с выраженной лихенизацией, шелушением и зудом кожи.
Аллергодерматозы - наиболее ранняя и частая клиническая форма проявлений аллергии у детей. Частота аллергических поражений кожи в структуре детских болезней неуклонно увеличивается. Особенно тревожным является значительный рост аллергических болезней кожи с хроническим и рецидивирующим течением, торпидных к традиционной терапии. В настоящее время аллергодерматозы рассматриваются как аллергическое воспаление кожи, обусловленное наследственной предрасположенностью к аллергии и IgE-зависимым механизмом формирования. Процесс характеризуется клиническим полиморфизмом и склонностью к хроническому или рецидивирующему течению. В соответствии с предложенной рабочей классификацией аллергических болезней кожи у детей наиболее часто встречаются атопический дерматит (72%), острая крапивница (15%), хроническая рецидивирующая крапивница (5%), отек Квинке (2,3%), строфулюс (1,8%). В последние годы увеличилась частота токсидермии, многоформной экссудативной эритемы, синдромов Стивенса-Джонсона и Лайелла, которые являются наиболее тяжелыми формами аллергодерматозов [1].
Ведущими факторами риска развития аллергодерматозов у детей являются наследственная предрасположенность к аллергии, внутриутробная сенсибилизация плода к различным аллергенам, раннее искусственное вскармливание, патология желудочно-кишечного тракта, частые эпизоды острых респираторных вирусных инфекций и очаги хронической инфекции, а также нарушение функций центральной и вегетативной нервной системы.
Важным звеном комплексного лечения аллергодерматозов у детей является местная терапия, которая обязательно проводится с учетом стадии болезни, фазы воспаления и степени выраженности кожных проявлений. Причем рациональное использование наружной терапии значительно влияет на разрешение воспалительного процесса в коже. В раннем возрасте, особенно у грудных детей, вследствие высокой проницаемости кожных покровов традиционная наружная терапия начинается с применения индифферентных паст, мазей, болтушек, содержащих противовоспалительные, кератолитические и кератопластические средства. При отсутствии эффекта данной терапии, а также при тяжелых формах аллергодерматозов возникает необходимость применения топических глюкокортикостероидов (ГКС) [2].
Топические ГКС при атопических болезнях кожи применяются уже более 40 лет. Первым топическим ГКС был ацетат гидрокор-тизона. Различные модификации этого гормона привели к разработке эффективных синтетических ГКС с более высокой активностью.
Механизм действия топических ГКС определяется их многообразным влиянием на процессы воспаления в коже [3]. Наиболее важными эффектами ГКС являются:
- увеличение связывания гистамина и серотонина в коже и уменьшение чувствительности нервных окончаний к нейропептидам и гистамину;
- угнетение синтеза интерлейкинов-4,5,13, гамма-интерферона и других цитокинов;
- уменьшение активности фосфолипазы А2 и продукции эйкозанодзов, а также снижение экспрессии молекул клеточной адгезии и чувствительности эндотелия к медиаторам аллергии;
- торможение миграции эозинофилов и пролиферации Т-лимфоцитов; снижение сосудистой проницаемости и нарушений микроциркуляции.
Длительное применение топических ГКС в виде аппликаций (особенно под окклюзионными повязками) может приводить к подавлению глюкокортикоидной функции коры надпочечников. К местным побочным эффектам относятся, прежде всего, развитие атрофии кожи вследствие подавления синтеза коллагена и задержки пролиферации фибробластов, а также формирование телеангиэктазий, гипер- и гипопигментации кожи, гипертрихоза, присоединение микробной и кандидозной инфекции [4]. В соответствии с Европейской классификацией активности местных ГКС по силе действия различают четыре класса препаратов: слабые, средние, сильные, очень сильные. Выделяют также ГКС, содержащие в структуре галогены (преимущественно фтор и хлор). Такие ГКС, как Синалар, Синофлан, Фторокорт, Флуцинар, Лоринден, Целестодерм, содержат фтор. Обладая мощным локальным действием и длительно задерживаясь в коже, эти ГКС дают большое число местных побочных эффектов, вплоть до атрофии кожи, особенно при длительном применении. Наличие хлора и боковой цепи фуроата в структуре мометазона способствует увеличению противовоспалительной активности и сохранению высокой безопасности этого препарата. Негалогенизированными ГКС являются Локоид, Дерматоп, Адвантан. Среди преимуществ этих ГКС выделяют высокую липофильность, быстрое проникновение через эпидермис и хорошее местное действие. Однако эти же свойства ГКС определяют их выраженные системные побочные эффекты при аппликации на большую поверхность кожи и особенно при применении более 4 недель [4].
При использовании местных ГКС необходимо учитывать циркадные ритмы активации коры надпочечников у детей, так как при сохранении нормальной чувствительности к ГКС именно в утренние часы отмечено наименьшее подавление функции системы гипофиз - надпочечники [5].
Принципы назначения топических ГКС при аллергических болезнях кожи. У детей до 6 мес. средством выбора является гидрокортизона ацетат 1%-ный, который следует применять 1 раз в день не более 4 дней подряд; у детей старше 6 мес., когда уровень кортизола в крови становится максимальным в утренние часы, можно использовать другие топические ГКС. При этом необходимо выбирать наиболее изученные и безопасные препараты ГКС. Для предупреждения нарушения функции коры надпочечников следует применять такие ГКС в утренние часы, 1 раз в сутки, короткими курсами не более 10-14 дней на поверхности кожи, не превышающей 20% общей площади кожных покровов. Не рекомендуется использовать окклюзионные повязки, особенно у маленьких детей, имеющих относительно низкое соотношение поверхности тела к его массе [2,5].
Идеальный топический ГКС-препарат должен обладать сильным противовоспалительным действием, низкой системной биодоступностью, быстрым началом действия и минимальными местными побочными эффектами. Этим требованиям в полной мере соответствует хорошо изученный в клинических условиях и использованный нами при лечении аллергодерматозов препарат Элоком.
Элоком (Elocom) - 0,1%-ный мометазона фуроат (mometasone furoate 0,1%) (Schering-Plough, США) - является новой своеобразной молекулярной структурой, базовым основанием которой служит метилпреднизолон, содержащий хлор в 9-й и 21-й позиции и боковую цепь сложного эфира двойной фуранилкарбоновой кислоты (фуроата) в 17-й позиции. Именно эта боковая цепочка фуроата в структуре Элокома определяет его уникальные свойства, значительно отличающие его от прочих ГКС [6, 7]. По сравнению с другими топическими ГКС аналогичной группы Элоком обладает высокой местной активностью, что позволяет отнести его к 3-му классу по силе действия, имеет низкий системный эффект и уровень безопасности, аналогичный слабым ГКС, таким как 1%-ный крем гидрокортизона. Элоком отличает особенно высокая переносимость: по данным клинических исследований, использование препарата у 22831 больного не выявило побочных эффектов, при этом клинически и гистологически не было зафиксировано ни одного случая атрофии кожи даже при длительном нанесении его на участки, более других подверженные атрофии (кожа лица, уши, подмышечные впадины) [4, 8]. В специальных испытаниях было установлено, что npи нанесении препарата под окклюзионную повязку в течение 8 ч только 0,7% препарата абсорбируется в системный кровоток, что указывает на отсутствие влияния Элокома на гормональную систему гипофиз - надпочечники [9].
Уникальное фармацевтическое преимущество Элокома - наличие трех лекарственных форм: крем, мазь, лосьон.
Крем Элоком "масло в воде" - единственная приемлемая форма для лечения атопического дерматита, сопровождающегося экссудацией и мокнутием, у детей до двух лет. 0,1%-ный крем Элоком может успешно применяться также при тяжелых формах аллергодерматозов (особенно при синдромах Стивенса-Джонсона и Лайелла) с обширными эрозивными поражениями кожи. Крем Элоком не проникает глубоко в кожу и удерживается в эпидермисе, что существенно снижает его всасывание и наличие системных эффектов.
Мы использовали 0,1%-ный крем Элоком у 96 детей в возрасте от 6 мес. до 12 лет для местной терапии аллергодерматозов (атонический дерматит - 52 ребенка, многоформная экссудативная эритема - 3 и синдром Стивенса-Джонсона - 1 ребенок). При этом к концу вторых суток было отмечено уменьшение экссудации и гиперемии, на четвертые сутки значительно уменьшался зуд кожи, а к концу седьмых - десятых суток ликвидировались воспалительные явления на коже при отсутствии нежелательных побочных эффектов. Анализ содержания 17-оксикортикостерои-дов (17-ОКС) в моче у этих больных не выявил существенных нарушений выделения этих соединений. В целом использование крема Элоком ускорило наступление ремиссии заболевания в 87% наблюдений и имело выраженное благоприятное психо-эмоциональное воздействие, особенно у детей старшего возраста.
Лосьон Элоком мы использовали с хорошим терапевтическим эффектом для лечения себорейных корочек (гнейс) волосистой части головы при атопическом дерматите. При этом к четвертому-пятому дню было отмечено значительное уменьшение образования корочек.
Мазь Элоком применена нами при лечении 40 детей в возрасте от 2 до 12 лет с атоническим дерматитом с синдромом лихени-зации и выраженным зудом. При этом на четвертые сутки было отмечено значительное уменьшение зуда и сухости кожи, а к десятым суткам - купирование воспалительного процесса в 76% наблюдений.
Применение препарата Элоком при различных формах аллергического поражения кожи давало выраженный положительный эффект к седьмому-десятому дню, что свидетельствует об отсутствии необходимости его длительного применения и особенно важно у детей. При использовании Элокома у всех обследованных нами больных с аллергодерматозами не было выявлено ни местных, ни системных побочных эффектов.
Полученные нами данные свидетельствуют о том, что крем Элоком дает наилучший эффект при наличии экссудации, мокнутия и больших эрозивных поверхностей на коже. Мазь Элоком более эффективна при аллергодерматозах с выраженной лихенизацией, шелушением и зудом кожи.
Таким образом, Элоком - высокоэффективный, безопасный топический ГКС последнего поколения и по фармакологическим свойствам приближается к идеальному препарату выбора для местного лечения аллергодерматозов у детей.
Литература
Разнородную группу хронически протекающих дерматозов отличают клинический полиморфизм, нередко тяжелое течение и как следствие — постоянный поиск оптимальных подходов к терапии. Проблема лечения и реабилитации таких больных в настоящее время приобретает особую научно-практическую и социальную значимость в связи с увеличением их числа, социальной дезадаптацией, резистентностью отдельных клинических форм к терапии [1, 2].
Мультифакторная концепция патогенеза и выявленные нарушения при исследовании различных органов обосновывают необходимость применения в терапии больных широкого спектра лечебных мероприятий, некоторые из них стали называться традиционными: гипоаллергенная диета, назначение антигистаминных, седативных средств, дезинтоксикационная терапия. Одно из ведущих мест занимает наружная терапия, которая должна отвечать следующим требованиям: устранять или уменьшать зуд, купировать воспалительные реакции, стимулировать репаративные процессы в коже, предупреждать и устранять вторичное инфицирование, увлажнять и смягчать кожу, восстанавливать ее защитные свойства [2—5].
Алгоритм наружной терапии достаточно традиционен и включает следующие положения:
- наружное лечение проводят с учетом возраста, клинической формы, стадии болезни, распространенности и тяжести процесса, эффективности и переносимости предшествующих методов лечения, сопутствующей патологии;
- в зависимости от стадии и клинической картины болезни средства наружной терапии используют в виде различных лекарственных форм: растворов, лосьонов, паст, кремов, мазей и т.д.
Выраженность воспалительной реакции кожи, сильный зуд, неэффективность предшествующего лечения препаратами, не содержащими кортикостероиды (КС), служат показанием к их наружному применению.
До настоящего времени нет лекарственных средств, которые могли бы стать полной альтернативой этой группе противовоспалительных препаратов.
Современные требования к топическим ГКС достаточно высокие [1, 6, 7]. Местный ГКС должен относиться к классу сильнодействующих (быстрый противовоспалительный эффект, предупреждение осложнений); обладать высокой эффективностью, причем эффективность и сила его действия должны быть доказаны в исследованиях, отвечающих стандартам доказательной медицины (многоцентровые рандомизированные клинические исследования соответствующие стандартам GCP, включающие большое количество пациентов); иметь разнообразные лекарственные формы для местного применения, необходимые для достижения эффекта на разных стадиях воспалительного процесса и на любом участке кожи; быть безопасным (низкая всасываемость, минимум побочных эффектов, использование в любом возрасте, возможность длительного многократного применения); быть удобным в применении (нанесение 1 раз в сутки, не иметь запаха, жирного блеска, не пачкать одежду).
Выбор конкретного препарата всегда определяется терапевтическим индексом: соотношением — эффективность/безопасность («польза/риск») [5, 8].
Современные подходы к выбору местного ГКС при лечении хронически протекающих дерматозов диктуют приоритет использования негалогенизированных (без фтора и хлора) топических стероидов из класса сильнодействующих [1, 3, 6, 9]. Таким высоким требованиям отвечает адвантан (метилпреднизолона ацепонат).
Несмотря на достаточную информированность об особенностях применения адвантана, дерматовенерологи допускают ряд тактических ошибок, анализ которых мы приводим.
Ошибка 1: адвантан — слабый препарат, поэтому его можно применять в детской практике («детский препарат») и на лице.
Основанием для этой распространенной ошибки являются широкое использование препарата при лечении детей, а также представления, к сожалению, не всегда правильные о «силе» ГКС. В случае с адвантаном существует подмена понятий: не содержит галогенов (фтора, хлора) — не значит слабый.
Правильно: необходимо помнить, что адвантан — препарат для детей и взрослых. Действительно, препарат нашел широкое применение в детской практике. Показания к его назначению с 4-месячного возраста — не ограничение применения возрастной группой, а свидетельство его безопасности. При этом нет оснований не назначать его взрослым [7, 10].
Адвантан — препарат уникальный: это негалогенизированный топический стероид со своеобразной химической структурой (рис. 1).
Рис. 1. Химическая структура метилпреднизолона ацепоната.
Введение метильной группы в положение С6 обусловливает высокую активность адвантана. Отсутствие фтора и хлора в положениях С6, С9 или С12, типичных для большинства сильных КС, дает возможность свести к минимуму местные и системные побочные эффекты. Двойная эстерификация (в положениях С17 и С21) обеспечивает оптимальную липофильность молекулы, быстрое проникновение через эпидермис и высокую концентрацию в дерме [10—12].
Клиническая эффективность адвантана убедительно продемонстрирована во многих клинических исследованиях с участием более 15 000 взрослых и детей. Это позволяет признать значительный клинический опыт применения данного препарата и возможность объективной оценки его эффективности [10, 13, 14].
Следует обратить внимание и на то, что под брендом «адвантан» часто понимают метилпреднизолон. Такое недопонимание и несоответствие возникло вследствие использования рядом исследователей и лекторов американской классификации ГКС по силе действия. Однако в ней нет адвантана, который является метилпреднизолона ацепонатом (МПА), а есть метилпреднизолон, действительно «слабый».
Ошибка 2: стремление рекомендовать нанесение адвантана на кожу в области типичных высыпаний в отсутствие воспаления для профилактики обострения хронических дерматозов (в период ремиссии).
Правильно использовать его только в период обострения и подострого течения, потому что это препарат с «умной» фармакокинетикой: метилпреднизолона пропионат (МПП) — пролекарство — активен только в очаге поражения без влияния на здоровую кожу. Такая избирательная биоактивация МПА определяет создание его стабильной концентрации, которая поддерживается в течение суток, и высокой активности [8, 10, 11].
Ошибка 3: представление о том, что увеличение кратности применения адвантана повысит его фармакологическую активность и эффективность.
Правильно: необходимо помнить, что за счет оптимальной липофильности концентрация адвантана поддерживается в воспалительном очаге в течение 24 ч — создается депо препарата. Нет необходимости двукратного использования адвантана — не повышает его эффективность!
Ошибка 4: представление о том, что применение «методики разведения» — смешивание с питательными или увлажняющими средствами снизит риск возникновения побочных реакций и уменьшит количество использованного препарата.
Правильно: следует знать, что «разведение» адвантана приведет к изменению его фармакокинетических свойств (липофильности, биодоступности), снижению терапевтической эффективности, необходимости увеличения длительности терапии — повышается риск развития побочных эффектов.
Ошибка 5: феномен «стероидофобии» как у врачей, так и у пациентов при лечении адвантаном.
Правильно: не забывать, что при его создании удалось фармакологически разделить высокую активность и побочные эффекты. Это стало возможно благодаря особой кинетике адвантана: оптимальная липофильность + биоактивация в дерме. В результате не требуется введения галогена для достижения высокой активности — это определяет высокую безопасность. Адвантан — сильный и при этом безопасный местный стероид (рис. 2) [8, 11, 12].
Рис. 2. Доказанная высокая безопасность адвантана.
Здоровые добровольцы. Стероиды в дозе 40 г/сут под окклюзионную повязку.
Очень важно помнить, что безопасность определяется не только и не столько проникновением ГКС в кровоток. Гораздо важнее быстрая и полная инактивация в крови его или метаболитов. В случае с адвантаном, попадая в кровоток, МПА трансформируется в активный метаболит — 17-метилпреднизолона пропионат (17-МПП), который быстро связывается с глюкуроновой кислотой и инактивируется. Отсутствие в крови препарата в активной форме определяет минимальное всасывание его из кожи в кровь и как следствие — минимум побочных эффектов. МПА и его метаболиты не кумулируются в организме [7, 10, 12].
Безопасность связана и с возрастными ограничениями. Считается обязательным наличие доказательной базы, четких указаний в инструкции соответствующих возрастных рамок (для адвантана — с 4 мес) возможного использования препарата. Для лекарственных средств, применяемых в дерматологии в течение многих десятков лет, так называемых старых препаратов доказательной базы, возможно, нет или эти факты малоизвестны. Вызывает удивление и недоумение отсутствие в инструкции указаний на «разрешенный возраст» начала применения новых распространенных ГКС. Применение «по умолчанию» — это тупиковый, бесперспективный и безграмотный путь. Возрастные показания к назначению адвантана, четко обозначенные в инструкции, также свидетельствуют в пользу его безопасности.
Ошибка 6: желание скорректировать лечение адвантаном с учетом возможности вторичного инфицирования (бактериальной и/или грибковой инфекциями) путем добавления антибиотиков (порой, «на глазок»).
Правильно: купирование инфицирования до начала лечения адвантаном.
Следует предостеречь врачей разных специальностей — «любителей» назначать без весомых на то показаний комбинированных препаратов для наружного применения, традиционно содержащие ГКС, антибиотик и антимикотик. Нерациональное применение этих лекарственных средств не будет профилактикой осложнений, не улучшит прогноз заболевания.
Кроме того, в литературе отмечен малоизвестный врачам факт: одним из продуктов метаболизма МПА является уксусная кислота, оказывающая антисептическое действие.
Ошибка 7: предпочтительное назначение одной (часто индивидуально выбранной врачом) лекарственной формы независимо от клинико-морфологических проявлений.
Правильно: осуществлять поэтапное применение, правильный выбор лекарственной формы в зависимости от стадии и проявлений патологического процесса (рис. 3).
Рис. 3. Разнообразие лекарственных форм адвантана.
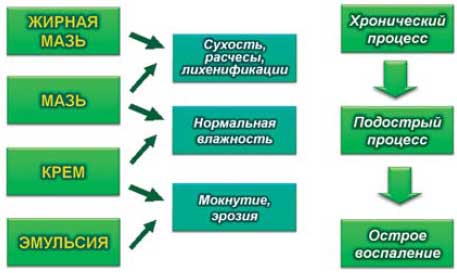
Каждая лекарственная форма адвантана обладает своими неповторимыми свойствами.
Следует указать на пристрастие некоторых дерматологов постоянно назначать пасты, «болтушки», которые имеют сложный состав и готовятся в аптеке. Да, нас так учили и мы так привыкли. Однако объективные условия изменились: производственных аптек мало (1—2 в округе), многие больные неправильно применяют выписанные лекарственные формы (особенно примочки, влажно-высыхающие повязки), что усугубляет течение патологического процесса на коже.
Кроме того, нам иногда кажется, что стоимость таких лекарственных средств будет меньше, чем готовых препаратов. Однако, как показал опрос пациентов, это не так. В настоящее время есть выбор: можно применять различные формы готовых препаратов — у адвантана их 5. При его назначении необходимо давать четкие указания, на применении какой формы настаивает дерматолог, предупреждая пациента о возможности этапной смены различных форм. В случае с адвантаном вместо примочек можно использовать эмульсию, вместо окклюзионной повязки — жирную мазь.
Ошибка 8: представление об экономической целесообразности назначения адвантана — «дорогой» препарат.
Правильно: необходимо помнить, что за счет высокой липофильности адвантан создает депо в эпидермисе: это позволяет использовать его 1 раз в сутки.
Кроме удобства, однократное применение позволяет избежать излишних трат на приобретение избыточного количества упаковок адвантана, особенно в сравнении с препаратами с 2—3-кратным применением.
Хотелось бы обратить внимание и на то, что в нашей стране распространена привычка «встречать по одежке». Эта традиция мало применима к медицинской практике: не следует по внешнему виду судить о финансовых возможностях пациента по приобретению того или иного препарата.
Кроме того, понятие «дорогой—дешевый» — для каждого свое. Для большинства пациентов, определяющим является эффект от применения лекарственного средства.
Таким образом, знание особенностей строения, фармакокинетики адвантана, сведения о многообразии его лекарственных форм позволит дерматовенерологам избежать тактических ошибок при его применении.
Все уникальные свойства адвантана дали нам основание применить его различные лекарственные формы у 65 больных в возрасте от 17 до 46 лет с хроническими дерматозами: атопическим дерматитом (n=18), экземой (n=35), хронической крапивницей (n=12).
Препарат наносили 1 раз в сутки в зависимости от степени тяжести заболевания в течение 7—21 дня. Системная и местная терапия другими ГКС не проводилась. Все больные получали традиционную общую терапию (ангиотропные, антигистаминные препараты, витамины).
В процессе использования адвантана у пациентов оценивали динамику основных клинических симптомов заболевания — эритема, отек, папулы/ лихенификация и субъективных жалоб (зуд, жжение).
Эффективность терапии оценивали традиционно (клиническая ремиссия, значительное улучшение, улучшение, без изменений, ухудшение).
Результаты оценки клинической эффективности использования адвантана у пациентов с хроническими воспалительными дерматозами представлены в таблице.
Результаты лечения препаратом адвантан больных с хроническими дерматозами (n=65)
| Результат лечения | Атопический дерматит (n=18) | Хроническая крапивница (n=12) | Идиопатическая экзема (n=35) |
| Клиническая ремиссия | 6 | 2 | 12 |
| Значительное улучшение | 9 | 8 | 18 |
| Улучшение | 3 | 2 | 5 |
| Без изменений | - | - | - |
| Ухудшение | - | - | - |
| Итого: | 18 | 12 | 35 |
Обобщая результаты применения различных лекарственных форм адвантана в терапии больных с хроническими воспалительными заболеваниями кожи, мы констатировали клиническую ремиссию в 30,8% (n=20) случаев, значительное улучшение — в 53,8% (n=35), улучшение — в 15,4% (n=10). Отсутствие эффекта или ухудшение кожного процесса не наблюдали.
Таким образом, адвантан максимально полно отвечает современным требованиям к топическому ГКС в лечении хронически протекающих дерматозов. Адвантан — топический кортикостероид:
- эффективный топический ГКС из класса сильнодействующих;
- с широким выбором лекарственных форм — эмульсия, крем, мазь, жирная мазь;
- безопасный — отсутствие галогенов, хлора и фтора, биоактивация только в очаге воспаления, минимальная системная абсорбция, быстрая и полная инактивация;
- удобный в применении — 1 раз в сутки, хорошие косметические свойства.
ЛИТЕРАТУРА
1. Белоусова Т.А., Лукашова Н.Н. Дифференцированный подход к выбору наружных глюкокортикостероидов в терапии дерматозов. Клин дерматол и венерол 2006;3:74—78.
2. Кохан М.М. Эффективность сочетанного применения наружных средств терапии и увлажнения кожи у больных атопическим дерматитом. Вестн дерматол и венерол 2007;4:55—60.
3. Машкиллейсон А.Л., Гомберг М.А., Борисенко К.К. Опыт применения «Адвантана» у больных дерматозами. Вестн дерматол и венерол 1997;6:35—41.
4. Fritsch P. Clinical experience with methylprednisolone aceponate in eczema. J. Dermatol Treat 1992;3:Suppl 2:17—19.
5. Кочергин Н.Г., Белоусова Т.А. К вопросу о местной кортикостероидной терапии. Рос журн кож и вен бол 2001;2:28— 31.
6. Luger T.A. Topische Dermatotherapie mit Glukokortikoiden — Thera-peutischer index. Leitlinie der Deutschen Dermatologischen Gesell-schaft 2004;7:629—634.
7. Luger T.A. Topische Dermatotherapie mit Glukokortikoiden — Therapeutischer index. Leitlinie der Deutschen Dermatologischen Gesellschaft 2004;7:629—634.
8. Mori M., Pimpinelli N., Gianotti B. Topical corticosteroids and unwanted local effects: improving the benefit/risk ratio. Drug Safety 1994;10:5:406—412.
9. Хамаганова И.В. «Адвантан» в лечении контактных аллергических дерматозов, обусловленных применением средств декоративной косметики. Вестн дерматол и венерол 2005;5:58—59.
10. Топические стероиды. «Адвантан». Информация о препарате. М 2001.
11. Meffert H., Schuppler J. Methylprednisolone aceponate lotion for treatment of acute eczema. Zeitschrift fur Hautkrankheiten 1999;74:88—94.
12. Zaumseil R.P., Fuhrman H. et al. Methylprednisolone aceponate (Ad-vantan) — an effective topical corticoid therapy with few side effects. Jabrbuch der Dermatologie 1992;3:247—263.
13. Ruzicka T. Methylprednisolone aceponate in eczema and other inflammatory skin disorders — a clinical update. Int J Clin Pract 2006;60:1:85—92.
14. Mensing H., Lorenz B. Experience with methylprednisolone aceponate in patients suffering from acute and chronic eczema. Results of a large observational study. Z Hautkr 1998;73:281—285.
Форма выпуска, упаковка и состав препарата Комфодерм ®
Мазь для наружного применения от белого до белого с сероватым или желтоватым оттенком цвета, однородная, полупрозрачная; допускается наличие характерного запаха.
| 100 г | |
| метилпреднизолона ацепонат | 0.1 г |
Вспомогательные вещества: вазелин - 44.7 г, парафин жидкий - 34.1 г, масло семян клещевины обыкновенной - 3.2 г, воск пчелиный белый - 17.9 г.
15 г - тубы алюминиевые (1) - пачки картонные.
30 г - тубы алюминиевые (1) - пачки картонные.
Фармакологическое действие
Активный компонент препарата Комфодерм ® - метилпреднизолона ацепонат - представляет собой негалогенизированный стероид.
При наружном применении метилпреднизолона ацепонат подавляет воспалительные и аллергические кожные реакции, также как и реакции, связанные с усиленной пролиферацией, что приводит к уменьшению объективных симптомов воспаления (эритема, отек, мокнутие и т.д.) и субъективных ощущений (зуд, раздражение, боль и т.д.).
При применении метилпреднизолона ацепоната наружно в рекомендуемой дозе системное действие минимально как у человека, так и у животных. После многократного нанесения препарата на большие поверхности (40-60% поверхности кожи), а также применении под окклюзионную повязку не отмечается нарушений функций надпочечников: концентрация кортизола в плазме и его циркадный ритм остаются в пределах нормы, снижения содержания кортизола в суточной моче не происходит.
Метилпреднизолона ацепонат (особенно, его основной метаболит - 6α-метилпреднизолон-17-пропионат) связывается с внутриклеточными глюкокортикоидными рецепторами. Стероид-рецепторный комплекс связывается с определенными участками ДНК клеток иммунного ответа, таким образом, вызывая серию биологических эффектов. В частности, связывание стероид-рецепторного комплекса с ДНК клетками иммунного ответа приводит к индукции синтеза макрокортина. Макрокортин ингибирует высвобождение арахидоновой кислоты и, тем самым, образование медиаторов воспаления типа простагландинов и лейкотриенов.
Ингибирование глюкокортикоидами синтеза вазодилатирующих простагландинов и потенцирование сосудосуживающего действия адреналина, приводят к вазоконстрикторному эффекту.
Фармакокинетика
Всасывание и распределение
Степень чрескожной абсорбции зависит от состояния кожи, лекарственной формы и способа применения (с использованием или без окклюзионной повязки). После попадания в системный кровоток 6α-метилпреднизолон-17-пропионат быстро конъюгирует с глюкуроновой кислотой и, таким образом, в форме 6α-метилпреднизолон-17-пропионат глюкуронида инактивируется.
Метилпреднизолона ацепонат и его метаболиты не кумулируют в организме.
Метаболизм и выведение
Метилпреднизолона ацепонат гидролизуется в эпидермисе и дерме. Главным и наиболее активным метаболитом является 6α-метилпреднизолон-17-пропионат, обладающий значительно более высоким сродством к глюкокортикоидным рецепторам кожи, что указывает на наличие его "биоактивации" в коже.
Метаболиты метилпреднизолона ацепоната элиминируются, главным образом, почками с Т 1/2 около 16 ч.
Показания препарата Комфодерм ®
Воспалительные заболевания кожи, чувствительные к терапии топическими ГКС:
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем и подготовлено для печатного издания справочника Видаль 2017 года.
Владелец регистрационного удостоверения:
Произведено:
Лекарственные формы
Форма выпуска, упаковка и состав препарата Адвантан ®
Крем для наружного применения белого или желтоватого цвета, непрозрачный.
| 1 г | |
| метилпреднизолона ацепонат | 1 мг |
Вспомогательные вещества: децилолеат - 100 мг, глицерила моностеарат 40-55% - 85 мг, цетостеариловый спирт (цетиловый спирт 60%, стеариловый спирт 40%) - 25 мг, жир твердый - 25 мг, софтизан 378 - 75 мг, макрогола стеарат - 30 мг, глицерол 85% - 50 мг, динатрия эдетат - 1 мг, бензиловый спирт - 10 мг, бутилгидрокситолуол - 60 мкг, вода очищенная - 597.94 мг.
5 г - тубы алюминиевые (1) - пачки картонные.
10 г - тубы алюминиевые (1) - пачки картонные.
15 г - тубы алюминиевые (1) - пачки картонные.
20 г - тубы алюминиевые (1) - пачки картонные.
25 г - тубы алюминиевые (1) - пачки картонные.
30 г - тубы алюминиевые (1) - пачки картонные.
50 г - тубы алюминиевые (1) - пачки картонные.
Мазь для наружного применения белого или слегка желтоватого цвета, гомогенная, непрозрачная.
| 1 г | |
| метилпреднизолона ацепонат | 1 мг |
Вспомогательные вещества: парафин белый мягкий - 350 мг, парафин жидкий - 239 мг, воск пчелиный белый - 40 мг, эмульгатор Дехимулс Е - 70 мг, вода очищенная - 300 мг.
5 г - тубы алюминиевые (1) - пачки картонные.
15 г - тубы алюминиевые (1) - пачки картонные.
20 г - тубы алюминиевые (1) - пачки картонные.
25 г - тубы алюминиевые (1) - пачки картонные.
30 г - тубы алюминиевые (1) - пачки картонные.
50 г - тубы алюминиевые (1) - пачки картонные.
Мазь для наружного применения (жирная) белого или слегка желтоватого цвета, полупрозрачная.
| 1 г | |
| метилпреднизолона ацепонат | 1 мг |
Вспомогательные вещества: парафин белый мягкий - 425 мг, парафин жидкий - 394 мг, воск микрокристаллический - 150 мг, масло касторовое гидрогенизированное - 30 мг.
5 г - тубы алюминиевые (1) - пачки картонные.
10 г - тубы алюминиевые (1) - пачки картонные.
15 г - тубы алюминиевые (1) - пачки картонные.
20 г - тубы алюминиевые (1) - пачки картонные.
25 г - тубы алюминиевые (1) - пачки картонные.
30 г - тубы алюминиевые (1) - пачки картонные.
50 г - тубы алюминиевые (1) - пачки картонные.
Эмульсия для наружного применения белого цвета, непрозрачная.
| 1 г | |
| метилпреднизолона ацепонат | 1 мг |
Вспомогательные вещества: триглицериды среднецепочные - 150 мг, софтизан 378 - 50 мг, полиоксиэтилен-2-стериловый спирт - 40 мг, полиоксиэтилен-21-стериловый спирт - 40 мг, глицерол 85% - 30 мг, динатрия эдетат - 10 мг, бензиловый спирт - 12.5 мг, вода очищенная - 675.5 мг.
20 г - тубы алюминиевые (1) - пачки картонные.
50 г - тубы алюминиевые (1) - пачки картонные.
Фармакологическое действие
При наружном применении Адвантан ® подавляет воспалительные и аллергические кожные реакции, также как и реакции, связанные с усиленной пролиферацией, что приводит к уменьшению объективных симптомов воспаления (в т.ч. эритема, отек, мокнутие и т. д.) и субъективных ощущений (в т.ч. зуд, раздражение, боль и т. д.).
При применении метилпреднизолона ацепоната наружно в рекомендуемой дозе системное действие выражено минимально как у человека, так и у животных. После многократного нанесения Адвантана на большие поверхности (40-60% поверхности кожи), а также при применении под окклюзионную повязку не отмечается нарушений функций надпочечников: уровень кортизола в плазме крови и его циркадный ритм остаются в пределах нормы, снижения уровня кортизола в суточной моче не происходит.
В ходе клинических исследований при применении Адвантана до 12 недель у взрослых и до 4 недель у детей (в т.ч. раннего возраста) не было выявлено развития атрофии кожи, телеангиэктазий, стрий и угреподобных высыпаний.
Метилпреднизолона ацепонат (особенно его основной метаболит – 6α-метилпреднизолон-17-пропионат) связывается с внутриклеточными глюкокортикоидными рецепторами. Стероид-рецепторный комплекс связывается с определенными участками ДНК клеток иммунного ответа, таким образом, вызывая серию биологических эффектов.
В частности, связывание стероид-рецепторного комплекса с ДНК клеток иммунного ответа приводит к индукции синтеза макрокортина. Макрокортин ингибирует высвобождение арахидоновой кислоты и, тем самым, образование медиаторов воспаления типа простагландинов и лейкотриенов.
Ингибирование ГКС синтеза вазодилатирующих простагландинов и потенцирование сосудосуживающего действия адреналина приводит к вазоконстрикторному эффекту.
Фармакокинетика
Степень чрескожной абсорбции зависит от состояния кожи, лекарственной формы и способа применения (с использованием или без окклюзионной повязки). При применении мази, крема или жирной мази чрескожная абсорбция у детей и взрослых с атопическим дерматитом (нейродермитом) и псориазом была не более 2.5%, что лишь незначительно выше по сравнению со здоровыми добровольцами (0.5-1.5%).
При применении препарата в форме эмульсии интенсивность абсорбции через кожу с искусственным воспалением была очень низкой (0.27%), что лишь незначительно выше, чем через здоровую кожу (0.17%). В случае обработки всего тела (например, при солнечном ожоге) системная доза составляет около 4 мкг/кг массы тела/сут, что исключает системные эффекты.
Метаболизм и выведение
Метилпреднизолона ацепонат гидролизуется в эпидермисе и дерме. Главным и наиболее активными метаболитом является 6α-метилпреднизолон-17-пропионат, обладающий значительно более высоким сродством к глюкокортикоидным рецепторам кожи, что указывает на наличие его биоактивации в коже.
После попадания в системный кровоток 6α-метилпреднизолон-17-пропионат быстро конъюгирует с глюкуроновой кислотой и, таким образом, в форме 6α-метилпреднизолон-17-пропионат глюкуронида инактивируется.
Метаболиты метилпреднизолона ацепоната элиминируются, главным образом, почками, T 1/2 - около 16 ч.
Метилпреднизолона ацепонат и его метаболиты не кумулируют в организме.
Показания препарата Адвантан ®
Мазь, крем, жирная мазь
Воспалительные заболевания кожи, чувствительные к терапии топическими ГКС:
- атопический дерматит, нейродермит, детская экзема;
- истинная экзема;
- микробная экзема;
- профессиональная экзема;
- дисгидротическая экзема;
- простой контактный дерматит;
- аллергический (контактный) дерматит.
Воспалительные заболевания кожи, чувствительные к терапии топическими ГКС:
Читайте также:

