Масло черного тмина при розацеа
Обновлено: 18.04.2024
Розацеа и купероз на лице – два заболевания, которые до сих пор многие не различают. Эти болезни кожи связаны с патологией сосудов, имеют общие симптомы и проявления, из-за чего происходит путаница. Чем отличается купероз от розацеа, следует знать, чтобы навсегда избавиться от сосудистых патологий кожи.
Отличие купероза от розацеа: ответы врача-косметолога
Розацеа и купероз – это разные болезни со множеством схожих признаков. Если купероз связан с патологическим изменением сосудов, то розацеа – болезнь, которая сопровождается специфическими уплотнениями.
Что такое купероз и розацеа?
Розацеа и купероз – разновидности сосудистых патологий, которые характеризуются появлением расширенных сосудов. В итоге кожа приобретает красноватый оттенок.
Розацеа – хроническое поражение кожи, протекающее с высыпаниями и покраснениями. Именно поэтому патология получила наименование, которое говорит само за себя, – розовые прыщи.
Сегодня пока не существует точных объяснений, почему возникает розацеа. Заболевание могут спровоцировать диеты, дисбаланс гормонов, предрасположенность. Способствуют возникновению розацеа употребление алкоголя, стрессы, переохлаждения, аллергии – любые факторы, которые провоцируют расширение сосудов.

Купероз – расширение мелких капилляров, которое вызывает покраснения кожи. Из-за расширений стенки сосудов истончаются и утрачивают эластичность. Сосуды переполняются кровью, придавая коже красноватый оттенок. Если заболевание прогрессирует, на коже формируются устойчивые сеточки из сосудов, покрывающие значительные зоны лица.
Купероз можно отнести к физиологической особенности, которая требует лечения. Длительные проявления купероза приводят к недостатку в клетках кожи кислорода и питательных компонентов. Кожа теряет воду, становится сухой, ухудшается её цвет, преждевременно запускаются процессы увядания.
Как выглядят розацеа и купероз? На коже появляются сосудистые звездочки и сеточки. Зачастую они возникают в Т-зоне. Наиболее подвержены сосудистым патологиям обладательницы чувствительной светлой кожи.
Какие отличия купероза и розацеа?
Что такое купероз и розацеа понять легко. Но заболевания сложно отличить друг от друга без квалифицированной помощи. Купероз или розацеа определить можно по симптомам. Главное отличие – купероз никогда не сопровождается гнойными воспалениями, кожа гладкая, без уплотнений.
Купероз и розацеа на лице имеют отличия в симптоматике. При куперозе поражаются малые и большие кровеносные сосуды, из-за чего кожа приобретает красноватый оттенок. В редких случаях купероз сопровождается огненным цветом кожи – возникает чувство, что кожа горит, но на самом деле болезненных симптомов нет.
В отличие от купероза розацеа сопутствуют болезненные ощущения. Кроме покраснений образуются гнойные воспаления, неровный рельеф. Отличие розацеа от купероза на лице – зуд.
Разница между куперозом и розацеа – течение заболевания. Розацеа проходит в несколько стадий:
- Эритематозная. Возникает временное покраснение кожи. В последующем покраснение приобретает стойкий характер.
- Папуло-пустулезная. В зоне покраснения появляются высыпания, наполненные красноватой жидкостью. Они возникают из-за нарушений метаболизма в коже и расширения сосудов. Кровь просачивается в окружающие ткани, окрашивая их в характерный цвет.
- Фимозная. На коже формируются уплотненные узелки и бляшки.
- Риноформа. Сопровождается увеличением размеров носа. Эта стадия характерна только для мужчин.
Как понять, что у тебя розацеа?
«Как понять, у меня купероз или розацеа?» – распространенный вопрос к врачу-косметологу.

Характерные признаки розацеа:
- Розовые высыпания. Со временем розовые бугорки наполняются гноем, под ними располагается покрасневшая кожа
- Покраснения лица в Т-зоне
- Возникновение сосудистой сеточки
Как ставят диагноз розацеа?
Независимо от характера болезни (купероз, демодекоз, розацеа), лечению предшествует диагностика. Врач-косметолог определит, розацеа или купероз у пациента. Потребуется осмотр, анализ крови, в отдельных случаях – соскобы пораженных зон кожи. При необходимости врач назначит УЗИ внутренних органов, чтобы исключить заболевания, которые могут провоцировать кожные реакции.
Задача врача-косметолога не только устранить внешние проявления розацеа на коже, но и установить причину заболевания. Для этого необходимо исследовать состояние ЖКТ и эндокринной системы – исключить гастриты, колиты, дисбаланс гормонов и т.д.
Что нельзя есть при розацеа?
Розацеа и купероз на лице – заболевания, к лечению которых нужно подходить комплексно. В первую очередь, это касается питания. Чтобы избавиться от розацеа, из рациона нужно исключить опасные и вредные продукты:
- Сладкое и мучное. Они содержат сахара, которые провоцируют воспаления
- Молочные продукты. Прогестерон, которым богаты молочные продукты, усиливает функции сальных желёз – гнойных воспалений на коже становится больше.
- Алкоголь. Научно доказано, что алкогольные напитки сами по себе не вызывают розацеа, но усугубляют течение болезни. Алкоголь расширяет сосуды и вызывает дополнительный румянец на лице.
- Продукты, содержащие кофеин (чай и кофе). Стимулируют выработку гормона кортизола, который запускает стресс. Стрессовые ситуации нередко приводят к появлению воспалений на коже.
- Консервированные, маринованные, соленые, жареные и острые продукты. Приводят к возникновению прыщей на коже, расширяют сосуды, ослабляют иммунитет.
- Цитрусовые и сладкие фрукты. Вызывают кожные воспаления.
Можно ли вылечить розацеа навсегда?
Независимо от того, телеангиэктазия, купероз или розацеа, лечение должно быть комплексным. Особенность розацеа в том, что несмотря на внешние признаки, причины скрываются глубоко в организме. И чтобы избавиться навсегда от розацеа, нужно установить и устранить причину заболевания.
Лечение розацеа и купероза проводят в нескольких направлениях. Как правило, эндокринолог и косметолог разрабатывают комплексный план терапии, который нацелен на быстрое устранение внешних проявлений заболевания и глубокое лечение причин розацеа.
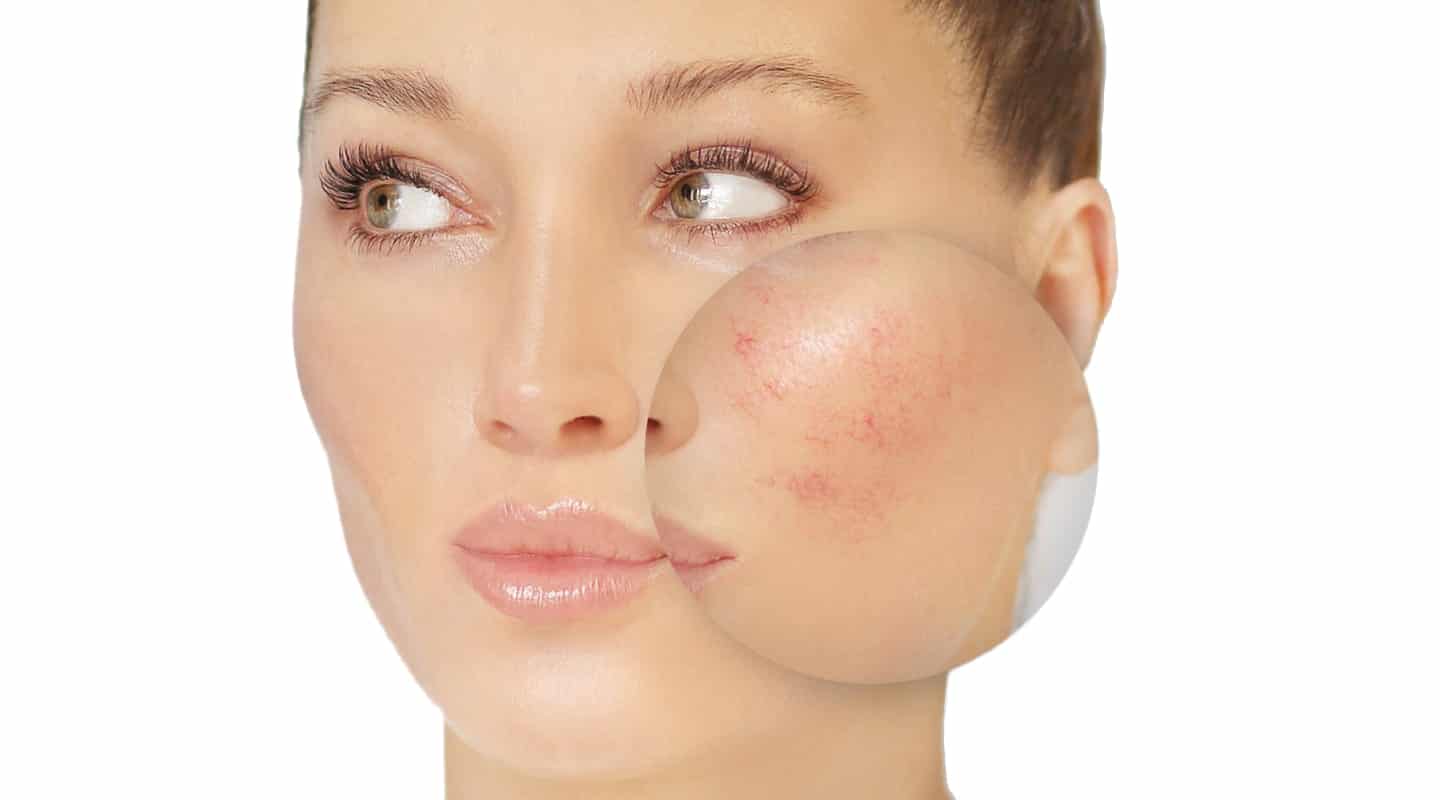
Лечение розацеа и купероза состоит из следующих этапов:
- Правильный уход за кожей. Тщательная гигиена, подбор косметических средств, ежедневное использование крема с SPF защитой. Кислотные пилинги, средства, содержащие спирт, грубые скрабы противопоказаны при розацеа.
- Терапевтическое лечение. Основано на использовании антибактериальных и антисептических средств, которые устраняют причины и последствия акне.
- Медикаментозное лечение. В зависимости от показаний пациенту могут быть назначены медикаменты, гормональные препараты и т.д.
- Аппаратное лечение. Устранение сосудистых звездочек аппаратными методами.
Какие косметические процедуры можно делать при розацеа?
При лечении купероза и розацеа на лице не обойтись без косметологических процедур. Но далеко не все они разрешены при сосудистых патологиях.
Эффективно избавиться от купероза и розацеа помогают:
- Фотолечение. Импульсный свет воздействует на патологические ткани. Мишени лучей – микроорганизмы и измененные капилляры. Под влиянием фотовспышек разрушаются старые коллагеновые волокна, запускается выработка новых. Главная особенность фотолечения – способность к склеиванию сосудов. Лучи нагревают сосуд до 60 градусов, что провоцирует свертывание крови и сосуды становятся пустыми.
- Плазмотерапия. Процедура основана на использовании аутогенной плазмы. Плазмотерапия запускает процессы восстановления клеток кожи, нормализует метаболизм, насыщает кожу полезными веществами. В дерме усиливается синтез коллагена, уменьшаются процессы воспаления.
Можно ли вылечить розацеа лазером?
Устранить купероз и розацеа можно лазером. Сосудистые сетки прижигают лазерными лучами. Метод эффективен на разных стадиях заболевания – как на начальной, так и в запущенных случаях.
Лазерные лучи быстро и надолго устраняют покраснения и сосудистые звездочки с поверхности кожи. От стадии розацеа и купероза зависит количество сеансов.
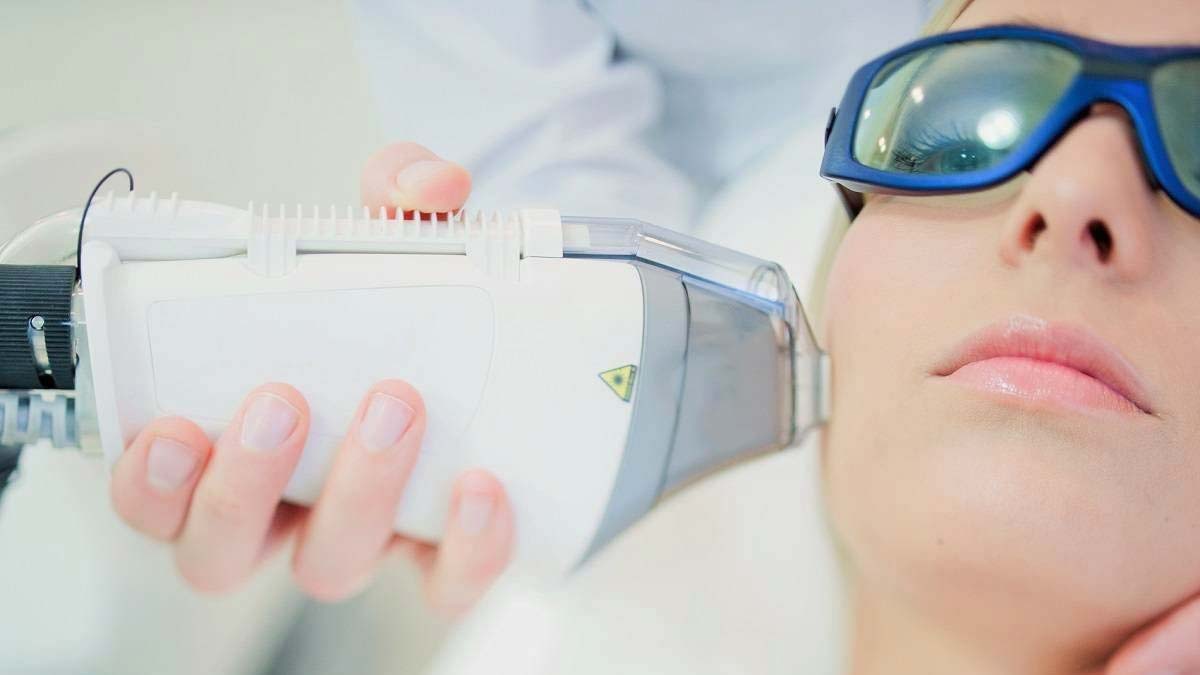
Удаление лазером купероза и розацеа – действенный метод от сосудистых звездочек. Процедура позволяет получить выраженный результат, не требует длительного периода восстановления. Эффект от процедуры длится несколько лет.
Сколько стоит лазерное лечение розацеа?
Прежде чем приступить к устранению купероза и розацеа лазером, врач-косметолог проведет диагностику – определит тяжесть заболевания и подберет эффективный комплекс процедур. Длительность корректировки кожных дефектов определяется запущенностью заболевания. От количества сеансов зависит стоимость лазерного лечения.
Можно ли делать химический пилинг при розацеа?
Купероз или розацеа на лице – заболевания, требующие бережного ухода за кожей. Агрессивные химические пилинги могут только усугубить течение заболевания. Непрофессионально проведенный кислотный пилинг провоцирует стойкие покраснения – кожа после процедуры долго заживает. Неквалифицированный подход к терапии и неграмотный подбор домашних средств усугубят течение заболевания. Как лечить розацеа и купероз на лице, знает врач-косметолог.
При розацеа и куперозе показаны только деликатные пилинги (например, с использованием миндальной или молочной кислоты). Антиоксидантные монопилинги назначают при эритематозной форме розацеа. Поверхностный миндальный пилинг не вызывает шелушений и жжения.
При пустулезной форме можно использовать комбинации азелаиновой и молочной кислоты. Они угнетают выработку активных форм кислорода, регулируют образование секрета кожных желёз. Кислотный состав для пилинга врач подбирает индивидуально в зависимости от характера и течения заболевания.
Что такое купероз и как от него избавиться?
Купероз может быть как самостоятельным проявлением изменений в коже, так и признаком серьезных болезней. Купероз протекает в несколько стадий:
- Быстрое покраснение без явных причин. Через время краснота пропадает без последствий – сосуды еще эластичны, чтобы восстановить свое первоначальное состояние.
- На коже появляется характерный узор из сосудов. Это признак того, что сосуды не могут вернуться к нормальному состоянию.
- Хронические нарушения циркуляции крови и недостаток питания клеток кожи.
Как лечить розацеа и купероз знает врач-косметолог. Избавиться от кожных патологий можно комплексно, установив причину заболевания. Если купероз вызван болезнью внутренних органов, в первую очередь лечить нужно их. Применение только наружных средств устранит проявления купероза, но не застрахует от появления новых сосудистых звёздочек. Сочетание методов терапии, которые дополняют друг друга, позволит добиться стойкого результата.
Почему появляется купероз?
Купероз на лице и розацеа отличаются причинами возникновения. Купероз вызывают следующие факторы:
- аутоиммунные заболевания
- резкие температурные перепады – бани, ледяные компрессы
- злоупотребление веществами, которые сужают сосуды – алкоголь, никотин
- продолжительное воздействие ультрафиолета
- постоянные стрессы
- хронические патологии ЖКТ и сердечно-сосудистой системы
Что нельзя делать при куперозе?
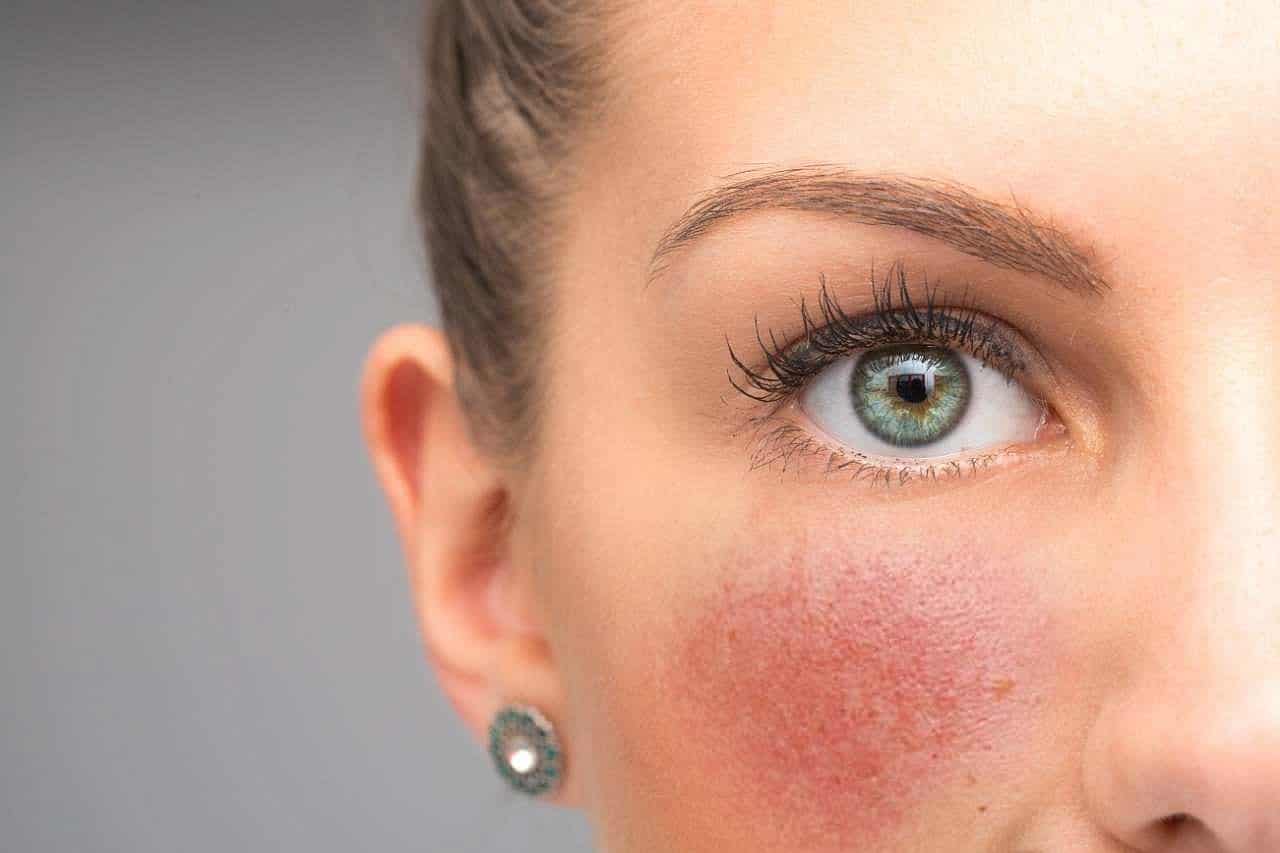
Розацеа и купероз хотя и не одно и то же, но имеют сходные ограничения. При куперозе стоит отказаться от следующего:
- бани и сауны
- искусственный загар в солярии
- травматические чистки лица
- лазерные шлифовки
- косметические средства с кислотами и спиртом
- скрабы и пилинги с жесткими частичками
- термальные маски
- контрастные умывания
Акне, купероз и розацеа следует лечить, исключив из рациона вредные продукты:
- алкоголь и газированные напитки
- хлебобулочные изделия, конфеты и пирожные
- все виды красного мяса
- консервированные, острые и соленые продукты
Как лечить купероз?
Чем лечить купероз и розацеа зависит от тяжести заболевания. Врач-косметолог проведет диагностику и подберет оптимальные методы устранения сосудистых патологий.
Эритроз, купероз и розацеа – заболевания, требующие комплексного подхода. Чтобы успешно устранить дефекты, нужно скорректировать рацион питания, физическую активность, гормональный фон, правильно подобрать домашний уход.
Лечение купероза и розацеа включает:
- Диета. Из рациона исключают продукты, которые провоцируют ломкость сосудов (алкогольные напитки, кофе, сладкое, острые и горячие блюда).
- Ежедневный уход. При куперозе используют щадящие средства ухода, не содержащие спирт и агрессивные компоненты.
- Очищение. Для купероза характерно обезвоживание кожи. Если использовать для умывания мыльные средства, они будут провоцировать разрушение защитной липидной пленки на поверхности кожи – чувствительная кожа будет терять воду. Чтобы исключить обезвоживание, при куперозе применяют деликатные очищающие средства. Для умывания нельзя применять горячую или холодную воду.
- Увлажнение и питание. Косметолог подберет средства, содержащие витамины и аминокислоты, которые укрепляют стенки сосудов. Чтобы уберечь кожу от ультрафиолета, следует применять дневные крема с SPF защитой.
Лечение купероза и розацеа базируется на применении косметологических процедур. Их подбирает врач-косметолог относительно особенностей организма и запущенности заболевания.
Как лечить купероз и розацеа – новые методы:
- Мезотерапия. Микроинъекции укрепляют стенки капилляров и нормализуют движение крови. Процедура показана в качестве профилактики и лечения сосудистых патологий.
- Лазеротерапия. Лазерные лучи прижигают стенки сосудов, позволяют быстро избавиться от сосудистых сеток.
- Фототерапия. Вспышки света помогут устранить обширные сосудистые сеточки, пигментные пятна, акне и морщины.
Автор статьи: Чем отличается купероз от розацеа

Охремчук Елизавета Дмитриевна
С отличием окончила лечебный факультет Кировской медицинской академии, затем клиническую ординатуру на кафедре неврологии и клиническую интернатуру на кафедре дерматовенерологии Краснодарского государственного медицинского университета. Профессиональная переподготовка по программе «Косметология».
Рассмотрена проблема возникновения демодекоза, обсуждена роль клеща Demodex в формировании папул и пустул на коже лица, приведены методы диагностики и подходы к лечению пациентов, меры профилактики.
The problem of demodecosis occurrence was considered, the role of Demodex tick in formation of papula and pustula on the skin of the face was discussed, methods of the diagnostics and approaches to the treatment of the patients were given, as well as the preventive measures.
Папулопустулезные дерматозы, основной локализацией которых является кожа лица (акне, розацеа, периоральный дерматит), остаются актуальной проблемой в дерматовенерологии. Среди различных причин возникновения этих заболеваний определенная роль отводится паразитарной теории [1]. Согласно ей, формированию папул и пустул на коже лица способствует клещ-железница (Demodex). Клещ принадлежит роду Demodex, семейству Demodicidae, подотряда Trombidiformes, отряда Acariformes. Впервые клеща выявил F. Berger в ушной сере слухового прохода человека в 1841 году, в том же году F. Henle обнаружил клеща на коже человека. Через год, в 1842 году, G. Simon установил наличие паразита в волосяных фолликулах и впервые описал морфологические свойства, назвав их Acarus folliculorum (от греч. — «сальное животное»). Позже G. Simon (1842) и R. Owen (1843) отнесли найденных клещей к роду Demodex. Намного позднее, более чем через полвека, английский акаролог S. Hirst (1917–1923) выделил 21 вид и несколько подвидов клещей рода Demodex у животных. Впоследствии, изучая паразитирование клеща на коже человека, Л. Х. Акбулатова (1970) обнаружила и описала две формы: Demodex folliculorum longus и Demodex folliculorum brevis [2].
Демодекоз (Demodecosis) — распространенное хроническое заболевание, преимущественно кожи лица. По разным данным, заболеваемость демодекозом составляет от 2% до 5% и стоит на седьмом месте по частоте среди кожных болезней [3, 4]. В структуре акнеформных дерматозов демодекоз составляет 10,5% [5]. Частота осложнений демодекозом у больных розацеа встречается в 88,7%, а периоральным дерматитом в 58,8% случаев [6].
Клещи рода Demodex одинаково распространены среди всех рас и всех возрастных групп [7]. Описаны редкие случаи обнаружения клеща у новорожденных [8], и в целом у детей регистрируется невысокий уровень обсемененности. По всей вероятности, это связано с более низкой выработкой кожного сала у детей по сравнению с взрослыми людьми [9]. Так, у пациентов моложе 20 лет распространенность клещей Demodex составляет 13–20%, а к 70 годам увеличивается до 95–100% [6]. У больных после 45 лет активность клещей поддерживается возрастными изменениями кожи и желез, климактерическими гормональными перестройками, а также различной соматической патологией. Наибольшее количество случаев поражения демодекозом отмечается у людей в возрастной группе 20–40 лет [10]. В лабораторных исследованиях Demodex folliculorum longus выявляется чаще, чем Demodex folliculorum brevis [1], в соотношении у мужчин — 4:1, у женщин — 10:1 [11].
Этиология и патогенез демодекоза
Как демонстрируют многие исследования, даже при наличии на кожном покрове клещей, клиническая картина заболевания развивается не всегда. Исходя из этого, можно утверждать, что клещи рода Demodex являются условно-патогенными паразитами [7]. До настоящего времени не установлены точные причины, приводящие к патогенности клещей рода Demodex, существующие теории разнообразны и противоречивы [12].
Самое распространенное мнение, что одним из пусковых факторов развития заболевания является нарушение микрофлоры кожного покрова. Следуя данной теории, развитию патогенности клеща благоприятствуют изменения функций сальных желез с последующим изменением состава кожного сала и микробиоценоза, что приводит к дисбактериозу кожи. Пусковым фактором для развития заболевания является нарушение симбиоза коринобактерий и условно-патогенной микрофлоры [5], а также усиление микробной колонизации вследствие изменения количества поверхностных липидов [13].
Согласно мнению многих авторов, успех терапии метронидазолом, не обладающим прямым антипаразитарным действием, связан с тем, что Demodex проявляет свои патогенные свойства в качестве переносчика микробов и вирусов в более глубокие отделы волосяных фолликулов и сальных желез [14]. Дополнительным фактором для развития воспалительного гнойно-некротического процесса является возможность занесения патогенных пиококков и Pityrosporum spp. в глубокие слои фолликул и сальных желез при перемещении клещей [14, 15].
Заслуживают внимания и другие теории развития воспаления в коже при демодекозе. Бацилла (Bacilluss oleronius), найденная на поверхности клеща, в результате своей жизнедеятельности способна повышать активность самих клещей, а также стимулировать другие микроорганизмы (стрептококки, стафилококки, Propionibacterium acnes, грибы рода Malassezia) [16], вырабатывать провоспалительные белки 62-Da и 83-Da, запуская каскад иммунных реакций [17].
Благоприятным фактором для возникновения демодекоза является наличие очагов хронической инфекции, нарушения функций желудочно-кишечного тракта, печени, нервной системы, эндокринных желез, длительного применения топических кортикостероидов [18–20]. Многими авторами отмечена связь подъема заболеваемости в весенне-летний период с повышенной инсоляцией, изменением температуры внешней среды [18]. Скорее всего, это можно объяснить тем, что выработка витамина D под действием ультрафиолетового излучения вызывает повышенный синтез кателицидинов (LL-37), поддерживающих активность воспалительного процесса [21, 22].
Большую роль в развитии инвазии клещами рода Demodex играет реактивность иммунной системы. Ряд авторов показали, что Demodex folliculorum встречается чаще у пациентов декретированных групп, например, при гемодиализе и Т-клеточных лимфомах [23], первичном или вторичном иммунодефиците [24], вирусе иммунодефицита человека, острой лимфобластной лейкемии и других злокачественных новообразованиях [25], после кортикостероидной [26] или цитостатической терапии [27].
Фактором для развития клещевой инвазии, поддержания активности патологического процесса, а также неэффективности проводимой терапии, по мнению большинства авторов, является дисбаланс в цитокиновом каскаде [3, 13, 28–30]. Обнаружено наличие инфильтратов вокруг клещей Demodex из эозинофилов и типичных гранулем, состоящих из CD4+ Т-хелперов [31], повышение готовности лимфоцитов к апоптозу и увеличенное количество NK клеток с Fc-рецепторами [32], снижение абсолютного числа лимфоцитов и увеличение уровня IgM [33].
Клиническая картина заболевания
Источником заражения демодекозом является человек (больной или носитель) и домашние животные. Клещи паразитируют у собак, лошадей, крупного рогатого скота. Демодекоз может быть первичным и протекать как самостоятельное заболевание и вторичным, как следствие уже имеющихся болезней кожи (розацеа, периоральный дерматит, себорейный дерматит и др.) [34].
Основная локализация клещей — сальные железы кожи лица, ушных раковин, спины, груди, мейбомиевые железы, фолликулы кожи в области сосков, редко — в области спины [2]. Атипичные локализации, где может быть найден Demodex, — половой член, ягодицы, эктопические сальные железы, слизистая оболочка рта. N. Stcherbatchoff (1903), обнаружив клещей в ресничных фолликулах век человека, доказала роль клеща в развитии блефаритов и блефароконъюнктивитов. Этиопатогенетическое влияние клещей при заболеваниях глаз достаточно велико и в настоящее время описывается многими авторами [35].
Заболевание возникает внезапно. Субъективно у больных появляются ощущения зуда, жжения, ползания, распирания и жара. Патологический кожный процесс локализуется преимущественно в области Т-зоны лица. Классические клинические проявления демодекозной инфекции — Pityriasis folliculorum, сопровождаются ощущениями зуда и жара, кожа становится истонченной, приобретая вид папирусной бумаги [1]. Акнеформный тип характеризуется преобладанием папул на коже лица, а наличие папулопустулезных элементов и диффузной эритемы говорят о розацеоподобном типе [1]. Клиническая картина demodicosis gravis имеет схожесть с гранулематозной формой розацеа, также характеризующейся наличием гранулем в дерме [1].
Интересно, что разные виды клеща вызывают различную клиническую картину, что связано, предположительно, с размерами самих клещей. При обнаружении Demodex folliculorum чаще наблюдается эритема и десквамация эпителия, при выявлении Demodex brevis — симметричные папулопустулезные элементы [36].
При поражении глаз отмечается гиперкератоз с наличием чешуек на ресничном крае и «воротничка» вокруг ресниц [37, 38]. Пациенты жалуются на чувство зуда и ощущение инородного тела в глазах [39].
В научной литературе существует предположение о роли Demodex в формировании андрогенной алопеции [40]. Возможно, механизм развития облысения связан с формированием инфильтрата в волосяном фолликуле, вызванным присутствием клещей Demodex. Активированные воспалением Т-лимфоциты индуцируют синтез коллагена, что, в конечном счете, приводит к фиброзному перерождению волосяного фолликула [35].
Длительное хроническое течение демодекоза характеризуется утолщением кожи, чувством стягивания, уменьшением эластичности и мягкости, наличием серозных или кровянисто-гнойных корочек. Присоединение вторичной пиококковой инфекции сопровождается возникновением крупных пустул, нодулярных элементов, макроабсцессов, что может приводить к обезображиванию лица [34].
Диагностика демодекоза
Диагностика демодекоза может проводиться несколькими методами. Лабораторная диагностика является наиболее простым методом. В ходе нее составляется акарограмма, которая основывается на подсчете личинок, нимф, яиц и имаго. Клеща возможно обнаружить на поврежденном участке кожи, при экстракции содержимого фолликула или извлечении ресниц или бровей без повреждения волосяных фолликулов [41]. Исследуемый материал помещают на предметное стекло с 10% раствором щелочи (с целью определения активности клещей применяют глицерин), накрывают предметным стеклом и просматривают под малым увеличением микроскопа. Для более точного микроскопического подсчета обнаруженных клещей рекомендуется добавлять в исследуемый материал раствор красителя флюоресцеина [42]. Микроскопический метод является единственным для определения наличия клещей в волосяных фолликулах. Критерием клещевой активности служит количество более 5 взрослых особей, личинок или яиц на 1 см2 [34]. При диагностике демодекоза ресниц нормой считается обнаружение одного клеща на 2–4 ресницах [43].
Преимущество методики заключается в возможности анализа сразу нескольких участков поражения, а также извлечении клещей не только с поверхности кожного покрова, но и непосредственно из сальных желез. Здесь возникает другая проблема — не всегда удается добраться до клещей в глубине сальных желез. В связи с этим соскоб не является высокоинформативным методом и не доказывает отсутствие клещей [44]. К недостаткам метода также относятся травматизация эпителия, обследование небольших по величине участков поражения, относительная болезненность процедуры и дискомфорт пациентов после эпиляции [45].
Для оценки проводимой терапии делают повторные акарограммы, с целью подсчета количества и определения активности клещей [45]. Если в соскобе обнаружены исключительно продукты жизнедеятельности и пустые яйцевые оболочки, проводят повторное исследование, т. к. в процессе лечения Demodex перемещается в зоны, необработанные акарицидными средствами. В таких случаях чаще всего клещи локализуются у кромки волосистой части головы [5].
Другим модифицированным методом диагностики является проведение поверхностной биопсии («скотч-проба») [44]. На обезжиренное покровное стекло наносят каплю клея цианокрилата (БФ-6, сульфакрилат), затем приклеивают к пораженной поверхности на 1 минуту. Во втором варианте используют скотч, размером 1 см 2 , который после снятия приклеивается к покровному стеклу. При удалении покровного стекла или скотча на их поверхности остается слой эпидермиса, содержимое сальных желез с имеющимися там клещами. Затем наносится раствор щелочи, накрывается поверх покровным стеклом и рассматривается под микроскопом на малом увеличении. В сравнении с прямым микроскопическим исследованием данный метод позволяет диагностировать демодекоз в большем числе случаев [46]. Преимущество метода — это проведение процедуры на любом участке кожного покрова, а также простота применения. Травматизация эпителия, трудность получения материала с крыльев носа, неполная стерильность получаемых препаратов являются недостатками метода [45].
М. В. Камакина (2002) выявила достоверную статистическую вероятность отрицательного результата лабораторного анализа на наличие клещей на коже при выраженной клинической картине заболевания, которая составила 1,5% [47]. Следовательно, лабораторные методы не являются абсолютно достоверными.
Более информативным методом диагностики демодекоза является проведение кожной биопсии с последующей гистологией полученных препаратов. С этой целью пункционным (панч) или эксцизионным (скальпель) методом берут небольшой участок кожи, фиксируют его в течение суток 10% нейтральным раствором формалина, уплотняют парафином и окрашивают гематоксилин-эозином. Гистологическое исследование дает массу преимуществ. В частности, можно полностью посмотреть сальную железу и окружающие ее участки. При ретроспективном патоморфологическом исследовании биоптатов кожи головы в 15% случаев наблюдалось сочетание демодекоза с грибковыми, воспалительными поражениями, невусами, фиброзом [48]. Главным недостатком метода является травматизация кожи с образованием рубца, а также невозможность обследования большой поверхности кожного покрова [45].
В качестве диагностического инструмента для выявления Demodex R. Segal и соавт. (2010) предложили использовать дерматоскоп. Метод дерматоскопии позволяет визуализировать клещей на поверхности кожного покрова, а также расширенные сосуды кожи [49]. Другим неинвазивным методом оценки наличия клещей Demodex является применение оптической когерентной томографии, позволяющей в режиме реального времени оценить состояние кожи больных в двух проекциях [50].
С появлением конфокального лазерного микроскопа стал доступен новый метод обследования больных на наличие клещей Demodex. Конфокальная лазерная сканирующая микроскопия позволяет визуализировать поверхностные слои кожного покрова in vivo, а также получить объемное четырехмерное изображение [51]. Преимуществами метода является высокая информативность, неинвазивность и, как следствие, отсутствие дискомфорта у пациентов.
Лечение демодекоза
При выборе терапии демодекоза необходимо учитывать клиническую картину заболевания, тяжесть процесса, а также сопутствующую патологию пациента [52, 67–69].
До сих пор на протяжении многих лет самым эффективным препаратом в терапии демодекоза остается метронидазол, являющийся производным нитроимидазольной группы [53]. Метронидазол обладает выраженным противовоспалительным [22], противоотечным [54], иммуномодулирующим действием [55]. Стандартная схема лечения метронидазолом — 250 мг 3 раза в день в течение 2–4 недель [52].
Другим препаратом выбора является орнидазол, назначаемый по схеме 500 мг два раза в день курсами по 10 дней [52]. Препарат имеет как противопаразитарное, так и бактериостатическое действие, повышает активность нейтрофилов, стимулирует адренергические структуры, усиливает репаративные процессы [52, 56].
Наружная терапия также должна включать антипаразитарные средства. Наиболее часто используется метронидазол (Клион, Метрогил) в виде мази или геля 2%, применяемый в течение 14 дней. В качестве альтернативной терапии возможно применение мази бензилбензоат [1, 10, 43, 57].
С целью достижения элиминации клещей назначают акарицидные препараты. Из фармакологической группы пиретроидов, обладающих антипаразитарными свойствами, доказал свою эффективность перметрин [4, 58]. Небольшое количество мази тонким слоем наносят на пораженные участки кожи. Мазь смывают водой через 24 часа. В большинстве случаев достаточно однократного применения, но при недостаточной эффективности (появление новых элементов сыпи, сохранение зуда) процедуру рекомендуется повторить через 14 дней.
Хорошо переносится и не вызывает серьезных нежелательных лекарственных реакций препарат Спрегаль, содержащий раствор эсдепалетрина и пиперонила бутоксида [18, 59].
При наличии папулопустулезных высыпаний показано назначение классических редуцирующих мазей и паст (цинк-ихтиоловая [60], 1–2% дегтярная и 1–2% ихтиоловая мази, 1% ихтиол-резорциновая паста) [61].
Некоторые авторы высоко оценивают терапевтическую эффективность геля Демотен (сера, гиалуроновая кислота, сок алоэ вера, поливинилпирролидон) [62].
Однако, несмотря на успешную терапию с применением классических средств, в практике дерматовенеролога все чаще встречаются резистентные к терапии и рецидивирующие формы демодекоза. В связи с этим разрабатываются новые методы и методики лечения. Например, Л. Р. Беридзе (2009) рекомендует использовать сочетанную методику криотерапии с кремом Розамет (метронидазол 1%) [57].
В случае акнеформного типа демодекоза или резистентности к антипаразитарным препаратам целесообразно использовать системные ретиноиды (изотретиноин) в дозировке 0,1–0,5 мг/кг массы тела в сутки в течение 2–4 месяцев [63].
При лечении демодекоза глаз используются антихолинэстеразные средства (холиномиметики): физостигмин, 0,02% фосфакол, 0,01% армин, 0,5% тосмилен [38]. Хорошие результаты лечения наблюдаются при применении Блефарогеля 1 и 2, Блефаролосьона [64].
Из физиотерапевтических методик рекомендуется использовать свойства узкополосного синего света (405–420 нм). Длины волн голубого света несколько больше длин волн ультрафиолетового излучения, поэтому узкополосный синий свет достигает сетчатого слоя дермы, проникая на глубину до 2,5 мм, соответствующей расположению сальных желез. Единичные наблюдения свидетельствуют о высокой эффективности данного метода при лечении акне, осложненных демодекозом [65].
Меры профилактики сводятся к соблюдению общегигиенических правил, адекватного и рационального ухода за кожей лица, полноценного питания и отдыха. Важно применение защитных средств против ультрафиолетового излучения, а также ограничение пребывания на солнце [66].
Таким образом, несмотря на то, что демодекоз часто встречающееся заболевание, до сих пор не раскрыты этиологические факторы, приводящие к патогенности клеща, и не установлен точный механизм развития воспаления кожи, не оценена роль Demodex в возникновении воспалительных дерматозов на коже лица. Противоречивость мнений различных авторов вызывает много споров и вопросов, требующих дальнейшего исследования. Лечение антипаразитарными средствами не всегда эффективно и часто провоцирует развитие хронически резистентных к терапии форм.
Литература
А. А. Кубанов, доктор медицинских наук, профессор
Ю. А. Галлямова, доктор медицинских наук, профессор
А. С. Гревцева 1
Российский государственный медицинский университет им. Н.И. Пирогова
ГБОУ ВПО "Российский научно-исследовательский медицинский университет им. Н.И. Пирогова", Москва, 117997, Российская Федерация
Российский государственный медицинский университет, Российская детская клиническая больница, Москва
ГОУ ВПО Первый московский государственный медицинский университет им. И.М. Сеченова Министерства здравоохранения и социального развития Российской Федерации
Российский государственный медицинский университет, Москва
Новые высокоэффективные препараты в лечении псориаза
Журнал: Клиническая дерматология и венерология. 2014;12(3): 77‑81
Короткий Н.Г., Кубылинский А.А., Тихомиров А.А., Уджуху В.Ю., Шарова Н.М. Новые высокоэффективные препараты в лечении псориаза. Клиническая дерматология и венерология. 2014;12(3):77‑81.
Korotkiĭ NG, Kubylinskiĭ AA, Tikhomirov AA, Udzhukhu VIu, Sharova NM. New highly effective drugs in treatment of psoriasis. Klinicheskaya Dermatologiya i Venerologiya. 2014;12(3):77‑81. (In Russ.).
Российский государственный медицинский университет им. Н.И. Пирогова
Неуклонный рост заболеваемости псориазом сопровождается снижением биологического возраста пациентов. Отмечается увеличение количества тяжелых, инвалидизирующих форм, развитие торпидности псориатического процесса к проводимой терапии. Цель исследования - совершенствование терапии пациентов, страдающих псориазом легкой и средней степени тяжести. Материал и методы. Под наблюдением находились 84 больных с псориазом различной степени тяжести. Тимодепрессин вводили внутримышечно по 1-2 мл раствора ежедневно в течение 7-10 дней, после 2-дневного перерыва аналогичный цикл повторяли. В дальнейшем назначали Тимодепрессин интраназально в качестве поддерживающей терапии и для профилактики рецидивов. Результаты. Сравнительный анализ результатов продемонстрировал высокую клиническую эффективность включения препарата Тимодепрессин в схемы лечения больных псориазом.
Российский государственный медицинский университет им. Н.И. Пирогова
ГБОУ ВПО "Российский научно-исследовательский медицинский университет им. Н.И. Пирогова", Москва, 117997, Российская Федерация
Российский государственный медицинский университет, Российская детская клиническая больница, Москва
ГОУ ВПО Первый московский государственный медицинский университет им. И.М. Сеченова Министерства здравоохранения и социального развития Российской Федерации
Российский государственный медицинский университет, Москва
На сегодняшний день псориаз считают одним из самых распространенных хронических дерматозов. По разным данным [1], этим заболеванием страдает от 0,2 до 8% населения земного шара.
Начало заболевания неодинаково у разных больных. Провоцирующими факторами могут быть травмы кожи, стресс, применение некоторых медикаментов, злоупотребление алкоголем, инфекционные заболевания (особенно вызванные стрептококком и вирусами) и др. [2, 3].
При псориазе легкой степени наиболее часто применяют смягчающие и увлажняющие средства, сочетая их с другими активными местными средствами. Кератолитические препараты уменьшают выраженность гиперкератоза и смягчают псориатические чешуйки, что в свою очередь способствует их удалению. Как и смягчающие средства, кератолитические также принято сочетать с другими препаратами. Различные лекарственные формы глюкокортикостероидов (ГКС) наиболее часто используют для лечения псориаза, однако их системная абсорбция приводит к возникновению ряда серьезных побочных эффектов.
Применение ретиноидов в течение 12 нед показывает хорошую клиническую эффективность, причем она может быть повышена при совместном использовании с ГКС.
В процессе развития заболевания, при увеличении числа элементов, их периферическом росте папулы сливаются и образуют бляшки разнообразных размеров и очертаний. В этот момент псориатические поражения характеризует высокая степень распространенности, выраженность эритемы и инфильтрации, что утяжеляет состояние больного. Как правило, степень тяжести и распространенности псориатического процесса (PASI) оценивается как средняя (10≤PASI≤30) или как тяжелая (30≤PASI≤72). Излюбленная локализация псориаза - разгибательные поверхности конечностей, особенно в области локтевых и коленных суставов. Высыпания могут поражать кожу туловища; часто поражается волосистая часть головы.
Лечение псориаза - сложная терапевтическая задача [8]. В соответствии с патогенетическими процессами терапия псориаза направлена на устранение воспаления, подавление пролиферации эпителиоцитов, нормализацию их дифференцировки. Во многих случаях терапевтические мероприятия могут быть успешными, так как имеется ряд методов терапевтического воздействия при этом дерматозе, но, к сожалению, все эти мероприятия дают лишь временный эффект [9]. Фармакотерапия и фототерапия могут очистить пораженные участки кожи и облегчить неприятные симптомы, однако ремиссия обычно кратковременна и в течение года у большинства пациентов наблюдается рецидив заболевания.
Для лечения псориатического процесса средней и тяжелой степеней назначают системную терапию: фототерапию, применение аналогов витамина А и различные варианты иммуносупрессии.
Фототерапия блокирует репликацию ДНК, понижая пролиферацию клеток кожи; этот метод достаточно эффективен, однако сопряжен с риском развития рака кожи, по причине чего его назначают больным старше 50 лет с интенсивным инвалидизирующим псориазом.
Аналоги витамина А главным образом назначают для лечения тяжелых и редких форм псориаза. Эти препараты обладают противовоспалительными свойствами, снижающими пролиферацию клеток кожи. Однако и их применение ассоциируется с тяжелыми нежелательными явлениями, в том числе такими, как повреждение печени и эмбриональные дефекты.
Псориаз - заболевание мультифакториальное. Несомненно, большую роль в его патогенезе играют изменения иммунной системы либо генетически обусловленные, либо приобретенные под влиянием внешних и внутренних факторов.
Нарушения иммунной системы выявляют как на клеточном, так и на гуморальном уровнях и заключаются они в активации иммунологических реакций, сопровождаясь изменениями содержания иммуноглобулинов основных классов, циркулирующих иммунных комплексов, пула лимфоцитов в периферической крови, В- и Т-популяций и субпопуляций лимфоцитов, клеток-киллеров, фагоцитарной активности сегментоядерных лейкоцитов. Для нормализации этих процессов используют различные препараты, относящиеся к группе иммуносупрессантов.
Метотрексат - аналог фолиевой кислоты, ингибитор синтеза ДНК обладает способностью останавливать деление клеток. Обычно метотрексат назначают для лечения очень тяжелых форм псориаза, не поддающихся лечению другими средствами, однако его применение сопряжено с подавлением всех делящихся ростков и ассоциируется с поражением печени.
Иммуносупрессоры, такие как циклоспорин, оказывают селективное действие на Т-клетки. Циклоспорин обычно используют в терапии тяжелого чешуйчатого псориаза, но и его применение ограничено лишь лечением больных с резистентной формой псориаза из-за нежелательных явлений, таких как почечная недостаточность, парестезии и гирсутизм.
Широкое применение для лечения псориаза в последние годы получили препараты генной инженерии - моноклональные антитела (МАТ). Названия препаратов, созданных на основе МАТ, отражают их структуру и основные свойства. Так, препараты с окончанием «-цепт» блокируют цитокины и, соответственно, предотвращают кооперацию клеток; препараты с окончанием «-ксимаб» содержат животные МАТ и, связываясь с фактором некроза опухоли α, блокируют его; с окончанием «-мумаб» - только человеческие (гуманизированные) МАТ с аналогичным механизмом действия.
МАТ в терапии псориаза характеризует высокая эффективность. За счет проявления антицитокиновой активности они воздействуют целенаправленно на звенья патологического процесса, в итоге заметно улучшается качество жизни больных, а также достигается длительный период ремиссии этого заболевания [10].
Назначение таких препаратов при их высокой клинической эффективности сопряжено с рядом противопоказаний и с появлением нежелательных реакций в виде тошноты, головной боли, снижения артериального давления. Были описаны случаи развития определенных аутоиммунных заболеваний, а также обострения инфекционных процессов на фоне их длительного применения. На сегодняшний день назначение МАТ остается терапией «избранных», так как широкое использование этих препаратов сдерживается их значительной курсовой стоимостью [11].
Высокая клиническая эффективность препаратов, позволяющих воздействовать на иммунологические механизмы развития псориаза, на сегодняшний день не вызывает сомнений, но остается актуальной проблема разработки новых иммунотропных средств, применение которых наряду с высокой эффективностью будет характеризоваться низким уровнем нежелательных явлений и доступностью для широкого использования в повседневной медицинской практике.
Современное становление российской фармацевтической отрасли в рамках стратегии развития фармацевтической промышленности Российской Федерации (РФ) на период до 2020 г. позволило вывести на рынок ряд высокотехнологичных отечественных фармакологических препаратов, характеризующихся высоким профилем эффективности и безопасности. Следует отметить и их низкую себестоимость, что позволяет значительно снизить курсовую стоимость лечения по сравнению с зарубежными препаратами.
Результатом многолетней напряженной работы стал первый представитель нового поколения синтетических пептидных иммунодепрессантов - Тимодепрессин. Тимодепрессин разработан коллективом исследователей ООО «Фарма Био» в содружестве с Медицинским радиологическим научным центром РАМН (Обнинск) и Институтом иммунологии МЗ РФ (Москва). Препарат разрешен Фармкомитетом Министерства здравоохранения РФ к медицинскому применению в 2000 г. (регистрационное удостоверение номер: Р №000022/01-2000; Р №000022/02-2000; Р №000022/03-2000; Р №000022/04-2000). Тимодепрессин - синтетический дипептид, состоящий из D-аминокислотных остатков глютаминовой кислоты и триптофана.
Тимодепрессин (γ -D-глутамил-D-триптофана динатриевая соль) - индивидуальное химическое соединение пептидной природы, полученное методом химического синтеза в результате структурно-функциональных исследований биологически активных низкомолекулярных пептидов. Выпускается препарат в виде 0,1% раствора для инъекций в ампулах по 1 мл (по 5 ампул в упаковке), а также в виде назального спрея во флаконах по 5 мл (0,5 мг).
Состоящий из неприродных D-аминокислот, соединенных γ -пептидной связью, Тимодепрессин представляет собой новый класс синтетических пептидных препаратов, селективно блокирующих процессы пролиферации клеток-предшественников иммунитета. Специфические свойства препарата Тимодепрессин позволяют избирательно подавлять функциональную активность иммунокомпетентных клеток, тормозить развитие аутоиммунных процессов, не затрагивая клетки других органов и тканей, сводя при этом к минимуму риск возникновения побочных эффектов. Тимодепрессин можно применять как в виде монотерапии, так и в комплексном лечении больных при различных заболеваниях. Препарат разрешен для лечения и профилактики аутоиммунных болезней различного генеза: аутоиммунных первичных и вторичных цитопений, гипопластических анемий, ревматоидного артрита, псориаза; в качестве цитопротекторной терапии для защиты и сохранения стволовых клеток, для предотвращения гранулоцитопении, при цитостатических химиотерапевтических воздействиях.
Вводят препарат Тимодепрессин внутримышечно и интраназально. На начальном этапе лечения препарат назначают системно; курс лечения и режимы дозирования подбирают индивидуально в зависимости от динамики клинических проявлений. Разовая доза составляет 1 мл 0,1% раствора, максимальная разовая доза - 2 мл 0,1% раствора. Препарат вводят ежедневно однократно.
Тимодепрессин применяют у взрослых и детей с двухлетнего возраста, используют как в монотерапии, так и в комплексном лечении и профилактике псориаза: препарат вводят внутримышечно по 1-2 мл раствора ежедневно в течение 7-10 дней, затем 2 дня перерыв, далее цикл повторяют. В зависимости от клинической ситуации можно проводить от 3 до 5 циклов.
Интраназально Тимодепрессин назначают преимущественно в качестве поддерживающей терапии и для профилактики рецидивов, а также при лечении детей. Препарат вводят по 1-2 дозы (0,5 мг) спрея назального в каждый носовой ход ежедневно в течение 7-10 дней, курс лечения может быть продолжен после 2-дневного перерыва.
Пациентам с генерализованной псориатической эритродермией Тимодепрессин вводят внутримышечно по 2 мл раствора ежедневно в течение 14 дней, затем интраназально с одновременным добавлением ГКС в средних дозах.
Сравнительный анализ результатов в рамках отделений, курируемых профессорско-преподавательским составом кафедры дерматовенерологии педиатрического факультета ГБУ ВПО Российского научно-исследовательского медицинского университета им. Н.И. Пирогова, в период с 2000 по 2013 г. продемонстрировал высокую клиническую эффективность включения препарата Тимодепрессин в схемы лечения больных псориазом. Причем выраженность терапевтического действия препарата Тимодепрессин не определялась особенностями клинического варианта псориаза - благоприятные результаты после проведенного лечения с примерно одинаковой частотой прослеживались при различных формах псориаза, что приводило к значительному улучшению качества жизни больных. В отдельных случаях по силе терапевтического ответа и динамике регресса псориатического процесса Тимодепрессин превосходил рутинные методики лечения псориаза. Применение препарата Тимодепрессин не сопровождалось развитием побочных эффектов, присущих известным иммунодепрессантам; кроме того, он удобен в применении как в стационаре, так и в амбулаторной практике.
В статье говорится о воздействии тимохинона содержащегося в масле семян черного тмина на слизистую оболочку полости рта.

4. Zaima Umar, Anas Sarwar Qureshi, Sarmad Rehan. Nigella sativa Boosts Testicular Activity A histologic and endocrinologic study LAP LAMBERT Academic Publishing (2015–01–30).
5. Amita Jaswal, Suchita Raghuvanshi, Sangeeta Shukla / Nigella sativa Linn. ameliorates D-galactosamine / LPS induced hepatitis Hepato-renal Protection LAP LAMBERT Academic Publishing (2015–05–04).
Чёрный тмин (Nigella sativa) растёт во многих странах и является тонколистным, травянистым растением высотой около 40 сантиметров. Он также известен как калинджи или чернушка посевная, сейдана, седана, нигелла и римский кориандр. На протяжении многих столетий его семена широко используются в кулинарии и народной медицине. В последние годы значительно увеличилось число научных исследований его химического состава и целебных свойств. В семенах чёрного тмина содержится около 20 % белка, 40 % углеводов и 35 % растительного масла. Целительные свойства этого растения связаны с эфирными маслами, которые содержатся в его семенах. Среди них самым действенным является вещество тимохинон, извлечённое из семян чёрного тмина. Это вещество было впервые получено в 1960 году профессором Аль-Дахахни. В дополнение к тимохинону, образующему 30–40 % эфирных масел, в семенах тмина содержится, по крайней мере, 15 различных веществ, в том числе тимол, цимол, туйон и о-цимол.
Содержание эфирного масла 2,3 %.
Тимохинон – это противоопухолевый, антиоксидантный, антибактериальный компонент масла черного тмина.
Тимохинон обладает противовоспалительным и болеутоляющим эффектом. Кроме того, было подтверждено его желчегонное действие (стимуляция выработки желчи), что делает его значимым при обмене жиров и детоксикации.
Исследования фармакологического факультета университета Анкары (1985) характеризуют тимохинон как средство, защищающее от приступов астмы и имеющее, бронхолитический и, в некотором роде, антигистаминный эффект. Таким образом, он аналогичен nigellone. Последующие турецкие исследования на базе сельскохозяйственного факультета Университета Эрзурума (1989) доказали антибактериальные и противогрибковые качества эфирного масла черного тмина. Это очень характерно и для тимохинона. Обнаружено, что тимохинон в эфирном масле черного тмина способен снижать концентрацию холестерина и триглицеридов в плазме крови.
Тимохинон ((CH?)?CHC?H? (=O)?CH?) – 2–метил-5–изопропил-1,4–бензохинон. Найден в эфирном масле Monarda fistulosa и Mosla grosserrata вместе с тимогидрохиноном. Очень много тимохинона (до 60 %) содержится в экстрактивном (CO2 – экстракция) эфирном масле Nigella sativa. Предполагается наличие в эфирном масле и сложного комплекса тимохинона и гидрохинона – тимохингидрона. Найдено, что эти соединения обладают антиоксидантными свойствами (прооксидантными – в случае высоких концентраций), а также способны защищать печень от химически-индуцированного повреждения. Тимохинон – кристаллическое вещество с запахом хинона и тимола. На свету медленно превращается в дитимохинон. Используется как антиоксидант в пищевых продуктах.
Согласно заключениям американских онкологов, тимохинон блокирует активность воспалительных цитокинов – таких, как ТНФ-альфа, интерлейкин-1бета, интерлейкин-8, Cox-2 и MCP-1. Также вещество препятствует выражению и синтезу NF-kappaB – фактора, влияющего на развитие воспалительных процессов. Активация этого фактора замечена у больных раком поджелудочной железы, из-за чего раковые клетки становятся устойчивыми к химиотерапевтическим агентам, поясняют терапевты. Испытания свойств тимохинона на организме животных показали, что растительный компонент на 67 % уменьшает объём опухоли и значительно сокращает уровни вредных цитокинов. Врачи возлагают большие ожидания на мощные и, что немаловажно, безопасные эффекты травы в качестве профилактики и терапии не только рака поджелудочной железы, но и рака простаты и толстой кишки.
В лабораторных исследованиях обнаружено, что масло семян черного тмина способно убивать клетки рака простаты. Ученые из Университета Тулейн выявили, что тимохинон (TQ) имеет противораковые свойства, которые подавляют рост и приводят к гибели агрессивные клетки рака простаты. Это открытие произошло врезультате поиска учеными природного средства с противораковыми свойствами. По словам доктора Debasis Mondal, который был в составе исследовательской группы, «Комплементарная и альтернативная медицина (CAM) становится очень важным дополнением терапии больных раком, смягчает побочные эффекты химиотерапии, а также повышает их антиопухолевые свойства».
Исследователи признали, что тимохинон, содержащийся в масле черного тмина (Nigella Sativa) имеет такой же эффект как убихинон или кофермент Q, который также является важным веществом, вырабатываемым организмом. Они обнаружили, что тимохинон быстро генерирует активные формы кислорода (АФК) против особенно агрессивных типов LNCaP и С4–2B клеток рака простаты. В раковые клетках, устойчивых к химиотерапии обнаружены высокие уровни глутатиона (GSH), кторый также снижается под воздействием соединений масла семян.
Предполагается, это совместное индуцирующее и подавляющее действие АФК уровня глутатиона тимохиноном, найденого в масле черного тмина, приводит к гибели клеток рака простаты. Д-р Стивен Р. Гудман, главный редактор Экспериментальной Биологии и Медицины говорит, что исследования «показали, тимохинон эффективно уничтожает гормон-зависимые и независимые раковые клетки простаты. Механизм действия, как представляется, заключается в том, что тимохинон вызывает окислительный стресс и подавляет GSH уровень. Это говорит о том, что окислительный стресс может привести к снижению роста опухоли и увеличению гибели клеток в очень агрессивных формах рака предстательной железы».
Было выявлено, что Тимохинон, найденный в масле семян черного тмина (Nigella Sativa), уничтожает клетки рака поджелудочной железы, рака толстой кишки, и был протестирован на предмет вылечивания рака молочной железы. Лабораторное исследование показало, что тимохинон убивает раковые клетки простаты и может лечить агрессивные формы рака простаты.
О лечебных качествах масла черного тмина было известно еще во времена Ибн Сины и Гиппократа. Официальная медицина заинтересовалась маслом черного тмина в пятидесятых годах девятнадцатого столетия. С тех пор множество лабораторий по всему миру пытается понять, в чем секрет удивительного действия масла черного тмина на человеческий организм. Был изучен химический состав масла черного тмина. Оказалось, что в этом уникальном продукте содержатся те самые полиненасыщенные жирные кислоты омега-6 и омега-3, которые придают замечательные лечебные свойства морепродуктам.
В 1960 году клинически было доказано, что масло черного тмина оказывает противовоспалительный эффект. В 1995 году группа ученых из научно-исследовательской лабораторий фармакологии Королевского Колледжа в Лондоне, проверила эффективность масла чернушки и его производного, тимохинона, как противовоспалительного средства. Ингибирование воспалительной реакции было выше чем могло ожидаться от одного тимохинона. Тогда и обратили внимание на микс эйкозадиеновой, эйкозотриеновой и эйкозеновой кислот, которые отвечают за повышение противовоспалительной активности.
В стоматологии тимохинон используется при лечении и профилактики зубов:
• гигиена полости рта (смазывание слизистых).
Эфирные масла, содержащиеся в семени черного тмина представителя семейства зонтичные , прекрасно освежают дыхание. Поэтому тмин используют для приготовления различных бальзамов и ополаскивателей для ротовой полости. Заживляющие и регенерирующие способности растения позволяют эти настойки эффективно использовать в комплексном лечении стоматитов, гингивитов и флюсов.
Ложку тмина кладете в рот и полощите в течение 2–3 минут. Повторяете несколько раз. В течение 2–3 дней стоматит либо проходит полностью либо исчезают болевые ощущения, остается лишь ранка которая затягивается в течении нескольких дней.
Черный тмин – эффективное средство для снятия зубной боли. Чтобы снять эти неприятные симптомы, достаточно приложить к больному месту тканевый мешочек с теплым тмином и подержать некоторое время.
Рецепты применения тихоменона (черного тмина) при зубных болях:
• полоскать рот смесью тмина и яблочного уксуса.
• смешать молотый черный тмин с оливковым маслом до образования пасты и нанести ее на больной зуб.
• отварить восемь унций яблочного уксуса с двумя столовыми ложками молотого черного тмина. Процедить. Полоскать рот полученной жидкостью в течении нескольких дней.
• растереть больное место (зуб, десну) несколькими каплями черного тмина.
Читайте также:

