Лучевые повреждения кожи при лучевом лечении
Обновлено: 30.04.2024
Как вести больных с солнечным кератозом? Служат ли “кожные рога” признаком злокачественности? Нужно ли удалять и исследовать гистологически кератоксантомы? Большинству чешуйчатоклеточных карцином (ЧКК) кожи предшествуют предраковые образования,
Как вести больных с солнечным кератозом?
Служат ли “кожные рога” признаком злокачественности?
Нужно ли удалять и исследовать гистологически кератоксантомы?
Большинству чешуйчатоклеточных карцином (ЧКК) кожи предшествуют предраковые образования, потенциал озлокачествления которых установлен. К этим предраковым образованиям относятся: лучевой (солнечный) кератоз, лучевой хейлит, болезнь Боуэна, эритроплазия Кейра, мышьяковый, дегтярный и пострадиационный кератозы и, по нашему мнению, кератоксантомы.
Некоторые из этих предраковых состояний, например лучевой кератоз, в ходе естественного развития долго не проявляют признаков клеточных изменений. Другие, такие как болезнь Боуэна, имеют микроскопические признаки внутриэпидермальной карциномы с самого начала. Образование считается злокачественным с момента разрыва или исчезновения базальной мембраны.
Хотя наиболее распространенной формой кожных злокачественных образований является базальноклеточная карцинома (БКК), дальше она обсуждаться не будет, поскольку у нее нет предраковых стадий.
Этиология. К началу нашего века была установлена канцерогенность некоторых химических веществ и радиации. Первым из признанных химических канцерогенов стала копоть, когда Персифаль Поттс отметила высокую заболеваемость раком мошонки у молодых трубочистов. В 1906 году Гайд [2] сообщил, что ультрафиолетовое (УФ) излучение обладает канцерогенными свойствами.
Предположение о связи иммунной системы с некоторыми раковыми заболеваниями было высказано Макфарленом Бюрнеттом [3], автором теории иммунного надзора.
Связь иммунной системы с кожным канцерогенезом хорошо иллюстрируется повышенной заболеваемостью немеланомными раками кожи, встречаемой у пациентов с трансплантантами, и зависимостью между иммуннодефицитом, наблюдаемым у ВИЧ-инфицированных, и различными кожными злокачественными новообразованиями. Остается высоким интерес к роли вирусов папилломы как канцерогенов или ко-канцерогенов для кожи и слизистых оболочек.
 |
| Рисунок 1. Лучевой кератоз проявляется у пожилых пациентов в виде округлых, шелушащихся кератозных, эритематозных образований, как правило, диаметром менее 1 см на коже, подвергающейся солнечному воздействию |
Изредка рак кожи может развиваться на местах застарелых рубцов, свищей и язв.
Лучевые кератозы. Клинически кератозы проявляются у пожилых пациентов в виде округлых шелушащихся кератозных, эритематозных образований, как правило, диаметром менее 1 см на коже, подвергающейся солнечному воздействию (рис. 1). Наиболее часто поражаются лицо, уши, скальп, тыл кистей и предплечья.
Географическая распространенность заболевания зависит от количества УФ-излучения, достигающего земли в рассматриваемой области, доли белокожего населения, времени, проводимого в помещении на работе и на отдыхе. В Австралии лучевой кератоз обнаруживается у 40-50% человек старше 40 лет [4]. Латентный период длится до десяти лет. ЧКК, развивающиеся при этом кератозе, растут медленно и, за исключением расположенных на ушах и губах, почти не метастазируют. Озлокачествление предполагается при уплотнении основания кератоза и увеличении васкуляризации и воспалении дермы.
Гистологически при лучевом кератозе выявляется эпителиальная дисплазия различной степени, которая обычно охватывает и придаточные структуры. Поверхностные повреждения удаляются быстрым замораживанием жидким азотом в течение 10 секунд. Разрушение прижиганием или диатермокоагуляцией, следующее за выскабливанием роговых образований, не менее эффективно, но чаще оставляет поверхностные рубцы. Индуративные зоны лучше иссечь. При солнечных кератозах не применяют радиотерапию.
В случае если большая часть поверхности кожи покрыта многочисленными кератозами, может помочь назначение местного 5-флюороурацила. Его наносят дважды в день в течение двух недель, затем делают двухнедельный перерыв и вновь повторяют курс. Если развивается тяжелое воспаление, применяют сильные местные кортикостероиды.
Меры профилактики, такие как избегание пребывания на солнце в разгаре дня, ношение шляпы с широкими полями и использование эффективного солнечного экрана, стоит применять как для лечения, так и для предотвращения развития хейлита.
Лучевые хейлиты. Это заболевание представляет собой лучевой кератоз красной каймы нижней губы. Его вызывает воздействие солнечного света. Курение и хроническое раздражение также способствуют развитию лучевого хейлита. Заболевание характеризуется появлением сухих, белесых, серых шелушащихся бляшек, в которых могут развиваться области эритемы, эрозий и изъязвлений. В прошлом белесоватые области назывались лейкоплакией.
ЧКК, как правило, развиваются спустя длительный латентный период и ведут себя более агрессивно по сравнению с развивающимися из обычного лучевого кератоза. Как и в случае последнего, при лучевом хейлите гистологические изменения состоят в появлении областей ортокератоза и паракератоза с нарушенным созреванием клеток эпидермиса, в повышенной митотической активности и различных цитологических нарушениях. Хороший результат достигается при срезании поврежденной области бритвой, захватывая поверхностные слои кожи. С недавнего времени успешно применяют СО2-лазер.
“Кожные рога”. “Кожный рог“ может располагаться в области диспластического или неопластического эпителия. Роговые пробки и наросты иногда вызываются другими изменениями эпителия, например вирусными бородавками, контагиозным моллюском, кератоксантомами, себоррейным кератозом или БКК.
Таким образом, “кожный рог“ скорее является клиническим маркером патологических изменений в подлежащем эпителии, чем собственно диагнозом. Обычно такие “рога” располагаются на открытых солнцу частях тела, например на лице и кистях рук (рис. 2).
 |
| Рисунок 2. “Кожные рога” указывают на области диспластического или неопластического эпидермиса |
Болезнь Боуэна. Это клиническое выражение ЧКК кожи in situ [5]. Она проявляется в виде асимптомного, хорошо отграниченного эритематозного шелушащегося пятна, центробежно расширяющегося (рис. 3). Различают бородавчатый, узловатый, эрозированный и пигментированный варианты. Проявления болезни Боуэна могут быть одиночными и множественными и локализоваться в любой области кожи или слизистых оболочек.
 |
| Рисунок 3. Проявления болезни Боуэна могут быть одиночными и множественными в любой области кожи или слизистых оболочек |
Изъязвление, как правило, служит признаком инвазивного роста и может на годы отставать от внутриэпителиальных изменений. Инвазивная ЧКК развивается у 8% нелеченых больных.
Инвазивная опухоль обладает 13-процентным метастатическим потенциалом. Заболевание необходимо отличать от простого лишая, псориаза и других папулосквамозных дерматозов. В неясных случаях, а также при малой эффективности местных стероидов следует подозревать болезнь Боуэна. Поверхностный тип БКК очень похож с виду на болезнь Боуэна, но, как правило, ее можно отличить по чуть приподнятому, как порог, краю.
Иногда не удается отличить эти образования от типичного плоского себоррейного кератоза. В сомнительных случаях проводят биопсию для определения полной толщины дисплазии эпидермиса и иногда волосяных фолликулов и сальных желез.
Эффективно разрушение эпидермиса замораживанием, прижиганием или диатермокоагуляцией. Для достижения наилучших результатов можно местно применить цитотоксические вещества, такие как 5-флюороурацил. Нередко встречаются рецидивы, в основном вследствие захвата карциномой придаточных структур, которые не были затронуты в процессе лечения. Если образование не слишком обширно, лучше всего произвести хирургическое иссечение.
Эритроплазия Кейра. Это заболевание представляет собой ЧКК in situ полового члена. Оно проявляется на головке полового члена, не подвергавшегося обрезанию, в виде четко очерченных, асимптоматичных ярко-красных блестящих и бархатистых бляшек (рис. 4). Подобные образования могут также поражать венечную борозду или внутреннюю поверхность крайней плоти.
 |
| Рисунок 4. Эритроплазия Кейра чаще всего развивается на головке полового члена, не подвергавшегося обрезанию |
Как и при болезни Боуэна, инвазивная карцинома может развиваться в 10% случаев; она обладает метастатическим потенциалом. Гистологические изменения те же, что и при ЧКК in situ. Лечение состоит в обрезании и криотерапии оставшихся образований. Конечно, необходимо тщательное наблюдение за такими пациентами.
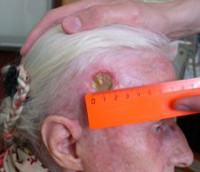
Кератоксантома. Это быстрорастущая опухоль кожи, развивающаяся на области, подвергающейся солнечному воздействию (рис. 5). Типичная кератоксантома представляет собой гладкий кожный узелок, вырастающий за несколько недель до размера 10-20 мм с роговой пробкой в центре. Затем рост прекращается и в течение трех месяцев может происходить обратное развитие образования.
 |
| Рисунок 5. Кератоксантома — это быстрорастущая опухоль кожи, развивающаяся на области, подвергающейся солнечному воздействию |
В прошлом оставался неясным вопрос, считать ли кератоксантомы доброкачественным или предраковым состоянием; в настоящее время мнения большинства специалистов склоняются в пользу последнего. Лечение состоит в выскабливании или широком иссечении и последующем гистологическом исследовании.
Мышьяковый и дегтярный кератоз. Более века неорганический мышьяк применяли при лечении множества различных состояний, пока не были обнаружены его побочные эффекты. Постепенно его заменяли более эффективными терапевтическими агентами, что привело к значительному уменьшению заболеваний, вызванных мышьяком.
Однако в питьевой воде некоторых мировых регионов, в частности в Южной Америке, а также в натуропатических лекарственных средствах обнаруживается высокая концентрация мышьяка. У более чем 40% пораженных людей развивается кератоз ладоней и подошв (рис. 6). У них чаще развиваются множественные раки кожи, включая болезнь Боуэна, БКК и ЧКК [6]. Могут обнаруживаться злокачественные опухоли внутренних органов, особенно легких и мочеполовой системы.
 |
| Рисунок 6. Мышьяковые кератозы развиваются на ладонях и подошвах в более чем 40% случаев |
Кожные образования, в виде мелких кератозных бляшек на лице и руках, наблюдаются у тех, кто работает с дегтем и смолой. Как правило, они исчезают при прекращении контакта с указанными веществами, однако могут иногда долго сохраняться и озлокачествляться, особенно на мошонке.
 |
| Рисунок 7. Пострадиационный кератоз может развиваться в области рубца, вызванного радиотерапией или избыточной флюороскопией |
Множественность мышьякового и дегтярного кератоза делает бессмысленным радикальное лечение. В этом случае могут помочь кератолитические присыпки и притирания. Периодически нужно обследовать пациента на предмет озлокачествления.
Пострадиационный кератоз может развиваться в области рубца, вызванного радиотерапией или избыточной флюороскопией. Он обнаруживается у радиологов, хирургов, дантистов и всех тех, кто бесконтрольно подвергает свою кожу частому воздействию малых доз рентгеновского излучения, хотя в настоящее время число таких случаев уменьшается.
Гистологически изменения эпидермиса подобны лучевому кератозу, в дерме коллаген активно заменяется рубцовым и гиалиновым материалом (рис. 7). Как и в других случаях дисплазии, необходимо адекватное лечение и тщательное наблюдение за пациентом.
Лучевые реакции и повреждения – патологические изменения, возникающие в результате воздействия ионизирующей радиации при проведении лучевой терапии в ходе лечения онкологических заболеваний. Могут быть общими и местными, легкими и тяжелыми, острыми или отдаленными. Поражают различные органы и системы. Наиболее частым проявлением лучевых реакций становятся характерные воспалительные изменения. Симптомы определяются областью поражения. Диагноз выставляется с учетом анамнеза, данных осмотра, КТ, МРТ, УЗИ, рентгенографии и других методик. Лечение - противовоспалительная терапия, витаминотерапия, физиотерапия, анальгетики, иммуностимуляторы и другие средства.
Общие сведения
Лучевые реакции и повреждения – обширная группа патологических состояний различных органов и систем, возникающих у онкологических больных на фоне лучевой терапии или через некоторое время после ее окончания. Рассматриваются как осложнения лучевой терапии. Различаются по степени выраженности, обратимости и необходимости проведения лечебных мероприятий. Лучевые реакции являются обратимыми патологическими процессами, проходят самостоятельно или после соответствующей терапии. Не оказывают отрицательного влияния на качество последующей жизни больных.
В отличие от лучевых реакций, лучевые повреждения относятся к категории необратимых изменений, однако могут в определенной степени компенсироваться после проведения лечения. Ухудшают состояние пациентов, могут становиться причиной инвалидности и негативно влиять на продолжительность жизни. Лечение лучевых реакций и повреждений осуществляют специалисты в сфере онкологии, гастроэнтерологии, дерматологии, урологии и других областей медицины (в зависимости от локализации патологического процесса).

Причины развития лучевых реакций
Вероятность возникновения лучевых реакций определяется дозой ионизирующего излучения, площадью облучения, временем облучения и уровнем радиочувствительности облучаемых тканей. Самой низкой толерантностью к облучению обладает костный мозг. Высокая радиочувствительность также выявляется у лимфатической системы, яичек и яичников, поэтому перечисленные органы и системы чаще всего страдают при проведении лучевой терапии. Кроме того, к числу часто встречающихся лучевых реакций относятся патологические изменения кожи, что обусловлено как ее достаточно высокой чувствительностью, так и попаданием кожных покровов в зону облучения при лечении большинства онкологических заболеваний.
К числу факторов, увеличивающих риск развития лучевых реакций, относятся повышенная индивидуальная радиочувствительность, ошибки при планировании и проведении лучевой терапии. Толерантность тканей к ионизирующему излучению может снижаться при кахексии, ожирении, аллергии, хронических воспалительных заболеваниях, болезнях кожи, сахарном диабете, диффузном токсическом зобе, гипокортицизме и болезнях почек. Вероятность возникновения лучевых реакций повышается в молодом и старческом возрасте, при переохлаждении, перегревании, чрезмерных физических нагрузках, травматических повреждениях, нарушениях целостности или нормального состояния кожи (при царапинах, расчесах, раздражении после использования местных препаратов раздражающего действия или проведения физиотерапевтических процедур).
Классификация лучевых реакций
Выделяют общие и местные лучевые реакции. При местных реакциях наблюдаются патологические изменения в области облучения, при общих страдают система кроветворения, ЦНС, сердечно-сосудистая система, другие органы и системы. Местные и общие лучевые реакции могут быть легкими и тяжелыми; острыми (наблюдающимися в течение нескольких дней или недель с момента облучения) и отдаленными (возникающими спустя месяцы и годы после окончания терапии). Различают четыре варианта лучевых реакций:
- Реакции, непосредственно связанные с облучением
- Отдаленные соматические реакции и поражения
- Генетические нарушения
- Тератогенные эффекты.
Генетические нарушения возникают в результате лучевого воздействия на яички или яичники. Проявляются внутриутробной смертью или врожденными пороками развития ребенка пациента (доминантная мутация) либо его потомков через несколько поколений (рецессивная мутация). Тератогенные эффекты отмечаются при проведении лучевой терапии в период беременности. Возможны аномалии развития конечностей, микроцефалия, гидроцефалия и другие врожденные уродства.
Виды лучевых реакций и повреждений
Общие лучевые реакции
Наиболее распространенной лучевой реакцией является так называемое лучевое «похмелье», которое проявляется слабостью, эмоциональной лабильностью, нарушениями сна, потерей аппетита, тошнотой, рвотой, учащением сердцебиения, гипотонией либо неустойчивостью АД. По анализам крови больных с этой лучевой реакцией определяются тромбоцитопения и лейкопения, иногда – в сочетании с анемией. Средствами профилактики являются белковая диета, обильное питье, употребление овощей и фруктов, прогулки, витамины, антиоксиданты и антигистаминные средства. Лечение лучевой реакции симптоматическое.
Реже возникает острая или хроническая лучевая болезнь, в развитии которой можно выделить четыре фазы: первичной общей реакции, мнимого благополучия, ярко выраженных симптомов и восстановления. Первая фаза проявляется слабостью, сонливостью, головной болью, тошнотой, рвотой, сухостью во рту, иногда – колебаниями пульса и АД с тенденцией к снижению. В фазе мнимого благополучия состояние больного улучшается, сохраняется лабильность пульса и артериального давления. В последующем наблюдаются прогрессирующие облысение, неврологические нарушения, лейкопения и другие изменения системы крови.
В фазе выраженных симптомов на первый план выходят поражения системы крови в сочетании со снижением иммунитета, инфекциями, геморрагическим синдромом и аутоинтоксикацией. Возникает клиническая картина, напоминающая септическое состояние. В фазе восстановления отмечается регрессия симптомов болезни. Лечение – дезинтоксикация, антибактериальная терапия, гемостатики, инфузионная терапия. В тяжелых случаях показана трансплантация костного мозга.
Лучевые реакции и повреждения кожи
Наиболее легким вариантом лучевой реакции кожи является эритема, сопровождающаяся зудом и локальной гиперемией. Выздоровление наступает самостоятельно. В качестве следующих стадий заболевания рассматривают сухой и влажный радиодерматит (лучевой дерматит). При сухом радиодерматите наблюдается гиперпигментация, выраженная гиперемия, отек, выпадение волос, шелушение и нерезкие боли. Как и эритема, данная лучевая реакция не требует проведения специальной терапии. Могут использоваться нейтральные растительные масла. При влажном радиодерматите к перечисленным выше симптомам добавляются отслойка эпидермиса и интенсивные боли. Лечение лучевой реакции – гормональные мази, мази с антибиотиками. В исходе наблюдаются атрофия кожи, исчезновение волос, нарушения пигментации и телеангиоэктазии.
К лучевым повреждениям кожи относятся лучевая язва и лучевой рак. Лучевая язва представляет собой дефект кожи с плотными приподнятыми бугристыми краями. Кожа вокруг язвы уплотнена. На дне язвы – фибрин, гной и некротические массы. В отличие от кожных лучевых реакций, самостоятельное выздоровление невозможно, наблюдается склонность к рецидивам. Возможна трансформация в лучевой рак. Лечение – как при влажном дерматите. При неэффективности консервативной терапии выполняют иссечение язвы и кожную пластику.
Лучевые реакции и повреждения легких и пищевода
Лучевые реакции и повреждения легких возникают при лучевой терапии онкологических заболеваний молочной железы, пищевода, легких и средостения. Могут быть острыми (пневмонит) или хроническими (пневмосклероз). При пневмонитах наблюдаются сухой кашель, одышка и гипертермия. На рентгенограммах определяется усиление легочного рисунка с последующим образованием очагов затемнения. Клинические проявления лучевой реакции исчезают через 1-2 недели, рентгенологические – через 2-3 месяца.
Пневмосклероз развивается через несколько месяцев после завершения курса лечения. Проявляется сухим кашлем, болями и нарастающей одышкой. Вызывает сердечно-легочную недостаточность. На рентгенограммах видны множественные линейные тени. Лечение пневмонита и пневмосклероза – антибиотики, противогрибковые средства, бронхолитики, антигемокоагулянты, витаминотерапия, ЛФК.
Лучевые реакции и повреждения пищевода возникают при тех же заболеваниях, что и аналогичные поражения легких. Проявляются болями при приеме пищи. Лечение – спазмолитики, масло облепихи и раствор новокаина внутрь.
Лучевые реакции и повреждения мочевого пузыря и прямой кишки
Поражения данной локализации возникают при лучевой терапии новообразований прямой кишки, шейки матки и мочевого пузыря. Лучевые реакции могут быть ограниченными или диффузными, развиваться в период проведения лучевой терапии или после ее окончания. Наиболее частым осложнением со стороны мочевого пузыря является цистит. Легкие формы цистита выявляются у большинства больных с неоплазиями мочевого пузыря и у 30-40% пациентов с опухолями близлежащих органов. Сопровождаются болями при мочеиспускании. Все проявления лучевой реакции редуцируются в течение нескольких недель. Тяжелые циститы встречаются реже, проявляются гематурией и резкой болезненностью. Склонны к продолжительному течению и рецидивированию, возможно сморщивание органа. Лечение – прием большого количества жидкости, дезинфицирующие препараты, мочегонные средства.
Самой распространенной лучевой реакцией прямой кишки является острый ректит, обычно возникающий перед завершением курса лечения. Наблюдаются ректальные кровотечения, при ректороманоскопии выявляются отечность и гиперемия слизистой. Все симптомы лучевой реакции исчезают через несколько недель. В тяжелых случаях развивается язвенный лучевой проктит, проявляющийся нарушениями стула, кровотечениями, примесями слизи и крови в кале, мучительными ложными позывами, интенсивными болями при дефекации и тупыми болями в остальное время. Отмечается склонность к хронизации и рецидивированию. Лечение лучевых реакций и повреждений прямой кишки – диетотерапия, клизмы, свечи с анальгетиками, антибактериальными и гормональными препаратами.
Лучевой дерматит (радиационный или рентгеновский дерматит) — это воспалительные изменения, происходящие в коже в результате воздействия ионизирующего излучения. Клинические проявления лучевого дерматита зависят от дозы облучения. В остром периоде возможно покраснение, возникновение пузырей и образование плохо заживающих язв. В более позднем периоде возникает сухость и атрофические изменения, может развиться рак кожи. Характерная клиническая картина и четкая связь возникновения заболевания с ионизирующим излучением обычно не вызывает сомнений в постановке диагноза.
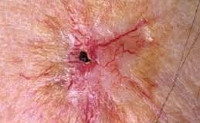
Общие сведения
В наше время лучевой дерматит может возникать в связи с профессиональной деятельностью (у рентгенологов) и при аварийных ситуациях. Он также может быть терапевтическим, то есть развившимся в результате лучевой терапии, которая применяется в лечении злокачественных опухолей и некоторых болезней кожи.

Симптомы лучевого дерматита
Повреждения кожи ионизирующим излучением делят на ранние и поздние. Ранние проявляются в период облучения или в течение 3-х месяцев после него. Поздние повреждения кожи могут развиваться спустя годы после лучевого воздействия. Между ранними и поздними лучевыми повреждениями существует промежуточный период длительностью от нескольких месяцев до многих лет.
Облучение кожи в дозе 12-20 Гр приводит к развитию буллезной формы лучевого дерматита. Она возникает на фоне покраснения, зуда, болезненности, отечности кожи и характеризуется появлением серозных пузырей. Когда пузыри вскрываются, на их месте образуются эрозии, которые покрываются корками и заживают в течение 2-3 месяцев. Буллезный лучевой дерматит сопровождается увеличением регионарных лимфоузлов, повышением температуры тела и выпадением волос.
При дозе облучения более 25 Гр развивается некротическая форма лучевого дерматита. Она сопровождается выраженными болями, высокой температурой, слабостью, бессонницей. Тяжесть состояния пациента зависит от площади пораженного участка кожи. Кожные проявления проходят от стадии покраснения и пузырей до образования длительно незаживающих язв. Причем язвы могут возникать в обход буллезной стадии.
Хронический лучевой дерматит может быть следствием острого или развивается первично в результате многократного воздействия на кожу малых доз ионизирующего излучения. Его возникновению способствуют повышенная инсоляция, сахарный диабет, воздействие на кожу химических раздражителей, сосудистая патология, гнойная инфекция и др. К проявлениям хронического лучевого дерматита относятся: сухость кожи, образование трещин, гиперкератоз, участки гипо- и гиперпигментации, атрофические лучевые язвы.
Лечение лучевого дерматита
Лечение эритематозной формы лучевого дерматита проводится кортикостероидными кремами. При буллезной и некротической формах показано купирование болевого синдрома и противовоспалительная терапия. Пузыри вскрывают или отсасывают их содержимое. Для улучшения заживления эрозий и язв применяют кортикостероидные мази и 10% метилурациловую мазь. Некротическая форма дерматита часто требует хирургического иссечения некротизированного участка.
Хронический лучевой дерматит с невыраженной кожной атрофией не нуждается в активном лечении. Необходимым является исключение раздражающих факторов и применение питательных кремов. При выраженной симптоматике назначают противовоспалительные и эпителизирующие средства (кортикостероидные мази, препараты из сыворотки крови молочных телят и др.). При образовании длительно незаживающей лучевой язвы показано ее иссечение.
Прогноз при лучевом дерматите
На фоне хронического лучевого дерматита может начаться развитие базалиомы или плоскоклеточного рака кожи. Примерно в половине случаев это происходит через 7-12 лет после многократного и длительного облучения. Однако возникновение подобных осложнений может наблюдаться и через десятки лет.
Лучевой проктит - это воспаление прямой кишки, развивающееся на фоне радиационной терапии рака тазовых органов. Местные симптомы включают болезненность в проекции прямой кишки, слизистые, гнойные или кровянистые выделения из анального отверстия. Кроме локальных проявлений лучевой проктит может сопровождаться общими симптомами: повышением температуры тела и выраженной слабостью. Для диагностики заболевания используется общий анализ крови, ректоскопия и исследование мазка со стенки прямой кишки. Лечение заключается в проведении местных противовоспалительных процедур, назначении антибактериальной терапии, антигистаминных препаратов и витаминотерапии.
МКБ-10
Общие сведения
Лучевой проктит представляет собой неспецифический воспалительный процесс, развивающийся в слизистой оболочке прямой кишки. Основной причиной заболевания является воздействие ионизирующей радиации при проведении лучевой терапии по поводу рака органов малого таза. Лучевой проктит является наиболее распространенной формой радиационного поражения кишечника, встречающейся в клинической проктологии. Поскольку около 60% пациентов с онкопатологией органов малого таза получают лучевую терапию, распространенность поражения прямой кишки у данной группы больных очень высока: лучевой проктит диагностируют примерно у 12% лиц, получающих радиационное лечение. Основная проблема, с которой приходится сталкиваться проктологам, наблюдающим таких пациентов, это частое развитие постлучевых стриктур прямой кишки, требующих оперативного вмешательства.

Причины
Лучевой проктит всегда является осложнением радиационной терапии онкопатологии органов малого таза. Чаще всего данное состояние развивается после проведения контактной гамма-терапии рака шейки и рака тела матки с использованием изотопов тория, реже – при применении чистого радия. Также лучевой проктит может быть следствием рентгенотерапии и дистанционной гамма-терапии рака органов малого таза. Радиационное повреждение прямой кишки возникает в том случае, когда суммарная очаговая доза излучения превышает 50 Гр (это толерантная доза, при которой частота поздних осложнений составляет около 5%). Вероятность патологии напрямую коррелирует с дозой облучения: риск развития лучевого проктита возрастает до 50% уже при показателе 65 Гр.
Воздействие радиационного излучения приводит к нарушению процессов пролиферации и созревания эпителия прямой кишки, к десквамации и атрофии клеток. Развивается неспецифическое воспаление слизистой и подслизистого слоя, в процесс может быть вовлечен и мышечный слой. Спустя несколько месяцев после лучевой терапии формируется воспалительный процесс в артериолах прямой кишки, приводящий к хроническому нарушению кровообращения в данной области, трофическим изменениям и рубцовому стенозированию. Недостаточная микроциркуляция часто становится причиной некрозов, язв, которые могут осложниться кровотечением, перфорацией, формированием свищей прямой кишки.
Классификация
В зависимости от сроков развития лучевой проктит классифицируют на ранний (возникает в первые 3 месяца после радиотерапии) и поздний (возникает позднее указанного срока). По характеру морфологических изменений, происходящих в прямой кишке, различают катаральный, эрозивно-десквамативный, некротический и инфильтративно-язвенный процесс. Отдельно выделяются такие осложнения лучевого проктита, как рубцовый стеноз, ректовезикальные и ректовагинальные свищи.
Симптомы лучевого проктита
Основным проявлением ранней формы заболевания являются болезненные позывы на дефекацию. Боль носит приступообразный характер и усиливается после опорожнения кишечника. Также пациентов может беспокоить зуд и дискомфорт в области заднего прохода. Из прямой кишки зачастую выделяется слизь, что является признаком воспаления слизистой оболочки кишечника. Иногда имеют место кровянистые выделения, указывающие на тяжелое течение заболевания. Помимо местных симптомов, лучевой проктит сопровождается общими клиническими проявлениями, такими как слабость и повышение температуры тела. Все симптомы ранней формы патологии обычно регрессируют спустя несколько дней после окончания противоопухолевой терапии. Однако через определенное время лучевой проктит может рецидивировать, а клиническая симптоматика часто возвращается в прежнем объеме.
Поздние лучевые поражения кишечника развиваются примерно в 10% случаев. При этом латентный период (промежуток времени между облучением и возникновением симптоматики) может длиться от нескольких недель до 5-10 лет. Характерны постоянные боли в области прямой кишки, частый стул небольшими порциями, а также развитие стеноза с явлениями частичной непроходимости. Возможно малосимптомное течение поздней формы лучевого проктита. В таком случае заболевание проявляется наличием слизи в кале и периодическим болевым синдромом в левой подвздошной области и в проекции прямой кишки.
На фоне лучевого проктита могут развиваться различные осложнения: кишечное кровотечение, язвы и эрозии, стеноз прямой кишки. Именно стриктура кишечника считается наиболее грозным и неблагоприятным осложнением с точки зрения прогноза. Если на фоне лучевой терапии рака органов малого таза у больного появляются слизистые или кровянистые выделения из анального отверстия, сопровождающиеся тенезмами и болью в области прямой кишки, это позволяет заподозрить лучевой проктит.
Диагностика
При появлении признаков лучевого проктита на фоне проведения радиотерапии пациента сразу же направляют к врачу-проктологу. Для диагностики данного заболевания используются клинические, лабораторные и инструментальные методы. Обследование начинается с объективного осмотра и выяснения жалоб. При лучевом проктите всегда прослеживается связь с проведением лучевой терапии. Из лабораторных методов применяется общий анализ крови, в котором, как правило, отмечаются воспалительные изменения, такие как лейкоцитоз, ускорение СОЭ и палочкоядерный сдвиг влево. Лабораторные диагностические методики позволяют определить степень тяжести воспаления, но они не могут применяться непосредственно для постановки диагноза лучевого проктита.
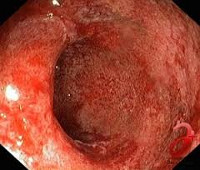
Ключевую роль в диагностике заболевания играет эндоскопия. Наиболее простым, доступным и информативным методом считается ректороманоскопия. При проведении этого исследования врач обнаруживает покраснение, отек слизистой и гиперпродукцию слизи в прямой кишке. Кроме того, методика позволяет выявить изменения, характерные для таких осложнений, как кровотечение, абсцедирование, образование язв. Язвы, как правило, локализуются на передней стенке прямой кишки; в ряде случае они могут приводить к формированию свищей. При ректоскопии обязательно проводится биопсия слизистой оболочки прямой кишки. Она дает возможность уточнить степень тяжести воспалительных и атрофических изменений слизистой. С целью определения наличия инфекционного агента проводится бактериологическое исследование мазка из прямой кишки.
Вследствие того, что симптомы лучевого проктита имеют много общего с неспецифическим язвенным колитом, основная дифференциальная диагностика должна проводиться между этими двумя заболеваниями. В пользу проктита свидетельствует факт проведения лучевой терапии в анамнезе. Кроме того, лучевой проктит отличает наличие язв на передней стенке и в средней трети прямой кишки. В то же время, при этом заболевании крайне редко поражается задняя стенка и нижняя часть прямой кишки. При неспецифическом язвенном колите воспалительные изменения являются диффузными и поражают весь ректальный отдел кишечника. Для окончательной дифференциальной диагностики между этими двумя заболеваниями используется биопсия.
Лечение лучевого проктита
При лечении лучевого проктита важно уменьшить негативное влияние ионизирующего излучения, которое приводит к запуску лучевых реакций. Больным назначают витамин С, витамины группы В, а также антигистаминные препараты, такие как хифенадин, клемастин, лоратадин и другие. При наличии выраженного воспаления и идентификации инфекционного возбудителя проводят антибактериальную и противовоспалительную терапию (в том числе, с использованием сульфаниламидных средств, глюкокортикоидов и облепихового масла).
Местная терапия является важным компонентом комплексного лечения лучевого проктита. Данный вид помощи в первую очередь предусматривает очищение кишечника и ликвидацию локальных воспалительных процессов: в период обострения пациентам показаны клизмы с раствором колларгола или отваром ромашки. Эффективными считаются масляные микроклизмы на основе рыбьего жира или винилина. Эти процедуры проводят после использования слабительных средств или очистительных клизм. Хороший эффект при лечении лучевого проктита дает теплый душ в области прямой кишки или сидячие ванны с использованием перманганата калия. Также целесообразно местное лечение глюкокортикостероидами, ректальными суппозиториями с месалазином и анестетиками.
В комплексной терапии лучевого проктита важную роль играет правильное питание. Диета при данном заболевании предусматривает полное исключение острой, соленой и кислой пищи, а также алкоголя, ограничение растительной пищи и сладких продуктов. Пищевой рацион при лучевом проктите должен содержать нежирное мясо, супы на бульонах без жира и кисломолочные продукты. Если симптомы заболевания регрессируют на фоне эффективного лечения, то диета может быть расширена. При развитии осложнений, таких как формирование свищей и сужений кишечника, используются хирургические методы лечения, в том числе реконструктивные вмешательства на прямой кишке.
Прогноз и профилактика
При лучевом проктите прогноз в основном благоприятный. Тяжелое течение патологии отмечается при сочетании поражения нескольких отделов кишечника, развитии осложнений в виде свищей, кровотечений. Своевременное комплексное лечение позволяет уменьшить вероятность возникновения обострений. Профилактика лучевого проктита заключается в использовании современных методик и протоколов лечения онкозаболеваний органов малого таза, которые оказывают меньший негативный эффект на здоровые ткани.
1. Лучевые ректиты при комплексном лечении рака органов малого таза (обзор литературы) / Клименко К.А., Цаллагова З.С. // Вестник Российского научного центра рентгенорадиологии Минздрава России - 2014-
2. Лучевые повреждения прямой кишки и мочевого пузыря у больных раком шейки матки / Жариков Г.М., Винокуров В.Л., Заикин Г.В. // Мир медицины - 2000 - №7-8
3. Радиационные (лучевые) поражения кишечника / Бурковская В.А. // Гастроэнтерология Санкт-Петербурга - 2013 - №3-4
Местные лучевые повреждения, развивающиеся преимущественно при лучевой терапии злокачественных опухолей, отличаются торпидностью к лечению различными медикаментозными средствами. Лучевые повреждения покровных тканей (кожи, слизистых) и внутренних органов
Местные лучевые повреждения, развивающиеся преимущественно при лучевой терапии злокачественных опухолей, отличаются торпидностью к лечению различными медикаментозными средствами. Лучевые повреждения покровных тканей (кожи, слизистых) и внутренних органов, как следствие воздействия ионизирующего излучения в суммарной очаговой дозе 60—70 Гр., проявляются в виде хронических эпителиитов и дерматитов, с прогрессированием их в лучевые язвы кожи, лучевые проктиты, циститы и т. п. В патогенезе таких повреждений, наряду с нарушением микроциркуляции, ведущее значение играет прямое воздействие излучения на клетки и подавление репаративных процессов. В дальнейшем на передний план выходят присоединение инфекции поврежденных тканей и усугубление негативных процессов заживления поврежденных тканей [1]. Вот почему в комплекс медикаментозных средств при лечении местных лучевых повреждений включаются вещества, воздействие которых направлено на улучшение тканевой микроциркуляции, повышение репараторных процессов и подавление инфекционного процесса. Для лечения местных лучевых повреждений апробированы практически все известные медикаментозные средства, удовлетворяющие перечисленным требованиям. Низкая терапевтическая эффективность имеющихся средств явилась основанием для поиска новых методов лечения. В отделении лечения лучевых повреждений МРНЦ РАМН ежегодно проходит лечение значительное число больных с лучевыми язвами конечностей и других областей тела, лучевыми повреждениями кишечника, мочевого пузыря и др. Основным компонентом местного лечения является препарат димексид (диметилсульфоксид, или ДМСО), применяющийся в виде перевязок раствора 5—10% или мази 10%. Это базовое лечение, назначаемое с учетом конкретных особенностей каждого больного, может дополняться назначением других антисептиков (диоксидин, хлоргексидин и др.), протеолитических ферментов, средств, стимулирующих репараторные процессы (куриозин, витаминизированные масла и др.). Разработанные схемы местного и общего лечения позволяют добиться благоприятных результатов у 57% пациентов [1, 2].
С сентября 2002 г. мы исследовали терапевтическую эффективность препарата гепон для лечения больных местными лучевыми повреждениями (см. таблицу 1).
Лучевые язвы у больных развились после лучевой терапии злокачественных опухолей (рак кожи — 16 пациентов, рак молочной железы — шесть, саркомы — четыре). Суммарная очаговая доза (СОД) составляла 45—70 Гр. Лучевые проктиты явились следствием лучевой терапии рака шейки и тела матки (13), рака мочевого пузыря (3) и прямой кишки (2). Лучевые циститы также наблюдались после лучевой терапии рака шейки и тела матки (13) и рака мочевого пузыря (4). Пневмофиброз — это следствие лучевой терапии лимфогранулематоза (6) и рака молочной железы (5 больных).
При лечении лучевых язв гепон применялся на первом этапе (7—10 дней) в виде орошения язвы раствором. Гепон (0,002) растворяли перед употреблением в 5 мл стерильного физиологического раствора. Орошение полученным раствором 0,04% гепона производилось ежедневно. На втором этапе, по мере развития грануляции, применялась мазь 0,04% (10—18 дней). Результаты лечения лучевых язв гепоном сопоставлялись с динамикой течения раневого процесса у более 800 больных, которым терапию проводили с принятыми в отделении методами лечения, состоящими в местном применении раствора 10% димексида (аппликации или электрофорез), электрофореза протеолитических ферментов и гепарина, использовании мазей левомиколя, ируксола, куриозина и эплана.
Эффективность применения гепона оценивалась клинически по состоянию раневой поверхности (уменьшение экссудации, скорости развития грануляций и скорости эпителизации язвы по Л. Н. Поповой (см. таблицу 2)), исчисляемой по формуле:
В оценке динамики заживления информативным оказалось изучение микрофлоры лучевых язв и чувствительности ее к антибиотикам. До применения гепона в раневом отделяемом у 67,5% посевов была установлена моноинфекция, преимущественно ассоциации стафилококка, а у 16,3% определялись и другие микробы (Escherichia coli, грамотрицательные ассоциации микробов и Candida). После 12–15-дневного применения гепона в 18,9% случаев выявлялась стерильность либо определялись сапрофиты (27%), характерные для нормальной кожи. По сравнению с исходным уровнем, 10 7-8 микробов на грамм ткани, к концу лечения гепоном обсемененность сокращалась до 10 2-3 , значительно повышалась чувствительность флоры к антибиотикам. Все вышеуказанное свидетельствует о несомненной эффективности проведенного лечения.
Положительный терапевтический эффект использования гепона мы склонны связывать в первую очередь с благоприятным его действием на микрофлору, что способствовало снижению воспалительного процесса и его негативных последствий (отек окружающих тканей, нарушение микроциркуляции и т. п.). Кроме того, важным аспектом действия гепона является его иммуномоделирующее действие, проявляющееся в активизации секреторного иммуноглобулина, снижении уровня противовоспалительных цитокинов, активизации a-интерферона, снижении адгезивной функции клеток и их апоптоза, прекращении вирусной репликации и повышении резистентности организма к бактериальной флоре.
В настоящее время, когда ранозаживляющее действие гепона доказано, лечение больных лучевыми язвами начинается с применения гепона, а затем дополняется, по показаниям, другими лекарственными средствами. Лечение лучевых ректитов (18 больных) и лучевых циститов (17 больных) проводилось в виде ежедневных двукратных микроклизм или инстилляций водного раствора 0,04% в течение 12—18 дней. Результаты применения гепона также сравнивались с результатами «традиционного» лечения, практиковавшегося в отделении в течение последних 25—30 лет (микроклизмы димексида 5—10%, эмульсии синтозона, витаминизированных масел и т. п.). Внутриполостное введение гепона уменьшало интенсивность болей и геморрагий и сокращало продолжительность лечения с 28—36 до 15—23 дней. Применение гепона активировало показатели иммунитета и у этой группы больных.
Таким образом, иммуномодулятор гепон в лечении больных с местными лучевыми повреждениями (лучевые язвы, лучевые ректиты и циститы) проявил себя как эффективное медикаментозное средство, способствующее быстрому снижению выраженности воспалительного процесса в поврежденных облучением тканях и ускорению репараторных процессов в них.
Литература
М. С. Бардычев, доктор медицинских наук, профессор
Медицинский радиологический научный центр РАМН (г. Обнинск)
Читайте также:

