Лечение шрамов при диабете
Обновлено: 26.04.2024
Зайцев П.П. 1 Власов А.П. 1 Давыдкин В.И. 1 Рубцов О.Ю. 1 Шейранов Н.С. 1 Аль-Кубайси Ш.С. 1 Аль-Совайди А.М. 1
В настоящее время в хирургии проблема лечения послеоперационных раневых осложнений является сложной и актуальной, особенно при сахарном диабете. Целью работы является оценка процесса заживления послеоперационной раны у больных сахарным диабетом, оперированных по поводу острого перитонита на фоне лазеро- и ремаксолотерапии. В исследование включены 48 больных острым перитонитом, сопряженным с сахарным диабетом. Выделены 4 группы: І (n=12) – больные острым перитонитом легкой степени, ІІ (n=12) – среднетяжелым, ІІІ (сравнения, n=12) и ІV (исследуемая, n=12) – тяжелым острым перитонитом. Для сравнения с нормой обследованы нормальные индивидуумы (n=10). Пациентам І–ІІІ групп проводилось комплексное лечение, включая дезинтоксикационный, антибактериальный, инфузионный, спазмолитический и др. компоненты. В 4-й группе дополнительно назначали ремаксоло- и лазеротерапию. Установлено, что острый перитонит у больных сахарным диабетом сопровождается повышенной гемокоагуляцией, снижением фибринолитической активности, фосфолипазной активацией, гипоксическим синдромом и ухудшением микроциркуляции. При легкой и среднетяжелой степени изменения устранялись к 7-м суткам. Заживление ран протекало сравнительно благоприятно. У больных 3-й группы процесс заживления характеризовался преобладанием первой фазы (воспалительной) над регенеративной, что нередко служит причиной развития раневых осложнений. Применение ремаксола и квантовой терапии при тяжелом остром перитоните приводило к сравнительно быстрому восстановлению гомеостаза, что оптимизировало течение репаративного процесса, уменьшило количество раневых осложнений. Полученные данные позволяют рекомендовать включение ремаксола и лазерной терапии в схему лечения больных сахарным диабетом, оперированных по поводу перитонита.

1. Ашуров Ф.А., Юсупанов Э.Ш., Гаджиев Г.А., Радуева З.Б. Пути улучшения диагностики перитонита // ScienceTime. 2017. № 3 (39). С. 16-19.
2. Власов А.П., Зайцев П.П., Власов П.А., Шевалаев Г.А., Власова Т.И., Кононенко С.В., Полозова Э.И. Особенности течения репаративного процесса и метаболизма тканевых структур кожной раны на фоне применения ремаксола // Экспериментальная и клиническая фармакология. 2017. Т. 80. № 3. С. 40-44.
3. Еськова А.Ю., Михайличенко В.Ю., Фомочкина И.И., Голубинская Е.П., Бессалова Е.Ю. Гистологические и иммуногистохимические особенности регенерации резаных ран под действием фермента трансглютаминазы в эксперименте // Таврический медико-биологический вестник. 2018. Т. 21. № 1. С. 56-62.
4. Кривощеков Е.П., Ельшин Е.Б., Ганжа Н.Ф., Романов В.Е. Некоторые сравнительные результаты местного лечения гнойных ран диабетической стопы // Colloquium-journal. 2018. № 5-1 (16). С. 19-21.
5. Мараев В.В., Елисеенко В.И., Мусаев М.М. Лазерные технологии в лечении длительно не заживающих язв различного генеза // Лазерная медицина. 2018. Т. 22. № 2. С. 13-18.
6. Москвин С.В., Фотеева Т.С. Плазмаферез и лазерная терапия // Вестник новых медицинских технологий. 2017. Т. 24. № 4. С. 231-248.
7. Оморов Т.Б., Жолдошбеков Е.Ж., Авасов Б.А. Течение раневого процесса после холецистэктомии в условиях высокогорья и низкогорья // Вестник Смоленской государственной медицинской академии. 2018. Т. 17. № 1. С. 84-88.
В настоящее время одной из актуальных патологий неотложной хирургии является заживление послеоперационных ран на фоне сахарного диабета (СД) [1]. Это связано со многими причинами, в том числе с развитием тяжелых гнойно-некротических осложнений, высокими ампутациями нижних конечностей и длительностью госпитализации, составляющей от 15–35 койко-дней [2].
Раневой процесс при сахарном диабете характеризуется медленной скоростью эпителизации, склонностью к развитию инфекционного процесса [3]. Известно, что заживление ран при сахарном диабете имеет свои особенности, поскольку оно сопряжено с выраженными расстройствами микроциркуляции, образованием микротромбов, развитием сладж-феномена, некротическими и дистрофическими процессами, доминированием воспалительного компонента над репаративным, подавлением клеточной пролиферации и фагоцитарной активности лейкоцитов, снижением общей и местной иммунологической реактивности, высокой микробной обсемененностью и др. [4; 5].
Для коррекции клеточных и биохимических нарушений и, как следствие, стимуляции регенеративного и репаративного процесса в послеоперационном периоде используются фармакопрепараты и различные физиотерапевтические способы [6].
Цель исследования. Оценить процесс заживления лапаротомной раны у больных сахарным диабетом, оперированных по поводу острого перитонита (ОП), на фоне лазеро- (ЛТ) и ремаксолотерапии.
Материал и методы исследования
Проведено исследование 48 больных сахарным диабетом преимущественно второго типа (77,1%) и острым перитонитом. Пациенты рандомизированы по полу и возрасту. Выделены 4 группы: І (n=12) – пациенты с легкой степенью острого перитонита, ІІ (n=12) – среднетяжелым острым перитонитом, ІІІ (сравнения, n=12) и ІV (исследуемая, n=12) – тяжелым острым перитонитом. Возраст больных исследования составил 56,6±5,11 года, мужчин было 26 (54,1%), женщин – 22 (45,9%). Больным первой-третьей групп проводилась стандартная терапия, включающая дезинтоксикационный, антибактериальный, инфузионный, обезболивающий и др. компоненты. В четвертой группе пациентам с острым перитонитом в комплексное лечение включали ремаксоло- и лазеротерапию. Ремаксол вводился внутривенно капельно по 400 мл в течение 10 дней. Лазеротерапия производилась ежедневно в течение 10 суток в проекции лапаротомной раны в течение 20 минут аппаратом «Матрикс».
Обследованию подлежали и здоровые индивидуумы (n=10) обоих полов в возрасте от 27 до 58 лет.
Все больные оперированы. Выполнены устранение причины, санация брюшной полости и дренирование. Основные причины ОП: острый аппендицит, прободная язва желудка или двенадцатиперстной кишки, острая кишечная непроходимость.
Больные рандомизированы с учетом возраста, пола, клинико-лабораторно-инструментальных методов и др. критериев.
Оценка степени тяжести больных произведена с помощью Мангеймского индекса перитонита. Выявлено, что в 1-й группе количество баллов было 16,1±1,26, во 2-й – 25,4±2,04, в 3-й – 34,1±3,15, в 4-й – 33,6±3,56. Согласно известным данным, если сумма баллов 29 – тяжелая [7].
Критериями включения в работу являлись информированное согласие на участие в исследовании, возраст от 27 до 62 лет, наличие сопутствующих заболеваний – сахарный диабет, проведение оперативных вмешательств. Критерии исключения: возраст старше 63 лет и моложе 27 лет, другая тяжелая соматическая патология.
Контрольный срок динамического наблюдения – 1, 5, 10-е сутки.
В исследовании были применены следующие методы.
Проведена оценка состояния гемостаза с помощью тромбоэластографа TEG® 5000 Thrombelastograph® (USA) (время реакции (R) и процент прочности сгустка (α-угол)), фосфолипазной активности (фосфолипаза А2), гипоксии – (коэффициент (КГ) гипоксии) и микроциркуляции по линии швов лапаротомной раны – (показатель микроциркуляции (ПМ) и индекс (ИЭМ) эффективности микроциркуляции).
Статистическая обработка данных произведена при помощи программы Statistica 12.0. Полученные результаты оценены с применением критерия t Стьюдента и критерия r.
Результаты исследования и их обсуждение
Нами установлено, что у пациентов с острым перитонитом на фоне сахарного диабета в раннем послеоперационном периоде отмечены нарушения системы гемостаза, активация фосфолипазы А2, гипоксические явления и существенные микроциркуляторные изменения в области ран (таблица).
Показатели функционального состояния гемостаза у пациентов с острым перитонитом на фоне сахарного диабета (М±m)
Синдром диабетической стопы (СДС) — очень серьезное осложнение сахарного диабета (СД). Это осложнение (в 85% случаев представленное трофическими язвами стоп разной тяжести) выявляется у 4—10% от общего числа пациентов с СД.
Синдром диабетической стопы (СДС) — очень серьезное осложнение сахарного диабета (СД). Это осложнение (в 85% случаев представленное трофическими язвами стоп разной тяжести) выявляется у 4—10% от общего числа пациентов с СД. Бытует мнение, что эффективность лечения язвенных дефектов стоп при СД низка, однако это не соответствует действительности. На самом деле при нейропатической форме (50—70% всех больных СДС) заживление трофической язвы происходит в 80—90% случаев. Для этого необходимо соблюдение нескольких обязательных условий (см. таблицу 1), тогда как низкая эффективность лечения часто связана с тем, что условия соблюдаются не полностью. Как показывает практика последних 10 лет, появление специализированных отделений и кабинетов «Диабетической стопы» значительно повысило эффективность лечения этих пациентов и снизило число ампутаций. Одна из не решенных пока проблем, актуальных для таких специализированных отделений, — низкая эффективность консервативного лечения диабетических язв при (нейро)ишемической форме СДС.
Ишемическая и нейроишемическая формы составляют менее половины всех случаев СДС (5—10% и 25—40%, соответственно) (Дедов, 1998, Shаw, 1996; Международная рабочая группа по диабетической стопе, 2000; Staroverova, 2001). Однако наличие выраженной ишемии принципиально меняет прогноз лечения у этих пациентов: вероятность заживления язвенных дефектов без восстановления магистрального кровотока составляет 10—30% (Международная рабочая группа по диабетической стопе, 2000). Следует помнить, что назначение большинства вазоактивных средств не повышает вероятность заживления язвенных дефектов. Согласно данным метаанализа (Loosemore, 1994), непростаноидные препараты (эффективные при II стадии хронической артериальной недостаточности, ХАН) неэффективны при III-IV стадиях. Простаниоды (алпростадил, илиопрост) влияют на прогноз при III-IV стадиях ХАН, но в основном — у больных с умеренными проявлениями критической ишемии (tcpO2>20 mmHg). Прогрессирование поражения и отсутствие заживления ран после малых ампутаций на фоне критической ишемии приводят к высокой ампутации у значительной части пациентов. Однако хорошо известно, что проведенное в таких условиях реконструктивное вмешательство на артериях нижних конечностей кардинально меняет прогноз лечения, позволяет избежать высокой, а в ряде случаев — и малой ампутации. Это привело к тому, что в последние годы хирургическая реконструкция артерий (путем шунтирования или эндоваскулярных вмешательств) рассматривается в качестве метода выбора при лечении как перемежающейся хромоты, так и язвенных дефектов ишемического происхождения при СД (American Diabetes Association, 1999; Международная рабочая группа по диабетической стопе, 2000). Была показана высокая эффективность реконструктивных операций у пациентов с СД, в ряде случаев сопоставимая с таковой у пациентов без нарушений углеводного обмена. Результатом широкого внедрения этих методов в зарубежных странах явилось значительное снижение числа ампутаций при ишемической форме синдрома диабетической стопы в Европе. Реконструктивные операции на артериях у больных сахарным диабетом проводятся и в России (Покровский, 2002; Гавриленко, 2002; Мухамадеев, 2002).
Еще один недавно вошедший в практику метод лечения — иммобилизирующая разгрузочная повязка (ИРП), в зарубежной литературе — Total Contact Cast. Такая фиксирующая повязка на голень и стопу представляет собой более или менее жесткий «сапожок» (из гипса или современных полимерных материалов, съемный или несъемный), переносящий нагрузку с области язвы на другие участки. Важно, что этот метод позволяет ходить по улице, работать и т. п., не подвергая при этом рану механической нагрузке. В большинстве зарубежных стран ИРП стал «золотым стандартом» разгрузки, но в России он практически не применялся из-за боязни возникновения осложнений (не всегда обоснованной). В нашей стране основным, хорошо себя зарекомендовавшим методом разгрузки сегодня является «полубашмак». Однако в ряде ситуаций «полубашмак» оказывается неэффективен либо существуют противопоказания к его применению. Это расположение язвы в средней части стопы или пяточной области, необходимость выходить на улицу, работать, а также несоблюдение пациентом предписанного режима разгрузки. В этих случаях требуется использование ИРП.
Пациент В., 57 лет, обратился за консультацией в отделение «Диабетическая стопа» ЭНЦ РАМН 15.04.2003. Диагноз: сахарный диабет 2 типа, тяжелого течения, декомпенсация. Диабетическая дистальная полинейропатия. Диабетическая макроангиопатия: атеросклероз артерий нижних конечностей, критическая ишемия левой нижней конечности (ХАН IV ст). Синдром диабетической стопы, нейроишемическая форма: инфицированный язвенный дефект левой пяточной области II-III cт. по Wagner. Диабетическая микроангиопатия: диабетическая нефропатия в стадии протеинурии с сохранной азотовыделительной функцией почек (IV ст. по Morgensen); диабетическая ретинопатия II ст. ИБС, стенокардия напряжения I ф. к. Многоузловой эутиреоидный зоб 0 ст. (ВОЗ).
СД 2 типа диагностирован в 1990 г. Пациент получал лечение диабетоном 80 мг 1-2 таб/сут (принимал препарат нерегулярно), контроль гликемии был нерегулярным. На момент осмотра уровень гликемии достиг 17,5 ммоль/л натощак.
Перемежающуюся хромоту не отмечал (однако вел малоподвижный образ жизни, редко проходил более 500 м).
23.02.2003 появился язвенный дефект левой пяточной области. Рана не заживала, несмотря на проводившееся амбулаторное и стационарное лечение (включавшее вазапростан 40 мкг/сут N 15), осложнилась раневой инфекцией (St. aureus, Enterococcus).
На момент осмотра: рана 4,5 х 3,5 см, глубиной до 3 см (см. рисунок 1). Стопа отечна, теплая на ощупь. Вибрационная чувствительность на стопах = 0-1 балл, пульсация на артериях правой стопы ослаблена, левой — не определяется.
Общее состояние: относительно удовлетворительное, температура тела в норме. ЧСС = 70 уд/мин, АД = 140—150/80—90 mmHg.
Рентгенологически: дефект мягких тканей пяточной области, признаков деструкции пяточной кости нет.
УЗДГ: справа — признаки стеноза ~50% бедренно-подколенного сегмента, артерий голени. Слева — стенотические изменения бедренно-подколенного сегмента (~50%), окклюзия передней тибиальной артерии, субтотальный стеноз задней большеберцовой артерии.
Дуплексное сканирование брюшного отдела аорты и артерий нижних конечностей (в ГКБ №81): сосудистая стенка неровная, утолщена в дистальных сегментах обеих задних большеберцовых артерий (ЗББА) с медиокальцинозом. Толщина комплекса «интима-медиа» до 1,2 мм. В просвете дистальных сегментов ЗББА — множественные микрокальцинаты, стенозирование ЗББА справа до 90%, слева до 80%.
Восстановление артериального кровотока
На основании данных обследования и с учетом неэффективности проводившейся консервативной терапии, пациент был направлен к ангиохирургу для проведения реконструктивного вмешательства на артериях нижней конечности. Указанное лечение осуществлялось в 25-м Центральном военном клиническом госпитале РВСН с 13.05.03 по 02.06.03.
При обследовании в стационаре были получены следующие данные.
Клинический анализ крови: гемоглобин — 128 г/л, эритр. — 4,36*10 12 /л, лейк. — 6,8*10 9 /л (пал. — 2%, сегм. — 62%, эоз. — 2%, лимф. — 28%, мон. — 6%), СОЭ — 23 мм/ч.
Клинический анализ мочи: уд. вес — 1014, белок — 1,22%, цил. — нет, лейк. — 2—4 в п/зр, эритр. — 3—5 в п/зр.
Биохимический анализ крови: общий белок — 69,0 ммоль/л, билирубин — 10,0 ммоль/л, креатинин — 120 мкмоль/л, мочевина — 6,1 ммоль/л, холестерин — 4,8 ммоль/л, β-липопротеиды — 40%, триглицериды — 1,0 ммоль/л, АЛТ, АСТ — в норме.
ЭКГ: ритм синусовый, правильный, 68 уд/мин. Горизонтальное положение электрической оси сердца.
Ro-графия органов грудной клетки: легочные поля прозрачны. Корни фиброзные, с петрификатами. Гипертрофия левого желудочка, уплотнена дуга аорты.
УЗИ органов брюшной полости: печень, селезенка, желчный пузырь, поджелудочная железа, почки — без патологических изменений.
Ангиография артерий нижних конечностей: абдоминальный отдел аорты с неровными контурами, просвет ее сохранен. Контуры магистральных артерий нижних конечностей неровные, просвет сохранен, выраженный кальциноз стенок артерий. Магистральные артерии обеих голеней с неровными контурами, резко истончаются ниже уровня щели голеностопных суставов. В дистальном отделе левой задней большеберцовой артерии определяются два тандемных критических стеноза. Подошвенные артериальные дуги разомкнуты.
Проведенное лечение
Антибиотикотерапия (офлоксацин 200 мг два раза в день), хирургическая обработка раны (иссечение некротизированных тканей из кармана глубиной до 3 см), дезинтоксикационная терапия, дезагреганты в/в. Пациент переведен на инсулинотерапию (актрапид 8 ЕД п/з, 6 ЕД п/о, 6 ЕД п/у; монотард 8 ЕД п/з, 8 ЕД — 22.00), достигнута компенсация углеводного обмена (гликемический профиль 25.06.03: 8,9–6,5–4,7–7,4–5,1 ммоль/л). В связи с диабетической нефропатией IV ст. пациент постоянно получает эналаприл 10 мг/сут.
20.05.03 произведена рентгеноэндоваскулярная ангиопластика задней большеберцовой артерии слева, восстановлен артериальный кровоток.
Операция проводилась под местной анестезией 0,5%—20,0 Sol. Novocaini, левосторонним чрезбедренным доступом антеградно пунктирована бедренная артерия. Через интродюсер диаметром 5F введен коронарный проводник в заднюю большеберцовую артерию дистальнее стенозов. В область критических стенозов подведен баллонный сегмент катетера размерами 2, 5x20, 0 мм. Выполнена ангиопластика под рабочим давлением до 5 атм. На контрольной ангиограмме стеноз устранен, препятствий для кровотока не определяется. Проводник удален. Интродюсер подшит к коже. Асептическая повязка. За период вмешательства больному внутриартериально введено 7 тыс. ЕД гепарина. Состояние пациента не изменилось.
После выписки: при допплеровском исследовании магистрального кровотока справа и слева в задних большеберцовых артериях — магистральный измененный кровоток (ЛПИ > 1), в тыльных артериях стопы — коллатеральный кровоток, но ЛПИ > 1 (возможно завышение лодыжечно-плечевого индекса, вследствие артериосклероза Менкеберга).
Чрескожное напряжение кислорода (tcpO2) на тыльной стороне левой стопы (через три месяца после ангиопластики): лежа — 19 mmHg, сидя — 20 mmHg (возможно занижение показателя вследствие отека стопы). По совокупности клинических данных, состояния раны и результатов инструментального обследования было сделано заключение, что явления критической ишемии устранены.
Применение индивидуальной разгрузочной повязки (Total Contact Cast)
Пациент был выписан для амбулаторного лечения, которое включало:
- ежедневные перевязки с промыванием раны раствором диоксидина, фурацилина, наложением атравматической повязки (Atrauman, Branolind);
- регулярное удаление гиперкератоза с краев раны;
- разгрузку пораженной конечности (костыли);
- компенсацию углеводного обмена (инсулинотерапия).
Признаков ишемии конечности не наблюдалось, рана заполнилась полноценной грануляционной тканью (см. рисунок 2), но скорость сокращения размеров раны оказалась ниже расчетной (см. рисунок 3).
Известно, что скорость заживления соответствует расчетной при отсутствии значимой ишемии, инфекции и механической нагрузки на рану. Учитывая, что разгрузка конечности с применением костылей не является оптимальной, было решено изготовить иммобилизирующую разгрузочную повязку.
Эквивалентный радиус раны рассчитывается как (d1+d2)/4, где d1 и d2 — соответственно максимальный и перпендикулярный ему минимальный диаметр раны.
Расчетная скорость заживления (черная линия) определяется по формуле Cavanagh: r = -0.74 + 1.04*r0 — 0.1*t — 0.012*r0*t, где r — эквивалентный радиус раны в данный момент, r0 — исходный эквивалентный радиус раны, а t — время с начала лечения (дни) (Cavanagh, 2001).
Реальные размеры раны наносились на график (красная линия) при каждом осмотре пациента (точка «0» — 1 месяц после баллонной ангиопластики). Из графика видно, что после изготовления ИРП скорость заживления (угол наклона графика) значительно выросла и достигла расчетной.
При применении этого метода разгрузки рана начала затягиваться гораздо быстрее, и к 10.09.03 было достигнуто заживление язвы (см. рисунок 4).
Основными методами реваскуляризации нижних конечностей являются шунтирующие операции и чрескожная транслюминальная баллонная ангиопластика (ЧТБА). Зачастую ЧТБА считают недостаточно эффективной и предлагают не использовать у пациентов с СД. Известно, что долговременный эффект шунтирования выше, чем у баллонной ангиопластики, причем у больных с СД эта разница выражена сильнее (Dyet, 2000). Но в критических ситуациях (язвенные дефекты, критическая ишемия) ангиопластика представляет собой малоинвазивный метод, позволяющий стабилизировать ситуацию и избежать ампутации, что зачастую более важно, чем отдаленные результаты вмешательства. Это так называемая limb-saving angioplasty — ангиопластика для спасения конечности.
История болезни, представленная выше, демонстрирует также, как важна постоянная оценка эффективности проводимого лечения (в нашем случае — сопоставление динамики размеров язвы с результатами расчета по формуле Cavanagh). Если эффект от лечения недостаточен, необходимо выявить причину, по которой это происходит. В нашем случае отсутствие оптимального режима разгрузки оказалось достаточной причиной для замедленного заживления раны, и эта проблема могла быть решена только с помощью нового метода — иммобилизирующей разгрузочной повязки. Следует особенно отметить, что для приближения к «идеальной» скорости заживления не потребовалось использования ни «стимуляторов заживления» (солкосерил, актовегин, метилурацил и т. п.), ни «сосудистых» средств. Эти препараты широко применяются, однако их эффективность в отсутствии необходимых условий для заживления (см. таблицу 1) крайне низка.
В настоящее время становятся доступными новые методы лечения СДС, внедрение которых в повседневную практику вполне возможно и крайне необходимо. Только адекватное комбинированное лечение позволяет достичь оптимальных результатов, особенно в сложных случаях, таких, как синдром диабетической стопы.
По вопросам литературы обращайтесь в редакцию
О. В. Удовиченко, кандидат медицинских наук
Г. Р. Галстян, кандидат медицинских наук
И. А. Ерошкин, кандидат медицинских наук
А. А. Ефимов, О. В. Носов
Ю. Г. Васильев, кандидат медицинских наук
Эндокринологический научный центр РАМН (Москва), 25-й Центральный военный клинический госпиталь РВСН (Одинцово)
Что такое диабетическая стопа? Причины возникновения, диагностику и методы лечения разберем в статье доктора Есипенко И. А., сосудистого хирурга со стажем в 37 лет.
Над статьей доктора Есипенко И. А. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Диабетическая стопа (синдром диабетической стопы, СДС) — это тяжёлое осложнение сахарного диабета в виде инфекции, язв или разрушения глубоких тканей, которое возникает в связи с нарушением макроструктуры стопы и микроциркуляции крови, по причине разрушения нервных окончаний и нервных волокон. [10]
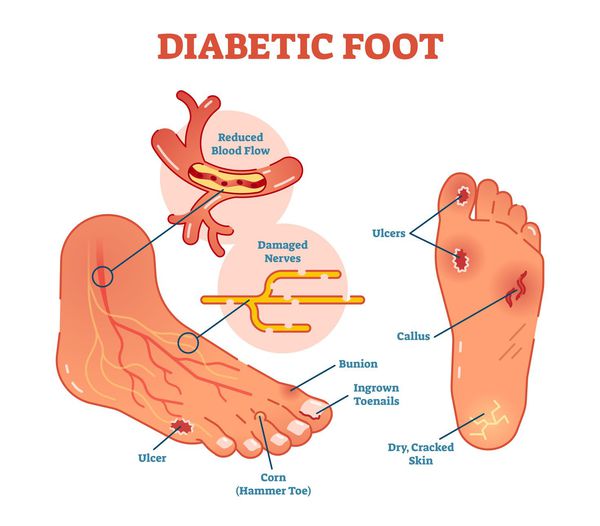
Главная причина ДС — это сахарный диабет (СД). И хотя синдром диабетической стопы не развивается с первого дня увеличения уровня глюкозы в крови более 7,0-8,0 ммоль/л, каждый пациент с диагнозом «сахарный диабет» должен помнить о таком грозном возможном осложнении.
Хронические раны на ногах у людей с сахарным диабетом встречаются в 4-15 % случаев. В некоторых случаях они становятся первым признаком развившегося диабета [10] .
Основные «пусковые механизмы» развития язв при СДС:
1. Ношение неудобной обуви. К изменению нагрузки на суставы стопы, сдавливанию или потёртости кожи, локальной микроишемии, инфильтрату, или некрозу могу привести любые дефекты обуви:
- несоответствующий размер обуви (меньше или больше, чем нужно);
- стоптанные и/или высокие каблуки;
- рубец на стельке;
- дефект подошвы;
- мокрая обувь;
- несоответствие обуви времени года.
2. Увеличенный вес тела. Учитывая площадь стоп, при увеличении веса тела (даже на 1 кг) увеличивается и нагрузка на каждый сустав стопы. Самая уязвимая область — подошвенная поверхность.
3. Разрастание эпидермиса (поверхности) кожи. Этот процесс происходит из-за нарушенных обменных процессов в коже на фоне СД (под утолщённым эпидермисом-"мозолью" в слоях кожи нарушается микроциркуляция, что приводит к микроишемии и некрозу).
4. Микротравмы:
- укусы животных;
- уколы шипами растений;
- порезы при педикюре и т. п.
5. Стенозы (сужение) и окклюзии (закупорка) магистральных артерий. В результате отсутствия кровоснабжения в стопах и голенях к микроишемии присоединяется макроишемия и развитие гангрены конечности.
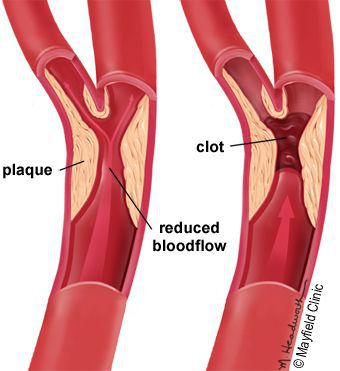
6. Условно патогенная или патогенная микрофлора. Активизация флоры (микробов и других микроорганизмов) на поверхности кожи в условиях СД приводит к воспалению кожного покрова, а в условия ишемии или микротравмы значительно ускоряется развитие гангрены.
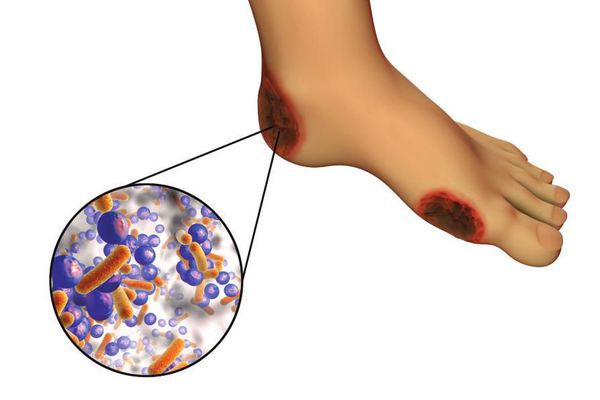
Часто наблюдается сочетание нескольких причин возникновения язв при СДС.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы диабетической стопы
Отправной точкой развития СДС считается не дата установления диагноза «Сахарный диабет», а время, когда были выявлены первые симптомы СД (однократные подъёмы глюкозы крови, сухость во рту и другие).
Симптомы СДС:
- онемение, зябкость, жжение, отёки в стопах и другие неприятные ощущения;
- выпадение волос на на стопах и голенях, потливость стоп;
- изменение окраски кожи (гиперемия, гиперпигментация, цианоз);
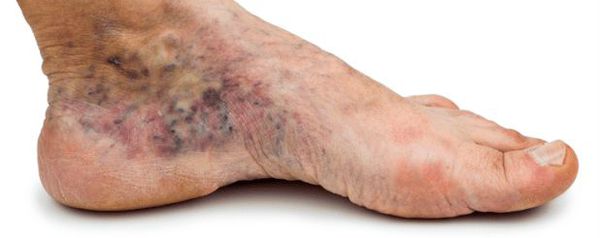
- утолщение, расслаивание, изменение формы и цвета ногтевых пластинок;
- кровоизлияния под ногтевой пластинкой в виде «синяков» под ногтями;
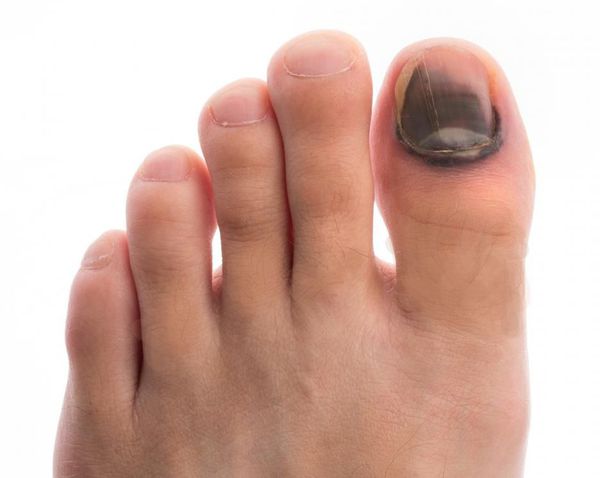
- деформация стоп;
- снижение чувствительности стоп — вибрационного, температурного, болевого и тактильного восприятия;
- боль в области стопы и язвы, возникающая как в покое или ночью, так и при ходьбе на определённые расстояния;
- истончение кожи, шелушение;
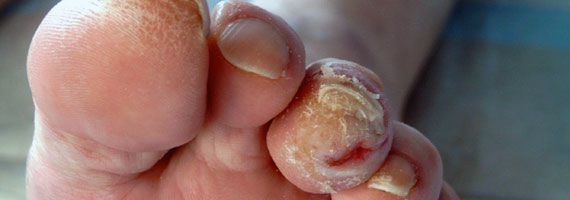
- понижение или увеличение температуры стоп и голеней;
- длительная эпителизация (заживление) микротравм — до двух месяцев, при этом остаются коричневые рубцы;
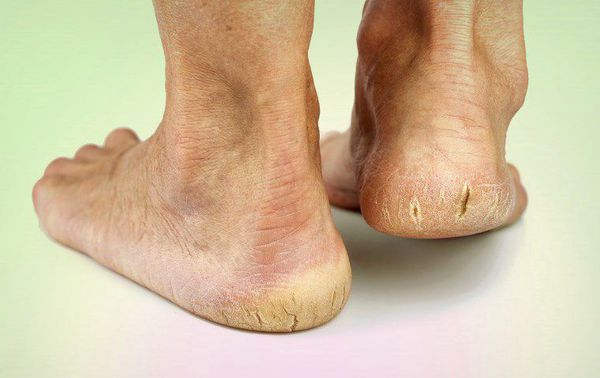
- трофические язвы, длительно не заживающие на стопах.
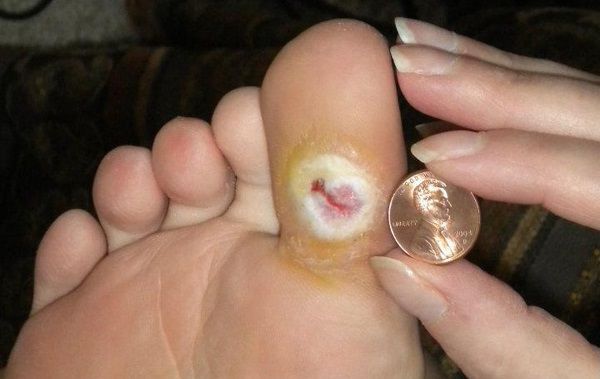
Чаще всего трофическим изменениям подвержены дистальные отделы конечности: пальцы и подошвенная поверхность стопы в проекции головок плюсневых костей. Зона образования трофической язвы зависит от причины её возникновения.
Патогенез диабетической стопы
Механизм развития СДС представляет собой следующую последовательность нарушений:
- Снижается выработка гормона инсулина.
- Увеличивается уровеь глюкозы в крови — развивается гипергликемия.
- Блокируется кровоток в мелких сосудах, через сосудистую стенку перестаёт поступать кислород и другие микроэлементы.
- Разрушаются нервные волокна и рецепторы.
- Наступает микро- и макроишемия тканей стопы.
- Образуются трофические язвы.
Таким образом, при СДС происходит повреждение всех тканей ноги.
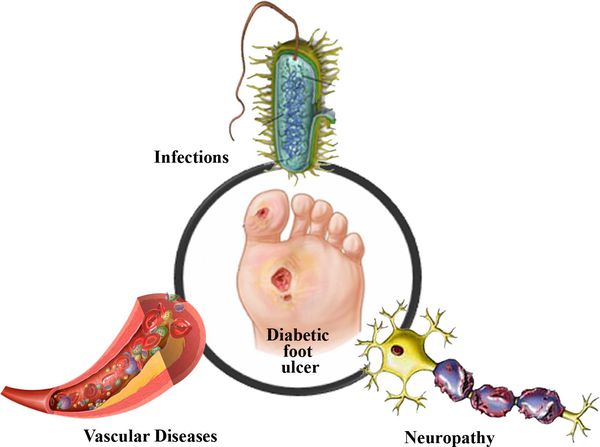
В результате дефицита инсулина в организме диабетика количество глюкозы в крови увеличивается. Это в свою очередь негативно сказывается на состоянии как мелких, так и крупных сосудов:
- на стенках сосудов скапливаются иммунологические вещества;
- мембраны становятся отёчными;
- просвет сосудов сужается.
В результате этих изменений кровообращение нарушается и образуются небольшие тромбы. Эти изменения в организме препятствуют поступлению достаточного количества микроэлементов и кислорода в клетки и тем самым приводят к нарушениям обменного процесса. Кислородное голодание тканей замедляет процесс деления клеток и провоцирует их распад.
Увеличение уровня глюкозы в крови также становятся причиной поражения нервных волокон — снижается чувствительность.
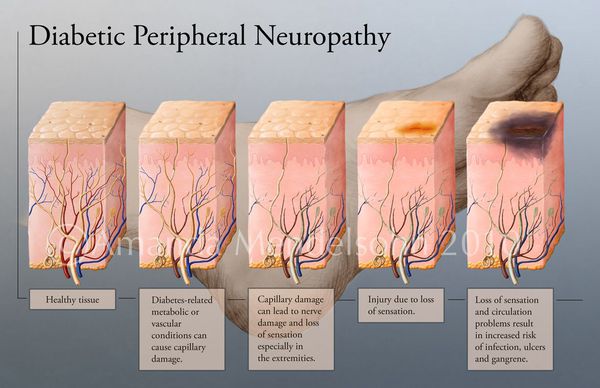
Все деструктивные процессы, происходящие в тканях стопы приводят к тому, что любое повреждение кожи становится лёгким процессом, а заживление — длительным. Усугубить состояние стопы могут присоединившиеся инфекции, которые способны привести к образованию гангрены — некрозу тканей. [9]
Классификация и стадии развития диабетической стопы
Классификация I Международного симпозиума по диабетической стопе
В 1991 году в Нидерландах на I Международном симпозиуме была принята классификация СДС, которая является наиболее распространённой. [1] Она предполагает разделение заболевания на три типа в зависимости от преобладающего патологического процесса:
- нейропатическая инфицированная стопа:
- длительное течение сахарного диабета;
- позднее возникновение осложнений;
- отсутствие болевого синдрома;
- цвет и температура кожи не изменены;
- уменьшение всех видов периферической чувствительности;
- наличие периферического пульса.
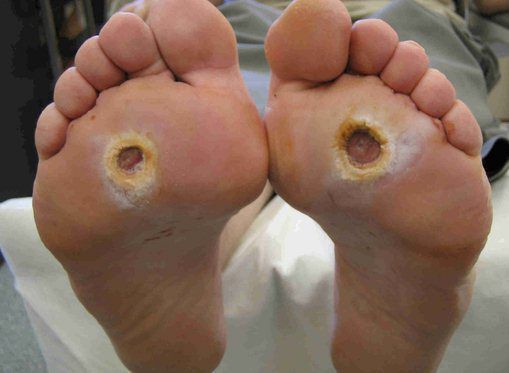
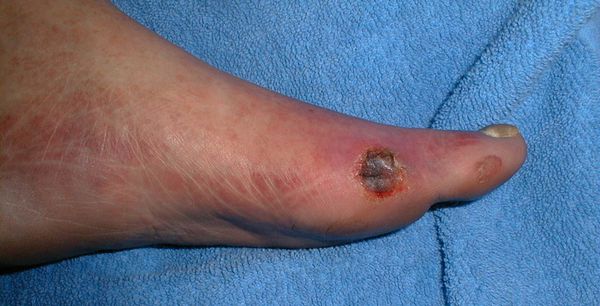
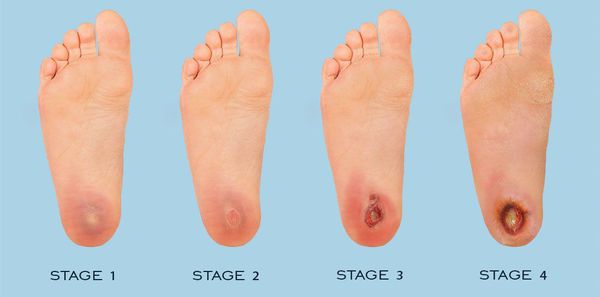
Классификация Вагнера
По степени выраженности поражений тканей стопы выделяют следующие стадии СДС: [6] [7]
- Стадия 0 — изменение костной структуры стопы — артропатия;
- Стадия 1 — изъязвление (язвы) кожи;
- Стадия 2 — изъязвление всех мягких тканей, дном язвы являются кости и сухожилия;
- Стадия 3 — абсцедирование и остеомиелит (воспаление костной ткани);
- Стадия 4 — образование гангрены дистальных отделов стопы (пальцев);
- Стадия 5 — образование гангрены стопы и отделов голени.
Классификация Техасского университета
Данная классификация была разработана в 1996-1998 годах. [8] В её основе лежит оценка язвы по глубине, наличию инфицирования и ишемии — риска ампутации конечности.
На сервисе СпросиВрача доступна консультация эндокринолога онлайн по любой волнующей Вас проблеме. Врачи-эксперты оказывают консультации круглосуточно и бесплатно. Задайте свой вопрос и получите ответ сразу же!

Здравствуйте, какой гликированный гемоглобин? Показатели сахара натощак и через 2 ч после еды ? Какие инсулины ? В каких дозах?
Дмитрий, спасибо ,что откликнулись. Завтра я отвечу на все ваши вопросы. Мама находится не рядом. Категорически отказывается ехать к врачу.Завтра я все разузнаю и напишу


Здравствуйте! От мазей может быть хуже. Сфотографируйте, если можете, рану.
Уточните у мамы лечение. Какое лекарство, в какой дозировке делает, сколько раз в день. Уровень глюкозы натощак и после еды через 2 часа.


Здравствуйте!
Какой уровень гликированного гемоглобина? какой уровень глюкозы на самоконтроле? Глубина раны?
Сделайте узи сосудов нижних конечностей, рентгенографию пальца на котором есть рана
Чем лечите рану? если есть возможность сделайте фото.

Здравствуйте, для того,чтобы понимать почему не заживает рана нужно знать ее показатели сахара крови натощак, и через 2 часа после еды. Давно сдавала гликозилированный гемоглобин, и какой показатель?
Какие мази и как применяла.
По хорошему, когда есть рана на стопе у пациентов с сахарным диабетом она сначала обрабатывается мирамистином или Хлоргексидином для очищения раны, затем накладывается мазь хорошем бактерицидным эффектом обладает бетадин мазь 2 -3 раза в день проводить такую процедуру.
Никакие дубящие средства (зеленка, йод и т.д.) в данном случае не используются, т.к. это закрывает рану и не дает ей очищаться .
Можно к этому добавить препараты Тиоктацид БВ, или Берлитион, или Тиогамма 600 мг по 1 таб 1 раз в день утром в течение 3 х месяцев.
Рубцы и шрамы представляют собой изменения на коже в результате последствия заживления после прыщей, ожогов, порезов, гнойничковых образований. Для их лечения используют лекарственные препараты и специальные процедуры. В отдельных случаях показано хирургическое вмешательство.
Разновидности рубцов и шрамов
В зависимости от особенностей структуры кожного покрова выделяют 3 основных вида рубцов и шрамов:
Атрофические – выглядят как ямки, которые как бы проваливаются под кожу. Появляются как последствия прыщей, стрии (растяжение кожи), ветряной оспы.
Гипертрофические – в отличие от первых, наоборот, поднимаются над поверхностью кожи. Они появляются на фоне угрей, а также после заживления ран.
Нормотрофиеские – лежат вровень с поверхностью кожи. Появляются в результате разных повреждений (ранения, ожоги, порезы и другие).
Эффективные способы лечения рубцов
Шрамы и рубцы лечат разными способами. Конкретный вид лечения подбирает врач в зависимости от причины, состояния пациента, сопутствующих заболеваний и других факторов. Основными методами терапии являются такие:
Специальные кремы – например, «Имофераза», «Дерматикс», «Нафтадерм», «Контрактубекс», «Клофибраза», «Нарбирил» и другие.
Химический пилинг – к этому методу прибегают в тех случаях, когда лечение мазями оказывается неэффективным.
Введение дермальных наполнителей на основе гиалуроновой кислоты или коллагена. Эти компоненты не только выравнивают поверхность кожи, но и активизируют синтез коллагена самим организмом.
Лазеротерапия позволяет устранить наиболее заметные рубцы. Они разрушаются под воздействием лазерного излучения, в результате чего также повышается синтез коллагена.
Хирургическое вмешательство показано в крайних случаях, когда нужно вырезать рубцовую ткань. Возможна пересадка небольшой части кожи или дермотензия.
Лазерная шлифовка
Лазерное излучение воздействует на поверхностный слой кожи и уничтожает ткани, образующие рубец. В результате удаляют омертвевшие клетки и активизируют восстановление здоровых тканей. Сегодня используется 2 метода лазеротерапии:
Углекислотный лазер на основе углекислого газа способствует удалению шрама и осветлению пострадавшей области.
ЛазерFracelприводит к размягчению рубцовых тканей и усиливает синтез коллагена.
Процедура доказала свою эффективность. Однако в ряде случаев ее проведение противопоказано:
образование грубых рубцов (келоидных);
проблемы свертываемости крови;
обострения хронических заболеваний;
все сроки беременности и лактации;
опухоли (в том числе доброкачественные).
Химический пилинг
Пилинг представляет собой разрушение рубцовой ткани за счет воздействия разных органических кислот. Они способствуют также оптимизации жирового обмена, благодаря чему можно избавиться и от угрей. Есть несколько разновидностей химического пилинга (в зависимости от используемого реагента):
Пилинг ТСА (используется 3-хлоруксусная кислота концентрацией 35-50%).
Ретиноевый (на основе ретиноевой кислоты, которая не только разрушает рубцы, но и обладает антибактериальным действием).
Феноловый (на основе фенола – он также способствует избавлению от рубцов и уничтожает бактерии). Однако фенол токсичен и может плохо повлиять на нервную систему.
Химический пилинг противопоказан в таких случаях:
рецидив появления угрей;
склонность к келоидным рубцам;
индивидуальная непереносимость используемых веществ.
Механический пилинг
Наряду с химическим есть и механический пилинг. Так называют методику удаления верхнего слоя дермы с помощью насадок-фрезов. Есть 3 вида процедуры:
Эксфолиация – поверхностное удаление кожи до 15 мкм.
Эпидермолиз – удаляют слой до 50 мкм.
Глубокая дермабразия – глубина до 150 мкм.
Процедура проводится с применением местного обезболивания. Но в первые дни могут наблюдаться такие побочные эффекты, как боль, отечность. Также пациентам трудно принимать пищу (Если они прошли чистку соответствующих участков лица). В ближайшие дни на поверхности будет образовываться новая корочка. Ее нужно обработать антисептическими препаратами, а также разными мазями для предотвращения воспалительных процессов. Полное восстановление занимает до 3 месяцев.
Лечение лекарственными препаратами
Наряду с описанными процедурами для лечения рубцов и шрамов используются специальные препараты. Они комплексно воздействуют на пораженный участок – размягчают рубцовую ткань и способствуют восстановлению за счет образования новых клеток. К наиболее распространенным препаратам относят:
«Контрактубекс» – гель, содержащий аллатоин. Размягчает рубец, способствует снятию воспаления. Наносится непосредственно на поверхность и хорошо втирается в кожный покров. Курс длится несколько недель, но если раны застарелые – до 12 месяцев.
«Дерматикс» содержит в своем составе кремний-органические соединения. Размягчает рубцовую ткань за счет увлажняющего эффекта. Используется для лечения всех частей тела, в том числе лица, общий курс до 2 месяцев.
«Имофераза» содержит в составе фермент гиалуронидазу. Она активно воздействует на соединительную ткань рубца, разрушая ее. Используется для лечения шрамов, постакне и других заболеваний.
«Цикартикс» – мазь на основе экстракта центеллы и сосны. Способствует выработке коллагена, благодаря чему активизируются процессы восстановления тканей, улучшается кровоток.
«Нафтадерм» – препарат на основе нафталанской нефти. Способствует рассасыванию рубцов и размягчению ткани. Угнетает воспалительные процессы, обладает антисептическим и противозудным действием.
Рубцы и шрамы поддаются лечению, причем в большинстве случаев достаточно использовать специальные мази. Но если нужного эффекта нет, прибегают к лазеротерапии, химическому пилингу и другим процедурам. В редких случаях рубцы можно удалить только в ходе хирургической операции.
Все представленные на сайте материалы предназначены исключительно для образовательных целей и не предназначены для медицинских консультаций, диагностики или лечения. Администрация сайта, редакторы и авторы статей не несут ответственности за любые последствия и убытки, которые могут возникнуть при использовании материалов сайта.
Читайте также:

