Лапчатка белая при витилиго
Обновлено: 26.04.2024
Витилиго — это часто встречающийся дерматоз, распространенность которого составляет 3–4% в структуре кожной патологии. Витилиго может появиться в любом возрасте (Р. С. Бабаянц, Ю. И. Лоншаков, 1978; M. Halder et al., 1996); 50% случаев приходится на возр
Витилиго — это часто встречающийся дерматоз, распространенность которого составляет 3–4% в структуре кожной патологии. Витилиго может появиться в любом возрасте (Р. С. Бабаянц, Ю. И. Лоншаков, 1978; M. Halder et al., 1996); 50% случаев приходится на возраст 10–30 лет. Мужчины и женщины болеют одинаково часто. Это мультифакторное заболевание, причем в каждом конкретном случае могут быть разные механизмы его патогенеза и разные уровни нарушения образования меланина в коже (В. Г. Панкратов, И. А. Евсеенко, 1999). Заболевание возникает при сочетании предрасполагающих и провоцирующих факторов. Оно часто сочетается с заболеваниями щитовидной железы, сахарным диабетом, В12-дефицитной анемией и др.
Для лечения витилиго используются различные методы, так как одного радикального способа нет (S. Changgeng, Y. Ganyun, 1995).
Стабильность химического состава организма является одним из важнейших и обязательных условий его нормального функционирования (Н. А. Агаджанян, А. В. Скальный, 2001). Патология человека, обусловленная дефицитом жизненно необходимых (эссенциальных) элементов, избыточным количеством как эссенциальных, так и токсичных элементов, а также дисбалансом микроэлементов, получила название микроэлементозов (А. П. Авцын и др., 1991). Изучение роли эссенциальных и токсичных элементов в патогенезе витилиго дает возможность расширить спектр методов лечения данной патологии (A. Vaisov et al., 1985; M. Molokhia et al., 1973).
Для оценки влияния среды обитания, алиментарных факторов на организм, а также выявления хронических заболеваний в последнее время все чаще используют мультиэлементный анализ волос, позволяющий своевременно обнаружить доклинические изменения в организме и назначить индивидуальную программу для устранения нарушений минерального обмена (А. В. Скальный, 1999).
Целью работы является изучение элементного статуса волос больных с диагнозом витилиго.
В ходе выполнения работы проведено обследование образцов волос 49 мужчин и 91 женщины в возрасте от 18 до 55 лет с установленным диагнозом витилиго. В качестве референтных значений использованы данные по аналогичным половозрастным группам лиц, не страдающих данным заболеванием и не имеющих других хронических заболеваний (А. В. Скальный, 2000).
Все образцы волос подвергались пробоподготовке и анализу согласно методическим указаниям МУК 4.1.1482-03, МУК 4.1.1483-03 (С. И. Иванов и др., 2003).
Аналитические исследования выполнены методами атомной эмиссионной спектрометрии с индукционно связанной аргоновой плазмой (АЭС-ИСП) и масс-спектрометрии с индуктивно связанной аргоновой плазмой (МС-ИСП) на приборах Optima 2000 DV и Elan 9000.
В образцах волос определяли содержание 22 химических элементов: K, Na, Ca, Mg, P, Co, Cr, Cu, Fe, Mn, Zn, Se, As, Sn, V, Si, Ti, Ni, Al, Cd, Pb, Hg.
Статистическая обработка результатов исследований проводилась с использованием программ Microsoft Excel XP.
Результаты проведенного исследования элементного состава волос больных витилиго представлены в таблице.
Анализ полученных данных показал, что у больных, страдающих витилиго, частота отклонений в минеральном составе волос в зависимости от пола имеет определенные различия. Прежде всего хотелось бы обратить внимание на содержание меди и марганца. Эти элементы участвуют в синтезе меланина и являются антагонистами. В литературных данных главная роль в патогенезе витилиго отводится меди (А. С. Ваисов, Е. А. Кадыров, М. А. Рахимова, Ш. Н. Муратходжаева, 1985), хотя, как видно из представленных в таблице данных, у женщин в 2 раза, а у мужчин в 8 раз чаще наблюдается дефицит Mn в волосах по сравнению с дефицитом Cu (p < 0,001). При этом дефицит меди в волосах чаще встречается у женщин, а марганца — у мужчин.
Также обращает на себя внимание нарушение содержания Zn в волосах в обеих группах. Дефицит Zn в волосах больных витилиго чаще встречается у мужчин, чем у женщин.
Уровни содержания в волосах Fe и Co существенно отличаются у мужчин в сравнении с женщинами, а Se, Si и Cr достоверно не отличаются (p > 0,05).
Также в обеих группах наблюдается избыток содержания в волосах тяжелых металлов (Ti, Ni, Al, Cd, Hg, Pb), которые могут существенно влиять на нарушение обмена эссенциальных элементов. У мужчин преобладает избыток в волосах Ni, Cd, Pb, у женщин — Ti и Al.
Таким образом, в результате сравнительных исследований нами получен «элементный портрет» больных витилиго. Так, содержание жизненно важных элементов у женщин указывает на преобладание дефицита элементов, участвующих в гормональной регуляции (Cu, Mn, K, Na, ), а у мужчин — стрессовых элементов (Mn, Mg). У пациентов обеих групп выявилось нарушение обмена химических элементов, участвующих в регуляции углеводного обмена (Cr, Mn, Zn), функции печени (Fe, Co, Se, Cu), а также накопление тяжелых металлов (Ti, Ni, Al, Cd, Hg, Pb).
Полученные данные свидетельствуют о влиянии нарушений обмена макро- и микроэлементов, а также тяжелых металлов на риск развития и течение витилиго. Таким образом, нам представляются перспективными исследования в данной области: возможно, они позволят сформировать правильный подход к пониманию механизмов возникновения витилиго и предложить эффективные схемы лечения.
Терапия витилиго
Целью лечения является остановка прогрессирования заболевания и достижение репигментации в очагах витилиго. Традиционно для лечения витилиго используют витамины, гепатопротекторы, глюкокортикоиды, иммуномодуляторы, ферменты, препараты меди и цинка, наружно назначают Мелагенин, кварц, ПУВА-терапию (с незначительным эффектом).
Наиболее эффективны методы с использованием ультрафиолетового (UV) излучения (А. А. Кубанова, 2005).
Для лечения витилиго используются аппарат X-Traq, способный синтезировать световой пучок в диапазоне UVB длиной 308 нм, а также Multi Clear (производитель — Cure Lighl, Израиль), который дает возможность использовать UVB 290–320 нм и совмещать UVB и UVA в одной вспышке с длиной волны 290–400 нм. Эффект основан на локальном воздействии светового пучка, вследствие чего меланоциты начинают вырабатывать пигмент.
Под нашим наблюдением находилось 158 пациентов (35 мужчин, 123 женщины) с различными формами витилиго. Возраст пациентов варьировал от 6 до 72 лет (в среднем 28,5 года). Продолжительность заболевания — от 3 мес до 43 лет, в среднем — 11,6 года; 3 пациента имели витилиго с рождения. Распространенность варьировалась от единичного пятна диаметром 5 мм до 40% площади тела. Локализация высыпаний на лице наблюдалась у 126 человек (80%), на конечностях — у 131 пациента (83%), в том числе на стопах и кистях — у 56 (36%) человек, на коже туловища — у 64 (41%) и на гениталиях — у 17 (11%). Количество процедур колебалось от 5 до 56. При использовании аппарата X-Traq получили лечение 122, аппарата Multi Clear — 36 человек.
Эффективность применяемых методик варьировалась в различных группах пациентов. Так, наилучший эффект наблюдался у лиц молодого возраста и до 50 лет со смуглой кожей (3–4-й тип по Фитспатрику), на очагах, где пигмент пропал не полностью и волосы не потеряли окраску. Лучше всего пигмент восстанавливался в области лица. Эффект практически отсутствовал у светлокожих блондинов, на длительно существующих очагах и при локализации высыпаний на кистях и стопах.
Эффект от лечения проявлялся в виде уменьшения площади и репигментацией внутри пятна витилиго, которые постепенно сливались и заполняли весь очаг депигментации. На здоровой коже, прилегающей к обрабатываемому участку, при этом появлялась гиперпигментация, которая со временем проходила. Надо отметить, что при использовании аппарата X–Traq пациенты жаловались на сильные ожоги, которые сопровождались пузырями и мокнутием; подобных осложнений в случаях применения аппарата Multi Clear не наблюдалось.
Кроме этого, больным проводилась общая терапия с применением гепатопротекторов, витаминов, иммуномодуляторов и коррекция нарушений обмена микроэлементов.
Таким образом, использование селективной UVA- и UVB-терапии на сегодняшний день является наиболее эффективным методом лечения витилиго, особенно у пациентов со свежими высыпаниями и смуглой кожей. Однако для повышения ее эффективности пациенты нуждаются в тщательном обследовании и подборе индивидуальной комплексной терапии с учетом патогенеза заболевания.
По вопросам литературы обращайтесь в редакцию.
И. В. Верхогляд, кандидат медицинских наук
РМАПО, Москва
Что такое тиреотоксикоз (гипертиреоз)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Курашова О. Н., эндокринолога со стажем в 28 лет.
Над статьей доктора Курашова О. Н. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Тиреотоксикоз (гипертиреоз) — гиперметаболический процесс, вызванный избытком тиреоидных гормонов в организме и их токсическим воздействием на различные органы и ткани. Клинически характеризуется увеличением щитовидной железы и поражением других систем и органов. [3] [5] [11]
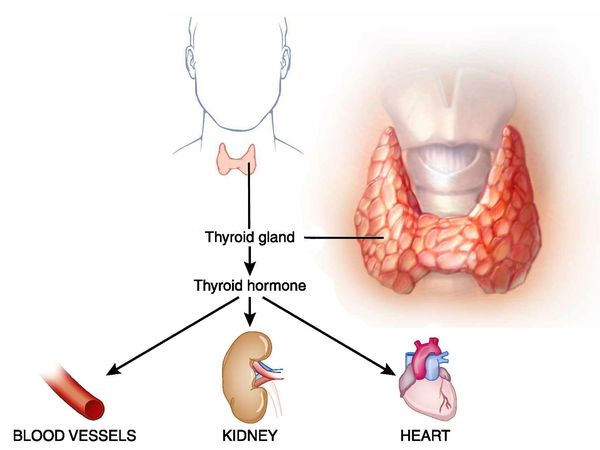
Первые описания этой патологии были найдены в работах персидского врача Джурджани, созданных в 1100 году. [5] [11]
Данный синдром встречается как у женщин (до 2%), так и у мужчин (до 0,2%). Чаще он возникает у людей в возрасте 20-45 лет.
Причины тиреотоксикоза
Причин возникновения тиреотоксикоза множество. К основным относятся:
- повышение продукции гормонов щитовидной железой вследствие различных заболеваний (диффузно-токсический, узловой зоб и другие);
- избыточный приём препаратов, содержащих гормоны щитовидной железы (нарушение назначенной схемы лечения гипертиреоза).
Факторы риска
Провоцирующим фактором синдрома является дополнительное количество йода, поступающее в организм при самостоятельном использовании йодных добавок.
Состояние тиреотоксикоза при диффузно-токсическом зобе является аутоиммунным заболеванием. Обычно оно развивается в результате избыточной выработки антител к рецептору тиреотропного гормона (ТТГ), производимого гипофизом.
Возникновение тиреотоксического состояния возможно при возникновении функциональной автономии уже существующего узла щитовидной железы — одно- и многоузлового зоба. Это заболевание развивается достаточно долго, в основном у людей, старше 45 лет. Так, в отсутствие воздействия ТТГ — основного физиологического стимулятора [7] [8] — узлы синтезируют количество тиреогормонов, превышающее потребность организма. [5] [6] [11]
Тиреотоксикоз при беременности
Во время беременности потребность организма женщины в тиреоидных гормонах возрастает на 30–50 %, поэтому изменение работы щитовидной железы происходит уже с первых недель беременности. Вследствие этого у 2 % беременных развивается гестационный гипертиреоз. Беременным рекомендуется вовремя обратиться к лечащему врачу, провести диагностику и подобрать необходимое индивидуальное лечение.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы тиреотоксикоза (гипертиреоза)
При опросе пациентов с подозрением на повышенную функцию щитовидной железы выявляются:
- непредсказуемая возбудимость, эмоциональная неустойчивость, беспричинная плаксивость;
- беспокойство и нарушение концентрации внимания, возникающее при нахождении в обществе;
- ежедневное нарушение сна;
- суетливость при выполнении любой работы;
- слабость во время ходьбы;
- повышенная потливость диффузного характера, не зависящая от физического или эмоционального напряжения, ощущение «жара»;
- периодические сердцебиения;
- дрожь в теле и нарастающая потеря веса (наблюдаются редко).
Эмоциональные расстройства сочетаются с двигательно-волевыми: появляется необходимость в постоянном движении и хореоподобные подёргивания. Причём тремор конечностей и тела - типичный симптом тиреотоксикоза. [2] [3] [5] [11]
Что такое очаговая алопеция? Причины возникновения, диагностику и методы лечения разберем в статье доктора Ерёминой Татьяны Александровны, дерматолога со стажем в 14 лет.
Над статьей доктора Ерёминой Татьяны Александровны работали литературный редактор Юлия Липовская , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина
Определение болезни. Причины заболевания
Выпадение волос (алопеция) — это патология, которая характеризуется воспалением в волосяных фолликулах и иногда ногтевых пластинах, а также стойкой или временной нерубцовой потерей волос.
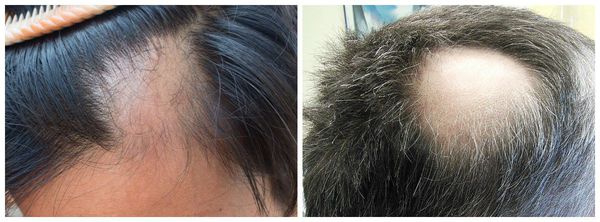
Алопеция по актуальности не уступает многим дерматологическим проблемам. Волосы — придаток кожи, они придают человеку определённый эстетический вид, из-за отсутствия волос возникает косметический дефект, который влечёт за собой снижение качества жизни пациента и проблемы с социальной адаптацией.
Выпадение волос бывает врождённым и приобретённым. Наиболее часто регистрируется приобретённая форма выпадения волос — очаговая, или гнёздная, алопеция (ГА). Гнёздная алопеция также известна как частичное или точечное облысение, волосы могут выпадать не только на голове, но и на теле, бровях и ресницах [1] . Как правило, она возникает спонтанно на фоне полного здоровья.

Алопеция развивается у обоих полов. Определённая роль в развитии патологии отводится факторам риска, к ним относятся:
- заболевания пищеварительного тракта: синдром нарушенного кишечного всасывания, хронический гастрит, ассоциированный с бактерией Helicobacter pylori ;
- инфекции: ОРВИ, грипп, кишечные инфекции и т. д.;
- приём медикаментов: антибиотиков, противовирусных препаратов, нестероидных противовоспалительных препаратов, витаминов группы В и т. д.);
- наследственность, хронические патологии (хронический синусит, тонзиллит, гайморит, хронический кариес и т. д.);
- вредные привычки, недостаток витаминов и микроэлементов (цинка, селена, меди, железа, молибдена и т. д);
- стрессы, депрессия, изменение в мочеполовой системе (воспалительные гинекологические заболевания, приводящие к изменению гормонального обмена): эндометриоз, поликистоз яичников, мультифолликулярные яичники;
- плохое питание, аутоиммунные заболевания (эутериоз, аутоиммунный токсический зоб, заболевания соединительной ткани) [2] .
Очаговая алопеция не заразна. Семейные случаи возможны, если у кого-то из первой линии родства было данное заболевание [6] . Убедительные доказательства взаимосвязи генетики и повышенного риска развития генёздной алопеции были найдены при изучении семей, где двое или более родственников страдали от выпадения волос. Это исследование выявило, по крайней мере, четыре области в геноме, которые, вероятно, содержат эти гены [7] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы очаговой алопеции
Клиническая картина специфична и имеет непосредственную связь с клиническими разновидностями форм очаговой алопеции. Типичными первыми симптомами являются небольшие залысины в виде одного или нескольких чётко очерченных очагов, которые чаще появляются в затылочной области. Количество очагов и их величина могут быть самыми различными (от одного небольшого очага до полной потери волос). На поредевших участках кожа не повреждена и внешне выглядит здоровой. Пятна могут быть различной формы, обычно они круглые или овальные [8] .
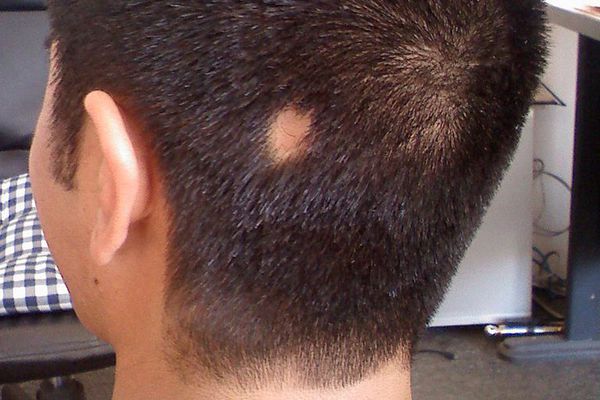
Следующие очаги возникают в отдалении от первого и нередко носят симметричный характер. Они имеют склонность к периферическому росту (увеличению очага по краям), очаги сливаются и образуют большие участки облысения. Выпадение чаще всего наблюдается на коже головы и бороды, но может возникать на любой части тела с волосами [9] .
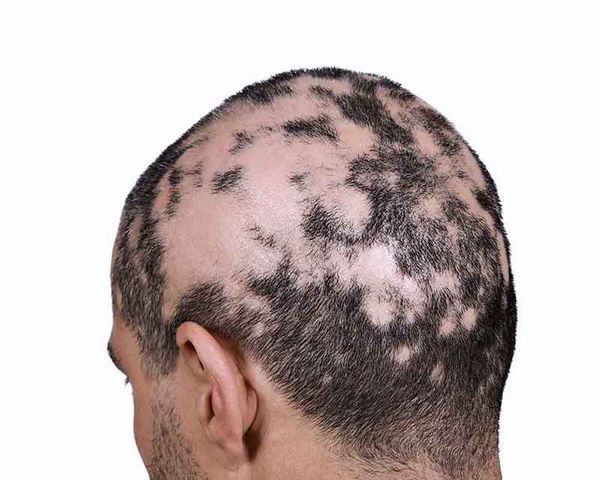
Область выпадения волос иногда сопровождается субъективными симптомами: покалыванием или болезненностью [10] . Волосы обычно выпадают в течение короткого периода времени, причём обычно с одной стороны выпадает больше волос, чем с другой. В очагах часто присутствуют так называемые "конические волоски" с более узким стержнем у корня, этот трихоскопический симптом еще называют "восклицательный знак" [9] . Такие волосы очень короткие (3-4 мм) и могут находиться вокруг проплешин [10] .
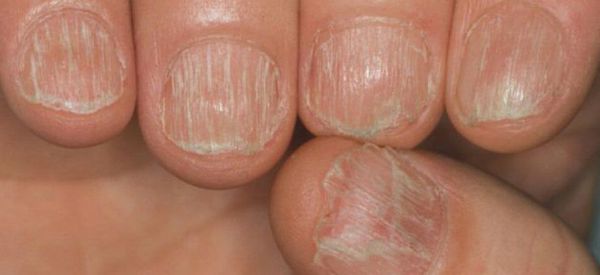
Болезнь может перейти в ремиссию на некоторое время или может быть постоянной. Патология имеет доброкачественное волнообразное течение (обратимый характер), волосы, как правило, отрастают на фоне лечения. Но при длительном существовании очагов без терапии волосяные фолликулы (луковицы) атрофируются и процесс приобретает злокачественную затяжную форму (необратимый характер). Зачастую выпадение волос появляется в тандеме с дистрофическими изменениями ногтевых пластин и носит название "трахионихия".
Патогенез очаговой алопеции
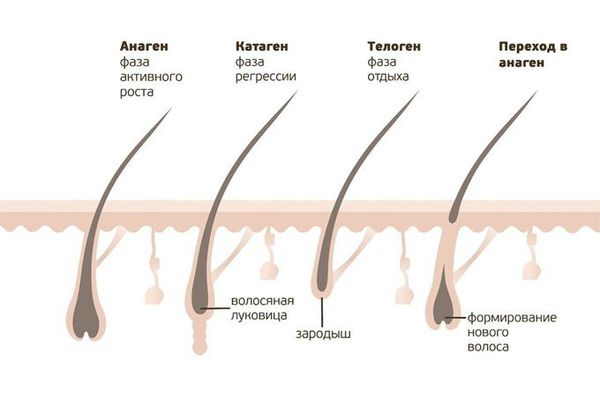
Основной механизм патогенеза очаговой алопеции включает разрушение луковиц волоса собственными иммунными клетками [2] . Организм ошибочно атакует собственные анагенные (находящиеся в фазе роста) волосяные фолликулы и подавляет или останавливает рост волос [9] . Например, Т-клеточные лимфоциты (клетки, отвечающие за защитную функцию организма) скапливаются вокруг поражённых фолликулов и в дерме, вызывая воспаление и последующее выпадение волос.
Запускается каскад цепных реакций: нарушение процессов кератинизации (шелушения), деструкция и гибель стержней волос, истощение репаративного (восстановительного) потенциала, затем при длительном течении алопеции (более двух лет) процесс репарации волосяного фолликула сопровождается его атрофией с развитием склеротических изменений (заменой нормальной ткани на соединительную) и склерозированием микрососудов. Было высказано предположение, что волосяные фолликулы в здоровом состоянии защищены от иммунной системы так называемой "иммунной привилегией" [4] [19] .
Развитие алопеции также связано с нарушением усвоения организмом серосодержащих соединений, которые изменяют процесс кератинизации волос и приводят к патологическим изменениям в их структуре [11] .
Классификация и стадии развития очаговой алопеции
Как правило, гнёздная потеря волос включает в себя следующие клинические разновидности:
- Локальная (ограниченная) форма описывает облысение только в одном месте [9][12] . Это может произойти на любом участке волосистой части головы.
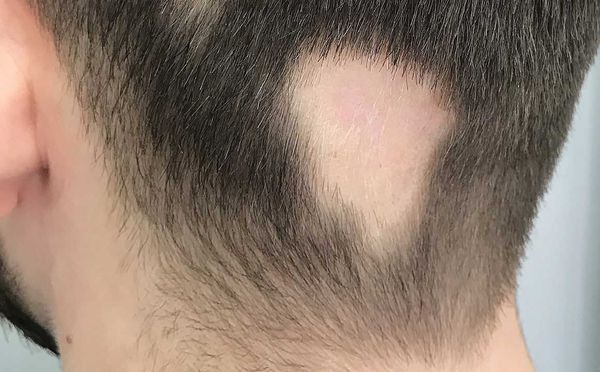
- Субтотальная форма — на голове отсутствует более 40 % волос. При офиазисе (отсутствии волос полностью по краевой зоне роста волос) очаги имеют лентовидную форму, затрагивают всю краевую зону роста волос в затылочных и височных областях по форме волны. При инверсном офиазисе очаги лентовидной формы распространяются на лобно-теменную и затылочные области.
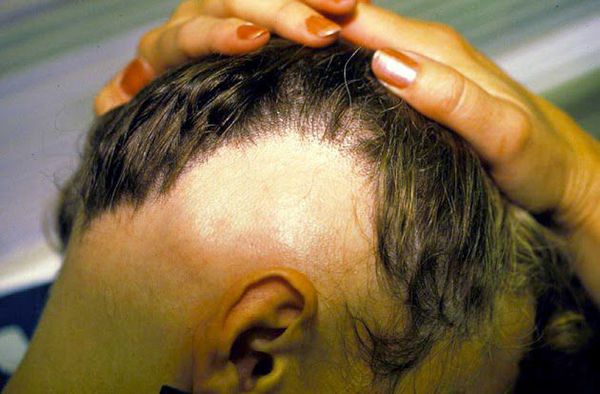
- Диффузная алопеция — волосы выпадают более рассеянно, рассредоточено по всей коже головы [9] .
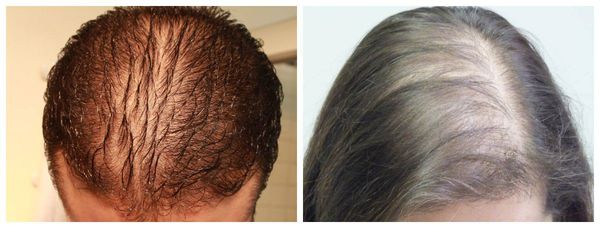
- Alopecia areata barbae — форма заболевания, при которой выпадение волос ограничивается только бородой [9] .

- Тотальная алопеция (areata totalis, или облысение) — характеризуется полной потерей терминальных (тёмных, жёстких и длинных) волос на волосистой части головы [2] .

- Alopecia areata universalis (универсальная) — такой диагноз ставится, если выпадают все волосы на теле, включая лобковые волосы [2] .
Тотальная и универсальная формы встречаются редко [13] .
Заболевание имеет несколько стадий.
- Активная стадия (проградиентная, прогрессирующая). Во время активной стадии типичные очаги поредения представляют собой участки нерубцового облысения округлой или овальной формы с неизменённым цветом кожи. Для оценки состояния волос проводится тест на натяжение волос. Н еобходимо захватить небольшой пучок волос (50-60 волос) между большим и указательным пальцами и с некоторым усилием, но не очень резко, потянуть волосы. Если в руках остаётся больше 10 % волос (более 6 волос), тест свидетельствует о наличии патологического выпадения волос (положительный тест). Меньшее количество извлечённых волос (до 2 шт.) свидетельствует о физиологическом выпадении волос. Процедуру следует провести в 4 зонах: в теменной области слева и справа, в лобной и затылочной области. В активной фазе заболевания на границах поражений тест на натяжение волос может быть положительным — это зона "расшатанных волос" . На начальном этапе выпадение не затрагивает седые волосы.
- Стационарная стадия — просуществовав 4–6 месяцев, процесс слияния мелких очагов в крупные приостанавливается.
- Стадия регресса — в очагах облысения восстанавливается нормальный рост волос.
Осложнения очаговой алопеции
На сегодняшний день гнёздная алопеция имеет доброкачественное течение. Она не влечёт за собой потерю работоспособности, нарушения общего состояния, инвалидизацию, не требует длительного нахождения в стационарах, но значительно сказывается на качестве жизни и психоэмоциональном состоянии пациентов. Необходимо понимать, что процесс обратим, так как волосяные фолликулы остаются жизнеспособными [15] .
Чаще всего врач трихолог-дерматолог сталкивается с нозогенными реакциями (психогенными расстройствами) своих пациентов: людей с алопецией беспокоит изменение своего внешнего вида и потеря собственной привлекательности, жалость в глазах окружающих; пациенты часто страдают депрессивными, тревожными, социофобическими расстройствами и сенситивными (фобическими) идеями. Чаще всего депрессивные расстройства у пациентов с алопецией проявляются лёгкими формами. Кроме того, у больных могут наблюдаться тревожные расстройства с опасениями возможного прогрессирования облысения и суицидальными наклонностями [16] . Все эти состояния не зависят напрямую от степени выраженности облысения, однако они заслуживают внимания специалистов.
Диагностика очаговой алопеции
Очаговая алопеция обычно диагностируется на основании клинических признаков.
Трихоскопия (исследование волос при помощи трихоскопа, который многократно увеличивает волосы) является основным методом установления данного диагноза. Трихоскопия показывает регулярно распределённые "жёлтые точки" (гиперкератотические пробки), небольшие "восклицательные знаки" и "чёрные точки" (поражённые волоски в отверстии волосяного фолликула) [17] . Для клинической диагностики ГА часто достаточно клинических проявлений в виде очагов выпадения волос и наличия волос, обломанных по типу "восклицательных знаков". Иногда в области облысения может появиться покраснение кожи (эритема) [5] . При эффективном лечении и возобновлении роста волос появляются пушковые волосы.

В редких случаях для постановки диагноза и помощи в лечении облысения требуется биопсия. Она применяется в спорных ситуациях для дифференциальной диагностики с другими заболеваниями и когда лечение не приносит результата. Биопсия позволяет определиться с тактикой лечения и прогнозом заболевания.
Результаты гистологических исследований показывают наличие перибульбарного лимфоцитарного инфильтрата (скопления лимфоцитов) по типу "рой пчёл". Иногда в неактивных зонах облысения воспалительные инфильтраты не обнаруживаются. Ещё одним характерным признаком является недержание пигмента в луковице волоса и фолликулярных стелах (анатомической структуре волосяного фолликула), а также сдвиг в соотношении анаген-телоген в сторону телогена (стадии выпадения волос).
Определённая роль отводится клиническим лабораторным и инструментальным методам исследования. Клинический минимум должен содержать:
- Общий анализ мочи.
- Биохимический анализ крови (АЛТ, АСТ, ГГТ, щелочная фосфатаза, глюкоза, билирубин общий, билирубин прямой, общий белок, холестерин (ЛПВН, ЛПНП), триглецириды, мочевина, креатинин, мочевая кислота, коэфициент атерогенности, гликированный гемоглобин, С-реактивный белок, ревматоидный фактор, С-пептид).
- Определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека.
- Определение антигена HBsAg (позволяет выявить гепатит Б).
- Определение антител классов M, G к вирусу гепатита С.
- Проведение реакции Вассермана (анализ крови на сифилис).
- Анализ крови на волчаночный антикоагулянт (специфический маркер такого заболевания, как дискоидная красная волчанка).
- Определение антинуклеарных антител.
- Анализ крови на железо, ферритин, трансферрин, гомоцистеин, фолиевую кислоту, цинк, селен, медь, магний, витамин В12, витамин Д.
- Анализ крови на гормоны: инсулин, гормоны щитовидной железы (ТТГ, Т3 свободный, Т4 свободный, антитела к тиреопераксидазе, антитела к тиреоглобулину).
Такой большой список показателей нужен для того, чтобы разобраться, что именно вызывает потерю волос. Необходимо исследовать каждый обмен веществ: липидный, углеводный, гормональный, белковый и исключить все метаболические нарушения.
По показаниям проводятся:
- Трихологический генетический тест (делается соскоб эпителиальных клеток слизистой полости рта с области щеки в специальную пробирку, где анализируется геном).
- Спектральный анализ волоса на микроэлементы (производится забор волоса с области затылка и отправляется в лабораторию на исследование нехватки или переизбытка микроэлементов).
- Соскоб на грибы с кожи волосистой части головы.
- УЗИ щитовидной железы.
- УЗИ сосудов шеи.
- МРТ головного мозга.
По мере необходимости для исключения очагов хронической инфекции пациент направляется на консультации к смежным специалистам [14] .
Лечение очаговой алопеции
При отсутствии на голове более 25 % волос необходимо осматривать состояние волосяного покрова на туловище и конечностях. Если в данных областях тоже наблюдается выпадение, это необходимо учитывать при выборе метода лечения. Также выбор терапии формируется с учётом формы, стадии, длительности процесса и возраста больного.
Сложность патологии в том, что ни один из существующих терапевтических вариантов не является на 100 % эффективным [18] , но если назначена адекватная терапия, то волосы во многих случаях могут самопроизвольно отрасти.
В некоторых случаях выпадения волос успеха можно достичь при помощи стероидных препаратов (кортикостероидов) в виде крема, мази, лосьона клобетазол, мометазон фуроат и инъекций кортикостероидов. Применение только кортикостероидных кремов на коже в области выпадения не так эффективно и требует больше времени для получения результатов. Стероидные вещества топического (местного) применения обычно используются на небольших зонах выпадения волос. Раствор биматопроста 0,03 % применяется только для бровей и ресниц. Препарат хорошо переносятся, он безопасен и эффективен при выпадении бровей и ресниц [20] [21] .
У применения кортикостероидов есть и недостатки: они часто не могут проникнуть в кожу достаточно глубоко, чтобы повлиять на луковицы волоса [7] . Пероральные кортикостероиды могут уменьшить выпадение волос, но только на период, в течение которого они принимаются, кроме того, эти препараты могут вызвать серьёзные побочные эффекты [7] .
При выпадении волос применяют также миноксидил, различные раздражители (пентоксифиллин, раствор никотиовой кислоты, красный перец), пептидные комплексы, средства стимулирующие рост волос, но только не в прогрессирующую стадию. В более тяжёлых случаях и при отсутствии эффективности лечения топическими стероидами назначают иммунотерапию циклоспорином и/или метотрексатом, иногда их применяют в различных комбинациях.
Физиотерапевтические методы лечения имеют определённую роль в лечении гнёздной алопеции, их применяют для лучшего проникновения лекарственных препаратов к волосяному сосочку. С этой целью назначают электрофорез (лечение микротоками), лазерную терапию, узкополосную фототерапию (лечение узкополосным светом).
Необходимо отметить, что ни одно лечение не является эффективным во всех случаях, и иногда ответа на лечение вообще может не быть. С чем это связано неизвестно.
Прогноз. Профилактика
В большинстве случаев, когда болезнь начинается с небольшого количества участков выпадения волос, волосы отрастают через несколько месяцев, иногда в течение года [8] . Если поражения более обширные, волосы либо отрастают в ответ на лечение, либо продолжают выпадать, вплоть до тотальной или, в редких случаях, универсальной алопеции [8] .
Особенность патологии в том, что спустя какое-то время после успешного лечения, волосы снова могут выпадать. У 85 % больных отмечается более одного эпизода заболевания, периоды ремиссии различны. Эпизоды очаговой алопеции до наступления полового созревания предрасполагают к хроническому течению заболевания [7] . Алопеция иногда становится причиной психологического стресса. Поскольку выпадение волос может привести к значительным изменениям во внешности, люди могут испытывать социальную фобию, тревогу и депрессию. Пациенты с выпадением волос требуют немедленного назначения лечения.
Специфической профилактики алопеции не существует. Рекомендуется вести здоровый образ жизни, правильно питаться, своевременно лечить хронические заболевания. По показаниям следует принимать витаминно-минеральные комплексы. Важно подобрать качественные средства для ухода за волосами, также в качестве метода профилактики можно посоветовать отказаться от плетения тугих косичек.
ГБОУ ВПО РНИМУ им. Н.И. Пирогова Минздравсоцразвития РФ, Москва
Российский государственный медицинский университет, Москва
Российский государственный медицинский университет им. Н.И. Пирогова
Современный взгляд на проблему лечения витилиго
Журнал: Клиническая дерматология и венерология. 2012;10(2): 118‑123
Усовецкий И.А., Шарова Н.М., Короткий Н.Г. Современный взгляд на проблему лечения витилиго. Клиническая дерматология и венерология. 2012;10(2):118‑123.
Usovetskiĭ IA, Sharova NM, Korotkiĭ NG. The current view of the problem of vitiligo therapy. Klinicheskaya Dermatologiya i Venerologiya. 2012;10(2):118‑123. (In Russ.).
ГБОУ ВПО РНИМУ им. Н.И. Пирогова Минздравсоцразвития РФ, Москва
Представлены результаты собственных исследований, посвященных особенностям клинического течения разных форм витилиго, некоторым патогенетическим аспектам развития данного заболевания и оценке клинической эффективности комплексной терапии сегментарной и несегментарной формы витилиго.
ГБОУ ВПО РНИМУ им. Н.И. Пирогова Минздравсоцразвития РФ, Москва
Российский государственный медицинский университет, Москва
Российский государственный медицинский университет им. Н.И. Пирогова
Витилиго характеризуется внезапным возникновением депигментированных пятен вследствие нарушения секреторной функции меланоцитов или их гибели, развивается у лиц с генетической предрасположенностью, сопровождается выраженными дисрегуляторными изменениями клеточно-опосредованных реакций иммунной системы, вегетативного дисбаланса с преобладанием симпатического тонуса и серьезной социальной дезадаптацией, обусловленной личностными особенностями и внешними социальными факторами.
Витилиго является распространенным дерматозом. В мире число больных с данным заболеванием превышает 1% всего населения. В 70% случаев заболевание начинается в возрасте 10—25 лет, дети младше 10 лет, в том числе новорожденные и грудного возраста, составляют приблизительно 25% всех больных витилиго [1]. Витилиго может возникнуть в любом возрасте, длиться неопределенно долго, самопроизвольное восстановление нормальной окраски кожи наблюдается редко.
Причины появления депигментированных очагов не известны. Недостаточно понятно, в результате каких нарушений резко прекращается синтез меланина и погибают меланоциты. Разные эндогенные и экзогенные факторы могут оказывать прямое и опосредованное повреждающее действие на меланоциты.
Среди внешних факторов наибольшее значение придают инфекционным и токсическим агентам, чрезмерному ультрафиолетовому облучению, стрессам. На протяжении многих десятилетий витилиго связывали с аутоиммунным тиреоидитом, ревматоидным артритом, красной волчанкой, атопическим дерматитом, заболеваниями печени инфекционного или токсического генеза, глистной инвазией и рядом врожденных синдромов [2]. Однако частота встречаемости витилиго у этих больных не выше, чем в популяции в целом. Ряд авторов [3, 4], подводя итоги многолетним исследованиям, считают, что больные витилиго в большинстве случаев не имеют никаких тяжелых или хронических сопутствующих заболеваний, а терапия выявленных у 28% больных функциональных расстройств органов пищеварения, вегетососудистой дистонии не оказывала влияния на результат репигментации.
Многие исследователи считают [5, 6], что витилиго является серьезным косметическим дефектом, возникает у лиц с генетической предрасположенностью и в у большинстве случаев, перенесших эмоциональные расстройства. Лишь у 4—7% больных витилиго сочетается с аутоиммунным тиреоидитом.
В современных генетических исследованиях продемонстрирована связь возникновения витилиго с разными аспектами наследования. Среди спорадических случаев витилиго в европейской популяции средний возраст возникновения заболевания составляет 24,2 года, тогда как в семьях с множественными случаями заболевания средний возраст составляет 21,5 года (статистически достоверные различия) [7]. Более раннее начало заболевания в «семейных» случаях и риск заболевания у отдаленных родственников является типичной характеристикой полигенного заболевания. Около 20% больных витилиго имеют не менее одного кровного родственника с подобным заболеванием. Формально-генетический сегрегационный анализ витилиго определяет существование многих локусов, нарушения в которых формируют предрасположенность к витилиго. Однако не обнаружены ключевые гены, ответственные за манифестацию, прогрессирующее течение или предрасположенность к данному заболеванию.
При витилиго обнаружено снижение антиоксидантного потенциала, приводящего к активному повреждающему воздействию на меланоциты свободных радикалов и накоплению продуктов перекисного окисления липидов [8, 9]. Позднее выяснилось, что свободные радикалы оказывают повреждающее действие на разные клетки, участвующие в воспалительных реакциях разного типа, и нарушения антиоксидантной защиты не являются основными механизмами депигментации при витилиго.
Теория нарушений иммунных механизмов регуляции является наиболее обоснованной. При длительном течении и распространенном патологическом процессе наблюдаются изменения в субпопуляционном составе Т-лимфоцитов. Одновременно с этим, особенно на начальных стадиях заболевания, повышаются уровни активационных рецепторов лимфоцитов, отражающие степень активации иммунокомпетентных клеток [10]. В настоящее время большинство исследователей полагают, что ведущая роль в развитии аутоиммунных заболеваний принадлежит клеточно-опосредованным реакциям, при которых наблюдается выраженный дисбаланс цитокинов. При витилиго выявляется снижение активности регуляторных Т-лимфоцитов, что подтверждается уменьшением количества трансформирующего фактора роста-β (TGF-β) и интерлейкина-10 (ИЛ-10) в сыворотке крови больных [11].
Лечение витилиго является сложнейшей задачей. Так как причины его возникновения неизвестны, в большинстве случаев заболевание развивается на фоне полного физического благополучия. Предлагается применять в основном топические стероиды и/или иммуномодуляторы при площади поражения до 20%, а также длительную фототерапию [12, 13]. В комплексную терапию включают ферментные препараты, гепатопротекторы, витамины и микроэлементы (цинк, медь) [14, 15]. В ряде рекомендаций содержатся сведения о применении седативных и антидепрессивных средств.
Цель настоящего исследования — изучение клинических особенностей течения витилиго и эффективности комплексной терапии, включающей иммуномодулирующий компонент — тимоген и наружно 1% пимекролимус, и коррекцию аффективных расстройств у больных разными формами витилиго с использованием препарата антидепрессивного действия агомелатин.
Материал и методы
Все больные разными формами витилиго были полностью обследованы (проведены клинические анализы крови и мочи, биохимический анализ крови, ультразвуковое исследование органов брюшной полости и щитовидной железы, гормоны щитовидной железы Т3, Т4, тиреотропный гормон — ТТГ и антитела к тиреоидной пероксидазе — АТ-ТПО по показаниям, консультация невропатолога по показаниям, консультация психиатра, иммунологические исследования — популяционный и субпопуляционный состав лимфоцитов, уровень провоспалительных и регуляторных цитокинов).
Результаты
Под нашим наблюдением с 2006 по 2011 г. находились 84 больных витилиго (46 женщин, 38 мужчин) в возрасте от 18 до 56 лет.

Давность заболевания варьировала от 6 мес до 30 лет, средняя продолжительность составила 6,5±4,8 года. Среди вероятных причин развития витилиго большинство больных называли перенесенный стресс (39 пациентов, 46%). Витилиго возникло после оперативных вмешательств у 3 (3,5%) пациентов, после травм — у 4 (4,5%). По мнению 4 (5%) женщин, впервые депигментированные пятна появились у них после родов, в период лактации, причем 1 пациентка отмечала, что после 2- и 3-х родов увеличивалась площадь поражения и появлялись свежие очаги. У 14 (17%) больных заболевание возникло после воздействия длительного ультрафиолетового излучения, 20 (24%) пациентов не могли связать появление депигментированных пятен с какими-либо значимыми причинами (рис. 1). Рисунок 1. Вероятные причины развития витилиго. У 21 больного среди ближайших родственников имелись проявления витилиго разной давности и степени распространенности, у 2 из них, помимо поражений кожи были обесцвечены участки волос.
При обследовании больных витилиго обнаружено, что наиболее часто (у 48 больных, 57,1%) встречаются дискинезия желчевыводящих путей и желчекаменная болезнь, хронический холецистит, жировой гепатоз. Гастрит обнаружен у 16 (19%) больных. В процессе обследования патология щитовидной железы (аутоиммунный тиреоидит, диффузный токсический зоб, кисты щитовидной железы) выявлена или подтверждена у 13 (15,4%) больных витилиго. Только у 4 больных из 13 с патологией щитовидной железы были обнаружены АТ-ТПО, что подтверждало диагноз аутоиммунный тиреоидит.

Гинекологические заболевания (дисфункциональные нарушения менструального цикла, миома) обнаружены у 5 (5,9%) женщин. У 10 (11,9%) больных подтверждена гипертоническая болезнь I—II степени, у 1 (1,2%) выявлен сахарный диабет 2-го типа, у 3 (3,5%) обнаружено алиментарное ожирение II—III степени. Достоверных отклонений от нормальных значений в клинических анализах крови не обнаружено. Тяжелых хронических заболеваний или декомпенсированных состояний у больных витилиго не выявлено (табл. 1).
Мы наблюдали за больными с разными формами витилиго (табл. 2). Среди них 7 (8,3%) больных имели сегментарную форму с площадью поражения 2% (рис. 2). Рисунок 2. Сегментарная форма витилиго. Вульгарная форма наблюдалась у 44 (52,3%) больных. В этих случаях площадь поражения составляла 3—70% площади кожного покрова (рис. 3, а, б). Рисунок 3. Пациентка (а) и пациент (б) с вульгарной формой витилиго. Отдельную группу составили больные с акрофациальной формой (31 человек, 36,9%) с депигментированными очагами на лице и конечностях (рис. 4, а—в). Рисунок 4. Акрофациальная форма витилиго (а—в). У 10 (11,9%) пациентов при клиническом обследовании обнаружены невусы Сеттона (рис. 5). Рисунок 5. Невусы Сеттона.
Витилиго является серьезной психологической проблемой [16, 17]. При исследовании уровня тревожности методом Спилбергера—Ханина низкий уровень реактивной тревожности наблюдается у 52 (61,9%) больных, а у 32 (38,1%) — умеренно выраженная реактивная тревожность. У 55 (77,4%) больных витилиго отмечен высокий уровень личностной тревожности, причем он не зависел ни от площади поражения, ни от давности заболевания. Наличие депрессивных расстройств подтверждены с помощью госпитальной шкалы Гамильтона (средний показатель 13,9±2,4 балла) и шкалы Бека (средний показатель 22,4±2,8 балла). У большинства обследованных выявлялись депрессивные расстройства невротического уровня, характеризующиеся подавленностью настроения, нарушением сна, тревожными и астеническими проявлениями.
Таким образом, в ходе обследования каких-либо тяжелых сопутствующих заболеваний не выявлено. По данным литературы, аффективные и вегетативные нарушения наблюдаются практически у всех больных витилиго и требуют адекватной коррекции.
При иммунологическом исследовании, проведенном 25 больным витилиго, обнаружены достоверные отклонения от контрольных значений в субпопуляционном составе Т-лимфоцитов и дисбаланс провоспалительных цитокинов (табл. 3; рис. 6). Рисунок 6. Содержание цитокинов в сыворотке больных витилиго. Примечание. ИЛ-2, ИЛ-8, ФНО-α, ИФН-γ, ИЛ-10 в пг/мл; TGFβ, в нг/мл. Так, содержание CD8+ в крови больных витилиго было достоверно выше, чем у здоровых, иммунорегуляторный индекс (ИРИ) также имел достоверные отличия от контрольных значений. В сыворотке крови больных витилиго обнаружено повышенное содержание ИЛ-2, ИЛ-6, ИЛ-8 и фактора некроза опухоли-α (ФНО-α), интерферона-γ (ИФН-γ) на фоне низкого уровня регуляторных цитокинов TGF-β и ИЛ-10 по сравнению с контролем.
Комплексное лечение больных проводили с учетом клинических особенностей витилиго, в том числе давности, распространенности и активности патологического процесса. Использовали направленную иммуномодулирующую терапию — тимоген (назальный спрей по 1 мл/сут в течение 20 дней) и пимекролимус (1% крем 2 раза в сутки в течение 4—6 мес). Психокорригирующую терапию проводили агомелатином, который является агонистом мелатонина (МТ1- и МТ2-рецепторов) и антагонистом 5НТ2с. Агомелатин больные витилиго принимали по 25 мг/сут 1 раз в день не менее 6 нед. После консультации психиатра 5 больным с умеренно выраженными признаками депрессии агомелатин был назначен в суточной дозе 50 мг на 12—24 нед.
Мы провели комплексное лечение 57 больным разными формами витилиго (3 пациента — с сегментарной формой, 25 — с акрофациальной, 29 — вульгарной).
У всех больных с сегментарной формой витилиго 100% репигментация наблюдалась через 4 мес после начала терапии.
У больных акрофациальной формой полная клиническая ремиссия отмечена в 16 (64%) случаях через 5 мес терапии. Значительное улучшение со 100% репигментацией большинства очагов и уменьшением площади очагов депигментации более чем на 60% имелось у 7 пациентов. Незначительная эффективность отмечена у 2 больных, причем полностью восстановилась нормальная окраска кожи в периорбитальных и периоральной областях, на тыльной поверхности кистей и в области фаланг площадь депигментированных очагов практически не изменилась, частично (до 40%) уменьшилась площадь очагов в области голеностопных суставов.
Положительные изменения после проведенной комплексной терапии наблюдались у всех больных вульгарной формой витилиго. Клиническая ремиссия отмечалась у 20 из 29 больных данной группы.
В течение первых 3 мес терапии (12 нед) у этих пациентов началась активная репигментация очагов, площадь которых сокращалась на 30—60%. К концу 6-го месяца цвет кожи восстановился полностью.

У 6 больных наблюдалось сокращение площади депигментированных очагов на 50—70% за счет полной репигментации отдельных очагов и частичного восстановления нормального цвета кожи отдельных участков. У 3 пациентов отмечались незначительные позитивные изменения, которые выражались в восстановлении пигментации свежих, небольших по площади участков (не более 2 см 2 ), сглаживании границ по периферии очагов депигментации (табл. 4).
Все больные хорошо переносили лечение, побочных эффектов, осложнений, отказов от терапии не было. В процессе терапии удалось изменить отношение пациентов к своему заболеванию, оценить позитивные изменения в процессе лечения. На фоне активной репигментации очагов нормализовались иммунологические показатели и произошла редукция признаков депрессивных расстройств.
Таким образом, полученные нами результаты свидетельствуют о возможности обоснованного эффективного и безопасного лечения витилиго.
Республиканский специализированный научно-практический медицинский центр дерматологии и венерологии Министерства здравоохранения Республики Узбекистан, Ташкент
Республиканский научно-практический медицинский центр дерматологии и венерологии Министерства здравоохранения Республики Узбекистан, Ташкент
Хирургические методы лечения витилиго
Журнал: Клиническая дерматология и венерология. 2013;11(1): 84‑90
Сабиров У.Ю., Ибрагимов Ш.И. Хирургические методы лечения витилиго. Клиническая дерматология и венерология. 2013;11(1):84‑90.
Sabirov UIu, Ibragimov ShI. Surgical techniques for vitiligo treatment. Klinicheskaya Dermatologiya i Venerologiya. 2013;11(1):84‑90. (In Russ.).
Республиканский специализированный научно-практический медицинский центр дерматологии и венерологии Министерства здравоохранения Республики Узбекистан, Ташкент
В статье описаны современные принципы лечения витилиго и хирургические методы коррекции.
Республиканский специализированный научно-практический медицинский центр дерматологии и венерологии Министерства здравоохранения Республики Узбекистан, Ташкент
Республиканский научно-практический медицинский центр дерматологии и венерологии Министерства здравоохранения Республики Узбекистан, Ташкент
Витилиго — приобретенное заболевание кожи, проявляющееся ее депигментацией. Прогноз и терапия пациентов с витилиго непредсказуемы. Существует много методов его лечения, но эффективного не выработано. Причиной возникновения заболевания является взаимодействие генетических факторов, связанных с иммунной системой и самими меланоцитами. Вследствие этого взаимодействия, спровоцированного определенными факторами, и развивается меланоцитарная деструкция. Успехи, достигнутые в понимании этиологии витилиго, будут способствовать разработке новых методик лечения данного заболевания [1].
По мере расширения технических возможностей в изучении морфологических и биохимических процессов в меланоцитах, дерматологическая наука получает новые данные о патогенезе и этиологии витилиго. Однако многие аспекты этих вопросов не выяснены. Например, еще неизвестны причины развития заболевания, оптимальное лечение, способное нормализовать нарушенные процессы [2].
Пока механизмы развития витилиго полностью не раскрыты, лечение данного заболевания является достаточно трудной задачей. В настоящее время основная цель терапии витилиго — устранение косметического дефекта и восстановление общей равномерной пигментации кожного покрова. Для этого используют разные методы как местные, так и системные (кортикостероиды, фото- и витаминотерапию, пересадку меланоцитов, лечение лазером, депигментацию кожи, солнцезащитные средства). Выбор метода лечения зависит от размеров и локализации депигментированных очагов, степени активности патологического процесса, соматического статуса пациента и предпочтения того или иного метода самим больным [1].
Знания о патогенезе витилиго увеличиваются. Его терапия направлена на предотвращение разрушения меланоцитов и стимуляцию резидуальных меланоцитов, способствующих репигментации.
Ограниченную форму витилиго лечат топическими стероидами, которые подавляют иммунную систему: снижают содержание иммуноглобулинов и их комплементов [3], а также топические ингибиторы кальциевых каналов, например, такролимус, который угнетает Т-клетки, замедляя регуляцию кодирующих генов провоспалительных цитокинов [4]. Кроме того, в исследованиях in vitro показано прямое действие такролимуса на кератиноциты, что создает благоприятные условия для меланоцитов, роста и миграции меланобластов [5—7].
При генерализованной форме витилиго в качестве первой линии терапии используют ультрафиолетовые лучи (UVA и UVB). Механизм их действия связан с иммуносупрессией и стимуляцией миграции и размножения меланоцитов. UVB активизируют Т-супрессоры, которые, в свою очередь, подавляют аутоиммунное состояние [8]. Плазма пациентов после UVA-терапии содержит высокий уровень фактора роста фибробластов (bFGF), стволового клеточного фактора и фактора роста гепатоцитов, которые также создают благоприятные условия для роста меланоцитов [9]. Пероральный псорален и UVA увеличивают количество резидуальных меланоцитов в основном за счет фактора роста меланоцитов, таких как bFGF и эндотелин 1 [10], и стимулируют миграцию пигментных клеток вдоль наружного корня волосяного фолликула к эпидермису.
Системные кортикостероиды используют не все врачи и только в случае, если витилиго быстро прогрессирует. Механизм их действия заключается в снижении содержания антител, токсичных к пигментным клеткам [11].
На фармацевтическом рынке имеется не так много терапевтических средств, которые могут длительно предотвращать меланоцитарное разрушение и при этом не вызывать значительных побочных осложнений. Кроме того, важным условием применения этих средств является обязательное наличие (в начале лечения) резидуальных меланоцитов в форме меланоцитарного резерва, чтобы достигнуть пролиферации и получить необходимый клинический эффект. Многие исследователи установили присутствие меланоцитарного резерва в нижней трети волосяного фолликула. Результаты исследований C. Loomis и соавт. [12] свидетельствуют о том, что меланоцитарные стволовые клетки выявляются в выпуклой зоне около входа мышцы волосяного фолликула. Важность меланоцитарного резерва клинически доказана тем, что при лечении на лице и шее достигается максимальный клинический эффект в отличие от конечностей и туловища. Акральные части конечностей и не волосистые части тела (локти, ноги, мужские гениталии) плохо подвергаются репигментации [13]. По данным A. Dutta и S.Mandal [14], присутствие лейкотрихии также является плохим прогностическим признаком.
В последние годы возобновились исследования по трансплантологии в виде аутотрансплантатов как кожи, так и аутологичных меланоцитов [15].
Примерно 30 лет назад витилиго лечили только консервативно. Первые результаты хирургического лечения данного заболевания были опубликованы P. Behl [16, 17] и R. Falabella [18].
Тканевая пересадка, или обычный метод пересадки кожи в форме покрышки пузырей, лоскута кожи или панч-пересадки не вовлекает клеточное разделение in vitro, и меланоциты стимулируют с помощью ультрафиолетовых лучей, чтобы усилить их распространение на пересаженном участке.
Мини- или панч-пересадку осуществляют следующим образом: биопсийный материал, предпочтительно с бедренной части, устанавливают внутрь отверстий, созданных схожими инструментами в необходимом месте, и укрепляют специальными покрытиями, которые удаляют через 7—14 сут. Основы проведения процедуры были впоследствии модифицированы для того, чтобы уменьшить побочные эффекты, увеличить пролеченную область, усилить и улучшить пигментацию. Размер трансплантатов — 1—3 мм, они устанавливаются на расстоянии 3—10 мм (расстояние определяют типом кожи и размером трансплантата) [3, 19]. Трансплантаты темнокожих пациентов могут быть расположены через 5—10 мм вдоль, благодаря меланоцитам, которые продуцируют крупные меланосомы. Однако у пациентов с 3-м и 4-м типами кожи меланоциты трансплантируются вдоль через 3—5 мм, так как они продуцируют мелкие меланосомы [19]. Булыжная мостовая (побочный эффект, который в основном наблюдается при этом методе) может быть предотвращена имплантированием трансплантатов по размеру больших, чем произведенные отверстия, удалением излишней жировой ткани со дна трансплантата [19] или созданием отверстий в месте введения на 1 мм глубже, чем толщина трансплантата. После пересадки обычно рекомендуется фототерапия для усиления распространения пигмента.
Показано положительное действие миниграфтинга (панч) при лечении локализованной формы витилиго: из 13 пациентов, у которых была достигнута 90—100% репигментация, лишь у 2 отмечен частичный эффект, и у 2 эффекта не наблюдалось, так как изначально они имели негативный миниграфт-тест. В целом у 23 пациентов (36 очагов) была оценена эффективность миниграфтинга при вульгарной форме витилиго: в 14 очагах получено 80—99% репигментации, в 12 — до 50%. По результатам проспективного исследования S. Malakar и S. Dhar у 880 (74,5%) пациентов репигментация достигнута в 90—100%, у 10,6% распространения пигмента не наблюдалось, а у 2,4% пациентов трансплантаты депигментировались.
Эпидермальная пересадка заключается в следующем: эпидермис из среза покрышек пузырей (получены путем негативного давления 300—500 мм рт.ст. на нормальную пигментированную кожу) переносят в место пересадки (аналогичный пузырь) и накладывают повязку на 7 суток. Эта техника впервые была описана U. Kistala [20] и впервые использована для лечения лейкодермы/витилиго Р. Фалабеллой [21]. С того времени было создано много аппаратов для манипуляций — масляный, вакуумный, соединенный с манометром [22], ручное аспирационное устройство с прозрачными пластиковыми чашками [23], одноразовые шприцы, прикрепленные к трехклапанному крану с трубкой, покрытой латексом и 50 мл шприцом для получения пузырей на донорской и реципиентной частях тела. Пузыри на обеих частях создают одновременно в течение 2—3 ч. Однако этот период может быть сокращен, если применять тепло и выбирать кожу над костными выступами [24].
M. Koga [22] произвел эпидермальную пересадку у 31 пациента с сегментарной формой витилиго и у 14 с вульгарной формой и наблюдал за ними в течение 6 мес. При сегментарной форме у 25 пациентов была достигнута нормальная репигментация, у 4 — частичный эффект, а у 2 — эффекта не было. У 11 больных с вульгарной формой изначально наблюдалась репигментация, но затем у 3 пигмент постепенно исчезал. S. Mutalik [23] указывал на хорошую репигментацию у 48 из 50 пациентов с локализованной стабильной формой витилиго, пролеченной эпидермальной пересадкой в течение 3-4 мес после трансплантации. В ретроспективных неконтролируемых исследованиях [25] положительные результаты были получены при генерализованной и сегментарной/фокальной формах витилиго (в 53 и 91% случаев соответственно).
Преимущества эпидермальной пересадки заключаются в минимальном образовании рубцов и хорошем косметическом результате. Однако этот метод занимает много времени и его можно использовать только на небольших участках во время одной хирургической манипуляции.
Пересадка кожи — самый первый метод, использованный для хирургического лечения витилиго. Для отбора лоскута кожи используют специально приспособленные аппараты: они переносят лоскут на подготовленную кожу путем лазерной абляции или дермабразии. Затем перенесенный лоскут покрывается хирургическим покрытием, который удаляется через 1 нед. По данным P. Behl [16], отличная репигментация наблюдалась у 70% пациентов. Преимущество метода заключается в том, что большие очаги могут быть вылечены при одной хирургической манипуляции. Однако соотношение донорской и реципиентной частей остается 1:1 и больничные расходы на лечение больших участков увеличиваются. Иногда наблюдаемое рубцевание (зависящее от опыта медицинского персонала) может быть предотвращено применением специальных инструментов. Несмотря на отличные результаты, популярность этого метода среди дерматологов невысока, его в основном используют хирурги.
При клеточной пересадке культивированных и некультивированных меланоцитов используют меланоциты, приготовленные в клеточной среде в виде суспензии, которые трансплантируют в место пересадки.
В настоящее время дерматологи Узбекистана используют хирургические методы лечения и в своей практике применяют пересадку аутологичных некультивированных меланоцитов. По нашим данным, пересадку меланоцитов проводили 21 больному (11 мужчинам, 10 женщинам) в возрасте 17—50 лет с сегментарной формой витилиго и длительностью заболевания от 1 мес до 16 лет. Стабильность очага поражения была не менее 1 года, максимальная зона поражения депигментированного очага — 110 см 2 , минимальная — 3 см 2 . Общая площадь проведенной трансплантации составила 715 см 2 (в среднем 34 см 2 у каждого пациента). У 16 пациентов после проведенной пересадки наблюдался отличный результат (95—100% репигментации депигментированных очагов), у 3 пациентов — хороший (65—94%), у 1 пациента — удовлетворительный (25—64%), у 1 пациента — плохой (0—24% репигментации). Вид до и после процедуры представлен на рисунке. Рисунок 1. Клинические проявления витилиго до и после пересадки аутологичных некультивированных меланоцитов. a, б — больной А.: состояние до (a) и после (б) лечения; в, г — больная Б.: состояние до (в) и после (г) лечения; д, е — больная В.: состояние до (д) и после (е) лечения. Рисунок 2. Клинические проявления витилиго до и после пересадки аутологичных некультивированных меланоцитов (продолжение). ж, з — больная Г.: состояние до (ж) и после (з) лечения; и, к — больная Д.: состояние до (и) и после (к) лечения.
Преимущества техники клеточной пересадки —это возможность лечить большие очаги депигментации с отличными косметическими результатами.
Таким образом, дерматовенерологическая наука настоятельно рекомендует традиционное терапевтическое лечение витилиго дополнять хирургическим лечением.
Миниграфтинг (панч-пересадка), пересадка эпидермиса, лоскутное наложение кожи, пересадка культивированных и некультивированных клеток – каждая из этих манипуляций имеет свои особенности, от которых зависит достигаемый эффект. Однако есть у этих методов и общее: все они являются надежным механизмом, длительно предотвращающим разрушение меланоцитов на любых анатомических участках, стимулирующим пролиферацию и обеспечивающим отличный косметический результат. Именно поэтому хирургическое лечение все более востребовано дерматологами. На фоне обычной фармакотерапии они позволяют получить успешные результаты в 90—100% случаев. Однако следует напомнить и о том, что хирургическое лечение требует от дерматолога тщательного обследования больного и выбора метода терапии в зависимости от его индивидуальных особенностей — возраста, длительности заболевания, стабильности процесса, площади поражения и других факторов.
Читайте также:

