Крем с цинком при атопическом дерматите для детей
Обновлено: 24.04.2024
Эта проблема вызывает дискомфорт, а в некоторых случаях страх и растерянность. Симптомы дерматита могут влиять не только на здоровье, но и на работу и личную жизнь. Особенную настороженность он вызывает у молодых родителей, как и любая болезнь малыша.
Дерматитом принято называть любого рода проявления на коже отличающиеся от ее нормального состояния: покраснения, шелушение, зуд и так далее.
При появлении любых изменений необходима консультация специалиста. Стоит отметить, что 10% всех посещений дерматолога связанно именно с проявлениями дерматита. Чаще обращаются женщины в силу большего контакта с бытовой химией.
Типы дерматита
Выделяют две основных группы дерматита: контактный и аллергический.
По проявлениям контактный дерматит бывает:
Острый - начало быстрое после однократного взаимодействия с веществами которые имеют выраженные раздражающее действие.
Хронический-развивается постепенно при постоянном контакте с раздражителем в течении нескольких дней или даже лет. В данном случае причиной будут являть слабые раздражители такие как: бытовая химия, мыльные растворы, сухой воздух, пыль.
Аллергический дерматит это проявление сбоя в работе иммунной системы организма на один или несколько раздражителей проявляющееся воспалением.
Самые частые места проявлений:
- Кожа рук
- Лицо
- Шея
- Подмышки
- Волосистая часть головы
- Аногенитальная область, чаще всего у детей.
- Уши
- Голени
- Стопы
Проявления острого контактного и аллергического дерматитов очень схожи это: покраснение, отек и высыпания в виде пузырьков и волдырей и «прыщиков». Так же будет ощущаться зуд, жжение, болезненность кожи. При аллергическом дерматите проявления не будут ограничиваться местом контакта кожи с раздражителем, реакция выходит далеко за ее пределы. Как следствие необходима обязательная консультация специалиста, для подтверждения верного диагноза и лечения.
При хроническом дерматите очаги выглядят не так ярко как при остром, но также имеют отек к которым могут присоединиться: трещины, гиперпигментация и повреждения целостности кожи, желание ее чесать и щипать. Даже после устранения воздействия раздражителя процесс может продолжаться до нескольких месяцев.
Для точного установления диагноза врачу будет необходимо подробно рассказать, как, когда и после чего возникло поражение кожи. Также будут проведены кожные пробы.

Дерматитом принято называть любого рода проявления на коже отличающиеся от ее нормального состояния
Лечение
Главной целью лечения является вернуть человеку прежний комфорт и состояние кожного покрова. Приоритет в лечении контактного дерматита это выявление раздражающего фактора и устранение его. При невозможности устранить контакт, к примеру при профессиональной необходимости, должна быть подобрана адекватная и надежная защита кожи (спецодежда, перчатки, защитные крема и мази). При простом контактном дерматите эффективность гормональных мазей и кремов недостаточно. Эффективность применения селективных ингибиторов альциневрина такролимуса и пимекролимуса при указанных в статье видах дерматита не доказана в ходе контролируемых исследований.
При выраженном зуде возможно применение антигистаминных препаратов - Зодак , Кларитин , Ксестин, Эриус , Супрастинекс, Дизал, Алегра, Ксизал, Фенистил.
- Кутивейт (флутиказон пропионат) крем, мазь течение 2 недель
- Триакорт, Фторокорт (триамцинолона ацетонид)мазь 0,025%, 0,1% в течение 2 недель, начинать лечение необходимо с большей дозы , Клобетазол , Псоридерм, Диласен,Пауэркорт (клобетазола пропионат) мазь на 3–4 недели , Белодерм, Целестодерм (бетаметазона валерат) крем, мазь 2 недели
- Унидерм, Элоком , (мометазона фуроат) крем, мазь 0,1% 2 недели
Бывает так, что к течению основного дерматита может присоединиться бактериальная инфекция. В этом случает стоит подключить дополнительную местную антибактериальную терапию:
-
(фузидовая кислота) крем, гель 2% в течение 1–2 недель , Бактробан (мупироцин) мазь 2% в течение 2 недель
При отсутствии результата при лечении аллергического дерматита возможно применение иммуносупрессивных препаратов циклоспорина, азатиоприна. Применение UV-B или PUVA-терапии.
Профилактикой дерматита является понимание того, что эта реакция пожизненная и даже кратковременного контакта нужно избегать.
Памятка по уходу за кожей рук при профессиональном контактном дерматите:
- Обязательно надевайте перчатки
- Пользуетесь заменителями мыла. Мыло удаляет защитный жировой слой кожи и повреждает роговой слой кожи который удерживает в себе воду тем самым в разы увеличивает проницаемость для любых веществ. К тому же некоторые компоненты мыла сами по себе оказывают раздражающее действие.
- Избегайте потенциально раздражающих веществ
- Соблюдать рекомендации врача в течении как минимум полугода
- Не носить кольца так как они являются местом скопления раздражителя, а если все таки человек не готов отказаться от ношения, то необходимо снимать его на время работы и выполнения домашних дел.
- Так же регулярно использовать эмоленты-это вещества сходные по составу с естественной защитной жировой пленкой кожи, воздействующие на верхние слои кожи. Она бывают: натуральные, химические, синтетические.
Доступные средства повседневного ухода которые можно приобрести в любой аптеке: Бепантен , Типикрем, Эмолиум , Мустела, Липобейз, Ла-кри.
Только для взрослых: Локоид , Дермовейт, Синалар. Их необходимо наносить только на чистую сухую кожу.
Одно из новых направлений это применение корнеопротекторов. Это средства восстанавливающие целостность непосредственно рогового слоя кожи. Физиогель, Ойлайтум, Липикар , Протопик .
Занимаясь самолечением, можно нанести непоправимый вред своему здоровью, обязательно обратитесь к врачу и следуйте его рекомендациям.
Литература: Федеральные клинические рекомендации по ведению больных контактным дерматитом, Москва - 2015
Атопический дерматит - сложное многофакторное заболевание, при котором возможна недостаточность или дефицит эссенциального микроэлемента (цинка), неблагоприятно влияющая на течение болезни. Применение активированного пиритиона цинка у больных атопическим дерматитом обосновано широким спектром фармакологического действия препарата на молекулярном уровне, что позволяет достигнуть максимальной скорости его всасывания и повышения способности проникать в глубокие слои кожи. Использование активированного пиритиона цинка в комплексной терапии больных атопическим дерматитом приводит к исчезновению кожных проявлений, снижению выраженности зуда и степени тяжести болезни.
Ключевые слова: атопический дерматит, дети, недостаточность цинка, коррекция, пиритион цинк активированный
Correction of zinc insufficiency in children with atopic dermatitis
Revyakina V.A., Mukhortykh V.A., Kuvshinova E.D., Larkova I.A., Kravschova P.O.
The Federal Research Centre of Nutrition and Biotechnology; 21, Kashirskoe shosse, Moscow, 115446, Russia
Atopic dermatitis is a complex multifactorial disease in which the essential microelement (zinc) is deficient, which adversely affects the course of the disease. The use of activated zinc pyrithione in the complex therapy of patients with atopic dermatitis is justified by a wide spectrum of it's pharmacological action at the molecular level, which allows achieving it's maximum absorption rate and increasing the ability to penetrate to deep layers of the skin. The use of activated zinc pyrithione in patients with atopic dermatitis leads to reduction of skin manifestations, and to decreasing of itch and the severity of the disease.
Key words: atopic dermatitis, children, zinc insufficiency, correction, zinc pyrithione
Атопический дерматит - важная медико-социальная проблема, значимость которой определяется ростом заболеваемости, хроническим, рецидивирующим течением болезни и сложностью проведения терапии 3. На эффективность проводимой терапии влияют многие факторы, среди которых недостаточность или дефицит макро- и микроэлементов у больных атопическим дерматитом в последние годы приобретает существенное значение. Именно недостаточность или дефицит ряда эссенциальных макро- и микроэлементов неблагоприятно влияет на течение болезни, формируя необратимые изменения кожи. Среди причин, провоцирующих дефицит или недостаточность макро-и микроэлементов, следует выделить изменение питания при назначении строгих элиминационных диет, предусматривающее порой необоснованное исключение многих пищевых продуктов у больных атопическим дерматитом [6]. Длительные элиминационные диеты могут быть причиной развития недостаточности микроэлементов вследствие низкого потребления продуктов животного и растительного происхождения. Среди этих микроэлементов особое значение принадлежит цинку, важнейшими пищевыми источниками которого являются рыба, яйца, мясо и птица, сыры, крупы, в особенности гречневая и овсяная, зернобобовые, хлеб. Цинк всасывается преимущественно в верхних отделах кишечника в виде ионов цинка. При смешанном питании степень абсорбции цинка составляет 20-40% от общего числа данного микроэлемента, поступающего с пищей. Усвояемость цинка из животных продуктов значительно выше, чем из злаков и овощей [7]. Недостаточность или дефицит цинка ассоциируется с нарушением иммунитета, повышением уровня заболеваемости, а в ряде стран и со смертностью от инфекционных заболеваний [8, 9]. Цинк является структурным компонентом протеинов, биологических мембран, клеточных рецепторов, входит в состав более чем 200 ферментных систем организма, принимает участие в таких процессах, как митоз, синтез ДНК и белка, экспрессия и активация генов. Это обусловливает исключительно важную роль цинка в нормальном функционировании многих органов и систем организма [10, 11].
Известно, что в коже и в некоторых других тканях с интенсивным обновлением концентрация цинка существенно выше. Так, содержание цинка в эпидермисе составляет 20% от общего числа его в организме [12, 13]. Цинк играет значительную роль в поддержании нормального состояния кожи, поскольку дефицит или недостаточность цинка сопровождается ее разнообразными поражениями и ухудшением заживления ран [12, 13]. С дефицитом цинка связывают снижение регенераторных возможностей кожи и слизистых оболочек, развитие иммунопатологических реакций. Цинк является одним из важнейших микроэлементов, участвующих в механизме персистирующего воспаления при атопическом дерматите. Имеются данные об участии ионов цинка в процессах апоптоза и его регуляции [14]. Очевидно, что ионы данного металла определенным образом действуют на ранних фазах программированной гибели клеток, а связывание цинка хелаторами может угнетать апоптоз [14]. Нарушение процессов апоптоза иммунокомпетентных клеток и кератиноцитов кожи рассматривается как одна из существенных особенностей патофизиологии атопического дерматита [15]. В этой связи при выборе системной и/или наружной терапии этого заболевания следует назначать лекарственные средства или их комбинации, которые эффективно воздействовали бы на все звенья патогенеза. В этой связи определенный интерес вызывают цинксодержащие препараты, применяемые системно и/или наружно. В качестве средств наружной терапии в последние годы используются активированный пиритион цинк (торговое название «Скин-кап»), противовоспалительный препарат, обладающий широким спектром взаимодополняющих фармакодинамических эффектов, обусловливающих его эффективность при атопическом дерматите. Свойство активированного пиритиона цинка активировать апоптоз определяется не только ионами цинка, но также и молекулой препарата в целом. Препарат обладает антибактериальной активностью, способен восстанавливать гомеостаз кератиноцитов и угнетать воспалительные реакции. Приведенные выше данные об особенностях влияния пиритиона цинка на аптоптоз указывают на то, что для проявления этим препаратом терапевтической эффективности он должен быть стабилен, в противном случае его активность (за счет распада на ионы цинка и стабильные производные пиритиона) будет немногим отличаться от растворимых солей цинка, таких как, например, сульфаты [16].
Поэтому неудивительно, что активированный пиритион цинка (оригинальный препарат «Скин-кап»), отличающийся от стандартного пиритиона цинка в 50 раз большей стабильностью в водных растворах, обладает существенно лучшей клинической эффективностью в сравнении с традиционно используемыми препаратами цинка.
Среди наблюдаемых больных атопическим дерматитом была выделена группа детей с низкими показателями физического развития, выраженной сухостью кожи, периоральным или периорбитальным дерматитом, частыми рекуррентными острыми респираторными заболеваниями. Исследуемую группу составили 27 больных атопическим дерматитом в возрасте от 3 до 7 лет с пониженной концентрацией цинка в сыворотке крови (менее 10 мкМоль/л). У детей без вышеперечисленных клинических проявлений концентрация цинка в сыворотке крови была в пределах нормативных значений.
Содержание цинка в сыворотке крови определяли методом атомно-абсорбционной спектроскопии на спектрофотометре С-115-М-1, согласно инструкции, прилагаемой к прибору. По данным Л.А. Даниловой (1992) нормальные значения цинка в сыворотке крови колеблются в пределах от 10 до 19,5 мкМоль/л. Рекомендуемая суточная норма потребления цинка, согласно утвержденным Нормам физиологических потребностей в витаминах для детей и подростков Российской Федерации (МР 2.3.1.2432-08), составляет для детей в возрасте от 0 до 6 мес - 3 мг; 7-12 мес - 4 мг; 1-3 лет - 5 мг; 3-7 лет - 8 мг; 7-11 лет - 10 мг; 11-14 лет - 12 мг [17].
При анализе сопутствующей патологии отмечено, что у детей с пониженным содержанием цинка в сыворотке крови в отличие от детей с нормальными показателями цинка достоверно чаще диагностировался хронический гастродуоденит, а также вторичные изменения поджелудочной железы. Наличие воспалительных изменений в слизистой оболочке желудка и двенадцатиперстной кишки, по-видимому, приводит к нарушению всасывания цинка и способствует снижению концентрации данного микроэлемента в крови. Выявлена обратная корреляционная взаимосвязь (r= -0,2; р=0,047) между уровнем цинка в сыворотке крови и увеличением размеров печени (по данным ультразвукового исследования).
Анализ анамнестических и клинических данных в сопоставлении с результатами обследования показал, что у детей с пониженным содержанием цинка достоверно чаще (р=0,004) отмечаются случаи вторичного инфицирования кожных покровов (82%). Склонность к частым острым респираторным вирусным инфекциям (в 6 раз и более) отмечалась у 85% детей. Установлено, что отставание в росте достоверно чаще (р<0,05) отмечалось у детей с низкими значениями данного микроэлемента.
В этой связи возникла необходимость использования активированного пиритиона цинка у детей с атопическим дерматитом, имеющих изменения в гомеостазе цинка. Низкие значения цинка в сыворотке крови у детей с атопическим дерматитом послужили основанием для расширения «скудных» диет переносимыми пищевыми продуктами животного происхождения (мясо кролика, постной свинины, индейки) и включения в качестве средства наружной терапии активированного пиритиона цинка (Скин-Кап) в виде аэрозоля и крема. Курс терапии составил от 14 до 21 дня.
При явлениях экзематизации, экссудации, отека на коже использовали аэрозоль активированного пиритиона цинка, при купировании экссудации - крем. В остром периоде без экссудации применяли крем 3-4 раза в день до стабилизации процесса, в подостром периоде 2 раза в день, затем 1 раз до полного разрешения высыпаний. На очаги лихенизаций наносили крем 1 раз в день под окклюзионную повязку; на участки сухости и шелушения - крем 1 раз в день с последующим снижением частоты применения.
Во время лечения других наружных средств не назначали. Параллельно больные получали традиционную терапию, включающую коррекцию питания с расширением переносимых продуктов питания, антигистаминные средства и препараты, нормализующие функцию желудочно-кишечного тракта. В ходе терапии оценивали течение атопического дерматита с учетом критериев шкалы SCORAD - площадь пораженной кожи, интенсивность клинических проявлений, выраженность субъективных проявлений (зуд, нарушение сна). Достоверное снижение выраженности клинических проявлений поражения кожи, выраженности зуда у наблюдаемых больных отмечалось на 7-10-е сутки терапии (р<0,05). В результате проведенной терапии индекс SCORAD снизился в 2,5 раза (исходно - 38,9±8,2 балла, через 21 день - 15,6±3,8 балла). Оценка общей терапевтической эффективности препарата активированного пиритиона цинка на фоне адекватной диеты доказала, что положительное лечебное действие было достигнуто у 88% детей. Активированный пиритион цинк обладал очень хорошим профилем безопасности, не вызывал раздражающего и повреждающего действия, а также развития побочных реакций.
Таким образом, полученные данные позволяют считать применение активированного пиритиона цинка у больных атопическим дерматитом высокоэффективным средством наружной терапии, положительный эффект которого выражался в исчезновении кожных проявлений, снижении интенсивности зуда и уменьшении степени тяжести заболевания. Для повышения эффективности лечения атопического дерматита, протекающего на фоне недостаточности или дефицита цинка, следует использовать комплексную терапию, включающую адекватную рациональную диетотерапию, комбинацию системных и наружных цинкосодержащих препаратов.
Информация об источниках финансирования
Финансовой поддержки в настоящей статье не было.
Конфликт интересов
Авторы заявляют, что они не имеют конфликта интересов
ЛИТЕРАТУРА
Информационная страница
Ревякина Вера Афанасьевна, ФГБУН ФИЦ питания и биотехнологии, г. Москва, доктор медицинских наук, профессор, зав. отделением аллергологии.
Мухортых Валерий Алекссевич, ФГБУН ФИЦ питания и биотехнологии, г. Москва, м.н.с.
Кувшинова Елена Дмитриевна, ФГБУН ФИЦ питания и биотехнологии, г. Москва, кандидат медицинских наук.
Ларькова Инна Анатольевна, ФГБУН ФИЦ питания и биотехнологии, г. Москва, кандидат медицинских наук.
Кравцова Полина Олеговна, ФГБУН ФИЦ питания и биотехнологии, г. Москва, ординатор отделения аллергологии.
Дополнительные утверждения
Авторы согласны на публикацию представленной работы.
Авторы подтверждают, что данная рукопись в настоящее время не представлена для публикации в другие издания и не была принята для публикации в других изданиях.
В пособии рассматриваются особенности течения атопического дерматита у детей с дефицитом цинка. Кратко освещаются вопросы обмена цинка в организме, его биологическая роль, лабораторная диагностика цинк-дефицитных состояний. Пособие рассчитано на врачей - педиатров, аллергологов, дерматологов и других специалистов.
Дефицит цинка и атопический дерматит
Одной из актуальных проблем в педиатрии и дерматологии является лечение атопического дерматита. По данным эпидемиологических исследований, в разных странах атопическим дерматитом страдают от 10 до 28% детей. В общей структуре аллергических заболеваний он занимает одно из ведущих мест. Острота проблемы атопического дерматита обусловлена не только его высокой распространенностью н популяции, но и ранним дебютом, быстротой развитая хронических форм, которые приводят к снижению социальной адаптации, качества жизни и инвалидизации детей. Трудности в лечении больных атопическим дерматитом связаны с недостаточным раскрытием механизмов развития заболевания, необходимых для разработки патогенетических методов лечения. Наиболее изучены в настоящее время механизмы иммунных реакций, лежащие в основе аллергического воспаления. Значение же других механизмов, участвующих в развитии аллергических заболеваний изучено недостаточно. По данным экспериментальных и клинических исследований, изменения баланса микроэлементов в организме могут в значительной мере влиять на течение иммунологических процессов, в том числе и на развитие аллергических реакций. Вследствие этого, в течение последних лет активно обсуждается значение цинка для здоровья детей.
Обмен цинка в организме
Как известно, цинк относится к эссенциальным микроэлементам. Его запасы в организме не велики. Так у взрослого человека содержится всего 1,5-2 г цинка, что, к примеру, в 2 раза ниже содержания железа. Цинк обнаруживается во всех органах и тканях организма, однако его наибольшие концентрации определяются в скелетной мускулатуре, которая содержит 62% его количества. Также богата цинком костная система, предстательная железа, роговица. У новорожденных 25% цинка может быть представлено в печени. Основное количество поступившего цинка (40-45%) всасывается в двенадцатиперстной кишке по механизму регулируемой диффузии. Установлено, что всасывание цинка обратно пропорционально его концентрации в просвете кишки. Поступив в энтероцит, цинк соединяется с металлотионеином, который по некоторым данным регулирует не только всасывание, но и выделение цинка. В кровяном русле основным лигандом цинка является альбумин, переносящий до 2/3 метаболически активного микроэлемента. Небольшие количества цинка переносятся в мозг гистидином и цистидином
Выделяется цинк в основном через кишечник (10 мг в сутки), с мочой (0,3-0,6 мг), с потом (в жару до 2-3 мг). Также цинк выводится с женским молоком (1,63мг/кг),
Биологическая роль цинка
Биологическая роль цинка многообразна. Он необходим для роста и деления клеток, развития костной ткани, процессов регенерации, репродуктивной функции, развития мозга и поведения. Являясь компонентом более 300 энзимов, цинк принимает участие во всех видах обмена, входит в состав генетического аппарата клетки, представляя около 100 цинксодержащих нуклеопротеидов. Цинк играет значительную роль в функционировании системы иммунитета. Тимулин-гормон тимуса, необходимый Т-лимфоцитам является цинкзависимым, вследствие чего, при дефиците цинка снижается общее количество Т-лимфоцитов и Т-супрессоров, а также фагоцитарная активность нейтрофилов. Цинк принимает активное участие в процессах регенерации, поскольку необходим для синтеза и стабилизации ДНК. Супероксиддисмутаза, участвующая в регуляции перекисного окисления липидов также является цинксодержащим ферментом, в связи с чем многие авторы относят этот микроэлемент к антиоксидантам.
Цинк-дефицитные состояния
Незаменимость цинка для течения кардинальных процессов жизнедеятельности явно проявляется при возникновении его дефицита. Классическим примером дефицита цинка является энтеропатический акродерматит. Он относится к редким, наследуемым по аутосомно-рецессивному типу заболеваниям. Манифестирует в грудном возрасте и без лечения приводит к смертельному исходу. Полагают, что в результате генетического дефекта в клетках Панета нарушается всасывание цинка в кишечнике. Клинически акродерматит проявляется типичными признаками дефицита цинка. На первый план выступают поражения кожи в виде хронического эритематозно-буллезного дерматита на конечностях и вокруг естественных отверстий тела, частое присоединением вторичного инфицирования, патологией роста ногтей и волос, аллопецией. Характерны тяжелые желудочно-кишечные расстройства с синдромом нарушенного всасывания, глазные симптомы (блефарит, конъюнктивит, фотофобия, помутнение роговицы), нервно-психические нарушения, замедление роста, гипогонадизм, анемия, гепатоспленомегалия, снижение остроты вкуса и обоняния. Дефицит цинка, испытываемый женщиной во время беременности, приводит к широкому спектру врожденных уродств у плода - расщеплению верхней челюсти, верхнего неба, микроцефалии.
Методы диагностики цинк-дефицитных состояний
Диагностика дефицита цинка основывается на определении уровня цинка в сыворотке крови, эритроцитах, моче, волосах. Наиболее информативным по мнению многих авторов является исследование цинка в сыворотке крови. По данным Карлинского М. В. концентрацию цинка в крови менее 13 мкмоль/л можно расценивать как цинк-дефицитное состояние, а содержание цинка менее 8,2 мкмоль/л является неблагоприятным прогностическим признаком. Однако необходимо учитывать, что не всегда уровень цинка в крови коррелирует с клиническими проявлениями. Так, концентрация цинка в крови может изменяться в течение дня в зависимости от приема пищи, стресса, перенесенной инфекции, при нарушениях забора и хранения крови. Поэтому при диагностике дефицита цинка необходимо учитывать не только концентрацию цинка в сыворотке крови, но и положительную динамику клинических симптомов, а также повышение концентрации цинка в ответ на терапию цинксодержащими препаратами.
Цинк-дефицитные состояния и атопический дерматит
Учитывая большую роль цинка для иммуногенеза и реальную возможность развития аллергических болезней кожи на фоне цинк-дефицитных состояний, нами было проведено специальное исследование по выявлению дефицита цинка у детей, больных атопическим дерматитом и целесообразности включения цинксодержащих препаратов в терапию атопического дерматита.
Пациенты и методы: Под наблюдением находилось 54 ребенка в возрасте от 11 месяцев до 13 лет. Клиническое обследование больных включало изучение анамнеза жизни и заболевания, клинический осмотр, аллергологическое обследование, иммунологическое обследование: определение содержания иммуноглобулинов А, М, G в сыворотке крови, определение общего иммуноглобулина Е в сыворотке крови; определение количества Т- и В-лимфоцитов, определение иммунорегуляторного индекса. Содержание цинка измерялось в сыворотке крови методом атомно-абсорбционной спектрометрии. Степень тяжести атопического дерматита оценивалась с использованием шкалы SCORAD, рекомендованной Европейской рабочей группой по проблеме атопического дерматита. Шкала SCORAD позволила не только наиболее полно отразить основные симптомы атопического дерматита, но и оценить динамику клинической симптоматики в процессе лечения. Показатели оценивались по шести основным симптомам: эритема, отек/папула, корки/мокнутие, экскориации, лихенизация, сухость. Степень выраженности каждого признака оценивалась по четырехуровневой шкале: 0 - отсутствие, 1 - слабая, 2 - умеренная, 3 - сильная. Так же оценивалась площадь поражения по схеме и субъективные симптомы - зуд, нарушение сна по визуальной аналоговой шкале. Степень тяжести отражал индекс SCORAD, рассчитанный по формуле:
SCORAD = площадь поражения * 0,2 + (7*сумма объективных признаков)*0,5 + сумма субъективных признаков.
На основании индекса SCORAD в выбранной нами группе 20 детей (37%) имели атопический дерматит тяжелой степени тяжести и 34- ребенка (63%) имели среднетяжелое течение атопического дерматита
Более половины детей, поданным анкетирования (54%), имели отягощенную наследственность по аллергическим заболеваниям, ранний срок начала заболевания от рождения и до 12 месяцев с преобладанием выраженного экссудативного компонента в дебюте заболевания (64%) у детей всех возрастных групп.
В зависимости от концентрации цинка в сыворотке крови дети были распределены на 3 группы. Первую группу составили дети, концентрация цинка у которых составляла менее 10ммоль/л (20 детей). Во вторую группу вошли дети с концентрацией цинка от 10 до 15 ммоль/л (17 детей). В третьей группе концентрация цинка была свыше 15 ммоль/л.
| № группы | Концентрация цинка, ммоль | Количество пациентов |
| 1 | Менее 10 | 20 |
| 2 | 10-5 | 17 |
| 3 | Более 15 | 17 |
Результаты исследования и их обсуждение: Между 1-й и 3-й группами был проведен статистический анализ данных, который позволил выявить некоторые отличия и клинические особенности течения атопического дерматита у детей с пониженным содержанием цинка в организме.
При анализе акушерского анамнеза было выявлено, что у матерей детей раннего возраста из 1 -й группы достоверно чаще встречалась анемия и острые респираторные заболевания во время настоящей беременности. Отмечалась тенденция к более высокой частоте угрозы прерывания беременности, патологических родов, слабости родовой деятельности, а также токсикозов 1-й и 2-й половины беременности, что косвенно свидетельствует о недостатке цинка в организме матери.
В раннем возрасте у детей 1 -й группы в отличие от детей 3-й группы более часто отмечалась перинатальная энцефалопатия, как результат патологических родов и беременности. На первом году жизни дети из 1-й группы более часто испытывали задержку психомоторного развития.
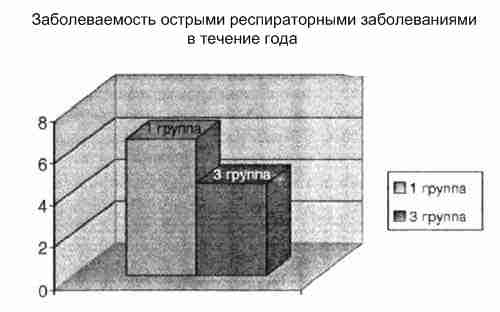
Дети с пониженным содержанием цинка в организме достоверно чаще болели острыми респираторными заболеваниями в течение года в отличие от детей 3-й группы с нормальными показателями цинка (6,5±1,29 и 4,4±1,8 соответственно).
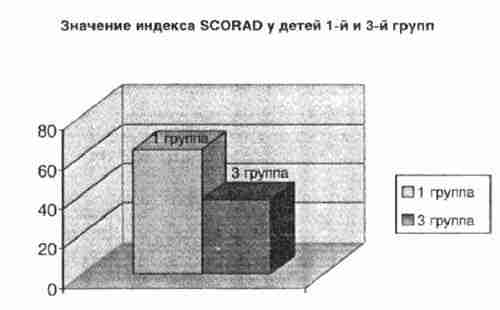
Анализируя клиническую симптоматику атопического дерматита в обеих группах можно сделать следующие выводы: в группе с пониженным содержанием цинка в сыворотке крови преобладают более тяжелые, непрерывнорецидивирующие формы атопического дерматита, резистентные к традиционным методам терапии. При оценке состояния кожных покровов, по оценке SCORAD, индекс SCORAD у детей 1 -й группы был выше и составлял 63,4±1,2, при значении того же показателя в 3 группе - 37,6±1,09.
Одновременно у детей с дефицитом цинка имелась тенденция к более выраженной сухости кожи (2,25±0,5 балла), в отличие от детей 3 группы (1,8±0,4 балла). У детей из 1 -и группы достоверно чаще отмечалось поражение дериватов кожи - дистрофические изменения ногтей, замедленный рост и ломкость волос.
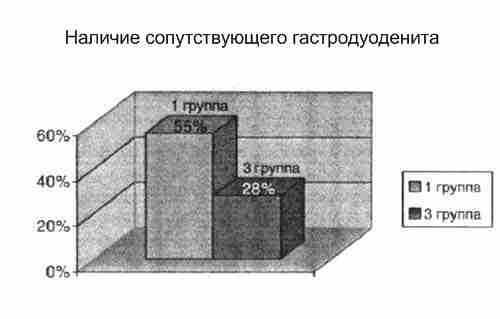
При дальнейшем обследовании детей была выявлена гепатомегалия (по данным ультразвукового обследования) у 75% детей 1 группы и 40% детей 3 группы. Характерно, что в группе с низкими показателями цинка более часто встречалась сопутствующая патология желудочно-кишечного тракта - хронические гастродуодениты - 55% и 23% соответственно.
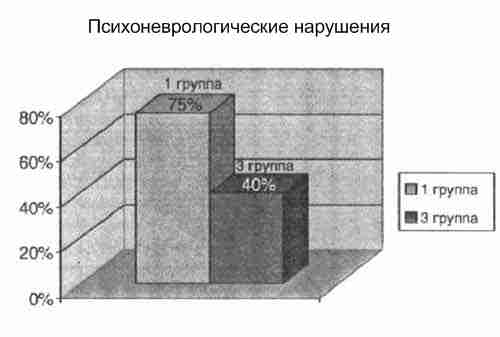
Изменения в психоневрологическом статусе (дефицит внимания, гиперактивность) имело 75% детей 1 группы, в отличие от 40% детей 3 группы
При анализе гематологических показателей не было выявлено достоверных различий между 1 -й и 3-й группами, однако имелась тенденция к более низким показателям гемоглобина (125,5± 12,6 и 143,2±19 соответственно).
Различий в иммунологических показателях крови при анализе двух групп не отмечалось. Все дети имели иммунологические нарушения, характерные для атопического дерматита.
Было сформировано две группы детей. Дети 1-й группы (15 человек) получали Цинктерал в составе комплексной терапии. Дети 2-й группы (15 человек) получали только традиционное лечение. С целью оценки эффективности проводимого лечения клинико-лабораторное обследование проводилось до и после окончания курса терапии. Оценка клинических проявлений атопического дерматита показала более выраженную положительную динамику у детей 1-й группы по сравнению с контролем. Так, в 1-й группе продолжительность яркой гиперемии и зуда (в днях) составляла 3,5±1, а во 2-й группе 6,6±9: сухость кожи 10,1 и 12,3 соответственно; нарушение сна 3,7 и 6,7 дней.

При анализе лабораторных данных было выявлено, что в 1-й группе достоверно увеличивалась концентрация цинка в сыворотке крови с 9,9 до 15,5 ммоль/л, тогда как в группе, не получавшей Цинктерал, концентрация цинка оставалась на прежнем уровне (12,7 до 13 ммоль/л).
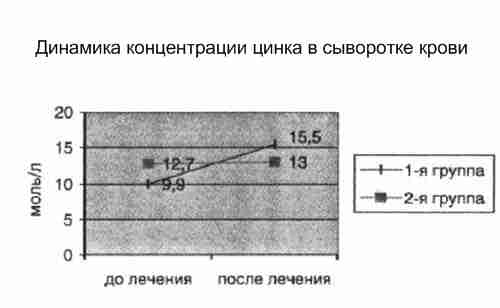
В 1-й группе отмечалось более выраженное понижение общего иммуноглобулина Е и повышение иммуноглобулина А, чем во 2-й группе (соответственно р
При использовании Цинктерала у 4 детей отмечались побочные эффекты в виде тошноты, болей в животе при приеме препарата до еды, после перехода на прием Цинктерала после еды эти явления купировались. У одного ребенка мы были вынуждены прекратить терапию Цинктералом в связи с появлением рвоты после каждого приема препарата. Аллергических реакций на препарат в нашем исследовании не отмечалось.
Выводы: Таким образом, можно заключить, что содержание цинка в организме коррелирует с тяжестью течения атопического дерматита, с особенностями клинических проявлений заболевания. Включение в комплексную терапию атопического дерматита препарата цинка "Цинктерал" повышало эффективность проводимого лечения, сокращало сроки наступления ремиссии заболевания.
Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова
Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова
Новое в коррекции кожного зуда у пациентов с зудящими дерматозами
Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова
Кожный зуд и воспаление доминируют при обострении большинства дерматозов и негативно сказываются на качестве жизни пациентов. Для купирования данных состояний необходима активная терапия, которая должна быть эффективной и безопасной. Цель исследования — сравнить сроки разрешения клинических проявлений зудящего дерматоза при использовании комбинированной терапии (Неотанин + топический глюкокортикостероид) и монотерапии топическим глюкокортикостероидом. Материал и методы. Данное открытое сравнительное клиническое исследование проводили с октября 2018 г. по апрель 2019 г. В работу были включены 40 пациентов обоих полов в возрасте от 7 до 43 лет с зудящими дерматозами в стадии обострения, с мокнутием и без, в том числе осложненными вторичной инфекцией, со сравнимыми поражениями на зеркальных частях тела. Критериями эффективности исследуемого препарата были динамика субъективных жалоб, объективная оценка состояния пациента (наличие и выраженность клинических симптомов), динамика дерматологического индекса качества жизни (ДИКЖ). Результаты. Использование комбинированной терапии (Неотанин + топический глюкокортикостероид) значительно уменьшает интенсивность зуда: к 3-му дню исследования она уменьшилась уже на 60%, при монотерапии топическим глюкокортикоидом — лишь на 22% (р=0,02). При включении в терапию Неотанина зуд купировался значительно быстрее (через 8—15 мин) по сравнению с монотерапией топическим глюкокортикоидом (в среднем через 60 мин), p
Кожный зуд — самая распространенная дерматологическая жалоба — характеризуется неприятным ощущением с непрерывной потребностью в ответном механическом раздражении кожи, вследствие чего может вызывать такие эффекты, как повреждение кожи, вторичная инфекция, образование шрамов. Кожный зуд также может существенно влиять на общее состояние и качество жизни пациентов, вызывая эмоциональные нарушения, бессонницу, тревожность, а в тяжелых случаях — депрессию и суицидальные мысли [1].
Зуд — один из наиболее частых субъективных симптомов в дерматологии, уступающий по распространенности только жалобам на косметические дефекты. При атопическом дерматите и крапивнице 100% пациентов предъявляют жалобы на зуд, при псориазе — до 87% пациентов [2]. Согласно клинико-эпидемиологическим данным H. Alexander и соавт. [3], 35% амбулаторных пациентов кожной клиники страдают от зуда, обусловленного такими дерматологическими заболеваниями, как узловатая почесуха, красный плоский лишай, атопический дерматит, экзема, ксероз и т. д.
cуществует как гистамининдуцированный, так и гистаминнезависимый зуд. Гистамининдуцированный вызывается механической, термической, электрической или химической стимуляцией безмиелиновых гистамин-чувствительных периферических нервных волокон С-типа. Негистаминовые нервные волокна также принимают участие в передаче сигнала зуда, в связи с чем многие формы зуда нечувствительны к антигистаминным препаратам. Зуд является одной из форм кожного анализатора, близкой к другим видам кожного чувства (прикосновение, боль). Сильный зуд облегчается путем тяжелых самоповреждений, приводящих к замещению ощущения зуда чувством боли [4, 5].
В связи с этим стоит упомянуть о порочном цикле зуд—расчесы—зуд. Повреждение кожного барьера и следующее за ним воспаление приводят к развитию зуда. В коже воспалительные клетки активируют сенсорные нервы, тучные клетки, фибробласты, макрофаги. Все вышеперечисленные клетки высвобождают медиаторы зуда, которые в дальнейшем усиливают воспаление. Сигнал зуда передается в головной мозг, вызывая чесательный рефлекс. Расчесы еще больше повреждают кожный барьер, усиливают воспаление. Т-лимфоциты и эозинофилы мигрируют в кожу, высвобождая медиаторы-пруритогены. В конечном итоге происходит сенситизация чувствительных нервных волокон и снижается порог активации. Факторы роста, высвобождающиеся эозинофилами, обусловливают пролиферацию нервных волокон. Эти изменения повышают чувствительность кожи, которая становится еще более уязвимой по отношению к эндо- и экзогенным факторам. Такой цикл сложно прервать. Цикл зуд—расчесы—зуд приводит к нарушениям сна, концентрации внимания и процессов восприятия, ограничивая тем самым социальную активность пациентов [6].
Клиническая картина
Субъективно пациенты характеризуют зуд как ощущение «ползания мурашек», покалывание, легкое жжение кожи и т. д. Интенсивность зуда может быть различной: от слабой до выраженной. Зуд, приводящий к нарушению сна, рассматривают как тяжелый. Биопсирующим зудом называется сильнейший зуд, при котором расчесывание приводит к значительным самоповреждениям кожи. При такой форме зуда появляющиеся при экскориировании кожи болевые ощущения приносят удовлетворение. Клинически состояние при длительном зуде у больного будет характеризоваться экскориациями (линейными повреждениями кожи с геморрагическими корочками), поствоспалительной пигментацией, рубцами, лихенификацией, вторичной пиодермией. Длительный зуд негативно влияет на общее самочувствие пациента: возможны развитие бессонницы и связанные с ней расстройства нервной системы [7].
Максимально быстрое облегчение и прекращение зуда является приоритетной задачей в терапии зудящих дерматозов. Симптоматическую терапию зуда необходимо назначать максимально рано для прерывания его циклического течения. Терапия зуда должна быть эффективной и безопасной, хорошо переноситься пациентами и положительно влиять на качество жизни [8].
Материал и методы
Клиническое исследование проводилось с октября 2018 г. по апрель 2019 г. Данное исследование было открытым сравнительным. В исследование были включены 40 пациентов обоего пола в возрасте от 7 до 43 лет с зудящими дерматозами в стадии об-острения с мокнутием и без, в том числе осложненные вторичной инфекцией, со сравнимыми поражениями на зеркальных частях тела. У 27 пациентов был диагностирован атопический дерматит, причем у 2/3 из них средней и тяжелой степени; 13 пациентов обратились за консультацией в связи с обострением экземы кистей. Диагностика дерматозов основывалась на комплексной оценке клинико-анамнестических данных.
Перед началом и в процессе лечения проводилась клиническая оценка состояния больного:
1. Оценка субъективных клинических признаков (жалобы пациента): зуд кожных покровов, жжение, болезненность и бессонница. Зуд кожных покровов и противозудное действие терапии оценивали для каждой половины тела по нескольким параметрам:
а) интенсивность кожного зуда по ВАШ (по 10-балльной системе);
б) время (в мин), через которое зуд прекращается; длительность противозудного действия после утреннего нанесения средства;
в) тяжесть зуда, частота приступов зуда, длительность зуда (оценка за последнюю неделю).
2. Оценка объективных признаков воспаления: эритема, отек, корки/мокнутие, экскориации, лихенификация, сухость кожи, трещины/эрозии.
3. Оценка эффективности терапии врачом:
а) выраженное улучшение — разрешение старых элементов, отсутствие зуда и болезненности кожных покровов;
б) улучшение — неполное разрешение старых элементов, отсутствие зуда и болезненности кожных покровов;
в) состояние без перемен — отсутствие изменений кожных покровов;
г) ухудшение — ухудшение клинической картины, появление зуда, болезненности кожных покровов.
4. Дерматологический индекс качества жизни (ДИКЖ).
Обследование проводилось 5 раз (один раз в 2—3 дня) на протяжении 12—16 дней. На пораженные участки кожи одной половины туловища все пациенты наносили топический глюкокортикостероид (крем Акридерм) 2 раза в день (утро и вечер), слегка втирая; на очаги второй половины туловища наносили два препарата — Неотанин (спрей/лосьон/крем) и крем Акридерм. Крем Неотанин был назначен 18 пациентам, лосьон Неотанин — 12, спрей Неотанин — 10. Сначала наносили Неотанин тонким слоем на пораженный участок кожи 3—4 раза в сутки. После нанесения дожидались высыхания обработанной поверхности. Через 15 мин 2 раза в день (утро и вечер) наносили Акридерм крем тонким слоем на пораженный участок кожи, слегка втирая.
В ходе исследования не допускалось назначение топических (кроме Акридерм) и системных глюкокортикостероидов, антигистаминных и антибактериальных препаратов, антисептиков. Часть пациентов дополнительно получали сопутствующую терапию: желчегонные, системные десенсибилизирующие средства, наружно — эмоленты.
На проведение исследования получено разрешение Этического комитета.
Для статистической обработки данных использованы критерии Манна—Уитни, Уилкоксона (для оценки динамики), χ 2 или двусторонний точный критерий Фишера.
Результаты

Так, на очагах, где использована комбинированная терапия (Неотанин + Акридерм), интенсивность зуда к 3-му дню исследования уменьшилась уже на 60% (с 10 баллов до 4), при монотерапии препаратом Акридерм — лишь на 22% (с 9 баллов до 7; p=0,02) (рис. 1). Рис. 1. Интенсивность зуда (по 10-балльной шкале).
Согласно данным ежедневных дневников пациентов, на участках тела, где наносили Неотанин, зуд купировался значительно быстрее: уже через 8—15 мин — по сравнению с монотерапией Акридермом, при которой прекращение зуда наблюдали в среднем только через 60 мин (p <0,01) (рис. 2). Рис. 2. Время купирования зуда после нанесения препарата, мин. Продолжительность противозудного действия после нанесения препаратов Неотанин + Акридерм в среднем составила 2—3 ч, Акридерма — лишь 30 мин (p <0,01) (рис. 3). Рис. 3. Длительность противозудного действия после нанесения, мин. Таким образом, длительность противозудного действия (сроки разрешения клинических проявлений) при комбинированной терапии Неотанина с топическим глюкокортикостероидом в 4 раза выше по сравнению с монотерапией топическим глюкокортикоидом (рис. 4).

Рис. 4. Сроки разрешения клинических проявлений при использовании комбинированной терапии по сравнению с монотерапией топическим глюкокоритикостероидом: а) у женщины 35 лет с атопическим дерматитом средней степени тяжести (обострение); б) у женщины 35 лет с острой экземой кистей.

Рис. 4. Сроки разрешения клинических проявлений при использовании комбинированной терапии по сравнению с монотерапией топическим глюкокоритикостероидом: в) у женщины 25 лет с атопическим дерматитом легкого течения (обострение).
Частота зуда на половине туловища, на которую наносили Неотанин + Акридерм, к концу 1-й недели снизилась на 75% — с показателя «очень частый зуд» до показателя «редкий зуд»; в области нанесения Акридерма на 25% — с показателя «очень частый зуд» до показателя «частый зуд» (p<0,01).
Тяжесть зуда оценивали по шкале от 0 до 4 баллов, где 0 баллов означает отсутствие зуда, 4 — сильный зуд. На 1-м визите средний балл составлял 4 на каждой из сторон. К концу 1-й недели на участках тела, на которые наносили Неотанин + Акридерм, тяжесть зуда снизилась до 2 баллов (слабый зуд); Акридерм — до 3 баллов (умеренный зуд) (p<0,02).
Каждый из признаков воспаления (эритема, отек, мокнутие, экскориация, лихенификация и сухость) оценивали по шкале от 0 до 3 баллов, где 0 баллов означает отсутствие симптома, 3 — выраженный признак. Интенсивность воспаления определялась суммой баллов всех признаков. Интенсивность воспаления кожи на 7-й день лечения уменьшилась на 50% на участках кожи после нанесения Неотанин + Акридерм, на 22% — на участках с монотерапией глюкокортикостероидами (p<0,01).
Кроме того, при монотерапии Акридермом у 3 пациенток регистрировали обострение кожного процесса на 5—7-й день терапии, у 1 пациентки было отмечено присоединение бактериальной инфекции на участке кожи.
В целом на фоне лечения было установлено повышение качества жизни практически у всех пациентов, включенных в исследование.
На участках тела, где наносили Неотанин + Акри-дерм, эффективность терапии на 4-м визите (10-й день) оценивалась врачом у 37 (92,5%) пациентов как выраженное улучшение, у 3 (7,5%) — как улучшение. После применения Акридерма показатели были следующие: у 7 (17,5%) пациентов — выраженное улучшение, у 27 (67,5%) — как улучшение, у 5 (12,5%) отмечено отсутствие перемен, у 1 (2,5%) — ухудшение.
ДИКЖ измеряли в начале и в конце лечения: отмечено снижение с 21 балла (заболевание оказывает чрезвычайно сильное влияние на жизнь пациента) до 9 (заболевание оказывает умеренное влияние на жизнь пациента).
Поскольку при обострении зудящих дерматозов ведущим симптомом в большей степени является зуд, оправдано назначение противозудных препаратов.
На современном этапе наиболее часто используемая группа препаратов — топические глюкокортикостероиды, оказывающие противовоспалительное, противоаллергическое, иммуносупрессивное действия. Однако, несмотря на создание нового поколения топических глюкокортикостероидов, обладающих минимальными побочными эффектами, нанесение их на большие площади и на продолжительное время приводит к повышению стероидной нагрузки на кожу и развитию ее дистрофии. Кроме того, противозудного действия топических глюкокортикостероидов часто бывает недостаточно для быстрого и длительного снятия зуда.
Выбор эффективного и безопасного препарата для лечения зудящих дерматозов, имеющего выраженное противозудное действие, оказался непростой задачей. В своем выборе мы остановились на серии препаратов Неотанин, включающей в себя лосьон, спрей и крем. Основными активными компонентами серии препаратов Неотанин являются синтетический танин и полидоканол, в лосьон добавлен оксид цинка.
M. Puschmann и C. Matthies доказали противозудный эффект танина методами гистамино-волдырного теста и стимуляции слизистой оболочки губ [9, 10]. Гистамино-волдырный тест был выполнен у 85 здоровых добровольцев. В связи с важной ролью тучных клеток кожи как эффекторных клеток в аллергических реакциях немедленного типа и заболеваниях, сопровождающихся зудом, Т. Zuberbier и соавт. [11] исследовали влияние синтетического танина на IgE-зависимую активацию тучных клеток человека. Влияние танина проявилось в дозозависимом угнетении анти-IgE-индуцированного выделения гистамина. Эффект показал себя более выраженным, чем тот, который наблюдается с дексаметазоном. Помимо противозудного, синтетический танин обладает вяжущим, противовоспалительным, противомикробным действиями, уменьшает трансэпидермальную потерю воды [12].
Вторым активным компонентом серии препаратов Неотанин является полидоканол, который обладает противозудным действием. Противозудный эффект полидоканола развивается через 5—10 мин после нанесения на кожу, длительность действия составляет в среднем 3—4 ч. Также полидоканол усиливает вяжущее, подсушивающее действие танина, способствует заживлению эрозий, обладает анестезирующим действием на кожу и слизистые оболочки, снижает чувствительность и проводимость чувствительных нервов. Полидоканол как противозудное и местно-анестезирующее средство входит в Европейское руководство по хроническому зуду (2012 г.), Рекомендации Ассоциации научных медицинских обществ в Германии (AWMF) по диагностике и лечению атопического дерматита (2016 г.), Рекомендации Европейского дерматологического форума (EDF) по лечению атопической экземы / атопи-ческого дерматита (2018 г.) [13—15].
Заключение
В настоящее время зудящие дерматозы остаются важной медико-социальной проблемой в силу их высокой распространенности и увеличения частоты перехода заболеваний в тяжелые и хронические формы. Это обусловливает резкое снижение качества жизни больного и всей его семьи, способствует формированию психосоматических нарушений, а в итоге ведет к ограничению жизнедеятельности и социальной дезадаптации. Для улучшения качества жизни пациентов с кожным зудом и достижения ремиссии необходимо назначать препараты, обладающие выраженным противозудным и противовоспалительным действиями. С другой стороны, эти препараты должны быть не только эффективными, но и безопасными.
Использование комплексной терапии серии наружных средств Неотанин с топическим глюкокортикостероидом у пациентов с обострением зудящих дерматозов позволило в абсолютном большинстве случаев добиться стойкой, практически полной медикаментозной ремиссии заболевания, значительно уменьшить интенсивность и длительность зуда, снизить стероидную нагрузку на кожу и значительно улучшить качество жизни пациентов.
Результаты нашего исследования позволяют рекомендовать комбинацию средств Неотанин с топическими глюкокортикостероидами как безопасную и эффективную терапию зудящих дерматозов.
Участие авторов:
Концепция и дизайн исследования — К.Н. Монахов
Сбор и обработка материала — Н.А. Холодилова
Статистическая обработка данных — Н.А. Холодилова
Написание текста — Н.А. Холодилова
Редактирование — К.Н. Монахов
Authors’ contributions:
The concept and design of the study — K.N. Monakhov
Collecting and interpreting the data — N.A. Kholodilova
Statistical analysis — N.A. Kholodilova
Drafting the manuscript — N.A. Kholodilova
Revising the manuscript — K.N. Monakhov
Сведения об авторах
КАК ЦИТИРОВАТЬ:
В дерматологии широко используются наружные средства, содержащие цинк. Применение цинка от дерматита оправдано, потому что он важен для поддержания нормальной функции кожи.
В дерматологии широко используются наружные средства, содержащие цинк. Применение цинка от дерматита оправдано, потому что он важен для поддержания нормальной функции кожи. Роль цинка неоценима не только для здоровья кожи, но и для всего организма. Он необходим для роста и деления клеток, процессов восстановления, репродуктивной функции, развития мозга и поведения. Цинк принимает участие в большинстве видах обмена, входит в состав генетического аппарата клетки, играет значимую роль в поддержании системы иммунитета. Цинк при дерматите участвует в механизме устранения воспаления при атопическом дерматите, псориазе и себорейном дерматите.
Считается, что наружная терапия на основе цинка является доступным по цене методом лечения, потому что многие еще помнят такие препараты, как Циндол или Цинковая мазь. Но на российском фармацевтическом рынке появились другие современные наружные препараты, в составе которых соединения цинка являются главным компонентом. Так чем же отличаются друг от друга цинк содержащие наружные средства?
Таблица. Цинк от дерматита – дерматопротекторные средства*.*
Данные из инструкций лекарственных препаратов
Торговое название
Активное вещество
Форма выпуска
Показания к применению
Лечение и профилактика пеленочной сыпи.
Препарат используют также как средство первой помощи при легких повреждениях кожи (небольшие ожоги, порезы, царапины и солнечные ожоги).
Суспензия для
наружного применения
Дерматиты, язвы кожи, опрелость.
Дерматит, опрелости, пролежни, ожоги, стрептодермия и др. поражения кожи.
Цинка окись (цинка оксид
Лечение «пеленочной» сыпи. Препарат используют также как средство первой помощи при легких повреждениях кожи (небольшие ожоги, порезы, царапины и солнечные ожоги).
Цинк пиритион
активированный
Псориаз, атопический дерматит, экзема, нейродермит, себорейный дерматит у взрослых и детей с 1 года.
Наружные средства с цинком можно разделить на препараты, содержащие – цинк оксид и цинк пиритион.
Разберем состав и активное действующее вещество на примере Циндола.
Циндол в народе называется «болтушка» - дешёвое средство, отпускается в стеклянной бутылочке, помогает избавиться от зуда, обладает выраженным подсушивающим действием. Благодаря своим свойствам часто применяется в лечении пеленочного дерматита, опрелостей, язв, когда имеются мокнущие поражения, требующие подсушивающего эффекта.
Состав Циндола- цинк оксид 12,5 г и вспомогательные вещества. Цинк оксид – хороший антисептик, отражает ультрафиолетовые лучи, является главным ингредиентом в солнцезащитных лосьонах, кремах для подгузников, детских порошках, средствах против прыщей, язв и ожогов. Тальк и крахмал удаляют лишнюю влагу. Глицерин помогает регулировать влажность кожи. Этанол оказывает выраженное подсушивающее действие. Потребители отмечают единственный минус в том, что Циндол может пачкать одежду, особенно тёмного цвета.
Следующая группа препаратов цинка – цинк пиритион содержащие средства, например Скин-кап. Цинк пиритион представляет собой комплексное активированное соединение, в котором цинк связан с атомами серы и кислорода.
Цинк пиритион активированный применяется от разных видов дерматита, потому что доказано его противовоспалительное действие при таких серьезных заболеваниях кожи, как атопический дерматит, псориаз и себорейный дерматит. В лечении данных заболеваний основная цель терапии – снять воспаление. Для пациентов с хроническими дерматитами важно иметь в арсенале безопасные, негормональные препараты с противовоспалительным действием.
Последние исследования цинк пиритиона активированного подтверждают его противогрибковые свойства, а поскольку одной из причин появления атопического и себорейного дерматитов является рост дрожжеподобных грибов на коже, то и здесь применение цинка пиритиона актуально.
Также цинк пиритион активированный обладает противомикробным действием, препятствуя заражению воспаленного участка при расчесах и механических повреждениях.
Цинк пиритион рекомендован врачебными стандартами лечения дерматологических заболеваний.
Таким образом, цинк пиритион активированный отличается от цинка оксида медицинскими показаниями к применению и наличием более широкой доказательной базой.
При острых и хронических процессах, при поражениях с сухостью и шелушением, дополнительно увлажняет кожу. Подходит для применения на кожу лица и другие участки тела
Читайте также:

