Кожный детрит что такое
Обновлено: 27.04.2024
Хроническое воспаление – один из главных биологических маркеров старения и элементов патогенеза возрастных заболеваний. В обзоре рассмотрены молекулярно-генетические механизмы персистирующего системного воспаления, сопровождающего физиологическое старение
Хроническое воспаление при старении
Fumihiro Sanada1, Yoshiaki Taniyama1,2*, Jun Muratsu1,2, Rei Otsu1, Hideo Shimizu1, Hiromi Rakugi2 and Ryuichi Morishita1*
1Department of Clinical Gene Therapy, Graduate School of Medicine, Osaka University, Suita, Japan
2Department of Geriatric and General Medicine, Graduate School of Medicine, Osaka University, Suita, Japan
Оригинал статьи: © 2018 Sanada, Taniyama, Muratsu, Otsu, Shimizu, Rakugi and Morishita, распространяется по лицензии CC BY 4.0.
Перевод статьи: © 2021 ООО «Издательство «Открытые системы», распространяется по лицензии CC BY-NC-ND 4.0.
Аннотация
Хроническое воспаление – один из главных биологических маркеров старения и элементов патогенеза возрастных заболеваний. В обзоре рассмотрены молекулярно-генетические механизмы персистирующего системного воспаления, сопровождающего физиологическое старение
Ключевые слова: Хроническое Воспаление, Старение, Клеточное Старение, Старение Иммунитета, Провоспалительные Цитокины, Система Свертывания Крови, Дисбактериоз Кишечника, Chronic Inflammation, Aging, Cell Senescence, Immunosenescence, Proinflammatory Cytokines, Coagulation System, Gut Dysbiosis
В процессе биологического старения системное воспаление прогрессирует в отсутствие патогенных факторов («воспалительное старение», «inflammaging») и характеризуется резистентностью к гиполипидемической (снижение уровня липопротеинов низкой плотности, ЛПНП) и гипотензивной (контроль активности ренин-ангиотензиновой системы, РАС) терапии.
При клеточном старении центральными звеньями патогенеза хронического воспаления являются иммунная дисрегуляция и нарушение активности системы свертывания крови. Обзор посвящен рассмотрению молекулярно-генетических механизмов персистирующего системного воспаления, сопровождающего физиологическое старение, и его роли в патогенезе возрастных заболеваний.
Введение
Системное воспаление при старении – один из главных элементов патогенеза сердечно-сосудистых, эндокринных и онкологических заболеваний (1), распространенность которых неуклонно растет с каждым годом. Несмотря на центральную роль немедикаментозной терапии (изменение образа жизни и рациона питания, снижение влияния сопутствующих факторов риска) в профилактике возрастных заболеваний, требуется разработка фармакологических подходов, основанных на регуляции ключевых клеточных и молекулярных механизмов, участвующих в прогрессировании хронического воспаления.
Важную роль в прогрессировании хронического воспаления играют диетические факторы, старение клеток, снижение уровня половых гормонов и курение. Кроме того, в процессе старения наблюдается повышение уровня циркулирующих провоспалительных факторов, включая интерлейкин-6 (ИЛ-6) и фактор некроза опухоли-α (ФНО-α) (2), способствующих повреждению ДНК, развитию мышечной атрофии, метаболических нарушений и онкологических заболеваний. Повышение образования и секреции ИЛ-6 и ФНО-α при старении также наблюдается в адипоцитах висцеральной жировой ткани (3, 4), увеличение количества макрофагов в которых пропорционально значениям индекса массы тела (ИМТ) и является важным биомаркером хронического воспаления и предиктором инсулинорезистентности у людей с ожирением (5, 6). Среди факторов внешней среды повышению уровня провоспалительных цитокинов – ИЛ-6, ФНО-α и интерлейкина-1-β (ИЛ-1-β) – в крови способствуют хроническое воздействие сигаретного дыма, психоэмоциональный стресс и воспалительные заболевания полости рта (7). Однако системное воспаление низкой интенсивности персистирует даже после коррекции провоспалительного статуса – уровня ЛПНП и активности РАС – и отказа курения, что указывает на существование секреторного фенотипа клеток, ассоциированного со старением (senescent associated secretory phenotype, SASP) и иммунологического импринтинга. В обзоре рассмотрены данные о ключевых биомаркерах, молекулярных механизмах и сигнальных каскадах, участвующих в развитии системного воспаления низкой интенсивности в процессе биологического старения (Рис. 1).
.jpg)
Рисунок 1. Молекулярные элементы системного воспаления, ассоциированного со старением: старение клеток, нарушение гемостаза, накопление клеточного детрита (в т.ч. циркулирующей митохондриальной ДНК, цмДНК), дисбактериоз и иммунная дисфункция. Дополнительные факторы: возраст, окислительный стресс, циркулирующие микроРНК и агалактозилированные N-гликаны.
Источники медиаторов хронического воспаления при старении
Острое воспаление – ключевой компонент в механизме формирования иммунного ответа на воздействие патогена или повреждение тканей и активации регенерации тканей. Системное воспаление низкой интенсивности, наоборот, вызывает хроническое повреждение клеток, способствуя развитию дегенеративных изменений в тканях (8). Воздействие провоспалительных цитокинов – ИЛ-6, ИЛ-1-β и ФНО-α – на структуры нервной и костно-мышечной систем (9) приводит к снижению активности анаболических процессов, опосредованных действием инсулина и эритропоэтина, вызывая развитие саркопении (10).
Клеточный детрит и накопление иммуноглобулинов
Накопление клеточного детрита и иммуноглобулинов в результате нарушения метаболических процессов в клетках стимулируют активацию иммунной системы и развитие системного воспаления. Важную роль в регуляции межклеточных и межмолекулярных взаимодействий и активности иммуноглобулинов играет гликозилирование – один из наиболее распространенных типов посттрансляционной модификации, основанный на присоединении углеводных остатков к аминокислотам (напр., к азоту аспарагиновых остатков в N-гликанах) (11, 12). Данные клинических (13–15) и экспериментальных исследований на животных (16–18) демонстрируют повышение уровня агалактозилированных N-гликанов, не имеющих в составе остатка галактозы в позиции Asn297 Fc-фрагмента IgG (IgG-G0), у пациентов с синдромом Гетчинсона-Гилфорда (прогерия) и некоторыми аутоиммунными заболеваниями.
Провоспалительный эффект IgG-G0 реализуется посредством усиления лектинового пути активации комплемента, связывания с Fcγ-рецепторами и образования агрегатов аутоантител. Кроме того, накопление IgG-G0 с возрастом служит независимым предиктором гиперактивации иммунной системы и развития системного воспаления.
Дополнительным биомаркером старения является митохондриальная дисфункция и высвобождение молекулярных паттернов, ассоциированных с повреждением (МПАП; damage-associated molecular patterns). Рядом исследований показана роль циркулирующих митохондриальных МПАП в патогенезе хронического воспаления и дегенеративных заболеваний (19, 20).
Старение сопровождается снижением барьерной функции эпителиальной выстилки кишечника и ротовой полости (21, 22), что способствует развитию дисбактериоза. Качественные и количественные изменения нормального состава кишечной микробиоты в процессе старения – снижения числа представителей «противовоспалительной» микрофлоры (напр., Clostridium XIVa, Bifidobacterium spp., F. prausnitzii) и увеличением количества условно-патогенных микроорганизмов (напр., Streptococcus spp., Staphylococcus spp., Enterococcus spp., Enterobacter spp.; 23) – может повышать уязвимость пожилых людей к инфекциям. Например, количество бактерий рода Bifidobacterium отрицательно коррелирует с уровнем провоспалительных цитокинов – ФНО-α и ИЛ-1β – в плазме крови.
Нарушение баланса микрофлоры кишечника в большинстве случаев вызвано особенностями рациона питания и наиболее выражено у пожилых лиц, длительно находящихся в учреждениях стационарного социального обслуживания по сравнению с пациентами в частных домах престарелых (24).
Старение клеток
Клеточное старение – необратимая остановка клеточного цикла и потеря способности клетки к делению. Остановка клеточной пролиферации происходит в результате ряда молекулярно-генетических изменений, включая укорочение теломер, генотоксический стресс, действие митогенных стимулов и провоспалительных цитокинов, активацию белка-супрессора опухоли p53 и/или ингибитора циклин-зависимой киназы p16 (25). С возрастом в различных тканях и органах увеличивается количество клеток, утративших способность к пролиферации и приобретающих секреторный фенотип, ассоциированный со старением. Это сопровождается высвобождением провоспалительных цитокинов и инициацией системного воспаления и лежит в основе патогенеза атеросклероза, онкологических заболеваний и сахарного диабета (26–28).
В исследованиях на животных неоднократно показана центральная роль процесса клеточного старения в прогрессировании дегенеративных заболеваний, включая атеросклероз и остеоартрит (29–31). Удаление стареющих клеток и контроль провоспалительных каскадов, участвующих в приобретении клетками секреторного фенотипа, ассоциированного со старением, может служить потенциальной терапевтической мишенью при разработке подходов к профилактике и терапии возрастных заболеваний.
Старение иммунной системы
Дисрегуляция системы врожденного иммунитета и активация воспалительного ответа является ключевым механизмом старения иммунной системы («иммуно-старение»; 32), который приводит к повышению уязвимости пациентов пожилого возраста к аутоиммунным, инфекционным и онкологическим заболеваниям, снижению иммунного ответа на вакцинацию и ухудшению регенерации тканей (33, 34). Хронические воспалительные заболевания, в свою очередь, также способствуют снижению количества клеток и нарушению функций иммунной системы. В частности, в процессе старения наблюдаются изменения характера экспрессии паттерн-распознающих рецепторов (pattern recognition receptors), активация которых при связывании с эндогенными лигандами – маркерами повреждения клеток – стимулирует секрецию провоспалительных цитокинов и прогрессирование хронического воспаления.
Таким образом, наряду с клеточным старением, возрастное снижение функции врожденной иммунной системы является важным элементом патогенеза системного воспаления низкой интенсивности при старении.
Система гемостаза: факторы свертывания крови и фибринолиза
Развитию возрастных заболеваний – атеросклероза и фиброза легких – у пациентов пожилого возраста способствует повышенная активация системы свертывания крови и стимуляция процесса фибринолиза, которые вызывают развитие хронического воспаления через активацию рецепторов, активируемых протеазами (protease-activated receptors, PAR; 35–38).
Увеличение сердечно-сосудистого риска, в частности риска развития тромботических заболеваний, с возрастом связано с повышением уровня факторов свертывающей системы плазмы крови I, V, VII, VIII и IX (39, 40) и концентрации фактора X в атеросклеротических бляшках эндотелиальных, гладкомышечных и иммунных клеток (41). Результаты клинического исследования ATLAS ACS 2–TIMI 51 Investigators показали, что высокоселективный прямой ингибитор фактора Xa ривароксабан снижает риск инфаркта миокарда, инсульта и сердечно-сосудистую смертность у пациентов с ишемической болезнью сердца (42). Увеличение активации системы свертывания крови и содержания фибриногена в плазме крови, наоборот, способствует развитию тромбоза, а повышение уровня фактора коагуляции Xa и тромбина усиливает провоспалительный каскад и вызываемую тромбином PAR-1/2-опосредуемую активацию тромбоцитов (43). Патогенетическая роль PAR-1/2-опосредованной сигнализации FXa и фибринолитического фактора плазмина в процессах клеточного старения и системного воспаления реализуется посредством повышения экспрессии протеина, связывающего инсулиноподобный фактор роста 5 (IGFBP-5; 37, 41, 44, 45). Как показали результаты работы Kojima et al., IGFBP-5, белок семейства сигнальных трансдукторов и активаторов транскрипции (STAT3), участвует в активации ИЛ-6-индуцированного образования активных форм кислорода (АФК), повреждению ДНК и гибели фибробластов (46).
IGFBP-5-опосредованная активация сигнального пути MAPK и транслокация EGR-1 в ядро приводит к активации транскрипции генов медиаторов воспаления и развитию фиброза, способствуя прогрессированию фибротического фенотипа (47). Важным звеном механизма старения гладкомышечных и эндотелиальных клеток является активация пути EGR-1-IGFBP-5-p53 с участием белков раннего ответа при повышении каталитической активности FXa (37). Все эти данные демонстрируют центральную роль IGFBP-5 в регуляции процессов «воспалительного старения», гиперкоагуляции и старения клеток (Рис. 2).
Учитывая равное распределение FXa- и IGFBP-5-положительных областей в атеросклеротических бляшках (41), можно утверждать, что, как и тромбин, местный синтез фактора коагуляции Xa является ключевым индуктором экспрессии IGFBP-5 и патогенетическим фактором SASP-опосредованного клеточного старения (41, 48).
.jpg)
Рисунок 2. Активация каскада свертывания крови в патогенезе клеточного старения и хронического воспаления.
Заключение
В норме элиминация патогенного фактора позволяет устранить воспаление и активировать регенерацию поврежденных тканей. Однако с возрастом хроническое воспаление низкой интенсивности прогрессирует в отсутствие инфекционного агента, способствуя развитию деструктивных изменений в тканях и органах. Хроническое повышение уровня провоспалительных медиаторов при системном воспалении является ведущим фактором риска развития онкологических, сердечно-сосудистых и нейродегенеративных заболеваний, сахарного диабета II типа, саркопении и остеопороза у пожилых пациентов. Учитывая многофакторную природу процесса старения, существующие методы симптоматической и противовоспалительной терапии возрастных заболеваний в большинстве случаев не позволяют достигнуть устойчивого снижения прогрессирования дегенеративных процессов, что делает актуальным разработку методов «сенолитической» терапии, направленной на селективное устранение стареющих клеток (49–52).
Список литературы
Дисклеймер: все утверждения, высказанные в статье, относятся к суждениям авторов и необязательно согласуются с точкой зрения аффилированных организаций, издателя, редакторов и рецензентов. Любой продукт или утверждение производителя не гарантируются и не поддерживаются издателем.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Бактериальный вагиноз: причины появления, симптомы, диагностика и способы лечения.
Определение
Бактериальный вагиноз — это инфекционное полимикробное заболевание, связанное с изменением микрофлоры влагалища, при котором происходит значимое уменьшение количества или полное исчезновение палочек Додерлейна (лактобактерий) и их замещение факультативными анаэробными микроорганизмами и/или возбудителем гарднереллеза. Увеличение уровня лейкоцитов в вагинальном отделяемом и признаки воспаления стенок влагалища могут отсутствовать.
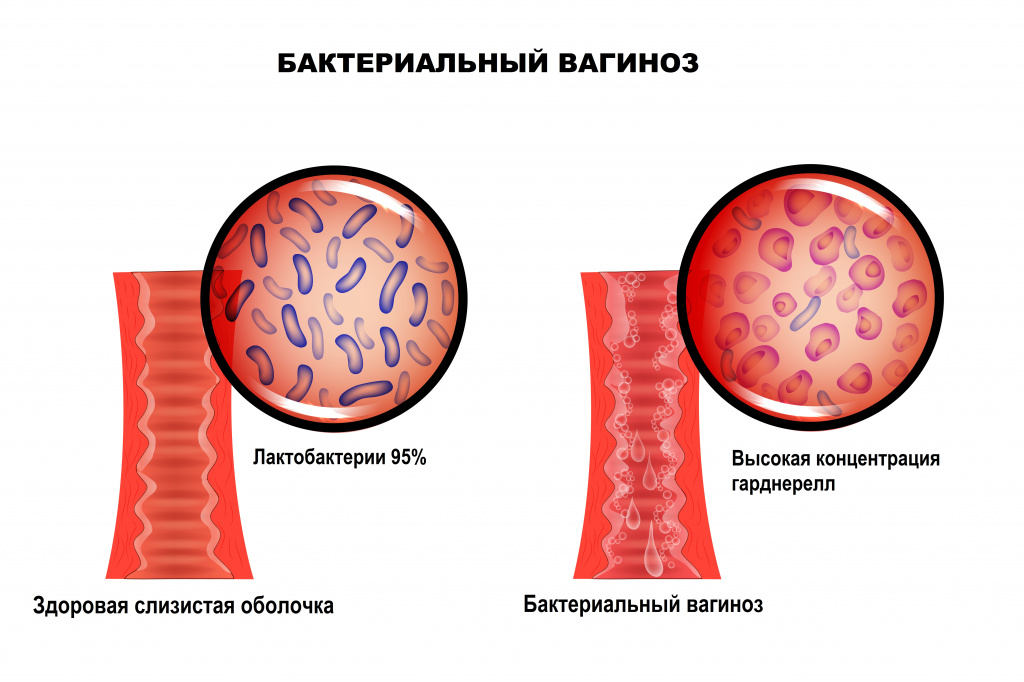
Отличительной особенностью заболевания является отсутствие какого-либо одного конкретного возбудителя. Микрофлора, приходящая на смену лактобактериям, может быть различной и чаще всего представлена условно-патогенными бактериями. Кислотность среды влагалища смещается в сторону ощелачивания. При нарушении экосистемы влагалища формируется хорошо структурированная полимикробная пленка (биопленка - форма микробных сообществ), покрывающая вагинальный эпителий и состоящая из анаэробных бактерий, что приводит к рецидивирующему течению бактериального вагиноза. В биопленках бактерии защищены от компонентов врожденного и приобретенного иммунитета.
В норме ведущее место (95%) в вагинальном микробиоценозе занимают палочки Додерлейна, продуцирующие перекись водорода и молочную кислоту.
Они поддерживают постоянство богатой кислородом кислой рН-среды и играют роль местных факторов защиты. В случае нарушения защитных механизмов патогенные или условно-патогенные микроорганизмы транзиторной или факультативной флоры прикрепляются к клеткам влагалищного эпителия с последующим размножением и повреждением тканей.
Бактериальный вагиноз является наиболее частой причиной патологических вагинальных выделений у женщин репродуктивного возраста, однако иногда он может наблюдаться и у девочек до менархе, и у женщин в период менопаузы.
Причины появления бактериального вагиноза
Предрасполагающие факторы, ведущие к развитию бактериального вагиноза:
- использование антибактериальных препаратов;
- длительное применение внутриматочных контрацептивов;
- ношение синтетического нижнего белья, злоупотребление прокладками на каждый день и тампонами, которые препятствуют проникновению кислорода;
- длительный прием антибиотиков;
- хронические заболевания кишечника и другие состояния, вызывающие дисбактериоз;
- использование пероральных контрацептивов;
- перенесенные ранее воспалительные заболевания урогенитального тракта;
- нарушение гормонального статуса, сопровождающееся нарушением менструального цикла, преимущественно по типу олигоменореи или аменореи;
- атрофия слизистой оболочки влагалища;
- снижение иммунитета;
- воздействие малых доз ионизирующего излучения;
- стрессовые воздействия на организм.
Классификация бактериального вагиноза на основании микроскопического исследования:
- Компенсированный бактериальный вагиноз — количество лактобактерий снижено, что является фактором риска заселения влагалища патогенными микроорганизмами.
- Субкомпенсированный — низкий уровень лактобактерий и растущее число условно-патогенных микроорганизмов.
- Декомпенсированный — в мазке выявляются условно-патогенные микроорганизмы, лактобактерии отсутствуют, выражены клинические симптомы бактериального вагиноза.
У большинства женщин бактериальный вагиноз протекает бессимптомно и может быть обнаружен случайно во время рутинного осмотра и взятия мазка.
Интенсивный рост факультативной флоры, образование патологических биопленок сопровождается появлением влагалищных выделений с характерным неприятным запахом.
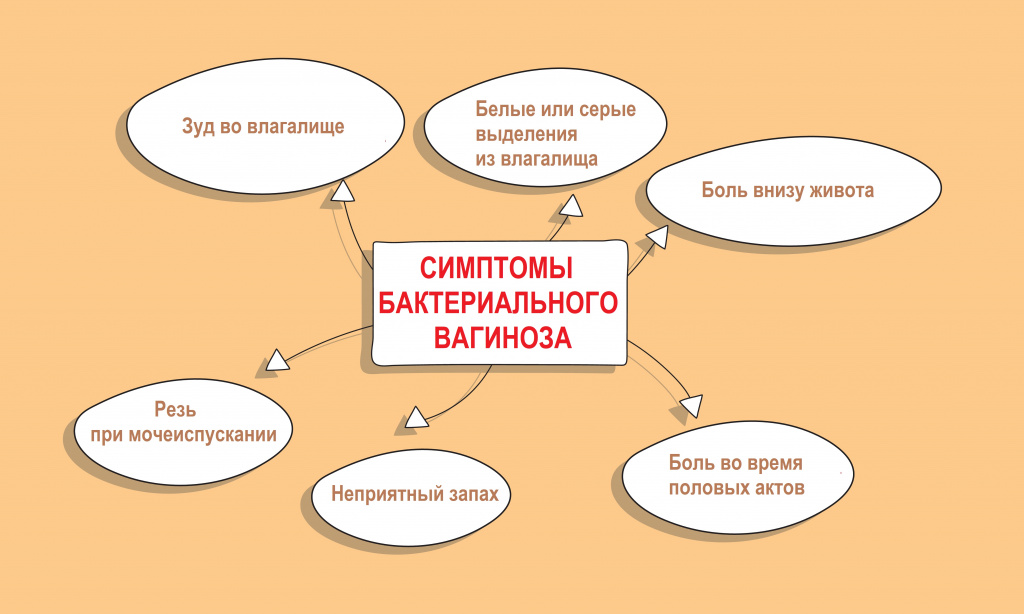
Острый бактериальный вагиноз проявляется выделениями из влагалища, имеющими серовато-белый цвет, однородную консистенцию, неприятный «рыбный» запах; болезненностью во время половых актов; дискомфортом, зудом и жжением в половых органах (могут быть выражены слабо либо отсутствовать); болезненностью, резью при мочеиспускании, болью внизу живота в надлобковой области (редко).
Хронический бактериальный вагиноз — это непрерывное течение заболевания более 2-х месяцев, несмотря на проводимое лечение. Как правило, он сочетается с нарушением гормонального фона и атрофией слизистой оболочки влагалища.
Диагностика бактериального вагиноза
При постановке диагноза у врача есть четыре критерия, которыми он пользуется. Наличие у пациентки трех из них говорит в пользу бактериального вагиноза.
- Наличие гомогенных беловато-серых выделений, равномерно распределяющихся по стенкам влагалища.
- Показатель кислотности при pH-метрии сдвигается в щелочную сторону, повышается уровень влагалищного рН >4,5.
- Положительный аминовый тест с 10% раствором гидроокиси калия (усиление специфического запаха гнилой рыбы) — определение летучих аминов.
- Обнаружение в нативных мазках и/или в мазках по Граму «ключевых клеток», т. е. клеток эпителия влагалища с плотно прикрепленными к их поверхности грамвариабельными микроорганизмами. Лейкоциты в этих мазках содержатся в пределах нормы, что говорит об отсутствии воспаления, а уровень лактобактерий снижен вплоть до полного отсутствия.
Микроскопическое (бактериоскопическое) исследование мазка, окрашенного по Граму. Материалом для оценки состояния флоры влагалища служат гинекологические мазки (отделяемое наружных половых органов, уретры, влагалища, шейки матки, полости матки).
Краткая характеристика Микроскопического исследования мазка, окрашенного по Граму Бактериоскопия (от лат. «скопео» – смотрю) – лабораторный метод исследования бактерий под микроскопом. Метод широко используется врачами разных специальностей при подозрении на инфекционный п.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Атерома: причины появления, симптомы, диагностика и способы лечения.
Определение
Атерома – это киста (патологическая полость) сальной железы, возникающая в результате затруднения или полного прекращения оттока секрета (кожного сала) из железы. Сальные железы относятся к железам наружной секреции и располагаются практически на всех участках кожного покрова, за исключением ладоней, подошв и тыльной стороны стоп. Производимый ими секрет входит в состав водно-липидной мантии кожи. Если проток железы закупоривается, то секрет начинает в нем накапливаться, растягивает его с образованием полости, выстланной эпидермисом и содержащей продукты секреции сальной железы, кристаллы холестерина, ороговевшие клетки эпидермиса и детрит (продукты распада) – это и есть атерома.
Атеромы встречаются у 5-10% населения, преимущественно образуются в возрасте 20-30 лет, с одинаковой частотой у мужчин и у женщин.
Причины возникновения атером
Атерома возникает в результате нарушения работы сальных желез, что проявляется повышенной выработкой кожного сала и закупоркой протока. К этому предрасполагает ряд факторов: повышенное потоотделение, недостаточная гигиена, узость протоков сальных желез, индивидуально обусловленная высокая вязкость кожного сала, хроническая травматизация кожи, гормональные нарушения, обморожения и ожоги. Влияет на развитие атеромы и наследственный фактор.
Классификация заболевания
Выделяют истинные и ложные кисты. Истинные сальные кисты являются наследственно-обусловленным заболеванием и встречаются крайне редко. Они развиваются в результате генетического дефекта, влияющего на формирование железы. Обычно такие кисты встречаются у новорожденных и имеют небольшие размеры. Ложные кисты – это собственно атеромы, возникшие из-за нарушения оттока секрета сальной железы.
Симптомы атеромы
Атеромы чаще всего возникают на участках тела, где много сальных желез, например, на волосистой части головы, лице, шее, в межлопаточном пространстве.
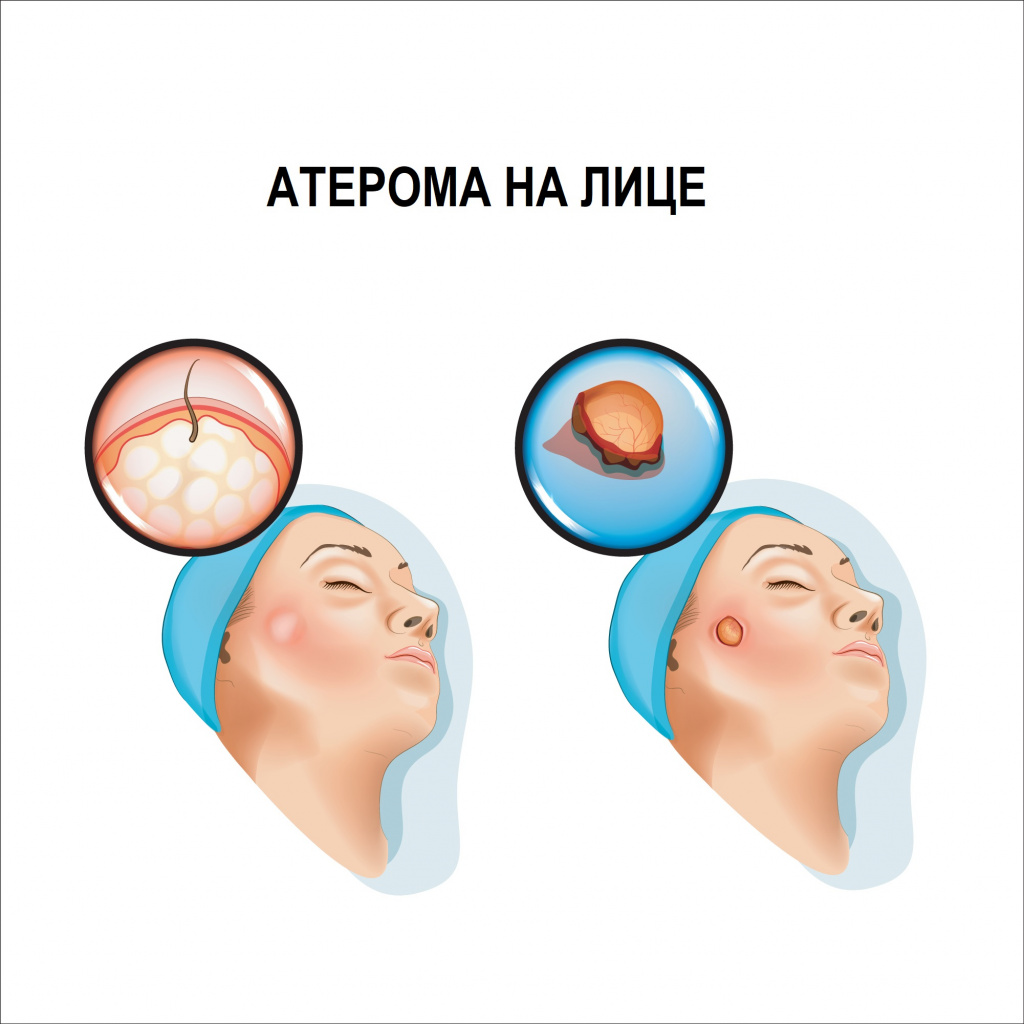
Атерома представляет собой подвижное образование округлой или слегка вытянутой формы, плотной или эластичной консистенции, покрытое неизмененной кожей. Характерным признаком атеромы, отличающим ее от других образований, является наличие точечной втянутости кожи (кратера) в области выводного протока железы и спаянность кожи с оболочкой кисты в этом же месте. Иногда посередине атеромы есть отверстие, через которое выделяется ее содержимое – творожистые массы с неприятным запахом.
Размер атеромы может варьировать от горошины до куриного яйца и даже больше, достигая 10 см. Атерома всегда возвышается над уровнем кожи, увеличивается медленно, обычно безболезненна.
Диагностика атеромы
Для постановки диагноза врач проводит клинический осмотр, в отдельных случаях может потребоваться ультразвуковое исследование.
Исследование мягких тканей для выявления патологических изменений и диагностики новообразований.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Утолщение кожи: причины появления, при каких заболеваниях возникает, диагностика и способы лечения.
Определение
Гиперкератоз – это аномальное утолщение верхнего слоя кожи (эпидермиса) в результате избыточной инсоляции, воздействия химических веществ, частого трения или давления. Кроме того, гиперкератоз может возникать на фоне некоторых заболеваний.
Утолщение кожи происходит в роговом слое эпидермиса, который является конечной точкой процесса дифференцировки кератиноцитов - клеток, содержащих белок кератин. Именно в роговом слое кератиноциты теряют воду и ядро и превращаются в чешуйки рогового слоя – корнеоциты.
При гиперкератозе происходит ускоренная дифференцировка кератиноцитов, а физиологическое слущивание роговых чешуек с поверхности кожи, наоборот, замедляется.
Разновидности гиперкератоза
В зависимости от происхождения выделяют приобретенный и наследственный гиперкератоз.
По клиническим проявлениям.
- Мозоли – часто встречающаяся разновидность гиперкератоза. Различают несколько видов мозолей, но все они появляются вследствие утолщения кожи в местах, наиболее подверженных механическому воздействию. Причем такое изменение кожи может быть связано как с усиленными физическими нагрузками, так и с различными хроническими заболеваниями, что характерно для пожилых пациентов.
- Роговая (тилотическая) экзема проявляется гиперкератозом ладоней и подошв.
- Псориаз - аутоиммунное воспалительное заболевание, при котором на коже формируются гиперкератотические чешуйчатые бляшки.
- Актинический кератоз обычно представлен небольшими красноватыми чешуйчатыми выпуклостями, которые появляются после избыточной инсоляции. Актинический кератоз – серьезное состояние с высокой вероятностью озлокачествления и требует обязательной консультации врача.
- Себорейный кератоз характеризуется маленькими коричневыми или черными пятнами, обычно локализующимися на лице, шее, плечах и спине. Это одно из наиболее распространенных доброкачественных новообразований кожи у взрослых.
- Фолликулярный гиперкератоз («гусиная кожа») характеризуется закупоркой устьев фолликулов ороговевшими клетками эпидермиса.
- Эпидермолитический гиперкератоз - редкое наследственное заболевание, которое проявляется сразу при рождении. Новорожденные имеют красноватую кожу, иногда покрытую небольшими волдырями.
Гиперкератоз кожи может возникнуть у людей, которые пренебрегают регулярными процедурами по уходу за кожей, в результате чего отмершие клетки рогового слоя скапливают и формируют кератомы – доброкачественные новообразования.
Наша кожа постоянно подвергается воздействию неблагоприятных внешних факторов, таких как хлорированная вода и моющие средства, УФ-излучение. В результате повреждается защитный липидный слой кожи, и влага начинает интенсивно испаряться с ее поверхности, а корнеоциты теряют способность к физиологическому слущиванию.
При сахарном диабете гиперкератоз становится следствием нарушения обмена веществ и ухудшения микроциркуляции кожи.
Ношение тесной или неудобной обуви, особенно при плоскостопии, врожденных патологиях стоп, ожирении, может стать причиной утолщение кожи на стопах.
Развитию гиперкератоза шейки матки (лейкоплакии) способствует вирус папилломы человека.
Причиной гиперкератоза может стать хроническое грибковое поражение, а также опоясывающий лишай.
Считается, что симптомы утолщения и сухости кожи могут быть вызваны дефицитом витаминов А, Е, D и С.
Гиперкератоз нередко становится следствием недостатка гормона эстрогена у женщин в период менопаузы.
Заболевания и состояния, при которых развивается гиперкератоз
- Сахарный диабет.
- Ожирение.
- Плоскостопие.
- Ихтиоз.
- Псориаз.
- Экзема.
- Менопауза.
- Грибковое поражение кожи.
- Опоясывающий лишай.
- Эритродермия.
- Атопический дерматит.
- Себорейный кератоз.
Чаще всего за первой консультацией по поводу утолщения кожи обращаются к врачу-дерматологу. После тщательного осмотра, сбора жалоб, выяснения медицинской и семейной истории пациента, проведения лабораторных и инструментальных исследований может потребоваться консультация врача-эндокринолога , врача-онколога , врача-инфекциониста.
Диагностика и обследования при утолщении кожи
Тщательный сбор анамнеза с учетом всех жалоб пациента, осмотр и проведение дополнительных методов диагностики помогут установить причину гиперкератоза.
-
Клинический анализ крови с развернутой лейкоцитарной формулой для выявления воспалительных процессов в организме.
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.

Некроз – заболевание, в результате которого вредные бактерии и микробы атакуют мягкие ткани и останавливают их жизнедеятельность. Такое состояние практически всегда является очень серьезным и требует длительного и качественного лечения в стационарной среде. Но перед тем, как приступать к терапии, необходимо провести детальное обследование больного, чтобы правильно поставить диагноз и установить причину появления заболевания.
Что собой представляет и как протекает болезнь
Некроз – одно из самых страшных заболеваний, при котором прекращается жизнедеятельность тканей, клеток и внутренних органов. Чаще всего к такому состоянию приводит деятельность вредоносных микроорганизмов, а также химические, механические и термические агенты, оказывающие разрушающее действие. Также болезнь может проявиться в результате сильных аллергических реакций или из-за проблем с кровообращением и сильным переохлаждением в этом участке. При сильном перегреве отмечается чрезмерный метаболизм, а в случае проблем с циркуляцией крови увеличивается вероятность появления некротического процесса.
Первыми признаками патологии является онемение, низкий порог чувствительности. В таком случае нужно сразу же обращаться за помощью к специалисту. Дополнительными симптомами является побледнение кожи, что связано с нарушением циркуляции крови. Спустя время кожные покровы могут стать нехарактерного оттенка – желтыми, серыми, зелеными или синими. В случае поражения ног, больной жалуется на быструю усталость при ходьбе, чувство холода и судороги. В результате этого образуются трофические язвы, которые не будут затягиваться и в скором времени приведут к омертвению тканей и кожи.
Все это в совокупности негативно отражается на работе центральной нервной системы, органов дыхания, почек и печени, общее состояние заметно ухудшается, ослабевает иммунитет, нарушается метаболизм, могут появиться заболевания крови.
Виды и формы некроза
Есть 2 основные формы патологии:
Сухой некроз. В медицине также называют коагуляционный. При нем происходит свертывание белка, который в скором времени становится похож на творожную массу. Кожа в проблемных местах станет желто-серой. При этой форме в месте, где происходит отторжение отмершей ткани, появляются язвочки, которые быстро превращаются в гнойники. После их вскрытия образуется свищ. На начальных этапах развития заболевания могут отмечаться следующие симптомы: повышенная температура тела, проблемы с функционированием проблемного органа.
Влажный некроз. Медицинский термин – колликвационный некроз. Проявляется активным увеличением мягких тканей. В местах погибших тканей происходит их разжижение, формируется гнилостная среда для распространения вредоносных микроорганизмов. В добавок появляется запах гнили, с которым невозможно ничего сделать, даже в случае проведения лечения. Такая форма болезни чаще затрагивает кожу, головной мозг и другие органы, в которых собирается много жидкости. При активном развитии болезни могут появиться осложнения. Если некроз поразил головной мозг, то не исключено, что пациент может потерять память.
Помимо форм есть и несколько видов:
пролежни – появляются у пациентов с лежачим образом жизни, которым не оказывают должного ухода;
гангрена – появляется после активно развивающегося некроза. Сопровождается омертвением кожи, слизистых оболочек, тканей мышц;
инфаркт – выявляется тогда, когда внезапно перестает поступать кровь к определенному органу;
асептический – появляется при травме головки бедренной кости. Его симптомы – нестерпимые болевые ощущения в пораженном месте, невозможность самостоятельно передвигаться. Проявляются на 2-3 день после начала болезни;
фибриноидный – выявляется в стенках кровеносных сосудов.
Как лечить заболевание
Несмотря на всю серьезность заболевания, его можно успешно вылечить. Но этим должны заниматься только опытные специалисты в медицинских учреждениях. Терапия в общих чертах выглядит следующим образом:
некроз зубов и десен выявляется весьма оперативно, так как при нем появляются нестерпимые боли и неприятный запах изо рта. Пациентам назначают определенные лекарственные препараты, оказывающие антибактериальное и дезинфицирующее действие. В некоторых случаях поврежденные мягкие ткани приходится удалять путем хирургического вмешательства;
омертвение тканей внутренних органах. Довольно часто болезнь выявляется на последних стадиях. Даже при своевременном обращении к врачу часто ставят другой диагноз, так как симптомы данной патологии носят «смазанный» характер. В случае поражения поджелудочной железы не обходится без оперативного вмешательства. В запущенных случаях грозит летальный исход;
некроз печени. Если при своевременном обнаружении заболевания еще можно ограничиться медикаментозным лечением, то на более поздних этапах без операции не обойтись;
омертвение костной ткани. В большинстве случаев лечится хирургическим путем. Если некроз поразил тазобедренный сустав, то необходимо удалить проблемную область и прибегнуть к эндопротезу. При своевременном выявлении проблемы лечение практически всегда приносит благоприятный исход.
В случае неблагоприятного течения заболевания количество гнойников увеличивается, что в итоге может привести к сильным кровопотерям, увеличении очага. В результате начнется развитие сепсиса. В случае положительного исхода ткани начнут расплавляться, соединительные ткани прорастут в остатки омертвевших участков, с дальнейшим появлением шрама.
В любом случае, при появлении тревожных признаков не стоит их игнорировать или заниматься самолечением. Своевременное обращение к врачам поможет избежать многих серьезных заболеваний и устранить их еще на начальных стадиях.
Все представленные на сайте материалы предназначены исключительно для образовательных целей и не предназначены для медицинских консультаций, диагностики или лечения. Администрация сайта, редакторы и авторы статей не несут ответственности за любые последствия и убытки, которые могут возникнуть при использовании материалов сайта.
Читайте также:

