Кожа при метаболических нарушениях
Обновлено: 24.04.2024
Нарастание частоты заболеваемости инсулинзависимым сахарным диабетом (ИЗСД) у детей и подростков требует расширения исследований по профилактическому и раннему выявлению как доклинических стадий сахарного диабета (СД), так и его осложнений, своевременное
Ряд авторов не только признают, что поражение кожи при ИЗСД является наиболее доступным признаком для клинической оценки врачом, но и прослеживают связь между поражением кожи при ИЗСД и такими осложнениями этого заболевания, как нефропатия, нейропатия, ретинопатия, развитие ограничения подвижности суставов (ОПС) — артропатия (хайропатия)
В настоящее время поражение кожи при ИЗСД у детей может быть классифицировано следующим образом: первичное, вторичное и смешанное (сочетанное) поражения кожи; метаболические нарушения кожи; поражение кожи, связанное с лечением ИЗСД
Нарастание частоты заболеваемости инсулинзависимым сахарным диабетом (ИЗСД) у детей и подростков требует расширения исследований по профилактическому и раннему выявлению как доклинических стадий сахарного диабета (СД), так и его осложнений, своевременное обнаружение и лечение которых являются основными факторами, позволяющими предотвратить инвалидизацию и сократить смертность больных. При ИЗСД поражаются все органы и ткани организма, наиболее общим механизмом поражения является формирование диабетической микроангиопатии. Ряд авторов не только признают, что поражение кожи при ИЗСД является наиболее доступным признаком для клинической оценки врачом, но и прослеживают связь между поражением кожи при ИЗСД и такими осложнениями этого заболевания, как нефропатия, нейропатия, ретинопатия, развитие ограничения подвижности суставов (ОПС) — артропатия (хайропатия). Большинство исследований, проведенных в основном у взрослых больных, страдающих как инсулиннезависимым сахарным диабетом (ИНСД), так и ИЗСД, статистически достоверно показывают, что частота встречаемости симптомокомплекса поражения кожи, чаще всего описываемого как «диабетическая дермопатия», возрастает с повышением частоты других специфических осложнений СД. Все исследователи отмечают, что своевременная диагностика и лечение, включающее повышение уровня гликемического контроля, уменьшают проявления осложнений, а на ранних стадиях делают возможным их обратное развитие.
Особенностью кожных покровов ребенка, обусловливающей их повышенную чувствительность к патологическим изменениям, является более тонкий, чем у взрослых, и более рыхлый слой эпидермиса за счет большего содержания воды. Граница между эпидермисом и дермой неровная, связь между ними слабее, чем у взрослых. Дерма имеет преимущественно клеточную структуру, особенно у детей до шести лет; коллагеновые волокна очень тонкие, эластические, слабо развиты, тогда как волокнистая структура у взрослых имеет малое количество клеточных элементов. За счет этих особенностей защитная функция кожи у детей ослаблена — кожа более ранима, склонна к инфицированию (недостаточная кератинизация рогового слоя, его тонкость, незрелость местного иммунитета), эпидермолизу (легкое отделение эпидермиса от дермы), особенно у детей до трех лет. Поверхность детской кожи суше, чем у взрослых, имеет более выраженную склонность к шелушению вследствие физиологического паракератоза и более слабого функционирования железистого аппарата кожи.
Большинство исследователей считают, что поражения кожи при СД встречаются довольно часто, и, учитывая микроскопические изменения, они могут достигать даже 100% при манифестации заболевания. С помощью гистологических и электронно-микроскопических исследований доказано сходство морфологического строения кожи больных СД в возрасте моложе 40 лет и практически здоровых людей старше 60 лет. У них исчезают эластические волокна и активируются фибробласты, отмечаются разрывы коллагеновых пучков, снижение синтеза эластина и полимеризации коллагена при повышении количества коллагеновых белков, глюкозоаминогликанов, структурных гликопротеинов. При этом установлено, что снижение количества эластических волокон на всех стадиях старения кожи обычно предшествует изменениям коллагена.
У детей, в отличие от взрослых, практически не встречаются такие разнообразные, распространенные при СД первичные формы поражения кожи микроангиопатического и макроангиопатического генеза (в связи с резистентностью к инсулину), как генерализованная кольцевидная гранулема (granuloma annulare), папуллезно-роговой дерматоз Карле (hyperkeratosis follicularis et parafollicularis in cutem penetrans), папиллярно-пигментная дистрофия кожи (acanthosis nigricans), эруптивные ксантомы (xantoma papuloeruptivum), склередема (scleredema), кальцифилаксия (calcifilaxia), а также исчезающие гранулемы, резипелоидоподобная эритема, пигментный пурпурный дерматоз, периунгвальные телеангиоэктазии. Также крайне редки у детей и такие вторичные инфекционные поражения, в том числе кожи, как злокачественный наружный отит — тяжелая инфекция, вызываемая Pseudomonas; неклостридиальная газовая гангрена, как правило вызываемая Proteus, Klebsiella, E. coli, Pseudomonas; некротизирующий фасциит — смертельная инфекция, поражающая поверхностную фасцию. Из метаболических нарушений кожи, сопровождающих СД, практически не встречаются у детей гемохроматоз и порфирия.
- классическая — единичные крупные очаги поражения, чаще встречаемые на коже голеней, нередко с изъязвлениями;
- атипичная — с двумя вариантами течения — склеродермоподобным и поверхностно-бляшечным.
Никакое современное лечение, направленное либо на коррекцию углеводного обмена и метаболических нарушений, либо на улучшение микроциркуляции и тканевой резистентности (лазеротерапия, рентгенотерапия, криодеструкция и др.), не позволяет добиться стойких радикальных результатов. В настоящее время большинство исследователей все же рассматривают ЛН как самостоятельное заболевание — хронический дерматоз.
Таким образом, в настоящее время поражения кожи при ИЗСД у детей может быть классифицированы следующим образом:
- первичное, вторичное и смешанное (сочетанное) поражение кожи;
- метаболические нарушения кожи;
- поражение кожи, связанное с лечением ИЗСД.
Первичное поражение кожи — это сосудистые поражения (осложнения) микроангиопатического генеза — структурные и функциональные нарушения в мелких кровеносных сосудах (артериолы, венулы, капилляры). Клинически проявляются эритемой конечностей, внешне напоминающей рожу, иногда с изъязвлениями. Микроскопически характерны утолщение базальных мембран сосудов и пролиферация эндотелиальных клеток. К ним относится диабетическая дермопатия и рубеоз. Собственно диабетическая дермопатия — одна из самых распространенных форм поражения кожи — выражается в образовании множественных бессимптомных двухсторонних атрофических гиперпигментированных пятен, чаще всего на голенях. Их присутствие свидетельствует о возможности микрососудистых изменений в других тканях. Специфическое лечение дермопатии не проводится. Также имеет место рубеоз — розовый оттенок кожи лица у больных ИЗСД, обусловленный функциональной микроангиопатией или повышенным сродством гликированного гемоглобина к кислороду.
Вторичное поражение кожи включает: кожные инфекции — бактериальные и грибковые; неврологические нарушения — сенсорные, моторные и автономные.
Больные СД склонны к развитию инфекционно-воспалительных заболеваний, особенно при неудовлетворительном контроле гликемии. На поверхности кожи больных СД выявляется в 2,5 раза больше микроорганизмов, чем у здоровых лиц, а бактерицидная активность кожи у больных СД ниже, чем у здоровых, в среднем на 20%, и это снижение прямо коррелирует с тяжестью течения СД, в связи с чем при СД, в том числе ИЗСД, часто наблюдаются различные инфекционно-воспалительные и инфекционно-грибковые заболевания кожи. Прежде всего они развиваются на коже нижних конечностей, пораженных нейропатией и ишемией. Это обычно полимикробные инфекции: золотистый стафилококк, гемолитический стрептококк, грамотрицательные аэробные бактерии и множество анаэробов. На ногах, в области мозолей или в других местах трения и нарушения целостности кожи, в области ногтевых лож образуются язвы или нагноения. Инфекция может распространиться на окружающие ткани, вызывая некротизирующий целлюлит, лимфангит, гнойный миозит, некротизирующий фасциит, остеомиелит или даже газовую гангрену (такие исходы распространения инфекции у детей практически не встречаются). Пиодермии, фурункулы, карбункулы, флегмоны, рожа, дерматиты, эпидермофития, кандидомикоз, хронические паронихии и панариции, инфицированная гангрена встречаются у больных СД значительно чаще, чем в популяции. По принятой нами классификации ИЗСД у детей и подростков инфекционно-воспалительные и инфекционно-грибковые заболевания, в том числе кожи, отнесены не к сопутствующим ИЗСД заболеваниям, а к неспецифическим осложнениям ИЗСД, что правомерно, так как распространенность, тяжесть этих поражений, сложность их лечения у детей обусловлена именно наличием ИЗСД. Фурункулез у больных СД протекает тяжело и длительно, а подкожные абсцессы головы могут привести даже к тяжелым поражениям мозга. У взрослых больных СД встречается и гангрена Фурнье, для которой характерно поражение подкожных тканей в области полового члена, мошонки и промежности, реже — стенки живота. Возбудителем этого поражения является смешанная аэробная и анаэробная микрофлора. Микробно-воспалительные процессы при СД могут привести к сепсису. Присоединение инфекционно-воспалительных и грибковых заболеваний кожи, как правило, приводит к тяжелым и длительным декомпенсациям СД и увеличивает потребность организма в инсулине. У лиц с хорошим контролем СД фурункулез и карбункулы встречаются не чаще, чем в популяции здоровых. Из грибковых поражений у детей с ИЗСД наиболее распространены кандидозы, чаще всего вызывающие ангулярные стоматиты, паронихии, вульвовагиниты или баланиты.
Эпидермофитии у детей с ИЗСД довольно редки, но часто осложняются вторичной бактериальной инфекцией. Крайне редки у детей трудно поддающиеся терапии фикомикоз, мукормикоз, при которых в процесс могут вовлекаться мозговые оболочки. У детей с ИЗСД довольно распространены дерматомикозы, особенно стоп и ладоней, кожа которых становится сухой и чешуйчатой.
Широко распространены вторичные нарушения кожи, связанные с неврологической патологией при СД. Среди них: сенсорные нарушения — онемение пальцев ног, постепенно распространяющееся выше, захватывающее стопы, способствующее развитию травматических язвенных поражений, вторичных инфекций и гангрены, особенно при наличии сосудистых изменений; моторные нарушения — слабость межкостных мышц вызывает уплощение стоп с потерей смягчающей функции подошвы стоп; автономные (вегетативные) нарушения — гипергидроз верхней половины тела и сухость кожи нижней части туловища. Эти проявления относятся к диабетической нейропатии, поражающей 5-50% больных СД. У детей с ИЗСД наиболее часто встречается дистальная симметричная сенсорно-моторная полинейропатия с минимальными кожными проявлениями (сухость кожи, гиперкератоз, мозоли, вторичное инфицирование пораженных участков кожи, нарушения роста ногтей), обратимая в фазе начальных проявлений. Именно нейропатия — один из ведущих патогенетических факторов развития в дальнейшем синдрома «диабетической стопы» (ДС). Среди больных СД, осложненным синдромом ДС, частота ампутации нижних конечностей в 15 раз выше, чем у остального населения. При преобладании нейропатических изменений над изменениями периферического кровотока развивается нейропатическая форма ДС, одним из вариантов течения которой является поражение кожи — нейропатическая язва. Она чаще возникает на участках стопы, испытывающих давление, — плантарной поверхности и межпальцевых промежутках. Длительно протекающая сенсорно-моторная нейропатия приводит к деформации стопы с перераспределением и повышением давления на ее отдельные участки. В этих местах отмечается утолщение кожи, гиперкератоз с высокой плотностью. В дальнейшем развивается аутолиз подлежащих мягких тканей с формированием язвенного дефекта, при этом больной может ничего не замечать из-за снижения болевой чувствительности. Язвенный дефект может вторично инфицироваться, в том числе анаэробной микрофлорой, с развитием гипертермии, лейкоцитоза, требующих срочного хирургического лечения с некроэктомией, антибактериальной терапией, улучшением гликемического контроля. У детей все формы ДС встречаются крайне редко, но начальные проявления имеют место в детском возрасте, что требует адекватного обучения, обследования и лечения больных, в том числе прицельного осмотра состояния кожи при ИЗСД.
К смешанному (сочетанному) поражению кожи при СД относятся: утолщение кожи (синдром «диабетической руки» — ОПС с утолщением кожи и склеродермоподобным синдромом), желтый цвет кожи и ногтей, синдром «диабетических пузырей», пруригус и повреждения волос. К нему же следует отнести склеродермоподобные изменения кожи пальцев и тыльной части кистей рук, снижающие их подвижность. Кожа утолщается в области пальцевых суставов и периунгвально. Эти изменения, иногда в сочетании с артропатией (ОПС), описываются некоторыми исследователями как синдром «диабетической руки». Часто с утолщением кожи ассоциируется гиперкератоз. Желтый цвет кожи и ногтей (ксантохромия) ранее связывался с гиперкаротинемией, но сейчас доказано, что при СД в крови сохраняется нормальный уровень каротина. В настоящее время этиология и патогенез не выяснены. Синдром «диабетических пузырей» возникает редко, как правило на коже конечностей. Выявляются одиночные или множественные пузыри, заживающие без рубцевания через две—пять недель. Возможна симптоматическая терапия. Пруригус — поражение кожи в аногенитальной области на фоне кандидоза (гиперемия, трещины, шелушения, вторичное инфицирование). Иногда при плохо контролируемом СД может быть диффузное выпадение, а у больных пониженного питания — избыточный рост волос (лануго) на коже рук и спины. Редко, обычно при плохом уровне гликемического контроля, наблюдаются повышенное шелушение кожи, себорейный дерматит, ихтиозоподобный синдром, особенно в области голеней.
К метаболическим нарушениям кожи при СД относится ксантоматоз, редко встречающийся в детском возрасте и являющийся следствием гиперлипидемии. Клинически ксантоматоз проявляется в виде плотных желтых папул с эритематозным ободком, чаще на кистях, стопах, ягодицах, разгибательных поверхностях верхних и нижних конечностей. Купируется адекватной инсулинотерапией.
Специфическими кожными осложнениями лечения ИЗСД являются липодистрофии, образующиеся в местах инъекций инсулина. Встречаются в виде липом или липогипертрофий (плюс-ткань) и липоатрофий (минус-ткань). В связи с широким применением в настоящее время хорошо очищенных биосинтетических человеческих инсулинов липоатрофии встречаются крайне редко. В настоящее время именно липогипертрофии, или липомы, представляют собой наиболее распространенную проблему для больных ИЗСД, даже при небольшом сроке заболевания. Они возникают в результате некорректной техники введения инсулина (нарушения схем ротаций мест инъекций инсулина, несоблюдение техники и правил введения препаратов), а иногда и без видимых причин; затрудняют абсорбцию и метаболизм инсулина, ухудшают компенсацию заболевания, увеличивают потребность в инсулине, создают косметические дефекты на коже. Кроме вышеописанных правил профилактики липодистрофий, в случае их появления дополнительно и с хорошим эффектом применяется массаж липом, физиотерапия. Также у некоторых больных периодически возникают кровоподтеки в местах инъекций инсулина. Эти места, как правило, теплее на ощупь, чем окружающая кожа.
Обобщая вышеизложенное, можно сказать, что исследование кожи, представляющей собой наиболее доступную неинвазивному клиническому осмотру систему организма, имеет огромное клиническое значение. Знание особенностей поражения кожи у детей при ИЗСД не только помогает в оценке фазы течения заболевания, но и имеет непреходящее значение для решения вопросов о направлении диагностического поиска, коррекции лечения и прогнозе течения ИЗСД.

- Метаболический синдром: критерии и клинические кожные проявления
- Почему возникает повышенная чувствительность кожи
- Барьерная функция, воспаление и чувствительность кожи
- Окислительный стресс, метаболический синдром и чувствительность кожи
- Влияние эндокринных нарушений при МС начувствительность кожи
Метаболический синдром: критерии и клинические кожные проявления
Метаболический синдром (МС) – заболевание, при котором у пациента наблюдается центральная форма ожирения (у женщин >80 см, у мужчин >94 см) и обеспечивается соответствие минимум двум из нижеприведенных критериев:
- повышенный уровень триглицеридов или глюкозы в крови;
- низкий уровень липопротеина высокой плотности;
- высокое давление крови.
Различные клинические кожные проявления, ассоциированные с метаболическим синдромом и/или его составляющими, были определены в ходе нескольких международных исследований.
Перечень заболеваний включает в себя:
- псориаз;
- андрогенетическую алопецию;
- акантокератодермию;
- мягкие фибромы;
- лишай Вильсона;
- инверсные угри;
- системную красную волчанку;
- и даже рак кожи.
Как известно, при метаболическом синдроме повышено количество воспалительных цитокинов и наблюдается хроническая воспалительная реакция в коже. Поэтому не исключается связь МС с повышенной чувствительностью кожи, которая сопровождается активацией иммунных клеток.
Почему возникает повышенная чувствительность кожи
Чувствительность кожи проявляется с различной степенью интенсивности, определяемой по субъективным показателям, таким как жжение и болевые ощущения, в ответ на раздражающие факторы (ветер, высокая температура, сухость, стресс, гормональный дисбаланс, неправильный уход за кожей).
Патофизиология повышенной чувствительности кожи не до конца изучена. Существует несколько теорий, объясняющих гиперчувствительность кожи, таких как:
- изменения кожного барьера;
- активация кератиноцитов;
- нейрогенное воспаление/нейронный механизм;
- снижение толерантности кожи;
- генетическая предрасположенность.
Даже при отсутствии задокументированных клинических признаков повышенной чувствительности кожи нельзя игнорировать субъективные симптомы пациентов, особенно с метаболическим синдромом.
Чаще всего рассматривают такие потенциальные механизмы:
- изменение функции барьера кожи;
- нейрогенное воспаление.
Нарушение барьерной функции рогового слоя эпидермиса делает уязвимыми клетки иммунной системы и чувствительные нервы, что приводит к выраженному ответу на не опасные в противном случае стимулы.
Барьерная функция, воспаление и чувствительность кожи
Одна из функций кожи – защита организма от негативных факторов внешней среды на трех уровнях:
- физический (защита от механического повреждения, неконтролируемой потери воды и растворенных в ней веществ) – роговой слой, ядерные клетки эпидермиса и десмосомы;
- химический/биохимический – внутренний иммунитет (жиры, органические кислоты, лизосомы и антимикробные пептиды);
- гуморальная и клеточная иммунная система (лимфоциты, нейтрофилы, моноциты и клетки Лангерганса).

Установлено, что у людей с болезненным ожирением восстановление кожного барьера нарушено. Кожный барьер формируется за счет дифференциации кератиноцитов и постоянной регенерации. В ходе дифференциации кератиноциты проходят через разные этапы развития. Это сложный процесс, в котором задействованы белки, жирные кислоты, жиры и ферменты. Их функции и экспрессия контролируются цитокинами и внеклеточными сигнальными молекулами и рецепторами. Потому, чтобы обеспечить надлежащие развитие эпидермального барьера, необходима правильная регуляция всех компонентов, вовлеченных в процесс дифференциации, а также их своевременная и достаточная экспрессия.
Различные цитокины действуют на различных уровнях, осуществляя контроль формирования кожного барьера. Потому в случае дисрегуляции экспрессии цитокинов:
- увеличивается трансэпидермальная потеря влаги;
- функция эпидермального барьера снижается;
- воспалительная реакция усиливается.
В ответ на минимальное внешнее раздражение из корнеоцитов и зернистых клеток высвобождаются IL-1α, IL-1β и TNF-α. Небольшие количества IL-6 находится в клетках эпидермиса. Однако в случае нарушения кожного барьера их количество стремительно увеличивается. Эти цитокины играют роль в формировании и восстановлении эпидермального барьера.
В коже больных метаболическим синдромом больше воспалительных цитокинов (TNF-α, IL-6, MCP-1), ангиотензина и прочих адипоцитокинов, вырабатываемых жировыми клетками, которые являются частью врожденной иммунной системы, регулирующей воспаление. Нарушение регуляции или секреции этих адипокинов, вызванное дисфункцией жировой ткани, может быть фактором развития осложнений, ассоциированных с ожирением. В то же время эти цитокины могут стимулировать эпидермальную пролиферацию и омоложение. Однако при хронически повышенном уровне воспалительных цитокинов, как в случае МС, воспалительный каскад может привести к системной активации иммунитета.
Окислительный стресс, метаболический синдром и чувствительность кожи
Окислительному стрессу отводят центральную роль в патогенезе метаболического синдрома. Кожа играет важную роль в метаболизме и выведении ксенобиотиков, эндогенных биоактивных веществ, жиров и холестерина.
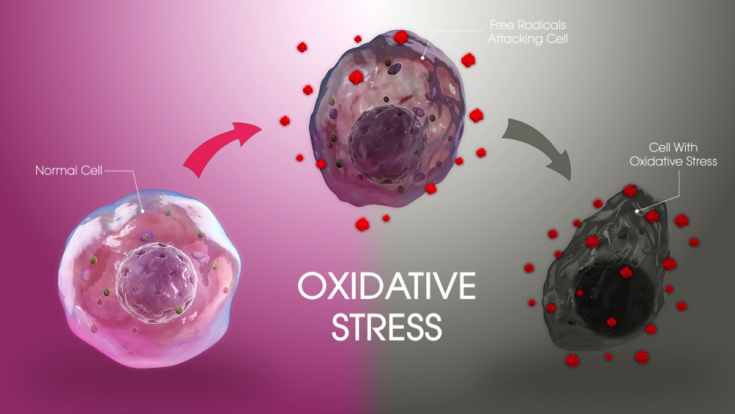
Ксенобиотики, такие как экзогенные химические вещества, лекарства, загрязняющие вещества, косметические средства и ингредиенты продуктов питания – основные источники активных форм кислорода, которые, как считается, могут быть составляющей патогенеза ряда заболеваний кожи.
Хорошо известно, что воспаление является одним из проявлений окислительного стресса, а пути, которые ведут к выработке медиаторов воспаления, таких как интерлейкины, связаны с окислительным стрессом.
Различные компоненты метаболического синдрома подвержены сезонным колебаниям: давление крови и уровень холестерина в крови повышаются зимой.
Будучи более чувствительной к температуре окружающей среды, чем другие органы, кожа, возможно, частично обусловливает связь между колебаниями кровяного давления и температурой окружающей среды.
Большинство пациентов с чувствительной кожей сообщают о неприятных чувствительных реакциях на низкие температуры и влажность, что приводит к снижению уровня влаги в роговом слое. Чаще такие условия возникают зимой. А потому сезонные вариации МС более выражены у пациентов с чувствительной кожей.
Влияние эндокринных нарушений при МС на чувствительность кожи
Адипоциты секретируют несколько эндокринных пептидов, таких как лептин и адипонектин. Эти вещества вовлечены в острые и хронические воспалительные процессы за счет регуляции экспрессии цитокинов, модулирующей баланс Т-клеток-хелперов 1 и 2 типа, а также изменения метаболизма глюкозы и биологию эндотелия сосудов.

У большинства пациентов с ожирением повышен уровень циркулирующего лептина в условиях функциональной устойчивости к лептину. Рецепторы лептина находятся в тканях, в т.ч. кератиноцитах, фибробластах, эндотелиальных клетках и жировой ткани. Лептин также играет роль в формировании эпидермального барьера, способствует заживлению ран, стимулирует:
- пролиферацию фибробластов;
- синтез коллагена;
- рост эндотелиальных клеток;
- ангиогенез.
Однако повышенные уровни лептина у пациентов с МС токсичны для сосудистой системы и приводят к капиллярной утечке и образованию аваскулярных зон.
В клинических случаях персистирующая или преходящая эритема и телеангиэктазия наблюдались у большинства пациентов с чувствительной кожей. Потому при повышенной чувствительности кожи и МС эти клинические признаки более выражены.
Адипонектин играет роль в выработке кожного сала, способствовуя формированию дифференцированных структур сальных желез и увеличением их количества.
Как известно, липиды себоцитов секретируются на поверхность кожи, где они выполняют важные барьерные функции.
Но у пациентов с метаболическим синдромом уровень адипонектина снижен. Помимо этого, его уровень обратно пропорционален количеству критериев МС – по мере увеличения количества критериев уровень адипонектина снижается, как и барьерная функция, а чувствительность кожи, соответственно, усиливается.
Для чувствительной кожи, пораженной метаболическим синдромом, характерны более выраженные:
- дисфункция кожного барьера;
- воспаление;
- иммунные реакции;
- окислительный стресс;
- сезонные вариации;
- сниженная способность к регенерации.
Однако информации о связи повышенной чувствительности кожи и метаболических заболеваний, таких как ожирение, диабет и метаболический синдром, недостаточно. Не до конца ясно, метаболический синдром вызывает чувствительность кожи или наоборот. Для ответа на этот вопрос требуются дальнейшие исследования.

- Метаболический синдром: критерии и клинические кожные проявления
- Почему возникает повышенная чувствительность кожи
- Барьерная функция, воспаление и чувствительность кожи
- Окислительный стресс, метаболический синдром и чувствительность кожи
- Влияние эндокринных нарушений при МС начувствительность кожи
Метаболический синдром: критерии и клинические кожные проявления
Метаболический синдром (МС) – заболевание, при котором у пациента наблюдается центральная форма ожирения (у женщин >80 см, у мужчин >94 см) и обеспечивается соответствие минимум двум из нижеприведенных критериев:
- повышенный уровень триглицеридов или глюкозы в крови;
- низкий уровень липопротеина высокой плотности;
- высокое давление крови.
Различные клинические кожные проявления, ассоциированные с метаболическим синдромом и/или его составляющими, были определены в ходе нескольких международных исследований.
Перечень заболеваний включает в себя:
- псориаз;
- андрогенетическую алопецию;
- акантокератодермию;
- мягкие фибромы;
- лишай Вильсона;
- инверсные угри;
- системную красную волчанку;
- и даже рак кожи.
Как известно, при метаболическом синдроме повышено количество воспалительных цитокинов и наблюдается хроническая воспалительная реакция в коже. Поэтому не исключается связь МС с повышенной чувствительностью кожи, которая сопровождается активацией иммунных клеток.
Почему возникает повышенная чувствительность кожи
Чувствительность кожи проявляется с различной степенью интенсивности, определяемой по субъективным показателям, таким как жжение и болевые ощущения, в ответ на раздражающие факторы (ветер, высокая температура, сухость, стресс, гормональный дисбаланс, неправильный уход за кожей).
Патофизиология повышенной чувствительности кожи не до конца изучена. Существует несколько теорий, объясняющих гиперчувствительность кожи, таких как:
- изменения кожного барьера;
- активация кератиноцитов;
- нейрогенное воспаление/нейронный механизм;
- снижение толерантности кожи;
- генетическая предрасположенность.
Даже при отсутствии задокументированных клинических признаков повышенной чувствительности кожи нельзя игнорировать субъективные симптомы пациентов, особенно с метаболическим синдромом.
Чаще всего рассматривают такие потенциальные механизмы:
- изменение функции барьера кожи;
- нейрогенное воспаление.
Нарушение барьерной функции рогового слоя эпидермиса делает уязвимыми клетки иммунной системы и чувствительные нервы, что приводит к выраженному ответу на не опасные в противном случае стимулы.
Барьерная функция, воспаление и чувствительность кожи
Одна из функций кожи – защита организма от негативных факторов внешней среды на трех уровнях:
- физический (защита от механического повреждения, неконтролируемой потери воды и растворенных в ней веществ) – роговой слой, ядерные клетки эпидермиса и десмосомы;
- химический/биохимический – внутренний иммунитет (жиры, органические кислоты, лизосомы и антимикробные пептиды);
- гуморальная и клеточная иммунная система (лимфоциты, нейтрофилы, моноциты и клетки Лангерганса).

Установлено, что у людей с болезненным ожирением восстановление кожного барьера нарушено. Кожный барьер формируется за счет дифференциации кератиноцитов и постоянной регенерации. В ходе дифференциации кератиноциты проходят через разные этапы развития. Это сложный процесс, в котором задействованы белки, жирные кислоты, жиры и ферменты. Их функции и экспрессия контролируются цитокинами и внеклеточными сигнальными молекулами и рецепторами. Потому, чтобы обеспечить надлежащие развитие эпидермального барьера, необходима правильная регуляция всех компонентов, вовлеченных в процесс дифференциации, а также их своевременная и достаточная экспрессия.
Различные цитокины действуют на различных уровнях, осуществляя контроль формирования кожного барьера. Потому в случае дисрегуляции экспрессии цитокинов:
- увеличивается трансэпидермальная потеря влаги;
- функция эпидермального барьера снижается;
- воспалительная реакция усиливается.
В ответ на минимальное внешнее раздражение из корнеоцитов и зернистых клеток высвобождаются IL-1α, IL-1β и TNF-α. Небольшие количества IL-6 находится в клетках эпидермиса. Однако в случае нарушения кожного барьера их количество стремительно увеличивается. Эти цитокины играют роль в формировании и восстановлении эпидермального барьера.
В коже больных метаболическим синдромом больше воспалительных цитокинов (TNF-α, IL-6, MCP-1), ангиотензина и прочих адипоцитокинов, вырабатываемых жировыми клетками, которые являются частью врожденной иммунной системы, регулирующей воспаление. Нарушение регуляции или секреции этих адипокинов, вызванное дисфункцией жировой ткани, может быть фактором развития осложнений, ассоциированных с ожирением. В то же время эти цитокины могут стимулировать эпидермальную пролиферацию и омоложение. Однако при хронически повышенном уровне воспалительных цитокинов, как в случае МС, воспалительный каскад может привести к системной активации иммунитета.
Окислительный стресс, метаболический синдром и чувствительность кожи
Окислительному стрессу отводят центральную роль в патогенезе метаболического синдрома. Кожа играет важную роль в метаболизме и выведении ксенобиотиков, эндогенных биоактивных веществ, жиров и холестерина.

Ксенобиотики, такие как экзогенные химические вещества, лекарства, загрязняющие вещества, косметические средства и ингредиенты продуктов питания – основные источники активных форм кислорода, которые, как считается, могут быть составляющей патогенеза ряда заболеваний кожи.
Хорошо известно, что воспаление является одним из проявлений окислительного стресса, а пути, которые ведут к выработке медиаторов воспаления, таких как интерлейкины, связаны с окислительным стрессом.
Различные компоненты метаболического синдрома подвержены сезонным колебаниям: давление крови и уровень холестерина в крови повышаются зимой.
Будучи более чувствительной к температуре окружающей среды, чем другие органы, кожа, возможно, частично обусловливает связь между колебаниями кровяного давления и температурой окружающей среды.
Большинство пациентов с чувствительной кожей сообщают о неприятных чувствительных реакциях на низкие температуры и влажность, что приводит к снижению уровня влаги в роговом слое. Чаще такие условия возникают зимой. А потому сезонные вариации МС более выражены у пациентов с чувствительной кожей.
Влияние эндокринных нарушений при МС на чувствительность кожи
Адипоциты секретируют несколько эндокринных пептидов, таких как лептин и адипонектин. Эти вещества вовлечены в острые и хронические воспалительные процессы за счет регуляции экспрессии цитокинов, модулирующей баланс Т-клеток-хелперов 1 и 2 типа, а также изменения метаболизма глюкозы и биологию эндотелия сосудов.

У большинства пациентов с ожирением повышен уровень циркулирующего лептина в условиях функциональной устойчивости к лептину. Рецепторы лептина находятся в тканях, в т.ч. кератиноцитах, фибробластах, эндотелиальных клетках и жировой ткани. Лептин также играет роль в формировании эпидермального барьера, способствует заживлению ран, стимулирует:
- пролиферацию фибробластов;
- синтез коллагена;
- рост эндотелиальных клеток;
- ангиогенез.
Однако повышенные уровни лептина у пациентов с МС токсичны для сосудистой системы и приводят к капиллярной утечке и образованию аваскулярных зон.
В клинических случаях персистирующая или преходящая эритема и телеангиэктазия наблюдались у большинства пациентов с чувствительной кожей. Потому при повышенной чувствительности кожи и МС эти клинические признаки более выражены.
Адипонектин играет роль в выработке кожного сала, способствовуя формированию дифференцированных структур сальных желез и увеличением их количества.
Как известно, липиды себоцитов секретируются на поверхность кожи, где они выполняют важные барьерные функции.
Но у пациентов с метаболическим синдромом уровень адипонектина снижен. Помимо этого, его уровень обратно пропорционален количеству критериев МС – по мере увеличения количества критериев уровень адипонектина снижается, как и барьерная функция, а чувствительность кожи, соответственно, усиливается.
Для чувствительной кожи, пораженной метаболическим синдромом, характерны более выраженные:
- дисфункция кожного барьера;
- воспаление;
- иммунные реакции;
- окислительный стресс;
- сезонные вариации;
- сниженная способность к регенерации.
Однако информации о связи повышенной чувствительности кожи и метаболических заболеваний, таких как ожирение, диабет и метаболический синдром, недостаточно. Не до конца ясно, метаболический синдром вызывает чувствительность кожи или наоборот. Для ответа на этот вопрос требуются дальнейшие исследования.
Нарушение обмена веществ происходит под воздействием внутренних и внешних причин. Помимо неприятных ощущений в теле и утраты физической выносливости при неправильном метаболизме мы можем сталкиваться с повреждениями кожи. Поговорим о причинах негативного влияние нарушений обмена веществ на состоянии кожи и способах борьбы с ними.
Почему так важен правильный обмен веществ
На форумах многие девушки жалуются, что у них появилась болезнь разный цвет кожи. Причина этого явления заключается в неправильном метаболизме. Когда в теле замедляются процессы усвоения полезных веществ, это приводит к замедлению естественной регенерации кожи. В дальнейшем могут появиться преждевременные признаки старения кожи лица.

Ухудшение состояние кожи может возникнуть на фоне отравления организма шлаками и токсинами. Такое явление наблюдается у людей, не проявляющих интереса к активному образу жизни и правильному питанию. Бледная кожа женщины может говорить о том, что в организме не хватает витаминов, необходимых для полноценного питания клеток.
Неровный цвет лица может говорить о проблемах кровоснабжения мягких тканей и органов, указывать на нарушения в работе лимфатических сосудов. К примеру, когда процесс метаболизма замедляется, это приводит к сокращению просвета в кровеносных сосудах, клетки кожи могут страдать из-за кислородного голодания. Если к этому прибавляется сокращение лимфатических сосудов, в мягких тканях может отмечаться застой жидкости. На лице это проявляется в виде мешков и кругов под глазами.
Многие девушки жалуются на прыщики на лице и шее. К этому могут приводить вредные привычки и неправильное питание. Повышение склонности к воспалительным процессам на коже отмечается при курении и склонности к перееданию. К нарушению процессов усвоения питательных компонентов может приводить обезвоженность кожи. Вода является необходимым компонентам для поддержания процессов жизнедеятельности клеток.
Причины, по которым нарушается обмен веществ
Дряблость кожи лица и другие повреждения эпидермиса могут возникнуть по следующим причинам:
- Недосыпание и переедание;
- Неправильное питание, например, соблюдение диеты с жесткими ограничениями;
- Депрессии и гормональные нарушения.
Все перечисленные факторы провоцируют дисбаланс обмена веществ в теле, что отражается на состоянии кожи.

Перечислим необходимые компоненты для поддержания здорового обмена веществ для человека:
- Белки — являются строительным материалом для клеток, регулируют в тканях водно-солевой баланс и сопровождают процессы ферментации (усвоения питательных веществ);
- Углеводы — нужны в качестве источника энергии для поддержания активного образа жизни;
- Жиры — выступают питательной средой для синтеза гормонов и участвуют в создании оболочки клеток кожи; — ускоряют внутриобменные процессы в организме, выступают в качестве катализаторов клеток.
Как неправильный обмен веществ отражается на коже
В зависимости от характера нарушений обменных процессов, у девушки могут появиться следующие проблемы с кожей:
- Появление преждевременных признаков старения;
- Дряблость кожи и ее обезвоживание;
- Появление отечности, воспалений на лице;
- Изменение оттенка кожи и ее рельефа.
Кожа лица одной из первых сигнализирует нам о том, что в организме что-то пошло не так, так как кожа выполняет защиту от внутренних и внешних факторов.
Как устранить дефекты кожи из-за неправильного обмена веществ
Наша главная задача — выявить причину, по которой возникли сбои обмена веществ в теле. Обычно нормальный обмен веществ поддерживаются за счет нескольких составляющих:

В косметологии существуют эффективные методики для борьбы с повреждениями кожи из-за нарушения обмена веществ.
К ним необходимо отнести инъекционные процедуры, которые позволяют доставить питательные компоненты к клеткам кожи, а также пилинги для полноценного очищения кожи и ускорения процессов регенерации. Высокую эффективность демонстрируют комплексные косметические средства по уходу за кожей.
Заключение
Нарушение обмена веществ отражается на нашем самочувствии и состоянии кожи. К повреждениям кожи из-за отклонений в метаболизме могут привести внутренние причины и факторы внешней среды. Поддержание сбалансированного питания и ведение активного образа жизни способствует нормализации метаболизма. В качестве средств профилактики и борьбы с проблемами кожи косметология рассматривает инъекционные процедуры, пилинги и использование линеек профессиональной косметики.
Что такое метаболический синдром? Причины возникновения, диагностику и методы лечения разберем в статье доктора Чернышева Андрея Владимировича, кардиолога со стажем в 33 года.
Над статьей доктора Чернышева Андрея Владимировича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Метаболический синдром (синдром Reaven) представляет собой симптомокомплекс, сочетающий в себе абдоминальное ожирение, инсулинорезистентность, гипергликемию (повышенное содержание глюкозы в крови), дислипидемию и артериальную гипертензию. Все эти нарушения связаны в одну патогенетическую цепь. Кроме того, такой синдром часто сочетается с гиперурикемией (избытком мочевой кислоты в крови), нарушением гемостаза (свёртываемости крови), субклиническим воспалением, синдромом обструктивного апноэ-гипопноэ сна (остановкой дыхания во сне). [4]
Метаболический синдром – хроническое, распространённое (до 35% в российской популяции), полиэтиологическое заболевание (возникающее по многим причинам), в котором главная роль принадлежит поведенческим факторам (гиподинамия, нерациональное питание, стресс). Имеет значение также наследственная предрасположенность к артериальной гипертензии, атеросклероззависимым заболеваниям и сахарному диабету второго типа. [5]
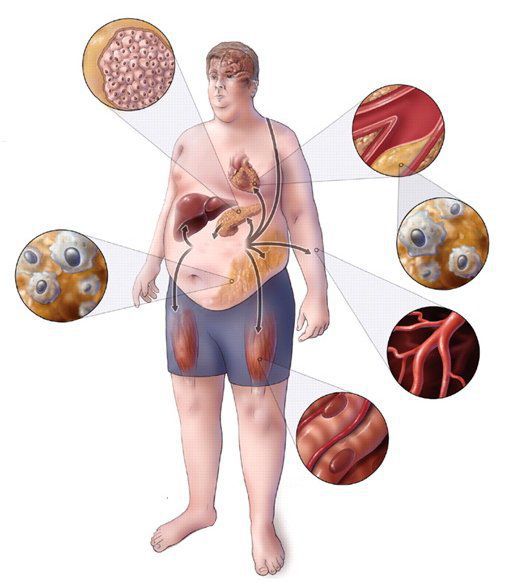
Практикующим врачам важно выделять группу риска метаболического синдрома. К данной группе относятся пациенты с начальными признаками заболевания и его осложнениями: артериальная гипертензия, углеводные изменения, ожирение и повышенное питание, ишемическая болезнь сердца, атеросклеротические заболевания периферических и мозговых артерий, нарушение пуринового обмена, жировая болезнь печени; синдром поликистозных яичников; постменопаузальный период у женщин и эректильная дисфункция у мужчин; гиподинамия, злоупотребление алкоголем, табакокурение, наследственная отягощенность по сердечно-сосудистым и обменным заболеваниям. [3] [7]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы метаболического синдрома
Клинические проявления метаболического синдрома соответствуют симптомам его составляющих:
- абдоминального ожирения;
- артериальной гипертензии;
- изменениям углеводного, липидного и пуринового обмена.
Если изменения составляющих синдрома Reaven носят субклинический характер (что встречается довольно часто), то и течение заболевания носит асимптомный характер.
Патогенез метаболического синдрома
Инсулинорезистентность — первопричина развития метаболического синдрома. Представляет собой нарушение утилизации глюкозы в органах-мишенях (поперечнополосатой мускулатуре, липоцитах и печени), связанное с дисфункцией инсулина. Инсулинорезистентность уменьшает усвоение и поступление в клетки скелетной мускулатуры глюкозы; стимулирует липолиз и гликогенолиз, что приводит к липидным и углеводным патологическим изменениям. Кроме того, инсулинорезистентность усиливает секрецию инсулина, в результате чего возникает компенсаторная гиперинсулинемия и активация эндокринных систем (симпатоадреналовой, ренин-ангиотензин-альдостероновой) с формированием артериальной гипертензии, дальнейшим нарушением метаболических процессов, гиперкоагуляции, субклинического воспаления, дисфункции эндотелия и атерогенеза. Эти изменения, в свою очередь, способствуют усилению инсулинорезистентности, стимулируя патогенетический «порочный круг».
Классификация и стадии развития метаболического синдрома
Чёткой классификации и стадийности метаболического синдрома не существует. Его деление некоторыми авторами на полный, включающий все составляющие синдрома, и неполный представляется необоснованным. Несмотря на это, выраженность симптомов, количество компонентов синдрома Reaven и наличие осложнений оказывают влияние на стратификацию риска и выбор тактики лечения у конкретного пациента. Для этого следует учитывать:
- степень ожирения и артериальной гипертензии;
- выраженность метаболических изменений;
- наличие или отсутствие сахарного диабета и заболеваний, связанных с атеросклерозом.
В зависимости от индекса массы тела (ИМТ), который рассчитывается делением веса (кг) на рост (м 2 ), классифицируются следующие типы массы тела (МТ):
Важную роль играет распределение жировой ткани. Различают два типа ожирения:
- гиноидный (по типу «груша»), когда избыточная жировая ткань распределяется преимущественно на бёдрах и ягодицах;
- андроидный (по типу «яблоко»; абдоминальное ожирение), с преимущественной локализацией жира в области верхней половины тела (живот, грудь, плечи, спина).

Второй тип ожирения является более патогенным в плане риска возникновения сердечно-сосудистых заболеваний и сахарного диабета. Это связано с ожирением внутренних органов, в том числе печени (висцеральное ожирение, неалкогольная жировая болезнь печени), снижением сатурации крови кислородом из-за перехода дыхания на грудной, поверхностный тип и эндокринной активностью висцеральной жировой ткани с патологическим изменением выработки адипокинов (лептин, грелин, адипонектин). Выявлена чёткая корреляция между увеличением абдоминальной жировой ткани и индекса массы тела с риском сопутствующих заболеваний. Считается, что риски начинают нарастать при увеличении окружности талии (ОТ) >80 см у женщин и 94 см у мужчин, а при ОТ >88 см и 102 см соответственно риск возрастает значительно.
Ещё один важный компонент метаболического синдрома — артериальная гипертензия, которая может носить вторичный характер. Нормальным считается систолическое артериальное давление (САД) 120-129 мм рт.ст и диастолическое артериальное давление (ДАД) 80-84 мм рт.ст. САД
- 1 ст. – САД 140-159, ДАД 90-99;
- 2 ст. - САД 160-179, ДАД 100-109;
- 3 ст. - САД ≥180, ДАД ≥110.
Повышение артериального давления характеризуется повышением риска сердечно-сосудистых событий.
Для метаболического синдрома характерны также изменения липидного обмена, которые классифицированы в таблице ниже (в ммоль/л).
Осложнения метаболического синдрома
Так как метаболический синдром является сочетанием факторов риска сердечно-сосудистых и обменных заболеваний, именно эти патологии и являются его осложнениями. Речь идёт, в первую очередь, о сахарном диабете, ишемической болезни сердца и их осложнениях: диабетическая ангио-, нейро- и нефропатия, острая коронарная недостаточность, сердечная недостаточность, нарушение сердечного ритма и проводимости, внезапная сердечная смерть, цереброваскулярные заболевания и болезни периферических артерий. [17] Прогрессирование артериальной гипертензии также приводит к поражению органов-мишеней и ассоциированным клиническим состояниям.
Диагностика метаболического синдрома
Для диагностики метаболического синдрома необходимо выявить у пациента основной признак — абдоминальное ожирение по измерению ОТ (>80 см у женщин и >94 см у мужчин) и хотя бы два дополнительных критерия, которые включают в себя:
- артериальную гипертензию (артериальное давление ≥140/90 мм рт.ст.);
- липидные показатели (ммоль/л) — повышение концентрации в крови триглицеридов ≥1,7; снижение ХС ЛПВП 3,0;
- углеводные показатели (ммоль/л) — гипергликемия натощак ≥6,1 и НТГ 7,8 – 11,1. [8]
В клинических условиях нужно дифференцировать метаболический синдром от механического сочетания факторов риска, например артериальной гипертензии, избыточной массы тела без признаков абдоминального ожирения и повышения уровня ОХ крови, что встречается довольно часто (до 30%). В сомнительных случаях рекомендовано дополнительное определение инсулинорезистентности по следующим методикам:
- оценка базальной гиперинсулинемии в крови натощак (гиперинсулинемия — >18 мкед/мл);
- показатель HOMA-IR — произведение значения инсулина натощак (мкед/мл) на величину глюкозы (ммоль/л), разделить на 22,5 (значение большее, чем 2,27, считается инсулинорезистентностью);
- индекс Caro — соотношение тощаковой глюкозы (в ммоль/л) к инсулину (в мкед/мл) (инсулинорезистентность – значение < 0,33). [12]
Лечение метаболического синдрома
Лечение метаболического синдрома следует разделить на немедикаментозное и медикаментозное.
Немедикаментозное лечение синдрома Reaven — это ведение здорового образа жизни, отказ от курения и злоупотребления алкоголем, оптимальная двигательная активность [14] , рациональное питание, а также разумное использование природных и преформированных физических лечебных факторов (массаж, подводный душ-массаж, гипокситерапия и гиперкапния, водолечение, талассотерапия, бальнео- и термотерапия, внутренний прём минеральных вод, общие магнитотерапевтические воздействия) [15] , психотерапевтических методик и обучающих программ. [13]
Медикаментозное лечение метаболического синдрома, в зависимости от наличия тех или иных его компонентов, может включать гиполипидемические, антигипертензивные препараты, медикаменты для снижения инсулинорезистентности, постпрандиальной гипергликемии и веса.
Основными препаратами, которые используют при лечении артериальной гипертензии у больных синдромом Reaven и сахарным диабетом, являются ингибиторы ангиотензинпревращающего фермента, сартаны и агонисты имидазолиновых рецепторов. Однако для достижения целевого уровня артериального давления часто необходимо сочетание различных классов медикаментов, таких как пролонгированных блокаторов медленных кальциевых каналов, высокоселективных бета-адреноблокаторов и тиазидоподобных диуретиков (индапамид) в сочетании с медикаментами первой линии. [10]
Для коррекции нарушений липидного обмена при метаболическом синдроме первоначально используются статины, возможно их сочетание с эзетролом и фибратами. Основной механизм действия статинов — снижение внутриклеточного синтеза ОХ за счёт обратимого блокирования фермента 3-гидрокси-3-метилглютарил-кофермент А редуктазы. Оно ведёт к увеличению количества рецепторов к ХС-ЛПНП на поверхности гепатоцита и снижению концентрации ХС-ЛПНП в крови. Помимо этого, статины имеют плейотропные эффекты, такие как антитромбогенный, противовоспалительный, улучшение функции эндотелия, что приводит к стабилизации атеросклеротической бляшки. Современные статины способны вместе со снижением ХС-ЛПНП до 55% уменьшать триглицериды до 30% и повышать ХС-ЛПВП до 12%. В то же время, ключевое достоинство статинотерапии — снижение сердечно-сосудистых осложнений и общей смертности [1] . Эффективней всего использовать аторвастатин (10-80 мг/сут) или розувастатин (5-40 мг/сут). [11]
При неэффективности монотерапии статинами целесообразно присоединение эзетрола в дозе 10 мг/сут, который препятствует всасыванию ОХ в кишечнике и может усиливать снижение ХС-ЛПНП на 15-20%.
Фибраты — ещё один класс липидснижающих препаратов. Они расщепляют богатые триглицеридами жировые частицы, снижают синтез свободных жирных кислот и повышают ХС-ЛПВП путём увеличения распада ЛНП. Это приводит к значительному уменьшению триглицеридов (до 50%), ХС-ЛПНП (до 20%) и увеличению ХС-ЛПВП (до 30%). Фибраты также имеют плейотропные эффекты: снижают концентрацию мочевой кислоты, фибриногена и улучшают инсулиночувствительность, однако их положительное влияние на прогноз пациентов не доказано. Наиболее эффективный и безопасный препарат этой группы — фенофибрат 145 мг/сут.
Для снижения инсулинорезистентности препаратом выбора является метформин, который обладает доказанным положительным эффектом на тканевую инсулинорезистентность через усиление поглощения глюкозы тканями-мишенями. Метформин уменьшает скорость всасывания углеводов в тонкой кишке, оказывает периферическое анорексигенное действие, уменьшает продукцию глюкозы печенью, улучшает транспорт глюкозы внутри клеток. Положительное воздействие метформина (1500-3000 мг/сутки) на конечные точки обусловлено снижением инсулинорезистентности, системными метаболическими эффектами (снижение веса, липидных нарушений, факторов свёртываемости крови и т.д.). [9]
Для снижения постпрандиальной гипергликемии используют акарбозу, которая обратимо блокирует глюкоамилазы, сахарозы и мальтазы в верхнем отделе тонкой кишки. В итоге непереваренные углеводы достигают нижние отделы кишечника, и абсорбция углеводов пролонгируется. Вместе с тем, у акарбозы выявлены дополнительные эффекты. В исследовании STOP-NIDDM (2002 год) у больных метаболическим синдромом, принимающих акарбозу дозировкой 300 мг/сут, продемонстрировано снижение развития сахарного диабета на 36%, новых случаев артериальной гипертензии на 34% и суммарного показателя сердечно-сосудистых событий на 46% [6] .
При наличии у пациента с синдромом Reaven сахарного диабета второго типа могут применяться современные классы сахароснижающих препаратов, такие как аналог глюкагоноподобного пептида-1, ингибитор дипептидилпептидазы-4 и ингибитор натрийзависимого переносчика глюкозы второго типа. Представитель последнего класса эмпаглифлозин (Джардинс) в исследовании EMPA-REG OUTCOME (2016 год) снизил сердечно-сосудистую смертность у больных сахарным диабетом второго типа на 36%.
Медикаментозная коррекция морбидного ожирения показана, если немедикаментозное лечение не приводит к снижению массы тела более чем на 5% от исходного. Препараты для лечения ожирения делятся на аноретики центрального действия (сибутрамин), и средства, воздействующие на желудочно-кишечный тракт, например орлистат (Ксеникал).
Препарат для снижения аппетита сибутрамин в меньшей степени воздействует на дофаминовые и холинергические процессы, но уменьшает потребление жиров и углеводов, что приводит к похудению и улучшает жировой и углеводный метаболизм. Артериальное давление и частота сердечных сокращений при этом повышается только на 5%.
Орлистат является ингибитором желудочной и панкреатической липаз, вследствие чего треть пищевых триглицеридов не всасывается и снижается их концентрация в крови, что приводит к уменьшению калоража пищи и веса. Кроме того, снижается артериальное давление, уровень глюкозы и инсулинорезистентности.
В медицинской практике лечение метаболического синдрома зависит от наличия и выраженности его компонентов. В таблице ниже показана тактика подбора терапии при вариантах синдрома Reaven, которые встречаются наиболее часто.
Читайте также:

