Коллост при лечения трофических язв
Обновлено: 25.04.2024
Кафедра патофизиологии ФППО врачей Московской медицинской академии им. И.М. Сеченова
ГБОУ ВПО Российский национальный исследовательский медицинский университет им. Н.И. Пирогова, кафедра госпитальной хирургии №1
ФГБОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России, Москва, Россия
ФГБОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России, Москва, Россия
Применение нативного коллагена в клинической практике для лечения хронических ран
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2017;(9): 78‑84
Кафедра патофизиологии ФППО врачей Московской медицинской академии им. И.М. Сеченова
Кафедра патофизиологии ФППО врачей Московской медицинской академии им. И.М. Сеченова
ГБОУ ВПО Российский национальный исследовательский медицинский университет им. Н.И. Пирогова, кафедра госпитальной хирургии №1
ФГБОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России, Москва, Россия
ФГБОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России, Москва, Россия
Уже несколько десятилетий не остывает интерес врачей к применению препаратов и медицинских изделий, содержащих коллаген, как для коррекции возрастных изменений кожи, так и для стимуляции заживления хронических ран. Коллаген является самым распространенным белком в организме млекопитающих, основным строительным материалом внеклеточного матрикса. Составляя 25—35% от всей белковой массы, он обеспечивает эластичность и прочность кожи, сухожилий, хрящей, костей, сосудов и других тканей [1]. Не менее важной является функция образования стромы паренхиматозных органов — «органической сети», в которой клетки располагаются в правильные геометрические ряды, что помогает им нормально функционировать и выполнять те физиологические обязанности, благодаря которым поддерживается наша жизнь. Кроме того, коллаген выполняет важную восстановительную функцию, выступая в качестве провизорного матрикса при осуществлении процессов репаративной регенерации соединительных тканей.
Массовая доля коллагена в тканях, в зависимости от выполняемой ими функции, варьирует от 10 до 80%, при этом наибольшее количество его в коже, которая у взрослого человека в основном содержит коллаген I типа (75—85%), гораздо меньше приходится на коллаген III типа (5—10%) и до 10% на коллагены V, VI, VII, XII, XIV и других малоизученных типов [2—4].
Как и любой белок, тем более испытывающий постоянные механические нагрузки, коллаген постоянно синтезируется и катаболизируется. В абсолютном большинстве случаев появление ран служит сигналом к дополнительной выработке биологически активных веществ для скорейшего закрытия поврежденных тканей. Для синтеза любого вещества, а тем более столь сложно устроенного, как белок коллаген, требуется большое количество энергии, которая в виде молекул аденозинтрифосфорной кислоты (АТФ) вырабатывается в митохондриях. Однако для эффективного синтеза АТФ в цикле трикарбоновых кислот требуется достаточное количество кислорода. Поэтому любое нарушение доставки кислорода к клеткам в результате поражения артериальной стенки (атеросклероз, сахарный диабет (СД)), нестабильное артериальное давление (нарушения ритма сердца, снижение сердечного выброса), газообмена (ХОБЛ, бронхиальная астма), гиперкапнии (варикозная болезнь, посттромбофлебитический синдром) неминуемо переключают гликолиз с аэробного на анаэробный, что ведет к снижению синтеза АТФ в несколько раз, и, соответственно, коллагена. Это и есть основной патофизиологический механизм образования трофических язв и хронических ран [5, 6]. Именно поэтому наряду с основными методами лечения к важным вспомогательным способам лечения по праву можно отнести применение коллагена у пациентов с различными хроническими ранами, затраты на лечение которых неуклонно растут и, согласно подсчетам, только в США они превышают 50 млрд долларов в год [7].
По степени сохранности морфологической структуры изделия коллагена дифференцируются на нативные и фракционные. При изготовлении препаратов/материалов нативного коллагена полностью сохраняется естественная структура укладки пучков его волокон, при этом удаляются клеточные элементы, а также участки кровеносных сосудов и волосяные фолликулы. Нативный коллаген является своеобразным «шаблоном» для миграции и дифференцировки клеток и, как следствие, для формирования собственной ткани, что является его исключительным преимуществом перед выпускаемыми в настоящее время изделиями на основе выделенного или фракционного (расщепленного) коллагена [8, 9]. Для производства современных раневых покрытий используют нативный коллаген в виде децеллюляризованного волокнистого матрикса соединительных тканей или же химически выделенный и очищенный различными способами белок.
Применение нативного коллагена для лечения пролежней (декубитальных язв) и трофических язв при хронической венозной недостаточности
Ряд исследователей применяли коллост для лечения не только пролежней, но и других хронических ран.
В.Н. Оболенский и Д.А. Ермолова [18] до 55 сут наблюдали 38 пациентов с хроническими ранами различной этиологии (пролежни, СДС, хронические венозные язвы), 24 из них дополнительно назначали разработанную авторами методику с использованием богатой тромбоцитами плазмы (БоТП) местно, 5 — коллост, 9 — комбинацию БоТП и коллост. Результаты исследования показали, что в период до 55 сут полное заживление раны в группе БоТП было у 66,7% (безуспешность — у 16,7%), коллост — 100% (однако на 10 сут дольше, чем в группе БоТП), в группе комбинированной терапии лечение оказалось успешным у 77,8%.
Таким образом, методика применения нативного коллагена при хронических ранах показала себя перспективным направлением.
Учитывая нарастающее количество больных с тяжелым течением СД, низкую эффективность у них стандартных методов лечения, многими хирургами и эндокринологами были сделаны попытки оценить эффективность коллоста у пациентов с СДС.
Применение нативного коллагена для лечения синдрома диабетической стопы
Впервые Б.С. Брискин и соавт. [8] доложили о перспективности применения биопластического материала коллост в комплексном лечении осложненных форм СДС в 2008 г. Из 15 пролеченных коллостом удалось добиться полного заживления ран в 12 (80%) случаях, в том числе у 2 больных с остеомиелитом фаланг пальцев. Биоматериал применяли в фазе репарации при обсемененности ран 10 6 —10 8 КОЕ.
В 2011 г. К.А. Корейба и соавт. [21] доложили на конференции о своих результатах внедрения в клиническую практику биопластического материала 36 больным с СДС. После кюретажа раны производилась аппликация коллостом (мембрана, порошок, жгут, шарики). Через 14—20 дней авторы выявляли гранулирующие раны без признаков воспаления или отторжения пластического материала. На основании этого были сделаны предварительные выводы о том, что применение коллоста позволяет ускорить процесс заживления ран, не прибегая к аутодермопластике, сократив при этом материальные расходы на лечение.
Через 3 года казанские исследователи К.А. Корейба и А.Р. Минабутдинов провели анализ результатов лечения 70 больных с СДС в возрасте 56,4±15,6 года (Wagner I—III, площадь дефекта 38,5±26,3 см 2 ) [22]. Было указано на такие преимущества применения коллоста, как возможность стимулирования регенерации ткани без дополнительной аутодермопластики. Препарат успешно применялся как в условиях стационара, так и амбулаторно, сократив при этом сроки лечения.
В дальнейшем количество пациентов увеличивалось и в 2016 г. был опубликован анализ результатов лечения 1195 пациентов с нейропатической формой СДС (в том числе Wagner II — 526, Wagner III — 116), в котором была показана целесообразность внедрения в клиническую практику разработанной и запатентованной методики лечения СДС [23]. Методика включает три основных этапа: 1) комплексная консервативная терапия (производные тиоктовой кислоты, витамины В1 и В6, габапентин, сулодексид; курс лечения до 2-х месяцев); 2) с 3—5-х суток от начала лечения присоединяется ультразвуковая гидрохирургическая обработка и, при необходимости, механическая некрэктомия с применением имплантации биоматериала коллост; 3) медикаментозная терапия с использованием интерактивных повязок, иммобилизации нижней конечности и, в дальнейшем, ортопедической обуви. При использовании вышеуказанной методики начало островковой эпителизации раневого дефекта было на 10,3±2,8 сутки. Авторы подчеркнули, что внедрение методики позволило уменьшить количество органоуносящих операций и осложнений на 15—33%, сроки пребывания пациентов в стационаре сократились на 20%, количество повторных обращений в специализированные хирургические стационары — на 13,4—18,5%.
В пилотном исследовании А.Г. Сонис и соавт. (2015) проанализированы результаты применения геля и мембраны коллост при лечении трофических язв у 27 пациентов с нейропатической формой СДС (Wagner II—III) [25]. К 15-м суткам закрытие дефекта отмечалось у 55,5% пациентов с язвами до 2 см в диаметре. В 29,6% случаев при дефектах размером 3—5 см понадобилось повторное наложение мембраны и эпителизация отмечалась к 30-м суткам. В 14,8% случаев наблюдалась лишь слабая краевая эпителизация язвы или отсутствие положительного эффекта лечения. Исходя из полученных результатов, авторы сделали вывод о том, что коллост значительно улучшает результаты лечения язвенных поражений стоп у пациентов с СДС.
К сожалению, эти исследования не имели группу сравнения, однако тенденция к ускорению процессов заживления была отмечена всеми упомянутыми авторами.
Впервые сравнительная оценка эффективности применения стандартной комбинированной терапии и дополнительного использования биоматериала коллост при лечении СДС была представлена на I Международном конгрессе «Раны и раневые инфекции» в Москве в 2012 г. [26]. М.Д. Дибиров и соавт. доложили результаты исследования 32 пациентов с СД 2-го типа и СДС II—III степени по классификации Wagner. В исследование включались 15 пациентов основной группы, которым на 6—7-е сутки после хирургической обработки (со 2-й фазы заживления при бактериальной обсемененности ран не выше 10 7 КОЕ) раневой дефект закрывался материалом коллост в различных модификациях, и 17 пациентов контрольной группы, в которой использовались водорастворимые мази. Через 8 дней после назначения коллоста уровень обсемененности составил в среднем 10 2 КОЕ/г, в контрольной группе — 10 5 КОЕ/г. Скорость очищения ран от некроза в основной группе в сравнении с контрольной была выше и составляла 0,14±0,02 см 2 /сут и 0,07±0,03 см 2 /сут соответственно (р<0,05).
Последующие исследования данного коллектива авторов вылились в цикл работ [27, 28], посвященных оценке эффективности последовательного местного применения ультразвуковой кавитации (УЗК) и коллоста у 133 пациентов с нейропатической и нейроишемической формами СДС (Wagner II—IV), 65 пациентов основной и 68 контрольной группы. Частота локальных осложнений была ниже в группе УЗК и коллоста. Вторичные некрозы были выявлены в основной группе у 5,41% пациентов, в контрольной у 38%, гнойные затеки у 8,11 и 48% соответственно. Авторы показали, что частота повторных операций в основной группе была в 13,8 раза меньше, чем в основной. В основной группе обсемененность на 4-е сутки лечения достигала 10 5 КОЕ л/г (такой же результат в группе контроля был лишь на 14-е сутки), на 7-е сутки роста микрофлоры выявлено не было. В группе коллоста скорость появления грануляций была в 2 раза выше, причем молодая грануляционная ткань образовывалась уже на 7-е сутки лечения, а продолжительность курса антибактериальной терапии сократилась в 2 раза. Это сопровождалось уменьшением продолжительности госпитализации в 1,5—2 раза. По мнению авторов, данная методика способствует раннему созреванию и стратификации грануляционной ткани, поскольку применение коллоста привело к улучшению цитологической картины: снижению количества нейтрофилов на 3—4-е сутки лечения, увеличению площади молодой грануляционной ткани с множеством сосудов и активированных фибробластов уже на 7-е сутки лечения на фоне смены лейкоцитарной инфильтрации грануляционной ткани лимфогистиоцитарной. Следовательно, коллост способствует нормализации развития второй фазы раневого процесса и скорейшему заживлению.
Д.В. Селиверстов и соавт. [30] провели обследование и лечение 57 пациентов с гнойно-некротическими формами СДС, у 26 пациентов для временного закрытия раневых дефектов перед наложением вторичных швов или аутодермопластикой использовали фиксированные швы к ране повязки с коллостом, пропитанные жидкостью с подобранным по результатам бактериологического исследования антибиотиком (группу сравнения составил 31 человек). Показано, что в основной группе быстрее активизировались процессы образования грануляционной ткани и краевая эпителизация. Применение коллоста в 1,8 раза сократило сроки подготовки раны к наложению вторичных швов или аутодермопластике. Длительность подготовки раны к дерматопластике составила 32,0±4,6 сут в основной группе и 56,8±8,7 сут в группе сравнения.
По результатам многоцентрового рандомизированного исследования [32] в 2017 г. была произведена оценка экономической эффективности применения коллоста в лечении пациентов с СДС [33]. Проведена оценка прямых медицинских затрат, связанных с применением стандартной терапии и стандартной терапии в сочетании с коллостом. Результаты расчетов показали, что стандартная тактика лечения СДС в комплексе с применением биоматериала коллост является экономически эффективным подходом, особенно при лечении язвенных дефектов II степени (по Wagner) площадью более 10 см 2 у пациентов с СДС. Наименьшим коэффициентом «затраты/эффективность» обладает методика, включающая применение коллоста. Расходы, рассчитываемые на гипотетическую когорту пациентов численностью 100 тыс. человек, с учетом нормативов финансовых затрат на 1 законченный случай лечения пациента с СДС по тарифам ОМС в Москве на 2017 г. (42,5 тыс. руб.) и стоимости курса лечения биоматериалом (14,0 тыс. руб.), на лекарственные препараты и перевязочные средства при использовании только стандартной тактики ведения пациентов составили 1,32 млн руб.; в случае использования коллоста — 2,72 млн руб. При этом затраты на одного эффективно пролеченного пациента (полная эпителизация) составили 166,2 тыс. руб. в группе стандартной терапии и 123,8 тыс. руб. в группе коллоста. Инкрементный анализ показал, что сумма дополнительных затрат, необходимая для излечения одного пациента с язвенным дефектом II ст. по Wagner и площадью более 10 см 2 , составляет 99,6 тыс. руб.
Следовательно, применение коллоста при СДС целесообразно не только с точки зрения клинической эффективности, но и с точки зрения экономии финансовых средств.
В таблице приведены основные исследования, посвященные сравнительной оценке эффективности биоматериала коллост для лечения хронических ран различного генеза.

Основные исследования, посвященные сравнительной оценке клинической эффективности биоматериала коллост для лечения хронических ран Примечание. ОГ — основная группа (коллост); ГС — группа сравнения; СДС — синдром диабетической стопы, ХВН — язвы при хронической венозной недостаточности.
Заключение
Увеличение числа больных с хроническими ранами, особенно с осложненным течением СД 2-го типа и неудовлетворительной эффективностью проводимой комбинированной терапии поставила перед практикующими хирургами задачу поиска более совершенных и эффективных методов лечения этих пациентов. Длительная и постоянная терапия, частый переход к ампутациям формируют «армию инвалидов», выключенных из продуктивной социальной жизни и накладывают дополнительные расходы на бюджеты всех уровней.
Анализ литературных источников в свободном доступе, посвященных результатам применения нативного коллагена (биоматериала коллост) у пациентов с хроническими ранами различной этиологии показал наибольшую эффективность этой методики не только в сравнении со стандартной терапией, но и с методиками лечения, включающими применение препарата эпидермального фактора роста, а также богатой тромбоцитами плазмы. Оценка клинико-экономической эффективности также подчеркивает преимущества данной методики.
Однако необходимо отметить, что не все опубликованные результаты исследований отвечают современным требованиям и принципам доказательной медицины. Для улучшения уже достигнутых результатов лечения было бы целесообразно провести развернутое исследование со сроками динамического наблюдения за больными не менее одного года. Это могло бы позволить уточнить вопросы тактики своевременного перехода на хирургические органосохраняющие методы лечения или склониться к ампутациям. Любая, основанная на объективных показателях тактика ведения этих больных, несомненно, даст ощутимый медико-экономический эффект и позволит оптимизировать финансовое обеспечение пациентов с хроническими ранами.
КОЛЛОСТ ® для восстановления соединительных тканей при серьезных повреждениях. Использование коллагенового материала способствует приживлению донорских участков кожи и ускорению заживления ран.
- Сокращает сроки заживления в 2 раза по сравнению со стандартными методиками
- Образует сходные с окружающими ткани в области раневого дефекта
- Уменьшает количество перевязок
до 1-ого раза в 5-7 дней


Применение в хирургии и травматологии
Диабетическая стопа
Осложнение сахарного диабета. Проявляется язвенными, гнойными и некротическими процессами, повреждениями суставов и костей стопы. Возникает в связи с нарушением макроструктуры стопы и микроциркуляции крови.
Трофическая язва
Одна из форм некроза. Часто является осложнением артериальных заболеваний, варикоза и сахарного диабета. Некротизированный участок кожи чувствителен не только к любым микротравмам, но и к инфекциям.
Пролежень
Некроз тканей на определенном участке тела. Возникает из-за нарушения кровообращения в сочетании с длительным давлением. Ему в основном подвержены ослабленные лежачие больные.
Преимущества коллостотерапии

Заживление ран в 2 раза быстрее.

Генерация тканей сходных с окружающими.

Снижение числа перевязок до 1-й в 5-7 дней.

Сочетается с антибиотиками и антисептиками.

Простота использования.
КОЛЛОСТ ® как регенератор
Травмы различной степени зачастую приводят к нарушению целостности и сбою в функционировании соединительных тканей. Данные ткани составляют от 60 до 90% массы внутренних органов и выполняют множество важных функций, включая защитную и опорную. КОЛЛОСТ ® успешно применяют в травматологии и хирургии для восстановления любых повреждений соединительной ткани:
- В качестве стерильного биопластического коллагенового импланта с полностью сохраненной природной структурой
- В послеоперационной остеопластике
- Для лечения посттравматических рубцов
- Для заживления хронических и острых рваных ран
- При травматической ампутации
- Для заживления рубцов, западающих ниже уровня кожи (атрофических)
- Для приживления донорской кожи в ожоговой медицине
Отзывы
Применение биопластического материала на основе коллагена I типа в комплексном лечении синдрома диабетической стопы позволяет стимулировать регенерацию ткани, сократить длительность лечения и пребывания больного в стационаре. Методика доступна как для стационарных, так и амбулаторных условий.
Руководитель центра «Диабетическая стопа» г. Казани, доцент кафедры общей хирургии Казанского Государственного Медицинского Университета, к.м.н.
Мы имеем многолетний опыт работы с биопластическим коллагеновым материалом Коллост, в особенности в лечении трофических язв нижних конечностей. Применение материала нативного коллагена позволяет добиться быстрого заживления ран с формированием полноценных покровных тканей.
Доцент кафедры факультетской хирургии Санкт-Петербургского Государственного Медицинского Университета им. И.П. Павлова, к.м.н.
Мы начали работу с биоматериалом Коллост гель для лечения язвенной болезни желудка и двенадцатиперстной кишки осложеннной кровотечением. По анализу результатов целого ряда клинических случаев необходимо отметить, что 7% гель достаточно хорошо проходит через эндоскопическую систему введения и способствует остановке кровотечения, а также стимулирует регенерацию в области язвенного дефекта.
Профессор кафедры госпитальной хирургии Московского Государственного Медико-стоматологического Университета, д.м.н.
Необходимо отметить очень важную составляющую: биопластический материал Коллост — отечественного производства и не имеет прямых аналогов в России и странах Европы. Кроме того, учитывая современную политическую и экономическую ситуацию, данный биоматериал заслуживает пристального внимания для широкого применения в хирургии.
Федеральный эксперт по хирургии МЗ РФ, зав. отделением гнойной хирургии Рязанской Областной Клинической Больницы, к.м.н.
Стерильный гель с содержанием коллагена 7% в инъекционных шприцах. Объем материала в шприце для инъекций 2.0 см3, в шприце для аллергической пробы 0,1 мл. Предназначен для однократного применения.
Фармакологическое действие
Коллаген, являясь основным фибриллярным белком соединительной ткани, обеспечивает ее структурную основу. Молекулы коллагена выполняют роль физиологической матрицы, обеспечивающей нормальные репарационные процессы.
Действие КОЛЛОСТ® в мягких тканях
КОЛЛОСТ® обеспечивает область коррекции основными биологическими ресурсами, которые требуются для заживления ран. Коллагеновый имплантат связывается с раной, фибробласты мигрируют к нему из окружающих тканей, и вторгаются в имплантат. Создается переходный матрикс, который стимулирует иммунную систему организма и активацию гранулоцитов, макрофагов и фибробластов, улучшает перенос факторов роста, высвобождающихся из клеток, усиливает миграцию фибробластов и пролиферацию эпителиальных клеток. При введении КОЛЛОСТ® продуцируются новые коллагеновые волокна, заполняющие полость в области имплантации, а сам имплантат постепенно рассасываясь, замещается аутотканью.
Действие КОЛЛОСТ® в костной ткани
КОЛЛОСТ® ускоряет передвижение остеобластов по коллагеновой матрице, при этом увеличивается толщина остеоидного слоя.
Срок биодеградации КОЛЛОСТ® геля зависит от ряда факторов, таких, как область имплантации, возраст пациента, концентрация геля, и в среднем составляет от 90 до 180 дней.
Показание к применению
Стоматология
Пародонтология:
- пародонтиты (малоинвазивные методы лечения и реконструктивные операции);
- рецессия десны.
Хирургия:
- удаление зуба (осложненное/неосложненное);
- резекция верхушки корня (РВК);
- цистэктомия;
- реплантация зуба;
- ликвидация фуркационного дефекта;
- травматические повреждения.
Имплантология:
- имплантация при дефектах костной ткани, при трещинах;
- синуслифтинг.
Челюстно-лицевая хирургия:
- восстановление врожденных и приобретенных дефектов костной и мягких тканей.
Хирургия
- хронические раны (пролежни, плохо заживающие диабетические и венозные язвы, трофические язвы);
- острые раны (рваные, колотые, резаные, хирургические);
- хирургия донорских участков;
- врожденные, приобретенные (в т.ч. посттравматические) дефекты мягких тканей;
- дефекты кости и костная пластика;
- стрессовое недержание мочи.
Противопоказания
- Положительная тест-проба;
- Тяжелые хронические заболевания в стадии обострения;
- Аутоиммунные заболевания;
- Повышенная чувствительность к компонентам препарата;
- Склонность к формированию гипертрофических и келоидных рубцов;
- Нарушения свертываемости крови;
- Дерматозы в стадии обострения.
Применение КОЛЛОСТ® в период беременности и лактации не изучено.
Взаимодействие с лекарственными препаратами
- Не рекомендуется использовать КОЛЛОСТ® гель одновременно с приемом антикоагулянтов, антиагрегантов, изотретиноина (Роаккутана), неспецифических противовоспалительных средств для наружного применения, ферментными препаратами.
- Допускается введение КОЛЛОСТ® геля с антибактериальными и антисептическими препаратами.
Руководство по применению
Этап 1. За 14 дней до введения КОЛЛОСТ® гель необходимо провести внутрикожную аллергическую тест-пробу. Для этого инъецировать внутрикожно в область предплечья 0,1 мл КОЛЛОСТ® гель с использованием иглы 27 1/2 G. В случае обнаружения аллергической реакции тест-пробу считать положительной, и в таком случае КОЛЛОСТ® не применять.
Этап 2. Перед инъекционным введением разогреть КОЛЛОСТ® гель до температуры 36-40 °С на водяной бане или в термостате. Не допускать превышения указанного интервала температур во избежание нарушения структуры коллагена. Допускается многократное нагревание КОЛЛОСТ® геля в процессе проведения процедуры одному пациенту.
Этап 3. КОЛЛОСТ® гель может применяться как самостоятельно, так и в комбинации с другими формами выпуска изделия медицинского назначения КОЛЛОСТ®.
* Не допускается самостоятельное применение изделия медицинского назначения КОЛЛОСТ®. Применение изделия медицинского назначения КОЛЛОСТ® возможно только квалифицированным медицинским персоналом при соблюдении правил асептики и антисептики.
Особенности применения
Хирургия
- Очистить рану от фибрина и некротизированных тканей, перевести раневой процесс из хронический стадии в острую. В некоторых случаях эта манипуляция не требует местной анестезии, поскольку выполняется на тканях с нарушенной иннервацией.
- В края раны внутрикожно по всей окружности ввести КОЛЛОСТ® гель в количестве 1,5-3,0 мл в зависимости от размеров раны.
- Далее возможно использовать один из нижеуказанных вариантов:
- В рану уложить вырезанную по размеру дефекта КОЛЛОСТ® мембрану, полностью заполняя полость. При глубоких дефектах использовать несколько мембран, уложенных одна на другую. Обеспечить полное прилегание КОЛЛОСТ® мембраны ко всем стенкам и дну дефекта. При необходимости наложить узловые провизорные швы, которые следует снять через 10-14 дней. При наружном применении на область раны уложить стерильную марлевую салфетку, смоченную раствором натрия хлорида изотоническим 0,9%, поскольку наилучший эффект действия КОЛЛОСТ® достигается во влажной среде. На салфетку уложить бумагу для компрессов и сверху фиксировать пластырем или давящей повязкой.
- Полость раны заполнить КОЛЛОСТ® гелем (принцип «биологической повязки»).
Стоматология
- При малоинвазивном методе лечения хронического пародонтита в пародонтальный карман вводится биокомпозиция КОЛЛОСТ® геля с антибактериальными препаратами через шприц с затупленной иглой. При этом не требуется предварительная подготовка геля (разогревание). Процедура повторяется через 7 дней и 6 месяцев.
- В хирургической стоматологической практике в дефект помещается изделие медицинского назначения КОЛЛОСТ® (выбор формы зависит от дефекта и клинической картины).
Побочные реакции и осложнения
Рекомендации для пациентов после вмешательства
После введения пациентам изделия медицинского назначения КОЛЛОСТ® рекомендуется избегать избыточной инсоляции, посещения бани, сауны непосредственно сразу после вмешательства. Проведение косметических или физиотерапевтических процедур в области вмешательства может вызвать ускорение метаболизма биоматериала или спровоцировать развитие воспалительной реакции.
Условия хранения
Хранить в сухом, защищенном от света месте при температуре от 5 до 25 °С. Не замораживать и не подвергать воздействию высоких температур. При повреждении герметичности первичной упаковки материал не использовать.
Срок годности
3 года со дня выпуска. Не использовать по окончании срока годности, указанного на упаковке. КОЛЛОСТ® с истекшим сроком годности и его остатки после использования помещают в емкость для нетоксичных отходов и направляют на утилизацию.
Трофическая язва — одна из форм некроза, дефект кожи или слизистой оболочки с малой тенденцией к заживлению. Язвы образуются после отторжения некротизированной ткани.
Провоцирующие факторы
- Травматические воздействия: ожоги, отморожения, обширные раны и др
- Хронические расстройства лимфо- и кровообращения
- Болезни нервной системы
- Нарушение обмена веществ
- Системные болезни: крови, кроветворных органов
- Инфекционные болезни
- Опухоли
- Артериальные заболевания, варикоз
- Сахарный диабет
![]()
Реальные результаты
На фото настоящие результаты, без обработки. Передвигайте бегунок для просмотра.
![]()
![]()
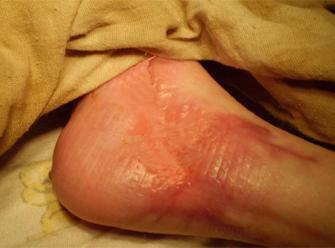
Пациент: женщина, 38 лет. Диагноз: трофическая язва на передней поверхности средней трети левой голени, развившаяся после травмы, полученной 8 месяцев назад. Сопутствующие заболевания: ХВН (CEAP C6), аденома гипофиза. Лечение до коллостотерапии: неоднократно лечилась стационарно, проходила амбулаторное лечение. Ссылка: Корейба К.А. "Биопластические материалы в лечении и обработке ран». Международный конгресс "Хирургическая обработка ран и гнойно-некротических очагов у детей и взрослых». Москва, 2014.
![]()
![]()
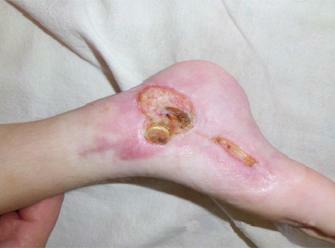
Пациент Женщина, 54 года Диагноз Полуциркулярная трофическая язва нижней трети правой голени в течение 2 лет. Лечилась стационарно. Было произведено 4 операции: аутодермопластика свободным расщепленным кожным лоскутом. Сопутствующие заболевания: ХВН (CEAP C6), сахарный диабет 2 типа.
![]()
![]()
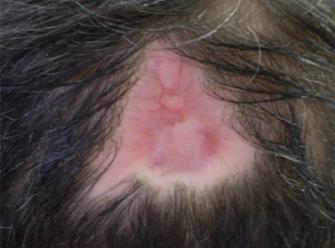
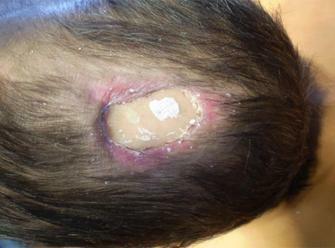
Пациент: мужчина, 45 лет. Диагноз: скальпированная рана волосистой части головы (3,5 года назад). Сопутствующие заболевания: сахарный диабет 2 типа, инсулинпотребный, субкомпенсированный, средней степени тяжести. Лечение до коллостотерапии: неоднократные попытки аутодермопластики успеха не имели.
![]()
![]()
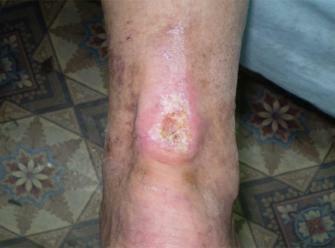
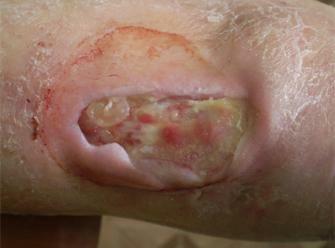
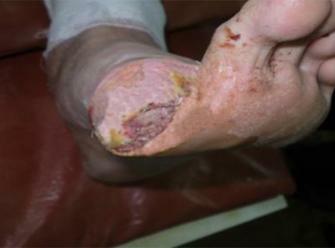
Пациент: мужчина, 62 года. Диагноз: длительно незаживающая рана правой голени. Сопутствующие заболевания: сахарный диабет ІІ типа, тяжелой степени тяжести, субкомпенсированный; ХВН ІІІ (CEAP C6), ПТФБ.
![]()
![]()
Пациент: девочка, 3 года 11 месяцев. Диагноз: глубокая некротическая незаживающая рана внутренней поверхности правого голеностопного сустава и правой стопы.
![]()
![]()
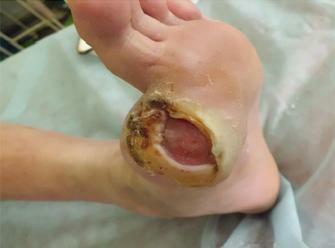
Пациент: мужчина, 46 лет. Диагноз: синдром диабетической стопы, трофические длительно незаживающие язвы левой стопы и левой голени. Диабетическая ангиопатия нижних конечностей. Ссылка: Селиверстов Д.В. Применение биоматериала Коллост в комплексном хирургическом лечении пролежней IV степени. РМЖ (хирургия), №6-2015
Преимущества процедуры
![]()
Ускоряет заживление дефектов до 2 раз.
![]()
Сокращает общую продолжительность терапии.
![]()
Минимизирует вероятность побочных эффектов.
![]()
Снижает уровень высоких ампутаций.
![]()
Нет необходимости в создании донорской раневой поверхности.
![]()
Стимулирует регенерацию эпителия.
Методика лечения
Методика лечения пациентов с трофическими язвами с применением биоматериала КОЛЛОСТ®
-
Язвенный дефект очищают от некротизированных тканей: хирургическая обработка, гидрохирургическая обработка, ферментные препараты, сорбенты
- паравульнарно, а затем в дно раны для стимуляции восстановления вводится гель КОЛЛОСТ®;
- на область раневого дефекта имплантируется мембрана КОЛЛОСТ® с последующей фиксацией к краям кожной раны отдельными узловыми швами.
При необходимости мембрана предварительно перфорируют для оттока раневых выделений.
Трофическая язва часто является осложнением артериальных заболеваний (к примеру, атеросклероза), болезней вен (варикоза), а также сахарного диабета. Биоматериал «КОЛЛОСТ» активно применяется в современных методиках лечения трофической язвы.
В 2014 г. число больных сахарным диабетом в мире достигло 387 млн человек, и сохраняется тенденция к дальнейшему росту и, кроме того, «омоложению» заболевания. Больные сахарным диабетом подвержены высокой опасности инвалидизации вследствие быстрого образования и длительного заживления раневых дефектов кожных покровов и мягких тканей, ведущих к ампутации нижней конечности. Очевидно, что с увеличением темпов распространения сахарного диабета и его осложнений будет расти и удельный вес больных с дефектами кожных покровов и мягких тканей нижних конечностей [1, 2, 4].
Лечение трофических нарушений является значительной проблемой в хирургии диабетической стопы. При синдроме диабетической стопы нарушается взаимоотношение белковых фракций (дезорганизация коллагена), имеющее существенное значение в течении репаративно-пролиферативной фазы раневого процесса. Таким образом, нарушается физиологическое течение раневого процесса, происходит хронизация язвенного дефекта, и, как результат, наступает раневая кахексия. У больных снижается количество продуцируемого фибробластами коллагена, что ведет к замедлению заживления раны, повышается уровень матриксных металлопротеаз, замедляются процессы формирования экстрацеллюлярного матрикса, ремоделирования и формирования новых тканей [2, 5]. Стандартные методы лечения больных с трофическими поражениями тканей при синдроме диабетической стопы не всегда позволяют достичь заживления раневого дефекта и предупредить ампутацию. Большой интерес вызывают методы регенеративной медицины, включая генные, клеточные [3] и матриксные ацеллюлярные технологии. В ряде исследований показана способность факторов роста стимулировать заживление нейропатических язв у больных с синдромом диабетической стопы при условии многократного введения и создания высоких локальных концентраций (это условие необходимо, так как пептидные факторы роста быстро разрушаются протеолитическими ферментами) [3].
Цель работы — провести сравнительную оценку эффективности практического применения препарата эберпрот-п и биопластического материала коллост у больных с синдромом диабетической стопы, направленного на оптимизацию и повышение качества лечения раневых дефектов кожи и мягких тканей; внедрение в клиническую практику и изучение эффективности новых научных разработок, повышение продуктивности хирургического пособия при данной патологии.
Материал и методы
Препарат эберпрот-п относится к фармакологической группе регенерантов и репарантов, действующее вещество которого представляет собой фактор роста эпидермальный человеческий рекомбинантный (Recombinant Human Epidermal Growth Factor) — ЭФРчр. ЭФРчр продуцируется штаммом дрожжей Saccharomycesсerevisiae, в геном которого методами генной инженерии встроен ген ЭФРчр. Фактор роста эпидермальный человеческий рекомбинантный, полученный на основе технологии рекомбинантной ДНК, по механизму действия идентичен эндогенному фактору роста эпидермальному, вырабатываемому в организме [1]. Производитель: Центр генной инженерии и биотехнологии (ЦГИБ), Республика Куба.
Эпидермальный фактор роста (ЭФР) ускоряет рост и деление эпителиальных клеток, в человеческом организме содержится в тромбоцитах, фагоцитах, моче, слюне, молоке и в плазме крови. ЭФР — один из членов семейства белков, отвечающих за деление клеток эпителиального покрова. Все члены этого семейства содержат одну или несколько характерных аминокислотных последовательностей, согласно формуле: CX 7 CX 4—5 CX 10—13 CXCX 8 GXRC, где X — любая аминокислота.
Биопластический материал коллост представляет собой нереконструированный коллаген I типа с полностью сохраненной нативной структурой. Коллост изготавливают из кожи крупного рогатого скота. В процессе обработки удаляется эпидерма, подкожный жировой слой и все дермальные клетки без разрушения коллагеновой матрицы, создается неиммуногенный, инертный и стойкий материал, волокна которого напоминают решетку. Он действует как шаблон для формирования новой ткани. Фибробласты, кровеносные и лимфатические сосуды, нервные волокна, внедряясь из окружающей ткани в коллагеновую решетку, распространяются по ней. Постепенно рассасываясь, коллост формирует новый аутодермальный слой [4] (ООО «Биофармахолдинг», Россия).
Основываясь на вышеизложенных свойствах, мы провели сравнительное исследование, направленное на изучение воздействия препарата эберпрот-п и биопластического материала коллост на течение раневых процессов у больных с верифицированным диагнозом «синдром диабетической стопы». Больные были разделены на две группы. В 1-ю группу вошли пациенты, которым в составе комплексной терапии вводили препарат эберпрот-п (n=16). 2-ю группу составили пациенты, которым при идентичных условиях имплантировали биоматериал коллост (n=28). Состав и характеристика 1-й и 2-й групп даны в табл. 1.
![]()
Таблица 1. Характеристика исследуемых больных по группам
Составляющие лечения больных в обеих группах были идентичны, за исключением указанных элементов местного лечения. В состав лечения входили: общая терапия, ангиохирургическая коррекция сосудистого русла (1-я группа: БПШ — 3 пациента, РЭД — 1 пациент; 2-я группа: БПШ — 4 пациента, РЭД — 1 пациент), местное лечение (aggressive surgical treatment).
Методика местного лечения включала в себя три этапа:
1) дебридмент раневого дефекта;
2 имплантацию препарата эберпрот-п (1-я группа) или биоматериала коллост (2-я группа);
3) создание благоприятных условий для дальнейшего течения раневого процесса.
На первом этапе у всех больных обеих групп применяли:
а) ультразвуковую гидрохирургическую обработку дефектов с подачей в систему слабого раствора анестетика (раствор новокаина 0,25% от 200 до 300 в зависимости от степени выраженности местных деструктивно-воспалительных процессов и площади раневой поверхности);
б) механическую некрэктомию с обработкой дна, стенок и краев дефекта; вскрытием и удалением гнойно-некротических карманов и затеков.
Второй этап у пациентов 1-й группы включал введение в раневой дефект препарата эберпрот-п. Для приготовления лекарственного раствора во флакон, содержащий 75 мкг лиофилизата, добавляли 5 мл воды для инъекций, после чего осторожно перемешивали в течение нескольких секунд до получения однородного прозрачного и бесцветного раствора без видимых твердых частиц. Полученный раствор сразу после приготовления вводили в область дна, стенок, краев раны, а также в область паравульнарных тканей. Количество введенного препарата соотносили с площадью дефекта мягких тканей исходя из нормы 0,5 мл препарата на 1 см 2 площади дефекта. При каждой новой инъекции использовалась новая стерильная игла. Глубина введения составляла около 0,5 см. Введение препарата производили каждые 48 ч в течение 3 нед. Число флаконов на одного пациента варьировалось от 8 до 48.
У пациентов 2-й группы на данном этапе производили имплантацию биоматериала коллост в виде 7% геля в дозе 1,5 мл (одна из официальных форм). Перед применением гель, находящийся в одноразовом стерильном шприце в контурной ячеистой упаковке, нагревали до 32—36 °С. Введение геля осуществляли в область дна, стенок, краев дефекта на глубину от 0,2 до 0,5 см под углом 15—25° на выходе иглы шприца для создания «туннеля». На одну манипуляцию требовалось, в зависимости от площади раневого дефекта, от 1 до 3 шприцев. Кратность процедуры —1 введение.
Третьим этапом больным 1-й группы после манипуляции поверхность раны закрывали влажной повязкой с физиологическим раствором и фиксировали сверху нетравматичной нейтральной повязкой, смену повязок производили ежедневно.
У пациентов 2-й группы после имплантации биоматериала на раневую поверхность накладывали самофиксирующиеся гидроколлоидные повязки, которые меняли каждые 48 ч. Через 12—15 сут после процедуры переходили на нетравматичные нейтральные повязки или их сочетание с повязками, содержащими ионы Ag.
Всем пациентам обеих групп на третьем этапе производилась разгрузка стоп с наложением иммобилизирующих повязок по технологии ТСС.
Результаты
Наблюдение за пациентами обеих групп осуществлялось с момента начала лечения в течение 12 мес. Наблюдению подлежали следующие факторы:
1) скорость и продуктивность репаративных процессов в ране и сроки эпителизации раневого дефекта;
2) относительная скорость заживления раны [5];
3) общее самочувствие пациентов и переносимость проводимой терапии;
4) частота рецидивов на фоне адекватной перманентной терапии;
5) количество осложнений, в том числе ампутаций, после имплантации препарата и биоматериала.
Результаты наблюдения представлены в табл. 2.
![]()
Таблица 2. Результаты лечения в исследуемых группах больных после введения препарата эберпрот-п и биоматериала коллост
Достигнутая положительная динамика раневого процесса у пациентов 1-й группы (применение препарата эберпрот-п) отмечена в следующие сроки: у 1 пациента — через 6 мес, у 1 — через 5 мес, у 1 — через 1 мес с момента начала лечения.
Отдаленные результаты в нескольких случаях остались неизвестны по причине отказа со стороны пациентов от дальнейшего лечения препаратом вследствие «плохой переносимости»: у 2 пациентов после 4-го и 5-го сеанса введения (головные боли, тахикардия, тошнота, снижение артериального давления, чувство жара, боль и жжение высокой интенсивности в области введения препарата); у 1 пациента после 6-го сеанса введения (жалобы: «становится очень плохо сразу же после процедуры, теряю сознание»). Во всех этих случаях проводилась медикаментозная коррекция. Ампутация на уровне пальцев стоп выполнена: 1 пациенту — через 5 нед, 1 пациенту — через 4 нед после 3-недельного цикла введения препарата из-за развития остеомиелита на фоне незакрывающегося дефекта и полного разрушения костных структур. Метатарзальная ампутация (1 пациенту) выполнена через 2 нед из-за развития гангрены. Ампутация на уровне голени выполнена: 1 пациенту — через 2 нед, 1 пациенту — через 6 нед из-за развития гангрены с субтотальным поражением стопы. Некрэктомия с аутодермопластикой выполнена у 2 пациентов (через 3 нед и 16 нед соответственно из-за отрицательной динамики и увеличения площади дефекта).
Начало эпителизации раневого дефекта у пациентов 2-й группы (имплантация биоматериала коллост) наступало через 10,3±2,8 сут. Гипертрофического рубцевания ран, рецидивов трофических нарушений кожи в течение заболевания, а также отказов от лечения из-за плохой переносимости процедуры во 2-й группе не отмечено.
Клинические примеры
1. Больная М., 1958 г. р. (рис 1, 2).
![]()
Рис. 1. Вид стопы. Диагноз: синдром диабетической стопы, нейроишемическая форма, W3. Трофическая язва левой стопы, ХАН 3. Состояние после рентгенэндоваскулярной вазодилатации слева. Диабетическая полинейропатия, сенсомоторная, умеренно выраженная.
За время лечения не наблюдалось значимого уменьшения размера язвы.
Отдаленные результаты: развитие гангрены 4 пальца левой стопы, с разрушением 4 плюснефалангового сустава, на фоне незаживающей язвы через 8 нед после окончания лечения; выполнена ампутация 4 пальца левой стопы, с резекцией головки 4 плюсневой кости.
2. Больной М., 42 года (рис 3—5).
![]()
Рис. 3. Вид стопы. Диагноз: синдром диабетической стопы, нейроишемическая форма, W2. Трофические язвы правой стопы, ХАН 3. Состояние после бедренно-подколенного шунтирования справа, ампутации 3 пальца правой стопы с резекцией дистальной головки 3 плюсневой кости. Диабетическая полинейропатия, сенсомоторная, умеренно выраженная. Диабетическая нефропатия. Диабетическая ретинопатия.
![]()
Рис. 4. Имплантация материала коллост (коллаген I типа) в виде геля 7%.
![]()
Рис. 5. Вид стопы на 27-е сутки после комплексного лечения с имплантацией материала коллост в виде геля 7%.
Отдаленные результаты: полная эпителизация дефекта.
Выводы
Применение биопластических материалов на основе нативного коллагена I типа отечественного производства в лечении дефектов тканей у больных с синдромом диабетической стопы на данном этапе предпочтительнее фактора роста эпидермального человеческого рекомбинантного соответствующего производителя. При применении ЭФРчр количество ампутаций пальцев стоп и метатарзальных ампутаций составило 19%, ампутаций на уровне голени — 12,5%. При применении биоматериала коллост на основе коллагена I типа во 2-й группе ампутаций за период наблюдения не отмечено. Эпителизация дефектов в отдаленные сроки при использовании ЭФРчр составила 19%, при применении биоматериала коллост — 89%. Индивидуальная непереносимость препарата на основе ЭФРчр составила 19%, что вызвало отказ от лечения со стороны данных пациентов. Напротив, при использовании биопластического материала коллост индивидуальной непереносимости в группе не отмечено.
Читайте также: