Когда вирусы герпес токсоплазмоз
Обновлено: 17.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Токсоплазмоз: причины появления, симптомы, диагностика и способы лечения.
Определение
Токсоплазмоз – широко распространенное паразитарное заболевание с поражением нервной системы, глаз, селезенки, печени, сердца. По данным ВОЗ, число лиц, инвазированных токсоплазмами, составляет около 1,5 млрд человек.
У взрослых токсоплазмоз обычно протекает бессимптомно. Заболевание с клиническими проявлениями часто развивается у наиболее восприимчивой и уязвимой группы населения – детей.
Причины появления токсоплазмоза
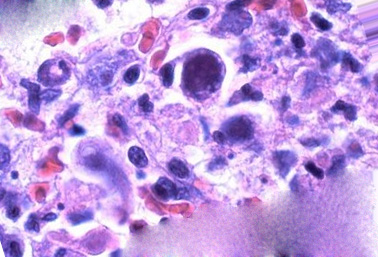
Возбудителем токсоплазмоза является Toxoplasma gondii. Токсоплазма – внутриклеточный паразит, который способен к размножению бесполым путем в клетках тканей человека. В процессе размножения образуются скопления паразитов внутри клетки с образованием псевдоцист. В случае хронизации процесса образуются истинные цисты с собственной оболочкой.
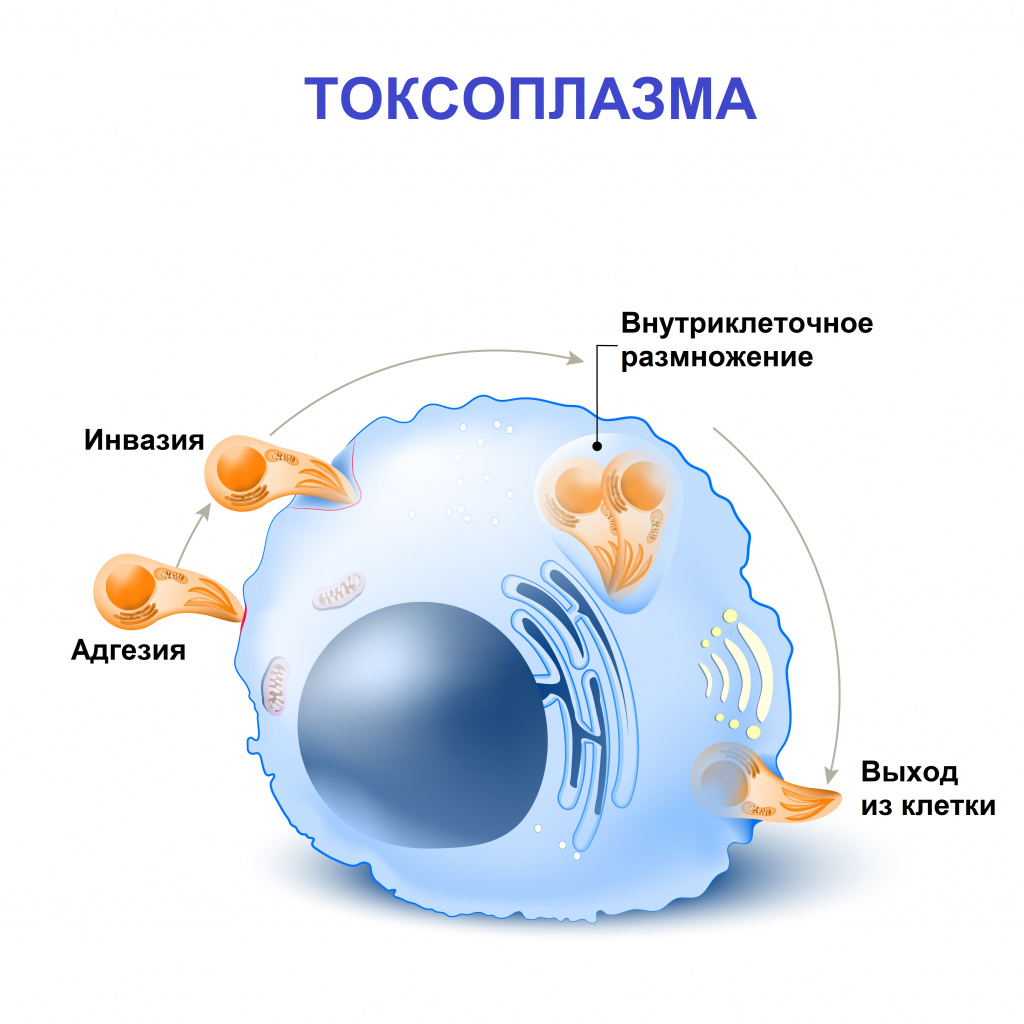
Человек является промежуточным хозяином и заражается спорозоитами – инвазивными формами токсоплазм, которые способны проникать в организм.
Спорозоиты выделяются с фекалиями кошек, и при нарушении правил личной гигиены происходит заражение человека (этим объясняется столь частое инфицирование токсоплазмами в раннем детском возрасте – в связи с особенностями поведения детей и не развитыми у них навыками гигиены).
Другая форма токсоплазм – цистозоиты – они проникает в организм человека при употреблении мяса больных животных, если оно было плохо термически обработано.

Токсоплазмы через желудочно-кишечный тракт попадают в лимфатическую систему и с током лимфы – в лимфатические узлы. На этом этапе на фоне интенсивного размножения токсоплазм формируются воспалительные изменения в лимфоидной ткани. Далее паразиты проникают в системный кровоток и разносятся по всему организму. В зависимости от конечной точки их миграции развивается соответствующая клиническая картина заболевания.
Размножение в клетках органов сопровождается выделением токсических продуктов жизнедеятельности токсоплазм, которые могут вызывать аллергические реакции организма.
Иммунная система со временем уничтожает все вегетативные формы, которые способны к размножению, и в организме остаются лишь цисты токсоплазм, спрятанные от иммунологического надзора благодаря толстой оболочке.
Под воздействием факторов, снижающих иммунные силы организма (например, ВИЧ, применение цитостатиков, глюкокортикостероидная терапия), возможна повторная активация токсоплазм с дальнейшим их распространением по всему организму.
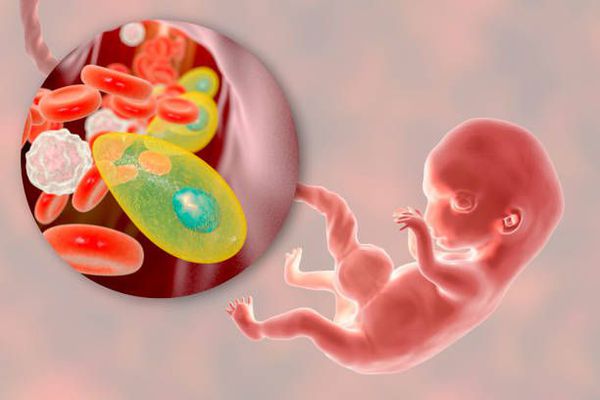
Если заражение произошло во время беременности (после 2-го месяца), токсоплазмы могут проникнуть в кровоток плода и привести к развитию заболевания, а также к формированию тяжелых пороков развития.
Классификация заболевания
В зависимости от сроков заражения токсоплазмами выделяют врожденный токсоплазмоз (при внутриутробном заражении) и приобретенный (когда заражение произошло после рождения).
При развитии клинической симптоматики выделяют легкую, среднетяжелую и тяжелую формы токсоплазмоза.
Симптомы токсоплазмоза
Клиническая картина токсоплазмоза зависит от формы заболевания.
Наиболее часто встречается бессимптомная первичная токсоплазменная инфекция, которая при отсутствии факторов иммунодефицита никак себя не проявляет.
В редких случаях инвазия токсоплазм в организм ранее здоровых людей вызывает повышение температуры тела, незначительное увеличение и болезненность лимфатических узлов, пятнисто-папулезную сыпь, часто принимаемую за крапивницу (красного цвета с небольшими возвышениями – папулами), и увеличение печени. Еще реже токсоплазмы вызывают воспалительные процессы в органах зрения.
Инкубационный период токсоплазмоза составляет от 3 дней до нескольких месяцев. Обычно он протекает бессимптомно, в редких случаях больные жалуются на слабость и головную боль.
При острой форме токсоплазмоза по завершении инкубационного периода внезапно поднимается температура до 39°C градусов, появляется выраженная слабость, головная и мышечная боль, снижается аппетит, иногда бывают высыпания на коже. Сыпь распределяется равномерно по всему телу, редко встречается на волосистой части головы, ладонях и стопах. Характер высыпаний – пятнисто-папулезный со склонностью к слиянию. В это же время увеличиваются лимфатические узлы, печень и селезенка. При поражении сердца фиксируются нарушения сердечного ритма. Возможны психические расстройства, потеря сознания, парезы и параличи, повторяющаяся рвота, резкие головные боли – все эти симптомы указывают на поражение центральной нервной системы.
При легкой форме острого токсоплазмоза заболевание проявляется недомоганием, незначительным подъемом температуры, тошнотой, диареей.
При хроническом течении токсоплазмоза не наблюдается столь яркой клинической картины. Выявляются симптомы хронической интоксикации: слабость, снижение аппетита, нарушение сна, дискомфорт в мышцах и суставах, быстрая утомляемость, раздражительность, головные боли, учащенное сердцебиение. Одним из частых проявлений хронического токсоплазмоза является прогрессирующее поражение глаз. В редких случаях – судороги.
Длительное течение болезни может привести к снижению интеллектуального развития и различным психическим нарушениям.
Врожденный токсоплазмоз также подразделяется на острый и хронический. При остром врожденном токсоплазмозе состояние ребенка с первых дней тяжелое, прогноз неблагоприятный.
При хронической форме часто отмечается поражение нервной системы с задержкой умственного и физического развития ребенка.
Более легкие формы проявляются в возрасте 5–7 лет в виде повышенной утомляемости, судорог и поражения глаз.
Диагностика токсоплазмоза
Диагностика токсоплазмоза проводится на основании жалоб пациента, данных осмотра и комплекса лабораторно-инструментальных методов обследования. Объем обследования может меняться в зависимости от клинической картины, тяжести заболевания, а также наличия осложнений.
Для выявления возбудителя могут быть назначены следующие методы диагностики:
-
токсоплазма, определение ДНК в сыворотке крови;
Определение ДНК токсоплазмы (Toxoplasma gondii) в сыворотке крови методом полимеразной цепной реакции (ПЦР) с детекцией в режиме «реального времени». Токсоплазмоз – распространенная инфекция, обусловленная внутриклеточным протозойным паразитом Тoxoplasma gondii. Осн.
Что такое токсоплазмоз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, паразитолога со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Токсоплазмоз — это острое и хроническое паразитарное заболевание человека в виде манифестных форм или носительства, вызываемое простейшими внутриклеточными паразитами — токсоплазмами, которые попадая в организм человека могут при условиях иммунодефицита поражать нервную ткань, среды глаза, сердечно-сосудистую и ретикулоэндотелиальную системы, вызывая поражение организма той или иной степени тяжести. Болезнь относится к группе TORCH-комплекса, т. е. вызывает врождённую патологию.
Этиология
Таксономия:
Вид — Toxoplasma gondii
Токсоплазмы обитают в мире в трёх формах:
- трофозоиты (тахизоиты);
- цисты (брадизоиты);
- ооцисты.
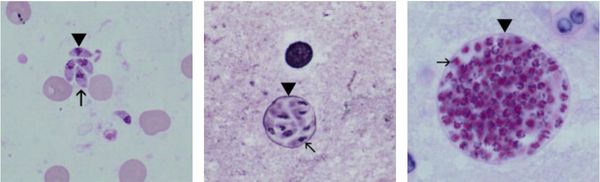
Трофозоиты достигают 4-7 мкм в длину и 2-4 мкм в ширину. Их тело по форме напоминает полумесяц с заострённым передним и закруглённым задним концами, состоит из пелликулы (покровной ткани) и различных органелл. Такие паразиты обитают во всех клетках млекопитающих кроме эритроцитов, размножаются путём деления. Могут создавать движение, активно проникая в клетки хозяина через клеточную мембрану или посредством фагоцитоза (захвата и переваривания клетки). Обнаруживаются в тканях в острой стадии инфекции. Их скопление внутри одной клетки называют псевдоцистой. Трофозоиты неустойчивы вне клетки и во внешней среде, быстро погибают при высушивании, прогревании и применении дезинфицирующих средств. Хорошо окрашиваются по Романовскому. Чувствительны к различным химиопрепаратам (сульфаниламидам, некоторым макролидам и другим).
Цисты размерами до 100 мкм отличаются плотной оболочкой, через которую не могут проникнуть антитела или лекарственные препараты. Внутри оболочки сосредоточено 3000-5000 паразитов, со временем они увеличиваются. Цисты формируются в организме хозяина (в основном в скелетных мышцах, миокарде и ЦНС) и живут там десятки лет. Чрезвычайно устойчивы к воздействиям внешних факторов. При адекватной иммунной системе могут пожизненно находиться в состоянии функционального покоя и не приносить никакого вреда организму человека.
Ооцисты играют основную роль в передаче инфекции. Они представляют собой овальные образования 10-12 мкм в диаметре. Их развитие и формирование длится 3-24 дня и проходит в слизистой оболочке тонкой кишки кошек. Затем в течение 7-20 дней паразиты выделяются с испражнениями, после этого срока новые фекалии кошки уже не заразны. За сутки с испражнениях животного выделяется до 10 миллионов ооцист. Спустя 2-3 дня при температуре 24 °C происходит споруляция ооцист — образование спор. При благоприятных условиях микроорганизмы сохраняются во внешней среде до года и дольше.
Существует множество штаммов токсоплазм, одни из которых отличаются высокой вирулентностью, а другие относительно маловирулентны. [1] [2] [7] [9]
Эпидемиология
Учитывая большое количество латентных форм, заболевание не поддаётся общему исчислению — им может быть заражено не менее 1,5 миллиардов человек. Только ежегодно регистрируется около 200 тысяч случаев внутриутробного инфицирования.
Распространение возбудителя повсеместное — токсоплазма обнаружена на всех материках. После заражения паразиты способны пожизненно сохранятся в организме большинства животных и птиц. Количество случаев приобретённого токсоплазмоза в разных странах колеблется: от 85 % во Франции и Мадагаскаре до 15 % в США и Англии.
- Фекально-оральный:
- водный и пищевой путь — при недостаточной термической обработке, чаще при употреблении сырого мяса и фарша;
- контактно-бытовой путь — при несоблюдении санитарных норм в повседневной жизни, например, при общении с кошками.
- Вертикальный путь (от матери к плоду) — преимущественно при первичном заражении матери во время беременности, часто у ВИЧ-инфицированных в стадии СПИДа.
- Артифициальный путь — при пересадке органов, в которых расположены цисты, пациенту с плохим иммунитету.
- Аэрогенный путь — при попадании инфицированной ооцистами пыли в рот человека.
- Контактный путь — при повреждении целостности кожных покровов. Встречается крайне редко, в основном у работников лабораторий и скотобоен, отмечен лишь в некоторых источниках, явного практического значения не имеет.
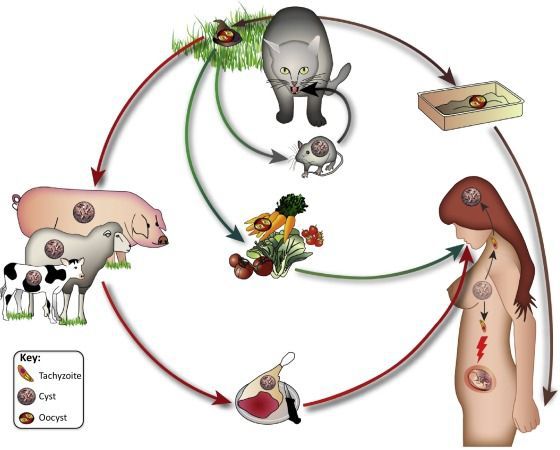
От человека к человеку заболевание не предаётся (кроме случаев каннибализма). Нельзя заразиться посредством укуса насекомых и при половом контакте.
Инфицирование токсоплазмой вызывает устойчивый пожизненный иммунитет к повторному заражению, однако известны случаи рецидива первичной инфекции при заражении другим высоковирулентным штаммом (у беременных, заразившихся при употреблении сырого мяса с другого континента). [1] [3] [5] [8] [9]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы токсоплазмоза
Инкубационный период при манифестных формах (явных проявлениях болезни) длится от двух недель до двух месяцев.
Специфичных симптомов, характерных именно для токсоплазмоза, не существует.
В большинстве случаев приобретённого токсоплазмоза заболевание протекает бессимптомно или со стёртой клиникой, напоминающей нетяжёлое ОРЗ: кратковременная лихорадка, слабость, недомогание, повышение температуры до 38,0 °C, увеличение периферических лимфоузлов, небольшое увеличение печени и селезёнки.
Доказано, что токсоплазма может оказывать влияние на психику человека. Это выражается в учащении рискованных действий, снижении концентрации внимания, повышенной нервозности, у лиц с тяжёлым острым или длительным хроническим активным течением повышен риск развития шизофрении.
Иногда заболевание проявляется изолированной глазной формой — длительно текущие увеиты, иридоциклиты и хориоретиниты. Как правило, эти нарушения являются поздними проявлениями нераспознанного ранее врождённого процесса.
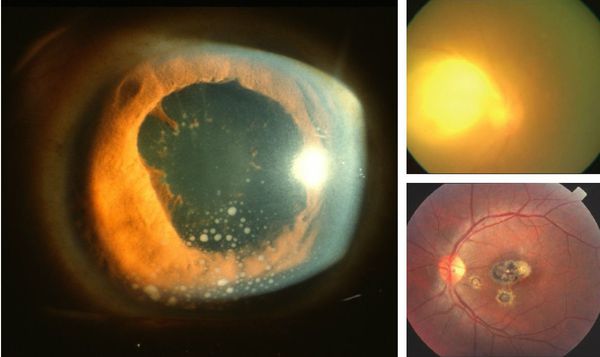
У людей с выраженным иммунодефицитом (ВИЧ, пересадка органов с последующей цитостатической терапией) возможно развитие генерализованного процесса с поражением нескольких органов (головного мозга, сердца, печени, почек, лёгких), нередко очень тяжёлого течения, проявляющегося в виде синдрома полиорганной недостаточности.
Токсоплазмоз у беременных может протекать в различных клинических вариантах и представляет опасность не столько для самой беременной (исключая тяжело протекающие патологии у беременных со СПИДом), сколько для плода.
При первичном заражении беременной токсоплазмозом имеет значение срок гестации:
- При инфицировании в первом триместре передача возбудителя плоду происходит лишь в 4 % случаев (к 13 неделе — в 6 %), но заканчивается, как правило, гибелью плода и выкидышем на ранних сроках. Если первичная инфекция у матери в первом триместре доказано, но выкидыш до 13 недели беременности не произошёл, то крайне высока вероятность, что внутриутробной передачи не было и ребёнок будет здоров.
- При инфицировании во втором триместре (особенно на 24-26 неделях) риск внутриутробной передачи резко возрастает и достигает 30-40 %, причём сопровождается развитием тяжёлых проявлений заболевания — одновременное увеличение селезёнки и печени, воспаление сосудистой оболочки и сетчатки глаза, поражения ЦНС в виде гидроцефалии, кальцификация, сыпь, миокардит, пневмония и другие.
- При заражении матери в третьем триместре передача инфекции ребёнку происходит с частотой до 90 %, однако проявления заболевания являются латентными или субклиническими и могут появиться спустя годы после рождения (отставание в развитии, нарушения зрения). [1][2][4][9]
Патогенез токсоплазмоза
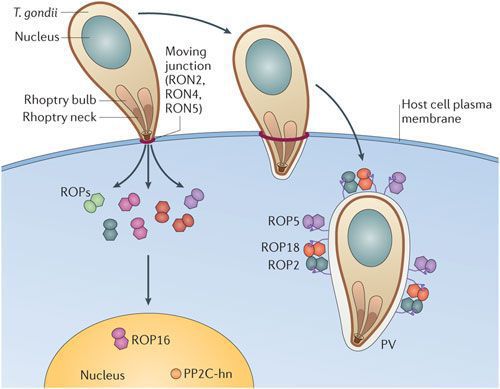
По мере развития и размножения токсоплазм поражённые клетки разрушаются, происходит заражение новых здоровых клеток, и при попадании возбудителя в кровоток паразиты разносятся по всему организму. Образуются некрозы с формированием фиброзной ткани и кальцификацией (отложение солей кальция в организме).
Под воздействием иммунитета безоболочечные трофозоиты превращаются в брадизоиты (оболочечные скопления токсоплазм), т.е. в тканевые цисты, которые сохраняются десятками лет в неактивном состоянии и при значительном снижении иммунитета способны к обратной трансформации с развитием обострения.
При первичной инфекции у беременных возбудитель проникает в ткани плода и вызывает воспалительный процесс, причём в разные периоды развития наблюдается различный характер воспаления: у эмбриона происходит лишь альтерация (дистрофия и некроз ткани без фиброза), в раннем фетальном периоде дополняется повышенным образованием соединительной ткани (фиброзом), а в позднем фетальном периоде присоединяется сосудистый компонент. Отсюда вытекают различные по характеру и тяжести поражения плода, которые зависят от сроков инфицирования матери. [1] [2]
Классификация и стадии развития токсоплазмоза
По течению процесса токсоплазмоз бывает:
- острым — до одного месяца;
- подострым - 1-3 месяц;
- хроническим — более трёх месяцев.
По клиническим признакам выделяют пять форм заболевания:
- Врождённый острый токсоплазмоз:
- манифестная форма (с указанием ведущих проявлений);
- субклиническая форма (с указанием способа верификации диагноза).
- Врождённый хронический токсоплазмоз:
- обострение / ремиссия;
- с резидуальными (остаточными) явлениями / без резидуальных явлений.
- Врождённый латентный токсоплазмоз.
- Приобретённый острый токсоплазмоз.
- Приобретённый хронический токсоплазмоз.
По степени тяжести заболевание бывает:
- лёгким;
- среднетяжёлым;
- тяжёлым (врождённая инфекция, токсоплазмоз при СПИДе).
По наличию осложнений выделяют:
- осложнённый токсоплазмоз;
- неосложнённый токсоплазмоз.
В Международной классификации болезней 10 пересмотра выделены шесть типов заболевания:
- B58.0 Токсоплазмозная окулопатия;
- B58.1 Токсоплазмозный гепатит (K77.0*);
- B58.2 Токсоплазмозный менингоэнцефалит (G05.2*);
- B58.3 Легочный токсоплазмоз (J17.3*);
- B58.8 Токсоплазмоз с поражением других органов;
- B58.9 Токсоплазмоз неуточнённый. [1][2][3]
Осложнения токсоплазмоза
При врождённой форме может возникнуть гидроцефалия, микроцефалия, задержка психомоторного развития и слепота. Эти осложнения сопровождаются увеличением или уменьшением размеров черепа, различными неврологическими расстройствами — косоглазием, судорогами, трудностью с сидением и держанием головы, рвотой и другими.
При глазной форме заболевания развивается слепота, снижение остроты зрения и воспалительные явления всех сред глаза. Причём возможно как рождение с грубыми дефектами зрения, так и появление воспалительных явлений и нарушения зрения спустя много лет после рождения.
Токсоплазмоз у иммунокомпрометированных людей осложняется шизофренией, токсоплазменный энцефалитом и полиорганной недостаточностью — тяжёлой патологией различных органов при выраженном иммунодефиците. При этом свойственна картина тяжёлого энцефалита. Прогноз, как правило, неблагоприятный. [1] [5] [8] [9]
Диагностика токсоплазмоза
Лабораторная диагностика:
- Клинический анализ крови: снижение уровня тромбоцитов, увеличение количества лимфоцитов и эозинофилов.
- Биохимический анализ крови: возможно повышение уровня трансаминаз и билирубина.
- Иммуноферментный анализ (ИФА):
- Выявление специфических антител класса M — острая инфекция или её реактивация. Имеет ряд недостатков — низкая специфичность, длительная циркуляция в организме, иногда до года после острого процесса. В сложных случаях уточнение следует производить при помощи метода "двойной сэндвич" или "иммунозахват" IgM ELISA.
- Выявление специфических антител класса G (клеток памяти) — носительство, инфицированность — появляются в среднем со второй недели заболевания и достигают пика на 1-2 месяце, сохраняются пожизненно, за исключением СПИД-ассоциированных заболеваний.
- Авидность IgG — уточнение давности заболевания. Недостатком является отсутствие стандартизации результатов, что зачастую приводит к различным ошибкам интерпретации. Наибольшее значение имеет высокая авидность, остальные результаты низкой и слабой авидности могут быть ошибочными и не должны трактоваться как недавно перенесённое заболевание при отсутствии других подтверждающих этот факт тестов.
- ПЦР-диагностика: выявление ДНК токсоплазмы в крови, других жидкостях и тканях человеческого организма. Особенно информативна в диагностике генерализованного, глазного и врождённого токсоплазмоза, в т. ч. в антенатальном периоде путём проведения амнио (не ранее 16 недель) и кордоцентеза (с 18 недели беременности).
- УЗИ-диагностика: внутриутробное выявление гидро- и микроцефалии, кальцификатов, гепатоспленомегалии и выраженной задержки развития. [1][2][4][5][6]
Дифференциальная диагностика
Токсоплазмоз — это инфекция с необычайно разнообразными проявлениями, поэтому ввиду неспецифичности проявлений основное место в дифференциальной диагностике отводиться лабораторному обследованию, а именно специфическим серологическим тестам.
Необходимо исключить следующие заболевания:
-
(ВЭБ-инфекцию) — боли в горле, преимущественное увеличение затылочных и заднешейных лимфоузлов, характерные изменения гемограммы (появление большого количества атипичных мононуклеаров и отсутствие столь выраженных изменений при врождённом течении), положительные IgM и ПЦР крови; — лимфоцитарный характер гемограммы, частое поражение слюнных желёз, положительные IgM, ПЦР крови;
- туберкулёз — длительное постепенное начало, лёгкий субфебрилитет (до 38,0 °C), ночная потливость, нездоровый румянец на щеках, кашель, специфические изменения в лёгких, положительные пробы на туберкулёз, выявление бациллы Коха в мокроте;
- лимфопролиферативные заболевания (лимфома Ходжкина, неходжкинские лимфомы) — специфические изменения при биопсии поражённой ткани (лимфоузлов);
- ВИЧ-инфекция — наличие факта возможного заражения, увеличение всех групп лимфоузлов, положительная серология;
- саркоидоз — специфические изменения в лёгких, положительные результаты гистологического исследования. [1][2][5]
Лечение токсоплазмоза
Большинство случаев приобретённого токсоплазмоза протекают в лёгкой или бессимптомной форме, они не регистрируются и, по-видимому, не нуждаются в каком-либо лечении.
Необходимость проведения специфической этиотропной терапии возникает лишь у некоторых групп пациентов:
- беременные с доказанным первичным инфицированием (в ряде случаев при реактивации хронической инфекции);
- дети с врождённой формой токсоплазмоза (при наличии явных клинических и лабораторных проявлений заболевания, субклинических и инаппарантных формах) — сроки и объём терапии зависят от конкретных данных;
- иммунокомпрометированные люди, у которых токсоплазмоз (острый или в фазе реактивации хронического процесса) протекает с выраженными клинико-лабораторными проявлениями. Основное направление воздействия в этом случае должно быть на устранение причины иммунодефицита, повышение уровня СД4 клеток.
Проведение лечения может осуществляться как в стационаре, так и амбулаторно в зависимости от выраженности процесса, реакции пациента на вводимые препараты, необходимости тех или иных вариантов патогенетического и симптоматического обеспечения. [1] [4] [7]
Прогноз. Профилактика
При приобретённом токсоплазмозе у иммунокомпетентных лиц прогноз благоприятный, у иммунокомпрометированных лиц (СПИД) прогноз серьёзен, нередки летальные исходы.
При врождённом токсоплазмозе исход заболевания зависит от сроков инфицирования плода:
- при инфицировании в первом триместре, как правило, происходит выкидыш;
- в более поздние сроки последствия варьируются от тяжёлых до резидуальных форм.
Основным методом профилактики приобретённого и врождённого токсоплазмоза является соблюдение санитарно-гигиенических правил, особенно беременными, не имеющими антител класса G к токсоплазмам:
- ограничение контакта с кошками;
- запрет на употребление сырого мяса, фарша и морепродуктов;
- тщательная промывка зелени, фруктов и овощей;
- мытьё рук перед едой;
- работа на приусадебном участке только в перчатках.
Для беременных особенно важен скрининг антител к токсоплазме, позволяющий выявить активно протекающее заболевание или риск его возникновения, а также вовремя провести медикаментозную профилактику острого токсоплазмоза беременной и снизить риск врождённой инфекции на 60 %. При отсутствии антител класса G в первом триместре необходимо отслеживать антитела IgM и IgG не только в тертьем, но и во втором триместре беременности.
В очаге токсоплазмоза противоэпидемические мероприятия не проводятся, вакцина на разработана. [2] [3]
Анализ на герпес позволяет определить присутствие в организме вируса герпеса.
Сегодня известно несколько типов вируса герпеса. Наиболее часто встречаются вирус простого герпеса (ВПГ) I-го типа, проявляющийся в виде характерных высыпаний на лице и слизистой рта (так называемая «простуда на губе»), ВПГ II-го типа (генитальный герпес, для которого характерна сыпь на слизистой половых органов), а также опоясывающий герпес (герпес III-го типа).
Герпес может передаваться различными путями – при непосредственном контакте (бытовым путем), воздушно-капельным путем; возможно внутриутробное заражение. В то же время типично заражение герпесом при половом контакте, поэтому герпес включается в число ЗППП (заболеваний, передающихся половым путем). Также герпес входит в число ToRCH-инфекций, объединяющих заболевания, способные причинить вред плоду во время беременности.
Вирус герпеса не всегда активен. Он может годами присутствовать в организме, не приводя к проявлению каких-либо явных симптомов и активизируясь лишь при снижении иммунитета.
Считается, что вирусом герпеса заражено большинство жителей Земли (по некоторым оценкам – до 90%). Поэтому так важно определить, являетесь ли Вы носителем вируса. Если нет, Вам следует быть особенно внимательным к угрозам возможного заражения, - это позволит Вам сохранить тот потенциал здоровья, которым Вы обладаете.
Анализ на герпес проводится для каждого конкретного типа вируса. Зная, присутствует ли данный тип вируса герпеса в организме или нет, врач получает необходимую информацию для диагностики заболеваний и оценки общего состояния организма.
На сегодняшний день медицина еще не располагает средствами, способными полностью победить герпес. Но подавить активность вируса или предотвратить его переход в активное состояние вполне возможно. Поэтому анализ на герпес является составляющей многих комплексных обследований, а в случае подозрения на герпес он необходим для точной диагностики и назначения адекватного курса лечения.
Когда назначается анализ на герпес
Анализ на герпес обычно назначается:
- при наличии симптомов, характерных для герпесной инфекции – для того, чтобы подтвердить их герпесную природу, а также для того, чтобы определить, каким именно типом вируса они вызваны;
- при планировании беременности – обоим партнерам;
- во время беременности;
- новоророжденным при инфицированности матери;
- для того чтобы установить, передалась ли герпесная инфекция при контакте с зараженным партнером.
Методы проведения
Основными методами анализа на герпес являются иммуноферментный анализ (ИФА) и ПЦР-диагностика.
Анализ крови на герпес иммуноферментным методом (ИФА)
Для иммуноферментного анализа на герпес биологическим материалом является кровь.
Организм отвечает на проникновение вируса тем, что вырабатывает для борьбы с ним специфические иммунные тела. Эти тела могут быть обнаружены в крови с помощью серологического исследования. Иммуноферментный анализ показывает наличие в крови антител к вирусу герепеса (Ig G и Ig M).
ПЦР-диагностика герпеса
Метод ПЦР (полимеразной цепной реакции) строится на анализе ДНК во взятом образце биологического материала. Выделяются фрагменты ДНК, характерные для данного типа вируса и многократно воспроизводятся. Умножение позволяет обнаружить вирус, присутствующий даже в незначительных количествах.
Биологическим материалом для ПЦР-диагностики обычно является соскоб (проба, взятая непосредственно с места высыпания), моча, кровь или слюна.
Подготовка к анализу на герпес
Где сдать анализ на герпес в Москве
Сделать анализ на герпес Вы можете в АО«Семейный доктор». Вы можете сдать анализ там, где Вам это наиболее удобно, выбрав поликлинику, которая находится в нужном Вам районе Москвы. В наших поликлиниках Вы можете сдать анализы в выходные и праздничные дни.
Оставьте телефон –
и мы Вам перезвоним
Не занимайтесь самолечением. Обратитесь к нашим специалистам, которые правильно поставят диагноз и назначат лечение.
Материал составлен на основе фундаментальных трудов западных ученых.
Токсоплазма, краснуха, цитомегаловирус и беременность
При беременности назначают анализы на антитела к инфекциям - токсоплазме, цитомегаловирусу и краснухе. Определяется два вида антител – IgG и IgM, по которым судят о встрече с инфекционным агентом, а также о времени этой встречи. Самое страшное – заражение во время беременности (краснуха, токсоплазма, ЦМВ) или активация инфекции (ЦМВ).
Часто пациенты получают неопределенный результат – «серая» или «неопределенная» зона. И им рекомендуют пересдать анализ через 2 недели. Это можно себе позволить, если вы только готовитесь к беременности. Но: при беременности ждать нельзя! Такие анализы должны сразу пересматриваться более точными методами. .
Специфические антитела класса IgM, в частности, антитела к краснухе, относятся к факторам, циркулирующим в крови экстремально низких концентрациях. Поэтому анализы не в цифрах (количественно), а в виде положительности (=реактивности) или отрицательности (=отсутствии реактивности). Отрицательный и положительный результаты отделяет друг от друга так называемый порог отсечки (cutoff). Цифры показателя выше данного порога считаются положительными, а ниже порога — отрицательными. Зона значений порог ± 10%) является „зоной неопределенности”.
Быстрые уточняющие методы диагностики
Используются два способа: подтверждающие анализы методом иммуноблот и анализ на авидность антител IgG.
Если Вы сдаете эти анализы, исчезает необходимость ЖДАТЬ 2 недели плюс дни готовности анализа. Вы получаете сведения о своем состоянии ВОВРЕМЯ.
Подтверждающие анализы на токсоплазму, краснуху, ЦМВ методом иммуноблот:
- Высокочувствительный и специфичный тест!
- Чувствительность 97 %
- Специфичность 99 %
Используется для подтверждения результатов скрининговых исследований, таких как ИФА (ELISA) или иммунофлуоресцентный анализ (IFA).
Будьте уверены в анализе!
Зачем это нужно:
- точное и своевременное выявление позволит правильно определить тактику ведения беременности
- нет необходимости терять время на ожидание следующего анализа
Тактика врача определяется в каждом конкретном случае по-разному (подготовка к беременности, начало беременности, период новорожденности и т.д.)
Авидность антител IgG
Определить время, когда произошло инфицирование можно и по авидности антител IgG. Этот анализ менее точен по срокам, чем подтверждающий анализ методом иммуноблот.
Низкоавидные антитела встречаются при острой, недавно развившейся инфекции
Высокоавидные антитела – если встреча с инфекцией состоялась давно.
Определение авидности антител помогает врачу оценить ситуацию по инфекции и решить вопрос о дальнейших действиях.
Кому нужно полное обследование на инфекции?
- женщинам во время подготовки к беременности
- беременным
- новорожденным для диагностики врожденного инфицирования
Дополнительная справка: если анализы сданы во время беременности
- IgM методом иммуноблот
- IgM методом иммуноблот
Основные сведения о цитомегаловирусе (ЦМВ)
ЦМВ человека относится к вирусам, вызывающим схожие заболевания у различных животных. Все эти заболевания связаны с появлением характерных увеличенных клеток - отсюда и название цитомегаловирус (цито - клетка, мегало - большая). Вирус может размножаться в различных клетках организма человека, но предпочтительно этими клетками являются фибробласты (клетки соединительной ткани).
В добавок к тому, что ЦМВ вызывает тяжелые врожденные дефекты, он может привести к целому ряду заболеваний у детей и взрослых.
Существует три основных клинических вида цитомегаловируса:
- Генитальная ЦМВ инфекция может привести к гепатоспленомегалии (увеличению печени и селезенки), ретиниту (воспаление сетчатки), появлению сыпи и поражению центральной нервной системы.
- У около 10 процентов детей и взрослых первичная цитомегаловирусная инфекция вызывает мононуклеозный синдром с лихорадкой, общим недомоганием, атипичным лимфоцитозом и фарингитом.
- Пациенты с трансплантантатами и ВИЧ-инфицированные люди могут заболеть угрожающим жизни заболеванием, которое охватывает легкие, желудочно-кишечный тракт, сетчатку, печень и центральную нервную систему.
Существует предположение, что вирус обладает онкогенным эффектом и в редких случаях может трансформировать фибробласты.
Подробнее о цитомегаловирусе (ЦМВ)
Эпидемиология цитомегаловирусной инфекции (ЦМВ)
Цитомегаловирус распространен по всему миру, но проживание в плохих социальных условиях и не соблюдение правил личной гигиены сильно способствует передаче микроба. Часто встречаются инфекции у новорожденных и маленьких детей. Вирус можно обнаружить в молоке, слюне, фекалиях и моче. Была прослежена передача вируса от маленького ребенка к его беременной матери, и затем к развивающемуся плоду. К счастью, вирус плохо передается при случайных контактах, так как для его передачи необходимо время. ЦМВ часто передается половым путем, его выделяют из семени или цервикальной слизи. Однажды заразившись, человек, возможно, будет носителем данного вируса в течение всей жизни.
Заболевания, вызываемые ЦМВ, и их клинические проявления
Генитальная цитомегаловирусная инфекция (ЦМВ)
Инфекции у плода варьируются от легких форм до тяжелых и диссеминированных. Петехии (точечные кровоизлияния), гепатоспленомегалия и желтуха - наиболее часто встречаемые проявления. Микроцефалия с (или без) церебральной кальцификации, внутриматочная задержка роста и преждевременное развитие встречаются (что это такое. ) в 30-50 процентах случаев. Лабораторные аномалии включают повышение уровня аланинаминотрансферазы, тромбоцитопению (уменьшенное число тромбоцитов), гипербилирубинемию (повышение уровня билирубина в крови), гемолиз (разрушение клеток крови) и увеличение уровня белка спинномозговой жидкости. Прогнозы для новорожденных с тяжелыми формами заболевания весьма печальны: процент смертности очень велик, а те, кому удается преодолеть болезнь, в будущем встречаются с трудностями в интеллектуальном развитии и развитии слуха.
Зачастую генитальный цитомегаловирус никак не проявляется у новорожденных, а потому не лечится своевременно, что приводит к отклонениям у таких детей в различных системах, которые проявляются в течение первых лет их жизни.
Перинатальная ЦМВ инфекция
Новорожденные могут заразиться ЦМВ при прохождении родового канала или при последующем контакте с материнским молоком или другими выделениями. Огромное количество случаев инфицирования новорожденных протекает асимптоматически. Однако длительная интерстициальная пневмония связана с цитомегаловирусом. Иногда она сопровождается присоединением других инфекций, таких как Chlamidia trachomatis или Ureaplasma urealyticum. Медленное набирание веса, аденопатия, сыпь, гепатит, анемия и атипичный лимфоцитоз также могут сопутствовать заболеванию.
Мононуклеозный синдром
Этот синдром возникает у 10 процентов первично зараженных людей, у оставшихся первичная инфекция протекает бессимптомно. Для пациентов с этим синдромом характерно наличие лихорадки, общего недомогания, атипичного лимфоцитоза и, в редких случаях, цервикальной аденопатии или гепатита.
Большинство пациентов выздоравливают без последствий, хотя послевирусная астения может продолжаться в течение нескольких месяцев.
ЦМВ и трансплантация органов
Считается, что ЦМВ является одним из основных патогенов, осложняющих трансплантацию органов. У пациентов, которым пересаживают почку, сердце, легкие и трансплантаты печени, ЦМВ вызывает множество синдромов, включающих лихорадку и лейкопению, гепатит, пневмонит, эзофагит, гастрит, колит и ретинит. Период максимального риска находится между первым и четвертым месяцами после трансплантации.
ЦМВ у людей с поражениями иммунной системы.
Цитомегаловирус признан важным паразитом у ВИЧ-инфицированных людей, у которых он вызывает ретинит или диссиминированные (охватывающие весь организм) заболевания. Хотя случаи серьезных ЦМВ заболеваний снизились, установление высокоактивного режима приема антиретровирусных препаратов иногда вызывает острые вспышки ЦМВ-ого ретинита в течение первых нескольких недель терапии.
Диагностика цитомегаловируса
Диагностику ЦМВ инфекции невозможно убедительно провести только по клиническим проявлениям. Необходимо выделение вируса или определение цитомегаловирусных антигенов или ДНК из клинических образцов. Кроме того, важно проследить рост уровня антител в крови. Вирус легко определяется в культуре фибробластов. Если содержание вируса велико, что зачастую имеет место при генитальной ЦМВ инфекции, характерные изменения в клетках будут видны в течение нескольких дней. Но если содержание вируса мало, как при цитомегаловирусном мононуклеозе, такая диагностика может занять несколько недель. Многие лаборатории применяют метод, включающий в себя центрифугирование и определение антител к раннему ЦМВ- антигену. Такое исследование может дать результат раньше, чем метод культур.
Группа ToRCH-инфекций объединяет заболевания, заражение которыми в период беременности представляет серьёзную угрозу для плода издоровья будущего ребёнка.
Аббревиатура ToRCH составлена из первых букв названий болезней:
- токсоплазмоз (Toxoplasmosis);
- краснуха (Rubella);
- цитомегаловирус (Cytomegalovirus);
- герпес (Herpes).
Все ToRCH-инфекции широко распространены. Перечисленными заболеваниями можно заболеть независимо от пола и возраста. Это совершенно разные болезни. Выделение их в отдельную группу обусловлено лишь одним: первичное заражение любой из ToRCH-инфекций во время беременности способно привести к смерти плода или сделать будущего ребенка инвалидом. Поэтому гинекологи обращают на них особое внимание, и женщине, планирующей беременность, обязательно надо выяснить, инфицирована она возбудителями этих заболеваний или нет - от этого будут зависеть ее дальнейшие действия.
Для этого необходимо пройти скрининг на ToRCH-инфекции, то есть сдать анализы, позволяющие выявить возбудителей данных заболеваний.
Токсоплазмоз (To в аббревиатуре ToRCH-инфекции)
Токсоплазмоз — заболевание, которое вызывается внутриклеточным паразитом — токсоплазмой.
![Изображение 1: ТoRCH-инфекции - клиника Семейный доктор]()
Токсоплазма живет и размножается в организме домашней кошки. Вместе с кошачьими испражнениями она попадает во внешнюю среду, где может сохраняться месяцами. Это приводит к заражению токсоплазмой других видов животных и птицы. Токсоплазма попадает в их мышечные ткани и таким образом оказывается в мясе, которое потребляет человек. Надлежащая термическая обработка убивает токсоплазму, но если мясо плохо прожарено или недоварено, токсоплазма сохраняется.
Другой путь заражения токсоплазмой — через грязные руки. Поэтому с токсоплазмозом обычно сталкиваются ещё в детстве.
Если с иммунитетом всё в порядке, токсоплазмозом можно переболеть, и даже не знать об этом. Обычно именно так это и происходит: первичное заражение протекает без явных симптомов. Считается, что в России в скрытой форме токсоплазмоз встречается у 30% населения. От человека к человеку токсоплазмоз не передается.
Токсоплазмоз представляет опасность, в основном, для плода. Если первичное инфицирование происходит во время беременности, плод может погибнуть, или ребенок рождается больным – с поражением печени, селезенки, лимфатических узлов и центральной нервной системы.
Краснуха (R в аббревиатуре ToRCH-инфекции)
![Изображение 2: ТoRCH-инфекции - клиника Семейный доктор]()
Краснуха передается от человека к человеку, как правило, воздушно-капельным путем. Основными проявлениями краснухи являются мелкая розовая сыпь по всему телу и повышение температуры до 38° C (наблюдается чаще у взрослых).
Краснухой чаще всего болеют в детстве, это классическая «детская» инфекция. В детском возрасте болезнь обычно переносится легко. У взрослых краснуха протекает, как правило, значительно тяжелее.
Краснуха опасна для плода, особенно в первом триместре беременности. Она поражает нервную ткань, ткани глаза, сердце ребенка и может привести к его смерти. На поздних сроках беременности опасность гораздо меньше.
Краснуха по-своему коварна. У человека, заболевшего краснухой, еще может не быть никаких симптомов (внешних проявлений) заболевания, а он уже заразен. Поэтому нельзя гарантировать, что вам удастся уберечься от краснухи, лишь избегая контактов с теми, кто уже очевидно болен этой болезнью.
Цитомегаловирус (C в аббревиатуре ToRCH-инфекции)
![Изображение 3: ТoRCH-инфекции - клиника Семейный доктор]()
Цитомегаловирус был обнаружен только в XX веке. Инфекция передается половым путем, с кровью, через слюну (например, при поцелуях), а также от матери к ребенку во время грудного вскармливания. В настоящее время считается, что около 80% женщин детородного возраста являются носителем этой инфекции.
В большинстве случаев цитамегаловирус находится в «спящем» состоянии. Иногда инфекция проявляется в виде обычной простуды, но чаще никаких симптомов заболевания не наблюдается. И только при значительном снижении иммунитета возникает угроза перехода заболевания в острую форму.
Для плода наибольшую опасность представляет первичное заражение цитамегаловирусом. Особенно опасно заразиться в первом триместре. Это может привести к недоразвитию или водянке головного мозга ребенка, желтухе, увеличению печени и селезенки, развитию пороков сердца и врожденных уродств.
Герпес (H в аббревиатуре ToRCH-инфекции)
![Изображение 4: ТoRCH-инфекции - клиника Семейный доктор]()
Сегодня известно несколько типов вируса герпеса. Наиболее часто встречаются герпес I-го и герпес II-го типов. Герпес I-го типа проявляется как «простуда на губе» - в виде характерных высыпаний на лице и слизистой рта. Герпес II-го типа – это генитальный герпес, для которого характерны высыпания на половых органах.
Герпес передается различными путями, в том числе бытовым (при непосредственном контакте), воздушно-капельным и др. Однако типично заражение герпесом половым путем.
По некоторым оценкам, герпес встречается у 90% населения нашей планеты. Вирус может годами находиться в латентном («спящем») состоянии, проявляясь только в периоды ослабления иммунитета.
Первичное заражение герпесом во время беременности для плода очень опасно: на ранних сроках инфекция может привести к выкидышу, во второй половине беременности может стать причиной появления врожденных аномалий, таких как микроцефалия, патология сетчатки, пороки сердца.
ToRCH-инфекции и беременность: как обрести уверенность и безопасность?
Заботиться о защите своего будущего ребенка от ToRCH-инфекций надо начинать еще на этапе планирования беременности. Прежде всего, следует пройти диагностику ToRCH-инфекций и выяснить, подверглись ли вы уже инфицированию или нет.
Если в Вашей крови будут выявлены антитела к какой-либо ToRCH-инфекции, это значит, что Ваш организм уже боролся с данной болезнью и выработал к ней специфический иммунитет.
Если вы уже переболели токсоплазмозом или краснухой (в организме присутствуют антитела к возбудителям этих болезней), повторное заболевание вам не грозит.
Если антител к токсоплазме не обнаружится, от вас потребуется повышенная бдительность: надо будет тщательно соблюдать правила гигиены, следить за тем, чтобы мясо, которое вы собираетесь есть, прошло должную термическую обработку, держаться от кошек подальше.
При отсутствии антител к краснухе вам могут порекомендовать сделать прививку. Прививка от краснухи обеспечивает иммунитет на длительный срок (до 20 лет). Однако, если вы уже забеременели, прививку делать нельзя.
Если анализы показали, что в организме присутствуют цитомегаловирус или вирус герпеса, но они находятся в «спящем» состоянии, прямой угрозы для будущего ребенка нет. Если вы являетесь носителем этих инфекций и вынашиваете ребенка, вам, прежде всего, надо заботиться о поддержании и укреплении иммунитета, что позволит избежать обострений заболевания. Если обострение всё же произошло, назначается лечение антивирусными препаратами и иммуномодуляторами.
Отсутствие антител к цитомегаловирусу и вирусу герпеса означает, что во время беременности возможно первичное заражение, а значит, в этот период надо особенно внимательно относиться к своему здоровью и контактам с окружающими людьми.
Оставьте телефон –
и мы Вам перезвонимМетоды диагностики ToRCH-инфекций
Для диагностики ToRCH-инфекций Вы можете обратиться в АО «Семейный доктор». Наиболее удобной формой диагностики является лабораторный профиль «Диагностика комплекса ToRCH-инфекций», который включает в себя серологические исследования на предмет выявления антител ко всем возбудителям, входящим в комплекс ToRCH-инфекций.
Тесты на авидность позволят определить, как давно в организме присутствует та или иная инфекция.
Врачи-гинекологи «Семейного доктора» проконсультируют по результатам анализов и дадут рекомендации, как обеспечить безопасность плода, выносить и родить здорового ребенка.
Серологический анализ позволяет выявить антитела к возбудителю конкретного заболевания. Для того, чтобы убедиться в отсутствии ToRCH-инфекций, необходимо провести анализы на антитела к каждому из четырёх заболеваний, входящих в данную группу.
Наиболее опасно заражение ToRCH-инфекциями непосредственно в период беременности. ToRCH-инфекции широко распространены, поэтому, если присутствие соответствующих антител в крови обнаружено, это ещё не означает, что заражение произошло уже во время беременности. Для того, чтобы узнать, не было ли инфицирования именно в этот период, проводится определение авидности (оценки прочности связи между антителом и антигеном). В начале заболевания связь эта довольно слабая. Со временем иммунная система вырабатывает антитела с более высокой авидностью. Поэтому обнаружение низкоавидных антител может свидетельствовать о сравнительно недавнем инфицировании.
Чтобы точно продиагностировать заболевание, запишитесь на прием к специалистам сети «Семейный доктор».
Читайте также: