Кавинтон попал под кожу что делать
Обновлено: 25.04.2024
Поликлиника №5, Ярославль
Полимодальность эффектов препарата кавинтон: экспериментальные и клинические доказательства
Журнал: Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски. 2010;110(9‑2): 8‑12
Касаткин Д.С. Полимодальность эффектов препарата кавинтон: экспериментальные и клинические доказательства. Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски. 2010;110(9‑2):8‑12.
Kasatkin DS. Polymorphic effects of cavinton: experimental and clinical evidence. Zhurnal Nevrologii i Psikhiatrii imeni S.S. Korsakova. 2010;110(9‑2):8‑12. (In Russ.).
Поликлиника №5, Ярославль
Поликлиника №5, Ярославль
За последние 15 лет данные, накопленные в области нейронаук, привели к полной реорганизации знаний в этой области и к иному пониманию функционирования нервной системы. Изменения в фундаментальных представлениях о базовых физиологических и патологических процессах, протекающих в нервной ткани, заставили по-новому взглянуть на клинику, патогенез и лечение многих неврологических заболеваний.
Независимо от причинного фактора, механизмы повреждения нейронов могут носить специфический и неспецифический характер. К неспецифическим механизмам альтерации относятся нарушения энергообеспечения нейронов; расстройства синтеза белка; дисбаланс ионов и жидкости в нейронах; повреждение мембран в результате перекисного окисления липидов; апоптоз. Патогенетическую основу большинства форм специфического повреждения нейронов составляют нарушения специфических для нейрона процессов метаболизма нейромедиаторов (синтеза, аксонального транспорта, секреции, удаления и утилизации). Механизмы повреждения нейронов тесно взаимосвязаны и нередко потенцируют друг друга, образуя порочный круг, в связи с чем для лечения неврологических расстройств перспективным будет препарат, препятствующий возможно большему числу механизмов альтерации нейронов, при этом положительно влияющий на уровень мозгового кровотока и микроциркуляции. Одним из лекарственных средств, обладающих подобными эффектами, является винпоцетин (кавинтон) [1].
Основным показанием для применения винпоцетина являются хронические расстройства мозгового кровообращения [1, 2], однако активно обсуждается вопрос об использовании препарата как при острых нарушениях мозгового кровообращения [3], так и при нейродегенеративных заболеваниях (болезнь Альцгеймера) [4, 5].
Основой сосудистого эффекта винпоцетина (кавинтона) является воздействие на метаболизм циклических нуклеотидов в клетках гладкой мускулатуры сосудистой стенки путем торможения Са 2+ /кальмодулин-зависимой фосфодиэстеразы 1-го типа [7]. Этот эффект приводит к преобладанию цАМФ над цГМФ, что способствует релаксации сосудов головного мозга, снижает агрегацию тромбоцитов [8] и патологически увеличенную вязкость крови [9], нормализует деформируемость эритроцитов [10, 11].
Важным представляется тот факт, что винпоцетин (кавинтон) избирательно повышает мозговой кровоток 14, уменьшает сопротивление мозговых сосудов без воздействия на системное кровообращение (практически не влияя на артериальное давление, минутный объем, частоту сердечных сокращений, общее периферическое сопротивление) [15, 16]. Он не вызывает феномена «обкрадывания», а наоборот, улучшает кровоснабжение пораженной области, причем кровоток в интактной зоне мозга сохраняется неизменным 16.
При пероральном приеме винпоцетина (кавинтона) у пациентов пожилого и старческого возраста с явлениями сенильной деменции в течение 3 нед в дозе 15-30 мг в сутки параллельно с увеличением концентрации АТФ в эритроцитах наблюдается усиление сродства гемоглобина к кислороду и его способности отдавать кислород [19]. Препарат активизирует дефицитный обмен веществ и увеличивает энергетическую емкость мозга путем улучшения утилизации глюкозы, кислорода и темпов синтеза АТФ. При помощи позитронно-эмиссионной томографии было показано увеличение доставки глюкозы (захвата и высвобождения) через гематоэнцефалический барьер [20, 21].
Нейропротективные эффекты винпоцетина (кавинтона), вероятнее всего, опосредованы несколькими механизмами. Ингибирование вольтажзависимых натриевых каналов на фоне приема винпоцетина в условиях эксперимента приводит к замедлению накопления натрия в клетке, снижая тем самым токсический эффект оксидантного стресса при аноксии и повреждения при реперфузии 24. Антиоксидантный эффект препарата проявляется вследствие снижения активности перекисного окисления липидов в синаптосомах [25, 26]. В условиях экспериментальной ишемии винпоцетин снижал размеры очага некроза нервной ткани на 60% [22]; по антиоксидантной активности в исследованиях на животных винпоцетин достоверно превосходил пентоксифиллин и пирацетам [27, 28].
Также на фоне приема винпоцетина отмечено снижение эксайтотоксичности и апоптоза за счет блокирования NMDA-рецепторов и снижения поступления ионов Ca 2+ в клетку 30.
Дополнительным важным фактором является усиление структурной динамики дендритов клеток коры в виде увеличения и удлинения шипиков, что приводит к увеличению пластичности нейронов, особенно в области гиппокампа [32, 33], и, вероятно, лежит в основе усиления когнитивных функций на фоне приема винпоцетина [34]. Эффект, по-видимому, является следствием блокирования поступления ионов кальция и натрия в клетку и усиления активности элементов цитоскелета нейронов [35, 36].
Помимо сосудистого и нейропротективного эффекта винпоцетин обладает влиянием на нейромедиаторные системы мозга, усиливая внутримозговой обмен норадреналина и серотонина [37] и стимулируя восходящую норадренергическую систему, в частности голубое ядро ствола [38].
Исследования эффективности винпоцетина (кавинтона)
На настоящий момент проведено 7 двойных слепых плацебо-контролируемых исследований, продемонстрировавших эффективность винпоцетина (кавинтона).
Впервые исследование винпоцетина (кавинтона) в сравнении с плацебо было проведено G. Lipani в 1984 г. [39]. В исследование были включены 44 пациента с хронической ишемией мозга, транзиторными ишемическими атаками и умеренными когнитивными расстройствами, распределенных в 2 группы: 22 больных получали винпоцетин в дозе 30 мг в сутки в течение 1 мес, затем 15 мг в сутки в течение последующих 2 мес, другие 22 пациента в течение 3 мес получали плацебо. Оценка результатов проводилась с использованием шкалы общего клинического впечатления (Clinical Global Impression -CGI), шкалы клинической гериатрической оценки Сандоз (Sandoz Clinical Assessment Geriatric Scale - SCAG), краткого опросника психического статуса (Mini Mental State Examination - MMSE), показателей неврологического статуса. Были получены достоверные отличия показателей в группе винпоцетина по сравнению с плацебо на 30-й и 90-й дни исследования.
В исследование M. Peruzza и M. DeJakobis [40] были включены 40 пациентов с дегенеративными заболеваниями центральной нервной системы, разделенных на 2 группы по 20 человек. Дизайн и методы оценки были аналогичны исследованию
Аналогичное по дизайну и числу пациентов (n=40) исследование было проведено Е. Manconi и соавт. [41]. В конечной точке исследования у 87% больных основной группы, лечившихся винпоцетином, наблюдалось снижение балла по шкале CGI против 11% в группе плацебо (p<0,001); при оценке неврологического статуса выраженные улучшения наблюдались у 59% больных, получавших винпоцетин, против 6% в группе плацебо (p<0,001). Аналогичные различия были получены по шкалам SCAG и MMSЕ.
В исследование Е. Fenzl и соавт. [42] вошел 201 пациент с умеренным психоорганическим синдромом ишемического и нейродегенеративного характера; 105 больных основной группы получали винпоцетин в дозе 60 мг в сутки в течение 1 года, 96 больных группы сравнения получали плацебо. В оценке результатов использовались шкала CGI, короткий синдромальный тест (Syndrome short test - SST) и индекс активности (Condition-index - CI). Показатели CGI через 6 и 12 мес лечения были достоверно ниже в группе винпоцетина, а индекс активности достоверно выше. Клиническое улучшение в неврологическом статусе через 12 мес наблюдалось у 86,7% пациентов основной группы против 54,2% в группе плацебо (p<0,001).
Исследование R. Balestreri и соавт. [43] соответствовало по дизайну ранее проведенным исследованиям 40, существенным отличием данного исследования явилось включение только пациентов с хронической ишемией мозга (n=80). Снижение балла по шкале CGI через 90 дней лечения винпоцетином составило 44% против 13% в группе плацебо (p<0,001). Улучшение наблюдалось также по шкалам SCAG и MMSЕ, при этом показатели были достоверно выше в основной группе.
В исследовании Н. Fuchs и H. Erzigkeit [44] было проведено сравнение 3 групп пациентов с умеренным психоорганическим синдромом без дифференцировки по этиологии (n=165): 2 основных групп, получавших винпоцетин в дозах 60 и 30 мг в сутки (55 и 56 больных соответственно), и группы плацебо (n=54). Длительность исследования составила 16 нед. При оценке результатов использовались шкалы CGI, SST и CI. После 16 нед лечения показатель CGI был достоверно ниже в обеих основных группах по сравнению с группой плацебо (p<0,001).Уровень CI достоверно не отличался.
L. Blaha и соавт. [45] провели исследование в 4 параллельных группах (n=213), в течение 12 нед получавших винпоцетин в дозах 60, 30 и 15 мг в сутки и плацебо (53, 55, 50 и 55 больных соответственно). В дополнение к шкалам CGI и SST была использована шкала депрессии (Erlangen depression scale - EDS). Через 3 мес терапии показатель CGI был достоверно ниже во всех группах, получавших винпоцетин, по сравнению с плацебо (p<0,001). Показатель по шкале EDS в группах лечения был ниже, чем в группе плацебо, однако достоверность отличий имела пороговые значения.
Результаты всех 7 исследований обобщены в мета-анализе, включившем данные о 731 пациенте [46].
Отдельно были проанализированы данные имевших сходный дизайн итальянских исследований (n=204) по показателю CGI, при этом было получено достоверное снижение на 1,22 балла (доверительный интервал, ДИ - 1,01-1,43; p<0,001) в основной группе по сравнению с группой плацебо на 30-й день и на 1,1 балла (ДИ - 0,89-1,31; p<0,001) на 90-й день исследования.
Эффективность винпоцетина (кавинтона) доказана также в ряде открытых и сравнительных исследований.
A. Szobor и M. Klein [47] исследовали эффективность винпоцетина в группе пациентов с церебральным атеросклерозом, гипертонической энцефалопатией, хронической недостаточностью мозгового кровообращения. В исследование были включены 100 пациентов, которые получали винпоцетин в дозе 30-45 мг в сутки перорально и в виде комбинации (перорально и инфузионно). По результатам исследования выявлено значимое улучшение клинического состояния в исследуемой группе.
В исследовании Е. Burtsev и соавт. [2], опубликованном в 1992 г., подведены итоги 10-летнего исследования применения винпоцетина у пациентов с различными формами цереброваскулярных заболеваний. Обзор включил в себя данные 967 пациентов. Наилучший результат получен у пациентов с ранними формами хронических заболеваний (вегетативная дисфункция, ранние стадии дисциркуляторной энцефалопатии).
Исследования безопасности винпоцетина (кавинтона)
В открытом клиническом исследовании, проведенном T. Perényi и соавт. [48], 100 пациентов получали винпоцетин в дозе 15 мг в сутки в течение 1 года, при этом ЭКГ-мониторинг не выявил значимых изменений и случаев аритмии. Аналогичные результаты имело и исследование, проведенное в Японии в рамках III фазы клинического испытания винпоцетина, включившее около 8000 пациентов в 1420 центрах [49].
Для уточнения аритмогенного влияния винпоцетина C. Farsang и соавт. [50] было проведено 2-летнее двойное слепое рандомизированное плацебо-контролируемое исследование, включившее данные о 85 пациентах, страдавших различными хроническими заболеваниями сердца. По результатам исследования был сделан вывод, что ни винпоцетин, ни плацебо не влияли на частоту сердечных сокращений, длительность интервалов PQ, QRS, QT и ST, не вызывали экстрасистол и не изменяли формы пика Т, т.е. длительный пероральный прием винпоцетина не приводит к возникновению аритмий.
В 1998 г. по результатам мета-анализа венгерской и международной литературы было установлено, что ни пероральное, ни внутривенное лечение винпоцетином не оказывало какого-либо значимого эффекта на сердечный ритм и проводимость даже при наличии факторов риска аритмии [46].
Тем не менее в случаях наличия хронических заболеваний сердца (особенно при гипертрофии левого желудочка, ишемии или малой фракции выброса левого желудочка), при электролитных нарушениях (гипокалиемия, гипомагниемия), удлинении интервала QT, применении лекарственных препаратов, являющихся блокаторами калиевых каналов (амиодарон, соталол) или ингибиторами цитохрома Р450 (циметидин, кларитромицин, флуоксетин и др.), парентеральную терапию винпоцетином следует проводить под контролем ЭКГ. Поскольку винпоцетин обычно применяют в повышающихся дозах (начиная с 20-25 мг и доходя до 60 мг в сутки), рекомендуется проведение ЭКГ после первой инфузии и после достижения максимальной дозы. В случае удлинения интервала QT (что в норме бывает редко) следует рассмотреть возможность снижения дозы кавинтона или отмены препарата.
Важным аспектом применения винпоцетина (кавинтона) является отсутствие влияния на функцию печени, в том числе на систему ферментов, метаболизирующих лекарственные вещества, а также отсутствие влияния на нормальные и патологически измененные функции почек [46]. В специально проведенных исследованиях не обнаружено взаимодействия кавинтона с бета-блокаторами (хлоранолол, пиндолол), клопамидом, метилдопой, дигоксином и гипотиазидом. Препарат может быть использован в обычных дозах у пациентов с почечной и печеночной недостаточностью; у него отсутствует кумулятивный эффект.
Кавинтон для инфузий химически несовместим с гепарином, поэтому эти препараты нельзя вводить в одном шприце, хотя возможно последовательное введение.
Е.И. Чукановой в 2003 г. было проведено фармакоэкономическое исследование нейрометаболических препаратов [51], включившее данные о 532 пациентах с дисциркуляторной энцефалопатией I и II стадии. Показано, что применение кавинтона способствует регрессу или стабилизации прогрессирования неврологических расстройств, при этом препарат имеет хороший профиль переносимости, стоимость курсового лечения и коэффициент «затраты/эффективность» оказались наиболее благоприятными по сравнению с другими препаратами.
Таким образом, несмотря на длительную историю применения кавинтона в широкой клинической практике (более 30 лет), интерес к изучению механизмов его действия среди биохимиков, молекулярных биологов, клиницистов не угасает, при этом с каждым годом выявляются ранее неизвестные свойства препарата, открывающие новые перспективы его применения. Именно множественность точек приложения кавинтона в сочетании с высокой клинической эффективностью и безопасностью применения позволяют ему длительно и успешно конкурировать с постоянно возрастающим числом новых лекарственных средств на фармакологическом рынке.
Что делать при попадании лекарств под кожу? Первая помощь при экстравазации
Лечение и первая помощь при экстравазации - попадании лекарств под кожу. Объем вмешательства зависит от стадии экстравазации, вводимого раствора и специфических антидотов. Схема лечения повреждений 3-4-й стадии не разработана. При отсутствии рандомизированных контролируемых исследований некоторые организации опубликовали протоколы лечения, основанные на собственном опыте, серии случаев и единичных достоверных данных.
1. Во всех случаях экстравазации - попадании лекарств под кожу выполняют следующее:
а. Немедленно прекращают внутривенную инфузию.
б. Убирают стягивающие повязки, которые могут действовать как жгут (например, при фиксации конечности).
в. Придают конечности возвышенное положение для уменьшения отека.
г. Местно применяют согревающие и охлаждающие пакеты, что спорно. Под действием тепла происходит местная вазодилатация, способствующая реабсорбции инфильтрированных растворов. Однако, согласно данным литературы, влажные согревающие пакеты могут вызывать мацерацию кожи.
2. Экстравазация 1-й и 2-й стадии:
а. Убирают внутривенный катетер.
б. Выбирают антидот.

Стадии экстравазации - попадания лекарств под кожу
3. Экстравазация 3-й и 4-й стадии:
а. Оставляют внутривенный катетер на месте и с помощью шприца объемом 1 мл аспирируют как можно больше введенной жидкости.
б. Убирают катетер, за исключением случаев, когда необходимо введение антидота.
в. Решают вопрос об использовании гиалуронидазы или антидота.
г. Метод многократных пункций. После экстравазации кислыми или гиперосмолярными растворами развивается напряженный отек с побледнением кожи над местом инфильтрации. Использование стилета после соблюдения мер асептики дает возможность свободно вытекать инфильтрированному раствору, при этом уменьшаются отек и вероятность развития некроза. Затем накладывают повязку, смоченную физиологическим раствором, в целях улучшения дренирования.
д. Промывание физиологическим раствором. Некоторые авторы рекомендуют использовать метод промывания физиологическим раствором подкожных тканей. После обработки и инфильтрации участка 1% лидокаином подкожно вводят 500-1000 ЕД гиалуронидазы. Затем выполняют четыре маленьких разреза скальпелем по периферии участка инфильтрации. Проводят промывание. Вводят физиологический раствор через катетер, установленный подкожно в один из разрезов, жидкость изливается через другой разрез. Образовавшееся вздутие массирующими движениями выдавливают в сторону разреза для облегчения удаления веществ, излившихся из сосуда.
4. Специфические антидоты лекарств:
а. Фентоламин:
(1) Применяют при лечении повреждений в результате экстравазации вазопрессоров, например допамина и адреналина, которые вызывают повреждение тканей за счет интенсивной вазоконстрикции и ишемии.
(2) Эффект развивается практически сразу. Наиболее эффективен в течение часа, но можно вводить до 12 ч. Биологический период полувыведения фентоламина при подкожном введении составляет менее 20 мин.
(3) Механизм действия: конкурентная блокада а-адренорецепторов, приводящая к расслаблению гладкомышечных клеток и гиперемии.
(4) Для новорожденных дозы не установлены. Они зависят от размера повреждения и массы тела новорожденного.
(5) Рекомендуемые дозы варьируют в пределах от 0,01 мг/кг на одно введение до 5 мл раствора с концентрацией 1 мг/мл.
(6) Раствор в концентрации 0,5-1,0 мг/мл вводят подкожно в инфильтрированную область после удаления внутривенного катетера.
(7) Меры предосторожности. Могут возникать гипотензия, тахикардия и нарушения ритма; следует вводить крайне осторожно у недоношенных; повторно вводить в малых дозах.
б. Нитроглицерин местно:
(1) Эффективен при лечении повреждений, обусловленных экстравазацией допамина.
(2) Механизм действия: расслабление гладких мышц сосудов.
(3) Применение: 2% нитроглицериновая мазь из расчета 4 мм/кг на пораженную область, возможно повторное применение каждые 8 ч, если перфузия тканей не улучшается.
(4) Также используют трансдермальные пластыри.
(5) Меры предосторожности. Всасывание через кожу может привести к гипотен-зии.
в. Тербуталин:
(1) Эффективен в лечении периферической ишемии, возникшей вследствие экс-травазации вазопрессоров у взрослых и детей старшего возраста; о применении в неонатологической практике публикации отсутствуют.
(2) Механизм действия: периферическая вазодилатация в результате активации бета2-адренорецепторов.
(3) Вводят подкожно в концентрации 0,5-1,0 мг/мл; дозы у взрослых варьируют от 0,5 до 1 мг.
5. Лечение раны после экстравазации - попадания лекарства под кожу:
Цель лечения раны у новорожденных с частичной или полной утратой кожи заключается в достижении заживления первичным или вторичным натяжением без образования рубцов, контрактур и проведения оперативного вмешательства. Используют разные схемы лечения в разных лечебных учреждениях.
а. Промывают поврежденную область стерильным физиологическим раствором.
б. На пораженный участок наносят сульфадиазиновую мазь и меняют повязки каждые 8 ч, осторожно очищая раневую поверхность, повторно наносят мазь. Сульфонамиды повышают риск ядерной желтухи, поэтому противопоказаны новорожденным в первые 30 дней жизни.
в. Аморфные гели на водяной основе, содержащие полимер карбоксиметилцеллюлозы, пропиленгликоль и воду, сохраняют рану влажной и облегчают ее заживление. Их выпускают в форме гелей и пленок, которые можно накладывать прямо на раневую поверхность и оставлять на месте при повторных перевязках. Гель легко удаляется с помощью физиологического раствора, его меняют каждые 3 дня. Более частую смену повязок проводят при избыточной экссудации.
г. Влажно-высыхающие повязки с физиологическим раствором и повязки с повидонйодом также эффективны. Обильное нанесение повидон-йода на открытую рану не рекомендуют у новорожденных с очень низкой массой тела, поскольку всасывание йода может угнетать функцию щитовидной железы.
д. Эффективность применения антибактериальных мазей не доказана.
е. Заживление раны оценивают каждый день. Для заживления необходимо от 7 дней до 3 мес.
ж. Если рана находится на сгибательной поверхности, выполняют пассивные упражнения в пределах физиологического объема при каждой смене повязки в целях предотвращения контрактур.
6. Консультация пластического хирурга:
а. Проводят при повреждениях всей толщины кожи и значительных по площади отдельных повреждениях, обусловленных экстравазацией.
б. Могут потребоваться ферментативная или хирургическая обработка раны или трансплантация кожи.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
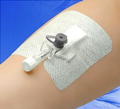
Вероятность инфильтрации и экстравазального введения значительно уменьшается, если медицинская сестра понимает причины этих явлений, правильно выбирает вену для пункции или катетеризации и оборудование, а также тщательно следит за пациентом.
В соответствии со стандартами сестринской практики, инфильтрацией называется непреднамеренное введение раствора лекарственного средства в ткани, окружающие вену. Такие лекарственные средства могу вызывать раздражение окружающих тканей, если они окажутся в подкожной клетчатке, если же они выливаются на кожу, может развиваться контактный дерматит. Экстравазация — это введение значительного количества раствора лекарства мимо вены, и в некоторых случаев она сопровождается даже тканевыми некрозами.
В связи с этим, надо помнить, что некоторые растворы лекарственных средств не предназначены для ведения в периферические вены. Инфильтрация и экстравазация возникают чаще всего тогда, когда катетер не полностью находится в просвете вены, или же в стенке вены есть разрыв, который способствует утечке раствора. Причины этого явления:
- Катетер введен в вену неправильно;
- Вена повреждена, вокруг имеется отек клетчатки, который препятствует правильному току крови, раствор задерживается и вытекает в окружающие ткани;
- Внутри вены или вокруг катетера формируется тромб, который задерживает раствор, он выходит в окружающие ткани. Также при этом развиваются флебит или тромбофлебит;
- Катетер прокалывает или развивает противоположную стенку вены, что также может сопровождаться флебитом или тромбофлебитом;
- Катетер вытягивается из просвета вены при движении пациента или вследствие ненадежной фиксации.
Хотя чаще всего инфильтраты и экстравазаты возникают при инфузии в периферическую вену, эти осложнения могут развиваться и при использовании центральных венозных катетеров и имплантируемых портов. В этом случае последствия могут быть катастрофическими вследствие большого объема используемого раствора, и еще потому, что эти устройства используются для введения концентрированных и вязких растворов.
В большинстве случаев инфильтраты не приводят к тяжелому поражению тканей, но для пациента они очень некомфортны. Также приходится удалять катетер из вены и устанавливать новый, что может уменьшить число потенциально доступных вен, отнимает время и увеличивает затраты.
Самые серьезные последствия наступают, когда вне просвета сосудов оказываются раздражающие растворы, например, содержащие кальций, калий или препараты для химиотерапии. Повреждение тканей может напрямую зависеть от рН раствора: сильно щелочные или кислые растворы вызывают самые настоящие химические ожоги. Значительно концентрированные лекарственные препараты могут даже вызывать некроз тканей.
Степень повреждения при инфильтрации или экстравазации может зависеть от того, как быстро будут предприняты все меры, так как даже небольшое количество жидкости создает компрессию и повреждение. При раннем выявлении и лечении инфильтратов и экстравазатов можно предупредить повреждение нервов и тканей, и предупредить хирургическое вмешательство. Неспособность своевременно распознать эти осложнения может привести к стойкой деформации, и потере функции, даже в том случае, если пациенту будет проведена реконструктивная операция. Часто такие ошибки заканчиваются судебным процессом.
Чтобы избежать проблем, нужно быть настороженным в отношении признаков и симптомов инфильтрации и экстравазации, которые включают в себя:
- «Надутую» кожу, которая выглядит блестящей, натянутой и плотной;
- Отек в месте введения иглы или катетера;
- Холодная наощупь кожа;
- Дискомфорт;
- Замедление или прекращение инфузии;
- Утечка раствора лекарственного препарата вокруг места введения или под повязкой;
- Если над местом инфузии наложить жгут, инфузия не прекращается;
- Нет тока крови по катетеру, если пережать вену и опустить пакет с раствором (наличие крови не исключает инфильтрацию).
Дискомфорт и жжение при инфузии раздражающего или вязкого раствора может указывать на повреждение сосуда. Жалоба на боль в месте установки катетера или иглы в вену — это основной признак того, что нужно быстро вмешиваться. В этом случае необходимо принять следующие меры:
- Прекратить инфузию;
- Если нет противопоказаний, установить катетер в вену на другой руке;
- При инфильтрате — наложить компресс, если произошла экстравазация, особенно хлорида кальция — срочно приглашайте врача.
До введения вязкого, могущего вызвать сужение сосуда, или токсичного раствора лекарственного средства, необходимо знать, какие нейтрализующие вещества (антидоты) применяются при экстравазации и инфильтрации.
Для предотвращения инфильтрации, нужно выбирать подходящую вену. Выбирайте гладкую и упругую вену, которая не похожа на веревку с узлами. Избегайте сгибательных поверхностей суставов, так как здесь смещение катетера происходит особенно часто. Если такое место — единственное, куда можно установить катетер, используйте шину. Если пациент в сознании, инфузия долгая, а ему хочется двигаться, и например, читать книжку, то лучше избегать использования вен кисти.
Чаще всего оптимально катетеризировать вены предплечья, особенно внутренней его части. Кости — это естественная шина, вены достаточно хорошо фиксированы, поэтому вероятность смещения катетера значительно уменьшается.
Начинайте выбирать вену на предплечье так низко, насколько это вообще возможно (не стоит использовать место сделанной недавно венепункции), но не стоит ипользовать вены на внешней поверхности предплечья около запястья, так как там близко проходят нервы. Лучше не использовать вены внутренней части ниже локтя (антекубитальная ямка) — инфильтрацию в этой зоне очень легко просмотреть и она бывает немаленькой. При значительно инфильтрации в антекубитальной ямке жидкость сдавливает важные анатомические структуры и может привести к повреждению нервов и некрозу тканей.
Чтобы раствор лекарственного препарата максимально смешивался с кровью, выбирайте катетер минимально возможного диаметра, это позволит крови смешиваться с инфузатом, и обеспечить его адекватное разведение.
Всегда водите иглу срезом вверх, чтобы уменьшить риск сквозного прокола вены, тщательно фиксируйте катетер, чтобы он не смещался, особенно у детей и пожитых.
После того, как врач установит катетер в центральную вену, или медсестра — периферическую, место пункции проверяют каждые час-два, особенно если проводится длительная инфузия. Убедитесь, что место пункции вены хорошо видно (лучше применять прозрачные заклейки, а не марлевые салфетки).
Регулярно проверяйте, не появилось ли напряжения и отека в месте введения катетера. Спрашивайте пациента, нет ли боли, если говорить он не может, проверяйте место пункции чаще. Если вы заметите инфильтрацию или экстравазацию, сразу же прекращайте инфузию, и проверяйте, что произошло. Если инфильтрат большой, или раствор был раздражающий — немедленно зовите врача. Если катетер остался на месте, можно попробовать шприцом аспирировать часть попавшей в ткани жидкости, также через катетер можно вести антидот.
После удаления катетера больную руку надо держать в приподнятом положении (например, на подушке), и приложить холодный компресс, если это лекарства для химиотерапии — то теплый компресс. Если появляется некроз (обычно через может быть необходимой консультация хирурга.
Как документировать осложнения инфузионной терапии
Во-первых, нужно измерить участок измененных тканей, чтобы потом можно было оценить эффективность лечения. Обязательно нужно отслеживать состояние кожи и мягких тканей, чтобы избежать тяжелых осложнений, также это помогает оценить качество медицинской помощи.
Применение устройств для фиксации конечности, особенно в детской и гериатрической практике, может давать удивительные результаты: частота смещения катетеров может снизиться до нуля, и не будет тяжелых последствий. Соблюдение описанных выше несложных приемов может предотвратить осложнение. Ну а если оно все-таки возникло, то последствия можно сделать минимальными, если быстро и адекватно реагировать на случившееся.
Отдельно — о центральных венозных катетерах и имплантируемых портах
В соответствии с международными стандартами, раствор лекарственного средства, имеющий рН менее 5 и более 9, не должен вводиться через периферические вены. Например, это — ванкомицин (pH, ∼2.4) и фенитоин (pH, ∼12). То же самое касается и растворов, содержащих более 5% гидролизата белков, или 10% глюкозы.
Поскольку экстравазация такого раствора может иметь катастрофические последствия, то все их вводят через центральный венозный катетер или имплантируемый порт. Если приходится однократно вводить такой раствор в периферическую вену, то его вводят через толстый катетер, через боковой порт во время инфузии физиологического раствора, предпочтительнее иметь отдельный катетер для таких целей.
При введении вязкого или раздражающего раствора через центральный венозный катетер, всегда следует проверять обратный ток крови по катетеру, и часто делать это повторно во время инфузии. Если обратного тока крови нет, то это можно указывать на выход катетера из просвета вены, и утечке раствора в окружающие ткани. Также может быть тромбоз катетера — в этом случае срочно останавливайте инфузию и зовите врача во избежание тяжелых последствий.
Иногда врач проводит контрастное исследование под контролем рентгена, чтобы убедиться в проходимости катетера и может растворить тромб.
Если венозный доступ осуществляется через имплантируемый порт, важно выбирать иглу адекватной длины, чтобы она не выскочила из порта, и раствор не ушел бы в окружающую клетчатку. Если же игла окажется слишком длинной, то это может привести к повреждению мембраны порта, в результате чего экстравазация будет происходить уже через мембрану.
Когда инфузия лекарственного средства проводится через имплантируемый порт, нужно часто осматривать место установки порта, как и при работе с периферическим венозным катетером, чтобы своевременно выявить любую утечку или отек подкожной клетчатки рядом с портом. Если пациент жалуется на ЛЮБОЙ дискомфорт, немедленно прекращайте инфузию и посмотрите, что случилось. При подозрении на проблемы с портом — срочно зовите врача. Иногда порт может отсоединяться от катетера, и в этом случае пациенту нужна немедленная операция.
Шкала оценки инфильтравии в месте инфузии (Journal of Infusing Nursing, 2006)
0 баллов — нет никаких симптомов
1 балл — напряженная кожа, отек до 2.5 см в диаметре, холодная наощупь кожа, боль может быть, а может и не быть
2 балла — Кожа натянута, отек от 2 до 12 см в любом направлении, кожа холодная наощупь, боль может быть, а может и не быть
3 балла — кожа напряжена и просвечивает, большой отек — больше 15 см, в любом направлении, кожа холодная наощупь, боль средняя или умеренная, может быть онемение
4 балла — Кожа напряжена, просвечивает, плотная, может быть даже повреждена, обесцвечена, имеется выраженный отек, более 15 см, в любом направлении, отек глубокий, есть нарушения кровотка, боль от умеренной до выраженной, могут быть синяки
К последней, самой тяжелой степени инфильтрации, также относится утечка любого препарата крови, раздражающего или очень вязкого раствора.

Лекарственный препарат, способствующий восстановлению кровоснабжения и питания тканей, расширяющий сосуды. Помогает замедлить развитие возрастных нарушений деятельности головного мозга, вестибулярного аппарата и органов зрения.
Химический состав и лекарственные формы
Активное соединение лекарственного средства — винпоцетин. Оно оказывает вазодилататорное (сосудорасширяющее), антиоксидантное, нейропротекторное действие, стимулирует обменные процессы в тканях, нормализует реологические свойства крови.
Кавинтон производится в двух фармацевтических формах:
Таблетки: в блистерах, белого цвета, с выгравированной надписью Cavinton на поверхности, дозировка активного вещества — 5 мг. Вспомогательные компоненты препарата: диоксид кремния, тальк, стеарат магния, крахмал.
Инфузионный раствор в ампулах по 2 и 5 мл, применяется внутривенно. Помимо винпоцетина содержит дистиллированную воду, аскорбиновую и винную кислоты, сорбитол.
Как действует Кавинтон
Инструкция по использованию лекарственного средства информирует, что винпоцетин относится к разряду церебровазодилатирующих веществ. Он стимулирует метаболизм и питание головного мозга, препятствует развитию атеросклеротических поражений, улучшает поглощение глюкозы и кислорода клетками. Кавинтон способствует улучшению работы надпочечников, помогает обмену норадреналина, серотонина и других гормонов.
Препарат работает избирательно. Воздействует на церебральный объем крови, уменьшает сопротивление сосудистой сети головного мозга. Этот процесс способствует восстановлению циркуляции в участках тканей, подвергающихся ишемии. При этом активность общего кровообращения не изменяется. Частота сердечных сокращений, уровень артериального давления после приема лекарства остаются прежними. Эффект так называемого обратного обкрадывания обеспечивает сохранение жизнеспособности пораженных областей. Кавинтон:
нормализует вязкость крови;
снижает избыточное слипание тромбоцитов;
увеличивает устойчивость клеток к гипоксическому воздействию;
замедляет проникновение аденозина в эритроциты, делая их более эластичными и предотвращая распад.
Таблетки лекарственного средства быстро растворяются в желудке и всасываются в кровь. Действие вещества достигает максимума в течение 1–1,5 ч. Эффективность инъекций несколько выше. В организме препарат не накапливается. Выводится полностью, не образуя метаболитов, вместе с каловыми массами и мочой в течение суток после приема.
Для чего применяют Кавинтон
Препарат устраняет поражение сосудов, восстанавливает кровообращение, микроциркуляцию и нормальный обмен веществ в различных локализациях. Поэтому список его показаний обширен.
вертебро-базилярная недостаточность сосудов головного мозга;
постинсультное состояние: в составе комплексного лечения;
транзиторные ишемические атаки;
энцефалопатии после черепно-мозговых травм, в результате гипертензии;
повреждения различных отделов головного мозга, связанные с нарушением их питания и кровоснабжения;
ухудшение памяти, психические расстройства;
расстройства координации движений;
В офтальмологии Кавинтон применяют для купирования сосудистых нарушений, вызвавших ухудшение зрения и развитие дегенеративных процессов:
при ангиоспазме, дистрофии сетчатой оболочки глазного дна;
атеросклеротических изменениях в капиллярах;
при вторичной глаукоме;
при диабетических поражениях глаз;
при тромбозах и эмболических процессах.
В отоларингологии Кавинтон используют при нарушениях слуха, поражениях вестибулярного аппарата:
осложнениях, вызванных воспалением среднего уха;
различных вазовегетативных патологиях.
Как правильно применять Кавинтон: инструкция
Медикамент разрешен пациентам с 18 лет. Лечение препаратом в таблетках требует длительного назначения. Полный курс составляет от 1 до 8 месяцев в зависимости от вида заболевания. В среднем, для достижения выраженного результата Кавинтон принимают 3–4 месяца подряд:
по 1 таб. трижды в сутки, не разжевывая;
запивать лекарство нужно большим объемом воды;
время приема: через 1–1,5 ч. после еды.
Инфузионный препарат необходимо вводить внутривенно: через шприц или посредством капельниц. Внутримышечное использование средства запрещено.
перед применением Кавинтон разводят в физрастворе из расчета: 20 мл концентрата на 500 мл жидкости;
подготовленный раствор годен к использованию в течение 3 часов;
терапию проводят, вводя 80 капель препарата в минуту.
Точную схему лечения формирует врач с учетом показаний и общего состояния организма пациентов. Отменять Кавинтон необходимо постепенно, поэтапно снижая дозировку на протяжении 3–5 суток.
Лекарство не оказывает токсического действия на почки и печень. С осторожностью применять его необходимо при геморрагическом инсульте: не ранее, чем через 7 суток с момента приступа.
Побочные эффекты препарата
Кавинтон хорошо переносится большинством больных. В редких случаях возможны:
изжога, сухость во рту;
кратковременное усиление головокружения;
Резкое ухудшение самочувствия может быть признаком непереносимости. В этом случае важно своевременно обратиться к врачу по поводу замены препарата.
Когда противопоказан Кавинтон
К числу противопоказаний относятся:
детский возраст: до 18 лет сосудистая система несовершенна;
при беременности и лактации: из-за недостаточно изученного действия средства на организм плода и новорожденных;
тяжелые поражения сердца, сопровождаемые аритмией;
повышенная чувствительность к компонентам лекарства.
Кавинтон запрещено использовать совместно с препаратами гепарина из-за опасности резкого снижения свертываемости крови. Одновременный прием алкоголя также запрещен, так как активное вещество усиливает его токсические свойства.
Аналоги и стоимость Кавинтона
Похожим действием обладают препараты Бравинтон, Карницетин, Ацефен, Нооклерин, Пирацезин.
Купить упаковку таблеток Кавинтона можно за 200–370 рублей. Цена 10 ампул объемом 2 мл — около 250 рублей. За упаковку средства в ампулах по 5 мл нужно заплатить 330–380 рублей.
Препарат отпускается по рецепту врача.
Все представленные на сайте материалы предназначены исключительно для образовательных целей и не предназначены для медицинских консультаций, диагностики или лечения. Администрация сайта, редакторы и авторы статей не несут ответственности за любые последствия и убытки, которые могут возникнуть при использовании материалов сайта.
Поликлиника №5, Ярославль
Полимодальность эффектов препарата кавинтон: экспериментальные и клинические доказательства
Журнал: Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски. 2010;110(9‑2): 8‑12
Касаткин Д.С. Полимодальность эффектов препарата кавинтон: экспериментальные и клинические доказательства. Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски. 2010;110(9‑2):8‑12.
Kasatkin DS. Polymorphic effects of cavinton: experimental and clinical evidence. Zhurnal Nevrologii i Psikhiatrii imeni S.S. Korsakova. 2010;110(9‑2):8‑12. (In Russ.).
Поликлиника №5, Ярославль
Поликлиника №5, Ярославль
За последние 15 лет данные, накопленные в области нейронаук, привели к полной реорганизации знаний в этой области и к иному пониманию функционирования нервной системы. Изменения в фундаментальных представлениях о базовых физиологических и патологических процессах, протекающих в нервной ткани, заставили по-новому взглянуть на клинику, патогенез и лечение многих неврологических заболеваний.
Независимо от причинного фактора, механизмы повреждения нейронов могут носить специфический и неспецифический характер. К неспецифическим механизмам альтерации относятся нарушения энергообеспечения нейронов; расстройства синтеза белка; дисбаланс ионов и жидкости в нейронах; повреждение мембран в результате перекисного окисления липидов; апоптоз. Патогенетическую основу большинства форм специфического повреждения нейронов составляют нарушения специфических для нейрона процессов метаболизма нейромедиаторов (синтеза, аксонального транспорта, секреции, удаления и утилизации). Механизмы повреждения нейронов тесно взаимосвязаны и нередко потенцируют друг друга, образуя порочный круг, в связи с чем для лечения неврологических расстройств перспективным будет препарат, препятствующий возможно большему числу механизмов альтерации нейронов, при этом положительно влияющий на уровень мозгового кровотока и микроциркуляции. Одним из лекарственных средств, обладающих подобными эффектами, является винпоцетин (кавинтон) [1].
Основным показанием для применения винпоцетина являются хронические расстройства мозгового кровообращения [1, 2], однако активно обсуждается вопрос об использовании препарата как при острых нарушениях мозгового кровообращения [3], так и при нейродегенеративных заболеваниях (болезнь Альцгеймера) [4, 5].
Основой сосудистого эффекта винпоцетина (кавинтона) является воздействие на метаболизм циклических нуклеотидов в клетках гладкой мускулатуры сосудистой стенки путем торможения Са 2+ /кальмодулин-зависимой фосфодиэстеразы 1-го типа [7]. Этот эффект приводит к преобладанию цАМФ над цГМФ, что способствует релаксации сосудов головного мозга, снижает агрегацию тромбоцитов [8] и патологически увеличенную вязкость крови [9], нормализует деформируемость эритроцитов [10, 11].
Важным представляется тот факт, что винпоцетин (кавинтон) избирательно повышает мозговой кровоток 12, уменьшает сопротивление мозговых сосудов без воздействия на системное кровообращение (практически не влияя на артериальное давление, минутный объем, частоту сердечных сокращений, общее периферическое сопротивление) [15, 16]. Он не вызывает феномена «обкрадывания», а наоборот, улучшает кровоснабжение пораженной области, причем кровоток в интактной зоне мозга сохраняется неизменным 18.
При пероральном приеме винпоцетина (кавинтона) у пациентов пожилого и старческого возраста с явлениями сенильной деменции в течение 3 нед в дозе 15-30 мг в сутки параллельно с увеличением концентрации АТФ в эритроцитах наблюдается усиление сродства гемоглобина к кислороду и его способности отдавать кислород [19]. Препарат активизирует дефицитный обмен веществ и увеличивает энергетическую емкость мозга путем улучшения утилизации глюкозы, кислорода и темпов синтеза АТФ. При помощи позитронно-эмиссионной томографии было показано увеличение доставки глюкозы (захвата и высвобождения) через гематоэнцефалический барьер [20, 21].
Нейропротективные эффекты винпоцетина (кавинтона), вероятнее всего, опосредованы несколькими механизмами. Ингибирование вольтажзависимых натриевых каналов на фоне приема винпоцетина в условиях эксперимента приводит к замедлению накопления натрия в клетке, снижая тем самым токсический эффект оксидантного стресса при аноксии и повреждения при реперфузии 23. Антиоксидантный эффект препарата проявляется вследствие снижения активности перекисного окисления липидов в синаптосомах [25, 26]. В условиях экспериментальной ишемии винпоцетин снижал размеры очага некроза нервной ткани на 60% [22]; по антиоксидантной активности в исследованиях на животных винпоцетин достоверно превосходил пентоксифиллин и пирацетам [27, 28].
Также на фоне приема винпоцетина отмечено снижение эксайтотоксичности и апоптоза за счет блокирования NMDA-рецепторов и снижения поступления ионов Ca 2+ в клетку 30.
Дополнительным важным фактором является усиление структурной динамики дендритов клеток коры в виде увеличения и удлинения шипиков, что приводит к увеличению пластичности нейронов, особенно в области гиппокампа [32, 33], и, вероятно, лежит в основе усиления когнитивных функций на фоне приема винпоцетина [34]. Эффект, по-видимому, является следствием блокирования поступления ионов кальция и натрия в клетку и усиления активности элементов цитоскелета нейронов [35, 36].
Помимо сосудистого и нейропротективного эффекта винпоцетин обладает влиянием на нейромедиаторные системы мозга, усиливая внутримозговой обмен норадреналина и серотонина [37] и стимулируя восходящую норадренергическую систему, в частности голубое ядро ствола [38].
Исследования эффективности винпоцетина (кавинтона)
На настоящий момент проведено 7 двойных слепых плацебо-контролируемых исследований, продемонстрировавших эффективность винпоцетина (кавинтона).
Впервые исследование винпоцетина (кавинтона) в сравнении с плацебо было проведено G. Lipani в 1984 г. [39]. В исследование были включены 44 пациента с хронической ишемией мозга, транзиторными ишемическими атаками и умеренными когнитивными расстройствами, распределенных в 2 группы: 22 больных получали винпоцетин в дозе 30 мг в сутки в течение 1 мес, затем 15 мг в сутки в течение последующих 2 мес, другие 22 пациента в течение 3 мес получали плацебо. Оценка результатов проводилась с использованием шкалы общего клинического впечатления (Clinical Global Impression -CGI), шкалы клинической гериатрической оценки Сандоз (Sandoz Clinical Assessment Geriatric Scale - SCAG), краткого опросника психического статуса (Mini Mental State Examination - MMSE), показателей неврологического статуса. Были получены достоверные отличия показателей в группе винпоцетина по сравнению с плацебо на 30-й и 90-й дни исследования.
В исследование M. Peruzza и M. DeJakobis [40] были включены 40 пациентов с дегенеративными заболеваниями центральной нервной системы, разделенных на 2 группы по 20 человек. Дизайн и методы оценки были аналогичны исследованию
Аналогичное по дизайну и числу пациентов (n=40) исследование было проведено Е. Manconi и соавт. [41]. В конечной точке исследования у 87% больных основной группы, лечившихся винпоцетином, наблюдалось снижение балла по шкале CGI против 11% в группе плацебо (p<0,001); при оценке неврологического статуса выраженные улучшения наблюдались у 59% больных, получавших винпоцетин, против 6% в группе плацебо (p<0,001). Аналогичные различия были получены по шкалам SCAG и MMSЕ.
В исследование Е. Fenzl и соавт. [42] вошел 201 пациент с умеренным психоорганическим синдромом ишемического и нейродегенеративного характера; 105 больных основной группы получали винпоцетин в дозе 60 мг в сутки в течение 1 года, 96 больных группы сравнения получали плацебо. В оценке результатов использовались шкала CGI, короткий синдромальный тест (Syndrome short test - SST) и индекс активности (Condition-index - CI). Показатели CGI через 6 и 12 мес лечения были достоверно ниже в группе винпоцетина, а индекс активности достоверно выше. Клиническое улучшение в неврологическом статусе через 12 мес наблюдалось у 86,7% пациентов основной группы против 54,2% в группе плацебо (p<0,001).
Исследование R. Balestreri и соавт. [43] соответствовало по дизайну ранее проведенным исследованиям 40, существенным отличием данного исследования явилось включение только пациентов с хронической ишемией мозга (n=80). Снижение балла по шкале CGI через 90 дней лечения винпоцетином составило 44% против 13% в группе плацебо (p<0,001). Улучшение наблюдалось также по шкалам SCAG и MMSЕ, при этом показатели были достоверно выше в основной группе.
В исследовании Н. Fuchs и H. Erzigkeit [44] было проведено сравнение 3 групп пациентов с умеренным психоорганическим синдромом без дифференцировки по этиологии (n=165): 2 основных групп, получавших винпоцетин в дозах 60 и 30 мг в сутки (55 и 56 больных соответственно), и группы плацебо (n=54). Длительность исследования составила 16 нед. При оценке результатов использовались шкалы CGI, SST и CI. После 16 нед лечения показатель CGI был достоверно ниже в обеих основных группах по сравнению с группой плацебо (p<0,001).Уровень CI достоверно не отличался.
L. Blaha и соавт. [45] провели исследование в 4 параллельных группах (n=213), в течение 12 нед получавших винпоцетин в дозах 60, 30 и 15 мг в сутки и плацебо (53, 55, 50 и 55 больных соответственно). В дополнение к шкалам CGI и SST была использована шкала депрессии (Erlangen depression scale - EDS). Через 3 мес терапии показатель CGI был достоверно ниже во всех группах, получавших винпоцетин, по сравнению с плацебо (p<0,001). Показатель по шкале EDS в группах лечения был ниже, чем в группе плацебо, однако достоверность отличий имела пороговые значения.
Результаты всех 7 исследований обобщены в мета-анализе, включившем данные о 731 пациенте [46].
Отдельно были проанализированы данные имевших сходный дизайн итальянских исследований (n=204) по показателю CGI, при этом было получено достоверное снижение на 1,22 балла (доверительный интервал, ДИ - 1,01-1,43; p<0,001) в основной группе по сравнению с группой плацебо на 30-й день и на 1,1 балла (ДИ - 0,89-1,31; p<0,001) на 90-й день исследования.
Эффективность винпоцетина (кавинтона) доказана также в ряде открытых и сравнительных исследований.
A. Szobor и M. Klein [47] исследовали эффективность винпоцетина в группе пациентов с церебральным атеросклерозом, гипертонической энцефалопатией, хронической недостаточностью мозгового кровообращения. В исследование были включены 100 пациентов, которые получали винпоцетин в дозе 30-45 мг в сутки перорально и в виде комбинации (перорально и инфузионно). По результатам исследования выявлено значимое улучшение клинического состояния в исследуемой группе.
В исследовании Е. Burtsev и соавт. [2], опубликованном в 1992 г., подведены итоги 10-летнего исследования применения винпоцетина у пациентов с различными формами цереброваскулярных заболеваний. Обзор включил в себя данные 967 пациентов. Наилучший результат получен у пациентов с ранними формами хронических заболеваний (вегетативная дисфункция, ранние стадии дисциркуляторной энцефалопатии).
Исследования безопасности винпоцетина (кавинтона)
В открытом клиническом исследовании, проведенном T. Perényi и соавт. [48], 100 пациентов получали винпоцетин в дозе 15 мг в сутки в течение 1 года, при этом ЭКГ-мониторинг не выявил значимых изменений и случаев аритмии. Аналогичные результаты имело и исследование, проведенное в Японии в рамках III фазы клинического испытания винпоцетина, включившее около 8000 пациентов в 1420 центрах [49].
Для уточнения аритмогенного влияния винпоцетина C. Farsang и соавт. [50] было проведено 2-летнее двойное слепое рандомизированное плацебо-контролируемое исследование, включившее данные о 85 пациентах, страдавших различными хроническими заболеваниями сердца. По результатам исследования был сделан вывод, что ни винпоцетин, ни плацебо не влияли на частоту сердечных сокращений, длительность интервалов PQ, QRS, QT и ST, не вызывали экстрасистол и не изменяли формы пика Т, т.е. длительный пероральный прием винпоцетина не приводит к возникновению аритмий.
В 1998 г. по результатам мета-анализа венгерской и международной литературы было установлено, что ни пероральное, ни внутривенное лечение винпоцетином не оказывало какого-либо значимого эффекта на сердечный ритм и проводимость даже при наличии факторов риска аритмии [46].
Тем не менее в случаях наличия хронических заболеваний сердца (особенно при гипертрофии левого желудочка, ишемии или малой фракции выброса левого желудочка), при электролитных нарушениях (гипокалиемия, гипомагниемия), удлинении интервала QT, применении лекарственных препаратов, являющихся блокаторами калиевых каналов (амиодарон, соталол) или ингибиторами цитохрома Р450 (циметидин, кларитромицин, флуоксетин и др.), парентеральную терапию винпоцетином следует проводить под контролем ЭКГ. Поскольку винпоцетин обычно применяют в повышающихся дозах (начиная с 20-25 мг и доходя до 60 мг в сутки), рекомендуется проведение ЭКГ после первой инфузии и после достижения максимальной дозы. В случае удлинения интервала QT (что в норме бывает редко) следует рассмотреть возможность снижения дозы кавинтона или отмены препарата.
Важным аспектом применения винпоцетина (кавинтона) является отсутствие влияния на функцию печени, в том числе на систему ферментов, метаболизирующих лекарственные вещества, а также отсутствие влияния на нормальные и патологически измененные функции почек [46]. В специально проведенных исследованиях не обнаружено взаимодействия кавинтона с бета-блокаторами (хлоранолол, пиндолол), клопамидом, метилдопой, дигоксином и гипотиазидом. Препарат может быть использован в обычных дозах у пациентов с почечной и печеночной недостаточностью; у него отсутствует кумулятивный эффект.
Кавинтон для инфузий химически несовместим с гепарином, поэтому эти препараты нельзя вводить в одном шприце, хотя возможно последовательное введение.
Е.И. Чукановой в 2003 г. было проведено фармакоэкономическое исследование нейрометаболических препаратов [51], включившее данные о 532 пациентах с дисциркуляторной энцефалопатией I и II стадии. Показано, что применение кавинтона способствует регрессу или стабилизации прогрессирования неврологических расстройств, при этом препарат имеет хороший профиль переносимости, стоимость курсового лечения и коэффициент «затраты/эффективность» оказались наиболее благоприятными по сравнению с другими препаратами.
Таким образом, несмотря на длительную историю применения кавинтона в широкой клинической практике (более 30 лет), интерес к изучению механизмов его действия среди биохимиков, молекулярных биологов, клиницистов не угасает, при этом с каждым годом выявляются ранее неизвестные свойства препарата, открывающие новые перспективы его применения. Именно множественность точек приложения кавинтона в сочетании с высокой клинической эффективностью и безопасностью применения позволяют ему длительно и успешно конкурировать с постоянно возрастающим числом новых лекарственных средств на фармакологическом рынке.
Читайте также:

