Кандидоз кожи при дисбактериозе
Обновлено: 24.04.2024
Для цитирования: Бурова С.А. Комплексный подход к терапии больных с кандидозом органов пищеварительного тракта. РМЖ. 2015;13:760.
Грибковые инфекции кожи и внутренних органов в настоящее время привлекают все большее внимание врачей различного профиля. Из потенциальных «болезней будущего» микозы превратились в актуальные «болезни настоящего». Пищеварительная система человека в значительной степени подвержена грибковым заболеваниям, особенно у пациентов из групп риска.
Грибы Candida – условно-патогенные микроорганизмы, заселяют пищеварительный тракт в норме, участвуют в процессе брожения, переваривания пищи и др. Этот феномен, называемый колонизацией, клинически протекает бессимптомно. Исследование взрослых здоровых добровольцев показало, что Candida albicans присутствует у них в орофарингеальной зоне в 20–30%, в тонком кишечнике – в 50–54%, в толстом кишечнике – в 55–70%, в фекалиях – в 65–70% случаев.
Итак, при физиологическом благополучии между макро- и микроорганизмами существует определенное равновесие, в котором играют роль, с одной стороны, факторы устойчивости организма к микроскопическим грибам, с другой – факторы патогенности грибов. Устойчивость организма зависит от принадлежности к группам риска и компетентности его иммунной системы. Для защиты важен также макрофагальный и нейтрофильный фагоцитоз, препятствующий диссеминации грибковой, особенно кандидозной инфекции.
По мнению большинства исследователей, бессимптомное пребывание грибов в желудочно-кишечном тракте (ЖКТ) может прекратиться, когда они приобретают патогенные свойства, а у пациента обнаруживается несостоятельность иммунной системы.
Наиболее частыми микозами пищеварительного тракта являются кандидоз пищевода и кандидоз кишечника, которые встречаются как у иммунокомпетентных, так и (гораздо чаще) у иммуносупрессированных лиц. Первичные микозы желудка, в т. ч. и кандидоз, диагностируют редко, что связано с физиологической кислотной средой желудка, где грибковые клетки погибают.
Факторами риска развития кандидоза пищевода и кишечника являются:
1. Заболевания ЖКТ:
- заболевания слизистых оболочек полости рта;
- гастроэзофагеальная рефлюксная болезнь;
- обсемененность желудка Helicobacter pylori;
- атрофический гастрит, гипоацидность желудка, ахалазия, бульбит;
- эрозивно-язвенные заболевания пищевода и кишечника;
- микст-инфекция кишки, дисбиоз;
- дивертикулез, полипоз;
- энтероколит, болезнь Крона, синдром раздраженного кишечника и др.
2. Другие заболевания:
- онкологические;
- гематологические;
- эндокринологические;
- аллергические;
- СПИД и ВИЧ-инфицированность.
3. Травмирование слизистой оболочки ЖКТ:
- пищеводно-желудочным зондом;
- ожоги пищевода;
- оперативные вмешательства.
4. Прием лекарственных препаратов:
- антибиотиков;
- цитостатиков;
- гормонов и других химиопрепаратов.
Нарушение питания, голодание, алкоголизм, курение, наркомания способствуют развитию кандидоза. К факторам риска относится также пожилой возраст, когда происходит старение иммунной системы, присоединяются многочисленные соматические заболевания, уменьшаются амплитуда продольных сокращений пищевода и сила сокращений сфинктеров, нарушаются процессы всасывания и т. д.
Клинически кандидоз пищеварительного тракта подразделяется на:
- орофарингеальный кандидоз (псевдомембранозный, атрофический, эритроматозный, ромбовидный глоссит, ангулярный хейлит);
- кандидозный эзофагит (эрозивный и без эрозий);
- кандидоз желудка (эрозивно-фибринозный и вторичный на фоне язвенной болезни);
- кандидоз кишечника (псевдомембранозный, коллагеновый, лимфоцитарный);
- кандидозный проктосигмоидит;
- перианальный кандидоз;
- секреторную диарею, ассоциированную с кандидозом.
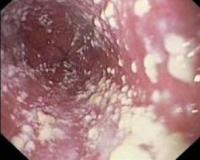
Кандидозный эзофагит в стационарах общего профиля встречается у 1,3–2,8% больных, в отделениях трансплантации – до 4%, при диссеминированном карциноматозе – от 2,8 до 6,7%. Это заболевание протекает часто без субъективных жалоб и выявляется случайно при исследованиях населения в 1–7% случаев. Иногда больные отмечают боль и дискомфорт при прохождении твердой и жидкой пищи, дисфагию, гиперсаливацию. По глубине поражения эндоскопически выделяют 4 типа: от легкого отека, гиперемии, единичных белых налетов
Кандидоз желудка, как правило, развивается вторично на фоне язвенной и гастроэзофагеальной рефлюксной болезни. Ахлоргидрия в свою очередь способствует колонизации грибов на слизистой с последующей инвазией, особенно в зонах дефекта (язвы, эрозии), что замедляет репарацию (заживление), появляется болевой синдром, иногда кровоточивость язвы.
Кандидозное поражение кишечника обычно проявляется абдоминальным дискомфортом, диареей, вздутием живота, болевым синдромом и другими симптомами. Изучение микробиоценоза кишечника позволяет конкретизировать аморфный «энтероколит», а именно: отдифференцировать псевдомембранозный колит, вызываемый Clostridium difficile, острый процесс в кишечнике, вызываемый ротовирусами и Escherichia coli, болезнь Крона, синдром раздражения толстой кишки от кандидоза или дисбактериоза с преимущественным кандидозным компонентом.
В большинстве случаев грибковые поражения ЖКТ сопровождаются изменением микробиоценоза и снижением колонизационной резистентности организма. Для лечения кандидоза ЖКТ применяют самые разнообразные антимикотики как системного, так и местного действия. Также одной из задач терапии является создание условий для роста и функционирования нормальной микрофлоры.
В современной научной литературе препараты для коррекции дисбиозов делят на 3 основные группы: пробиотики – содержат жизнеспособные микроорганизмы; пребиотики – содержат стимуляторы роста микрофлоры; синбиотики – содержат живые микроорганизмы и пребиотики. Существуют пробиотические комплексы, представляющие собой комбинацию из перечисленных выше компонентов, а также сорбентов, витаминов и микроэлементов. Средств коррекции нарушений микрофлоры кишечника достаточно много, постоянно появляются новые варианты и разновидности.
Дальнейшим развитием традиционных пробиотиков являются натуральные метабиотики. Термины «метабиотики», «метаболические пробиотики», «постбиотики», «биологические лекарства» или «фармакобиотики» используются для обозначения небольших молекул, которые являются структурными компонентами пробиотических (симбиотических) микроорганизмов и/или их метаболитов, и/или сигнальных молекул с определенной (известной) химической структурой, которые способны влиять на микробиом и/или метаболические и сигнальные пути человека. Одним из представителей метабиотиков является Бактистатин.
В состав комплекса Бактистатин включены дополняющие друг друга природные компоненты: сорбент, пробиотик, пребиотик. Одним из преимуществ комплекса Бактистатин является отсутствие живых бактерий, чужеродных для ЖКТ человека, длительное присутствие которых в больших количествах нежелательно. Вместо живых бактерий в состав комплекса Бактистатин включены продукты их жизнедеятельности – активные метаболиты. Поэтому Бактистатин начинает работать сразу, и его действие направлено на восстановление собственной нормальной микрофлоры, которая уникальна у каждого человека.
Нами проведено исследование по оценке эффективности и безопасности пробиотического комплекса Бактистатин в схемах терапии больных с кандидозным эзофагитом и энтероколитом.
В ходе исследования оценивались эффективность и безопасность 2-х схем лечения кандидоза пищевода и кишечника в 2-х группах: 1-я группа – контрольная, в которой пациенты получали этиотропную противогрибковую терапию; 2-я – основная группа пациентов, у которых в схему вышеназванной терапии включен комплекс Бактистатин.
В обеих группах больных проводили селективную деконтаминацию современными эффективными противогрибковыми препаратами направленного действия в течение 7–14 дней. Пациенты основной группы дополнительно получали Бактистатин по 2 капсулы 2 р./сут 20 дней.
Для изучения клинических, эндоскопических и лабораторных показателей в динамике на фоне лечения больных кандидозным эзофагитом и энтероколитом была разработана специальная анкета, включающая физикальное обследование, гастроскопию, колоноскопию, бактериологическое исследование кала.
Результаты сравнения балльной оценки клинической симптоматики показали, что на фоне приема комплекса Бактистатин быстрее уходили проявления кандидоза пищевода и кишечника. Так, до лечения общий балл выраженности симптоматики кандидозного эзофагита был 355, после лечения этот показатель снизился до 123 в контрольной группе и до 60 у пациентов основной группы, принимающих Бактистатин (рис. 1). В отношении кандидозного энтероколита до лечения общий балл выраженности симптоматики составлял 645, после лечения – 317 в контрольной группе и 120 в основной группе (рис. 2).
Кроме того, применение комплекса Бактистатин в лечении кандидоза ЖКТ существенно влияло на восстановление микробиоценоза толстой кишки за счет увеличения числа бифидо- и лактобактерий и уменьшения количества энтеробактерий, неферментирующих бактерий и грибов.
Полученные данные свидетельствуют, что использование метабиотика Бактистатин позволяет избежать побочного действия системных антимикотиков на микрофлору кишечника, улучшить состояние пищевода и кишечника в короткие сроки за счет более выраженного снижения степени тяжести заболевания.
Таким образом, применение комплекса Бактистатин в схемах терапии грибковых поражений ЖКТ способствует быстрому созданию условий для роста и функционирования нормальной микрофлоры и уменьшению побочных эффектов системных антимикотиков.
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Инвазивный кандидоз – это генерализованная грибковая инфекция, при которой наблюдается кандидемия и поражение внутренних органов грибами рода Кандида. До половины случаев заболевания вызвано возбудителем C. albicans, в тройке самых распространенных патогенов находятся C. parapsilosis и C. glabrata. Клинические проявления болезни определяются локализацией очага инфекции и степенью иммунного ответа. Для диагностики назначают серологические и культуральные исследования крови, инструментальные методы визуализации. Лечение требует индивидуального подбора противогрибковых препаратов.
МКБ-10


Общие сведения
Инвазивный кандидоз считается одной из самых распространенных инфекций среди госпитализированных пациентов. Ежегодно регистрируется более 250000 случаев, причем эксперты уверены, что истинная встречаемость инфекции намного выше. Заболевание чаще развивается у новорожденных и людей пожилого возраста. Высокая распространенность, неблагоприятный прогноз и сложности своевременной идентификации кандидоза заставляют специалистов искать новые пути диагностики и лечения болезни.

Причины
Возбудитель заболевания – грибы рода Candida, которые принадлежат к семейству Сахаромицеты, классу Аскомицеты. Известно более 20 патогенных для человека видов, однако до 90% случаев инвазивного кандидоза провоцируют только 5 из них: C. albicans, C. glabrata, C. tropicalis, C. parapsilosis и C. krusei. Лидирующее место в России продолжает занимать C. albicans (48%), часто встречаются возбудители C. parapsilosis (17%) и C. glabrata (14%).
Основным фактором риска инвазивного кандидоза является иммунная недостаточность, поскольку все звенья иммунитета участвуют в борьбе с грибковой инфекцией. Заболевание в основном встречается среди пациентов отделений интенсивной терапии, причем возраст больного до 1 года и старше 65 лет резко повышает вероятность грибковой инфекции. Выделяют и другие факторы риска:
- Пересадка внутренних органов. На долю кандидоза приходится более 53% всех инвазивных микозов, которые развиваются у пациентов после трансплантации. Наибольший риск имеет пересадка тонкого кишечника, поджелудочной железы и печени. Грибковая инфекция развивается у 3-4% больных с трансплантированным сердцем, почками, легкими.
- Постановка катетера. Центральный венозный катетер представляет собой оптимальные входные ворота для грибковых возбудителей. В его просвете формируются биопленки из грибов Кандида, которые вызывают катетер-ассоциированную кандидемию. Патология чаще встречается у новорожденных и вызвана видом C. parapsilosis.
- Антибиотикотерапия. Противомикробные препараты широкого спектра действия подавляют полезную микрофлору кишечника, повышают грибковую контаминацию ЖКТ. Наиболее опасными признаны цефалоспорины III поколения, которые в 2 раза увеличивают риск развития микозов.
- Онкопатология. Наибольшему риску подвергаются пациенты с гемобластозами, у которых отмечается выраженная нейтропения, нарушения выработки иммуноглобулинов и патологии системы комплемента. На поздних стадиях солидных опухолей также возрастает вероятность инвазивного кандидоза.
Патогенез
Большинство случаев связано с эндогенным путем передачи инфекции: проникновением грибов через слизистые оболочки желудочно-кишечного тракта либо через поврежденные полые органы брюшной полости. Заражению способствует увеличение грибковой нагрузки в кишечнике на фоне антибиотикотерапии. Реже наблюдается экзогенное инфицирование при инвазивных медицинских манипуляциях (постановка катетера, парентеральное питание, хирургическое вмешательство).
После проникновения грибов Кандида в кровеносную систему развивается кандидемия, обуславливающая гематогенное распространение возбудителя и формирование очагов во внутренних органах. Основным механизмом тканевой инвазии является способность к образованию псевдомицелия, который препятствует поглощению грибов макрофагами. К факторам патогенности относят ферменты (аспартилпротеиназы, фосфолипазы), фенотипическую нестабильность.

Симптомы инвазивного кандидоза
У трети пациентов наблюдается кандидемия без органических патологий внутренних органов, которая не имеет специфических признаков. Основным симптомом присоединения грибковой инвазии является резкий подъем температуры на фоне антибиотикотерапии. Лихорадка зачастую имеет волнообразное течение. При глубоком иммунодефиците проявления системного воспалительного процесса стерты или полностью отсутствуют.
При вовлечении в процесс внутренних органов клиническая картина разнообразна. Поражение органов брюшной полости проявляется классическими признаками перитонита: резкие боли по всему животу, напряжение мышц передней брюшной стенки, многократная тошнота и рвота. Инфицирование мочевых путей сопровождается кандидозным циститом и пиелонефритом. Частным признаком инфекции является пневмония, которая протекает без особенностей.
При установке ликворных шунтов и других инвазивных нейрохирургических манипуляциях возможно поражение ЦНС. Инвазия грибами Кандида чаще всего проявляется менингитом с подострым течением. При воспалении мозговых оболочек возникает сильная головная боль, длительная лихорадка, светобоязнь. Отличием грибкового менингита считается отсутствие ригидности затылочных мышц.
Поражение тканей сердца развивается у пациентов после установки искусственных клапанов. Клинические проявления манифестируют в течение 2 месяцев после операции. Больные страдают от лихорадки, одышки, болей в области сердца. Быстро присоединяются признаки сердечной недостаточности, гепатоспленомегалия, узелки Ослера. Есть риск вовлечения опорно-двигательного аппарата с развитием кандидозного артрита и остеомиелита.
Инвазивный кандидоз у новорожденных характеризуется классической картиной неонатального сепсиса. Возникает заторможенность, отказ от кормлений, одышка с эпизодами апноэ. Характерна сердечно-сосудистая нестабильность, затяжная желтуха. Фебрильная лихорадка наблюдается только в 50% случаев, при этом до 40% пациентов имеют физиологическую норму лейкоцитов крови.
Осложнения
Несмотря на достижения практической инфектологии, летальность при инвазивном кандидозе остается стабильно высокой. У взрослых уровень смертности составляет 40%, среди иммунокомпрометированных больных он может достигать 50-70%. Суммарная детская смертность при инвазивной форме кандидоза варьирует в пределах 37-44%, неонатальная – 43-54%. Прогностически неблагоприятным фактором является задержка идентификации возбудителя на 48 часов и более.
Жизнеугрожающие последствия инвазивного кандидоза в основном связаны с септическим шоком и полиорганной недостаточностью. Причинами смерти выступают критические поражения головного мозга, сердечно-легочной системы и почек. Большую опасность представляют коагулопатии, тромбоэмболии, синдром диссеминированного внутрисосудистого свертывания (ДВС).
Диагностика
Поскольку инвазивный кандидоз в основном развивается у госпитализированных больных, обследование проводит лечащий врач совместно с реаниматологом и инфекционистом. Большое значение уделяют сбору анамнеза, выяснению иммунного статуса, анализу текущей схемы фармакотерапии. При осмотре определяются признаки системного воспаления и полиорганной недостаточности. Для подтверждения диагноза назначаются такие методы:
- Определение поверхностного антигена Candida. Наличие в анализе маннана и антиманнановых антител специфично для кандидозной инфекции. Позитивные результаты на 5-6 дней опережают ответ при посеве гемокультуры, имеют важное значение для своевременного старта терапии. Чувствительность и специфичность метода составляют 80-85%.
- Исследование гемокультуры. Выявление грибов Кандида в образцах крови, взятых из трех разных вен, является достоверным признаком инвазивного кандидоза. Такой метод требует длительного времени и дает положительные результаты только у 75% пациентов, поэтому он не подходит для ранней диагностики.
- Инструментальная визуализация. Для обнаружения очагов кандидозной инфекции используют ультразвуковое исследование, чреспищеводную эхокардиографию, компьютерную и магнитно-резонансную томографию. Подтвердить грибковую этиологию воспалительных очагов удается путем анализа биоптатов.
- Прогностические шкалы. Поставить точный диагноз помогает шкала «Кандида» и прогностическое правило, представленное в Российских клинических рекомендациях. Для определения индивидуального риска используют индекс колонизации Candida.

Дифференциальная диагностика
Ввиду отсутствия патогномоничных проявлений, при постановке диагноза исключают бактериальный сепсис, генерализованную герпетическую инфекцию, аспирационную и вентилятор-ассоциированную пневмонию. Дифференциальную диагностику проводят с малярией, системной красной волчанкой, васкулитами. У новорожденных необходимо исключить респираторный дистресс-синдром.
Лечение инвазивного кандидоза
Основу лечения составляет длительное парентеральное введение противогрибковых препаратов. Лекарства назначают эмпирически до получения результатов посева крови, предварительно взяв биоматериал для микробиологической диагностики. При выборе препарата для лечения кандидоза обращают внимание на иммунный статус пациента, наличие и характер сопутствующих заболеваний, анамнестические данные о грибковых инфекциях.
Стандартные протоколы терапии включают препараты из группы полиеновых антибиотиков, азоловых антимикотиков, эхинокандинов. Клинический ответ на проводимое лечение развивается в течение 3 дней. При его отсутствии необходим пересмотр режима дозирования антимикотиков или их замена. Критерием завершения антимикотической терапии служат отрицательные посевы крови в течение 14 суток.
Фармакотерапия инвазивного кандидоза сочетается с лечением основного заболевания. Значимые усилия прикладывают для нормализации иммунного статуса, если это возможно. Для исключения повторного инфицирования грибками проводят замену катетеров. При тяжелом иммунодефиците, состоянии после трансплантации костного мозга или внутренних органов пациенты проходят лечение в стерильном боксе.
Прогноз и профилактика
У пациентов с сохранными функциями иммунной системы, которым вовремя начата терапия антимикотиками, удается достичь полного выздоровления. При иммунодефиците и тяжелом соматическом статусе прогноз остается сомнительным даже при ранней и комплексной медицинской помощи. Для профилактики инвазивного кандидоза пациентам из группы высокого риска рекомендован прием флуконазола в стандартной дозировке.
3. Инвазивный кандидоз: современные аспекты эпидемиологии, диагностики, терапии и профилактики у различных категорий пациентов (в вопросах и ответах)/ А.В. Веселов, Р.С. Козлов. – 2016.
4. Инвазивный кандидоз в отделениях реанимации и интенсивной терапии/ Н.А. Карпун, С.А. Бурова, Е.А. Евдокимов, Н.И. Чаус// Неотложная медицина. – 2014. – №2.
Кандидоз кишечника – инфекционное поражение пищеварительного тракта, вызванное собственной грибковой флорой пациента (Candida spp.) на фоне значительного ослабления иммунитета. Клинические проявления кандидоза кишечника варьируют в зависимости от формы заболевания: разжижение стула, повышенный метеоризм, неопределенные боли в животе, язвенный колит и грибковый сепсис. Диагноз ставится на основании эндоскопического исследования, гистологического и культурального анализа биоптатов, кала. Лечение включает три основных направления: назначение антимикотиков, нормализацию микрофлоры кишечника и коррекцию иммунного статуса пациента.

Общие сведения
Кандидоз кишечника – грибковое поражение слизистой оболочки пищеварительного тракта. Является актуальной проблемой современности, так как диагностика и определение критериев данного заболевания представляют сложность для многих клиницистов. Связано это с повсеместной распространенностью грибов рода Candida, в том числе и в организме здоровых людей (носительство грибов рода Candida в кишечнике присуще 80% населения). Инвазивный кандидоз кишечника практически никогда не встречается у людей с нормально функционирующим иммунитетом, почти всегда это оппортунистическая инфекция, связанная с иммунным дисбалансом организма.
Кроме того, для многих специалистов бывает достаточно сложно дифференцировать транзиторное кандидоносительство и неинвазивный кандидоз кишечника (именно он составляет подавляющее большинство всех клинических случаев кандидоза пищеварительной системы). Разграничить два этих состояния возможно только при наличии современного диагностического оборудования. Для установления правильного диагноза необходимо наличие трех диагностических критериев: выявление одного или нескольких факторов риска, эндоскопические признаки кандидоза кишечника, положительный результат культурального исследования. Таким образом, тактика назначения антимикотиков при первом обнаружении в посевах грибов рода Candida, без дальнейшего обследования, является ошибочной.

Причины кандидоза кишечника
Специалисты в области гастроэнтерологии выделяют две патогенетические формы кандидоза кишечника – инвазивную и неинвазивную. В клинической практике чаще встречается неинвазивный кандидоз кишечника на фоне дисбактериоза и смешанной кишечной инфекции (грибково-бактериальной, грибково-протозойной и др.). Висцеральная форма развивается на фоне выраженной нейтропении (практически полное отсутствие нейтрофильных лейкоцитов) и поздних стадий СПИДа.
Факторы риска
Для формирования кандидоза кишечника необходимо наличие хотя бы одного из предрасполагающих факторов:
- физиологического снижения иммунитета (период новорожденности или пожилой возраст, сильный стресс, беременность);
- врожденного иммунодефицита (синдром Di George, Nezelof и др.);
- онкопатологии, особенно в период полихимиотерапии;
- аутоиммунных и аллергических заболеваний (усугубляет угнетение иммунитета лечение кортикостероидными гормонами);
- приема иммунодепрессантов после трансплантации органов;
- тяжелых эндокринных заболеваний, соматической патологии, требующей интенсивной терапии;
- длительного лечения антибактериальными препаратами резервного ряда;
- синдрома первичного иммунодефицита;
- выраженного дисбаланса питательных веществ в рационе (особенно недостатка белка и витаминов).
В клинической практике чаще встречается кандидоз кишечника, обусловленный сочетанием нескольких из перечисленных факторов.
Патогенез
При неинвазивной форме грибы рода Candida начинают неконтролируемо размножаться в просвете кишки, не проникая в толщу ее слизистой. При этом выделяются специфические грибковые токсины, образуются ядовитые продукты ферментации, оказывающие раздражающее действие на слизистую оболочку кишечника. Перечисленные токсические агенты провоцируют дальнейшее усугубление дисбиоза, формирование микотической аллергии, вторичного иммунодефицита.
Патогенез инвазивного кандидоза кишечника иной. При условии ослабления местного и общего иммунитета грибы рода Candida интимно прикрепляются к эпителию кишечника (они имеют тропность к плоскому многослойному эпителию), затем внедряются в его толщу, трансформируясь в нитчатую форму. При наличии выраженной супрессии клеточного иммунитета Candida проникают в кровоток и распространяются по организму, вызывая висцеральный кандидоз (поражение печени, поджелудочной железы).
Симптомы кандидоза кишечника
Кандидоз кишечника встречается в трех основных клинических формах: инвазивный диффузный, инвазивный фокальный и неинвазивный. Критериями диагностики инвазивного диффузного кандидоза кишечника являются тяжелое состояние пациента на фоне выраженной интоксикации, повышение температуры тела, сильная боль в животе, диарея, примесь крови в стуле, системные проявления микоза (поражение печени, поджелудочной железы, селезенки, желчного пузыря и др.). Если эта форма кандидоза кишечника является случайной находкой во время обследования по поводу других заболеваний, в первую очередь следует думать о дебюте СПИДа или сахарного диабета. Инвазивный диффузный кандидоз кишечника не характерен для людей с нормально функционирующей системой иммунитета.
Инвазивный фокальный кандидоз кишечника может осложнять течение язвенной болезни двенадцатиперстной кишки, неспецифического язвенного колита. Заподозрить данную форму кандидоза можно у пациентов с упорным и затяжным течением фонового заболевания, не поддающегося стандартной терапии. Для этого варианта микоза характерна локальная инвазия нитчатой формы Candida в местах нарушенной эпителизации (на дне язв кишечника). При этом в окружающих тканях, других отделах кишки друзы грибов не выявляются. Клиническая картина соответствует основному заболеванию, а псевдомицелий обнаруживается случайно при гистологическом исследовании биоптатов.
Неинвазивный кандидоз кишечника является наиболее распространенной формой данного заболевания. Эта патология не ассоциируется с проникновением грибов в толщу кишечной стенки, а связана с массивным размножением Candida в просвете кишки. При этом выделяется огромное количество токсичных метаболитов, которые оказывают как местное, так и общее резорбтивное действие. Сегодня установлено, что неинвазивный кандидоз составляет примерно треть всех случаев дисбиоза кишечника. Клинически неинвазивный кандидоз кишечника протекает на фоне удовлетворительного состояния пациента, сопровождается умеренными явлениями интоксикации, дискомфортом в животе, метеоризмом, неустойчивым стулом. Часто у таких больных обостряются различные аллергические заболевания. Эту форму кандидоза зачастую путают с синдромом раздраженного кишечника.
Диагностика
Диагностика кандидоза кишечника затрудняется отсутствием типичных клинических признаков, а также достаточно специфичных и чувствительных методов выявления грибов рода Candida в образцах тканей и кале. В общем анализе крови при тяжелых формах заболевания определяется уменьшение количества лейкоцитов, лимфоцитов, эритроцитов. Обязательна консультация врача-эндоскописта для выбора оптимального метода исследования кишечника. Во время эндоскопии обычно обнаруживают неспецифические признаки поражения слизистой, поэтому решающее значение в постановке диагноза имеет эндоскопическая биопсия и морфологическое исследование биоптатов.
Трудности диагностики заключаются в том, что псевдомицелий грибов можно выявить не во всех пробах материала, поэтому достаточно часто встречаются ложноотрицательные результаты. Визуально при диффузном инвазивном кандидозе кишечника определяются признаки язвенно-некротического поражения слизистой, а при неинвазивном – катаральное воспаление. Диагностическим критерием инвазивного кандидоза кишечника служит наличие кандидозного псевдомицелия в биоптатах и отпечатках слизистой оболочки кишки.
Всем пациентам с грибковым поражением кишечника обязательно проводится анализ кала на дисбактериоз, бактериологическое исследование кала. Чаще всего эти анализы выявляют смешанную флору: не только грибы рода Candida, но и кишечную палочку, клебсиеллы, стафилококки и др. Выявление более 1000 колониеобразующих единиц на грамм патологического материала свидетельствует в пользу кандидоза кишечника и исключает носительство грибковой флоры. Основной задачей культурального исследования является установление вида возбудителя, определение чувствительности выделенной микрофлоры к антимикотикам.
Лечение кандидоза кишечника
Консультация гастроэнтеролога при кандидозе кишечника позволяет выявить факторы риска данного заболевания, определить объем необходимых исследований. Так как кандидоз кишечника не имеет специфических клинических признаков, заподозрить эту патологию бывает достаточно сложно. При наличии лабораторных свидетельств кандидоза кишечника выбор тактики лечения зависит от клинического варианта, наличия сопутствующей патологии, переносимости антимикотических препаратов. Обязательными звеньями лечебного процесса при кандидозе кишечника являются: коррекция фонового заболевания, приведшего к снижению иммунитета и активации грибковой флоры; назначение целевого противогрибкового средства; модуляция иммунитета.
Пациенты с диффузной инвазивной формой кандидоза кишечника госпитализируются в стационар. Препаратами выбора для инвазивных микозов являются азольные антимикотики (кетоконазол, флуконазол, итраконазол и пр.), которые активно всасываются из кишечника и оказывают системное действие. Начинают лечение обычно с введения амфотерицина В, затем переходят на терапию флуконазолом.
Для эрадикации грибковой флоры при неинвазивных формах кандидоза кишечника используют противогрибковые препараты нерезорбтивного действия – они плохо всасываются слизистой оболочкой кишки и оказывают сильное местное действие. Нерезорбтивные полиеновые антимикотики имеют ряд преимуществ – у них практически нет побочных действий, они не угнетают нормальную микрофлору кишечника, не вызывают привыкания. К полиеновым препаратам относят натамицин, нистатин. Так как в патогенезе неинвазивного кандидоза имеют значение состояние дисбиоза и смешанная флора, обязательно назначают противомикробные препараты, эубиотики. В качестве симптоматического лечения применяют пищеварительные ферменты, сорбенты, спазмолитики и анальгетики.
Прогноз и профилактика
При диффузной инвазивной форме кандидоза кишечника прогноз серьезный, так как она может приводить к генерализации процесса. Прогноз при инвазивном кандидозе кишечника значительно отягощается наличием тяжелых фоновых заболеваний. При остальных вариантах заболевания прогноз благоприятный при своевременном начале лечения.
Профилактика кандидоза кишечника заключается в устранении предрасполагающих к этой патологии факторов; лечении заболеваний пищеварительного тракта, приводящих к дисбиозу. Для поддержания нормальной микрофлоры кишечника следует разнообразно питаться, ограничивая содержание простых углеводов, употреблять достаточное количество клетчатки. Пациенты, входящие в группу риска по развитию кандидоза органов ЖКТ (ВИЧ, тяжелая эндокринная патология, полихимиотерапия, лечение кортикостероидными гормонами и пр.), требуют пристального внимания и регулярного обследования.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Диcбактериоз: причины появления, симптомы, диагностика и способы лечения.
Определение
Дисбактериоз, или дисбиоз – это качественное и количественное изменение микрофлоры в организме. Для него характерно увеличение или резкое уменьшение бактерий, снижение их разнообразия. Дисбактериоз может возникнуть на любом участке, где присутствуют бактерии, включая кожу, влагалище, ротовую полость и т.д.
Микрофлора играет важную роль в поддержании работы иммунной системы, но существует и обратная связь – при серьезном снижении иммунитета возникает дисбактериоз.
Причины появления дисбактериоза
В кишечнике человека присутствует от 70 до 80% клеток иммунной системы. Поэтому любая нестабильность кишечной микрофлоры может нарушить естественные защитные механизмы организма, настроенные против болезней и недомоганий.
Дисбактериоз кишечника связан не только с кишечными расстройствами, но и с множеством других состояний, на первый взгляд не относящихся к пищеварению, – кожными проблемами (акне, экзема), неврологическими расстройствами и т.д.
Среди причин развития дисбактериоза отмечают:
- Увеличение числа болезнетворных бактерий и дрожжевых грибов (например, кандида) и недостаток полезных микроорганизмов.
- Проникновение микроорганизмов, в норме находящихся в толстом отделе кишечника, в тонкий кишечник. Это происходит при хронических заболеваниях, характеризующихся поражением слизистой оболочки желудочно-кишечного тракта (болезнь Крона или неспецифический язвенный колит).
- К другим факторам врачи относят генетическую предрасположенность, несбалансированное питание с низким содержанием клетчатки, но с высоким содержанием сахара и обработанных продуктов, физический и психологический стресс, чрезмерное потребление алкоголя, частое применение антибактериальных препаратов и средств от изжоги, плохую гигиену полости рта.
- Дисбактериоз у практически здоровых лиц:
- возрастной дисбактериоз – изменения микрофлоры у людей пожилого возраста;
- сезонный дисбактериоз – изменения микрофлоры в холодное время года;
- нутритивный дисбактериоз – связанный с несбалансированным питанием;
- профессиональный дисбактериоз – при различных профессиональных вредностях.
- Дисбактериоз, сопровождающий различные заболевания органов пищеварения (желудка, поджелудочной железы, печени и желчевыводящих путей, кишечника, при синдроме мальабсорбции (нарушенном всасывании питательных веществ)).
- Дисбактериоз при других заболеваниях:
- инфекционных,
- иммунодефицитных,
- при гипо- и авитаминозах (уменьшенном поступлении в организм или плохой усвояемости необходимых витаминов),
- при интоксикациях и воздействии на организм человека радионуклидов (радиоактивных изотопов, которые можно встретить в местах с повышенным радиационным фоном, в ограниченном количестве и под строгим контролем они используются для диагностики и лечения некоторых заболеваний).
- Лекарственный дисбактериоз. Возникает вследствие приема антибиотиков, иммунодепрессантов, антацидов, антисекреторных, слабительных средств, химиотерапии и других лекарственных препаратов.
- Стрессорный дисбактериоз. Возникает как результат длительного эмоционального или физического стресса.
- Бессимптомная форма дисбактериоза.
- Локальная, или местная форма дисбактериоза. Наблюдается при развитии локального воспалительного процесса в кишечнике (у больного появляются симптомы колита или энтерита – воспалительных заболеваний толстого или тонкого кишечника).
- Распространенная форма дисбактериоза. Проявляется выраженными нарушениями пищеварения.
- 1-я степень тяжести;
- 2-я степень тяжести;
- 3-я степень тяжести;
- 4-я степень тяжести.
- Экзогенные (внешние) факторы, способствующие проникновению грибков в организм:
- профессиональные вредности, приводящие к частым повреждениям кожи;
- длительное пребывание в теплой и влажной среде;
- нарушение целостности слизистых оболочек.
- Факторы, приводящие к снижению сопротивляемости организма:
- наличие хронических заболеваний;
- длительный прием препаратов, способствующих нарушению естественной микрофлоры;
- несбалансированное питание;
- частые стрессы, нарушения режима сна и отдыха.
- Нарушения обмена веществ (гиповитаминозы), заболевания иммунной системы (ВИЧ-инфекция), эндокринные патологии (сахарный диабет и пр.).
- Длительный прием некоторых препаратов: гормональных контрацептивов, системных глюкокортикостероидов, антибиотиков широкого спектра действия, цитостатиков.
- Длительное пребывание или проживание в местности с повышенной влажностью и температурой, комфортными для циркуляции спор грибков в окружающей среде.
- Урогенитальный кандидоз.
- Кандидоз слизистой оболочки полости рта.
- Поверхностный кандидоз.
- Межпальцевый кандидоз.
- Кандидоз околоногтевых валиков и ногтей.
- Кандидоз желудочно-кишечного тракта.
- Появление бело-желтых творожистых или сливкообразных выделений из половых путей. Интенсивность выделений может усиливаться перед менструацией, что связано с изменением гормонального фона.
- Неприятные ощущения, зуд в области гениталий, зачастую усиливающиеся при половом контакте или мочеиспускании.
- Покраснение и отечность слизистой вульвы и влагалища, наличие повреждений на коже половых органов (трещины, микротравмы).
- При хроническом течении УГК развивается сухость слизистых оболочек половых путей.
- Покраснение, отечность, неприятные ощущения в области половых органов.
- Беловатые выделения творожистой структуры из половых путей.
- Боль и жжение при половом контакте и при мочеиспускании.
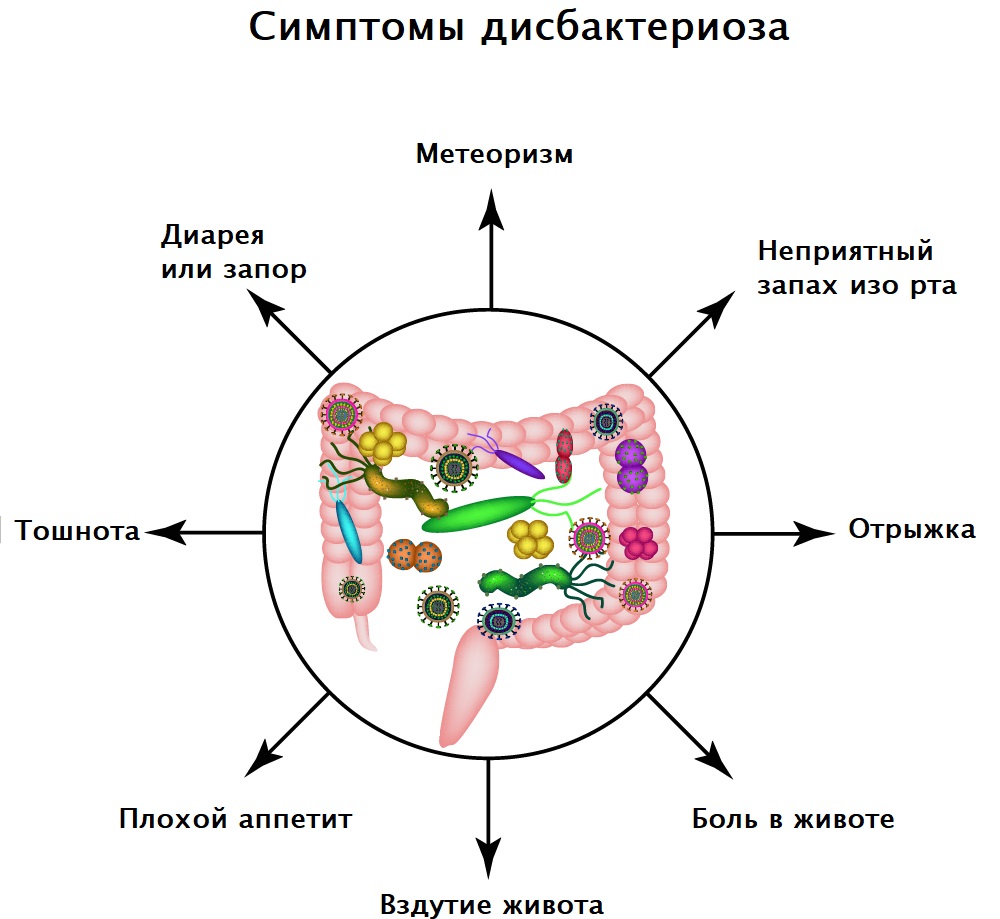
Симптомы дисбактериоза зависят от формы и степени тяжести течения заболевания. Пациенты могут предъявлять жалобы на расстройство желудка, тошноту, диарею или запор, повышенное газообразование и вздутие живота, снижение аппетита, необъяснимую усталость и проблемы с концентрацией внимания, неприятный запах изо рта, высыпания на коже.
Диагностика заболевания
При постановке диагноза врач обращает внимание на жалобы, симптомы заболевания и результаты осмотра. Но для оценки степени тяжести дисбактериоза обычно требуются лабораторные и инструментальные обследования.
-
Клинический анализ крови с развернутой лейкоцитарной формулой.
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Кандидоз: причины появления, симптомы, диагностика и способы лечения.
Кандидоз – инфекционное заболевание, вызываемое дрожжеподобными грибками рода Candida. Оно обусловлено активным размножением грибка на слизистых оболочках полости рта, половых и внутренних органов и на коже.
Все представители рода Candida относятся к условно-патогенным микроорганизмам, то есть они постоянно присутствуют в составе нормальной микрофлоры. Но при снижении иммунитета, изменении гормонального фона и по ряду других причин эти грибки могут начать активно колонизировать слизистые оболочки и кожу.
Наиболее распространенные представители рода – Candida albicans и C. tropicalis. В 90-95% случаев урогенитального кандидоза именно C. albicans является доминирующим возбудителем.
![shutterstock_714362212 [преобразованный].jpg](https://www.invitro.ru/upload/medialibrary/d29/d29b49ccfe770f215bf7b01b406a2d2f.jpg)
Первый контакт с грибками рода Candida происходит во время прохождения ребенка по родовым путям. Однако в медицинской литературе описаны случаи обнаружения этих микроорганизмов в околоплодных водах, что свидетельствует о возможности вертикального (трансплацентарного) пути передачи. Также встречается передача грибка рода Candida при грудном вскармливании, кожном контакте ребенка с матерью, бытовым и пищевым путями.
Эти микроорганизмы вырабатывают эндотоксины и ферменты, вызывающие гибель клеток и некроз тканей, что способствует усилению адгезивной (прикрепление к клеткам слизистых оболочек или кожи) способности грибка и обеспечивает проникновение в ткани.
Гиперпродукция этих и ряда других веществ обуславливает патогенность представителей семейства Candida.
Причины возникновения кандидоза
По локализации процесса выделяют:
Урогенитальный кандидоз (УГК) – широко распространенное заболевание: по данным медицинской статистики, около 75% женщин репродуктивного возраста хотя бы единожды регистрировали у себя симптомы УГК.
Выделяют острую и хроническую форму урогенитального кандидоза, кандидоз вульвы, вагины и других урогенитальных локализаций. В ряде случаев при диагностике используют уточнение: осложненный или неосложненный УГК, что отражает количество обострений в год и степень выраженности заболевания.
Симптомы женского урогенитального кандидоза
Межпальцевый кандидоз локализуется в пространстве между пальцами. При этом отмечается покраснение участков кожи с последующим появлением пузырьков в прозрачным содержимым. Заболевание быстро распространяется в тесных коллективах (в детских садах, школах и т. д.).
Кандидоз слизистой оболочки полости рта (КСОПР)
Кандидоз полости рта вызывает неприятные ощущения, особенно при приеме пищи – жжение, боль, сухость. В зависимости от локализации процесса выделяют несколько форм кандидоза полости рта.
Часто КСОПР и желудочно-кишечного тракта сопровождает иммунодефицитные состояния: ВИЧ-инфекцию, синдром приобретенного иммунодефицита человека (СПИД) или врожденный иммунодефицит (например, при патологии Т-лимфоцитов). При наличии этих заболеваний кандидоз протекает с максимально выраженными симптомами, с трудом поддается лечению, носит агрессивный характер.
Самое частое проявление КСОПР – кандидозный стоматит, поражающий в основном грудных детей и взрослых с ослабленным иммунитетом.
При этой патологии слизистая оболочка полости рта краснеет, отекает, на ней появляются белесоватые пленки, имеющие творожистую консистенцию. На начальных стадиях болезни налет легко снимается. С течением заболевания пленки становятся плотнее, отделяются с трудом, при снятии обнажается кровоточащая слизистая оболочка.
При кандидозном стоматите возможно поражение языка, что проявляется покраснением спинки языка, появлением налета и слущиванием эпителия. Эти симптомы сопровождаются сильными болевыми ощущениями пораженной области при разговоре, приеме пищи и при пальпации (прощупывании) языка.
У курильщиков чаще других видов КСОПР развивается хронический гиперпластический кандидоз, сопровождаемый образованием белых, сливающихся между собой бляшек, которые возвышаются над поверхностью гиперемированной слизистой.
При этой патологии изменяется консистенция слюны: она становится вязкой и пенящейся; появляются неприятный запах изо рта, налет на слизистой серого или белого цвета. В 10-40% случаев эта клиническая форма кандидоза малигнизируется (т. е. приобретает злокачественный характер).
У пожилых людей чаще всего развивается хроническая атрофическая форма кандидоза полости рта. Слизистая оболочка при этом краснеет и отекает. Поражение часто локализуется под зубными протезами, что вызывает болевые ощущения.
Кандидозный хейлит и кандидоз углов рта в основном встречаются у детей и пожилых. Поражение обычно двустороннее, при этом образуются красные болезненные трещины в углах рта, покрытые легко снимающимся белым налетом или чешуйками. При длительном течении заболевания возможно присоединение бактериальной инфекции.
Диагностика кандидоза
Алгоритм диагностического поиска при кандидозе любой локализации включает в себя взятие материала с пораженной области с последующей его микроскопией, посевом для определения вида грибка и его чувствительности к антимикотическим (противогрибковым) препаратам.
В целях диагностики состояний, приведших к снижению иммунитета, используется общий анализ крови;
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Читайте также:

