Какой анализ на вирус папилломы человека сдавать при эрозии шейки матки
Обновлено: 18.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
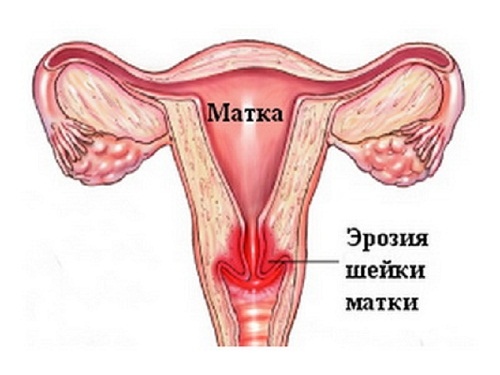
Эрозия шейки матки: причины появления, симптомы, диагностика и способы лечения.
Определение
В структуре гинекологических заболеваний патология шейки матки занимает ведущее место. По своей сути эрозия представляет собой язву, ранку на поверхности шейки матки. Эрозия может быть травматической, инфекционной, воспалительной, химической и т.п. Однако термин «эрозия» исторически, к сожалению, подразумевает практически всю линейку патологических состояний на шейке матки. Но чаще всего с этим понятием все-таки связывают диагноз «эктопия цилиндрического эпителия шейки матки».
Эктопия (псевдоэрозия) — заболевание шейки матки, при котором происходит смещение границ между плоским эпителием, расположенным на поверхности шейки матки, и цилиндрическим эпителием, выстилающим цервикальный канал, на влагалищную часть шейки матки. Эктопия встречается примерно у 40% женщин и не является патологией.
Для того чтобы понять, что такое эктопия, необходимо обратиться к анатомии. Между телом матки и влагалищем располагается шейка – канал, который соединяет эти два органа. Изнутри шейка матки выстлана цилиндрическим эпителием, клетки которого расположены в один слой. Наружная часть шейки матки покрыта многослойным плоским эпителием. Все болезни на шейке матки затрагивают зону перехода этих двух видов эпителия, называемую зоной трансформации. Эта зона является входными воротами для бактериальной и вирусной инфекции, «платформой» для развития диспластических конфигураций в шейке матки.
Перемещение цилиндрического эпителия за пределы цервикального канала на внешнюю часть шейки матки называется эктопией.
Причины появления эрозии шейки матки
В период развития половой системы у новорожденной девочки отмечается перемещение цилиндрического эпителия за наружный маточный зев и его расположение в виде овала вокруг наружного зева. В таких случаях говорят о врожденной эктопии, что является очень распространенным физиологическим явлением шейки матки. Цилиндрический эпителий попадает в несвойственную ему кислую среду влагалища и выглядит как ярко-красное пятно на шейке матки, поэтому создается обманчивое впечатление эрозии этого участка.
Эктопия цилиндрического эпителия — нормальное состояние для девушек и женщин до 23 лет. У большинства девочек эктопия присутствует перед первой менструацией и сохраняется длительное время. В детородном возрасте граница цилиндрического и плоского эпителия в большинстве случаев отходит к наружному зеву шейки матки. Эктопия шейки матки чаще всего выявляется у молодых женщин, у женщин старше 40 лет встречается реже.
Истинная эрозия — заболевание шейки матки, при котором наблюдается дефект слизистого слоя, покрывающего влагалищную часть шейки матки, ярко красного цвета, неправильной формы, с относительно четкими границами, который легко травмируется и кровоточит.
Появлению эрозии способствуют нарушения гормонального фона (низкий уровень женских половых гормонов), механические воздействия (например, грубые половые контакты), некоторые инфекционные заболевания. Эрозивные очаги похожи на неглубокие язвы.
Поскольку клетки слизистой хорошо регенерируют (восстанавливаются), обычно эрозия заживает, замещается цилиндрическим эпителием уже в течение недели и формирует зону эктопии шейки матки. Незаживающая истинная эрозия встречается редко (примерно у 1% женщин, чаще в постменопаузе, а также при атрофических процессах, после лучевой терапии, химического или электрического ожога) и требует наблюдения и лечения.
Классификация заболевания
- фолликулярная (железистая) эктопия, то есть состоящая из железистых ходов (крипт) и кист;
- железисто-папиллярная эктопия, поверхность которой покрыта разрастаниями цилиндрического эпителия;
- врожденная эктопия, формирующаяся под влиянием высокого уровня гормонов материнского организма. Нередко врожденная псевдоэрозия самоликвидируется, когда цилиндрический эпителий втягивается назад в цервикальный канал;
- приобретенная эктопия – самоизлечение такого вида эрозии тоже возможно, но маловероятно.
- с инфекционными факторами при раннем начале половой жизни, большом количестве половых партнеров, наличии в анамнезе воспалительных заболеваний половых органов;
- с травматическими факторами (травмами шейки матки во время родов и абортов, применением барьерных методов контрацепции);
- с нарушением гормонального фона (ранним началом менструаций, нарушениями менструального цикла и репродуктивной функции);
- с изменениями иммунного статуса (наличием хронических заболеваний, профессиональных вредностей).
Симптомы эрозии шейки матки
В большинстве случаев заболевание никак себя не проявляет и протекает бессимптомно, поэтому диагностировать эрозию шейки матки можно только во время осмотра врачом-гинекологом.
Цилиндрический эпителий канала шейки матки секретирует слизь, поэтому при эктопии шейки матки может увеличиться количество обычных слизистых выделений из влагалища. Если к эктопии присоединяется инфекция, то выделения приобретают желтоватый оттенок.
Поверхность эктопированного цилиндрического эпителия достаточно ранима и легко кровоточит, поэтому при обширных, длительно существующих эрозиях могут наблюдаться кровянистые выделения из влагалища (вне менструации) после полового акта и физических нагрузок.
При беременности и во время приема гормональных противозачаточных средств в эктопии могут формироваться отечные полипозные конфигурации в виде гиперплазированных вытянутых сосочков.
Диагностика эрозии шейки матки
Врач может определить наличие изменений шейки матки при осмотре с помощью гинекологического зеркала и кольпоскопии. Основные (обязательные) диагностические обследования, которые необходимо ежегодно проходить женщине на амбулаторном уровне:
- общий гинекологический осмотр;
- мазок на степень чистоты влагалища. Анализ исключает или подтверждает воспалительный процесс, определяет количество полезных и патогенных микроорганизмов. Обязательно назначается при осложненной форме эрозии с симптомами зуда и нетипичными выделениями. Благодаря этому мазку выявляются сопутствующие инфекционные заболевания;
В норме влагалище у новорождённых девочек в первые часы жизни стерильно. К концу первых суток после рождения оно заселяется аэробными и факультативно-анаэробными микроорганизмами. Микрофлора влагалища здоровых женщин репродуктивного возраста включает широкий спектр микроаэрофилов, факульта.

Итак, если вы дочитали статью до этой части, вы наверняка почерпнули немало полезной информации, а самое главное – правдивой и современной, о вирусе папилломы человека, предраковых и раковых состояниях шейки матки и о пресловутой вакцине от рака шейки матки. Давайте подведем итоги выше сказанного, чтобы перейти к практическим рекомендациям, которыми могут воспользоваться как женщины, так и врачи, желающие повысить свой уровень знаний по этим вопросам.
• Эрозия шейки матки не является предраковым состоянием и в рак шейки матки не переходит. Этот термин не используется в современной гинекологии.
• Предраковое состояние шейки матки включает всего лишь один вид состояний – тяжелую дисплазию.
• Термин «дисплазия» является устаревшим и заменен термином «интраэпителиальное поражение».
• Диагноз этого предракового состояния является лабораторным диагнозом – его не возможно поставить на глаз, а только с помощью исследования тканевого покрова шейки матки – цитологически и/или гистологически.
• Ни эктопия, ни полип, ни лейкоплакия, ни легкая дисплазия не относятся к предраковым состояниям шейки матки, поэтому не требуют срочного лечения, а тем более хирургического лечения.
• Из 40 типов ВПЧ, поражающих аногенитальную область человека, в возникновении рака шейки матки чаще всего участвуют ВПЧ 16 и ВПЧ 18, а в возникновении генитальных бородавок – ВПЧ 6 и ВПЧ 11.
• Генитальные бородавки не переходят в рак и являются доброкачественным процессом.
• Натуральный жизненный цикл вируса ВПЧ является безвредным для организма человека. • ВПЧ-инфекция обнаруживается у 70-80% молодых людей, ведущих половую жизнь.
• 90% женщин с ВПЧ-инфекцией избавляются от вируса ВПЧ без негативных последствий для их организма.
• У 10% женщин с персистирующей ВПЧ инфекцией случаи рака возникают чрезвычайно редко, хотя могут быть отклонения в цитологических мазках.
• Лечения ВПЧ-инфекции не существует.
• В целом, 99.9% женщин никогда не заболеют раком шейки матки, независимо от того, были ли они хоть когда-то инфицированы ВПЧ или нет.
• Рак шейки матки является редким заболеванием.
• На развитие рака из состояния тяжелой дисплазии уходит не меньше 15-20 лет, поэтому спешки в диагностике и лечении при обнаружении ВПЧ или незначительных отклонений в цитологии не должно быть.
• ВПЧ-инфекция сама по себе не является показателем для проведения хирургического лечения шейки матки (прижигание, замораживание, лазер, радиоволновая терапия), если у женщины не обнаружена тяжелая дисплазия.
• Существует две вакцины – ВПЧ4 (Гардасил) и ВПЧ2 (Цервиракс) для профилактики ВПЧ-инфекции и рака шейки матки.
• Эффективность ВПЧ-вакцин не наблюдается после 3-4 лет.
• Более продолжительные периоды (до 10 лет) эффективности вакцины не доказаны.
• ВПЧ-вакцины являются лекарственными препаратами, поэтому их назначение должно быть с учетом строгих противопоказаний. Женщины и мужчины должны предупреждаться о побочных явлениях прививания.
• Применение вакцины при беременности или в период планирования беременности противопоказано.
• Эффективность прививания не может быть достигнута, если не введены все три дозы вакцины. Полное прививание (три дозы) проходит только незначительное количество женщин.

Конечно, можно сделать и другие выводы, и каждый читатель наверняка сделает свои собственные выводы.
Мы подошли к вопросу, как на фоне этих многочисленных противоречивых фактов, этого панического страха перед раковыми заболеваниями, коммерческого влияния фармацевтических магнатов на современных ученых, врачей и многих других людей найти оптимальный план-стратегию по выявлению рака шейки матки? Я предлагаю вам алгоритм обследования и наблюдения женщин, который поддерживают многие прогрессивные врачи. Эти рекомендации могут кардинально отличаться от тех, которыми руководствуются ваши врачи. Однако они основаны на серьезном рациональном подходе с учетом имеющихся научных данных по вопросам ВПЧ-инфекции и рака шейки матки. Это ваше личное дело руководствоваться этими рекомендациями или пользоваться старыми, ибо ваше здоровье в ваших руках.
Прививаться или не прививаться от ВПЧ-инфекции?
Мое личное мнение, которое совпадает с мнением многих врачей, возраст в 9-12 лет не является рациональным, т.е. оптимальным, для проведения вакцинации. Во внимание также должно приниматься желание самого подростка быть привитым без манипулирования его решением через запугивание, что, если ребенок не будет вакцинирован, то у него обязательно возникнет рак. Это ответственность каждого родителя строить здоровые отношения со своими детьми и обучать их здоровому образу жизни, в том числе вопросам половых отношений и половой гигиены.
Женщинам до 30 лет, которые имеют половые отношения с одним постоянным партнером и у которых не обнаружен ВПЧ, вакцинация не обязательна и выбор должен оставаться всегда за женщиной. Манипулирование решением с использованием аргумента, что партнер женщины может изменять ей и впоследствии заразить ВПЧ, являются неэтичным.
Женщинам после 30 лет ВПЧ-вакцина не показана.
У женщин, у которых обнаружен ВПЧ 16 и/или ВЧП 18, прививание не будет эффективным в отношении защиты от предраковых и раковых состояний шейки матки. Защитный эффект может быть только от ВПЧ 6 и ВПЧ 11, если они ими не заражены. При наличии других типов ВПЧ применение вакцины также не эффективно.
Из-за отсутствия достоверных данных о продолжительности защитного действия ВПЧ вакцины, женщины и мужчины должны знать, что клинически эффект вакцины наблюдается только в течение 3-4 лет. Нужна ли дополнительная ревакцинация – убедительных данных по этому вопросу не существует.
Как и когда проводить скрининг на раковые заболевания?
Цитологическое исследование женщин должно начинаться с 21 года, независимо от того, в каком возрасте до этого женщина начала половую жизнь.
ВПЧ-тестирование является дополнительным методом скрининга и в комбинации с цитологическим исследованием позволяет выявить от 88 до 95% тяжелых дисплазий. Однако наличие ВПЧ не является показанием для дополнительного обследования и лечения при нормальных результатах цитологии.
Теперь рассмотрим возможную комбинацию результатов анализов:
Цитологическое исследование – норма
ВПЧ – отрицательный
Повторное цитологическое исследование можно провести через 3 года.
Цитологическое исследование – норма
ВПЧ – положительный
Повторное цитологическое исследование можно провести через 1-2 года.
Цитологическое исследование – атипические клетки
ВПЧ – отрицательный
Провести микробиологическое исследование, исключить другие влагалищные инфекции или при наличии пролечить. Повторный цитологический мазок – через 6-12 месяцев.
Цитологическое исследование – атипические клетки
ВПЧ – положительный
Провести микробиологическое исследование, исключить другие влагалищные инфекции или при наличии пролечить. Повторный цитологический мазок – через 3-6 месяцев.
Цитологическое исследование – легкая дисплазия
ВПЧ – отрицательный
Повторное цитологическое исследование через 6-12 месяцев.
Цитологическое исследование – легкая дисплазия
ВПЧ – положительный
Можно провести кольпоскопию, но не обязательно. Повторное цитологическое исследование через 3-6 месяцев. Биопсия при легких дисплазиях не показана.
Цитологическое исследование – умеренная дисплазия
ВПЧ – отрицательный или положительный
Необходимо провести кольпоскопию. При подозрении на тяжелую дисплазию рекомендована биопсия. Цитологическое исследование повторить через 3-6 месяцев.
Цитологическое исследование – тяжелая дисплазия
ВПЧ – отрицательный или положительный
Рекомендована кольпоскопия и биопсия. При подтверждении диагноза кольпоскопически и гистологически, проводится хирургическое лечение шейки матки одним из имеющихся методов (прижигание, замораживание, лазер, радиоволновая терапия, реже конизация). Если гистологически тяжелая дисплазия не подтверждена, повторное цитологическое исследование и кольпоскопию проводят через 3 месяца.
При обнаружении рака женщина должна быть направлена к онкологический диспансер незамедлительно.
Небольшое дополнение о кольпоскопии: с помощью этого метода без дополнительных обследований можно выявить умеренные и тяжелые дисплазии эпителия ШМ только в 2/3 случаев. Считается, что врач, чтобы начать самостоятельный кольпоскопический осмотр ШМ, должен провести не менее 200 кольпоскопий под наблюдением высококвалифицированного врача-кольпоскописта и поддерживать свой профессиональный уровень, проводя не менее 25 кольпоскопий в год.
Биопсия с гистологическим исследованием биоптированного препарата имеет строгие показания и противопоказания — это инвазивный метод обследования, поэтому проводится только после получения письменного или словесного согласия пациента. После биопсии женщине следует избегать коитуса в течение 7-10 сут для предупреждения инфицирования и дополнительной травматизации биоптированного участка.
Если женщина привита от ВПЧ, приоритетом действий врача всегда должны быть результаты цитологического мазка, а не наличие или отсутствие ВПЧ инфекции. Поэтому прививание женщины от ВПЧ инфекции не устраняет необходимость таких женщин проходить цитологическое исследование регулярно.
Женщины в возрасте 65-70 лет и старше при наличии 10-летней истории (3 цитологических мазков каждые 3 года) нормальных результатов цитологии могут прекратить скрининг на предраковые и раковые заболевания шейки матки. Исключение составляют женщины, ведущие активную половую жизнь и имеющие несколько половых партнеров.
Таким образом, из всех состояний шейки матки хирургического лечения требуют только тяжелая дисплазия и рак. Рак insitu (стадия 0) не считается инвазивной формой рака, поэтому чаще всего его лечение проводят с сохранением матки.
Когда врачи спешат с прижиганиями и прочими хирургическими вмешательствами, запугивая возможным развитием рака, я всегда советую таким женщинам снять очки страха и включить в своем сознании-мышлении систему безопасности для собственного тела. Сначала необходимо обследование (если оно действительно необходимо, потому что достаточно просто пересдать цитологический мазок через несколько месяцев), а уже потом — «кромсанье» шейки на части, но не наоборот. Если у вас нет тяжелой дисплазии, а врач настойчиво давит на вашу психику хирургическим лечением, постарайтесь забыть дорогу к такому врачу.
Также, мало кто из врачей объясняет молодым перепуганным пациенткам, что хирургическое лечение шейки матки имеет немало осложнений. Что это за осложнения?
• бесплодие из-за стеноза цервикального канала, уменьшения выработки цервикальной слизи, функциональной неполноценности ШМ и вторичной трубной дисфункции вследствие восходящей инфекции;
• формирование рубцов ШМ и ее деформация;
• возникновение карциномы из-за неполного или неточного обследования;
• нарушение менструальной функции;
• обострение воспалительных заболеваний мочеполовой системы;
• преждевременные роды и преждевременный разрыв плодных оболочек (значительный риск этого осложнения наблюдается после ДЭК и криодеструкции, поэтому врач должен серьезно подходить к выбору лечения у женщин репродуктивного возраста, особенно нерожавших, у которых хирургическое лечение может быть отложено на определенный период времени).
Если вы прошли хирургическое лечение (по показаниям или без них), важно понимать, что на восстановление покровного эпителия шейки матки необходимо время. В течение всего периода выздоровления (минимум 4 нед) женщина не должна поднимать тяжести, пользоваться тампонами, спринцеваться, жить половой жизнью, так как все это провоцирует травматизацию с последующим кровотечением, инфекционные процессы ШМ. Нормальная гистологическая картина шеечного эпителия восстанавливается у 60% женщин через 6 недель после лечения, у 90% – через 10 недель. Цитологический мазок необходимо повторять не раньше чем через 3-4 месяца после лечения. Процесс заживления ШМ после оперативного лечения порой длится до 6 месяцев, поэтому раннее кольпоскопическое или цитологическое обследование иногда приводит к ложно-положительным результатам и необоснованному подозрению на наличие остаточных явлений цервикальной интраэпителиальной неоплазии.
В заключение мне бы хотелось акцентировать ваше внимание на вопросах профилактики рака шейки матки. Кто-то из вас удивится: разве не посвящена этому вся статья и разве не для этого созданы вакцины. Как раз вся беда в том, что почти вся мировая общественность, особенно медицинская, зациклена на прививках от ВПЧ. Знаете почему? Потому что за этим кроется получение дохода. А как на счет других методов профилактики? Разве их нет или они неэффективны? Они есть, но они не приведут к созданию дохода коммерчески-настроенных врачей и фармакологических компаний. Они могут сохранить немало денег их владельцам, но для многих людей проще положить пилюлю в рот или сделать укольчик, чем начать и вести постоянно здоровый образ жизни. Поэтому сами же люди становятся врагами собственного тела.
Что же это за другие виды профилактики, если речь не идет о вакцинах? Я уже упоминала о факторах риска по развитию предраковых и раковых состояний ШМ. Если влияние этих факторов устранить или уменьшить, понизится и шанс возникновения рака. Давайте еще раз посмотрим на эти факторы риска, но уже через призму профилактики рака ШМ. Что мы можем изменить, где можно провести серьезную работу?
• Большое количество родов – количество родов во многих странах уменьшается, потому что современные женщины не хотят рожать больше 1-2 детей, однако важно уменьшить количество абортов, потому что они тоже могут сопровождаться травматизацией шейки матки. Кроме того, правильное ведение родов убережет многих женщин от разрывов шейки матки – это полностью зависит от квалификации врачей и акушерок.
• дефицит витаминов А, С и β-каротина в питании женщин – рациональное питание поможет в предотвращении не только рака ШМ, но и многих других заболеваний;
• длительное (более 5 лет) использование гормональных контрацептивов – пролиферативное влияние эстрогенного компонента КОК – многие врачи до сих пор назначают старые формы контрацептивов с высоким содержанием гормонов. Повышение уровня образования и опыта врачей и женщин в вопросах современной контрацепции поможет уменьшить негативное влияние гормональной контрацепции на организм женщины;
• женщины, у партнеров которых обнаружен рак головки полового члена, который в ряде случаев может быть вызван ВПЧ онкогенных типов – рак головки полового члена встречается чаще у тех мужчин, которые вели или ведут беспорядочную половую жизнь с частой сменой партнеров.Женщины не виноваты в том, что их здоровье во многом зависит от ответственности их супругов как половых партнеров, и научить мужчин рациональности и осторожности в половой жизни или предотвратить супружескую измену – не просто, однако остается регулярный цитологический скрининг у женщин, партнеры которых имеют или имели рак головки полового члена;
• иммунодефицитные состояния, включая СПИД, а также применение медикаментов, подавляющих иммунитет (пересадка органов, лечение онкологических заболеваний и др.) – когда лечение необходимо, то деваться некуда, но чрезмерное увлечение стероидными препаратами, антибиотиками, биостимуляторами к добру не приводит, Контроль применения препаратов, которые могут понижать защитные силы организма – это важная задача как врачей, так и людей, которые пользуется этими препаратами;
• индивидуальная генетическая предрасположенность к гинекологическим злокачественным процессам – встречается редко, но здесь важно обращать внимание на историю заболеваемости раком шейки матки у близких родственников;
• инфекции, передающиеся половым путем, которые нередко могут подавлять защитные механизмы покровного эпителия шейки матки – профилактика полностью зависит от самого человека, вступающего в половые отношения, и его уровня знаний, обеспокоенности о том, как можно уберечь себя от половых инфекций; Просветительная работа здесь не помешает;
• вирус папилломы человека (ВПЧ) – чаще всего передается через секс, все зависит от самого человека – насколько он понимает важность и необходимость защитных мер от разного рода половых инфекций;
• количество половых партнеров (больше трех) — количество никогда не отражается лучшим качеством, и философский закон отражается и на уровне половых отношений: важно не количество половых партнеров, от которых можно заразиться многими заболеваниями, а стабильные качественные половые отношения с одним партнером.
• курение (активное и пассивное) – курение имеет связь со многими серьезными заболеваниями, поэтому бросайте курить, если вы до сих пор курите, и это понизит ваш риск про развитию рака шейки матки, если вы женщина, значительно;
• наличие в анамнезе цитологических мазков с отклонениями от нормы – чем чаще и больше таких отклонений, тем больший шанс развития рака, поэтому цитологическое исследование – это не только метод диагностики, но и метод профилактики рака ШМ;
• низкий социальный уровень – плохая гигиена, в том числе половой жизни, беспорядочная половая жизнь, отсутствие своевременного и качественного медицинского обслуживания – государственные программы необходимо развивать и направлять в сторону улучшения жизни людей с низким социальным уровнем. Тогда не будет роста туберкулеза, половых инфекций, преступлений и многих других социальных проблем;
• паттерн сексуального поведения – бисексуалы, гомосексуалисты, беспорядочная половая жизнь – люди сами выбирают сексуальную ориентацию, и их нельзя за это наказывать, но обучение защиты от половых инфекций и создание стабильных, длительных половых отношений поможет предотвратить те виды рака, которые вызываются ВПЧ;
• первый половой акт в раннем возрасте (до 16 лет) – половое образование подростков зависит в первую очередь от родителей, их отношений с детьми и наличия доверия. В школах должны быть введены более эффективные программы по вопросам сексуального образования. Средства массовой информации должны пропагандировать не развратную жизнь пиарной элиты и всякого рода «звезд», а принимать участие в моральном, духовном и телесном оздоровлении нации.
Ваше здоровье – в ваших руках, а ваши знания – это ваша сила, которая защитит вас по жизни от искусственно созданных проблем. Берегите себя!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Напоминаем вам, что самостоятельная интерпретация результатов недопустима, приведенная ниже информация носит исключительно справочный характер
Определение ДНК вируса папилломы человека: показания к назначению, правила подготовки к сдаче анализа, расшифровка результатов и показатели нормы.
Показание к назначению исследования
Вирусы папилломы человека (ВПЧ) - это группа генетически разнообразных ДНК-содержащих вирусов, относящихся к семейству Papillomaviridae и поражающих эпителий кожных покровов и слизистых оболочек ротовой полости и аногенитальной зоны.
Инфицирование вирусом папилломы человека клинически может проявляться остроконечными кондиломами, папилломами или злокачественной трансформацией клеток. По данным, которые приводит Всемирная организация здравоохранения, 50-80% населения инфицировано ВПЧ, а 5-10% из них имеют клинические проявления заболевания.
Наследственный материал (геном) вируса папилломы человека заключен в белковую оболочку, состоящую из больших (L1) и малых (L2) структурных белков. В зависимости от строения генома L1 были выявлены и описаны различные типы вируса папилломы человека. К настоящему времени выявлено и описано более 200 генотипов вируса папилломы человека, около 45 из них могут инфицировать эпителиальный слой урогенитального тракта.
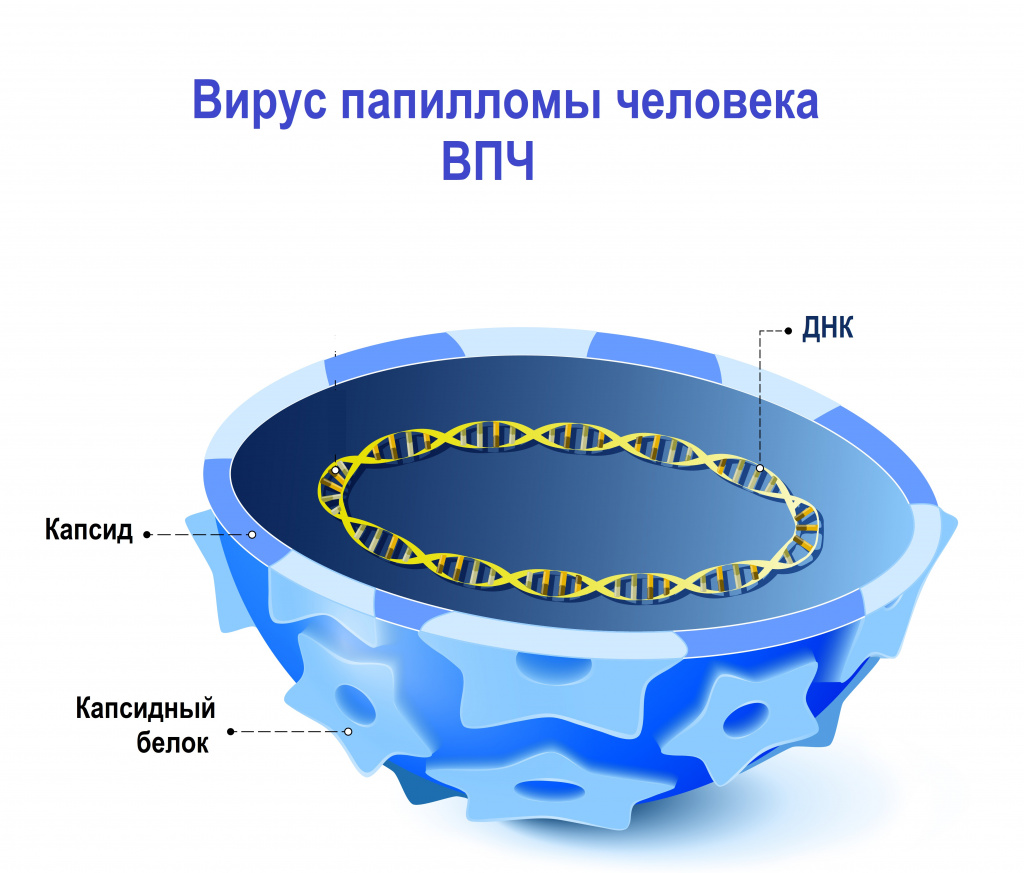
ВПЧ обладает тропностью (свойством поражать определенные органы и/или ткани) к коже и слизистым оболочкам. Источником возбудителя инфекции является больной человек или вирусоноситель.
Основной путь передачи возбудителя - половой (генитально-генитальный, мануально-генитальный, орально-генитальный), однако возможна передача и при соприкосновении (при кожном контакте). Кроме того, ВПЧ может передаваться от матери плоду во время родов.
Риск передачи при однократном половом контакте равен 80% - особенно у девушек, не достигших половой зрелости, из-за особенностей строения эпителия шейки матки в юном возрасте.
Факторы, способствующие инфицированию вирусом папилломы человека и развитию заболевания:
- раннее начало половой жизни;
- частая смена половых партнеров;
- сопутствующая урогенитальная инфекция и нарушение биоценоза влагалища;
- частые роды и аборты;
- иммунодефицитные состояния;
- генетическая предрасположенность и гормональные факторы.
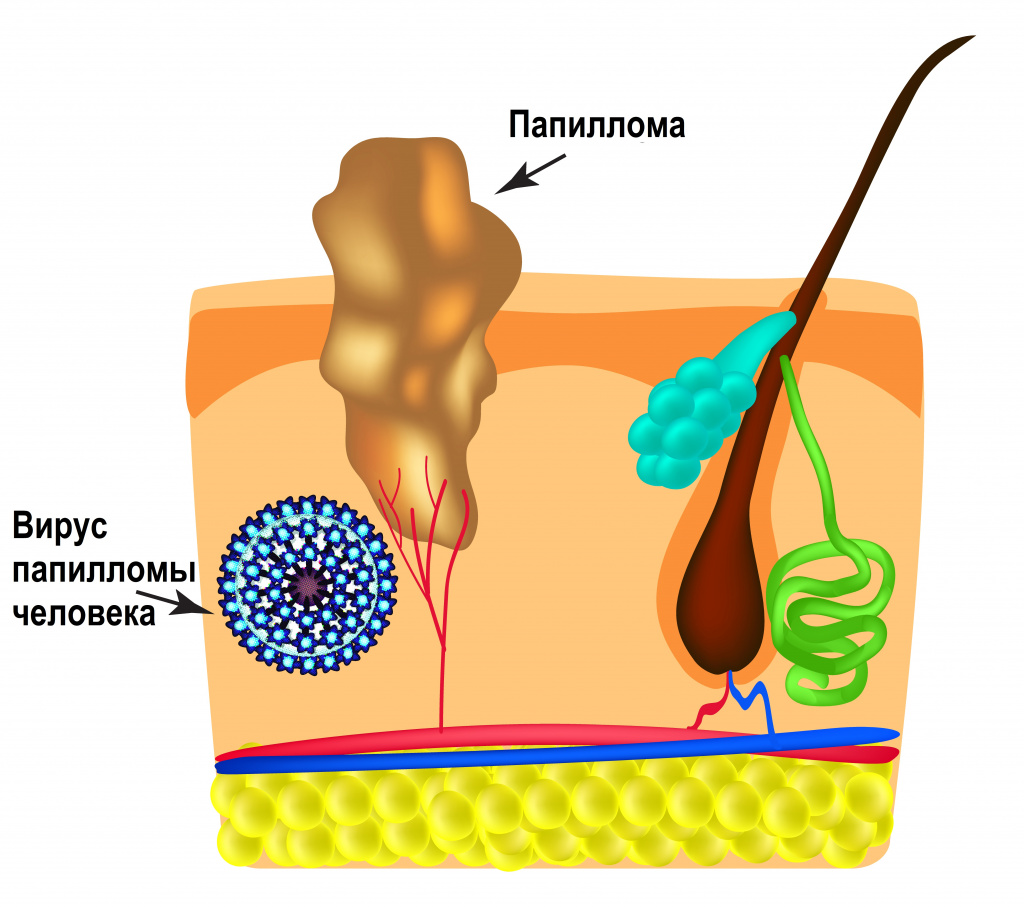
Интервал между инфицированием ВПЧ и инвазивным (проникающим) раком составляет около 10 лет или более.
Инвазивному раку предшествуют предраковые поражения шейки матки, вульвы, влагалища, анального канала, полового члена различной степени тяжести.
Вирус папилломы человека не проникает в кровь, поэтому инфекционный процесс протекает без развития воспалительной реакции.
Выделяют вирусы высокого онкогенного (или канцерогенного) риска (типы 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59) и низкого онкогенного риска (типы 6, 11, 42, 43, 44).
Типы ВПЧ низкого канцерогенного риска связаны с развитием остроконечных кондилом, папиллом и дисплазиями легкой степени. Типы ВПЧ высокого канцерогенного риска, наряду с остроконечными кондиломами и дисплазиями, также могут вызывать злокачественную трансформацию эпителия, приводя к развитию рака.
Например, высокоонкогенные типы ВПЧ 16 и 18 вызывают в 70% случаев рак шейки матки, в 80% рак вульвы и влагалища, в 92% анальный рак, в 95% рак ротовой полости, в 89% рак ротоглотки, в 63% рак полового члена. Генотипы ВПЧ 6 и 11 обуславливают практически все виды аногенитальных бородавок и большинство случаев рецидивирующего респираторного папилломатоза.
Таким образом, дифференцированное определение ДНК вируса папилломы человека назначают в следующих случаях:
- для подтверждения ВПЧ при наличии папилломатозных разрастаний и изменений на слизистых оболочках половых органов;
- для скрининга (обследования лиц, не считающих себя больными) с целью выявления скрыто протекающего заболевания;
- для контроля эффективности проводимой терапии.
- с 21 года до 29 лет - не реже 1 раза в 3 года;
- с 30 до 69 лет - не реже 1 раза в 5 лет.
Высокая сексуальная активность предполагает проведение скрининга с18 лет.
Подготовка к процедуре
Обследование женщин целесообразно проводить в первую половину менструального цикла, но не ранее 5-го дня. Допустимо обследование во второй половине цикла, но не позднее, чем за 5 дней до предполагаемого начала менструации.
Накануне и в день обследования пациентке не рекомендуется спринцевать влагалище. Забор биоматериала не следует осуществлять ранее 24-48 часов после полового контакта, интравагинального УЗИ и кольпоскопии.
Соскоб из уретры проводят до или через 2-3 часа после мочеиспускания.
Мужчинам необходимо исключить половые контакты за 1–2 суток до взятия мазка (соскоба). Нельзя мочиться в течение 1,5-2 часов до процедуры.
Срок исполнения
До 2 рабочих дней, указанный срок не включает день взятия биоматериала.
Что может повлиять на результат
В случае несоблюдения правил подготовки полученный результат может быть некорректным.
Дифференцированное определение ДНК ВПЧ (вируса папилломы человека, Humanpapillomavirus, HPV) 21 типа (6, 11, 16, 18, 26, 31, 33, 35, 39, 44, 45, 51, 52, 53, 56, 58, 59, 66, 68, 73, 82) + КВМ
Синонимы: Анализ урогенитального соскоба на ВПЧ. HPV DNA, 21 Types, Scrape of Urogenital Epithelial Cells. Краткое описание исследования «Дифференцированное определение ДНК ВПЧ (Вирус папилломы человека, Human papillomavirus, HPV) 21 типа (6, 11, 16, 18, 26, 31, 33, 35, 39.
Сдать анализ крови на дифференцированное определение ДНК ВПЧ 21 типа можно в ближайшем медицинском офисе ИНВИТРО. Список офисов, где принимается биоматериал для лабораторного исследования, представлен в разделе «Адреса».
Метод определения: ПЦР с детекцией в режиме «реального времени».
Исследуемый материал: соскоб эпителиальных клеток урогенитального тракта.
Форма представления результатов: количественный результат по каждому выявляемому показателю.
Единицы измерения: логарифм копий ДНК ВПЧ на 105 эпителиальных клеток (lg копий ДНК/105 эпит. клеток).
До проведения тестов по выявлению ДНК ВПЧ выполняется контроль взятия материала (КВМ). Если в пробе значение КВМ неудовлетворительное (менее 4 lg (10000) копий ДНК человека в пробе), исследование ДНК ВПЧ не проводится и рекомендуется повторное взятие биологического материала.
Интерпретация результатов исследования содержит информацию для лечащего врача и не является диагнозом. Информацию из этого раздела нельзя использовать для самодиагностики и самолечения. Точный диагноз ставит врач, используя как результаты данного обследования, так и нужную информацию из других источников: анамнеза, результатов других обследований и т. д.
Расшифровка показателей
Количественный формат теста позволяет выявить вирус, оценить степень риска и возможное наличие предраковых изменений при высокой вирусной нагрузке.
Интерпретация положительного результата
В анализируемом образце биологического материала обнаруженная ДНК, специфичная для вируса папилломы человека исследуемых типов в выявленной концентрации, свидетельствует о наличии возбудителя.
Если абсолютное содержание ВПЧ превышает клинически значимое, напротив обнаруженного штамма вируса указывается его концентрация. Чем выше значение, тем выше риск развития болезней, вызываемых вирусом папилломы человека.
Рост вирусной нагрузки через 3, 6 и 9 мес. после проведенного лечения свидетельствует о возможности рецидива.
- генотипы низкого онкогенного риска: 6, 11, 44;
- генотипы высокого онкогенного риска: 16, 18, 26, 31, 33, 35, 39, 45, 51, 52, 53, 56, 58, 59, 66, 68, 73, 82.
Выявление нескольких генотипов вируса предполагает менее благоприятный прогноз течения заболевания и более высокий риск персистенции.
При обнаружении 16 и 18 генотипов рекомендуется проводить кольпоскопическое обследование, не откладывая.
При выявлении других типов высокого риска назначают цитологическое обследование, а при его положительном результате - кольпоскопию.
Интерпретация результата «не обнаружено»
Результат «не обнаружено» свидетельствует либо об отсутствии фрагментов ДНК, специфичных для вируса папилломы человека исследованных типов, либо о слишком низкой концентрация ДНК возбудителей в образце (ниже границы чувствительности метода).
Дополнительное обследование при отклонении от нормы
Врач интерпретирует результат анализа с учетом данных о пациенте и болезни, заключений осмотра, цитологического и гистологического исследований.
Гинеколог, уролог или проктолог может назначить дополнительные исследования:
-
цитологическое исследование биоматериала соскобов вульвы и влагалища, кроме шейки матки (окрашивание по Папаниколау, Рар-тест);
В цитологическом методе диагностики для окрашивания биологического материала используют несколько способов окраски. Применение определённого метода окрашивания позволяет решить специфические задачи. Каждый метод окрашивания имеет свои особенности, специфику, например, характер окрашивания ядра, ц.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Вирус папилломы человека: причины появления, симптомы, диагностика и способы лечения.
Определение
Вирусы папилломы человека (ВПЧ) — это группа чрезвычайно распространенных и генетически разнородных ДНК-содержащих вирусов, поражающих эпителий кожных покровов и слизистых оболочек. Вирус папилломы человека относится к семейству папилломавирусов. Было выявлено и описано более 190 типов ВПЧ. Каждый тип отличается более чем на 10% от ближайшего родственного штамма. Из их числа более 30 типов ВПЧ могут инфицировать эпителиальный слой урогенитального тракта. В зависимости от онкогенного потенциала выделяют вирусы высокого (типы 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59) и низкого (типы 6, 11, 42, 43, 44) онкогенного риска.
На долю двух высокоонкогенных типов ВПЧ (16 и 18) приходится до 70% случаев рака шейки матки, 80% рака вульвы и влагалища, 92% анального рака, 95% рака ротовой полости, 89% рака ротоглотки, 63% рака полового члена.
При этом 16-й тип имеет самый высокий канцерогенный потенциал. Генотипы ВПЧ 6 и 11 вызывают практически все виды аногенитальных бородавок и большинство случаев рецидивирующего респираторного папилломатоза, который наблюдается в основном у детей младше 5 лет или у лиц 20-30 лет.
Причины появления ВПЧ
Заболевания, вызванные вирусом папилломы человека (ВПЧ), относятся к болезням с латентным началом, хроническим персистирующим течением и проявляются доброкачественными и злокачественными новообразованиями в зоне входных ворот инфекции.
Источником возбудителя инфекции является больной человек или носитель. ВПЧ передается от человека к человеку при оральном, генитальном и анальном половых контактах, а также контактно-бытовым и вертикальным (от матери к ребенку) путями.
Вирус папилломы человека — единственный вирус, который не проникает в кровь, вследствие чего инфекционный процесс протекает без развития воспалительной реакции. В процессе инфицирования вирус папилломы человека поражает незрелые клетки, чаще базального слоя, которые затем становятся постоянным источником инфицирования эпителиальных клеток. Инфицированию способствует наличие микротравм и воспалительных процессов кожи и слизистых оболочек, приводящих к снижению местного иммунитета.
Вирус способен персистировать (хронически присутствовать) в месте проникновения как угодно долго. Инкубационный период заболевания может длиться от нескольких месяцев до нескольких лет. Среднее время между инфицированием ВПЧ и развитием аногенитальных бородавок составляет от 3 месяцев у женщин и до 11 месяцев у мужчин. Инфицирование человека может происходить как одним, так и несколькими типами ВПЧ.
Интервал между инфицированием ВПЧ и прогрессированием до инвазивного рака составляет, как правило, 10 лет или более.
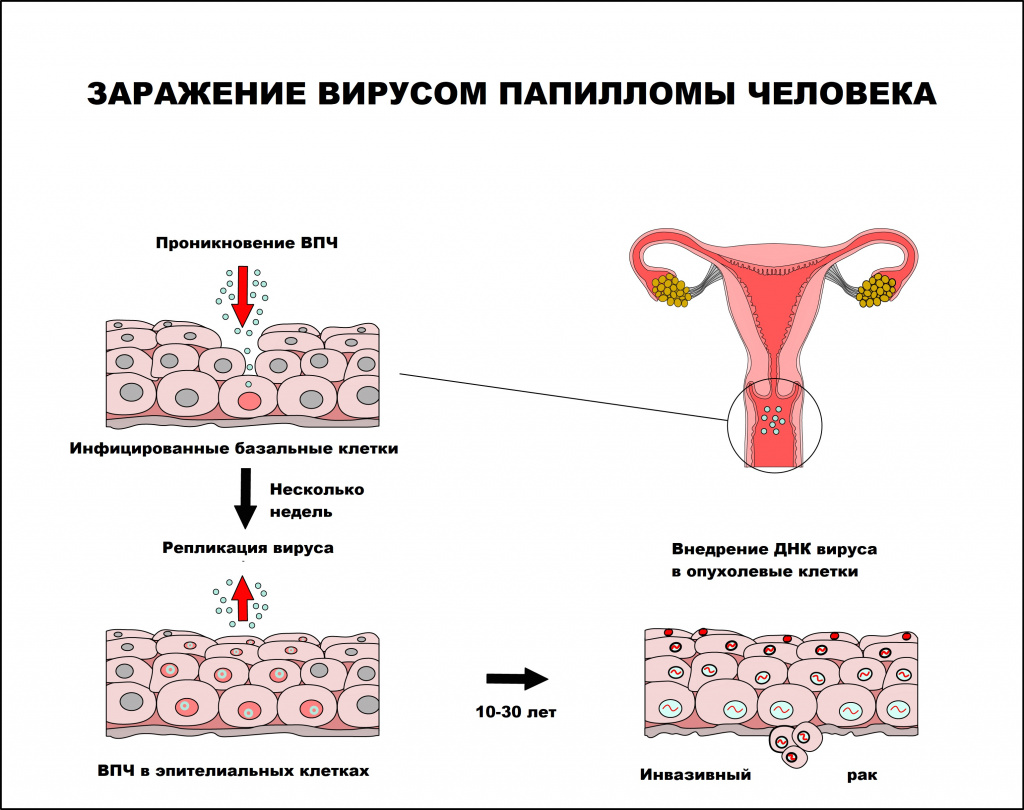
Папилломавирусная инфекция чаще регистрируется у лиц молодого возраста, имеющих большое число половых партнеров. По данным ВОЗ, 50-80% населения инфицировано ВПЧ, но лишь 5-10% инфицированных лиц имеют клинические проявления заболевания.
Классификация заболевания
Общепринятой классификации аногенитальных (венерических) бородавок не существует. Однако выделяют несколько их клинических разновидностей:
- остроконечные кондиломы;
- бородавки в виде папул;
- поражения в виде пятен;
- внутриэпителиальная неоплазия;
- бовеноидный папулез и болезнь Боуэна;
- гигантская кондилома Бушке-Левенштайна (карциномоподобная остроконечная кондилома).
Симптомы ВПЧ
- наличие одиночных или множественных образований в виде папул, папиллом, пятен на кожных покровах и слизистых оболочках половых органов;
- зуд и парестезии (расстройство чувствительности) в области поражения; болезненность во время половых контактов (диспареуния);
- при локализации высыпаний в области уретры наблюдается зуд, жжение, болезненность при мочеиспускании (дизурия); при обширных поражениях в области уретры – затрудненное мочеиспускание;
- болезненные трещины и кровоточивость кожных покровов и слизистых оболочек в местах поражения.
Бородавки в виде папул – папулезные высыпания без пальцеобразных выпячиваний, локализующиеся на кератинизированном эпителии половых органов.
Поражения в виде пятен – серовато-белые, розовато-красные или красновато-коричневые пятна на коже и/или слизистой оболочке половых органов;
Бовеноидный папулез и болезнь Боуэна – папулы и пятна с гладкой или бархатистой поверхностью; цвет элементов в местах поражения слизистой оболочки – бурый или оранжево-красный, а поражений на коже – пепельно-серый или коричневато-черный.
Гигантская кондилома Бушке-Левенштайна – мелкие бородавчатоподобные папилломы, сливающиеся между собой и образующие очаг поражения с широким основанием.
Респираторный папилломатоз – заболевание, при котором папилломы формируются в дыхательных путях, ведущих от носа и полости рта в легкие.
Диагностика ВПЧ
Латентно протекающая инфекция диагностируется только с помощью молекулярно-биологических методов исследования. Субклиническая инфекция диагностируется при молекулярно-биологическом, кольпоскопическом, цитологическом и морфологическом исследовании.
Для улучшения визуализации аногенитальных бородавок может быть проведена проба с 3-5% раствором уксусной кислоты. Тест считается отрицательным, если после обработки уксусной кислотой на поверхности шейки матки нет белых участков. И положительным при выявлении на шейке матки участков белого цвета (ацетобелых участков), отличных от остальной поверхности шейки матки.
Изменения эпителия шейки матки, вызванные ВПЧ, могут быть выявлены цитологическим методом микроскопии слущенных клеток с окраской по Папаниколау (Пап-тест).
Метод окрашивания по Папаниколау - специально разработанный метод, позволяющий с наибольшей степенью достоверности выявить ранние предраковые заболевания шейки матки. Рак шейки матки в структуре злокачественных новообразований репродуктивной системы занимает третье место. До 1992 г. заб.

Чаще всего эрозия протекает без ярко выраженных симптомов, поэтому диагностировать данный недуг можно лишь при регулярном посещении гинеколога.
Комплексный подход и применение разных диагностических методов позволяет максимально точно определить тяжесть заболевания и степень повреждения слизистой.
Гинекологический осмотр
Врач-гинеколог может определить эрозию во время обычного осмотра. Яркие пятна, нарушение в структуре эпителия – признаки, которые свидетельствуют о развитии данного заболевания.
Исходя из симптомов, врач может диагностировать не только наличие эрозии, но и определить ее вид:
- Красная ранка присутствует при воспалительной эрозии.
- Серозные выделения из ранки – при сифилитической эрозии.
- Большое количество ран развивается, если заболевание имеет туберкулёзное происхождение.
- Кровянистые выделения из ранки, налет могут свидетельствовать о том, что эрозия перешла в злокачественное образование.
Для того, чтобы полностью оценить картину заболевания и масштабы поражения применяются и другие диагностические методы.
Инструментальный метод диагностики эрозии шейки матки
Инструментальные методы, которые используются для обследования эрозии шейки матки, позволяют подтвердить диагноз и определить вид эрозии.
Среди наиболее востребованных: кольпоскопия и биопсия.

-
Кольпоскопия – процедура обследования шейки матки с помощью специального аппарата, кольпоскопа. Данный метод позволяет определить повреждения и нарушения в структуре слизистой.
Биопсия проводится в несколько способов. Наиболее распространенным является метод забора материала с помощью радиоволновой энергии. Также применяется ножевая биопсия – процедура, при которой материал получают при помощи скальпеля.
Данный метод является травматическим, поэтому выполняется пациенткам, которые в будущем не планируют беременность.
Анализы при эрозии шейки матки – гинекологический мазок
Исследование выделений из половых органов позволяет определить состояние микрофлоры влагалища, узнать о наличии воспалительного процесса.
Если в ходе обследования были выявлены инфекции (хламидиоз, микоплазмоз, папилломавирус и т.д.), в первую очередь назначаются меры по их устранению, а уже после этого формируется схема лечения эрозии.
Для более точных анализов эрозии шейки матки проводится бак-посев – процедура, которая позволяет определить нарушения и наличие патогенных микробов.
Анализ крови
Диагностика эрозии шейки матки включает анализ крови на гепатит В, С, сифилис и СПИД. Эти заболевания провоцируют снижение иммунитета, в результате чего развивается данное заболевание.
Анализ крови необходим, если лечение будет проводиться хирургическим методом.
Цитологическое исследование при эрозии
Цитология – это один из основных методов исследования патологий шейки матки. Данная процедура позволяет изучить особенности строения клеток, выявить нарушения и патологические процессы. Метод является безболезненным, поэтому в анестезии нет необходимости.
В чем заключается процедура?
С помощью специального инструмента проводится забор слоя клеток. Для изучения берут биоматериал с участка, где покровный эпителий соединяется с внутренним, цилиндрическим эпителием.
Материал изучается врачом-цитологом, который в результате исследования определяет наличие либо отсутствие атипичных клеток. Нарушения в структуре, строении клеток могут свидетельствовать о развитии злокачественного процесса.
Дополнительные методы диагностики эрозии шейки матки
В зависимости от формы и истинной природы заболевания, проводится дополнительное обследование:
- Консультация у дерматовенеролога проводится при наличии сифилитической эрозии.
- Если заболевание имеет туберкулезное происхождение, может понадобиться обследование у врача-фтизиатра.
- При развитии рака шейки матки или быстрого прогрессирования эрозии, пациентке необходимо пройти обследование у онкогинеколога. Проконсультироваться с этим специалистом необходимо перед тем, как проводить лечение лучевой эрозии.
Длительное существование эрозии может перейти в злокачественное образование, поэтому ни в коем случае нельзя откладывать визит к гинекологу. Ранняя диагностика позволяет сформировать схему эффективного лечения и предотвратить развитие тяжелых осложнений.
Читайте также:

