Какое заболевание кожи приводит к развитию сепсиса
Обновлено: 19.04.2024
Сепсис (инфекционное заражение крови) – это тяжелое патологическое состояние, которое описывается, как нахождение возбудителя (микроба или грибков) в крови.
Развитие септического процесса является опасным для жизни состоянием и при несвоевременном лечении может приводить к гибели человека.
Возбудителями могут становиться микробы или патогенные грибки. Основными микробными агентами являются:
- синегнойная палочка, патогенные штаммы стафилококка,
- патогенные штаммы кишечной палочки,
- пневмококк, менингококк, клебсиелла,
- туберкулезная микобактерия,
- в редких случаях может возникать сепсис, вызванный грибками Candida или другими видами грибков.
Процесс развивается в случае снижения общей сопротивляемости организма к инфекции, истощения иммунной системы хроническими инфекционными процессами или наличием гнойных очагов, в случае снижения защитной функции естественных барьеров – кожи, кишечника, легких.
В результате организм не может локализовать и уничтожить микробы, они беспрепятственно проникают в кровь, в то время как в крови, за счет нарушения иммунитета, снижено количество бактерицидных компонентов и иммунных клеток.
В каждом конкретном случае очаги первичной инфекции могут быть разными – от кариозных зубов и миндалин, до абсцессов в брюшной полости и гнойных ран кожи.
Обычно сепсис возникает
- при диабете,
- при онкологических заболеваниях,
- при рахите или иммунодефицитах (врожденных или приобретенных),
- при тяжелых травмах или ожогах,
- при длительном приеме иммуносупрессоров или в случае длительной рентгено- и химиотерапии.
Выделяется несколько видов сепсиса, отличающихся по механизму развития и типам возбудителей:
- Кожный сепсис - очаги инфекции первично возникают на коже (ожоги, раны, гнойные процессы).
- Ротовой (оральный) сепсис - первичные очаги расположены в полости рта или глотке (кариозные полости, пульпиты, остеомиелиты челюсти, миндалины, заглоточные абсцессы).
- Акушерский (гинекологический) с первичными очагами в матке или половой сфере после родов, при воспалительных процессах малого таза.
- Отогенный сепсис, с первичным очагом в области среднего уха или рядом с ним.
- Хирургический (диагностический) - возникает после оперативных вмешательств с заносом инфекции или после проведения диагностических манипуляций.
- Криптогенный, с неизвестным или невыясненным первичным очагом заражения.
- Внутрибольничный сепсис - особое состояние, характеризующееся инфицированием опасными штаммами микробов, устойчивых к терапии.
Крайне важно выяснение «входных ворот» или первичного очага сепсиса, так как это дает ключ к причинам инфекции и примерному списку возможных возбудителей, а значит, позволяет выбрать наиболее эффективную терапию.
В отличие от обычных инфекций, сепсис имеет особенные условия протекания. Для него характерно:
- Обязательное наличие первичного очага, пусть даже и невыясненного, но он имеется всегда. Причем, этот очаг должен быть тесно связан с кровеносными или лимфатическими путями.
- При сепсисе возбудитель должен многократно проникать в кровь (это состояние называют септицемией).
- Характерно формирование вторичных инфекционных очагов, в которых размножается возбудитель и вновь проникает в кровь (септикопиемия).
- Организм не в состоянии обеспечить должный иммунный ответ на инфекцию и активизировать защитные реакции клеток и тканей против возбудителей.
Только при наличии всех этих условий выставляется диагноз сепсиса.
Признаки сепсиса во многом зависят от первичного очага и типа возбудителя, но для септического процесса характерно несколько типичных клинических симптомов:
- сильные ознобы,
- повышение температуры тела (постоянное или волнообразное, связанное с поступлением в кровь новой порции возбудителя),
- сильная потливость со сменой нескольких комплектов белья за сутки.
Это три основных симптома сепсиса, они являются наиболее постоянными проявлениями процесса. К ним в дополнение могут быть:
- бледность кожи и слизистых, восковой цвет лица,
- усталость и безучастность пациента, изменения в психике от эйфории до сильной апатии и ступора,
- впалые щеки с сильно выраженным румянцем на щеках на фоне общей бледности,
- кровоизлияния на коже в виде пятен или полосок, особенно на руках и ногах,
- герпесоподобные высыпания на губах, кровоточивость слизистых,
- нарушение дыхания, снижение давления,
- уплотнения или гнойнички на коже,
- уменьшение объема мочи.
Процесс может развиваться по следующим сценариям:
- молниеносно – развивается за 1-3 суток,
- остро - развивается спустя 4-60 суток с момента формирования первичного очага,
- подостро - течение длится от двух до шести месяцев,
- хронически - длится более полугода,
- рецидивирующе - чередуются периоды развития сепсиса с периодами полного здоровья.
Диагноз устанавливается при наличии типичной картины сепсиса с подтверждением его лабораторными данными.
Производится посев крови и отделяемого из очагов воспаления. Проведение посевов с обнаружением возбудителя должно быть многократным, так как у возбудителей существуют жизненные циклы, а проведение терапии может существенно изменять картину крови и уровня микроба в ней.
При обнаружении в крови и содержимом первичного очага аналогичных микробов, диагноз подтверждается.
Для уточнения лечения проводится еще и определение чувствительности микробов к антибиотикам.
Кроме того, проводятся общий анализ крови с выявлением воспалительной картины, биохимический анализ крови с выявлением воспалительных сдвигов, газовый состав, электролитный состав и ее свертываемость.
Проводят рентген грудной клетки, УЗИ внутренних органов с поиском первичных очагов инфекции.
Одни и те же симптомы могут быть признаками разных заболеваний, а болезнь может протекать не по учебнику. Не пытайтесь лечиться сами — посоветуйтесь с врачом.
Сепсис лечится только в инфекционном или терапевтическом стационаре, в отделении реанимации и интенсивной терапии.
Принципы лечения аналогичны лечению других очагов инфекции, но учитываются общее тяжелое состояние и риск летального исхода.
- антибиотики в максимальных дозах с учетом чувствительности, внутривенно.
- проводят активную борьбу с токсикозом,
- активизируют собственную иммунную систему, корректируют нарушенные процессы жизнедеятельности.
Необходимо создание покоя и изоляции, назначается особая диета, в случае тяжелого состояния – искусственное внутривенное питание.
Важно удаление инфекции из первичного очага, применение двух и более антибиотиков иногда в сочетании с гормонами.
При необходимости больным производят вливание плазмы крови, гамма-глобулина и глюкозы.
При формировании вторичных гнойных очагов необходимо их хирургическое лечение – вскрытие абсцессов, удаление гноя и промывание ран, иссечение пораженных участков.
Не смотря на все мероприятия, прогноз при сепсисе серьезный – летальность достигает 60%, инвалидизация после перенесенного сепсиса также довольно высока.
Сепсис новорожденных – генерализованная гнойно-септическая инфекция, характеризующаяся наличием первичного очага и циркуляцией инфекции в крови. Сепсис новорожденных проявляется признаками инфекционного токсикоза (температурной реакцией, вялостью, диспепсией, землистой окраской кожных покровов) и образованием гнойных метастатических очагов в различных органах (мозговых оболочках, легких, костях, печени и пр.). Диагноз сепсиса у новорожденных устанавливается на основании клинических критериев и выделения возбудителя при бактериологическом посеве крови. Лечение сепсиса новорожденных включает системную антибиотикотерапию, санацию первичного и метастатических гнойных очагов, посиндромную терапию.
Общие сведения
Сепсис новорожденных – общий инфекционный процесс, обусловленный попаданием условно-патогенной и гноеродной микрофлоры из локальных очагов в кровяное русло и сопровождающийся тяжелыми системными проявлениями. По данным зарубежной педиатрии, частота сепсиса новорожденных составляет 0,1-0,8%; среди недоношенных и детей с перинатальной патологией, находящихся в ОРИТ, - 14%. Неонатальная смертность, обусловленная сепсисом новорожденных, высока и стабильна – около 30-40%. Развитию сепсиса способствуют недостаточная сформированность барьерных механизмов и иммунитета у новорожденных, пограничные состояния периода новорожденности, патологическое протекание перинатального периода, сложность ранней диагностики септических состояний.

Причины
В настоящее время доминирующее место (около 50%) среди возбудителей сепсиса новорожденных принадлежит грамположительной флоре (главным образом, стафилококкам, гемолитическому стрептококку группы А). Чуть реже (до 40% случаев) выявляется грамотрицательная микрофлора (кишечная палочка, синегнойная палочка, клебсиелла и др.); в 10% этиологическими агентами выступает смешанная флора (часто ассоциация стафилококка с грибами Candida).
Со стороны матери факторами, способствующими бактериальной контаминации новорожденного, выступают бактериальный вагиноз, кольпиты, эндометрит. Большое значение имеет степень и характер иммуносупрессии у новорожденного, которые могут быть связаны с неполноценным питанием или приемом лекарств беременной, наследственным иммунодефицитом или ВИЧ-инфекцией. В отдельных случаях причиной вспышек сепсиса новорожденных становится несоблюдение санитарного режима в родильных или детских отделениях.
Классификация
По времени развития выделяют внутриутробный и постнатальный (ранний неонатальный и поздний неонатальный) сепсис новорожденных. Внутриутробный сепсис предполагает антенатальное или интранатальное инфицирование плода; при этом первичный гнойно-септический очаг располагается вне организма ребенка (чаще всего в его роли выступает плацентит, хорионит, хориоамнионит и т. д.). В случае постнатального сепсиса первичный гнойно-воспалительный очаг всегда располагается в организме самого новорожденного.
Ранний неонатальный сепсис новорожденных развивается в первые 4-ро суток жизни ребенка. Клинические течение заболевания обычно молниеносное, с быстрым развитием полиорганнной недостаточности, летальным исходом в 5-20% случаев. Поздний неонатальный сепсис новорожденных манифестирует на 5-й день и позднее. Характеризуется медленно прогрессирующим течением, возникновением вторичных септических очагов, 5-10%-ной летальностью.
Течение сепсиса новорожденных может быть молниеносным (3-7 дней), острым (до 4-8 недель), подострым (до 1,5-3 месяцев), затяжным (более 3 месяцев). С учетом локализации первичного септического очага и входных ворот различают: пупочный, кожный, легочный, ринофарингеальный, отогенный, риноконъюнктивальный, кишечный, урогенный, катетеризационный и др. виды сепсиса новорожденных. Сепсис новорожденных может протекать в форме септицемии или септикопиемии.
Симптомы сепсиса новорожденных
Септицемия или сепсис новорожденных без метастазов обычно развивается на фоне предшествующего мокнущего пупка, конъюнктивита, гнойничковой сыпи, опрелостей, стоматита. Предвестниками сепсиса новорожденных могут выступать вялость или беспокойство, снижение аппетита, обильные частые срыгивания, плохая прибавка в весе. В период разгара развивается температурная реакция (гипер- или гипотермия), отечный синдром или эксикоз, гипотрофия. Характерным признаком сепсиса новорожденных является грязновато-серый (землистый) оттенок кожных покровов, желтушность, мраморность кожи, сыпь.
Вследствие токсического поражения различных органов возникают гепатоспленомегалия, пневмопатия (тахипноэ, цианоз), кардиопатия (тахикардия или брадикардия, артериальная гипотензия), диспепсия, мочевой синдром (олигурия, анурия, ОПН), геморрагический синдром, надпочечниковая недостаточность. Чаще всего септицемия осложняется присоединением пневмонии, которая выступает как самостоятельное интеркуррентное заболевание.
Септикопиемия или сепсис новорожденных с гнойными метастазами характеризуется возникновением на фоне интоксикации вторичных очагов отсева в мозговых оболочках, легких, костях, печени, других органах. Чаще всего септикопиемия протекает с развитием гнойного менингита, абсцедирующей пневмонии, остеомиелита; реже – с формированием абсцесса печени, гнойного артрита, панофтальмита, медиастинита, флегмоны желудка или кишечника. В восстановительном периоде происходит санация пиемических очагов, стихание токсикоза, постепенное восстановление нарушенных функций.
Молниеносная форма сепсиса новорожденных протекает с развитием септического шока: стремительным ухудшением состояния ребенка, снижением температуры тела, брадикардией, кровоточивостью, отеком легких, острой почечной недостаточностью. Летальный исход при молниеносном течении сепсиса новорожденных наступает в течение 3-5 суток.
Диагностика сепсиса новорожденных
Диагноз сепсиса новорожденного может быть заподозрен неонатологом или педиатром на основании лихорадки свыше 3 дней или прогрессирующей гипотермии; гиперлейкоцитоза, сменяющегося лейкопенией; повышением содержания в крови маркеров инфекционного процесса (СРБ, интерлейкина-8, прокальцитонина).
Факт бактериемии при сепсисе новорожденных подтверждается путем посева крови на стерильность. Важное значение имеет выявление первичного гнойного очага и метастатических очагов, микробиологического исследование отделяемого из них (бактериологическое исследование мазка с конъюнктивы, мочи на микрофлору, соскоба/отделяемого с кожи на микрофлору, мазка из глотки, кала на дисбактериоз и т. п.).
Дифференциальная диагностика сепсиса новорожденных осуществляется с локализованными гнойно-воспалительными заболеваниями (пневмонией, медиастинитом, перитонитом, менингитом, энтероколитом), генерализованными вирусными инфекциями (цитомегалией, герпесом, энтеровирусной инфекцией) и микозами (кандидозом, аспергиллезом) и др. Для этого используются дополнительные лабораторные методы – ПЦР, ИФА, микроскопия.
Лечение сепсиса новорожденных
Терапия при сепсисе новорожденных проводится одновременно в нескольких направлениях и включает санацию септического и пиемических очагов, подавление циркуляции возбудителя в крови, коррекцию нарушенных функций.
Основу этиологического лечения сепсиса новорожденных составляет антибиотикотерапия: эмпирическая комбинированная до уточнения характера микрофлоры) и целенаправленная после получения антибиотикограммы. Противомикробные препараты вводятся внутривенно, в максимальных возрастных дозировках в течение 10-15 суток с последующей сменой. Чаще всего в клинической практике для лечения сепсиса новорожденных в различных сочетаниях используются цефалоспорины, аминогликозиды, аминопенициллины, карбапенемы и др.
С целью местного лечения гнойных очагов производится вскрытие фурункулов и абсцессов, перевязки с антибактериальными и ферментными препаратами; назначается УВЧ, СВЧ, электрофорез.
Патогенетическая терапия сепсиса новорожденных включает иммунокоррекцию (плазмаферез, гемосорбцию, введение иммуноглобулинов), проведение дезинтоксикационной терапии (внутривенной инфузии глюкозо-солевых растворов и свежезамороженной плазмы), адекватную кислородотерапию и т. д. При сепсисе новорожденных обязательно проводится мониторинг состояния жизненно-важных функций: АД, ЧСС, ЭКГ, КОС и газового состава крови, биохимических показателей (сахара крови, креатинина, электролитов), гематокрита.
В остром периоде сепсиса целесообразно пребывание новорожденных в кувезе, кормление материнским молоком, тщательный уход. В восстановительном периоде к лечению подключается гимнастика, массаж, лечебные ванны.
Прогноз и профилактика сепсиса новорожденных
Прогноз сепсиса новорожденных серьезный: летальность составляет от 30-40% до 60% среди глубоко недоношенных детей. У выздоровевших детей в отделенном периоде могут отмечаться частые ОРВИ, пиелонефрит, анемия, перинатальная энцефалопатия.
Профилактика сепсиса новорожденных включает выявление и санацию инфекций мочеполовой сферы у беременной, соблюдение противоэпидемических мероприятий медперсоналом родильных домов и отделений новорожденных, тщательный гигиенических уход за новорожденным, естественное вскармливание. Вопрос о сроках вакцинации новорожденных с сепсисом против туберкулеза и против гепатита В , проводимой в первые дни жизни, решается в индивидуальном порядке.
Пупочный сепсис – это генерализованное инфекционное заболевание новорожденных, возникающее при проникновении возбудителей через пупочную ранку. Заболевание развивается при инфицировании стафилококками, кишечной палочной, условно-патогенными грибами. Клинически неонатальный сепсис проявляется лихорадкой или гипотермией, сердечно-легочной недостаточностью, угнетением сознания и рефлексов. Диагностика болезни включает бактериологический посев крови, определение острофазовых показателей, УЗИ пупочной области. Основу лечения составляет массивная антибиотикотерапия, которая дополняется патогенетической терапией и иммунокоррекцией.
МКБ-10


Общие сведения
Специалисты в области неонатологии регулярно сталкиваются с проблемой сепсиса новорожденных: он диагностируется у 0,1-0,2% доношенных и 1-1,5% недоношенных детей. По времени развития выделяют ранний, возникающий в первые 72 часа после рождения, и поздний, который проявляется после 3-х дней жизни младенца. Первый вид в основном вызван внутриутробным или интранатальным инфицированием младенца. Пупочный сепсис относится к позднему, он развивается при заражении патогенными бактериями, проникшими через пупочную ранку из окружающей среды.

Причины
Основные возбудители пупочного сепсиса – грамположительные бактерии Staphylococcus epidermidis и Staphylococcus aureus. Эти микроорганизмы в небольших количествах обитают на коже, входят в состав вагинальной микрофлоры у 60% женщин. Заражение новорожденного происходит дома при общении с родителями и гигиеническом уходе, в отделении новорожденных при осмотре врачом и проведении медицинских манипуляций.
Второй по частоте возбудитель инфекции – кишечная палочка (Escherichia coli). Бактерия является постоянным обитателем толстого отдела кишечника, поэтому она способна колонизировать пупочную рану. Для позднего госпитального сепсиса новорожденных типичны грибково-бактериальные ассоциации: одновременное заражение грибами рода Кандида, стафилококками, стрептококками и другими видами бактерий.
Факторы риска
Сепсис зачастую вызван условно-патогенной микрофонной, которая у провоцирует тяжелые инфекции у одних детей и не влияет на здоровье других. В связи с этим значимую роль приобретают предрасполагающие факторы, которые способствуют заражению, генерализации инфекционного возбудителя и реализации его системных эффектов на организм младенца. К факторам риска относятся следующие:
- Осложнения беременности и родов. Сепсис чаще развивается у новорожденных, матери которых страдали длительными гестозами, имели очаги хронической инфекции урогенитального или желудочно-кишечного тракта. Вероятность инфекционных заболеваний повышается при трудных родах, недоношенности, низкой оценке по шкале Апгар.
- Ненадлежащий уход за ребенком. При позднем внебольничном сепсисе источником инфекции становятся родители и ближайшие родственники, которые общаются с ребенком. Несоблюдение санитарно-гигиенических норм при смене подгузника, обработке пупочного остатка и купании – основные причины заражения инфекцией. Сначала развивается омфалит, который затем осложняется сепсисом.
- Медицинские манипуляции. Новорожденные, которые госпитализируются в реанимационные отделения, подвергаются риску заражения госпитальными штаммами бактерий. Вероятность заболевания коррелирует с длительностью стационарного лечения, объемом инвазивных диагностических и лечебных процедур.
- Иммунодефицитные состояния. Генерализация бактериальной и грибковой инфекции чаще наблюдается у детей со сниженным иммунным статусом. В периоде новорожденности причиной такого состояния выступают врожденные иммунодефициты: синдром Ди Джорджи, атаксия-телеангиэктазия Луи-Бар, ТКИД и многие другие.
Патогенез
Пупочный сепсис начинается с первичного очага инфекции, которым выступает гнойный омфалит. Поскольку у новорожденных наблюдается незрелость фагоцитарно-макрофагальной системы и физиологическое угнетение Т- и В-системы лимфоцитов, бактериальное воспаление не ограничивается пупочной ранкой. Возбудители легко проникают в системный кровоток и взаимодействуют с факторами иммунной защиты.
В основе заболевания лежит неадекватная реакция иммунитета, которая сопровождается резким повышением уровня провоспалительных медиаторов, повреждением клеточных мембран, генерализованными нарушениями микроциркуляции. Одновременно с этим развивается гипоксия тканей и критически снижается продукция макроэргов, что способствует развитию полиорганной недостаточности.

Симптомы пупочного сепсиса
Заболевание возникает на фоне уже имеющегося омфалита на 3-14 дне жизни новорожденного. У ребенка резко ухудшается состояние: температура тела повышается более 40°С или снижается менее 35°С, наблюдается учащенное дыхание и сердцебиение. Новорожденный становится вялым, отказывается от груди и бутылочки. Кожа приобретает землистый оттенок, черты лица заостряются, возникают мелкие подкожные кровоизлияния.
Наблюдаются характерные изменения пупочного остатка. Пупок и окружающие ткани ярко-красные и горячие на ощупь, вокруг них усиливается рисунок венозной сети и появляются красные полосы – признак лимфангита. При надавливании на кожу вокруг пупка из раны выделяется гной с резким неприятным запахом. При некротической форме воспаления кожа становится темно-багровой.
Осложнения
Тяжелой формой сепсиса является септикопиемия – образование метастатических гнойных очагов. Чаще всего развивается гнойный перитонит, остеомиелит, менингит, плеврит и абсцессы легких. Возможны флегмоны мягких тканей разных участков тела. Уровень смертности остается стабильно высоким и составляет 30-40%. При септических осложнениях чаще умирают недоношенные и маловесные дети, имеющие сопутствующую соматическую патологию.
Диагностика
Осмотр новорожденного с признаками генерализованной инфекции проводится врачом-неонатологом. При первичном обследовании обращают внимание на состояние пупочной ранки, наличие клинических проявлений сепсиса, анамнез беременности и родов. По показаниям к диагностике привлекают детского хирурга. Для уточнения диагноза и идентификации возбудителя назначают следующие методы исследования:
- УЗИ.Сонография мягких тканей проводится при подозрении на флегмону, чтобы оценить степень и глубину поражения клетчатки. При подозрении на перитонит и внутрибрюшные абсцессы назначают УЗИ органов брюшной полости.
- Посев крови. Бактериологическое исследование требуется для определения вида возбудителя сепсиса и его чувствительности к антибиотикам. Для получения наиболее достоверных результатов забор биоматериала проводят на высоте лихорадки до начала антибиотикотерапии.
- Базовая лабораторная диагностика. Признаками сепсиса в клиническом анализе крови является высокий лейкоцитоз или лейкопения, резкое возрастание СОЭ. Информативны биохимические показатели системного воспаления: повышенный С-реактивный белок и прокальцитонин.
Дифференциальная диагностика
При выявлении очага гнойного омфалита и характерных клинико-лабораторных признаков диагноз пупочного сепсиса не подвергается сомнению. В неясных случаях неонатологу необходимо исключить диссеминированную цитомегаловирусную, аденовирусную и энтеровирусную инфекцию. Дифференциальная диагностика проводится с респираторным дистресс-синдромом новорожденных, некротическим энтероколитом, абсцессом мозга.

Лечение пупочного сепсиса
Консервативная терапия
При первых признаках сепсиса новорожденного обязательно госпитализируют в реанимационное отделение. При тяжелом состоянии ребенка диагностика выполняется параллельно с лечебными мероприятиями, поскольку начало терапии в первые 6 часов от появления симптомов значительно повышает шансы на выздоровление. Медицинская помощь при сепсисе включает несколько направлений:
- Антибактериальная терапия. До получения результатов бакпосева медикаменты выбирают эмпирически. Препаратами выбора являются бактерицидные антибиотики с максимальным спектром действия, которые способны проникать через ГЭБ и обладают минимальной токсичностью. Средняя длительность лечения составляет 4 недели.
- «Терапия сопровождения». Учитывая длительность применения антибиотиков, их дополняют лекарствами для нейтрализации возможных побочных эффектов. Профилактику грибковой инфекции проводят антимикотиками, для поддержания работы ЖКТ применяются пробиотики.
- Патогенетическая терапия. Для нормализации гемодинамики и гомеостаза назначается массивная инфузионная терапия. При тяжелой форме пупочного сепсиса проводится противошоковое, иммунокорригирующее лечение (лейкоцитарные взвеси, поликлональные антитела). Для оптимизации транспорта кислорода и ликвидации гипоксии показана респираторная поддержка.
Реабилитация
Второй этап лечения начинается по мере исчезновения признаков пупочного сепсиса. В этот период возможно развитие вторичных инфекционных процессов, нарушений обмена веществ, психоневрологических осложнений. Для реабилитации после пупочного сепсиса применяется метаболическая терапия, которая стимулирует анаболические реакции, нормализует окислительно-восстановительные процессы. С этой целью применяют ферменты, витаминно-аминокислотные комплексы.
Прогноз и профилактика
Несмотря на усовершенствование этиопатогенетической терапии сепсиса, большой процент новорожденных умирает от полиорганной недостаточности в первые дни от начала заболевания. Более благоприятный прогноз для иммунокомпетентных младенцев, которые родились доношенными и не имеют признаков септикопиемии. Профилактика пупочного сепсиса включает правильный гигиенический уход за новорожденным, минимизацию инвазивных процедур, рациональное ведение беременности и родов.
1. Неонатальный сепсис. Руководство. 2-е издание, переработанное и дополненное/ Г.А. Самсыгина. – 2020.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Сепсис: причины появления, симптомы, диагностика и способы лечения.
Определение
Сепсис – это патологический процесс, в основе которого лежит реакция организма в виде генерализованного воспаления на инфекцию различной природы. При сепсисе бактерии преодолевают иммунную защиту человека и распространяются из очага воспаления по всему организму. Местное воспаление, сепсис, тяжелый сепсис и септический шок – это различные формы выраженности воспалительной реакции организма на инфекционный процесс.
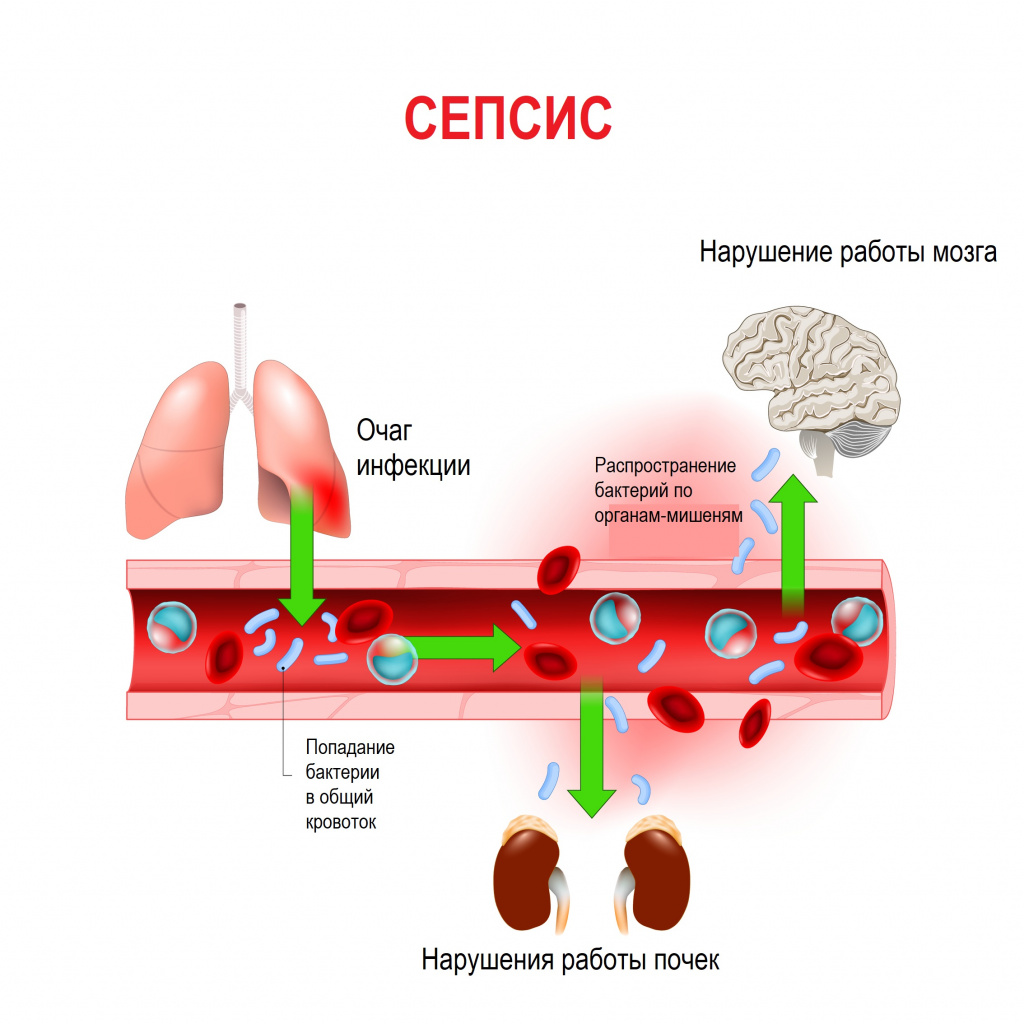
Истинная частота возникновения случаев сепсиса остается неизвестной, однако по оценкам исследователей, во всем мире сепсис является лидирующей причиной летальности у пациентов в критическом состоянии. Согласно результатам большого европейского исследования SOAP, включившего 3147 пациентов из 198 европейских медицинских центров, сепсис развился в 37,4% случаев, а госпитальная летальность от него колебалась от 14% случаев в Швейцарии до 41% в Португалии, в среднем составив 24,1%. Данные другого крупного исследования PROGRES (12 881 больной тяжелым сепсисом в 37 странах) показали, что госпитальная летальность в среднем составила 49,6%.
Причины возникновения сепсиса
Возбудителями сепсиса могут быть бактерии, вирусы или грибы. Но чаще сепсис имеет бактериальную природу - его причиной становятся стафилококки, стрептококки, пневмококки, менингококки, сальмонеллы, синегнойная палочка и др.
В большинстве случаев патологический процесс вызывают условно-патогенные микроорганизмы, которые присутствуют на коже, слизистых оболочках дыхательного и пищеварительного трактов, мочевыводящих путей и половых органов. Иногда при сепсисе выделяют сразу 2-3 микроорганизма.
Причиной сепсиса могут стать гнойно-воспалительные заболевания кожи (абсцессы, фурункулы, флегмоны), обширные травмы, ожоги, инфекционно-воспалительные заболевания мочевыводящей системы (пиелонефрит), живота (например, гнойно-некротический деструктивный панкреатит), тяжелая ангина, гнойный отит, пневмония, инфицирование во время родов или абортов и др.
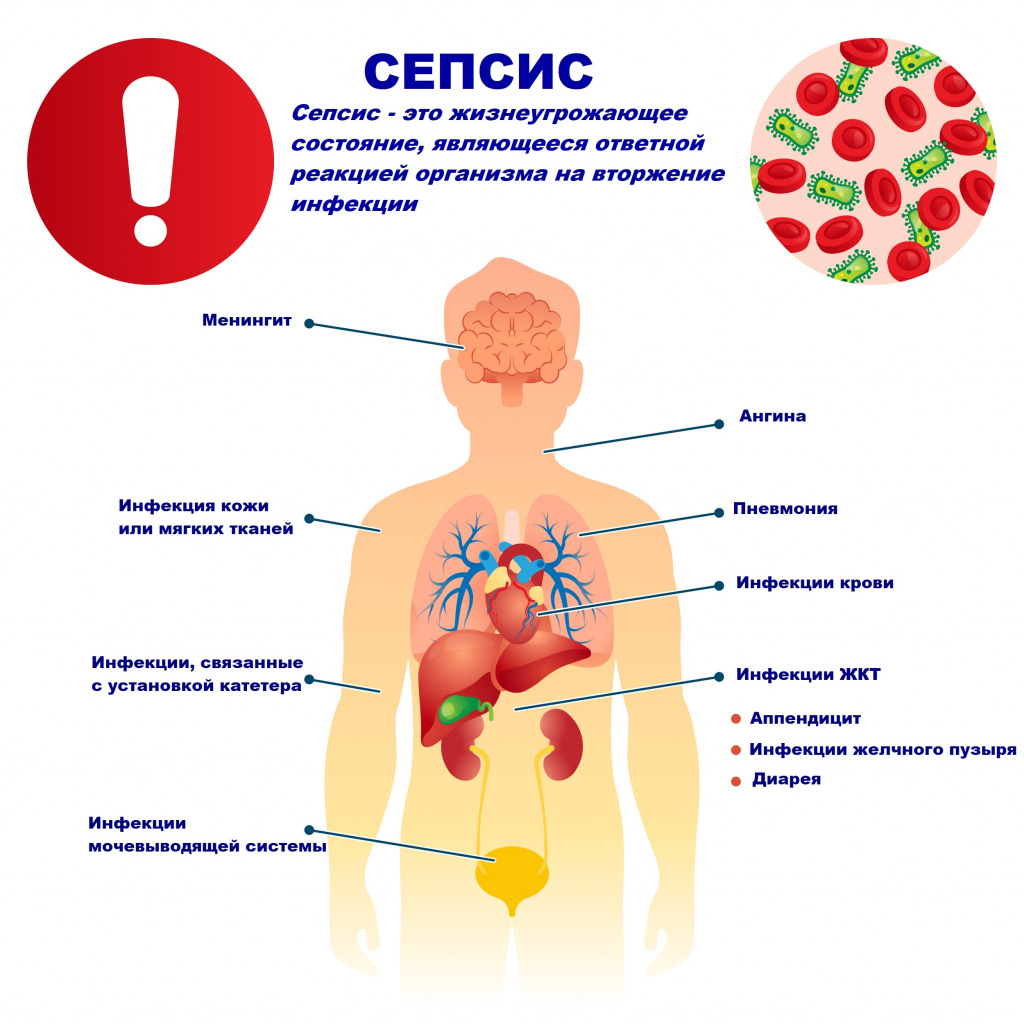
Возможность возникновения сепсиса зависит не только от свойств возбудителя, но и от состояния иммунной системы человека - нарушения в ее работе предрасполагают к распространению инфекции. Причинами таких нарушений могут быть врожденные дефекты иммунитета, хронические инфекционные болезни (ВИЧ, гнойные процессы), эндокринные заболевания (сахарный диабет), онкологические болезни, хронические интоксикации (алкоголизм, наркомания), проникающая радиация, прием иммуносупрессоров (кортикостероидов, цитостатиков) и др.
Первичный гнойно-воспалительный очаг может возникать прямо у места входных ворот или во внутренних органах. В норме иммунные клетки организма быстро очищают кровь от чужеродных агентов. Но при ослабленном иммунитете инфекционный процесс распространяется и генерализуется, формируются вторичные септические очаги. Бактерии, «путешествуя» по крово- и лимфотоку, активно производят токсины, что приводит к интоксикации и может стать причиной инфекционно-токсического (септического) шока.
В ответ на внедрение возбудителя вырабатываются цитокины – особые белковые молекулы, которые выполняют защитные функции сначала на местном уровне, а затем, попадая в системный кровоток, продолжают работать уже на уровне всего организма. Цитокины бывают провоспалительными и противовоспалительными. В самом начале инфекционного процесса их количество находится в равновесии. Если регулирующие системы организма не способны поддерживать это равновесие, то цитокины накапливаются в кровотоке в сверхвысоких объемах, начинают доминировать их деструктивные, разрушающие эффекты, в результате повреждается сосудистая стенка, запускается синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром) и полиорганная дисфункция. Вследствие полиорганной дисфункции печени, почек, кишечника появляются новые повреждающие факторы (лактат, мочевина, билирубин и др.), которые усиливают деструктивные процессы. При ДВС-синдроме в сосудах микроциркуляторного русла образуются множественные тромбы в сочетании с несвёртываемостью крови, приводящей к множественным кровоизлияниям.
Классификация заболевания
В зависимости от локализации входных ворот и первичного очага сепсис подразделяют на:
- перкутанный (чрескожный) – развивается при попадании возбудителя в организм через поврежденный кожный покров (ранки, царапины, фурункулы и др.);
- акушерско-гинекологический – развивается после родов и абортов;
- оральный (одонтогенный и тонзиллогенный) – развивается в результате первичной инфекции в полости рта;
- оториногенный – развивается в результате распространения инфекции из полости уха и/или носа;
- пневмогенный – при наличии инфекционного очага в нижних дыхательных путях;
- хирургический;
- урологический;
- пупочный – развивается у новорожденных вследствие проникновения инфекционных агентов в кровь через пупочную ранку;
- криптогенный (идиопатический, эссенциальный, генуинный) – сепсис неизвестного происхождения: первичный очаг гнойного воспаления неизвестен.
- молниеносный сепсис,
- острый сепсис,
- подострый сепсис,
- хронический сепсис (хрониосепсис).
По клиническим признакам:
1. Синдром системного воспалительного ответа (ССВО) – системная реакция организма на воздействие различных сильных раздражителей (инфекции, травмы, операции и др.) характеризуется двумя или более признаками:
- температура тела ≥ 38°С или ≤ 36°С;
- частота сердечных сокращений (ЧСС) ≥ 90 ударов в минуту;
- частота дыхания (ЧД) > 20 в минуту или гипервентиляция (РаСО2 ≤ 32 мм рт. ст.);
- лейкоциты крови > 12х109 /л или < 4х109 /л, или незрелых форм >10%.
По виду и характеру возбудителя:
- аэробный сепсис,
- анаэробный сепсис,
- смешанный сепсис,
- грибковый сепсис,
- вирусный сепсис.
Клинические проявления сепсиса могут варьировать от незначительных до критических. При молниеносном течении патологическое состояние развивается бурно - за несколько часов или суток. При остром сепсисе симптомы развиваются за несколько дней. Для хрониосепсиса характерно вялое течение и наличие малозаметных изменений, формирующихся месяцами. Рецидивирующий сепсис протекает с эпизодами обострений и затуханий.
Инкубационный период после выявления ворот инфекции или первичного очага составляет от 1 до 3-5 суток. Начало сепсиса, как правило, острое, хотя иногда может быть подострым или постепенным. Интоксикация проявляется резкой слабостью, адинамией, анорексией, нарушением сна, головной болью, расстройством сознания, менингеальным синдромом (поражением оболочек головного и спинного мозга), тахикардией, артериальной гипотензией. Температура тела держится высокой, со скачками утром и вечером. Признаки интоксикации особенно выражены на высоте лихорадки. На коже у трети больных появляется геморрагическая сыпь.
Со стороны дыхательной системы наблюдаются одышка и хрипы в легких. При нарушении функции почек снижается количество выделяемой мочи (олигурия) вплоть до полного прекращения мочеиспускания (анурия), в моче появляются следы крови, гноя. Наблюдается ухудшение функции печени с развитием желтухи и явлениями гепатита, увеличивается селезенка. Повреждение органов ЖКТ проявляется нарушением пищеварения, отсутствием аппетита, язык сухой, обложенный, нередко наблюдаются упорные септические поносы, тошнота и рвота. Метастазирование возбудителя из первичного очага с образованием вторичных очагов инфекции может приводить к инфаркту легкого, гангрене легкого, гнойному плевриту, эндокардиту (поражению внутренней оболочки сердца), воспалению сердечной мышцы (миокардиту), воспалению околосердечной сумки (перикардиту), гнойному циститу, абсцессам мозга и воспалению оболочек мозга (гнойному менингиту), гнойным артритам, флегмонам и абсцессам в мышцах.
Недостаточность функции одного органа длительностью более суток сопровождается летальностью до 35%, при недостаточности двух органов – 55%, при недостаточности функции трех и более органов летальность к четвертому дню возрастает до 85%.
Диагностика сепсиса
Для постановки диагноза «сепсис» необходимо наличие установленного или предполагаемого очага инфекционного процесса и два или более признака синдрома системной воспалительной реакции.
Производят посевы крови, мочи, ликвора, мокроты, гнойного экссудата из элементов сыпи, абсцессов, пунктатов плевры, суставов и других септических очагов. Посевы делают многократно, чтобы определить чувствительность к максимальному количеству антибиотиков. Используется также обнаружение антигенов в крови методом ИФА и определение генома возбудителя методом ПЦР.
Одним из наиболее специфичных и чувствительных маркеров бактериальной инфекции служит прокальцитониновый тест. Прокальцитонин – один из основных маркёров системного воспаления, вызванного бактериями.
Синонимы: Анализ крови на прокальцитонин; ПКТ. Procalcitonin; PCT. Краткая характеристика определяемого вещества Прокальцитонин Прокальцитонин является прогормоном кальцитонина, состоящим из 116 аминокислот с молекулярной массой 14,5 кDa. Биосинтез прокальцитонина в физиологических условиях прои.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Рожа: причины появления, симптомы, диагностика и способы лечения.
Определение
Рожа – это инфекционное заболевание, возбудителем которого чаще всего становится β-гемолитический стрептококк группы А. Болезнь протекает с выраженными симптомами интоксикации и очаговым поражением кожи.
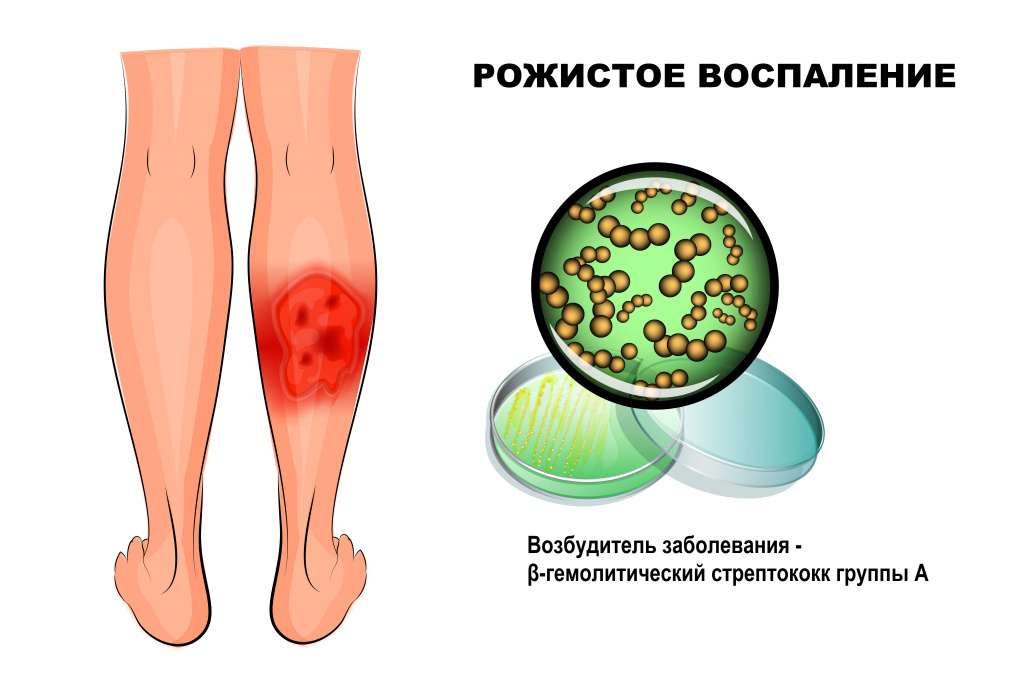
Причины появления рожистого воспаления
Стрептококк группы А (Streptococcus pyogenes) широко распространен в окружающем мире, может являться возбудителем инфекций мягких тканей (импетиго, рожи), верхних дыхательных путей (фарингита, тонзиллита), инфекционных заболеваний (скарлатины), ревматической болезни сердца, постстрептококкового гломерулонефрита и др.
Занос возбудителя на кожу происходит через руки из первичного источника инфекции (например, из носоглотки) при наличии любых (даже минимальных) нарушениях целостности кожного покрова. Инкубационный период составляет от 2 до 7 дней.
Из очагов стрептококковой инфекции процесс может распространяться лимфогенно (по лимфатическим путям) или гематогенно (с током крови). Наличие в крови бактерий и их токсинов приводит к интоксикации (повышению температуры тела, ознобу, слабости и др.).
Предрасполагающими факторами развития рожи могут быть:
- сопутствующие заболевания (микозы стоп, сахарный диабет, ожирение, хроническая венозная недостаточность при варикозной болезни вен, хроническая недостаточность лимфатических сосудов (лимфостаз), экзема и др.);
- наличие очагов хронической стрептококковой инфекции (тонзиллита, отита, синусита, кариеса, пародонтоза, остеомиелита, тромбофлебита, трофических язв);
- профессиональные вредности, связанные с повышенной травматизацией, загрязнением кожных покровов, ношением резиновой обуви и др.;
- хронические соматические заболевания со снижением иммунитета;
- пожилой возраст.
Классификация заболевания
По кратности течения выделяют следующие виды рожистого воспаления:
- первичное;
- повторное (через два года и более после первого случая заболевания или в более ранние сроки, но при иной локализации процесса);
- рецидивирующее (рецидивы возникают в период от нескольких дней до 2 лет при одной и той же локализации процесса).
- эритематозная рожа;
- эритематозно-буллезная рожа;
- эритематозно-геморрагическая рожа;
- буллезно-геморрагическая рожа.
- рожистое воспаление на лице;
- на волосистой части головы;
- на верхних конечностях;
- на нижних конечностях;
- на туловище;
- на половых органах.
- легкая рожа;
- средней тяжести рожа;
- тяжелая рожа.
- локализованное рожистое воспаление - местный процесс захватывает одну анатомическую область (например, голень или лицо);
- распространенное (мигрирующее) рожистое воспаление - местный процесс захватывает несколько смежных анатомических областей;
- метастатическое рожистое воспаление с возникновением отдаленных друг от друга очагов (например, голень и лицо и т.д.).
На участках кожи, где впоследствии возникают локальные поражения, некоторые пациенты ощущают расстройство чувствительности, распирание, жжение, болезненность.
Увеличиваются и становятся болезненными регионарные лимфатические узлы. Затем на коже появляется небольшое красное или розовое пятно, которое превращается в эритему – четко отграниченный участок покрасневшей кожи с неровными границами в виде зубцов, языков. Кожа в области эритемы уплотнена, напряжена, горячая на ощупь, умеренно болезненная при пальпации, напоминает кожуру апельсина.
При эритематозно-буллезной и буллезно-геморрагической форме воспаления происходит отслойка эпидермиса с образованием пузырей. При буллезно-геморрагической роже пузыри (буллы) разных размеров заполнены геморрагическим (кровянистым) или фиброзно-геморрагическим содержимым, имеются обширные кровоизлияния в кожу.
Для эритематозно-геморрагической формы рожи характерны кровоизлияния различных размеров (от небольших до обширных сливных) в кожу на фоне рожистой эритемы.
По выраженности симптомов интоксикации, распространенности и характеру местного процесса определяют тяжесть течения рожи.
Легкая форма рожистого воспаления протекает с субфебрильной температурой тела (не выше 38°С), слабо выраженными симптомами интоксикации. Температура держится 1-2 дня. Чаще всего наблюдается эритематозный характер поражения кожи.
Для тяжелого течения характерно повышение температура тела до 40°С и выше более 4 дней, выраженные симптомы интоксикации, сходные с симптомами менингита (сильная головная боль, рвота, иногда бред, спутанность сознания, судороги). Местный процесс – выраженный и распространенный, часто с наличием обширных булл и геморрагий.
При своевременно начатом лечении и неосложненном течении заболевания продолжительность лихорадки составляет не более 5 суток.
Лихорадка, длительность которой превышает 7 суток, свидетельствует о генерализации процесса и неэффективности терапии.
Выздоровление начинается с нормализации температуры и исчезновения симптомов интоксикации. Острые местные проявления рожи сохраняются при эритематозной форме до 5-8 суток, а при геморрагических - до 12-18 суток и более.
До нескольких недель и даже месяцев после выздоровления могут сохраняться застойная гиперемия, пастозность и пигментация кожи в местах поражения рожей, плотные сухие корки на месте булл, отечный синдром.
Диагностика рожистого воспаления
Рожа подозревается при наличии у пациента следующих проявлений:
- острого начала заболевания с повышением температуры тела;
- выраженной интоксикации;
- локального чувства жжения и распирания в пораженной области;
- характерного поражения кожи (эритемы с четкими границами, краевым валиком и отеком);
- регионального лимфаденита.
-
Клинический анализ крови с определением концентрации гемоглобина, количества эритроцитов, лейкоцитов и тромбоцитов, величины гематокрита и эритроцитарных индексов (MCV, RDW, MCH, MCHC), лейкоформула и СОЭ (с микроскопией мазка крови при наличии патологических сдвигов).
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Читайте также:

