Каким эпителием представлена слизистая оболочка пищевода
Обновлено: 22.04.2024
Пищевод. Слизистая пищевода. Строение стенки пищевода.
Источником развития эпителия пищевода является материал прехордальной пластинки. Остальные ткани стенки пищевода за некоторым исключением развиваются из мезенхимы. Выстилка пищевода сначала представлена однослойным цилиндрическим эпителием. Затем этот эпителий становится двухслойным. Сильно разрастаясь, он полностью закрывает просвет пищевода.
Последующий апоптоз клеток ведет вновь к образованию просвета, а выстилка пищевода к 3-му месяцу эмбриогенеза состоит из многорядного мерцательного эпителия. С 6-го месяца эмбриогенеза эпителий преобразуется в многослойный плоский с островками мерцательных или ороговевших клеток. Постепенно усложняется строение и всех остальных тканей в составе стенки пищевода.
В стенке пищевода взрослого человека различают слизистую оболочку, подслизистую основу, мышечную и адвентициальную оболочки. Слизистая оболочка состоит из многослойного плоского неороговевающего эпителия, собственной соединительнотканной и гладкомышечной пластинок. В эпителии ведущий клеточный дифферон представлен эпителиоцитами, находящимися на последовательных стадиях дифференци-ровки. Вместе с тем встречаются немногочисленные клетки Лангерганса и эндокринные клетки.
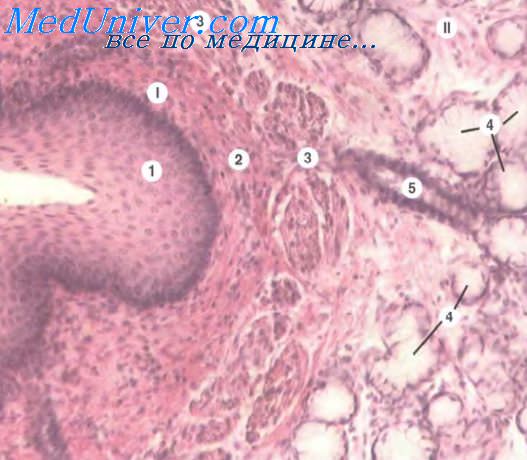
В собственной пластинке слизистой оболочки пищевода в верхней и нижней его трети расположены кардиаль-ные железы пищевода, которые по своему строению схожи с таковыми желудка. Это простые разветвленные трубчатые железы, концевые отделы которых образованы однорядным кубическим эпителием, в составе которого много мукоцитов и разновидностей эндокриноцитов. Из этих желез возникают кисты и опухоли.
Появление кардиальных желез в пищеводе объясняется меторизисом. Этим термином В.М. Шимкевич (1908) обозначил смещение границ между производными двух соседних эмбриональных зачатков. Полагают, что в области перехода пищевода в желудок материал кишечной энтодермы смещается в сторону пищевода и дает начало железам желудочного типа в пределах слизистой оболочки пищевода.
Мышечная пластинка слизистой оболочки состоит из продольно ориентированных пучков гладких мышечных клеток, изменение тонуса которых способствует прохождению пищи по пищеводу в желудок.
В подслизистой основе располагаются собственные слизистые железы пищевода — производные эпителия пищевода. Это альвеолярно-трубчатые железы. Их концевые отделы образованы мукоцитами, постоянно выделяющими слизь. Расширенные выводные протоки выстланы низким цилиндрическим эпителием, переходящим в многослойный плоский эпителий. Среди его клеток встречаются эндокринные клетки — серотониноциты.
Мышечная оболочка пищевода в верхней трети образована поперечнополосатой мышечной тканью миотомного происхождения, в нижней трети — гладкой мезенхимной природы, а в средней трети — и той, и другой мышечными тканями. Эти ткани расположены в виде внутреннего циркулярного и наружного продольного слоев. Утолщения внутреннего циркулярного слоя мышечной оболочки образуют сфинктеры пищевода: верхний — на уровне перстневидного хряща гортани и нижний — в области перехода пищевода в желудок. Мышечная ткань иннервируется преимущественно волокнами блуждающего нерва. Сокращение ее способствует продвижению пищи из пищевода в желудок.
Адвентициальная оболочка пищевода образована рыхлой волокнистой соединительной тканью, содержащей кровеносные сосуды, нервы и нервные сплетения.
Регенерация пищевода как физиологическая, так и репаративная выражена достаточно хорошо. После хирургических операций на пищеводе в связи с опухолевыми процессами, ожогами, ранениями и т. д. происходит обычно полное восстановление эпителия и соединительнотканных структур в составе стенки пищевода.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Нормальная анатомия, физиология пищевода
Пищевод — мышечная трубка, соединяющая ротоглотку с желудком. Он начинается на уровне нижнего края перстнегло-точной мышцы. Длина пищевода приблизительно 25 см. Верхняя треть его образована поперечно-полосатой мускулатурой, остальная часть — гладкой. Изнутри мышечная трубка выстлана плоским эпителием.
В средостении пищевод окружен двумя стволами блуждающего нерва, трахеей, аортой, сердцем. С помощью рентгеновского исследования при контрастировании барием на пищеводе можно обнаружить вдавления от аорты и левого бронха, при этом можно увидеть не только структуру нормальной слизистой оболочки, но и небольшое сужение приблизительно на 2 см ниже диафрагмы; расширение под ним называют «желудочком», или «ампулой диафрагмы».
При рентгеновском исследовании это образование не следует путать с пищеводной грыжей. Пищевод впадает в желудок в области угла сразу под диафрагмальной вырезкой и приблизительно на расстоянии 40 см от края резцов.
Пища проходит по пищеводу благодаря координированному сокращению его мышечных слоев. Эта волна перистальтики относительно медленная: скорость ее движения по направлению к желудку составляет 2—6 см/с. В ответ на жевание возникает первичная перистальтика, а вторичная начинается ниже подглоточной области в отсутствии предшествующих жевательных движений. Барьерная функция пищевода зависит от функционального состояния верхнего перстнеглоточного сфинктера и нижнего пищеводного сфинктера (НПС).
В области НПС давление достаточно высокое (в норме 15—35 мм рт.ст.), на протяжении нижних 3—4 см пищевода оно имеет сходные значения; в данном случае определенной анатомической структуры не существует. Манометрию подвижности пищевода обычно проводят с помощью трансназального катетера. В норме при глотании перстнеглоточный сфинктер расслабляется до прохождения пищевого комка, происходит его сокращение, а затем — перистальтические сокращения вдоль тела пищевода.
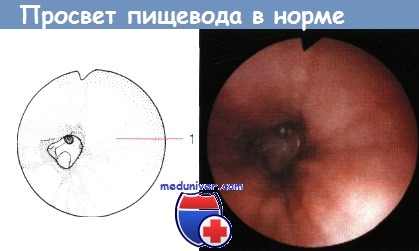
Эндоскопическая картина пищевода здорового человека. Видна бледно-розовая слизистая оболочка:
1 — нормальная слизистая оболочка
НПС расслабляется только непосредственно перед тем, как его достигает волна сокращений, обеспечивая, таким образом, прохождение пищевого комка в желудок. Однако одного сокращения НПС недостаточно для предотвращения гастро-эзофагеального рефлюкса — одновременно происходит сжатие поддиафрагмальной части пищевода в результате увеличения внутрижелудочного или внутрибрюшного давления. Вхождение пищевода в желудок под углом в данном случае играет роль дополнительного фактора защиты.
Внутри пищевода рН обычно достигает значений 5—7, длительный низкий его уровень (менее 4) считается ненормальным. Кислотность лучше всего оценивать с помощью 24-часового рН-мониторирования.
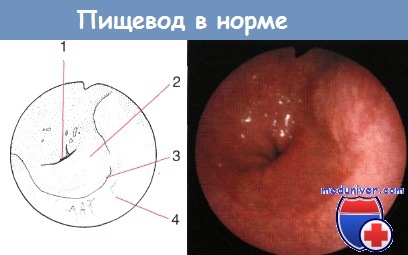
Вариант нормы. Переход плоского эпителия в цилиндрический (Z-линия):
1 — вход в желудок;
2 — цилиндрический эпителий (слизистая оболочка «желудочного» типа);
3 — переход плоского эпителия в цилиндрический (Z-линия);
4 — плоский эпителий слизистой оболочки пищевода
При эндоскопии пищевод выглядит как гладкая трубка с видимыми сосудами в подслизистом слое. В области соединения пищевода с желудком переход слизистой оболочки одного органа в слизистую оболочку другого органа обычно имеет вид неправильной круговой полосы, известной как Z-линия, или желудочная розетка. При обследовании часто можно наблюдать волны перистальтики.
Просвет пищевода выстлан неороговевающим плоским эпителием. Сосочки — выпячивания собственной пластинки слизистой оболочки — проникают на небольшое расстояние в эпителий. Собственная пластинка отделена от подслизистого слоя волокнами гладкой мускулатуры, или мышечной пластинкой слизистой оболочки. Круговые мышечные волокна лежат глубже подслизистого слоя, между ними и внешними продольными мышцами проходит межмышечное нервное сплетение.
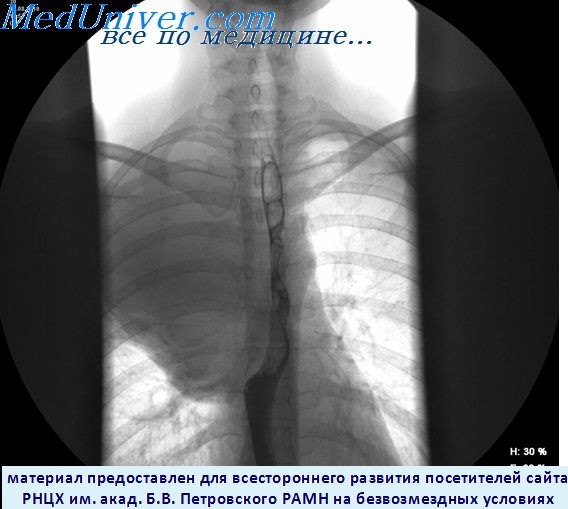
Эзофагография при низкодифференцированном раке верхней доли правого легкого
Учебное видео по анатомии пищевода и его сужений
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Пищевод (лат. – oesophagus, эзофагус) является структурным элементом ЖКТ (желудочно-кишечного тракта).
Строение и функции

Пищевод соединяет глотку с желудком. В начальном отделе ЖКТ, в ротовой полости, пища измельчается, увлажняется слюной, и частично переваривается. В желудке осуществляется ее дальнейшее переваривание. А эзофагус служит для механического продвижения пищи.
Орган представляет собой полую эластичную трубку. Эта трубка состоит из трех оболочек:
- Внутренняя. Слизистая оболочка с подслизистым слоем. Служит для увлажнения и плавного продвижения пищеводного комка.
- Средняя. Мышечная оболочка, в свою очередь, представлена двумя слоями – наружным продольным, и внутренним круговым или циркулярным. Сокращение гладких циркулярных мышц приводит к сужению пищеводного просвета, а сокращение продольных мышц – наоборот, к его расширению. Содружественная работа гладких и поперечных мышц обеспечивает перистальтику, волнообразные сокращения пищевода для продвижения пищи. Кроме того, в пищеводе имеются два сфинктера, мышечные клапаны верхний, глоточный, и нижний кардиальный. Оба сфинктера, смыкаясь, изолируют пищевод от глотки и желудка.
- Наружная. Адвентициальная оболочка. Представлена рыхлой соединительной тканью, и снаружи покрывает шейный и грудной отделы пищевода. Брюшной отдел покрыт брюшиной.
Пищевод берет начало в шее на уровне VI-VII позвонков, простирается через грудную полость, и через отверстие в диафрагме входит в брюшную полость. В этой связи выделяют 3 отдела пищевода:
- Шейный. От VI-VII шейного до II грудного позвонка. Длина 5-8 см.
- Грудной. Основной отдел длиной 15-18 см, простирается до входа в диафрагму.
- Брюшной. От диафрагмального отверстия до входа в желудок. Длина 1-3 см.
А всего длина пищевода у взрослого человека составляет 25-30 см. Диаметр внутреннего просвета – 2-2,5 см, но может расширяться до 4-4,5 см. В пищеводе имеются три анатомических сужения. Их локализация:
- Переход глотки в пищевод.
- Уровень V грудного позвонка, соответствующий раздвоению или бифуркация трахеи на два бронха.
- Прохождение пищевода через диафрагму.
Частичная или полная непроходимость пищевода для пищи, как правило, формируется в области этих сужений.
Заболевания и симптомы
В клинической практике чаще всего приходится сталкиваться с воспалениями слизистой оболочки пищевода, эзофагитом. К эзофагиту предрасполагает раздражение слизистой оболочки грубой, острой, горячей пищей, алкоголем.
Иногда эзофагит обусловлен обменными расстройствами, авитаминозами, аллергическими реакциями, бактериальной и вирусной инфекцией. Зачатую в основе эзофагита лежит рефлюкс, заброс желудочного содержимого в пищевод. Давление внутри желудка выше, чем внутри пищевода. В норме кардиальный сфинкер сомкнут, и это препятствует рефлюксу.
При заболеваниях желудка, других отделов ЖКТ, неврологических расстройствах из-за несостоятельности кардиального сфинктера желудочное содержимое забрасывается в нижнюю часть пищевода. Кислое содержимое желудка разъедает пищеводную слизистую. Здесь формируется воспаление, а затем появляются язвы пищевода.
Рефлюкс-эзофагит настолько типичен для патологии ЖКТ, что его выделили в самостоятельное заболевание. Рефлюкс-эзофагит и пищеводные язвы нередко сочетаются с грыжей пищеводного отверстия диафрагмы, когда часть желудка вместе с брюшным отделом пищевода через диафрагмальное отверстие смещается из брюшной полости в грудную. На фоне хронического воспаления формируются пищеводные полипы. Со временем эти доброкачественные опухоли могут трансформироваться в рак пищевода.
Иногда врачам-хирургам приходится сталкиваться с синдромом Маллори-Вейса. Этот синдром характеризуется наличием линейных разрывов слизистых нижних отделов пищевода и кардиального отдела желудка при общем тяжелом состоянии пациента. Причины: хронические эзофагиты, гастриты, систематический прием некоторых лекарств, злоупотребление алкоголем.
Еще одна частая патология – дискинезия пищевода, характеризующаяся спазмом или параличом сфинктеров, нарушением моторики, двигательной активности, пищевода. Дискинезия, как правило, связана с функциональными расстройствами вегетативной нервной системы при неврозах. Но могут быть и более серьезные причины – мозговые инсульты, черепно-мозговые травмы, опухоли головного мозга, когда нарушается мозговая регуляция пищеводной моторики.
Типичные симптомы заболеваний пищевода:
- дисфагия (нарушения глотания);
- жжение, болезненность за грудиной по ходу пищевода, усиливающееся во время еды;
- рвота съеденной пищей;
- регургитация – в отличие от рвоты пассивный процесс, по сути, срыгивание;
- боль в глотке при глотании из-за раздражения кислым содержимым.
В редких случаях отмечаются инородные тела пищевода вследствие случайного заглатывания посторонних предметов. При этом существует опасность перфорации, разрыва пищеводной стенки. Еще одна опасность по неосторожности – химический ожог пищевода кислотами и щелочами. По мере заживления ожог осложняется рубцовым сужением, стенозом пищевода с его частичной непроходимостью.
Диагностика
Самый простой метод диагностики – рентгенография пищевода с контрастированием бариевой взвесью. Пациент глотает взвесь бария сульфата, а врач на рентгенаппарате оценивает, как она продвигается.
Более надежный метод – ФГДС (фиброгастродуоденоскопия). С помощью эндоскопической аппаратуры врач оценивает состояние слизистых оболочек пищевода, желудка, и 12-перстной кишки.
Современные методы исследования пищевода – эзофагоманометрия и импеданс рН-метрия. При этих исследованиях используют зонды, снабженные датчиками и измерительными приспособлениями. После введения этих зондов в пищеводный просвет определяется сократительная способность мускулатуры пищевода, внутрипищеводное давление, кислотность (рН) внутрипищеводной среды. Данные методы используют для диагностики дискинезии, гастроэзофагального рефлюкса.
Препарат 34.
| Пищевод; поперечный срез. Окраска гематоксилин-эозином. |
(Нижеследующее описание основывается на материале раздела 23.3.)
А. Общий план строения
слизистая оболочка (I),
подслизистая основа (II),
мышечная оболочка (III),
адвентициальная оболочка (IV),
Рассмотрим строение этих оболочек более подробно.
Б. Слизистая оболочка
2. Слизистую оболочку составляют:
многослойный плоский неороговевающий эпителий (1)
(в пожилом возрасте - частично ороговевающий),

б) (Среднее увеличение)
собственная пластинка (2) , образованная рыхлой соединительной тканью;
и мышечная пластинка (3) :
в верхней трети пищевода это лишь отдельные продольные пучки гладких миоцитов;
ниже - они сливаются в единую пластинку.
в) (Большое увеличение)

кардиальные железы пищевода (на снимке не видны);
на уровне перстневидного хряща гортани и
у входа в желудок.
В. Подслизистая основа
рыхлой волокнистой соединительной тканью с большим содержанием адипоцитов.
б) По морфологии это
сложные разветвлённые альвеолярно-трубчатые железы;
в) (Большое увеличение)
г) Их в ыводные протоки (5) проходят через слизистую оболочку и открываются на поверхности эпителия.
3. Заметим: в последующих отделах желудочно-кишечного тракта железы с такой же локализацией (в подслизистой основе) встречаются лишь
Г. Мышечная оболочка
внутренний (6) -
у человека циркулярный,
а у собаки (см. препарат) - продольный;наружный (7 ) -
у человека - продольный,
у собаки (см. препарат) - циркулярный.
3. Тип мышечной ткани в мышечной оболочке зависит от уровня пищевод а:
в верхней трети - это только поперечнополосатая мышечная ткань,
в средней трети - и поперечнополосатая, и гладкая мышечные ткани,
в нижней трети - только гладкая мышечная ткань ( у человека), (у собаки - оба типа).
Д. Адвентициальная (серозная) оболочка
Е. Интрамуральный нервный аппарат
2. Он включает 3 нервных сплетения:
подслизистое - в подслизистой основе,
межмышечное - между двумя слоями мышечной оболочки,
подсерозное или субадвентициально е - на границе между мышечной и серозной (адвентициальной) оболочками.
3. В составе этих сплетений -
интрамуральные нервные ганглии (один из которых мы видели в мышечной оболочке)
и соответствующие отростки нервных клеток.
4 . С участием интрамуральных сплетений могут замыкаться рефлекторные дуги различной протяжённости -
местные, или периферические;
дуги, включающие ядра спинного мозга;
дуги, включающие ядра головного мозга.
Ж. Отличия препарата пищевода от препарата мочеточника
поскольку они изготовлены из органов разных животных, ожидаемого различия размеров обычно нет.
б) Остаётся ориентироваться на гистологические особенности.
в пищеводе он многослойный плоский неороговевающий (форма поверхностных клеток - плоская);
в мочеточнике - другая разновидность многослойного эпителия: переходный эпителий (форма поверхностных клеток - округлая, точнее - куполообразная).
2. Подслизистая основа:
в пищеводе она содержит много достаточно крупных слизистых желез;
в мочеточнике железы встречаются лишь в нижней половине органа, будучи при этом мелкими и редкими;
фактически же в студенческом препарате их, как правило, нет.
3. Мышечная пластинка слизистой оболочки:
в пищеводе между собственной пластинкой слизистой оболочки и подслизистой основой имеются гладкие миоциты мышечной пластинки;
в мочеточнике же такой пластинки нет, так что собственная пластинка слизистой оболочки непрерывно переходит в подслизистую основу.
1 ФГБОУ ВО «Ростовский государственный медицинский университет» Министерства здравоохранения Российской федерации

1. El-Serag H.B. Update on the epidemiology of gastroesophageal reflux disease: a systematic review / H.B. El-Serag, S. Sweet, C.C. Winchester, J. Dent // Gut. – 2014. – Vol. 63, № 6. – P. 871-878.
2. Бордин Д.С. Алгоритм ведения больных гастроэзофагеальной рефлюксной болезнью // Человек и лекарство. – 2011. – Т. 2. – С. 326–338.
4. Kgomo M. Non-acid gastro-oesophageal reflux is associated with squamous cell carcinoma of the oesophagus / M. Kgomo, T.R. Mokoena, A.J. Ker // BMJ Open Gastroenterol. – 2017. – Vol. 4, № 1. – P. 000180.
5. Monkemuller K. Role of tight junction proteins in gastroesophageal reflux disease / K. Monkemuller, T. Wex [et al.] // Gastroenterol. – 2012. – Vol. 12, № 128. – P. 1-12.
6. Kandulski A. Histomorphological differentiation of non- erosive reflux disease and functional heartburn in patients with PPI-refractory heartburn / A. Kandulski, D. Jechorek C. Caro [et al.] // Aliment. Pharmacol. Ther. – 2013. – Vol. 38. – P. 643–651.
8. Souza R.F. From Reflux Esophagitis to Esophageal Adenocarcinoma // Dig Dis. – 2016. – Vol. 34, № 5. – P. 483-490.
9. Amaral J.D. Bile acids: regulation of apoptosis by ursodeoxycholic acid / J.D. Amaral, R.J. Viana, R.M. Ramalho [et al.] // J. Lipid. Res. - 2009. – Vol. 50, № 9. – P. 1721–1734.
11. Pardon N. Effect of the perfusion of acidic and weakly acidic solutions on mucosal integrity and expression of cell-to-cell adhesion proteins in humans / N. Pardon, H. Vanheel, J. Toth // Neuro gastroenterol. Motil. – 2014. – Vol. 26. – P. 36-37.
12. Oshima T. Acid modulates the squamous epithelial barrier function by modulating the localization of claudins in the superficial layers / T. Oshima, J. Koseki, X. Chen [et al.] // Lab. Invest. – 2012. – Vol. 92. – P. 22–31.
13. Ивашкин В.Т. Гастроэзофагеальная рефлюксная болезнь. Клинические рекомендации / В.Т. Ивашкин, И.В. Маев, А.С. Трухманов [и др.] // Российский журнал гастроэнтерологии гепатологии, колопроктологии. – 2017. – Т. 27, № 4. – С. 75-95.
14. Swami S. E-cadherin expression in gastroesophageal reflux disease, Barrett's esophagus, and esophageal adenocarcinoma: an immunohistochemical and immunoblot study / S. Swami, S. Kumble, G. Triadafilopoulos // Am J. Gastroenterol. – 1995. – Vol. 90. – 1808–1813.
15. Jovov B. Role of E-cadherin in the pathogenesis of gastroesophageal reflux disease / B. Jovov, J. Que., N.A. Tobey [et al.] // Am. J. Gastroenterol. – 2011. – Vol. 106. – P. 1039–1047.
Несмотря на несомненные успехи в лечении и контроле ряда кислотозависимых заболеваний, проблема гастроэзофагеальной рефлюксной болезни (ГЭРБ) сохраняет актуальность ввиду высокой распространённости, рефрактерности течения на фоне стандартной терапии и высоких рисков осложненного течения с развитием факультативного предракового состояния - пищевода Барретта (ПБ) [1; 2]. Среди известных пусковых факторов заболевания [3] особый интерес представляют изменения функционального состояния слизистой оболочки (СО) пищевода под воздействием рефлюктата разного характера [4]. Кроме этого, установлено, что проницаемость эпителиального барьера регулируется с помощью молекул межклеточной адгезии и межклеточных контактов [5], которые могут выступать биомаркерами ГЭРБ даже при эндоскопически неизмененной СО пищевода [6]. Однако при его нарушении и повреждении субэпителиального пространства развивается каскад реактивных воспалительных, пролиферативных, регенераторных, а часто и дисрегенераторных процессов, что определяет развитие и тяжесть ГЭРБ [5]. При оценке влияния рефлюктата различной кислотности на морфологическую картину СО пищевода, по данным эндоскопического исследования и 24 часовой pH-импедансометрии, была выявлена прямая зависимость между продолжительностью ацидификации пищевода и выраженностью воспалительных изменений [7]. Так, у пациентов с преимущественно кислым характером рефлюктата частота эрозивно-язвенных изменений СО выше, чем у пациентов со смешанным и щелочным рефлюктатом, у которых имеются высокие риски метаплазии эпителия [8], что объясняется его воздействием на процессы апоптоза и клеточной дифференцировки [9]. Таким образом, под воздействием агрессивного характера рефлюктата происходит ослабевание межклеточных соединений с дальнейшим повреждением эпителия и подлежащих тканей, при этом кислотный «ожог» вызывает гибель клеток и лейкоцитарную инфильтрацию, а некроз, в свою очередь, запускает процессы регенерации, пролиферации базальных клеток и папиллярную гиперплазию базальных кератиноцитов [9].
Анализ литературы позволяет сделать выводы о том, что изменение соотношения и морфологии белков межклеточных контактов коррелирует с увеличением тяжести ГЭРБ [10]. На сегодняшний день наиболее изученными из них являются окклюдины 1, 2, 3, 4, E-кадгерин, семейство клаудинов (1,2), ß-катепсин, реже - EpСАМ, CD44, v4, v5, v6, но полученные данные остаются противоречивыми и требуют уточнения. Так, Pardon N. еt al. (2014), оценивая влияние кислого рефлюктата на функциональную целостность эпителиального барьера и экспрессию белков семейства клаудинов (1, 2, 4), оксида азота-1, филлаггина и оклюдина, не зарегистрировали статистически значимых изменений изучаемых показателей, что, возможно, обусловлено преимущественной локализацией данных белков в зоне кардиоэзофагеального перехода и их «перераспределением» в ответ на воздействие компонентов гастроэзофагеального рефлюктата [11]. К аналогичным выводам ранее пришли Oshima Т. еt al. (2012) - воздействие кислоты на СО пищевода вызывает «делокализацию» клаудин-4 в поверхностном слое пищеводного эпителия [12]. В исследовании Björkman E.V. (2013) была рассмотрена роль щелочного рефлюкса в функциональной состоятельности эпителиального барьера и белков межклеточных контактов эпителия [10]. Установлено, что желчные кислоты и низкие концентрации трипсина увеличивают экспрессию клаудина-1, в то время как высокие - снижают экспрессию Е-кадгерина, клаудина-3 и -4, что позволило авторам сделать выводы, что щелочной рефлюктат повреждает эпителиальный барьер пищевода путем модуляции белков межклеточных контактов [10].
Известно, что E-кадгерин (cadherin) - одна из центральных молекул клеточной адгезии в эпителиальных тканях, локализованная на мембране и участвующая в образовании адгезионных контактов, являющихся характерной особенностью этих тканей. Установлено, что в тканях взрослого человека E-кадгерин участвует в формировании эпителиального пласта [10]. При этом две молекулы E-кадгерина, прилегающих к друг другу клеток, соединяются посредством внеклеточного домена, функционирующего исключительно в присутствии ионов Са2+, образуя между ними адгезионные контакты. В немногочисленных экспериментальных исследованиях была показана роль E-кадгерина в обеспечении клеточной пролиферации и дифференцировки [10]. Имеющиеся в настоящее время данные свидетельствуют о том, что функции, связанные с E-кадгерином и β-катенином, играют двойственную роль: с одной стороны, участвуют в формировании межклеточных контактов, а с другой - выступают регуляторами сигнальных путей. По данным ряда авторов [14], изменения экспрессии Е-кадгерина при ГЭРБ, особенно при ее осложненном течении, позволяют рассматривать эту молекулу в качестве раннего маркера прогрессирования заболевания. Так, в исследовании Jovov B. еt al. (2011) установлено, что проницаемость эпителиального барьера зависит от структурной целостности E-кадгерина, расщепление которого, вероятно, является пусковым фактором в патогенезе ГЭРБ. Авторы предположили, что идентификация расщепленных фрагментов молекулы E-кадгерина может быть ценным биомаркером ГЭРБ [15]. Кроме этого, Roy C. Orlando et al. в 2011 г. зарегистрировали патент «E-кадгерин как биомаркер ГЭРБ», показав прямую связь между изменением концентрации концевых N-фрагментов указанного белка в сыворотке крови и тяжестью ГЭРБ. Таким образом, представляется целесообразным рассмотреть эти аспекты более подробно.
Цель: изучить экспрессию отдельных компонентов межклеточных соединений при различных формах ГЭРБ и ПБ.
Настоящее исследование выполнено в период с 2016 по 2017 г. на базе консультативно-диагностической поликлиники и гастроэнтерологического отделения клиники ФГБОУ ВО «РостГМУ». На I этапе проводилось комплексное клиническое обследование по стандартному протоколу для пациентов с ГЭРБ [13]. Диагноз верифицирован с использованием клинико-анамнестических данных, инструментальных методов обследования, включающих: видеоэзофагогастродуоденоскопию с детальным осмотром дистального отдела пищевода в режиме NBI с биопсией и морфологическим исследованием эзофагобиоптатов; 24-часовую внутрипищеводную pH-импедансометрию. Критериями включения пациентов в исследование являлись: амбулаторные и стационарные больные с диагнозом ГЭРБ и ПБ в возрасте от 18 до 55 лет, ограничение приема антисекреторных препаратов в течение 1 мес. Ранжирование больных проводилось в зависимости от результатов 24-часовой внутрипищеводной pH-импедансометрии, демонстрирующих особенности преобладающего характера рефлюктата. Сформированы две исследовательские когорты больных: 1-я группа – 22 пациента (13 женщин и 9 мужчин, средний возраст 44,1±15,3 года) с кислым и слабокислым характером рефлюктата, 2-я группа – 12 больных (4 женщины, 8 мужчин, средний возраст 48,7±12,1 года) с преимущественно щелочным и слабощелочным рефлюксом. В 1-й группе преобладали пациенты с градацией эрозивного эзофагита (ЭЭ) А и В, во 2-й - больные с ЭЭ градации С, D и ПБ (Лос-Анджелесская классификация рефлюкс-эзофагита, 1994) (табл. 1). Группу сравнения составили 20 здоровых добровольцев.
Распределение пациентов с ГЭРБ в зависимости от градации рефлюкс-эзофагита и характера рефлюктата
Читайте также:

