Какие препараты принимают при вирусе папилломы человека
Обновлено: 07.05.2024
В последние годы увеличивается заболеваемость папилломавирусной инфекцией. По данным ВОЗ, ежегодно в мире около 250 000 женщин с ВПЧ-инфекцией умирает от рака шейки матки. На этом фоне поиск эффективных методов лечения этой инфекции становится чрезвычайно важным. Проблема ее диагностики и лечения привлекает внимание врачей различных специальностей: дерматологов, гинекологов, урологов, онкологов, иммунологов, вирусологов, патоморфологов. На данный момент большинство ученых пришли к единому мнению – с проявлениями вируса папилломы человека можно бороться при помощи применения иммуномодуляторов с противовирусной активностью.
Что такое иммуномодуляторы
К иммуномодулирующим средствам относятся препараты химической и биологической природы, способные модулировать (угнетать или стимулировать) реакции иммунитета. При этом иммунологический эффект иммуномодуляторов зависит от исходного состояния иммунитета человека: эти лекарственные средства понижают повышенные и повышают пониженные показатели иммунитета. Особенно данный постулат относится к препаратам интерферона. К иммунотерапии также относятся методы лечения, основанные на использовании иммунотропных средств при заболеваниях, в патогенезе которых имеются нарушения, затрагивающие систему иммунитета.
Основной критерий для назначения иммуномодуляторов – это клиническая картина заболевания (острого или хронического инфекционно-воспалительного процесса), который сопровождается снижением параметров иммунитета и трудно поддается лечению. В этом случае иммуномодуляторы играют роль главного помощника, который способствует эффективной терапии и избавляет от проявлений многих заболеваний.

Поскольку ВПЧ-инфекция тоже относится к недугам, с которыми достаточно непросто бороться, а исход лечения зависит от состояния иммунитета, при лечении этой инфекции широко применяют различные иммуномодуляторы.
Иммуномодуляторы при ВПЧ: список препаратов
Препараты, которые являются синтетическими комплексными производными пурина
Эта группа иммуномодуляторов, применяющихся при лечении проявлений вируса папилломы человека, обладают иммуностимулирующей активностью и неспецифическим противовирусным действием. Они восстанавливают активность лимфоцитов, которые являются главными клетками иммунной системы. Клинически доказано, что именно низкая активность лимфоцитов является предрасполагающим фактором к яркому развитию клинических проявлений ВПЧ. Также этот вид препаратов повышает функционирование натуральных киллеров и так называемыхТ-хелперов – T-лимфоцитов, главной функцией которых является координация иммунного ответа.
Некоторые из препаратов этой группы имеют обширный список побочных действий, включающих проблемы с работой ЖКТ, печени и желчевыводящих путей. Также возможны побочные реакции в виде головной боли, сонливости, бессонницы, зуда и болей в суставах. Среди противопоказаний – детский возраст до 3 лет, беременность, заболевания почек и повышенная чувствительность к компонентам препарата.
Препараты с действующим веществом глюкозаминилмурамилдипептид (ГМДП)
ГМДП – это фрагмент оболочки патогенных бактерий, вызывающих инфекционно-воспалительные заболевания различных органов и систем. При попадании этого фрагмента в организм иммунная система воспринимает его как чужеродный патогенный агент и сразу же начинает выработку антител. Благодаря этому происходит общая активация всей иммунной системы, что способствует выздоровлению или же снижению частоты рецидивов вирусных инфекций, в том числе ВПЧ.
Среди побочных эффектов – повышение температуры тела до субфебрильных и фебрильных значений, также возможна диарея. Препараты этой группы противопоказаны при нарушениях обмена веществ и женщинам в период беременности и грудного вскармливания.
Препараты, содержащие в качестве активных компонентов натуральное растительное сырье
Эта группа препаратов была создана на основе открытия лауреата Нобелевской премии Н.Н. Семенова о мощных иммуностимулирующих свойствах биологически активных веществ, содержащихся в клетках растений. Экстракты из растений и вспомогательные компоненты усиливают неспецифическое звено иммунитета, что повышает устойчивость организма человека к различным вирусным и некоторым бактериальным инфекциям. Иммуномодулирующий эффект активизирует лейкоциты, что особенно важно при борьбе с хроническими и затяжными воспалительными процессами.
При применении этих препаратов возможны аллергические реакции. Среди противопоказаний к применению – заболевания выделительной системы, беременность, период лактации и детский возраст до 18 лет.
Противовирусные препараты против ВПЧ
После заражения клетки вирус может пребывать в свободном виде или проникает в геном клетки. В любом случае вирус изменяет нормальные клеточные процессы. И вместо того, чтобы производить все необходимое для своей жизнедеятельности, клетка обеспечивает механизмы синтеза вирусных молекул ДНК, которые в дальнейшем будут использоваться для создания новых вирусных частиц. Но не всегда вирусы способны вызывать заболевание. При адекватном иммунном ответе организм самостоятельно избавляется от вируса. При неэффективном иммунном ответе организма возможно долгое носительство вируса, что может привести к доброкачественным или злокачественным, в зависимости от типа вируса, проявлениям болезни.
Чтобы разорвать цепь бесконечного размножения вируса и последующего развития заболевания, признана необходимость лечения ВПЧ-инфекции иммуномодуляторами с противовирусной активностью, т.к. на сегодняшний день не разработано ни одного противовирусного от ВПЧ, действующего прицельно на вирус папилломы человека.
ВИФЕРОН при ВПЧ
Существуют ли препараты, которые борются с вирусами и одновременно способствуют восстановлению иммунной системы? Безусловно, такие препараты есть. Одним из таких препаратов, способствующих восстановлению иммунной системы и обладающих широким спектром противовирусной активности, является препарат ВИФЕРОН.
Рекомбинантный интерферон альфа-2b, который входит в состав этого препарата, препятствует синтезу вирусных ДНК и блокирует размножение вируса, способствует восстановлению иммунной системы, а также обладает антипролиферативными свойствами. Он идентичен человеческому интерферону альфа-2b, но производится с помощью современных технологий без использования донорской крови.
Препарат, который выпускается в виде свечей, геля и мази, разработан в результате фундаментальных исследований в области иммунологии, доказавших, что в присутствии антиоксидантов (витамины С, Е) усиливается противовирусное действие интерферона.
Способ применения и дозировки свечей ВИФЕРОН при ВПЧ
ВИФЕРОН Свечи производятся в виде ректальных суппозиториев пулевидной формы бело-желтого или желтого цвета. В процессе лечения препарат подавляет активность вирусов и повышает эффективность собственного иммунного ответа организма на патогенные микроорганизмы.
Препарат в виде Свечей (суппозиториев) можно применять при беременности (с 14-й недели), а также в период грудного вскармливания и при лечении детей.

Рекомендуемая доза для взрослых – ВИФЕРОН 500 000 ME по 1 суппозиторию 2 раза/сут через 12 ч ежедневно в течение 5-10 суток. По клиническим показаниям терапия может быть продолжена.
Можно ли применять ВИФЕРОН Свечи при ВПЧ вагинально?
Противовирусные суппозитории ВИФЕРОН выпускаются только для ректального использования. Вагинальное использование не предусмотрено в инструкции к лекарству. Применение в комплексной терапии препарата направлено на повышение уровня иммунной защиты организма в целом. Поэтому введение свечей непосредственно в очаг инфекции не требуется.
В прямой кишке присутствует множество кровеносных сосудов, всасывающих лекарство, непосредственно введенное в полость прямой кишки. Кровь от прямой кишки, минуя печень, непосредственно попадает в большой круг кровообращения. Таким образом обеспечивается системное действие препарата. Более того, печень не претерпевает дополнительной нагрузки, что является неоспоримым преимуществом препаратов с ректальным способом введения.
Лечение слизистой при ВПЧ у мужчин
При лечении проявлений вируса папилломы на слизистой у мужчин также применяются суппозитории ректальные ВИФЕРОН, которые помогут избавиться от неприятных проявлений вируса и будут способствовать укреплению иммунной системы.
Без консультации уролога не рекомендуется применять никакие лечебные кремы и мази, заниматься самолечением или вообще отказываться от терапии, назначенной врачом. При отсутствии лечения кондиломы могут разрастаться, охватывая все новые территории и поражая мочеиспускательный канал и другие внутренние органы. Предупредить развитие осложнений можно при помощи своевременного обращения к специалисту и применения противовирусных препаратов.
Альтернативные методы лечения ВПЧ на коже
Медикаментозная терапия проявлений вируса папилломы человека прекрасно сочетается с удалением новообразований в виде бородавок, папиллом на теле и кондилом, которые располагаются у мужчин и женщин в аногенитальной области (включая кожу гениталий, анус и слизистую оболочку влагалища, шейки матки, головки полового члена, прямой кишки).
Сегодня существует несколько продуктивных методов избавления от указанных новообразований, которые в большинстве своем безболезненны, безопасны и не оставляют шрамов.
Методы удаления папиллом и кондилом
Хирургическое иссечение
В настоящее время подобное вмешательство применяется нечасто, в основном используется при лечении злокачественных новообразований, когда необходимо широкое иссечение.
Медикаментозное удаление (прижигание) при ВПЧ
Это удаление наростов на коже при помощи лекарственных препаратов – растворов кислот, щелочей, солей. Новообразования на коже удаляются с помощью этих препаратов путем прижигания. Как правило, на месте удаления образуется корочка, которая отпадает в течение 5-7 дней. Полное заживление тканей происходит в течение 10-14 дней. При множественных новообразованиях могут потребоваться дополнительные процедуры.
Лазерное удаление папилломы
При этом способе удаления папилломы и кондиломы сжигаются при помощи луча лазера. При удалении не повреждаются соседние участки. После процедуры обычно остается микроскопичная ранка, которая заживает в течение 2-3 недель. Удалить лазером можно как единичные, так и множественных образования, расположенные на лице и теле, в том числе в деликатных местах (на веках, подмышками, в промежности).
Радиоволновое удаление при ВПЧ
При этом способе используют прибор Surgitron. Основная рабочая часть аппарата – электрод, который представляет собой тонкую вольфрамовую нить. На конце электрода концентрируются радиоволны высокой частоты. Воздействуя на органическую ткань, пучок волн приводит в движение молекулы воды в клетке, вследствие чего происходит разрыв клетки и она испаряется, в результате происходит «холодный» разрез тканей на нужном участке кожи или слизистой. При этом окружающие ткани, сосуды остаются неповрежденными, что в некоторых случаях позволяет избежать обильного кровотечения. После разреза радионожом на операционной ране образуется фибриновая пленка, а затем корочка, которая постепенно сходит и остается незаметный рубец.
Криодеструкция папиллом
Криодеструкция папиллом заключается в точечном воздействии на образование очень низкой температурой (около -196° С). Для этого обычно применяется жидкий азот и специальная металлическая точечная насадка, выполняющая роль проводника. Во время такой процедуры клетки папилломы погибают. Здоровые ткани в области ее формирования покрываются небольшой коркой, которая через небольшой промежуток времени отваливается.
Электрокоагуляция папиллом при ВПЧ
Этот метод предусматривает удаление патологических тканей путем воздействия на них электрическим током. Процедуру проводят при помощи специальных аппаратов, оснащенных электродом или петлей, которые нагреваются под воздействием электрического тока до высоких температур. На месте удаленной бородавки также образуется корочка, которая со временем отпадает.
Все методы удаления папиллом и кондилом имеют свои плюсы и минусы, оценить которые можно только со своим лечащим врачом с учетом индивидуальных особенностей пациента. Применение любых рецептов народной медицины, найденных на просторах интернета, также допускается только после консультации со специалистом.
Таблеток и процедур, которые раз и навсегда избавят от вируса папилломы человека, пока не существует. Однако уже сегодня существуют препараты и методы лечения, которые помогут сократить рецидивы проявлений инфекции или вообще забыть о них.
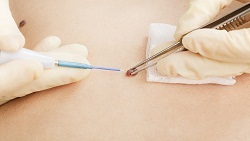
Существует множество методов лечения остроконечных кондилом.
Ни один из них не является идеальным или универсальным.
Каждый из этих методов имеет свои преимущества и недостатки.
В настоящее время лечения, избавляющего от вируса папилломы, не существует.
Современное лечение остроконечных кондилом по своей сути является симптоматическим и преследует цель удалить или уменьшить симптомы заболевания.
Оно не избавляет от вируса папилломы и не предупреждает дальнейшей передачи вируса папилломы.
После любого метода лечения остроконечных кондилом возможны рецидивы.
Методы лечения остроконечных кондилом, применяемые в настоящее время, не имеют преимуществ друг перед другом в снижении риска рецидивов.
После любого лечения остроконечных кондилом риск рецидивов составляет около 30%.
Применение таблетированных противовирусных препаратов в виде монотерапии не дает эффекта. Наиболее предпочтительна комбинированная противовирусная и иммуномодулирующая терапия, сочетающаяся с деструкцией кондилом.
В клинике "Частная практика" проводится удаление папилломатозных элементов при помощи криодеструкции, электрокоагуляции и лазера. Для максимального эффекта это осуществляется на фоне комбинированной противовирусной терапии.
Только такой подход к лечению папилломавирусной инфекции позволил снизить частоту рецидивов и сократил число таких осложнений, как рак шейки матки и полового члена.
Врач клиники "Частная практика" дерматовенеролог, уролог Волохов Е.А. рассказывает о папилломо вирусной инфекции ВПЧ.
Содержание статьи проверил и подтвердил на соответствие медицинским стандартам главный врач клиники "Частная Практика"
Что такое папилломавирусная инфекция (ВПЧ)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Борисовой Элины Вячеславовны, гинеколога со стажем в 35 лет.
Над статьей доктора Борисовой Элины Вячеславовны работали литературный редактор Юлия Липовская , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Папилломавирусная инфекция — это состояние, развивающееся при заражении какой-либо разновидностью вируса папилломы человека (ВПЧ). Возбудители данной группы могут существовать только в человеческом организме, поражая кожу и слизистые оболочки, приводя к появлению папиллом, бородавок, плоских и остроконечных кондилом. [1] [2] [4]
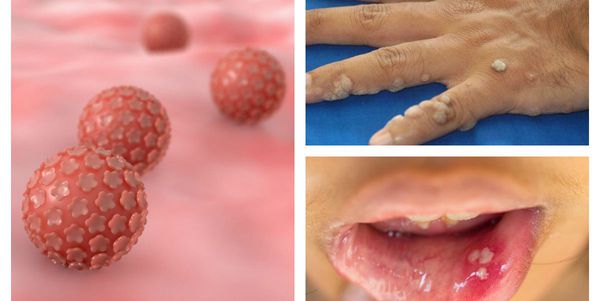
ВПЧ довольно широко распространён в человеческой популяции, особенно среди сексуально активных людей, а это свыше 80% всего населения. До недавнего времени вирусы этой группы считались относительно безобидными, вызывающими лишь косметические дефекты, но последние научные исследования показывают, что проблема гораздо серьёзнее. [9]
На сегодняшний день науке известно несколько сотен штаммов (типов) папилломавирусов . Около 40 из них преимущественно поражают аногенитальную область и передаются половым путём. Особую опасность представляют штаммы высокого онкогенного риска, так как они могут спровоцировать развитие онкологических заболеваний, в том числе рака шейки матки.
Чаще всего заражение происходит в молодом возрасте, как правило, с началом половой жизни, при этом возможно неоднократное инфицирование. Наиболее уязвимой группой в плане вероятности заражения ВПЧ и развития неблагоприятных последствий являются молодые женщины в возрасте 15-30 лет.
Помимо этого ВПЧ может перейти от инфицированной матери к ребёнку, например, при родах. Не исключается и контактно-бытовой способ передачи возбудителя, например, при соприкосновениях и даже при совместном использовании предметов личной гигиены.
К факторам риска, способствующим заражению ВПЧ, развитию хронической папилломавирусной инфекции и её переходу в предраковые состояния с потенциальным перерождением в злокачественную опухоль, относятся:
- иммунодефицит любого происхождения, в том числе вследствие ВИЧ-инфекции, лучевых поражений, применения иммунодепрессантов при трансплантации органов и тканей, лечения цитостатиками и других причин;
- подавленное состояние иммунитета во время беременности;
- раннее начало половой жизни;
- частая смена половых партнёров, незащищённый секс;
- инфицированность высокоонкогенными штаммами ВПЧ;
- заражение одновременно несколькими типами ВПЧ;
- наличие других инфекций, передающихся половым путём, например, герпесвирусной и цитомегаловирусной инфекции, вируса Эпштейна — Барр, гепатитов В и С, гонореи и трихомониаза;
- стресс, истощение, гиповитаминоз, гормональный дисбаланс;
- многократные роды и аборты;
- тяжёлые хронические заболевания, в том числе сахарный диабет;
- вредные привычки (курение, злоупотребление спиртным);
- низкий социальный статус, плохие условия жизни, неудовлетворительная интимная гигиена;
- пренебрежение регулярными профилактическими обследованиями (один из важнейших факторов риска);
- низкий уровень развития медицины в регионе проживания.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы папилломавирусной инфекции
Далеко не всегда человек догадывается о наличии в своём организме папилломавирусной инфекции, оставаясь при этом источником заражения для потенциальных партнёров. [1] [2] Дело в том, что заболевание может долгое время протекать бессимптомно: вирус скрыто существует в организме от нескольких месяцев до нескольких лет, никак себя не проявляя. Кроме того, уже имеющиеся проявления инфекции не всегда доступны для наружного обзора. Например, если папилломы, бородавки и кондиломы на открытых участках тела и поверхности гениталий ещё можно заметить самостоятельно, то патологические изменения, локализующиеся на шейке матки, сможет обнаружить только специалист в ходе осмотра с применением соответствующих инструментов.
И всё же существует несколько симптомов, которые прямо или косвенно могут указывать на наличие папилломавирусной инфекции и её неблагоприятных последствий. [3] К ним относятся:
- появление на коже и/или слизистых оболочках каких-либо разрастаний различных форм (на тонкой ножке или с широким основанием, нитевидной, округлой или плоской конфигурации, в форме цветной капусты или петушиного гребня) и размеров (от образований в несколько миллиметров до разрастаний, занимающих всю промежность);
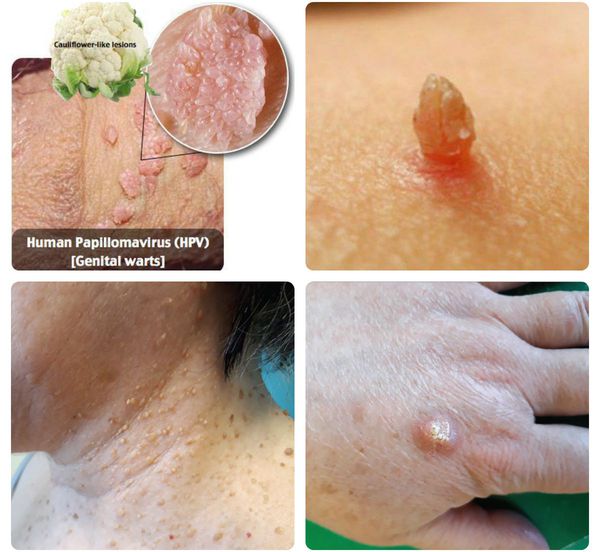
- отёчность и воспалительная инфильтрация папилломатозных разрастаний (остроконечных кондилом), их ранимость и кровоточивость, что приводит к присоединению вторичной инфекции с появлением гнойного отделяемого с неприятным запахом;
- зуд, жжение, мокнутие в области промежности, появление обильных белей, даже при отсутствии видимых патологических образований;
- межменструальные кровянистые выделения, в том числе появляющиеся в результате полового контакта:
- дискомфорт во время полового акта.
Наиболее тревожными признаками заболевания являются:
- постоянные боли в области спины и таза;
- слабость;
- беспричинная потеря веса;
- опухание одной или обеих ног.
Патогенез папилломавирусной инфекции
Заражение папилломавирусной инфекцией происходит при попадании вирусных частиц на кожу или слизистую оболочку. [1] [2] Излюбленная локализация инфекции на теле женщины — промежность, большие и малые половые губы, вульва, влагалище и шейка матки, у мужчин — половой член. Может также произойти поражение слизистой полости рта, пищевода, мочевого пузыря, трахеи, конъюнктивы и других органов и тканей.
Заражению способствуют микротравмы и потёртости. Особенно благоприятные для инфицирования условия создаются при половом акте. В 60–80% случаев достаточно однократного сексуального контакта с больным папилломавирусной инфекцией или бессимптомным носителем ВПЧ. К развитию заболевания может привести попадание в организм буквально единичных вирусных частиц.
При наличии предрасполагающих факторов (микроповреждения, слабого иммунитета и других) возбудитель проникает в эпителиальную ткань до её базального слоя. Там он прикрепляется к оболочке незрелой клетки и внедряется сначала в её цитоплазму, а затем и в ядро, где повреждает генетический аппарат. После этого начинается деление клеток с изменённым геномом, что приводит к появлению в месте внедрения вируса генитальных кондилом (образований, которые постепенно разрастаются), а, например, на шейке матки — к развитию диспластических процессов различной степени тяжести (дисплазия шейки матки).
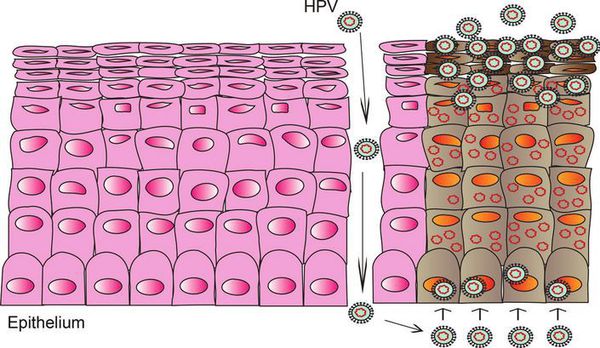
В случае ВПЧ высокого онкогенного риска определённые гены в вирусной ДНК кодируют синтез специфических белков-онкопротеинов (Е6 и Е7), которые подавляют противораковую защиту клеток. Под действием онкопротеинов нарушается стабильность генома клеток, стимулируется их размножение и снижается способность к дифференцировке — всё это со временем может привести к онкопатологии. [12]
Формирование новых полноценных вирусных частиц, способных инфицировать другого человека, происходит уже не в базальном, а в самых поверхностных слоях поражённого эпителия. Возбудитель может содержаться в слущивающихся отмирающих клетках, которые отделаются слизистой оболочкой. Таким образом они переходят к новому хозяину при тесном (сексуальном или бытовом) контакте.
Классификация и стадии развития папилломавирусной инфекции
По способности индуцировать развитие злокачественных новообразований ВПЧ подразделяют на четыре группы: [8]
- неонкогенные штаммы ВПЧ (типы 1-5);
- ВПЧ низкого онкогенного риска (типы 6, 11, 40, 42-44, 54, 61, 70, 72, 81);
- ВПЧ среднего онкогенного риска (типы 26, 31, 33, 35, 51-53, 58, 66);
- ВПЧ высокого онкогенного риска (типы 16, 18, 39, 45, 56, 59, 68, 73, 82).
Клинические формы папилломавирусной инфекции: [5]
- латентная — скрытая форма, не имеющая клинических и морфологических признаков, но обнаруживаемая иммунохимическими и молекулярно-биологическими методами;
- субклиническая — возникает у лиц с нормальным иммунитетом, определяется только специальными диагностическими методами (пробы с растворами-индикаторами, гистологические и цитологические исследования);
- манифестная — появляется у лиц с временным или стойким снижением иммунитета, в случае генитальной папилломавирусной инфекции характеризуется появлением кондилом.
Латентная инфекция может переходить в субклиническую и манифестную форму в случае возникновения предрасполагающих условий (факторов риска), но чаще всего она протекает бессимптомно, не манифестируя.
Клинические проявления папилломавирусной инфекции:
- кожные поражения: подошвенные, плоские и обычные (вульгарные) бородавки, бородавчатая эпидермодисплазия, бородавки Бютчера и небородавчатые поражения кожи;
- поражения слизистых оболочек гениталий: кондиломы, некондиломатозные поражения, карциномы;
- поражения слизистых вне гениталий: папилломатоз гортани, карциномы шеи, языка и другое.
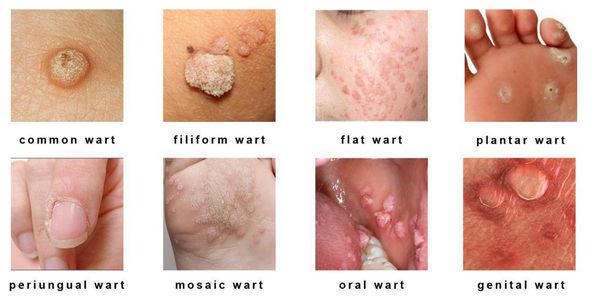
Разновидности поражений:
- экзофитные — видимые разрастания в виде папиллом и бородавок;
- эндофитные — образования, располагающиеся в толще ткани, которые не видны невооружённым глазом.
Осложнения папилломавирусной инфекции
Основными наиболее опасными осложнениями папилломавирусной инфекции являются злокачественные новообразования. Но возможны и другие серьёзные последствия:
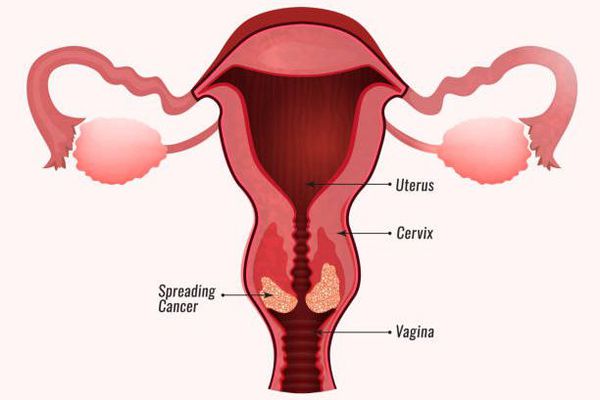
- Злокачественные новообразования заднего прохода, вульвы, полового члена и ротоглотки. Повышение риска их развития также связывают с высокоонкогенными штаммами ВПЧ. [6]
- Остроконечные кондиломы на гениталиях, папилломатоз верхних дыхательных путей (рецидивирующий респираторный папилломатоз, веррукозный ларингит). Причиной возникновения могут стать 6-й и 11-й типы вируса, несмотря на свой низкий онкогенный риск. В случае папилломатоза есть вероятность полной потери голоса, обструкции (перекрытия) гортани с развитием асфиксии. Это довольно редкое заболевание может возникать у детей, рождённых женщинами с папилломавирусной инфекцией. По разным данным, заражение может происходить как во время родов, так и внутриутробно. Как правило, респираторный папилломатоз начинает проявляться в детском и подростковом возрасте, он склонен к неоднократным рецидивам после удаления множественных папиллом, перекрывающих дыхательные пути.
- Гнойно-септические осложнения. Папилломатозные разрастания на слизистых оболочках очень ранимы, легко травмируются, и через участки мокнутия, расчёсов и потёртостей может проникать вторичная инфекция, которая в свою очередь и вызывает нагноение.
Диагностика папилломавирусной инфекции
Основные цели диагностических мероприятий: [3]
- ранняя диагностика папилломавирусной инфекции для динамического наблюдения и лечения;
- своевременное обнаружение и лечение предраковых изменений, что позволяет на 80% предотвратить развитие злокачественных новообразований;
- выявление онкологических новообразований на ранних стадиях, что в большинстве случаев даёт хороший прогноз эффективного излечения;
- решение вопроса о целесообразности вакцинации.
Для выявления папилломавирусной инфекции на сегодняшний день существует целый комплекс диагностических процедур:
- Гинекологический осмотр в зеркалах — позволяет увидеть папилломатозные разрастания (аногенитальные кондиломы) и другие изменения.
- Классический тест Папаниколау (мазки с поверхности шейки матки и стенок влагалища для цитологического исследования) — обнаруживает ранние признаки дисплазии и злокачественного перерождения.
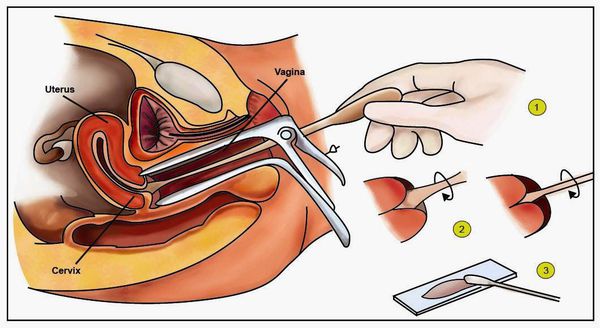
- Пробы с уксусной кислотой и раствором Люголя — выявляют участки поражения слизистой шейки матки.
- Кольпоскопия, в том числе с биопсией подозрительных участков и их гистологическим исследованием, — определяет характер имеющегося новообразования.
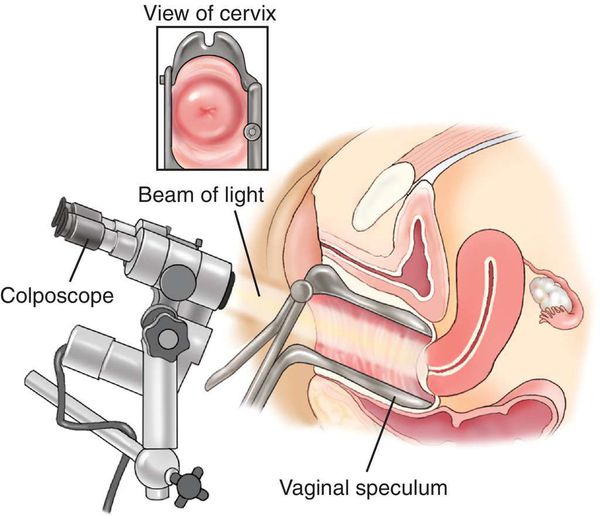
- Иммунофлюоресцентный анализ (ИФА) обнаруживает в цервикальном соскобе онкопротеины (Е7 и Е6). Этот метод достаточно новый, с его помощью можно различить носительство ВПЧ и первые признаки злокачественного перерождения в клетках, [12] оценить агрессивность данного процесса, сделать предположения относительно прогноза заболевания.
- Полимеразная цепная реакция (ПЦР) находит вирусную ДНК в биологическом материале (соскоб со слизистой), определяет тип ВПЧ, степень его онкогенности, а также количество вирусных частиц, что косвенно позволяет судить о характере течения папилломавирусной инфекции у данного пациента, возможности спонтанного излечения или высокого риска прогрессирования. Обнаружение ВПЧ с помощью этого возможно даже при латентном течении болезни, когда цитологические и гистологические методы не эффективны.
Целесообразно дополнительное обследование пациента на наличие других инфекций, передающихся половым путём, так как папилломавирус в 90% случаев с ними сочетается, и это может осложнять течение заболевания.
Лечение папилломавирусной инфекции
Лечение папилломавирусной инфекции должно быть комплексным и включать следующие составляющие: [3] [5]
- деструкцию (удаление) видимых проявлений (аногенитальных кондилом и др.);
- иммуномодулирующую терапию;
- противовирусную терапию;
- лечение сопутствующих инфекций, передающихся половым путём.
Деструктивные методы делятся на две основные группы:
- химические — с применением трихлоруксусной кислоты, а также таких препаратов, как "Солкодерм", "Колломак", "Ферезол" и др.;
- физические — хирургическое удаление, электрокоагуляция, криодеструкция, радиоволновая и плазменная коагуляция, лазеротерапия.
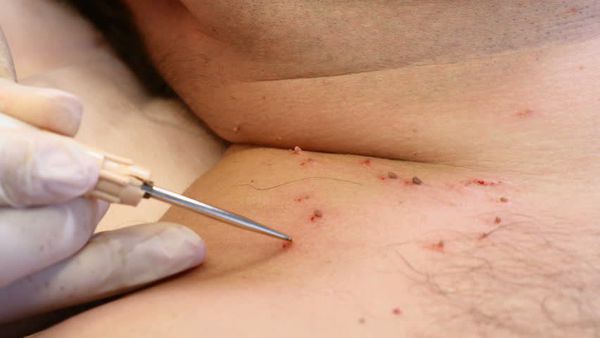
Лечение сопутствующих половых инфекций проводят до начала деструктивной терапии на фоне адекватной иммунокоррекции.
Удаление видимых проявлений папилломавирусной инфекции должно сочетаться с противовирусной терапией — как с общей, так и с применением препаратов местного действия после удаления кондилом.
Следует помнить, что успешно проведённое лечение не исключает развитие рецидивов в дальнейшем, особенно у пациентов с нарушениями иммунитета. Поэтому за ними устанавливается динамическое наблюдение в течение как минимум 1-2 лет.
Прогноз. Профилактика
В 90% случаев здоровая иммунная система человека справляется с папилломавирусной инфекцией самостоятельно за период от полугода до двух лет с момента инфицирования, после чего происходит полное выздоровление с исчезновением вируса из организма. При этом не формируется напряжённого пожизненного иммунитета, то есть человек может заразиться повторно.
В других случаях, при наличии предрасполагающих факторов, заболевание приобретает хроническую форму, склонную к длительному скрытому течению с периодическими рецидивами и возможным развитием тяжёлых осложнений.
От момента попадания вируса в организм до развития предраковых состояний и тем более возникновения рака может пройти достаточно много времени, иногда десятки лет. Поэтому регулярные профилактические обследования, своевременное выявление и лечение предраковых состояний — вполне реальный и эффективный способ избежать самого неблагоприятного варианта развития событий. [13] С этой целью Всемирная организация здравоохранения рекомендует всем женщинам старше 30 лет при первичном скрининге проходить не только “рутинное” цитологическое исследование, но и делать тест на наличие ВПЧ. [10]
Регулярное посещение гинеколога (при отсутствии каких-либо жалоб — раз в год) с проведением теста Папаниколау позволяет своевременно обнаружить начальные признаки дисплазии и предпринять все необходимые меры для предотвращения прогрессирования процесса и его перехода в онкологическое заболевание.
Использование методов барьерной контрацепции хоть и не полностью защищает от инфицирования, но несколько снижает его вероятность.
Главным методом первичной профилактики папилломавирусной инфекции считается вакцинация. [11] Современные вакцины разработаны с целью защиты от наиболее опасных, высокоонкогенных штаммов ВПЧ, ответственных за 70-80% случаев развития рака шейки матки. Стандартный курс, состоящий из трёх прививок, даёт вполне надёжную защиту.
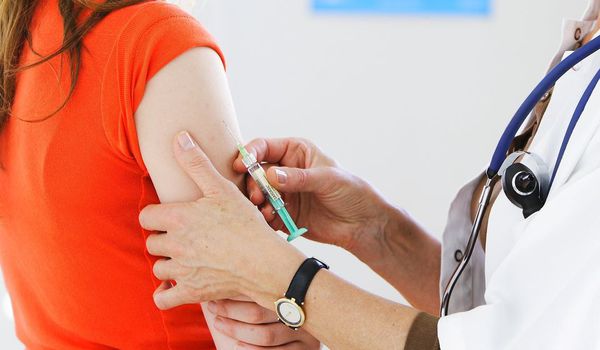
Первый стол регулярно отпускает местные противовирусные и иммуномодулирующие препараты, показанные для лечения герпетической и/или папилломавирусной инфекции (ВПЧ). Обе инфекции принадлежат к числу самых распространенных в мире патологий, передающихся половым путем. Как качественно и деликатно консультировать клиентов с этими болезнями, какие советовать противовирусные лекарственные средства при ВПЧ, какие от герпеса и на что обращать внимание — читайте в нашей статье.
ВПГ и ВПЧ: сходства и отличия
Прежде всего, важно понимать, что вирус простого герпеса (ВПГ) и вирус папилломы человека (ВПЧ), провоцирующие герпетическую и папилломавирусную инфекции соответственно, кардинально отличаются друг от друга.
«Галавит» при герпесвирусной инфекции способствует:
- Выраженной элиминации вирусов из организма
- Повышению эффективности противовирусной терапии
- Сокращению периода высыпаний и ускорению процессов регенерации
- Увеличению продолжительности ремиссии
У взрослых и подростков старше 12 лет в комплексной терапии:
Суппозитории — 5 дней по 1 суппозиторию, затем по одному через день. Курс — 2 упаковки суппозиториев.

Таблетки подъязычные — 10 дней по 1 таблетке 4 раза в день. Затем продолжить прием через сутки в течение 10 дней по 4 таблетки в день.

ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ. НЕОБХОДИМО ПРОКОНСУЛЬТИРОВАТЬСЯ СО СПЕЦИАЛИСТОМ.
Генитальный герпес ассоциирован с заражением ВПГ 1‑го или 2‑го типа. По статистике, заболеванием страдают около 12 % популяции [1]. Однажды проникнув в организм, вирус «поселяется» в нем навсегда — на сегодняшний день не существует метода лечения от вируса герпеса, которое позволило бы окончательно избавиться от возбудителя. Симптомы генитального герпеса, которые возникают периодически, во время рецидивов, значительно снижают качество жизни. Интересно, что частота новых эпизодов заболевания зависит от типа вируса: при инфицировании ВПГ-1 фиксируют примерно 1 рецидив в год, в то время как при заражении ВПГ-2 их число может достигать 6 и более [2].
Несмотря на то, что специфического лечения ВПГ не существует, ряд препаратов может облегчить состояние при обострениях. Согласно отечественным и западным рекомендациям, с этой целью применяют пероральные противовирусные средства от герпеса на основе ацикловира и валацикловира. Однако в России также рекомендована местная терапия, не включенная в западные стандарты. За границей такие методы в рекомендациях отсутствуют ввиду их меньшей активности по сравнению с таблетками [3].
Несколько по‑другому обстоит ситуация с папилломавирусной инфекцией (ВПЧ). Она считается самым распространенным в мире заболеванием, передаваемым половым путем [4]. В какой‑то момент жизни ВПЧ заражается большинство взрослых людей, однако в 90 % случаев в течение двух лет после заражения происходит естественная элиминация вируса. В противном случае инфицированный становится пожизненным носителем.
К сожалению, лекарства от вируса папилломы человека не существует, так же как и в случае с вирусом простого герпеса. Однако первый, в отличие от второго, может быть смертельно опасен: ВПЧ 16‑го и 18‑го типов ассоциированы со злокачественными новообразованиями — в частности, с раком шейки матки и некоторыми другими опухолями. Единственное эффективное на сегодня медикаментозное лечение папилломавирусной инфекции заключается в эрадикации кондилом, которые являются проявлениями клинической и субклинической форм инфекции. С этой целью при лечении вируса папилломы человека применяют ряд местных противовирусных препаратов, доказавших активность в исследованиях. В то же время в отечественной практике врачи назначают и ЛС, имеющие сомнительную доказательную базу. Рассмотрим их преимущества и недостатки более детально.
Локальные иммуномодуляторы при ВПЧ и ВПГ
К числу «универсальных» средств, которые могут назначаться при различных вирусных инфекциях — от банальных респираторных до герпетической и папилломавирусной, — относятся интерфероны. В частности — препараты интерферона альфа-2b человеческого рекомбинантного.
+ Высокий профиль безопасности.
! Целесообразность применения местных форм ацикловира при генитальном герпесе подвергается серьезным сомнениям ввиду недостаточной активности, что подтверждено в западных рекомендациях [3].Препараты интерферона альфа-2b, как моно-, так и комбинированные, отпускаются как по рецепту, так и без — в зависимости от указания на правила отпуска в инструкции конкретного препарата. Важно обратить внимание посетителя на то, что препараты от ВПЧ первой линии лечения — пероральные формы ацикловира и валацикловира — должен выписать врач, поэтому нужно посоветовать незамедлительно обратиться за консультацией к доктору.
Синтетические противовирусные местные препараты
Эту группу ЛС можно условно разделить на средства, применяемые при генитальной герпетической инфекции, и противовирусные препараты, назначаемые для лечения папиллом и кондилом, связанных с папилломавирусной инфекцией.
Местные препараты при генитальном герпесе
Тромантадин
Противовирусный препарат от герпеса, производное адамантана (подобно известным противовирусным римантадину и амантадину). Ингибирует прикрепление вируса к поверхности клеточной мембраны, препятствуя проникновению возбудителя внутрь клетки. Предотвращает слияние клеток и затрудняет распространение вируса за счет изменения синтеза гликопротеинов [5]. Выпускается в форме геля для наружного применения, который можно наносить на слизистые оболочки при обострении ВПГ-инфекции [5].
Отпуск: без рецепта.
! Есть данные о развитии контактной аллергической реакции при использовании препарата [7].
Иммуномодулятор, способный регулировать активность клеток врожденного и приобретенного иммунитета, в том числе макрофаги, нейтрофилы и натуральные киллеры. При этом этот противовирусный препарат против герпеса повышает устойчивость организма к бактериальным, вирусным и грибковым инфекциям, сокращая их частоту, выраженность и длительность (5). Кроме того, препарат нормализует образование антител и регулирует выработку интерферонов, а также блокирует избыточный синтез провоспалительных цитокинов и снижает уровень оксидантного стресса (5).
Отпуск: Без рецепта
+ Высокий профиль безопасности (5).
Азоксимера бромид
Российский препарат, предположительно, проявляющий иммуностимулирующий эффект. По данным инструкции [5], напрямую влияет на фагоциты и естественные киллеры, стимулирует образование антител и синтез интерферона, проявляет антиоксидантные и детоксикационные свойства. В отечественной практике применяется при широком спектре заболеваний — от гриппа до злокачественных новообразований.
Вагинальные суппозитории азоксимера бромида применяются для профилактики рецидивов генитального герпеса.
Отпуск: без рецепта.
! Суппозитории азоксимера бромида не показаны для лечения активной формы герпеса!
Местные противовирусные препараты для лечения ВПЧ (папилломавируса)
Некоторые топические противовирусные препараты, активные в отношении папилломавирусов, в отличие от ряда препаратов, помогающих от вируса герпеса, имеют прочную доказательную базу и применяются во всем мире для лечения проявлений ВПЧ — в частности, кондилом.
Имихимод
Модификатор иммунного ответа, не оказывающий противовирусного действия. Активность проявляет за счет способности индуцировать выработку интерферона-альфа и других цитокинов. Показан для лечения остроконечных кондилом в урогенитальной зоне [5].
Отпуск: по рецепту.
+ Прочная доказательная база. Препарат определенно снижает вирусную нагрузку. Доказано, что применение крема имихимода 5 %-ного 3 раза в неделю на ночь на протяжении 16 недель эффективно и безопасно для лечения кондилом. Частота рецидивов оценивается как низкая [8]. Имихимод рекомендован для лечения генитальных кондилом авторитетным американским регулятором FDA [8].
! При нанесении имихимода более чем в 10 % случаев наблюдаются зуд и боль [5], о чем следует предупредить покупателя.
Местные противовирусные средства растительного происхождения
Аммония глицирризинат
Активный компонент препарата — активированную глицирризиновую кислоту — получают из корня солодки. Оказывает комплексное иммуностимулирующее, противовирусное, противовоспалительное, противозудное действие. Глицирризиновая кислота прерывает репликацию ряда ДНК и РНК вирусов, в том числе вируса простого герпеса, папилломы человека, цитомегаловируса [5].
Показана в качестве препарата для лечения папилломавирусной инфекции и вируса простого герпеса, в том числе и при инфицировании вирусами онкогенного типа. Выпускается в форме спрея, который распыляют на слизистые оболочки и пораженные участки кожи.
Отпуск: без рецепта.
+ Имеет широкий спектр показаний, среди которых профилактика и лечение кандидозного вульвовагинита, дискомфорт в области половых органов. Может применяться при беременности и кормлении грудью; хорошо переносится.
Подофиллотоксин
Активный компонент подофиллина, производного растительных экстрактов, выделяемых из корневищ с корнями подофилла щитовидного — растения семейства барбарисовых. Обладает выраженными противоопухолевыми и противовирусными свойствами, оказывает цитотоксическое действие. При наружном применении прижигает и мумифицирует кондиломы. Применяется в качестве препарата для местного лечения от вируса папилломы человека. Выпускается в форме раствора для обработки остроконечных кондилом [8].
Отпуск: по рецепту.
+ Доказанный эффект. По данным исследований, 0,5 %-ный раствор подофиллотоксина уменьшает число аногенитальных бородавок с 6,3 до 1,1, разрушая около 70 % образований [8].
! Необходимо соблюдать осторожность при применении — попадание на здоровую кожу может приводить к изъязвлению. Местные реакции при применении, аллергические реакции. Первостольник, отпуская этот противовирусный препарат от папиллом и кондилом, должен обратить внимание клиента на эту особенность и напомнить, что ЛС следует хранить в недоступном для детей месте.
Тетрагидроксиглюкопиранозилксантен
Российский препарат. Активный компонент выделяют из растения копеечника альпийского или копеечника желтеющего.
Согласно инструкции, обладает противовирусной активностью в отношении ВПГ-1 и ВПГ-2, а также цитомегаловируса и некоторых других ДНК-содержащих вирусов. Кроме того, предположительно, препарат активирует клеточный и гуморальный иммунитет, ингибирует рост ряда бактерий и патогенных простейших, в том числе трихомонад, а также оказывает умеренное противовоспалительное действие. Применяют в форме мази в составе комбинированного лечения острых и рецидивирующих форм герпеса, в том числе генитального [5].
Отпуск: без рецепта.
+ Благоприятный профиль безопасности, возможность применять в составе комплексного лечения.
Полисахариды побегов Solanum tuberosum
Рецептурный российский препарат, активный компонент получают из побегов паслена клубненосного. По данным инструкции, проявляет противовирусный эффект в отношении ВПГ-1 и ВПГ-2, способствует индукции интерферонов и повышает иммунный ответ [5]. Следует заметить, что фармакокинетические свойства препарата не изучались. Вагинальные суппозитории применяются в комплексной терапии генитального герпеса.
Отпуск: без рецепта.
+ Высокий профиль безопасности. Побочные эффекты проявляются редко.
Десмодиума канадского травы экстракт
Противовирусный препарат от герпеса растительного происхождения, созданный из сухого экстракта травы десмодиума канадского. По данным инструкции, проявляет противовирусную активность в отношении вирусов герпеса, стимулирует выработку интерферона [5]. Мазь показана для применения при острых и рецидивирующих формах герпеса, в том числе урогенитального.
Отпуск: без рецепта.
+ Высокий профиль безопасности — побочные эффекты не выявлены.
Гипорамина экстракт
Российская разработка на основе экстракта листьев облепихи. По данным инструкции, активен в отношении вирусов простого герпеса, цитомегаловирусов и некоторых других [5]. Мазь, содержащая экстракт гипорамин, показана для лечения и профилактики эпизодов герпеса, в том числе и генитального.
Отпуск: без рецепта.
+ Высокий профиль безопасности; возможность использовать во время беременности и лактации (после консультации с врачом).
Мелиссы лекарственной листьев экстракт
По данным инструкции, проявляет противовирусную активность в отношении ВПГ, оказывает противовоспалительное действие [5]. Крем, содержащий экстракт листьев мелиссы, применяют при поражениях слизистых и кожи, в том числе и в урогенитальной зоне.
Отпуск: без рецепта.
+ Высокий профиль безопасности.
В заключение хочется еще раз подчеркнуть: широкий ассортимент позволяет первостольникам предлагать разные ЛС при запросах на местные средства для лечения проявлений ВПГ или лекарства от ВПЧ. Но при этом не следует забывать о необходимости рекомендовать посетителю обратиться к врачу, ведь именно доктор должен назначить препараты первой линии и подобрать при необходимости комплексную схему лечения папилломавирусной инфекции.
Проблема лечения генитальных вирусных инфекций стоит в настоящее время наиболее остро. Исходя из биологии вирусов, эти инфекции наиболее трудно поддаются эпидемиологическому контролю и лечению. Среди вирусных инфекций, поражающих аногенитальную область,
Проблема лечения генитальных вирусных инфекций стоит в настоящее время наиболее остро. Исходя из биологии вирусов, эти инфекции наиболее трудно поддаются эпидемиологическому контролю и лечению. Среди вирусных инфекций, поражающих аногенитальную область, наиболее распространены герпетическая и папилломавирусная инфекция. Целью данной статьи является обзор современных консервативных методов лечения больных с аногенитальными поражениями, вызванными вирусом папилломы человека (ВПЧ-поражений).
К ВПЧ-поражениям относят (по J. Handley [1]): клинические формы — аногентальные бородавки (остроконечные кондиломы, вульгарные бородавки), симптоматические внутриэпителиальные неоплазии на ранних стадиях при отсутствии дисплазии (плоские кондиломы); субклинические формы — бессимптомные внутриэпителиальные неоплазии при отсутствии дисплазии; латентные формы (отсутствие морфологических или гистологических изменений при обнаружении ДНК ВПЧ).
Принципиально лечение аногенитальных ВПЧ-поражений направлено либо на разрушение папилломатозных очагов тем или иным методом, либо на стимуляцию противовирусного иммунного ответа, либо на сочетание этих подходов. Оптимальной представляется следующая классификация методов лечения аногенитальных бородавок.
I. Деструктивные методы
II. Цитотоксические препараты:
- подофиллин (ПФ);
- подофиллотоксин (ПФТ);
- 5-фторурацил.
III. Иммунологические методы:
IV. Комбинированные методы:
При выборе оптимальной лечебной тактики врач все чаще вынужден учитывать мнение представителей страховой медицины как в обязательном, так и в добровольном ее вариантах, поскольку оплата за диагностику и лечение зависит от тех стандартов, которые принимаются во внимание страховыми компаниями.
В связи с этим особую роль приобретают справочные руководства, в которых представлена официальная тактика лечения, одобренная Министерством здравоохранения. Сегодня одним из самых авторитетных справочных изданий такого типа является «Федеральное руководство по использованию лекарственных средств» (ФР), последнее, 4-е издание которого датируется 2003 г. К сожалению, этот справочник пока не содержит раздела, посвященного терапии папилломавирусной инфекции. Такая информация, по-видимому, будет присутствовать в российских стандартах по лечению ИППП, но они пока не изданы. Единственными руководствами для практикующих врачей, работающих в этой области, могут являться различные методические материалы, выпускаемые авторитетными учреждениями и организациями. К таким пособиям можно отнести «Методические материалы по диагностике и лечению наиболее распространенных инфекций, передаваемых половым путем (ИППП), и заболеваний кожи», изданные ГУ ЦНИКВИ в 2001 г. и «Методические материалы по диагностике и лечению наиболее распространенных инфекций, передаваемых половым путем (ИППП), и ассоциированных с ними заболеваний» Российской ассоциации акушеров и гинекологов, утвержденные в 2000 г. В этих руководствах для лечения ВПЧ-поражений рекомендуются физические и химические деструктивные методы, использование подофиллотоксина, а также комбинированные методы, основанные на сочетании деструкции поражений с системной и местной иммунотерапией.
Кроме упомянутых руководств при выборе наиболее оптимального метода в каждом конкретном случае врачу необходимо руководствоваться четырьмя основными характеристиками:
- эффективностью при данной патологии;
- частотой рецидивов после лечения;
- переносимостью (минимум побочных эффектов);
- простотой выполнения процедур.
Физические деструктивные методы
Основным отличием этих методов от остальных является то, что при их применении происходит быстрое, как правило, одномоментное разрушение поражений. При использовании других методов очаг поражения подвергается воздействию, и необходимо время — от нескольких часов до нескольких недель, — чтобы поражения ликвидировались. Как правило, этот период сопоставим со временем заживления очагов после воздействия физических методов. Частота рецидивов, по данным литературы, не зависит от выбора метода лечения. Таким образом, очевидные, казалось бы, преимущества физических методов нивелируются. Для применения физических деструктивных методов необходимы специальные помещения, дорогостоящее оборудование, обученный персонал, имеющий сертификаты на данный вид медицинской деятельности. Все это ограничивает использование данных видов лечения в широкой практике, особенно в условиях небольших медицинских центров или в районах, где имеются лишь дерматовенерологический, гинекологический или урологический кабинет в поликлинике. Поэтому особый интерес представляют консервативные методы лечения, доступные для применения любому практикующему врачу.
Химические деструктивные методы
Применяются концентрированные растворы кислот, щелочей, солей и др. Среди таких препаратов можно упомянуть ферезол, перекись водорода, растворы акрихина и хингамина, препараты на основе салициловой и молочной кислот, уксусную и азотную кислоту, соки туи и чистотела. Все эти лекарственные средства обладают невысокой, плохо прогнозируемой эффективностью, многочисленными побочными эффектами. Упорядоченных данных относительно действенности этих препаратов немного. Среди применяемых в нашей стране и за рубежом химических препаратов, обладающих деструктивным действием, о которых достаточно данных в литературе, можно выделить трихлоруксусную (ТХУ) кислоту и азотную кислоту, а также комбинированный кислотный препарат — солкодерм.
Трихлоруксусная и азотная кислоты
ТХУ кислота применяется в концентрации 80—90% и вызывает образование локального коагуляционного некроза. Таким же действием обладает раствор азотной кислоты. Из-за своей дешевизны и доступности метод применяется довольно широко. Кислоты эффективны для лечения кондилом вульвы, крайней плоти, венечной борозды и головки полового члена, особенно в случаях, когда противопоказано применение цитотоксических методов и лазера (например, во время беременности). Препараты обычно не рекомендуются для лечения вагинальных и уретральных бородавок. Прижигания проводят один раз в неделю в течение пяти-шести недель. Эффективность ТХУ и азотной кислот составляет примерно 70–80%. У 1/3 больных может развиваться местная реакция в виде мокнутия и изъязвлений.
Солкодерм
Солкодерм — это водный раствор, в качестве активной составляющей которого выступают продукты взаимодействия органических кислот (уксусной, щавелевой и молочной) и ионов металлов с азотной кислотой.
Представленные ниже свой-ства и механизм действия солкодерма выделяют его среди других деструктивных методов: при местном применении солкодерм вызывает немедленную прижизненную фиксацию ткани, на которую он наносится; действие препарата строго ограничивается местом применения; признаком немедленного эффекта является изменение окраски обрабатываемого участка; девитализированная ткань высыхает и темнеет (мумифицируется); «мумифицированный» струп отторгается самостоятельно; процесс заживления непродолжителен, а осложнения (вторичная инфекция или рубцевание) редки. Лечение практически безболезненно и проводится амбулаторно, так как не требует специальной аппаратуры.
Солкодерм высокоэффективен для лечения остроконечных кондилом любой локализации, в большинстве случаев достаточно однократного применения.
Цитотоксические препараты
Подофиллин
Подофиллотоксин
Для ПФТ показатель эффективности составляет 26—87% у мужчин и 50—77% у женщин. Столь большой разброс в показателе эффективности связан с различным сроком наблюдения за больными, а также с тем, что в некоторых работах авторы не учитывают рецидивы. По данным Hendley, полное исчезновение бородавок наблюдается только в 30—40% случаев, по данным Bonnez — только у 29% больных, по данным Wang — у 86,5%, по данным Kinghorn et al. — у 86% мужчин и 72% женщин. По данным Syed, рецидивы наблюдаются в 5,5% случаев при применении раствора 0,3% и крема и в 51% — при использовании кремов 0,3% или 0,5%, по данным von Krogh, при использовании раствора 0,5% — в 38% случаев, по данным Wang — у 17% больных, по данным Hellberg — у 23% (при использовании крема 0,5%).
Наиболее частыми побочными эффектами ПФТ являются местные воспалительные реакции (у 57% пациентов), эритема, жжение (у 48%), болезненность (у 47%), зуд (у 44%), незначительное мокнутие и эрозии в области аппликации (у 39%). Хотя и не было описано системных побочных эффектов, рекомендуется ограничивать применение ПФТ в количестве 0,2 мл за одну процедуру.
Handley считает ПФТ препаратом выбора для самостоятельного применения больными с небольшим количеством неороговевающих кондилом, располагающихся на крайней плоти, головке полового члена, в венечной борозде и вульве. Препарат малоэффективен при лечении бородавок перианальной области, влагалища и уретры.
Недостатками ПФТ являются его высокая стоимость, большая длительность лечения при не самой высокой эффективности.
5-фторурацил
5-фторурацил (5-ФУ) является антагонистом пиримидина и способен нарушать синтез как клеточной, так и вирусной ДНК. Для лечения бородавок аногенитальной области его назначают в виде крема 5%. По мнению Handley, 5-ФУ — это эффективный метод лечения интравагинальных бородавок и кондилом терминальной части уретры. При лечении интравагинальных бородавок препарат назначается один раз на ночь в течение недели или один раз в неделю в течение 10 недель. Хотя препарат при такой схеме лечения обладает достаточно высокой эффективностью (85—90%), при его применении могут возникать мокнущие эрозии на слизистой влагалища, вплоть до развития тяжелого мокнущего контактного дерматита.
При лечении бородавок терминальной части уретры крем вводится сразу после мочеиспускания, на ночь, в течение трех—восьми дней. Полное излечение внутриуретральных бородавок наблюдается у 90—95% мужчин. Однако так же, как в случае с женщинами, при лечении мужчин наблюдается множество побочных эффектов: стеноз и стриктуры уретры, дизурия, изъязвления.
Несмотря на достаточно высокую эффективность 5-ФУ, доступность и дешевизну, его применение ограничено в широкой практике из-за высокой частоты побочных эффектов. Препарат противопоказан при беременности.
Одним из основных показателей эффективности любого метода является отсутствие рецидивов. Так как частота рецидивов ВПЧ-инфекции не зависит от метода деструкции поражений (физическая, химическая или цитотоксическая), то представляет интерес еще одна группа консервативных методов — это терапия иммунными препаратами, которые могут применяться самостоятельно или в комбинации с деструктивными методами.
Иммунологические методы
Интерфероны (ИФ)
Так как ВПЧ сохраняется в эпителиальных клетках и использование деструктивных методов не гарантирует от рецидивов, перспективным в этом плане является применение интерферонов как в качестве монотерапии, так и в комплексе с другими методами лечения.
ИФ представляют собой эндогенные цитокины, обладающие противовирусным, антипролиферативным и иммуномодулирующим действием. Существует три основных класса интерферонов: α-ИФ (лейкоцитарный), β-ИФ (фибробластный) и γ-ИФ (Т-лимфоцитарный). ИФ можно применять местно, внутриочагово и системно (подкожно, внутримышечно или внутривенно). Установлено, что при применении ИФ у пациентов в очагах поражения снижается количество вирусной ДНК (по данным ПЦР), что коррелирует с клиническим улучшением или исчезновением поражений.
В большинстве исследований была показана невысокая эффективность наружного применения ИФ. Некоторые авторы считают, что важным показанием для наружного применения ИФ является наличие субклинических очагов ВПЧ-инфекции и цервикальных внутриэпителиальных неоплазий (ЦВН), особенно вызванных типами ВПЧ высокого онкогенного риска.
По данным различных авторов, при системном применении α-ИФ в дозе от 1,5 до 3 млн МЕ внутримышечно или подкожно через день в течение четырех недель полное исчезновение бородавок наблюдается у 11—100% пациентов.
Из побочных эффектов при системном применении ИФ обычно наблюдаются гриппоподобные явления, выраженность которых зависит от полученной дозы. Эти побочные воздействия можно ослабить приемом нестероидных противовоспалительных препаратов.
Учитывая, что эффективность системной монотерапии ИФ все-таки недостаточно предсказуема и не очень высока, а также принимая во внимание высокую стоимость такого лечения, этот метод не получил широкого распространения в клинической практике.
На российском рынке сегодня представлен широкий выбор интерферонов различных производителей, как отечественных, так и зарубежных, — виферон, кипферон, реаферон, роферон-А, интрон А, реальдирон и т. д. Предпочтительнее сегодня использовать рекомбинантные, а не человеческие интерфероны.
Комбинированные методы
Более предпочтительным является применение ИФ или его индукторов, а также других активаторов противовирусного иммунитета, в качестве адъювантной терапии в комбинации с различными деструктивными методами. Иммунные препараты повышают эффективность лечения и позволяют снизить частоту рецидивов. Определенное значение комбинированная иммунотерапия имеет при лечении упорных, плохо поддающихся лечению бородавок. Для лечения предложены различные методики, основанные на применении иммунных препаратов в сочетании с криотерапией, лазеротерапией, электрокоагуляцией, солкодермом и т. д.
Так, например, выявлено, что сочетание ИФ с лазеротерапией более эффективно, чем только лазеротерапия: полное исчезновение бородавок наблюдается у 52–81,5% и 19–61% пациентов соответственно. СО2-лазерное иссечение в сочетании с терапией низкими дозами α-ИФ (по 1—3 млн МЕ в сутки в течение пяти—семи дней, затем перерыв три-четыре недели, таких три-четыре цикла) повышает эффективность лечения и позволяет снизить процент рецидивов, наблюдающихся после применения только лазеротерапии. При небольших остроконечных кондиломах дополнение лазерной терапии или электрокоагуляции местным применением геля, содержащего β-ИФ 0,1 млн МЕ/г пять раз в день в течение четырех недель эффективно предотвращает рецидивы.
Однако, по данным The Condylomata International Collaborative Study Group, применение α-ИФ (три раза в неделю в течение четырех недель) после удаления всех видимых кондилом СО2-лазером не дает каких-либо положительных результатов в сравнении с плацебо (полное излечение у 18%, рецидивы у 35% больных). Согласно M. R. Hopel соавт., сочетание α-ИФ (3—6 пятидневных курсов с интервалом в две недели) с деструктивными и/или хирургическими методами, несмотря на повышение эффективности лечения упорных, не поддающихся терапии кондилом, не предотвращает развитие рецидивов (они возникают у 50% больных).
При лечении кондилом заднего прохода предлагается сначала хирургическое удаление крупных образований, затем прижигание очагов эл/током и одна инъекция α-ИФ в дозе 500 тыс. МЕ в прямую кишку. Применение ИФ таким способом позволяет сократить число рецидивов (12% при применении ИФ, 39% — без ИФ).
Повысить эффективность лечения, воздействуя на противовирусный иммунитет, можно благодаря применению индукторов эндогенного интерферона и других активаторов иммунитета. На российском аптечном рынке представлено множество индукторов интерферона, в основном отечественных производителей; наиболее известные из них — гепон, ридостин, циклоферон, неовир — при системном и/или местном применении позволяют повысить эффективность лечения, воздействуя на частоту рецидивов. Так, например, аппликации гепона на очаги ВПЧ-поражений после их удаления каким-либо деструктивным методом (от трех до шести аппликаций через день) позволяют ускорить процесс заживления и снижают уровень рецидивирования.
Комбинированные методы терапии, основанные на сочетании деструкции видимых поражений с назначением активаторов противовирусного иммунитета (интерферонов, их индукторов, иммуномакса), наиболее соответствуют критериям выбора оптимального способа лечения — высокая эффективность и низкая частота рецидивов.
Таким образом, существует множество различных консервативных методов удаления аногенитальных бородавок. Эффективность методов, по данным разных авторов, варьирует от 50% до 94%. Ни один из способов лечения не может быть признан панацеей, так как частота рецидивов, являющаяся очень важным показателем любого метода, достаточно высока при любом способе лечения. Врач выбирает терапию в зависимости от сопутствующих обстоятельств, включая пожелания самого больного. Лечение должно быть индивидуальным: в каждом конкретном случае необходимо подбирать наиболее оптимальный метод. Проблема рецидивов не зависит от выбора терапии. Уровень рецидивирования составляет в среднем 25—30% в течение трех месяцев после лечения. Рецидивы аногенитальных бородавок чаще всего связаны с реактивацией инфекции, а не с реинфекцией от полового партнера. При отсутствии терапии существуют три варианта развития событий: бородавки могут разрешаться самостоятельно, оставаться без изменений или прогрессировать. При этом всегда нужно принимать во внимание возможность персистенции вируса при отсутствии каких-либо клинических проявлений.
При лечении аногенитальных бородавок кроме удаления самих очагов следует решать следующие важные задачи:
Читайте также:


