Какие кортикостероиды при дерматите
Обновлено: 23.04.2024
Местные кортикостероиды для лечения болезней кожи
Топические кортикостероидные препараты (КСП) выпускаются во всех лекарственных формах. Они отличаются не только формой, но и силой действия, в зависимости от нее они подразделяются на 8 классов. Врачу полезно знать один или два наименования для каждого класса. Желательно осведомиться о наличии и стоимости этих препаратов в местных аптеках.
На лице и в интертригинозных зонах в большинстве случаев следует применять препараты слабой силы действия, поскольку более сильные препараты могут вызвать атрофию, телеангиэктазии и гипопигментацию. Независимо от силы действия препарата, необходимо внимательно следить за появлением вызванных кортикостероидами изменений.
Они встречаются редко, если терапия ограничена 2-4 нед. Пациенты, получающие длительную терапию на чувствительных участках, должны часто делать перерывы в лечении (например, 1 нед. каждый месяц) и постепенно сокращать количество аппликаций препаратов по мере возможности.
Можно, помимо уменьшения частоты аппликаций, снижать дозу, смешивая препарат с нейтральным эмолентом, например, вазелином. Кортикостероидные препараты (КСП) могут замаскировать инфекцию и подавить местный и системный иммунные ответы. Следовательно, они противопоказаны большинству пациентов с вирусными, грибковыми, бактериальными или микобактериальными инфекциями.

Топические кортикостероидные препараты (КСП)
| Класс/сила действия и действующее вещество | Торговое название |
| Сверхсильные -класс I Бетаметазона дипропионат 0,05% | Diprolene мазь 0,05% |
| Клобетазола пропионат 0,05% | Clobex лосьон, спрей, шампунь 0,05% Cormax крем, раствор 0,05% Dermovate 0,05% Embeline Е 0,05% Olux Е пенка 0,05%, Olux пенка 0,05% Temovate крем, мазь, раствор 0,05% |
| Дифлоразона диацетат 0,05% | ApexiCon Е крем 0,05% Nerisone forte 0,3% (UK) |
| Флуоцинонид 0,1% | Vanos крем 0,01% |
| Халобетазола пропионат 0,05% | Ultravate крем, мазь 0,05% |
| Очень сильные - класс II Амцинонид 0,1% | Cyclocort мазь 0,1% |
| Дезоксиметазон 0,25%, 0,05% | Topicort крем, мазь 0,25%, гель 0,05% |
| Дифлоразона диацетат 0,05% | Apexi Е крем 0,05% Florone крем 0,05% Maxiflor мазь 0,05% Psorcon крем 0,05%, мазь 0,05% |
| Халцинонид 0,1% | Halog, Halog Е мазь, крем 0,1% |
| Флуоцинонид 0,05% | Lidex крем, мазь 0,05% Metosyn крем, мазь 0,05% |
| Мометазона фуроат 0,1% | Elocon мазь 0,01% |
| Средней силы класс III Амцинонид 0,1% | Cyclocort крем, лосьон 0,01% |
| Бетаметазона дипропионат 0,05% | Diprosone крем 0,05% |
| Бетаметазона валерат 0,1% | Valisone мазь 0,1% Betacap 0,1%(UK) |
| Клобетазона бутират 0,05% | Eumovate мазь, крем 0,05% (UK) |
| Флуоцинонид 0,05% | Lidex мазь, крем, гель 0,05% |
| Флуоцинонид 0,05% | Cutivate мазь 0,05% |
| Средней силы -класс IV Бетаметазона валерат 0,12% | Luxiq пенка 0,12% |
| Клокортолона пивалат 0,1% | Cloderm крем 0,1% |
| Дезоксиметазон 0,05% | Topicort LP крем 0,05% |
| Флуоцинолона ацетонид 0,025% | Synalar мазь 0,025% |
| Флурандренолид 0,05% | Cordran мазь, лосьон, лента 0,05% |
| Гидрокортизона пробутат 0,1% | Pandel крем 0,1% |
| Гидрокортизона валерат 0,2% | Westcort мазь 0,2% |
| Мометазона фуроат 0,1% | Elocon крем, лосьон 0,1% |
| Предникарбат 0,1% | Dermatop мазь 0,1% |
| Триамцинолона ацетонид 0,1%, 0,025% | Kenalog мазь 0,1%, 0,025% |
| Средней силы -класс V Бетаметазона дипропионат 0,05% | Diprosone лосьон 0,05% |
| Бетаметазона валерат 0,1% | Valisone крем, лосьон 0,1% |
| Флуоцинолона ацетонид 0,025% | Synalar 0,025%, крем 0,01% |
| Флурандренолид 0,05% | Cordran крем, лосьон 0,05% |
| Флутиказона пропионат 0,05% | Cutivate крем, лосьон 0,05% |
| Гидрокортизона бутират 0,1% | Locoid липокрем, мазь, лосьон, раствор 0,1% |
| Гидрокортизона валерат 0,2% | Westcort крем 0,2% |
| Предникарбат 0,1% | Dermatop мазь, крем 0,1% |
| Триамцинолона ацетонид 0,1% | Kenalog крем, лосьон 0,1% |
| Средней силы - класс VI Алклометазона дипропионат 0,05% | Aclovate мазь, крем 0,05% Modrasone мазь, крем 0,05% |
| Дезонид 0,05% | DesOwen мазь, крем, лосьон 0,05% Desonate гель 0,05% Tridesilon крем 0,05% |
| Флуоцинолона ацетонид 0,01% | Synalar крем, раствор 0,1% Derma-Smoothe/FS масло |
| Слабые - класс VII Гидрокортизон 2,5% | Hytone крем, лосьон 2,5% Cobadex 1% Dioderm0,1% Mildison 1% Hydrocortisyl 1% Hytone мазь 1% |
| Дексаметазон | Hexadrol крем 0,04% |
| Метилпреднизолона ацетат | Medrol мазь 0,25% |
| Преднизолон | Meti-derm крем 0,5% |
| Слабые - класс VIII Гидрокортизон 0,5% | Cortoid крем 0,5% |
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
В.Р. Воронина, врач-дерматовенеролог, к. м. н., ГБОУ ВПО «Российский национальный исследовательский университет им. Н.И. Пирогова», Обособленное структурное подразделение - Научно-исследовательский клинический институт педиатрии им. академика Ю.Е. Вельтищева
Сокращения: ТГКС - топические глюкокортикостероиды, ТИК - топические ингибиторы кальциневрина, АтД - атопический дерматит
Ключевые слова: атопический дерматит, наружная терапия, базовая терапия, топические глюкокортикостероиды, топические ингибиторы кальциневрина
Key words: atopic dermatitis, topical treatment, basic treatment, topical corticosteroids, topical calcineurin inhibitors
Атопический дерматит (АтД) - мультифакторное заболевание кожи, возникающее, как правило, в раннем детском возрасте у лиц с наследственной предрасположенностью к атопическим заболеваниям, имеющее хроническое рецидивирующее течение, возрастные особенности локализации и морфологии очагов воспаления, характеризующееся кожным зудом, обусловленное гиперчувствительностью как к аллергенам, так и к неспецифическим раздражителям [1, 2]. Заболевание в типичных случаях начинается в раннем детском возрасте и значительно нарушает качество жизни больного и членов его семьи. Распространенность среди детского населения составляет до 20%, тогда как у взрослых достигает только 1-3% [2]. Лечение АтД должно быть комплексным и патогенетически обоснованным, включающим элиминационные мероприятия, диету, гипоаллергенный режим, местную и системную фармакотерапию, обучение больного и членов его семьи [3]. Наружная терапия является абсолютно необходимой для достижения улучшения состояния и должна проводиться дифференцированно с учетом изменений кожи, мультифакторного генеза заболевания (интегральный подход) [4, 5].
При назначении терапии следует включать:
Всем больным АтД вне зависимости от тяжести, распространенности, остроты кожного процесса, наличия или отсутствия осложнений назначаются средства базового ухода за кожей. Базовая терапия должна включать рациональный уход за кожей, направленный на восстановление нарушенной функции кожного барьера путем использования смягчающих и увлажняющих средств, средств для очищения кожи, а также выявление и устранение контакта со специфическими и неспецифическими триггерами [5].
Купание ребенка с АтД является необходимой процедурой, позволяющей очистить кожу от нанесенных ранее слоев препаратов, слущивающихся чешуек эпидермиса, корок. Очищение кожи позволяет достигнуть непосредственного контакта лекарственного средства с кожей. Исключением является наличие очагов выраженного мокнутия, вторичного инфицирования кожи. В этот период целесообразно воздержаться от принятия ванной, общего душа в течение нескольких дней, для того, чтобы избежать диссеминации инфекции. Далее купание можно проводить ежедневно, соблюдая комфортную для малыша температуру воды. Вода для купания должна быть 35-36 градусов и желательно дехлорированной (отстаивание воды в течение 1-2 часов). Один-два раза в неделю используются не щелочные моющие средства (так называемые синдеты), без использования жестких мочалок. Высушивание кожи проводится промокающими движениями, без травмирующего растирания кожи. После очищения кожи необходимо обработать расчесы, трещины раствором антисептика (фукорцин, зеленка, мирамистин или др.). Это позволяет свести к минимуму риск вторичного инфицирования и возникновения инфекционно-зависимых обострений дерматита, избежать попадания компонентов наружных средств на участки с нарушенной целостностью кожных покровов, ведущее к возникновению неприятных субъективных ощущений в виде жжения и зуда.
Сразу после купания необходимо использование увлажняющих, релипидирующих средств по уходу за кожей. Это позволяет удержать влагу в эпидермисе, исключить пересыхание кожи [6, 7]. Следует избегать нанесения средств косметического ухода за кожей на очаги острого и подострого воспаления. Конкретный препарат и его лекарственная форма подбираются индивидуально на основании предпочтений пациента, индивидуальных особенностей кожи, сезона, климатических условий, а также времени суток.
Общие рекомендации по применению увлажняющих и смягчающих средств согласно федеральным клиническим рекомендациям по лечению атопического дерматита [2]:
Средства с противовоспалительной активностью выбираются в соответствии со стадией воспалительного процесса (табл.) [7,11].
Таблица.
Применение лекарственных форм при различных стадиях атопического дерматита
| Характер воспалительного процесса | Лекарственная форма |
Острое воспаление с мокнутием (фото 1, 2)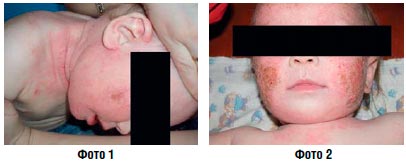 | Примочка Аэрозоль Лосьон Раствор |
Острое воспаление без мокнутия (фото 3)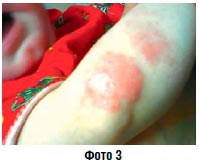 | Водные болтушки Крем Липокрем Паста Аэрозоль |
Подострое воспаление (фото 4, 5)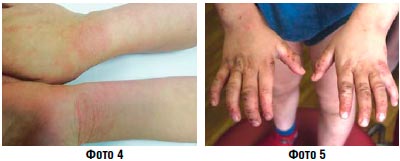 | Крем Липокрем Паста |
Хроническое воспаление (фото 6)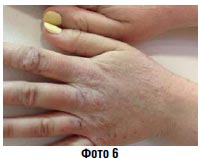 | Мазь Паста Компресс |
Количество топического препарата для наружного применения измеряется согласно правила «длины кончика пальца» (FTU, FingerTipUnit), при этом одна 1 FTU соответствует столбику мази диаметром 5 мм и длиной, равной дистальной фаланге указательного пальца, что соответствует массе около 0,5 г. Этой дозы топического средства достаточно для нанесения на кожу двух ладоней взрослого человека, что составляет около 2% всей площади поверхности тела. Наружные противовоспалительные лекарственные средства необходимо наносить на увлажненную кожу, непосредственно на очаги поражения кожи. Их применение прекращают при разрешении процесса и переходят на базовую терапию. В последнее время рекомендуют метод проактивного лечения: длительное использование малых доз топических противовоспалительных препаратов на пораженные участки кожи в сочетании с применением эмолиентов на весь кожный покров и регулярное посещение дерматолога для оценки состояния кожного процесса [2,12]. Эффективность наружной терапии зависит от трех основных принципов: достаточная сила препарата, достаточная доза и правильное нанесение. При атопическом дерматите с противовоспалительной целью используются топические глюкокортикостероиды, топические ингибиторы кальциневрина, активированный пиритоин цинка. Также возможно использование экстемпоральных мазей, паст, примочек, имеющих в своем составе салициловую кислоту, вазелин, вазелиновое масло, метилурацил, ланолин, нафталан, ихтиол, дерматол, цинк, крахмал, висмут, тальк, борную кислоту, йод, масло оливковое, они обладают комплексным противовоспалительным, кератолитическим, кератопластическим, дезинфицирующим, высушивающим действием.
На сегодняшний день основой местной терапии при обострениях АтД являются топические глюкокортикостероиды (ТГКС). Выбор ТГКС определяется тяжестью течения и обострения. Согласно Европейской классификации (Miller J., Munro D., 1980), выделяют четыре класса данных препаратов в зависимости от их активности. Основные глюкокортикостероидные препараты, рекомендуемые для лечения АтД у детей: гидрокортизон, флутиказона пропионат, мометазона фуроат, гидрокортизона бутират, метилпреднизолона ацепонат. Наружные глюкокортикостероидные препараты наносят на пораженные участки кожи от 1 до 3 раз в сутки, в зависимости от выбранного препарата и тяжести воспалительного процесса. Не рекомендуется разведение официнальных топических препаратов индифферентными мазями, так как такое разведение изменяет концентрацию действующего вещества, но не снижает частоту появления побочных эффектов. Необходимо избегать использования ТГКС высокой активности на кожу лица, область гениталий и интертригинозные участки. Для этих областей обычно рекомендуются ТГКС с минимальным атрофогенным эффектом (мометазона фуроат, метилпреднизолона ацепонат, гидрокортизона-17-бутират). Во избежание резкого обострения заболевания дозу ТГКС следует снижать постепенно. Это возможно путем перехода к ТГКС средствам меньшей степени активности с сохранением ежедневного использования или путем продолжения использования сильного ТГКС, но со снижением частоты аппликаций (интермиттирующий режим) [2, 13]. В ряде клинических исследований было показано, что использование топических ТГКС совместно со смягчающими/увлажняющими средствами позволяет уменьшить курсовую дозу ТГКС [14].
При наличии или подозрении на инфекционное осложнение показано назначение ТГКС, комбинированных с антибиотиками и противогрибковыми средствами (фото 2, 5). Следует учитывать. Что многие комбинированные препараты содержат высокоактивный бетаметазона дипропионат, применение которого у детей нежелательно.
Группа топических ингибиторов кальциневрина (ТИК) включает такролимус и пимекролимус. Фармакологическое действие ТИК обусловлено ингибированием кальциневрина и дальнейшего выделения Т-лимфоцитами и тучными клетками воспалительных цитокинов и медиаторов.
Общие рекомендации по применению ТИК [13]:
Такролимус - наиболее активный представитель топических ингибиторов кальциневрина. Предназначен для лечения АД средней тяжести и тяжелого течения, в том числе стероидрезистентных форм. Многочисленные клинические исследования продемонстрировали, что такролимус обладает эффективностью, сравнимой с таковой сильных ГКС, при этом лишен присущих ГКС побочных эффектов (в частности, не вызывает атрофии кожи) [5]. Показаниями к назначению такролимуса являются среднетяжелое и тяжелое течение АтД в случае резистентности к стандартной терапии. У детей применяется 0,03%-я мазь таролимус. Режим применения - 2 раза в день ежедневно до достижения очищения кожи. Двухкратный режим дозирования должен использоваться не дольше 3 недель, далее мазь наносится однократно. Клинический эффект достигается как правило в течение первой недели. У пациентов, подверженных частым рецидивам заболевания, такролимус необходимо наносить на все обычно поражаемые при обострениях участки кожи 1-2 раза в неделю (перерыв между нанесениями должен составлять 2-3 дня). При возникновении обострения - вновь перейти на режим применения 2 раза в день. Если в течение 6 недель не удается достигнуть улучшения, при переходе на поддерживающий режим дозирования препарата возникает обострение - дальнейшее использование препарата нецелесообразно. Длительность профилактического использования такролимуса - 12 месяцев, затем необходимо провести освидетельствование пациента для принятия решения, продолжать или отменить терапию такролимусом. Во время курса лечения необходимо избегать инсоляции, использовать фотозащитный крем на открытые участки кожи, обрабатываемые мазью такролимус.
Наиболее частые побочные эффекты - покраснение, чувство жжения, усиление зуда на участках обрабатываемых такролимусом. Эти симптомы беспокоят, как правило, в первые дни лечения и разрешаются к концу первой недели. Тяжесть их коррелирует с остротой атопического дерматита. Охлаждение мази в холодильнике перед нанесением и использование увлажняющего средства за 10-15 минут до мази ТИК уменьшает выраженность реакции. Эффекты раздражения кожи можно уменьшить, применяя ацетилсалициловую кислоту внутрь.
Вакцинацию необходимо провести до начала применения мази или спустя 14 дней после последнего использования мази такролимус. В случае применения живой аттенуированной вакцины этот период должен быть увеличен до 28 дней.
Пимекролимус 1%-й крем показан при атопическом дерматите легкого и среднетяжелого течения и может применяться у детей старше 3 месяцев. Однако в ряде стран Европы, США и Канаде пимекролимус разрешен к применению у детей старше 3 лет. Препарат обладает выраженным действием на большинство штаммов Malazessia, что может быть полезно в случаях сенсибилизации к этому грибу [3]. В 2013 году рядом авторов предложен новый алгоритм терапии атопического дерматита легкой и средней тяжести с применением 1%-го крема пимекролимус [13]. При длительно существующем АтД легкой степени тяжести препарат используется дважды в день при появлении первых признаков обострения. Острый АтД легкой и средней тяжести: на протяжении 3-4 дней использование ТКС, с дальнейшим назначением пимекролимуса дважды в день на все пораженные участки до исчезновения симптомов. Предложено проведение поддерживающей терапии длительностью до 3 месяцев 1 раз в день или реже, по усмотрению лечащего врача, на ранее пораженных участках кожи для предотвращения обострений заболевания.
Активированный пиритион цинка (аэрозоль 0,2%, крем 0,2% и шампунь 1%) является нестероидным препаратом, обладающим широким спектром фармакологических эффектов. Может применяться у детей от 1 года, допускается использование на всех участках тела без ограничений по площади. Препарат снижает колонизацию кожи Malassezia furfur, другими грибами, а также S. aureus, участвующими в патогенезе атопического дерматита. Его применение сопровождается уменьшением выраженности кожного зуда, уменьшением степени тяжести и активности кожного процесса, снижением потребности в использовании топических и антигистаминных препаратов. Крем наносят 2 раза в сутки, возможно применение под окклюзионную повязку. Аэрозоль используют в случаях выраженного мокнутия, распыляют с расстояния 15 см 2-3 раза в сутки [2].
Таким образом, современный интегральный подход к терапии АтД включает ступенчатое использование ТГКС, ТИК или других противовоспалительных средств, постоянное использование базовой терапии эмолиентами, бережное очищение кожи, своевременное назначение наружных антисептиков, антибактериальных, противогрибковых препаратов.
ЛИТЕРАТУРА
На основании собственных и литературных данных проведен анализ эффективности и безопасности применения нового топического глюкокортикостероидного препарата - Элоком (мометазона фуроат 0,1%-ный) для лечения различных нозологических форм аллергических болезней кожи (аллергодерматозов)у детей. При использовании Элокома у всех обследованных нами больных с аллергодерматозами не было выявлено ни местных, ни системных побочных эффектов.
Полученные данные свидетельствуют, что крем Элоком дает наилучший эффект при наличии экссудации, мокнутия и больших эрозивных поверхностей на коже. Мазь Элоком более эффективна при аллергодерматозах с выраженной лихенизацией, шелушением и зудом кожи.
Аллергодерматозы - наиболее ранняя и частая клиническая форма проявлений аллергии у детей. Частота аллергических поражений кожи в структуре детских болезней неуклонно увеличивается. Особенно тревожным является значительный рост аллергических болезней кожи с хроническим и рецидивирующим течением, торпидных к традиционной терапии. В настоящее время аллергодерматозы рассматриваются как аллергическое воспаление кожи, обусловленное наследственной предрасположенностью к аллергии и IgE-зависимым механизмом формирования. Процесс характеризуется клиническим полиморфизмом и склонностью к хроническому или рецидивирующему течению. В соответствии с предложенной рабочей классификацией аллергических болезней кожи у детей наиболее часто встречаются атопический дерматит (72%), острая крапивница (15%), хроническая рецидивирующая крапивница (5%), отек Квинке (2,3%), строфулюс (1,8%). В последние годы увеличилась частота токсидермии, многоформной экссудативной эритемы, синдромов Стивенса-Джонсона и Лайелла, которые являются наиболее тяжелыми формами аллергодерматозов [1].
Ведущими факторами риска развития аллергодерматозов у детей являются наследственная предрасположенность к аллергии, внутриутробная сенсибилизация плода к различным аллергенам, раннее искусственное вскармливание, патология желудочно-кишечного тракта, частые эпизоды острых респираторных вирусных инфекций и очаги хронической инфекции, а также нарушение функций центральной и вегетативной нервной системы.
Важным звеном комплексного лечения аллергодерматозов у детей является местная терапия, которая обязательно проводится с учетом стадии болезни, фазы воспаления и степени выраженности кожных проявлений. Причем рациональное использование наружной терапии значительно влияет на разрешение воспалительного процесса в коже. В раннем возрасте, особенно у грудных детей, вследствие высокой проницаемости кожных покровов традиционная наружная терапия начинается с применения индифферентных паст, мазей, болтушек, содержащих противовоспалительные, кератолитические и кератопластические средства. При отсутствии эффекта данной терапии, а также при тяжелых формах аллергодерматозов возникает необходимость применения топических глюкокортикостероидов (ГКС) [2].
Топические ГКС при атопических болезнях кожи применяются уже более 40 лет. Первым топическим ГКС был ацетат гидрокор-тизона. Различные модификации этого гормона привели к разработке эффективных синтетических ГКС с более высокой активностью.
Механизм действия топических ГКС определяется их многообразным влиянием на процессы воспаления в коже [3]. Наиболее важными эффектами ГКС являются:
- увеличение связывания гистамина и серотонина в коже и уменьшение чувствительности нервных окончаний к нейропептидам и гистамину;
- угнетение синтеза интерлейкинов-4,5,13, гамма-интерферона и других цитокинов;
- уменьшение активности фосфолипазы А2 и продукции эйкозанодзов, а также снижение экспрессии молекул клеточной адгезии и чувствительности эндотелия к медиаторам аллергии;
- торможение миграции эозинофилов и пролиферации Т-лимфоцитов; снижение сосудистой проницаемости и нарушений микроциркуляции.
Длительное применение топических ГКС в виде аппликаций (особенно под окклюзионными повязками) может приводить к подавлению глюкокортикоидной функции коры надпочечников. К местным побочным эффектам относятся, прежде всего, развитие атрофии кожи вследствие подавления синтеза коллагена и задержки пролиферации фибробластов, а также формирование телеангиэктазий, гипер- и гипопигментации кожи, гипертрихоза, присоединение микробной и кандидозной инфекции [4]. В соответствии с Европейской классификацией активности местных ГКС по силе действия различают четыре класса препаратов: слабые, средние, сильные, очень сильные. Выделяют также ГКС, содержащие в структуре галогены (преимущественно фтор и хлор). Такие ГКС, как Синалар, Синофлан, Фторокорт, Флуцинар, Лоринден, Целестодерм, содержат фтор. Обладая мощным локальным действием и длительно задерживаясь в коже, эти ГКС дают большое число местных побочных эффектов, вплоть до атрофии кожи, особенно при длительном применении. Наличие хлора и боковой цепи фуроата в структуре мометазона способствует увеличению противовоспалительной активности и сохранению высокой безопасности этого препарата. Негалогенизированными ГКС являются Локоид, Дерматоп, Адвантан. Среди преимуществ этих ГКС выделяют высокую липофильность, быстрое проникновение через эпидермис и хорошее местное действие. Однако эти же свойства ГКС определяют их выраженные системные побочные эффекты при аппликации на большую поверхность кожи и особенно при применении более 4 недель [4].
При использовании местных ГКС необходимо учитывать циркадные ритмы активации коры надпочечников у детей, так как при сохранении нормальной чувствительности к ГКС именно в утренние часы отмечено наименьшее подавление функции системы гипофиз - надпочечники [5].
Принципы назначения топических ГКС при аллергических болезнях кожи. У детей до 6 мес. средством выбора является гидрокортизона ацетат 1%-ный, который следует применять 1 раз в день не более 4 дней подряд; у детей старше 6 мес., когда уровень кортизола в крови становится максимальным в утренние часы, можно использовать другие топические ГКС. При этом необходимо выбирать наиболее изученные и безопасные препараты ГКС. Для предупреждения нарушения функции коры надпочечников следует применять такие ГКС в утренние часы, 1 раз в сутки, короткими курсами не более 10-14 дней на поверхности кожи, не превышающей 20% общей площади кожных покровов. Не рекомендуется использовать окклюзионные повязки, особенно у маленьких детей, имеющих относительно низкое соотношение поверхности тела к его массе [2,5].
Идеальный топический ГКС-препарат должен обладать сильным противовоспалительным действием, низкой системной биодоступностью, быстрым началом действия и минимальными местными побочными эффектами. Этим требованиям в полной мере соответствует хорошо изученный в клинических условиях и использованный нами при лечении аллергодерматозов препарат Элоком.
Элоком (Elocom) - 0,1%-ный мометазона фуроат (mometasone furoate 0,1%) (Schering-Plough, США) - является новой своеобразной молекулярной структурой, базовым основанием которой служит метилпреднизолон, содержащий хлор в 9-й и 21-й позиции и боковую цепь сложного эфира двойной фуранилкарбоновой кислоты (фуроата) в 17-й позиции. Именно эта боковая цепочка фуроата в структуре Элокома определяет его уникальные свойства, значительно отличающие его от прочих ГКС [6, 7]. По сравнению с другими топическими ГКС аналогичной группы Элоком обладает высокой местной активностью, что позволяет отнести его к 3-му классу по силе действия, имеет низкий системный эффект и уровень безопасности, аналогичный слабым ГКС, таким как 1%-ный крем гидрокортизона. Элоком отличает особенно высокая переносимость: по данным клинических исследований, использование препарата у 22831 больного не выявило побочных эффектов, при этом клинически и гистологически не было зафиксировано ни одного случая атрофии кожи даже при длительном нанесении его на участки, более других подверженные атрофии (кожа лица, уши, подмышечные впадины) [4, 8]. В специальных испытаниях было установлено, что npи нанесении препарата под окклюзионную повязку в течение 8 ч только 0,7% препарата абсорбируется в системный кровоток, что указывает на отсутствие влияния Элокома на гормональную систему гипофиз - надпочечники [9].
Уникальное фармацевтическое преимущество Элокома - наличие трех лекарственных форм: крем, мазь, лосьон.
Крем Элоком "масло в воде" - единственная приемлемая форма для лечения атопического дерматита, сопровождающегося экссудацией и мокнутием, у детей до двух лет. 0,1%-ный крем Элоком может успешно применяться также при тяжелых формах аллергодерматозов (особенно при синдромах Стивенса-Джонсона и Лайелла) с обширными эрозивными поражениями кожи. Крем Элоком не проникает глубоко в кожу и удерживается в эпидермисе, что существенно снижает его всасывание и наличие системных эффектов.
Мы использовали 0,1%-ный крем Элоком у 96 детей в возрасте от 6 мес. до 12 лет для местной терапии аллергодерматозов (атонический дерматит - 52 ребенка, многоформная экссудативная эритема - 3 и синдром Стивенса-Джонсона - 1 ребенок). При этом к концу вторых суток было отмечено уменьшение экссудации и гиперемии, на четвертые сутки значительно уменьшался зуд кожи, а к концу седьмых - десятых суток ликвидировались воспалительные явления на коже при отсутствии нежелательных побочных эффектов. Анализ содержания 17-оксикортикостерои-дов (17-ОКС) в моче у этих больных не выявил существенных нарушений выделения этих соединений. В целом использование крема Элоком ускорило наступление ремиссии заболевания в 87% наблюдений и имело выраженное благоприятное психо-эмоциональное воздействие, особенно у детей старшего возраста.
Лосьон Элоком мы использовали с хорошим терапевтическим эффектом для лечения себорейных корочек (гнейс) волосистой части головы при атопическом дерматите. При этом к четвертому-пятому дню было отмечено значительное уменьшение образования корочек.
Мазь Элоком применена нами при лечении 40 детей в возрасте от 2 до 12 лет с атоническим дерматитом с синдромом лихени-зации и выраженным зудом. При этом на четвертые сутки было отмечено значительное уменьшение зуда и сухости кожи, а к десятым суткам - купирование воспалительного процесса в 76% наблюдений.
Применение препарата Элоком при различных формах аллергического поражения кожи давало выраженный положительный эффект к седьмому-десятому дню, что свидетельствует об отсутствии необходимости его длительного применения и особенно важно у детей. При использовании Элокома у всех обследованных нами больных с аллергодерматозами не было выявлено ни местных, ни системных побочных эффектов.
Полученные нами данные свидетельствуют о том, что крем Элоком дает наилучший эффект при наличии экссудации, мокнутия и больших эрозивных поверхностей на коже. Мазь Элоком более эффективна при аллергодерматозах с выраженной лихенизацией, шелушением и зудом кожи.
Таким образом, Элоком - высокоэффективный, безопасный топический ГКС последнего поколения и по фармакологическим свойствам приближается к идеальному препарату выбора для местного лечения аллергодерматозов у детей.
Литература
Представлены результаты клинического мониторирования эффективности и безопасности терапии больных атопическим дерматитом взрослых с использованием различных лекарственных форм метилпреднизолона ацепоната. Показана рациональность дифференцированного назнач
Tactics of topical therapy of patients with atopic dermatitis using various dosage forms of topical glucocorticosteroid N. V. Kungurov, M. M. Kokhan, Yu. V. Keniksfest, E. I. Stukova, N. P. Toropova
The results of clinical monitoring of the effectiveness and safety of therapy in adult patients with atopic dermatitis using various dosage forms of methylprednisolone aceponate are presented. The rationality of differentiated prescription of dosage forms of methylprednisolone aceponate in the localization of skin manifestation in the problem areas, on the skin of the torso and limbs, and according to the clinical manifestations is shown. The safety of the drug methylprednisolone aceponate in the treatment of patients with atopic dermatitis, the absence of side effects in the treatment at the specified time was confirmed.
До настоящего времени широкая распространенность атопического дерматита (АтД) фиксируется в развитых странах, в том числе и в Российской Федерации, а проблема эффективной и безопасной наружной терапии заболевания находится в фокусе внимания практических специалистов дерматовенерологов [1–3]. АтД — это мультифакториальное воспалительное заболевание кожи, возникающее, как правило, в раннем детском возрасте у лиц с наследственной предрасположенностью к атопическим заболеваниям, имеющее хроническое рецидивирующее течение, возрастные особенности локализации и морфологии очагов воспаления, характеризующееся кожным зудом и обусловленное гиперчувствительностью как к аллергенам, так и к неспецифическим раздражителям [3–5].
Актуальные подходы к терапии больных АтД определены в отечественных [4] и зарубежных [5–7] клинических рекомендациях и включают следующие основные направления:
- профилактические стратегии (элиминационные меропрятия);
- гипоаллергенная диета;
- рациональный уход за кожей (умывание и купание, увлажнение);
- топическая, наружная терапия;
- противозудная терапия (топическая и системная);
- иммуносупрессивная терапия (системные глюкокортикостероиды (ГКС), иммунодепрессанты, в том числе генно-инженерные биологические препараты);
- противоинфекционная терапия (антибиотики, антимикотики, противовирусные препараты);
- фототерапия;
- аллерген-специфическая иммунотерапия;
- образовательные программы для детей, членов их семей и для взрослых пациентов.
Крайне важным из указанных направлений ведения больных АтД признается наружная противовоспалительная терапия, «первой линией» которой остаются топические глюкокортикостероидные (ТГКС) препараты, применяемые для купирования воспалительных проявлений АтД у детей и взрослых [4, 5, 8]. Среди современных ТГКС-препаратов последнего поколения присутствует метилпреднизолона ацепонат (МПА) (Адвантан®) — негалогенизированный топический глюкокортикостероид, относящийся к классу сильных ТГКС. Доказана высокая эффективность противовоспалительного действия МПА, особые механизмы которого заключаются в активации пролекарства в очаге воспаления за счет ферментов — эстераз; высокой скорости проникновения в кожу и быстром начале действия, благодаря высокой липофильности и сродству к рецепторам клеток — эффекторов воспаления. Активность МПА в составе Адвантана определяется количеством эстераз, таким образом кожа может сама регулировать необходимое количество МПП в зависисмости от выраженности воспаления. Важным фактором является, что механизм биоактивации, равно как и данные по безопасности и эффективности молекулы были исследованы только для МПА в составе Адвантана. Добавление дополнительных компонентов к молекуле Адвантана не изучалось с точки зрения эффективности препарата. МПА имеет дальнейшее минимизированное проникновение (0,27–2,5%) в кровь и полную быструю инактивацию за счет связывания с глюкуроновой кислотой, благодаря компактности молекулы [9, 10].
Особые фармакологические свойства МПА определяют высокую степень противовоспалительного действия препарата, что сочетается с минимальными нежелательными явлениями. Проведены исследования по сравнительному анализу комплекса клинических и лабораторных данных различных ТГКС: эффективности — по балльной оценке степени вазоконстрикции, сравнительной эффективности ТГКС при АтД; а также степени выраженности нежелательных явлений — по возможному развитию атрофии кожи, влиянию на системный баланс ГКС, аллергическому потенциалу. Соотношение указанных «про» и «контра» факторов исчисляется как «терапевтический индекс» (ТИ, Therapeutic index — TI) ТГКС. Установлено, что МПА имеет один из самых высоких терапевтических индексов (TI 2,0), в сравнении с ТГКС более ранних генераций [11, 12].
В работе, представленной Европейским дерматологическим форумом и посвященной применению топических глюкокортикостероидов у беременных, подтверждаются данные об эффективности и безопасности МПА 0,1%, подчеркивается целесообразность однократного в течение суток применения наружной гормональной терапии [13]. В недавнем обзоре А. Torrelo [14] анализируются данные нескольких клинических исследований МПА 0,1% при АтД, автор обоснованно указывает, что применение МПА 0,1% у младенцев и детей демонстрирует минимальные местные или системные побочные эффекты, даже при частых обострениях процесса и нанесении препарата на обширные участки кожи.
Уникальным для МПА (препарат Адвантан) является факт наличия четырех лекарственных форм препарата, содержащих 0,1% МПА, — эмульсии, крема, мази и жирной мази. В перечисленных лекарственных формах препарата Адвантан введено различное содержание воды: в эмульсии — 67,5%, в креме — 60% («масло в воде»), в мази — 30% («вода в масле»), а жирная мазь практически не содержит воды, при этом снижение содержания воды увеличивает липофильные свойства препарата и способствует скорости проникновения в эпидермис.
Отечественный опыт использования препарата Адвантан в клинической практике значителен и свидетельствует о высокой эффективности данного ТГКС, однако тактические вопросы дифференцированного назначения различных лекарственных форм МПА 0,1%, в зависимости от клинико-морфологических особенностей кожного процесса при АтД остаются до конца неизученными [15–17].
В клинике ГБУ СО «Уральский научно-исследовательский институт дерматовенерологии и иммунопатологии» осуществлена наблюдательная программа контроля эффективности и безопасности МПА 0,1% (эмульсия, крем, мазь, жирная мазь) в терапии больных АтД.
Все пациенты (n = 25) были проинформированы о необходимости соблюдения гипоаллергенного режима и диеты, получали стандартную системную терапию в соответствии с тяжестью кожного процесса, при этом исключалось введение системных глюкокортикостероидных гормонов, иммуносупрессивных средств, других ТГКС. Лечение проводилось в стационарном и амбулаторном режимах.
Определение тяжести процесса до начала и в динамике лечения проводилось с использованием индекса EASI (Eczema area and severity index) [18]. Индекс EASI определялся по общепринятой методике, где врачом проводилась оценка заболевания по основным его проявлениям (Е — эритема; I — инфильтрация; Ех — экскориации; L — лихенификация), то есть фиксировалась интенсивность объективных симптомов АтД отдельно в 4 локализациях: верхние конечности (A), нижние конечности (B), туловище (C), голова/шея (D) с применением балльной оценки выраженности симптомов от 0 до 3 баллов. Проводилась оценка площади поражения кожи (S), которая также оценивалась по балльной системе с применением градаций: 0 — нет высыпаний; 1 балл < 10% площади кожи; 2 балла = 10–29%; 3 балла = 30–49%; 4 балла = 50–69%; 5 баллов = 70–89%; 6 баллов = 90–100% площади кожи.
Общий индекс EASI исчислялся как сумма показателей всех локализаций (табл. 1). Подсчет индекса EASI проводился до начала лечения, в процессе лечения (еженедельно) и через 4 недели после окончания терапии.
Выраженность зуда оценивалась с использованием визуально-аналоговой шкалы (ВАШ зуда) от 0 до 10 баллов, лечащими врачами фиксировалось наличие пиогенных проявлений и возникновение побочных нежелательных явлений, переносимость терапии препаратом Адвантан.
В табл. 2 приведены характеристики наблюдаемых больных с АтД.
Назначение лекарственных форм МПА 0,1% и препаратов для ухода за кожей проводилось лечащими врачами дифференцированно в зависимости от клинико-морфологического характера проявлений и при различных локализациях процесса, при этом учитывались рекомендации, отражающие базовые принципы проведения наружной терапии дерматозов [4, 5].
До начала лечения средний показатель индекса EASI в группе больных АтД составил 16,6 ± 4,8 балла, при этом локальная составляющая индекса EASI, характеризующая тяжесть процесса на нижних конечностях (В), достигала 7,1 ± 2,2 балла, а в области головы/шеи (D) — 1,7 ± 0,6 балла (рис. 2). В процессе проведения терапии общий индекс EASI снижался при пропорциональном уменьшении всех его локальных составляющих: в области верхних и нижних конечностей, туловища, головы и шеи.
К окончанию срока терапии, продолжавшейся от 7 до 28 дней, отмечалось практически полное очищение кожи от высыпаний, общий среднегрупповой индекс EASI (EASI 4) составил менее 1,0 балла. При осмотре через месяц после прекращения лечения полный регресс высыпаний сохранялся у всех пациентов с АтД, а индекс EASI 5 также был менее 1,0 балла.
Анализ динамики регресса симптомов АтД при проведении топической терапии МПА 0,1% (Адвантан), исчисляемый по отношению к исходному показателю EASI, показал, что после первой недели лечения происходило снижение выраженности симптомов заболевания во всех локализациях: в области кожи головы/шеи на 41,2%, конечностей и туловища на 34,3–40,7% от исходного (табл. 3).
Достижение состояния клинической ремиссии с регрессом индекса EASI на 75% и более от исходного наблюдалось между 2-й и 3-й неделей лечения, а при последующих осмотрах (EASI 4) и через 4 недели после окончания терапии (EASI 5) снижение выраженности проявлений АтД достигало 88,2–94,0% от исходного, то есть сохранялось полное очищение кожи во всех локализациях.
До начала терапии выраженность зуда кожи у больных АтД по данным ВАШ зуда фиксировалась от 4 до 10 баллов, в среднем по группе 8,1 ± 1,9 балла. В динамике терапии уже после 1 недели лечения среднегрупповые показатели ВАШ оценки зуда снизились до 2,5 ± 0,7 балла, в последующие недели показатель зуда не превышал 2,0–2,2 балла.
Сопоставление динамики регресса выраженности зуда и индекса EASI (рис. 3) показало, что уменьшение чувства зуда происходило раньше, чем регресс других симптомов и площади поражения кожи, после 2 недели лечения эти показатели не отличались, через 4 недели и после окончания терапии — объективные симптомы регрессировали полностью (на 94% от исходного), а зуд носил минимальный остаточный характер.
Анализ показал, что для терапии проявлений АтД в области головы и шеи более половины специалистов (56%) рекомендовали использование лекарственной формы эмульсии Адвантана, а в 40% — крема (рис. 4). При локализации высыпаний в области кожи туловища врачи назначали практически с одинаковой частотой (40% и 48%) Адвантан в форме крема и мази, эмульсию использовали реже (8%). Терапия высыпаний на коже верхних конечностей проводилась преимущественно кремом и мазью Адвантан (48% и 32%), а у 8% больных АтД врачи использовали лекарственную форму жирной мази. Большинство дерматологов (52%) назначали для терапии высыпаний в области нижних конечностей мазь Адвантан и крем (24%), 16% специалистов проводили терапию АтД в данной локализации жирной мазью Адвантан.
Лечащие врачи отмечали, что с учетом многообразия проявлений АтД у взрослых, когда в одних локализациях преобладали гиперемия, отечность, очаги мокнутия, а в других — инфильтрация различной степени выраженности, лихенификация, фиссуризация, пациентам назначались дифференцированно несколько лекарственных форм препарата Адвантан: например, на кожу лица и шеи — эмульсия, на кожу конечностей — мазь или жирная мазь.
Результаты проведенной работы, клинический опыт позволили разработать алгоритм применения эмульсии, крема, мази и жирной мази Адвантан в зависимости от характера проявлений кожного процесса (острый, хронический), локализации поражений и основных, преобладающих симптомов заболевания (рис. 5).
В процессе терапии и в течение 4 недель после ее окончания больным АтД проводился уход за кожей с использованием эмолентов, что обеспечивало восстановление липидного состава эпидермиса, комплексное увлажнение кожи.
В процессе проведения наружного лечения препаратом МПА 0,1% (Адвантан) лечащими врачами фиксировалось возникновение нежелательных явлений и побочных эффектов терапии: усиление зуда, гиперемии на начальном этапе терапии у 2 больных, появление пиогенных, вирусных осложнений у 2 пациентов. Явлений атрофии кожи, гипертрихоза, сосудистых нарушений зафиксировано не было.
Заключение
Анализ фактических данных, полученных в ходе наблюдательной программы, свидетельствует о высокой клинической эффективности препарата МПА 0,1% (Адвантан) в терапии больных АтД, характеризовавшейся достижением клинической ремиссии у больных АтД после 3 недель лечения с регрессом индекса EASI на 88,6% от исходного уровня. Практически полное очищение кожи, минимальная выраженность зуда или его отсутствие сохранялись у всех больных в течение 4 недель после окончания лечения. Значимым, определяющим дополнительную результативность лечения, является дифференцированный подход к назначению различных лекарственных форм МПА 0,1% (Адвантан), когда эмульсия и крем применяются при локализации высыпаний в проблемных зонах в условиях преобладания симптомов гиперемии, отечности; мазь — в терапии высыпаний на коже туловища и конечностей при наличии очагов воспалительной инфильтрации, жирная мазь — в случае формирования стойких поражений кожи в области нижних конечностей, присутствия плотной инфильтрации, лихенификации, гиперкератоза. Клинические наблюдения показали, что редукция чувства зуда при топическом лечении МПА 0,1% (Адвантан) предшествует регрессу объективных симптомов в первые недели терапии.
Подтверждена безопасность использования препарата МПА 0,1% (Адвантан) в терапии больных АтД, отсутствие формирования побочных эффектов при лечении в указанные сроки. Представляется обоснованным широкое использование препарата МПА 0,1% (Адвантан) для топического применения у больных АтД, при этом достаточные сроки наружного лечения, обоснованное дифференцированное назначение эмульсии, крема, мази и жирной мази, а также адекватный уход за кожей обеспечивают высокую клиническую результативность терапии и сохранение ремиссии.
Литература
- Bieber T. Atopic Dermatitis // Ann. Dermatol. 2010; 22 (2): 125–137.
- Darsow U., Wollenberg A., Simon D., Ta?¨eb A., Werfel T., Oranje A. Gelmetti C., Svensson A., Deleuran M., Calza M., Giusti F., Ring J. ETFAD⁄EADV eczema task force 2009 position paper on diagnosis and treatment of atopic dermatitis // JEADV. 2010; 24: 317–328.
- Голдсмит Л. А., Кац С. И., Джилкрест Б. А. и др. Дерматология Фицпатрика в клинической практике / Пер. с англ. под общ. ред. Потекаева Н. Н., Львова А. Н. Изд. 2-е. Издательство Панфилова, 2015. Т. 1, с. 182–200.
- Федеральные клинические рекомендации. Дерматовенерология 2015: Болезни кожи. Инфекции, передаваемые половым путем. 5-е изд., перераб. и доп. М.: Деловой экспресс, 2016. 768 с.
- Wollenberg A., Barbarot S., Bieber T., Christen-Zaech S., Deleuran M. et al. GUIDELINES Consensus-based European guidelines for treatment of atopic eczema (atopic dermatitis) in adults and children: part I // JEADV. 2018, 32: 657–682.
- Calzavara Pinton P., Cristaudo A., Foti C., Canonica G. W., Balato N. et al. Diagnosis and management of moderate to severe adult atopic dermatitis: a Consensus by the italian Society of dermatology and Venereology (SidemaSt), the Italian association of Hospital dermatologists, the Italian Society of allergy, asthma and Clinical immunology (SiaaiC), and the italian Society of allergological, environmental and occupational dermatology (SidaPa) // Giornale italiano di dermatologia e Venereologia. 2018; 153 (2): 133–145.
- Ilgen Ertam, Özlem Su, Sibel Alper, Hayriye Saricaoglu, Ayse Serap Karadag et al. The Turkish guideline for the diagnosis and management of atopic dermatitis — 2018 // Turkderm-Turk Arch Dermatol Venereology. 2018; 52: 6–23.
- Кунгуров Н. В., Кохан М. М., Кениксфест Ю. В., Гришаева Е. В., Кащеева Я. В., Куклин И. А. Оптимизация наружной терапии стероидчувствительных дерматозов // Вестн. дерматол. и венерол. 2007; 4: 45–51.
- Haria M., Balfour J. A. Methylprednisolone aceponate. A review of its pharmacological properties and therapeutic potential in the topical treatment of eczema // Clin Immunother. 1995; 3: 241–253.
- Brazzini B., Pimpinelli N. New and established topical corticosteroids in dermatology: clinical pharmacology and therapeutic use // Am J. Clin. Dermatol. 2002; 3: 47–58.
- Luger T., Loske K., Elsner P. et al. Topical skin therapy with glucocorticosteroids — therapeutic index // J Deutsch Dermatol Ges. 2004; 7: 629–634.
- Luger T. A. Balancing efficacy and safety in the management of atopic dermatitis: the role of methylprednisolone aceponate // JEADV. 2011; 25: 251–258.
- Chi C. C., Kirtschig G., Aberer, Gabbud J.-P., Lipozencic J., Karp S. et al. Updated evidence-based (S2e) European Dermatology Forum guideline on topical corticosteroids in pregnancy // JEADV. 2017; 31: 761–773.
- Torrelo A. Methylprednisolone aceponate for atopic dermatitis // Int J Dermatol. 2017; 56 (6): 691–697.
- Кохан М. М., Кениксфест Ю. В., Новиков Г. М. Эффективность сочетанного применения наружных средств терапии и увлажнения кожи у больных атопическим дерматитом // Вестн. дерматологии и венерологии. 2007; 4: 55–60.
- Волкова Е. Н., Ланге Д. А., Родина Ю. А., Тарасова М. В. Метилпреднизолона ацепонат в комплексной терапии хронических дерматозов: анализ тактических ошибок применения // Клиническая дерматология и венерология. 2010; 5: 97–102.
- Дворянкова Е. В., Корсунская И. М., Сакания Л. Р., Невозинская З. А. К вопросу о рациональном выборе топической терапии при атопическом дерматите // Consilium medicum. Дерматология, 2015; 1: 70–74.
- Hanifin J. M., Thurston M., Omoto M., Cherill R., Tofte S. J., Graeber M. The eczema area and severity index (EASI): assessment of reliability in atopic dermatitis // EASI Evaluator Group. Exp Dermatol. 2001; 10 (1): 11–18.
Н. В. Кунгуров, доктор медицинских наук, профессор
М. М. Кохан 1 , доктор медицинских наук, профессор
Ю. В. Кениксфест, доктор медицинских наук
Е. И. Стукова
Н. П. Торопова, доктор медицинских наук, профессор
ГБУ СО УрНИИДВиИ, Екатеринбург
Дерматит и экзема. Глюкокортикостероиды, циклоспорин и пимекролимус при дерматите
Это взаимозаменяемые термины, обозначающие форму воспаления кожи, которая характеризуется присутствием межклеточного отека (спонгиоза) в эпидермисе. Термин часто используют для обозначения атопической экземы, но причиной заболевания могут также быть контакт с раздражающими агентами, например сильными кислотами или контактными аллергенами, такими как никель; гиперчувствительность к лекарственным средствам, дрожжам Pityrosporum (себорейный дерматит); местные факторы, например венозный стаз (варикозная экзема).
Рациональное лечение экземы заключается в попытках устранить или свести к минимуму влияние указанных этиологических факторов, а также лекарств, применяемых для ослабления воспалительной реакции (глюкокортикостероиды, циклоспорин, азатиоприн). Повреждение кожи, вызванное воспалением, приводит к повышенной чрезэпидермальной потере воды, которую частично можно скорригировать применением местных смягчающих средств. Следует использовать заменители мыла для уменьшения раздражения кожи и антагонисты Н1-рецепторов для борьбы с зудом, который может привести к дальнейшему повреждению кожи в результате расчесывания.
Местное применение глюкокортикостероидов служит основой терапии атопической экземы. Они оказывают противовоспалительный и сосудосуживающий эффекты и подавляют деление кератиноцитов. Глюкокортикостероиды можно подразделить на 4 группы соответственно их сосудосуживающей активности в тесте МакКензи, которая хорошо коррелирует с клиническим эффектом.
Следует учесть, что соли гидрокортизона существенно различаются по эффективности, поэтому дерматологи избегают назначать глюкокортикостероиды вне зависимости от их специфики. Фторированные глюкокортикостероиды обладают особенно сильным действием и системной абсорбцией. Есть сведения о том, что новые глюкокортикостероиды, флутиказона пропионат и мометазона фуроат, представляют собой сильные местные глюкокортикостероиды с менее выраженной системной абсорбцией.
Системное применение глюкокортикостероидов редко бывает необходимым в лечении атопической экземы, даже у взрослых. Системное действие глюкокортикостероидов относительно малоэффективно, наблюдается тахифилаксия и действие, обратное ожидаемому, они способны нарушать рост, особенно в период интенсивного роста у подростков.
Эффективность циклоспорина, облегчающего симптомы атопической экземы, была обнаружена случайно у пациентов, перенесших трансплантацию органов и одновременно страдавших экземой. Клинические испытания, проведенные на взрослых пациентах и детях, показали эффективность этого агента, часто проявляющуюся уже вскоре после начала лечения. Однако через несколько недель после окончания терапии заболевание рецидивировало. В настоящее время циклоспорин рекомендуют для кратковременного лечения атопической экземы у взрослых пациентов в случае отсутствия реакции на обычные способы терапии.
Циклоспорин действует главным образом на Т-лимфоциты, однако может влиять непосредственно на синтез ДНК и пролиферацию кератиноцитов.
До начала лечения циклоспорином необходимо тщательно обследовать пациентов, особенно в отношении функции почек. Уровень лекарственного средства в крови у пациентов с заболеваниями кожи обычно не определяют, т.к. используемые дозы (максимум 5 мг/кг) существенно ниже применяемых при трансплантации органов. Пациентам, принимающим циклоспорин, рекомендуется избегать избыточного солнечного освещения, а также лечения ультрафиолетовым облучением. Это обусловлено хорошо известным повышением числа случаев рака кожи у пациентов после трансплантации органов, что частично связано с иммуносупрессивной терапией.
Циклоспорин чаще используют для лечения псориаза, а не атопической экземы. Показанием являются случаи тяжелого псориаза, когда общепринятая терапия неэффективна или неприменима. Хороший эффект получен также при псориатической артропатии. Циклоспорин при этом заболевании можно использовать в сочетании с метотрексатом, чтобы снизить токсичность и кумулятивную дозу каждого агента.
Значение циклоспорина как средства лечения редких и тяжелых дерматозов, например гангренозной пиодермы, является предметом исследований.
Пимекролимус, Т-клеточный ингибитор второго поколения, также предназначен для лечения атопической экземы.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

