Какие гормональные препараты помогут при угревой сыпи
Обновлено: 19.04.2024
Е. Н. Волкова, Л. А. Ильин, А. Б. Воробьев, Е. О. Рюмина
Кафедра дерматовенерологии (зав. — проф. Е. Н. Волкова) московского факультета ГОУ ВПО Российский государственный медицинский университет Росздрава; Кожновенерологический диспансер № 9, Москва
Анализируются типичные ошибки в назначении и применении дифферина, описаны его структура и уникальная кинетика, результаты исследования терапевтической эффективности различных лекарственных форм. Приведены факты, свидетельствующие о высокой эффективности и безопасности дифферина в терапии угревой болезни.
Ключевые слова: вульгарные угри, постакне, адапален, дифферин, ошибки применения, эффективность
Typical mistakes in prescription and usage of differin are analyzed. Structure and unique kinetics of this preparation are described and results of effectiveness studies of different drug formulations are presented. Authors present facts illustratinf high effectiveness and safety of differin in acne therapy.
Key words: acne, post-acne, adaplen, differin, therapeutic mistakes, effectiveness
Заболевание, в основе которого лежит патология пилосебоцейного комплекса, правильнее называть угревой болезнью — УБ (точка зрения авторов), так как оно представлено комплексом симптомов, патогенетически объединенных в единый патологический процесс, и психоэмоциональными нарушениями. Термин "вульгарные угри" и "акне" характеризуют лишь один конкретный симптом заболевания [2, 7].
Сегодня накоплен огромный опыт терапии УБ, разработаны алгоритмы лечения в зависимости от степени тяжести с учетом терапевтического индекса акне как основы дифференцированного подхода к ведению больных. Современные схемы включают назначение системных препаратов и средств наружной терапии на фоне правильно подобранного базового ухода [1, 2, 8].
На сегодняшний день наиболее эффективным противоугревыми средствами для местного применения являются ретиноиды, которые способны вызывать специфический биологический ответ в результате связывания и активации рецепторов ретиноевой кислоты. К ретиноидам 3-го поколения для местной терапии акне относят адапален, представляющий собой производное нафтойной кислоты с ретиноидподобным действием.
Несмотря на продолжительное использование дифферина для местного лечения УБ, обширного опыта его клинического применения отмечаются отдельные ошибки при его использовании. Часть из них связана с недостаточной информированностью врача и неправильной трактовкой имеющейся информации. Существует и "страх врача" при назначении местных ретиноидов.
Проведем работу над ошибками.
Ошибка 1: неправильный выбор лекарственной формы.
Адапален имеет 2 лекарственные формы для наружного применения — гель и крем. При выборе лекарственной формы следует помнить, что эффективность действия препарата определяется взаимосвязями в системе "препарат—основа—кожа". Именно правильное увлажнение рогового слоя значительно усиливает проникновение веществ.
Обычно лечение начинают с геля. Если у пациента чувствительная и сухая кожа, то рекомендован дифферин-крем. Он содержит увлажняющие некомедогенные компоненты.
Необходимо соблюдать режим дозирования. Гель и крем бережно, без особого усилия, наносят на пораженные участки кожи 1 раз в день на ночь на чистую сухую кожу.
Ошибка 2: необоснованные "завышенные" ожидания быстрого результата.
Дифферин — препарат патогенетического действия, поэтому назначение препарата сегодня не приведет к проявлению результата завтра! Это необходимо учитывать врачу и объяснять пациенту (проводить его "обучение"). Отсутствие быстрого визуального эффекта может приводить к отказу пациентов от лечения! А между тем препарат является высокоэффективным средством в лечении УБ. Его терапевтическая эффективность связана с тем, что молекула адапалена селективно связывается с ретиноидчувствительными рецепторами (RAR) у-типа сально-волосяных фолликулов (СВФ), что приводит к уменьшению сцепленности кератиноцитов и ускоряет их десквамацию (т. е. реализуется комедонолитическое действие препарата) [9, 11]. Отсутствие взаимодействия с рецепторами RAR-a СВФ, стимуляция которых ведет к появлению шелушения и резкой сухости кожи, позволяет свести к минимуму побочные реакции, которые наблюдались ранее при использовании ретиноидов 1-го поколения. Антипролиферативная активность дифферина по отношению к себоцитам связана со стимуляцией RXR-a. В результате уменьшаются размеры сальной железы и сокращается продукция кожного сала. Третьим звеном патогенеза, на которое воздействует препарат, является воспаление. Адапален ингибирует API — участок в промоторной зоне гена, что приводит к подавлению образования цитокинов — интерлейкинов (ИЛ)-1а, ИЛ-1р, и ИЛ-8; фактора некроза опухоли (ФНО-a), системы комплемента. Инактивация фермента циклооксигеназы ведет к уменьшению образования ЛТВ4 — главного посредника во взаимодействии нейтрофилов, лимфоцитов, моноцитов и эозинофилов в воспалительной реакции. Кроме того, адапален блокирует Toll-рецептор 2-го типа (TLR-2), рецепторы моноцитов, предотвращая связывание с ними микроорганизмов и последующий выброс противовоспалительных цитокинов. Таким образом, дифферин оказывает действие на все звенья патогенеза УБ [3, 8, 9, 11].
Ошибка 3: неправильное формирование группы больных.
Дифферин — не панацея для лечения всех видов акне — это тоже ошибка: для его назначения существуют определенные показания (рис. 1).
Рис. 1. Показания для применения дифферина.
Ошибка 4: неправильное определение продолжительности лечения дифферином.
В среднем курс лечения составляет до 12 нед, для этого требуется не менее 30 г препарата в форме геля или крема (при нанесении препарата только на область лица). Терапевтический эффект развивается после 4—8 нед лечения, стойкое улучшение — после 3-месячного курса. Такая длительная терапия не только наиболее рациональна и эффективна, но и предотвращает формирование постакне.
Ошибка 5: неинформированность об особенностях дифферина.
Следует знать о двух нюансах.
Нюанс 1: состав основы, ее физикохимические характеристики определяют как свойства препарата, так и его способность к проникновению в кожу (рис. 2).
Рис. 2. Фармакодинамическая характеристика дифферина (0,1% адапелена-геля).
Нюанс 2: размер микрокристаллов действующего вещества.
Микрокристаллы адапалена в препарате имеют диаметр от 3 до 10 мк. Оказывается, если диаметр микрокристаллов действующего вещества составляет менее 3 мк — препарат беспорядочно распределяется между сально-волосяным фолликулом и роговым слоем кожи; при диаметре более 10 мк — препарат остается на поверхности кожи.
Правильный размер частиц активного вещества в дифферине — залог эффективного лечения [9, 11]. Вопрос — так ли это в джинерике? (результатов таких исследований не предоставлено).
Ошибка 6: не учитывается возможность комбинирования препаратов.
Дифферин сохраняет лечебное действие в комбинации с местными антибактериальными противоугревыми средствами (эритромицин, клиндамицин, бензоила пероксид) [3, 6, 10, 12]. Это расширяет возможности его применения даже при обилии пустулезных элементов. Наиболее целесообразно назначать дифферин в комбинации с базироном АС (рис. 3).
Рис. 3. Применение Дифферина в комбинации с Базироном АС.
Ошибка 7: недооценка показаний к применению дифферина.
Дифферин — местное средство не только для базового патогенетического лечения больных акне. Он показан как препарат поддерживающей терапии, а также при переводе пациента с системной терапии, например акнекутаном, на местную. Такая тактика — не только залог эффективного лечения, но и стойкой длительной ремиссии и профилактики постакне.
Таким образом, правильное применение дифферина позволяет избежать ошибок, преодолеть страх перед назначением ретиноидов. Повысить эффективность лечения больных УБ. Вся история применения дифферина свидетельствует о том, что он является высокоэффективным базовым препаратом для лечения акне легкой и средне-тяжелой степени — показания к его применению строго определены.
Для достижения выраженного и стойкого эффекта необходимо длительное назначение дифферина, что предотвращает появление и развитие новых элементов. При наличии папуло-пустулезных элементов целесообразно применение дифферина в комбинации с препаратом антибактериального действия — базироном АС.
Эффективность и переносимость терапии дифферином были оценены нами при наблюдении 62 пациенток в возрасте от 16 до 22 лет с длительностью заболевания от 1 года до 6 лет. У 26 (42%) пациенток высыпания локализовались только на лице, у 23 (37,1%) — на лице и груди, у 13 (20,9%) — на спине.
В зависимости от степени тяжести УБ пациентки были распределены на 2 группы. 1-ю группу (n = 29) составили больные легкой степенью акне, у которых доминировали комедоны и единичные папулы; 2-ю (n = 33) — больные папуло-пустулезной формой заболевания.
Больным 1-й группы проводили только наружное лечение дифферином в виде геля или крема (в зависимости от состояния кожи) в сочетании с правильным уходом. Препарат наносили тонким слоем 1 раз в день вечером на предварительно очищенную кожу лосьоном сетафил.
Больным 2-й группы дифферин назначали в комбинации с базироном АС в виде геля, который наносили на предварительно очищенную кожу однократно утром. Контроль количества открытых и закрытых комедонов, папул и пустул производили до начала терапии, а также каждый месяц.
Окончательный эффект от терапии наблюдали к концу 4—5-го месяца, когда комедоны и папулопустулезные высыпания регрессировали более чем на 70—75%. Выявлено, что нанесение базирона АС на поствоспалительные гиперпигментированные пятна и рубцы приводило к их побледнению. В результате лечения клиническая ремиссия наступила у 22 (35,5%) больных, значительное улучшение (регресс высыпаний на 70—80%) — у 26 (42%), улучшение (регресс высыпаний на 50—60%) — у 13 (21%) и неэффективным лечение оказалось у 1 больной.
Таким образом, дифферин является высокоэффективным базовым препаратом первого выбора для патогенетической терапии акне.
Для достижения выраженного и стойкого терапевтического эффекта необходимо длительное назначение дифферина. Препарат сохраняет лечебное действие в комбинации с местными антибактериальными средствами (базирон АС), что определяет целесообразность применения дифферина при наличии папуло-пустулезных элементов. Оригинальная основа (гель на водной основе), равномерная дисперсия микрокристаллов адапалена определяют эффективную доставку активного вещества в пораженную кожу (избирательно в сальноволосяной фолликул), лучшую переносимость препарата и оптимальные косметические свойства.
Рациональная терапия дифферином — залог успешной терапии угревой болезни и профилактики постакне.
1. Волкова Е. Н. // Лечащий врач. — 2007. — № 4. — С. 21— 28.
2. Волкова Е. Н., Осипова Н. К. // Рос. журн. кож. и вен. бол. — 2009. — № 5. — С. 53—58.
3. Волкова Е. Н, Осипова Н. К // Клин. дерматол. и венерол. — 2010. — № 2. — С. 72—77.
4. Гущина Н. С., Корчевая Т. А. // Рус. мед. журн. — 2005. — Т. 13, № 7. — С. 482—485.
5. Орлова Н. А // Клин. дерматол. и венерол. — 2003. — № 4. — С. 53—56.
6. Самгин М. А., Монахов С. А. // Вест. дерматол. и венерол. — 2003. — № 4. — С. 37—39.
7. Самгин М. А., Монахов С. А. // Рос. журн. кож. и вен. болезней. — 2005. — № 3. — С. 55—64.
8. Самгин М. А., Монахов С. А. // Рос. журн. кож. и вен. болезней. — 2006. — № 6. — С. 85—87.
9. Data on file. Galderma Laboratories, Ins. Medical Departament. — 1994.
10. Eady E. A., Farmery M. R, Ross J. I. et al. // Br. J. Dermatol. — 1994. — Vol. 131. — P. 331—336.
11. Michel S., Jomard A., Demarschez. // Br. J. Dermatol. — 1998. — Vol. 139 (suppl. 52). — P. 3—7.
12. Swinyer L. J., Baker M. D, Swinyer T. A., Mills O. H. Jr. // Br. J. Dermatol. — 1988. — Vol. 119, N 5. — P. 615—622.
Акне являются андрогензависимым поражением пилосебоцейного комплекса, в связи с чем представляется оправданным использование комбинированных оральных контрацептивов, содержащих прогестины с антиандрогенной активностью, для лечения этого заболевания в сочетании с другими методами терапии. В статье приводится физиологическое обоснование использования препаратов, содержащих диеногест при лечениии акне.
Ключевые слова: акне, комбинированные оральные контрацептивы, диеногест.
Акне являются андрогензависимым поражением пилосебоцейного комплекса, манифестируют, как правило, во время адренархе в возрасте 8–10 лет, клинические проявления достигают пика в возрасте около 17 лет. Все женщины страдали этим заболеванием в тот или иной момент подросткового периода [1]. Хотя акне традиционно считается проблемой пубертата, у взрослых женщин они встречаются достаточно часто. Так, по данным A.C. Perkins и соавт., 45% женщин в возрасте 21–30 лет, 26% в возрасте 31–40 лет и 12% в возрасте 41–50 лет страдают акне [2].
Негативный психосоциальный эффект акне неоспорим, а влияние этого заболевания на качество жизни сравнимо с таковым при бронхиальной астме, сахарном диабете и эпилепсии [3]. Среди взрослых с тяжелым течением акне уровень безработицы выше в сравнении с их здоровыми сверстниками [4]. Тяжелое течение заболевания может привести в последствии к рубцеванию и выраженным пожизненным косметическим дефектам.
Патогенез акне
В патогенезе акне основную роль играют такие факторы, как увеличение продукции кожного сала, гиперколонизация Propionibacterium acnes, гиперпролиферация/гиперкератоз устья (воронки) пило-себоцейного комплекса и воспаление. В последние годы появились данные, свидетельствующие о том, что воспалительные явления предшествуют развитию гиперкератинизации волосяного фолликула. В экспериментах было показано, что интерлейкин-1α стимулирует образование комедонов вне зависимости от колонизации Propionibacterium acnes. Наследственные факторы, избыток андрогенов, липиды пищи, курение могут влиять на функцию себоцитов и стимулировать подобное преклиническое стерильное воспаление [1, 5].
Продукция кожного сала увеличивается в результате физиологического и патологического изменения секреции андрогенов. У женщины источниками андрогенов являются в первую очередь яичники и надпочечники. Акне чаще всего манифестирует в период адренархе, когда надпочечник начинает синтезировать в больших количествах дегидроэпиандростерон. Кроме того, акне может развиваться при заболеваниях, сопровождающихся избытком андрогенов, таких как синдром поликистозных яичников, неклассическая форма врожденной дисфункции коры надпочечников, синдром HAIRAN, андрогенпродуцирующие опухоли. Вспышки акне также наблюдаются в периоды стресса, который сопровождается увеличением продукции адреналовых андрогенов [1]. В пилосебоцейном комплексе есть все необходимые ферменты как для синтеза андрогенов de novo, так и для периферической конверсии 17-кетостероидов в тестостерон, 50% которого у женщин образуется именно этим путем. В культуре клеток себоцитов было показано, что анд-рогены вызывают дозозависимую пролиферацию себоцитов, а липогенная активность определяется лигандами рецепторов, активируемых пролифераторами пероксисом (peroxisome proliferator-activated receptor, PPAR), в частности линолевой кислотой. Чувствительность дериватов кожи к андрогенам обусловлена не только наличием в них андрогеновых рецепторов, но и активностью фермента 5α-редуктазы, которая обеспечивает периферическую конверсию тестостерона в его более активный метаболит дигидротестостерон. В культуре клеток себоцитов было продемонстрировано, что тестостерон увеличивает продукцию 5α-дигидротестостерона. Таким образом, PPAR и его лиганды являются кофакторами, необходимыми для полноты развития эффекта андрогенов в отношении сальной железы [6, 7].
Методы лечения акне
Учитывая мультифакторность патогенеза акне, сочетание нескольких методов терапии зачастую приводит к оптимальному результату вследствие воздействия на большее количество механизмов его развития. Наружная терапия назначается больным независимо от степени тяжести заболевания, в том числе в комбинации системной терапией. Для системной терапии акне применяют антибиотики, ретиноиды и гормональные препараты; и именно две последние группы обеспечивают снижение продукции кожного сала. У женщин с акне и другими симптомами гиперандрогении и/или гиперандрогенемией патогенетически обоснованным представляется назначение гормональной терапии.
Основной целью гормональной терапии является снижение продукции кожного сала, однако она также может играть роль в уменьшении гиперкератинизации волосяного фолликула.
Комбинированные оральные контрацептивы (КОК) включают эстрогеновый компонент (в большинстве случаев этинилэстрадиол) и прогестиновый компонент, который может варьировать. Эстрогены уменьшают продукцию кожного сала, действуя как локально, на уровне сальных желез, так и системно. Во-первых, эстрогены способны регулировать гены, вовлеченные в продукцию себума и рост сальных желез [8]. Во-вторых, они снижают овариальную продукцию андрогенов за счет подавления секреции гонадотропинов. В-третьих, эстрогены увеличивают синтез глобулина, связывающего половые гормоны в печени [1].
Следует помнить о том, что КОК являются препаратами второй линии терапии вне зависимости от гормональных нарушений [9]. При этом необходимо учитывать тот факт, что при беременности противопоказаны почти все препараты топического действия (за исключением азелаиновой кислоты), тетрациклины, а также изотретиноин, что требует использования надежных методов контрацепции у женщин репродуктивного возраста [10]. В систематическом обзоре А.О. Arowojolu и соавт. было показано, что КОК эффективны в отношении как воспалительных, так и невоспалительных форм акне, на фоне их приема уменьшается число поражений и степень их выраженности. Различия в сравнительной эффективности КОК, содержащих различные типы и дозы прогестинов, не столь очевидны [11]. Согласно рекомендациям Европейского дерматологического форума (European Dermatology Forum, EDF) системные антиандрогены не рекомендуются для лечения комедональных акне, а также легкой и среднетяжелой степени папуло-пустулезной формы заболевания. Назначение антиандрогенов оправдано в сочетании с системной антибактериальной или топической терапией при тяжелой степени папуло-пустулезных акне, а при конглобатной форме заболевания – только в сочетании с системной антибиотикотерапией [5].
Большинство прогестинов, входящих в состав в КОК, являются дериватами тестостерона и обладают андрогенной активностью. Реализация андрогенного эффекта синтетических прогестинов обусловлена повышением свободного тестостерона в крови, что связано со следующими механизмами: связыванием и активацией рецепторов к андрогенам из-за структурного сходства с тестостероном, вытеснением тестостерона из связи с глобулином, связывающим половые гормоны; угнетением синтеза глобулина, связывающего половые гормоны в печени. Остаточный андрогенный эффект нежелателен, так как нивелирует положительное влияние эстрогенов и клинически может проявляться в появлении андрогензави-симых симптомов, неблагоприятном изменении липидного спектра крови, ухудшении толерантности к глюкозе, увеличении массы тела вследствие анаболического действия.
Эволюция прогестинов проходила по пути увеличения селективности и снижения андрогенной активности, которая у их представителей III поколения, таких как дезогестрел и гестоден, сведена к минимуму. Некоторые прогестины, в том числе ципротерона ацетат и дроспиренон, не являются производными тестостерона и действуют как антагонисты андрогеновых рецепторов. Прогестаген IV поколения диеногест является производным 19-нортестостерона, однако в его составе отсутствует этиниловая группа в позиции С-17 и имеется дополнительная двойная связь в «В» кольце (С 9-10), что придало ему ряд специфических свойств. Он обладает выраженной гестагенной активностью, сравнимой с таковой 19-нортестостерона, при этом у него нет эстрогенной, глюкокортикоидной и андрогенной активности. Уникальная особенность гибридных гестагенов, к которым относится диеногест, заключается в том, что они объединили преимущества 19-норстероидов и производных прогестерона.
Для первых характерны следующие положительные качества: высокая биодоступность при приеме внутрь, короткий плазменный период полувыведения, выраженный гестагенный эффект на эндометрий, надежное подавление овуляции. Преимущества производных прогестерона заключаются в отсутствии андрогенного эффекта, метаболической нейтральности и минимальной способности к связыванию с глобулином, связывающим половые гормоны. Диеногест не связывается с этим типом транспортных белков, не вытесняет тестостерон из связи с ним, что безусловно усиливает его антиандрогенные свойства. В фармакологических тестах Хершбергера in vivo оценивалась антиандроген-ная активность прогестинов относительно таковой ципротеронацетата, которая была принята за 100%. Диеногест обладал наиболее выраженным антиандро-генным эффектом, который составил 40%, дроспиренон и хлормадинона ацетат характеризовались менее выраженной антиандрогенной активностью, которая составила 30 и 20% соответственно [12]. Что касается клинической эффективности диеногест-содержащих КОК в отношении акне, то в двойном слепом рандомизированном контролируемом исследовании они были сравнимы с ципротерона ацета-содержащим КОК и достоверно значимо эффективнее плацебо [13]. Эти данные подтверждают целесообразность использования КОК, содержащих диеногест, у женщин со склонностью к акне.
Что касается применения КОК в педиатрической популяции, то основной вопрос состоит в том, какой возраст начала их приема можно считать безопасным. Согласно рекомендациям Американского общества акне и розацеа, которые были одобрены Американской академией педиатрии, КОК могут назначаться девушкам пубертатного возраста, страдающих среднетяжелыми и тяжелыми формами акне, в качестве терапии второй линии. В связи с опасениями в отношении роста и минеральной плотности костной ткани многие эксперты рекомендуют воздерживаться от назначения КОК с целью лечения акне, не ассоциированного с эндокринной патологией, до момента истечения 1 года после менархе [14].
Заключение
Таким образом, учитывая тот факт, что акне является андрогензависимым заболеванием, патогенетически обоснованным представляется назначение гормональной терапии, которая, однако, не может быть самостоятельным методом лечения. При этом у женщин репродуктивного возраста, страдающих акне, может возникнуть необходимость в надежной контрацепции, которую могут обеспечить КОК, и именно этому методу контроля фертильности следует отдать предпочтение в данной клинической ситуации.
При выборе препарата предпочтение следует отдавать КОК, содержащим прогестины последнего поколения, обладающие метаболической нейтральностью и антиандрогенной активностью, каковым и является диеногест.
Сведения об авторе:
Гродницкая Елена Эдуардовна, к.м.н., врач акушер-гинеколог консультативно-диагностического отделения ГБУЗ Центр планирования семьи и репродукции Департамента здравоохранения г. Москвы.
Адрес: 117209, Россия, Москва, Севастопольский проспект, д. 24А.
Литература/references
1. Salvaggio H.L., Zaenglein A.L. Examining the use of oral contraceptives in the management of acne. Int. J. Womens Health. 2010; 2: 69-76.
2. Perkins A.C., Maglione J., Hillebrand G.G., Miyamoto K., Kimball A.B. Acne vulgaris in women: prevalence across the life span. J. Womens Health (Larchmt). 2012; 21(2): 223-30.
3. Mallon E., Newton J.N., Klassen A., Stewart-Brown S.L., Ryan T.J., Finlay A.Y. The quality of life in acne: a comparison with general medical conditions using generic questionnaires. Br. J. Dermatol. 1999; 140(4): 672-6.
4. Cunliffe W.J. Acne and unemployment. Br. J. Dermatol. 1986; 115(3): 386.
5. Nast A., Dréno B., Bettoli V., Degitz K., Erdmann R., Finlay A.Y. et al.; European Dermatology Forum. European evidence-based (S3) guidelines for the treatment of acne. J. Eur. Acad. Dermatol. Venereol. 2012; 26 (Suppl. 1): 1-29.
6. Chen W., Yang C.C., Sheu H.M., Seltmann H., Zouboulis C.C. Expression of peroxisome proliferator-activated receptor and CCAAT/enhancer binding protein transcription factors in cultured human sebocytes. J. Invest. Dermatol. 2003; 121(3): 441-7.
7. Rosenfield R.L., Deplewski D., Kentsis A., Ciletti N. Mechanisms of androgen induction of sebocyte differentiation. Dermatology. 1998; 196(1): 43-6.
8. Thiboutot D., Chen W. Update and future of hormonal therapy in acne. Dermatology. 2003; 206(1): 57-67.
9. Kraft J., Freiman A. Management of acne. Can. Med. Assoc. J. 2011; 183(7): E430-5.
10. Whitney K.M., Ditre C.M. Management strategies for acne vulgaris. Clin. Cosmet. Investig. Dermatol. 2011; 4: 41-53.
11. Arowojolu A.O., Gallo M.F., Lopez L.M., Grimes D.A. Combined oral contraceptive pills for treatment of acne. Cochrane Database Syst. Rev. 2012; (6): CD004425.
12. Oettel M., Bervoas-Martin S., Elger W. , Golbs S., Hobe G., Kaufmann G. et al. A 19-norprogestin without 17α-ethinyl group II: Dienogest from a pharma-cokinetic point of view. Drugs Today. 1995; 31(7): 499-516.
13. Palombo-Kinne E., Schellschmidt I., Schumacher U., Gräser T. Efficacy of a combined oral contraceptive containing 0.030 mg ethinylestradiol/2 mg dienogest for the treatment of papulopustular acne in comparison with placebo and 0.035 mg ethinylestradiol/2 mg cyproterone acetate. Contraception. 2009; 79(4): 282-9.
14. Eichenfield L.F., Krakowski A.C., Piggott C., Del Rosso J., Baldwin H., Friedlander S.F. et al.; American Acne and Rosacea Society. Evidence-based recommendations for the diagnosis and treatment of pediatric acne. Pediatrics. 2013; 131(Suppl. 3): S163-86.
С. Остапенко
Медико-санитарная часть №5, Самара Сотрет (изотретиноин) – эффективное медикаментозное средство для системной терапии акне, действующее на все основные звенья патогенеза заболевания: образование кожного сала, комедогенез, колонизацию P. acnes. Прием препарата рекомендуется при среднетяжелых и тяжелых формах акне, высокой степени рубцевания, отсутствии эффекта традиционных методов лечения.
Ключевые слова: акне, системные ретиноиды, Сотрет.
Experience with Sotret in patients with moderate and severe acne
S. Ostapenko
Medical Sanitary Unit Five, Samara Sotret (isotretinoin) is an effective medication for systemic therapy of acne, which acts on the basic components of the pathogenesis of the disease: sebum production, comedogenesis, and P. acnes colonization. The drug is recommended in cases of moderate-to-severe acne, high scarring, and ineffective traditional treatments.
Key words: acne, systemic retinoids, Sotret.
Акне (вульгарные угри) – хроническое кожное заболевание, которое является самой распространенной дерматологической патологией в подростковом периоде. В 30% случаев угревая сыпь сохраняется и в зрелом возрасте. Более чем в 1/3 случаев это заболевание требует длительного лечения.
Наиболее часто при акне поражаются лицо и верхняя часть шеи, но в процесс могут быть вовлечены также грудь, спина и плечи. На коже появляются элементы сыпи – папулы, пустулы, кисты и др. В лечении акне используют местные бактерицидные средства (при легких формах – препараты, содержащие бензоилпероксид, менее эффективен триклозан), антибиотики (наружно применяются доксициклин, эритромицин, клиндамицин, спирамицин или антибиотики тетрациклинового ряда). У женщин эффективна гормональная терапия акне – применяют комбинированные препараты эстрогена и прогестогена. Наиболее эффективен ципротерон в сочетании с эстрогеном; можно использовать спиронолактон (особенно у больных с синдромом поликистоза яичника, а также локальные инъекции кортизона). В настоящее время разрабатываются новые концепции и перспективы в лечении акне, предусматривающие возможность использования генетических методов лечения. Ученые ищут возможные гены, ответственные за данную патологию; планируется также использование фагов, элиминирующих бактерии.
Ретиноиды – производные (изомеры) витамина А (третиноин, изотретиноин, адапален, тазаротен) влияют на жизненный цикл клеток кожи и таким образом нормализируют кератинизацию и десквамацию эпителиальных клеток. Для местного применения используют гели, содержащие ретиноиды: Эффезел (адапален и бензоила пероксид, оказывающий противомикробное действие и не вызывающий резистентности), Клензит (адапален), Изотрексин (включающий изотретиноин и антибиотик эритромицин). Показано, что эритромицин в сочетании с изотретиноином эффективен против эритромицинрезистентных штаммов Propionibacterium acnes, однако препараты с адапаленом (по данным Global Alliance to Improve Outcomes in Acne) являются препаратами 1-го выбора при лечении акне.
Для терапии тяжелых и резистентных форм акне ретиноиды применяют внутрь. Синтетическое производное витамина А – изотретиноин (13-cis ретиновая кислота, Сотрет) считается самым эффективным средством для системного лечения акне. Оптимальной ежедневной дозой считается 0,5 мг на 1 кг массы тела; при приеме лекарства в такой дозировке улучшение наблюдается уже через 2–4 нед. Реакция на терапию примерно у 50% пациентов сопровождается кратковременным ухудшением состояния кожи, связанным с высвобождением филаментов и воспалительным преобразованием комедонов. Повышение дозы до 1 мг/кг показано при тяжелой себорее, выраженном конглобатном акне или при локализации акне на туловище. Более низкие суточные дозы (0,2 мг/кг) также эффективны, однако необходима более длительная терапия, иначе количество рецидивов существенно увеличивается.
Изотретиноин является единственным терапевтическим средством лечения акне, которое влияет на 4 главных звена патогенеза заболевания: себорею, нарушения ороговения, воспаление и размножение бактерий P. acnes. Он интенсивно снижает секрецию сальных желез, одновременно уменьшая их, причем не обладает гормональным эффектом. Препарат устраняет инфраинфундибулярный ретенционный гиперкератоз и оказывает противовоспалительное действие. Кроме того, он подавляет бактериальную кожную флору в рамках себостатического эффекта, не обладая антибактериальной активностью. Изотретиноин также характеризуется иммуномодулирующими свойствами.
При акне происходят качественные и количественные изменения продукции кожного сала сальными железами и нарушения кератинизации в сально-волосяных протоках. Эти процессы контролируются нейрогуморальными механизмами. Среди гормональных нарушений наиболее важен уровень продукции андрогенов в организме. В результате возросшего влияния андрогенов на сально-волосяные фолликулы в андрогензависимых участках кожного покрова (лицо, спина, грудь, плечи) отмечаются избыточная продукция кожного сала в сальных железах, а также повышенная адгезия корнеоцитов, выстилающих сально-волосяные протоки, что затрудняет их десквамацию в просвет протока. Эти нарушения влекут за собой замедление или прекращение перемещения кожного сала и ороговевших клеточных масс по протоку. В результате происходит его закупорка, что клинически проявляется формированием открытых и (или) закрытых комедонов. В таких условиях создается благоприятная среда для роста и размножения бактериальной флоры (P. acnes, Staphylococcus epidermidis), что, в свою очередь, способствует развитию реактивного и иммунного воспаления в окружающей дерме. Клинически это проявляется образованием воспалительных элементов акне разной степени тяжести (папулы, пустулы, узлы, кисты, конглобатные, абсцедирующие, флегмонозные угри).
Нами изучена эффективность изотретиноина (Сотрета) как препарата для системной терапии среднетяжелых и тяжелых форм акне. Под наблюдением находились 18 пациентов с акне. Диагностическое обследование включало:
- выяснение анамнеза заболевания (наследственная предрасположенность; длительность заболевания; факторы, обострившие или спровоцировавшие появление угревой сыпи; предшествующая терапия акне; сопутствующая кожная и соматическая патология);
- клиническую оценку с определением формы и тяжести течения заболевания на основе анализа патологических элементов, их количества и локализации;
- выявление осложнений в виде рубцевания и пигментации кожи.
Дополнительно проводили: общий анализ крови; биохимический анализ крови (содержание билирубина, холестерина, β-липопротеидов, липидов, триглицеридов аланин- и аспартатаминотрансферазы, щелочной фосфатазы, креатинина, мочевины, глюкозы); у женщин – тест на беременность.
Больные были в возрасте от 19 до 26 лет: 8 пациентов мужского пола (2 больных – от 19 до 20 лет; 1 – 20 лет, 2 – 22 лет, 2 – 23 года и 1 – 25 лет) и 10 – женского (3 – в возрасте 19 лет, 2 – 20 лет, 2 – 21 года, 1 – 23 лет и 2 – 26 лет).
Длительность акне от 2 до 3 лет отмечалась у 5 пациентов; в пределах 4–6 лет – у 8; в 5 случаях угри существовали около 10 лет. На сезонное обострение акне (ухудшение состояния кожи в зимнее время) указали 12 больных.
Генетическая предрасположенность к заболеванию отмечена у 11 пациентов: у 4 обследованных акне страдала мать, у 3 – отец, у 2 – сестра и у 2 – брат. Обострение угревой сыпи на фоне нервно-психических перегрузок отметили 4 пациента, после переохлаждения – 2, в результате погрешностей в диете – 5.
Предшествующая терапия акне включала системное лечение до 1 мес доксициклином (у 5), рифампицином (у 1), витаминами группы В (у 3); крем Ретин А местно применяли 3 пациента, растворы салициловой кислоты – 4, гель бензоилпероксид – 6, солнцезащитные кремы – 3. Таким образом, 6 больных никогда не использовали системных препаратов для лечения акне. У 2 пациентов отмечен раздражающий эффект Ретина А и у 4 – салициловой кислоты (жжение и зуд).
Основными критериями для выбора Сотрета в качестве препарата для системной терапии были:
- среднетяжелое, тяжелое и очень тяжелое течение акне;
- тяжелые формы угревой сыпи (узловато-кистозная, конглобатная, абсцедирующая) с распространенной и генерализованной локализацией патологических элементов;
- высокая частота рубцевания, в том числе наличие келоидных рубцов;
- отсутствие выраженного эффекта от предыдущего лечения акне с использованием системных антибиотиков и комбинированной местной терапии.
Сотрет назначали с учетом массы тела пациента из расчета 0,5 мг/кг в сутки, что составляло 20–40 мг/сут. Длительность курса терапии – от 5 до 8 мес (в зависимости от выраженности клинического эффекта). Больным, которые применяли препарат более 2 мес, снижали дозу на 0,1 мг/кг в сутки ежемесячно. До начала лечения и ежемесячно в процессе терапии проводили клинико-лабораторный мониторинг биохимических показателей сыворотки крови для исключения лабораторных признаков заболеваний печени, почек, гиперлипидемии, сахарного диабета.
В зависимости от клинических проявлений акне в качестве местных препаратов 6 пациентов использовали крем Скинорен, 12 – гамма эфаклар, 16 – солнцезащитный крем с фактором защиты 50.
Клинический контроль проводили ежемесячно с учетом уменьшения количества патологических элементов, а также снижения степени тяжести акне и выраженности рубцовых изменений.
У всех пациентов наблюдались побочные эффекты в виде сухости кожи, слизистых оболочек глаз, губ. Однако эти явления легко устранялись с помощью увлажняющих кремов. У 2 пациентов в 1-й месяц приема Сотрета появились носовые кровотечения, но после снижения дозы препарата они прекратились. Клиническое улучшение было достигнуто у всех пациентов уже через 1 мес после начала приема Сотрета с регрессом патологических элементов на 30–35%. После 2 мес лечения наблюдался значительный эффект с регрессом патологических элементов на 55–60%. У 4 пациентов с тяжелым течением акне улучшение на 70–75% наступило через 3 мес терапии. У 9 пациентов (у 3 – очень тяжелое течение и у 6 – тяжелое) прием препарата был продлен до 8 мес. Клинический эффект в виде улучшения в этой группе составил 80%. Кроме уменьшения количества элементов, снижались частота и выраженность рубцовых изменений, а также степень тяжести акне (рис. 1, 2).
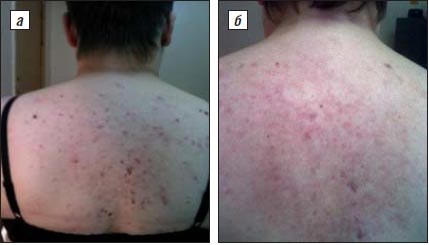
Рис. 1. Элементы сыпи при акне у больной А., 24 лет (узловатые акне тяжелой степени, конглобатные акне, IV степень тяжести, по классификации из Европейского руководства по лечению акне, 2012 г.):
а – до лечения; б – после лечения
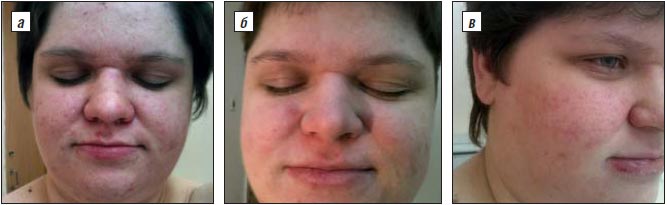
Рис. 2. Проявления акне у больной В., 26 лет (тяжелые папулопустулезные акне, III степень тяжести):
а – до лечения; б – в ходе терапии; в – после лечения
Полученные результаты показали, что изотретиноин (Сотрет) оказывает выраженное себостатическое действие и уменьшает количество P. acnes. Подавление секреции кожного сала (на 85%) происходит за счет сокращения размеров сальной железы (на 50–90%), снижения выраженности воспалительной реакции в этой области. Плотность заселения бактериями P. acnes сально-волосяного аппарата уменьшается на несколько порядков. Изотретиноин снижает сцепление кератиноцитов в сальных фолликулах, препятствуя таким образом формированию микрокомедонов, инициирующих воспалительный процесс.
Таким образом, Сотрет (изотретиноин) является эффективным медикаментозным средством для системной терапии среднетяжелых и тяжелых форм акне. Препарат действует на все основные звенья патогенеза акне – образование кожного сала, комедогенез, колонизацию P. acnes.
Прием Сотрета рекомендуется при среднетяжелых и тяжелых формах акне, высокой степени рубцевания, отсутствии значительного клинического эффекта традиционных методов лечения угревой сыпи.

A кне – хроническое воспалительное заболевание сальных желез, известное большинству женщин как прыщи.
Проблема акне касается далеко не только подростков. Так, до 22% женщин старше 25 лет страдают от этого заболевания.
Причины акне
Причины многообразны, но в основе развития заболевания лежат:
- гипекератоз (патологическое утолщение рогового слоя эпидермиса),
- размножение бактерии Propionibacterium acnes,
- увеличенная выработка кожного сала и
- воспалительный ответ как реакция на все вышеперечисленное.
Ряд факторов способствуют появлению акне:
- погрешности в диете,
- генетическая предрасположенность,
- эндокринные нарушения (в частности, гиперандрогения — повышение выработки и/или активности мужских половых гормонов у женщины),
- и другие.
Варианты лечения акне
Существуют разнообразные варианты лечения, и чаще всего используется комплексный подход. К основным вариантам лечения относятся:
- Многообразие препаратов, наносимых на кожу (лосьоны/гели/кремы/мази/суспензии и т.д.),
- Антибиотики,
- Гормональные препараты,
- Ретиноиды,
- Физическое воздействие на очаги воспаления (лазер/химический пилинг и другие варианты),
- Альтернативные подходы (народная медицина, гипноз и др.).
Гормональные препараты при лечении акне
Почему же при выборе способа лечения все чаще обращаются к гормональным препаратам?
- примерно у 80% пациентов антибактериальная терапия оказывается неудачной,
- примерно у 30% пациенток возможен рецидив акне после терапии ретиноидами,
- акне могут являться симптомом некоторых гинекологических заболеваний (синдром поликистозных яичников, например), требующих назначения гормональных препаратов, а не самостоятельным заболеванием.
Учитывая, что гиперандрогения является одним из важнейших факторов развития акне, логично использовать для лечения этого заболевания препараты с антиандрогенным эффектом (то есть препараты, снижающие содержание андрогенов в крови). Однако есть данные, подтверждающие, что гормональные препараты эффективны и у пациенток с исходно нормальным уровнем мужских гормонов. Комбинированные контрацептивы (КОК) входят в возможные схемы терапии последних международных руководств по лечению акне (в составе комплексной терапии).
Возможно применение различных гормональных препаратов при лечении акне. В этой статье мы остановимся на эффектах КОК.
Многие комбинированные контрацептивы могут применяться при лечении акне благодаря своей способности уменьшать уровень мужских половых гормонов в крови.
Каким образом обеспечивается антиандрогенный эффект КОК?
- эстроген, входящий в состав КОК, стимулирует выработку глобулина, связывающего половые гормоны, в печени, который, в свою очередь, связывает андрогены, снижая уровень тестостерона и дегидроэпиандростерон-сульфата (ДГЭА-С);
- эстроген, входящий в состав КОК, снижает выработку гонадотропинов гипофиза, в результате чего падает продукция адрогенов в яичниках и надпочечниках.
Каков принцип назначения КОК при акне?
Следует рассмотреть возможность и необходимость назначения КОК в следующих ситуациях:
- доказанная гиперандрогения (повышение уровня мужских половых гормонов),
- позднее начало акне (в 25 лет и старше),
- локализация, главным образом, в области нижней челюсти,
- «волнообразное» течение акне, совпадающее с менструальным циклом,
- комедоны + себорея,
- неэффективность других подходов к лечению акне.
Что стоит учитывать при планировании гормональной терапии?
- Несмотря на многообразие вариантов КОК, при сравнении с плацебо все варианты КОК (третьего поколения и далее) демонстрируют хорошую эффективность у большинства пациенток;
- Вариантов КОК много, но пока ни один из современных препаратов (третьего поколения и далее) не отличился в научных исследованиях как самый удачный и самый лучший в отношении акне;
- Для достижения эффекта необходим прием препарата в течение 3-6 месяцев (не меньше);
- Возможно ухудшение состояния в первые месяцы приема;
- Возможны разнообразные побочные эффекты и нежелательные явления, поэтому недопустимо самостоятельное назначение КОК;
- Возможно возобновление симптомов после отмены препарата.
Важно помнить, что первые поколения КОК содержали прогестиновый компонент с андрогенным эффектом, а потому могли усугублять проблему акне.
При выборе КОК с целью лечения акне следует отдавать предпочтение препаратам с антиандрогенным действием.
Еще один интересный аспект: несмотря на многообразие КОК, продемонстрировавших свою эффективность в терапии акне, только три препарата одобрены FDA для лечения акне (т.е. лечение акне указано в инструкции на основании имеющихся доказательств), и не все эти препараты представлены в России.
Проблема прыщей знакома многим женщинам, они могут появиться в любом возрасте, быть более или менее выраженными, проходить самостоятельно в короткие сроки или с ним необходимо долго и скрупулезно бороться. Причин появления прыщей множество, серьезную опасность представляют гормональные угри. В статье разберем, причины прыщей на лице у женщин, как они выглядят, из-за каких гормонов появляются, как избавиться от них и другую полезную информацию.
Что такое гормональные прыщи
Кожа является самым большим органом тела человека, она реагирует не только на внешние раздражители, но и на внутренние. Различные сбои в работе внутренних органов и систем могут отражаться на коже. Прыщи - важный сигнал для анализа образа жизни и поведения. Некоторые виды воспалений связаны с изменениями в организме (половое созревание, беременность), когда организм перестроится, то они пройдут сами, но другие могут быть сигналом о неполадках.

Чаще всего прыщи на лице у женщин возникают из-за гормонального сбоя, когда одних гормонов становится по какой-либо причине больше, а другие угнетаются.
Прыщи из-за гормонов могут называть по-разному: предменструальные, гиперандрогенные, постменопаузальные, ранние, поздние и т.п. Однако все они говорят о серьезном сбое в организме и требуют лечения.
Гормональное акне может иметь различный вид, у кого-то это имеет более выраженную природу, у кого-то менее, это зависит от запущенности и серьезности происходящих в организме перестроек. В запущенных случаях можно видеть прыщи на челюсти у женщины, на щеках, шее, плечах и груди.
Опасность прыщей не только в причине их появления, но и в том что они могут вызвать серьезные проблемы самой кожи: пустулы, комедоны, милиумы, кистозные шишки, гнойные образования и даже заражение крови.
Отсутствие правильного лечения самой кожи и параллельное устранение причины их появления будет только усугублять проблему: под действием гормонов кожное сало будет вырабатываться постоянно и все в большем количестве, клетки будут стараться обновляться быстрее и отмершие их части будут еще больше забивать поры, кожа становится толще, чувствительнее, увеличивается жизнедеятельность бактерий.
Какие прыщи при гормональном сбое
Прыщи, акне, угревая сыпь - человеку, далекому от медицины тяжело разобраться в разнице между этими понятиями. Заподозрить у себя гормональные прыщи, можно по таким признакам:
- множество комедонов открытых или закрытых;
- воспаленные участки на лице;
- сыпь;
- глубокие рубцы после некоторых видов прыщей;
- если наблюдается излишнее выделение кожного сала на лице;
- излишняя волосатость (на лице или теле).

Причины гормонального сбоя
Женская гормональная система очень подвижна, на нее влияет множество факторов, от внутреннего состояния до факторов окружающей среды. Каждый месяц гормональная система женщины проходит один и тот же путь изменения концентрации гормонов в зависимости от дня цикла. Колебание любого гормона может вызвать изменение работы всей системы и в итоге гормональный сбой, который может стать причиной возникновения прыщей на лице у женщины.
Гормональные прыщи у взрослой женщины на лице не редкость. Известно, что ими страдает до половины всех женщин репродуктивного возраста, и могут они появиться в любой период: после 30 лет, в подростковый период, в 25 лет и т.д.
Основные причины, провоцирующие гормональный сбой:
- излишняя физическая активность;
- набор веса, ожирение;
- плохое питание, скудный рацион;
- злоупотребление вредными привычками (курение, алкоголь);
- прием некоторых лекарственных препаратов;
- патологии щитовидной железы, яичников, надпочечников, гипоталамуса или других органов;
- стресс;
- наследственные факторы и другое.
В зависимости от причины повлекшей сбой гормональной системы будет формироваться лечение.

Какие гормоны влияют на прыщи
Существует два типа гормонов: мужские (андрогены) и женские (эстрогены). В женском организме в большом количестве содержатся эстрогены, а в мужском андрогены. Если у женщины мужские половые гормоны начинают вырабатываться в большем количестве, чем нужно, то происходит сбой, который ведет к проблемам с репродуктивной функцией, прыщами и излишним ростом волос на теле.
Наибольшее влияние на образование прыщей у взрослых женщин играют:
- дигидротестостерон - при его избытке увеличивается чувствительность рецепторов сальных желез;
- прогестерон - влияет на силу течения болезни;
- тестостерон - увеличивает выработку кожного сала, которое не успевает утилизироваться и забивает поры, а они и так могут быть чувствительны из-за дигидротестостерона;
- пролактин - снижает выработку эстрогенов, тем самым провоцируя излишнее образование андрогенов.

Диагностика
Так как причин, почему на лице у женщин появляются прыщи, множество, то перед тем, как принимать какие-либо действия по лечению, необходимо точно выяснить причину и начать с ее устранения.
В первую очередь необходимо обратиться к врачу, это может быть один из специалистов: врач-дерматолог, врач-эндокринолог, врач-гинеколог. Специалист сможет оценить состояние кожи, предположит причины появления и назначит необходимые исследования. Стандартными методами диагностики, если у женщины прыщи являются:
- сдача крови на половые гормоны и гормоны щитовидной железы;
- ультразвуковое исследование органов малого таза и щитовидной железы;
- общий и биохимический анализ крови;
- анализ мочи.
Исходя из полученных данных будет назначено лечение, либо консультация специалиста другой области, либо рекомендовано проведение дополнительного обследования, например МРТ надпочечников или другое.

Как лечить гормональные прыщи
К лечению необходимо подходить комплексно. Кроме того что специалист после выявления причины повлекшей гормональный сбой и прыщи назначит препараты и процедуры для их лечения, необходим правильный уход за кожей, коррекция питания и образа жизни.

Главное правило: не пытайтесь давить воспаления! Лицо имеет множество неглубоко расположенных сосудов, инфекция, которая попадет в них мигом разбежится по всему лицу и усугубит ситуацию.
Часто используемые вспомогательные методы лечения при любых причинах появления прыщей на лице у женщины:
- рацион питания - снизить потребление продуктов, вызывающих большой выброс сахара (мучные изделия, молочные продукты, простые сахара и т.п.);
- ретиноиды - серьезные препараты с большой концентрацией витамина А, они местно предотвращают образование новых прыщей и воспалений;
- кислоты - помогают эффективно избавляться от отмерших клеток, проникают внутрь воспаления и немного растворяют его содержимое, подходят не всем типам кожи;
- гидрокортизон - обычно в виде крема с небольшим содержанием стероидов, который помогает снимать воспаление, пользоваться им долго нельзя;
- изотретиноин - препарат, который блокирует выработку кожного сала, используется при серьезных степенях поражения тканей с имеющимися признаками рубцевания;
- спиронолактон - препарат, который способствует уменьшению выработки мужских половых гормонов.
Лечение гормональных прыщей должно проводиться под надзором врача, уход за кожей и косметологические процедуры также лучше обсуждать со специалистом, который, опираясь на свои знания, тип кожи пациента и его анамнез сможет в короткие сроки добиться положительной динамики.

К какому специалисту обратиться
Большинство причин образования гормональных прыщей может лечить эндокринолог. Я, Романов Георгий Никитич, врач-эндокринолог с 20-летним стажем помог не одному своему пациенту избавиться от гормональных причин. Я имею богатый опыт работы, современные знания в области эндокринологии. Если Вам необходима консультация специалиста по вопросам диагностики или лечения, то у меня доступна услуга онлайн-консультации, где я уделяю максимум времени и внимания пациенту, его проблеме. Записаться на консультацию можно напрямую в одном из предложенных источниках: Viber, Telegram, Instagram, WhatsApp, Skype, Вконтакте.
Читайте также:


