Как выглядит на коже грибок кандида
Обновлено: 23.04.2024
Грибковый вагинит (в народе – молочница) очень распространен и составляет от 25 до 35% всех вагинитов. В 80–90% случаев воспаление вызывается Candida Albicans, диморфным грибком, встречающимся у человека в двух формах: бластоспоры и мицелий. В 5-20% случаев возбудителями грибкового вагинита являются Candida Glabrata и Candida Tropicalis.
Candida albicans является условно-патогенным грибком, потому что у 20-25% бессимптомных женщин он обнаруживается во влагалище как неотъемлемая часть физиологической микрофлоры.
За исключением области половых путей он также может быть обнаружен в полости рта и прямой кишке. Образует нитчатые (гифы и псевдогифы) и яйцевидные формы (конидии, споры и почки). В отличие от Candida Glabrata не образует нитчатых форм.
Группы риска и пути передачи кандидоза
Можно найти разные данные о кандидозе: одни эксперты классифицируют его как заболевание, передающееся половым путем, а другие не считают его частью этой группы.
Рост грибков чаще всего связан с изменениями уровня эстрогена. Именно поэтому он сильнее всего проявляется после менструации и во время беременности.
Увеличение количества грибков также было обнаружено у тех женщин:
- принимающих высокие дозы гормональных контрацептивов;
- болеющих диабетом;
- беременных;
- после лечения кортикостероидами или антибиотиками, так как нарушается баланс бактерий и увеличивается количество грибков.
Хотя кандидоз чаще является результатом этих состояний, нельзя игнорировать его возможную передачу при незащищенном половом акте. 15% мужчин могут испытывать симптомы баланопостита (воспаление головки полового члена и крайней плоти) после полового акта с женщиной, зараженной этой инфекцией.
Симптомы кандидоза
Симптомы кандидоза у женщин:
- зуд;
- покраснение;
- отек и боль в области влагалища;
- характерные выделения из влагалища – белые, густые, творожистые, без особого запаха;
- боль при мочеиспускании – дизурия, при половом акте – диспареуния.
Симптомы кандидоза у мужчин:
- зуд, жжение и раздражение под крайней плотью или кожей головки;
- покраснениеа под крайней плотью или головкой;
- проблемы с ретракцией крайней плоти;
- редкие или густые творожистые выделения под крайней плотью;
- боль при мочеиспускании.
В результате зуда могут возникнуть ссадины (царапины) и вторичная бактериальная инфекция. Женщинам полезно определять pH влагалища.
Диагностика кандидоза
Диагноз ставится в следующем порядке анализов:
- В анамнезе: зуд, жжение, пациентки в особых состояниях (постменструальный период, беременность, антибактериальная терапия). Воспаление не обязательно должно быть связано с половым актом или партнером.
- Осмотр: покраснение, отек, бляшки.
- Выделения: белые, творожистые, густые, без запаха, pH ниже 4,5.
- Влажный препарат – мазок: уменьшение количества лактобацилл, мало лейкоцитов, мицелия.
- Влажный препарат с добавлением 10-20% раствора КОН: при исчезновении эритроцитов и лейкоцитов легче появляются гифы и псевдогифы.
- Культивирование на специальной среде (Никерсон): более 103 микроорганизмов.
- Слайд-тест латекса: длится 2 мин, чувствительность 75%.
Несмотря на типичный анамнез, вульвовагинальный кандидоз не всегда легко доказать. При исследовании отделяемого (влажный препарат) в 40-50% случаев гифы не обнаруживаются.
Также следует отметить, что Candida Glabrata в 15% случаев не образует гиф.
Лечение кандидоза
Лечение кандидозного вульвовагинита может быть системным или местным, а также часто комбинированным. Считается, что лечение облегчает симптомы в 90% случаев. Однако рецидивы очень часты (от 20 до 40% после 4-6 недель лечения). Всегда полезно лечить обоих партнеров одновременно.
В лечении используются местные и системные противогрибковые препараты. Для местного лечения чаще всего используются нистатин, клотримазол, миконазол, эконазол, а для системного – флуконазол и итраконазол.
Некоторые системные противогрибковые препараты нередко могут быть гепатотоксичными – вызывать повреждение печени. Большинство противогрибковых препаратов (кроме нистатина) надо избегать в первом триместре беременности и во время кормления грудью. К сожалению, нистатин показывает самую слабую степень излечения при беременности (от 70 до 80%).
В случае рецидива, комбинированная терапия системных и местных противогрибковых является обязательной. При устойчивом кандидозе также можно использовать 1% промывание отваром горечавки, борной кислотой или повидон-йодом.
При частых рецидивах молочницы встает вопрос о назначении иммуномодуляторов, поэтому препаратом выбора для местного применения может быть только Гепон. Который подходит для лечения хронического вагинального кандидоза, активизируя клетки для защиты от грибов и усиливает устойчивость к инфекциям, вызванных вирусами и бактериями. У препарата выражен местный противовоспалительный эффект, что подтверждают многочисленные исследования и клинический опыт применения. Уже через два дня использования Гепона 83% пациенток с кандидозом отметили отсутствие красноты, отечности, болезненности и зуда.
В гипоэстрогенных условиях вводятся дополнительные эстрогены.
Системное лечение кандидоза очень эффективно даже при однократном лечении. Согласно анализу результатов, опубликованных в мировой литературе, излечимость кандидоза вне беременности составляет от 80 до 90%.
Естественное исцеление
Хотя лечение фармацевтическими препаратами является наиболее успешным, существуют методы профилактики и лечения естественными средствами. Вредные привычки в еде и образе жизни могут привести к возвращению грибков, поэтому необходимо следующие правила:
Инвазивный кандидоз – это генерализованная грибковая инфекция, при которой наблюдается кандидемия и поражение внутренних органов грибами рода Кандида. До половины случаев заболевания вызвано возбудителем C. albicans, в тройке самых распространенных патогенов находятся C. parapsilosis и C. glabrata. Клинические проявления болезни определяются локализацией очага инфекции и степенью иммунного ответа. Для диагностики назначают серологические и культуральные исследования крови, инструментальные методы визуализации. Лечение требует индивидуального подбора противогрибковых препаратов.
МКБ-10
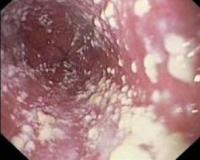


Общие сведения
Инвазивный кандидоз считается одной из самых распространенных инфекций среди госпитализированных пациентов. Ежегодно регистрируется более 250000 случаев, причем эксперты уверены, что истинная встречаемость инфекции намного выше. Заболевание чаще развивается у новорожденных и людей пожилого возраста. Высокая распространенность, неблагоприятный прогноз и сложности своевременной идентификации кандидоза заставляют специалистов искать новые пути диагностики и лечения болезни.

Причины
Возбудитель заболевания – грибы рода Candida, которые принадлежат к семейству Сахаромицеты, классу Аскомицеты. Известно более 20 патогенных для человека видов, однако до 90% случаев инвазивного кандидоза провоцируют только 5 из них: C. albicans, C. glabrata, C. tropicalis, C. parapsilosis и C. krusei. Лидирующее место в России продолжает занимать C. albicans (48%), часто встречаются возбудители C. parapsilosis (17%) и C. glabrata (14%).
Основным фактором риска инвазивного кандидоза является иммунная недостаточность, поскольку все звенья иммунитета участвуют в борьбе с грибковой инфекцией. Заболевание в основном встречается среди пациентов отделений интенсивной терапии, причем возраст больного до 1 года и старше 65 лет резко повышает вероятность грибковой инфекции. Выделяют и другие факторы риска:
- Пересадка внутренних органов. На долю кандидоза приходится более 53% всех инвазивных микозов, которые развиваются у пациентов после трансплантации. Наибольший риск имеет пересадка тонкого кишечника, поджелудочной железы и печени. Грибковая инфекция развивается у 3-4% больных с трансплантированным сердцем, почками, легкими.
- Постановка катетера. Центральный венозный катетер представляет собой оптимальные входные ворота для грибковых возбудителей. В его просвете формируются биопленки из грибов Кандида, которые вызывают катетер-ассоциированную кандидемию. Патология чаще встречается у новорожденных и вызвана видом C. parapsilosis.
- Антибиотикотерапия. Противомикробные препараты широкого спектра действия подавляют полезную микрофлору кишечника, повышают грибковую контаминацию ЖКТ. Наиболее опасными признаны цефалоспорины III поколения, которые в 2 раза увеличивают риск развития микозов.
- Онкопатология. Наибольшему риску подвергаются пациенты с гемобластозами, у которых отмечается выраженная нейтропения, нарушения выработки иммуноглобулинов и патологии системы комплемента. На поздних стадиях солидных опухолей также возрастает вероятность инвазивного кандидоза.
Патогенез
Большинство случаев связано с эндогенным путем передачи инфекции: проникновением грибов через слизистые оболочки желудочно-кишечного тракта либо через поврежденные полые органы брюшной полости. Заражению способствует увеличение грибковой нагрузки в кишечнике на фоне антибиотикотерапии. Реже наблюдается экзогенное инфицирование при инвазивных медицинских манипуляциях (постановка катетера, парентеральное питание, хирургическое вмешательство).
После проникновения грибов Кандида в кровеносную систему развивается кандидемия, обуславливающая гематогенное распространение возбудителя и формирование очагов во внутренних органах. Основным механизмом тканевой инвазии является способность к образованию псевдомицелия, который препятствует поглощению грибов макрофагами. К факторам патогенности относят ферменты (аспартилпротеиназы, фосфолипазы), фенотипическую нестабильность.

Симптомы инвазивного кандидоза
У трети пациентов наблюдается кандидемия без органических патологий внутренних органов, которая не имеет специфических признаков. Основным симптомом присоединения грибковой инвазии является резкий подъем температуры на фоне антибиотикотерапии. Лихорадка зачастую имеет волнообразное течение. При глубоком иммунодефиците проявления системного воспалительного процесса стерты или полностью отсутствуют.
При вовлечении в процесс внутренних органов клиническая картина разнообразна. Поражение органов брюшной полости проявляется классическими признаками перитонита: резкие боли по всему животу, напряжение мышц передней брюшной стенки, многократная тошнота и рвота. Инфицирование мочевых путей сопровождается кандидозным циститом и пиелонефритом. Частным признаком инфекции является пневмония, которая протекает без особенностей.
При установке ликворных шунтов и других инвазивных нейрохирургических манипуляциях возможно поражение ЦНС. Инвазия грибами Кандида чаще всего проявляется менингитом с подострым течением. При воспалении мозговых оболочек возникает сильная головная боль, длительная лихорадка, светобоязнь. Отличием грибкового менингита считается отсутствие ригидности затылочных мышц.
Поражение тканей сердца развивается у пациентов после установки искусственных клапанов. Клинические проявления манифестируют в течение 2 месяцев после операции. Больные страдают от лихорадки, одышки, болей в области сердца. Быстро присоединяются признаки сердечной недостаточности, гепатоспленомегалия, узелки Ослера. Есть риск вовлечения опорно-двигательного аппарата с развитием кандидозного артрита и остеомиелита.
Инвазивный кандидоз у новорожденных характеризуется классической картиной неонатального сепсиса. Возникает заторможенность, отказ от кормлений, одышка с эпизодами апноэ. Характерна сердечно-сосудистая нестабильность, затяжная желтуха. Фебрильная лихорадка наблюдается только в 50% случаев, при этом до 40% пациентов имеют физиологическую норму лейкоцитов крови.
Осложнения
Несмотря на достижения практической инфектологии, летальность при инвазивном кандидозе остается стабильно высокой. У взрослых уровень смертности составляет 40%, среди иммунокомпрометированных больных он может достигать 50-70%. Суммарная детская смертность при инвазивной форме кандидоза варьирует в пределах 37-44%, неонатальная – 43-54%. Прогностически неблагоприятным фактором является задержка идентификации возбудителя на 48 часов и более.
Жизнеугрожающие последствия инвазивного кандидоза в основном связаны с септическим шоком и полиорганной недостаточностью. Причинами смерти выступают критические поражения головного мозга, сердечно-легочной системы и почек. Большую опасность представляют коагулопатии, тромбоэмболии, синдром диссеминированного внутрисосудистого свертывания (ДВС).
Диагностика
Поскольку инвазивный кандидоз в основном развивается у госпитализированных больных, обследование проводит лечащий врач совместно с реаниматологом и инфекционистом. Большое значение уделяют сбору анамнеза, выяснению иммунного статуса, анализу текущей схемы фармакотерапии. При осмотре определяются признаки системного воспаления и полиорганной недостаточности. Для подтверждения диагноза назначаются такие методы:
- Определение поверхностного антигена Candida. Наличие в анализе маннана и антиманнановых антител специфично для кандидозной инфекции. Позитивные результаты на 5-6 дней опережают ответ при посеве гемокультуры, имеют важное значение для своевременного старта терапии. Чувствительность и специфичность метода составляют 80-85%.
- Исследование гемокультуры. Выявление грибов Кандида в образцах крови, взятых из трех разных вен, является достоверным признаком инвазивного кандидоза. Такой метод требует длительного времени и дает положительные результаты только у 75% пациентов, поэтому он не подходит для ранней диагностики.
- Инструментальная визуализация. Для обнаружения очагов кандидозной инфекции используют ультразвуковое исследование, чреспищеводную эхокардиографию, компьютерную и магнитно-резонансную томографию. Подтвердить грибковую этиологию воспалительных очагов удается путем анализа биоптатов.
- Прогностические шкалы. Поставить точный диагноз помогает шкала «Кандида» и прогностическое правило, представленное в Российских клинических рекомендациях. Для определения индивидуального риска используют индекс колонизации Candida.

Дифференциальная диагностика
Ввиду отсутствия патогномоничных проявлений, при постановке диагноза исключают бактериальный сепсис, генерализованную герпетическую инфекцию, аспирационную и вентилятор-ассоциированную пневмонию. Дифференциальную диагностику проводят с малярией, системной красной волчанкой, васкулитами. У новорожденных необходимо исключить респираторный дистресс-синдром.
Лечение инвазивного кандидоза
Основу лечения составляет длительное парентеральное введение противогрибковых препаратов. Лекарства назначают эмпирически до получения результатов посева крови, предварительно взяв биоматериал для микробиологической диагностики. При выборе препарата для лечения кандидоза обращают внимание на иммунный статус пациента, наличие и характер сопутствующих заболеваний, анамнестические данные о грибковых инфекциях.
Стандартные протоколы терапии включают препараты из группы полиеновых антибиотиков, азоловых антимикотиков, эхинокандинов. Клинический ответ на проводимое лечение развивается в течение 3 дней. При его отсутствии необходим пересмотр режима дозирования антимикотиков или их замена. Критерием завершения антимикотической терапии служат отрицательные посевы крови в течение 14 суток.
Фармакотерапия инвазивного кандидоза сочетается с лечением основного заболевания. Значимые усилия прикладывают для нормализации иммунного статуса, если это возможно. Для исключения повторного инфицирования грибками проводят замену катетеров. При тяжелом иммунодефиците, состоянии после трансплантации костного мозга или внутренних органов пациенты проходят лечение в стерильном боксе.
Прогноз и профилактика
У пациентов с сохранными функциями иммунной системы, которым вовремя начата терапия антимикотиками, удается достичь полного выздоровления. При иммунодефиците и тяжелом соматическом статусе прогноз остается сомнительным даже при ранней и комплексной медицинской помощи. Для профилактики инвазивного кандидоза пациентам из группы высокого риска рекомендован прием флуконазола в стандартной дозировке.
3. Инвазивный кандидоз: современные аспекты эпидемиологии, диагностики, терапии и профилактики у различных категорий пациентов (в вопросах и ответах)/ А.В. Веселов, Р.С. Козлов. – 2016.
4. Инвазивный кандидоз в отделениях реанимации и интенсивной терапии/ Н.А. Карпун, С.А. Бурова, Е.А. Евдокимов, Н.И. Чаус// Неотложная медицина. – 2014. – №2.
Эти микроскопические грибки вызывают наиболее распространенные грибковые инфекции кожи — грибок стопы (Tinea pedis), грибок стопы (Tinea cruris), грибок головы (Tinea capitis), грибок ногтей (Tinea unguium), грибок тела (Tinea unguium). Tinea corporis). Грибок тела появляется на паху, лице, волосистой части головы или бороде.
Чаще всего грибковая инфекция дерматофитов поражает поверхностный слой кожи, доходя только до эпидермиса. Иногда дерматофиты поражают также волосяные фолликулы, дерму, тогда эту инфекцию называют гранулемой Майокки. Грибковая инфекция головы и бороды повреждает волосы, но не их фолликулы.

Грибковая инфекция головы
Грибковые инфекции, вызванные дерматофитами, можно заподозрить на основании клинических признаков, но для подтверждения диагноза также рекомендуются диагностические тесты, поскольку другие кожные заболевания могут вызывать очень похожие симптомы.
Инфекцию диагностируют с помощью гидроксида калия (КОН), культивирования грибковых культур или теста на дерматофиты. Если кожная дерматофитная инфекция не распознается и для начального лечения назначается кортикостероидная мазь, клинические симптомы меняются. Тогда бывает трудно распознать грибковую инфекцию, а сама болезнь продолжает прогрессировать и может достигать более глубоких слоев кожи, дермы, волосяных фолликулов. У больных появляется эритема, перхоть, исчезает сыпь.
Грибковые инфекции дерматофитов могут одновременно преобладать на нескольких участках (например, грибок стопы и паха, грибок стопы и ногтей). Пациента необходимо тщательно обследовать с головы до пят, кожу, волосы и ногти. Некоторые пациенты с грибковыми кожными инфекциями, вызванными дерматофитами, могут испытывать вторичную кожную реакцию вдали от очага инфекции. Это приводит к иммунологической реакции на грибковую инфекцию.
Для лечения используются противогрибковые препараты местного или системного действия:
- Дерматофитные кожные инфекции, поражающие только поверхностный слой кожи, лечат с помощью местных противогрибковых препаратов, таких как бутенафин, циклопирокс, толнафтат, аллиламин.
- Нистатин, который эффективен при лечении грибковых инфекций, вызванных Candida, не подходит и неэффективен при лечении грибковых инфекций, вызванных дерматофитами.
- Системные препараты (флуканозол, гризеофульвин , итраконазол или тербинафин) используются в случаях, когда грибковая инфекция является рецидивирующей, хотя и поверхностной, или когда поражены более глубокие слои (волосяные фолликулы, дерма) и ногти.
- Пациентам не следует назначать системный препарат кетоконазол из-за возможного поражения печени, надпочечниковой недостаточности и взаимодействия с другими препаратами.
Совместное применение противогрибковых препаратов с кортикостероидами средней и тяжелой степени может быть эффективным и может облегчить симптомы поверхностной дерматофитной инфекции кожи, но не рекомендуется, поскольку кортикостероиды не являются необходимыми для успешного лечения заболевания и могут вызывать атрофию кожи (2). Сообщалось, что такое лечение (противогрибковые препараты в сочетании с кортикостероидами) было совершенно неэффективным (3–5).
Иммуносупрессивные состояния являются одним из факторов риска развития грибковых инфекций, вызванных дерматофитами, что затрудняет их лечение и повторение инфекции после излечения. Пациента с трудноизлечимой дерматофитной инфекцией следует обследовать на иммунодефицитные заболевания.
В этой статье мы обсудим наиболее частые дерматофитные кожные инфекции, их симптомы, диагностику и лечение.
Грибок стопы: диагностика и лечение
Грибок стопы (Tinea pedis) — наиболее частая дерматофитная инфекция. Грибок стопы может возникать между пальцами ног, развиваться при гиперкератозе или везикобулезе, а в очень редких случаях может вызывать язвенное повреждение кожи.
Обычно грибок стопы преобладает между пальцами ног, часто грибок ногтя и стопы (паха) развивается вместе. Грибок стопы чаще всего диагностируется у взрослых (особенно у молодых мужчин). Подсчитано, что у 70% грибок стопы будет развиваться на протяжении всей жизни. человек. Грибок стопы вызывается дерматофитами Trichophyton rubrum, Trichophyton interdigitale и Epidermophyton floccosum. Заражение чаще всего происходит при ходьбе босиком в кабинках для переодевания, саунах или бассейнах при прямом контакте с патогенами.
Пациенты с грибком стопы между пальцами ног обычно жалуются на сильный зуд, перхоть между пальцами ног, покраснение кожи. Грибок чаще распространяется под подошвой, реже повреждается тыльная сторона стопы. В частности, между третьим и четвертым пальцами возникают трещины, которые могут быть очень болезненными. Менее распространенной формой заболевания является грибок ногтей на ногах вместе с язвами, когда следует подозревать вторичную бактериальную инфекцию.
Грибок гиперкератоза стопы (также называемый грибком мокасинового типа) проявляется в виде диффузного гиперкератоза подошв, латеральных и медиальных поверхностей стопы. Кожа чешуйчатая, всегда присутствует эритема.

Грибок гиперкератоза стопы
Воспалительный или пузырчатый грибок стопы болезнен, проявляется сильным зудом, волдырями и волдырями на коже, которые могут лопнуть. Эти поражения сопровождаются выраженной эритемой. Чаще всего травмируется медиальная сторона стопы.
Основные методы диагностики — исследование царапин на коже после окрашивания КОН. Микроскопическое исследование царапин кожи, окрашенных KOH, на которых видны сегментированные гифы мицелиальных грибов, помогает отличить грибок стопы от негрибкового заболевания стопы, а в случае инфекции Candida виден кластерный грибок с псевдогифией.
При везикулярной болезни везикулы используют для микробиологических исследований (посев на специальной среде). В случае образования язв, трещин на коже следует взять мазок и исследовать культуру на вторичную бактериальную инфекцию.
В клинической практике грибок стопы можно заподозрить исключительно на основании признаков и типа поражения, но рекомендуется подтвердить диагноз клиническими испытаниями, поскольку симптомы грибковой инфекции могут быть аналогичны другим дерматологическим заболеваниям — кандидозной инфекции пальцев рук, атопическому дерматиту.
Основные цели лечения — облегчить симптомы (зуд и боль), снизить риск вторичных бактерий и остановить дальнейшее распространение грибковой инфекции как на пациента, так и на окружающих.
- Препараты первого ряда — это противогрибковые препараты местного действия, а препараты системного действия — резервные, назначаемые в случаях, когда препараты местного действия неэффективны или неэффективны сами по себе.
- Противогрибковые препараты местного действия включают аллиламин, бутенафин, циклопирокс, толнафтат. Данные метаанализа 2005 г. подтверждают эффективность местного лечения опоясывающего лишая стопы.
Противогрибковые препараты местного действия назначают 1-2 раза в день и продолжение лечения не менее 4 недель. Пациенты, нуждающиеся в системной терапии, получают итраконазол (250 мг 2 раза / сут в течение 1 недели) и тербинафин (250 мг 1 раз / сут в течение 1 недели) 2 недели) или флуконазол (150 мг 1 неделю в неделю в течение 2-6 недель).

Противогрибковые препараты местного действия
Гризеофульвин также можно использовать для лечения грибка стопы, но он не так эффективен, как другие системные противогрибковые препараты, и требует более длительного лечения (1000 мг / день в течение 4-8 недель или 660 или 750 мг / день в течение 4-8 недель).
Помимо местных противогрибковых препаратов пациентам с гиперкератозом можно назначать слабые растворы салициловой кислоты (1). Повязку, смоченную этим продуктом, следует наложить на пораженные участки и удерживать в течение 2–0 минут, повторяя процедуру 2–3 раза в день.
Грибок тела: диагностика и лечение
Tinea corporis — дерматофитическая инфекция кожи . Самый распространенный грибок тела вызывается T. rubrum. Другие патогены могут включать Trichophytontonsurans, Microsporum canis, T. interdigitale, Microsporum gypseum, Trichophyton violaceum и Microsporum audouinii.

Tinea corporis — дерматофитическая инфекция кожи
Инфекция чаще всего возникает после прямого контакта кожи с больным грибком тела, может передаваться от животных или инфекция может распространяться на самого пациента из других мест, если у него есть грибок на голове, ногах или других областях. Взрослые могут заразиться грибком тела T.tonsurans от детей с грибком головы, который часто вызывается этим возбудителем. Инфекция M. canis передается от больных кошек или собак. Возможны вспышки грибка тела у юных спортсменов, много контактирующих с другими спортсменами (баскетболистами, борцами и т. д.),
Клиническими признаками грибка на теле являются зудящие, круглые или овальные, эритематозные, шелушащиеся бляшки, эксцентрично распространяющиеся. По мере прогрессирования болезни середина сыпи становится немного светлее, а края выступают вперед. Формируются круглые кольцевые пластины.
Эти бляшки могут сливаться и образовываться волдыри. Инфекции у животных, особенно у молодых котят и щенков, более тяжелые и преимущественно воспалительные. В случае широко распространенной сыпи следует учитывать возможность иммунодефицитного заболевания (например, ВИЧ-инфекции) или диабета.
Основной метод диагностики — исследование кожных царапин с помощью раствора КОН. Дерматофиты представляют собой сегментированные нитчатые гифы. Для анализа необходимо взять срезки кожи с наиболее активного очага заболевания — края круглой пластины.
Ряд дерматологических кожных заболеваний необходимо различать между грибком тела. Подозрение, что это не грибок организма, должно быть вызвано тем, что перхоти нет, лечение малоэффективно, отрицательный ответ на тест КОН, сыпь очень часто. Грибок на теле необходимо дифференцировать от других кожных заболеваний, которые проявляются в виде кольцевой сыпи. К таким заболеваниям относятся подострая кожная красная волчанка, круговая гранулема и центробежная круговая эритема .
Причина подострой красной волчанки идиопатическая, она может быть связана с системной красной волчанкой или с применением некоторых лекарственных препаратов. Заболевание проявляется на подверженных воздействию солнечных лучей участках тела в виде круговых эритематозных бляшек перхоти.
Круговая гранулем а — доброкачественный воспалительный дерматоз. Его клинические признаки — одна или несколько эритематозных кольцевых бляшек на конечностях, но перхоть отсутствует. Центробежная циркулярная эритема — воспалительное заболевание кожи неизвестной причины, также проявляющееся кольцевидными эритематозными бляшками.



Tinea corporis эффективно лечится местными противогрибковыми средствами, такими как азолы, аллиламин, бутенафин, циклопирокс и толнафтат (2). Исследования показывают, что лечение грибка тела и стоп двумя противогрибковыми препаратами очень эффективно (изучалось действие тербинафина и нафтифина) (2). Нистатин неэффективен при лечении дерматофитных инфекций. Препараты местного действия вводят 1-2 раза / сут. 3 недели. Лечение прекращают после исчезновения всех клинических признаков.
Системное лечение назначается пациентам, у которых было неэффективное лечение местными противогрибковыми препаратами или заболевание очень распространено. Наиболее распространенными вариантами лечения являются тербинафин (250 мг 1 день / день в течение 1-2 недель) и итраконазол (200 мг / день в течение 1 недели).

Тербинафин
Гранулема Майокки: диагностика и лечение
Гранулема Майокки — более редкая грибковая дерматофитная инфекция, поражающая более глубокие слои кожи — дерму, подкожную клетчатку и волосяные фолликулы. Наиболее частым возбудителем является T. rubrum, но инфекция также может быть вызвана другими дерматофитами. Развитие гранулемы Майокки может быть вызвано травмой кожи или окклюзией волосяных фолликулов.
Бритье ног — один из факторов развития гранулем Майокки. Пациенты с ослабленным иммунитетом и нарушенным иммунитетом подвергаются повышенному риску развития гранулемы Майокки. Кортикостероидная терапия при дерматофитных поверхностных инфекциях не рекомендуется, так как это может привести к местной иммуносупрессии и развитию гранулемы Майокки.
Клинические признаки инфекции возникают на локализованном участке тела, где видны эритематозные, перифоликулярные папулы или небольшие узелки, пустулы. У пациентов с иммуносупрессивными состояниями подкожно могут образовываться узелки и абсцессы. В редких случаях также возможно распространение болезни.

Гранулема Майокки
Заболевание диагностируется на основании истории болезни пациента и клинических признаков, диагноз подтверждается биопсией кожи, а патогистологическое обследование подтверждает наличие грибковых форм в дерме. Ответ на опрос посевов помогает определить точного возбудителя. Тест с КОН может быть отрицательным, поскольку грибковая инфекция в этом случае развивается в более глубоком слое кожи.
Местные противогрибковые препараты для лечения гранулем Майокки неэффективны, потому что они не проникают через дерму и подкожно. Рекомендуется лечение системными противогрибковыми препаратами. Обычная рекомендация — тербинафин 250 мг 1 в / день. 2–6 недель, продолжительность лечения зависит от реакции на лечение. Лечение продолжают до исчезновения всех клинических признаков.
Резюме
Грибковые инфекции кожи чаще всего вызываются дерматофитами из родов Trichophyton, Epidermophyton и Microsporum. Эти дерматофиты метаболизируют кератин и могут встречаться в различных частях тела — ногах, паху, голове, ногтях, волосах бороды, могут повредить более глубокий слой кожи, дерму и волосяные фолликулы.
Грибковые инфекции, вызванные дерматофитами, часто можно заподозрить, оценив клинические признаки, но диагноз также должен быть подтвержден тестами. В случае ошибочного диагноза пациенту могут быть назначены кортикостероиды, что затрудняет как подтверждение дерматофитного диагноза, так и сам процесс заживления.
Большинство кожных инфекций, вызванных дерматофитами, излечимы с помощью местных противогрибковых препаратов, таких как азол, аллиламин, циклопирокс, бутенафин и толнафтат.
Источники
- Adam O Goldstein, et al. Дерматофитные (дерматофитные) инфекции. 2019 г. UpToDate.
- Эль-Гохари М. и др. Местные противогрибковые препараты для опоясывающего лишая и тинея тела. Кокрановская база данных Syst Rev 2014.
- Гринберг Х.Л. и др. Клотримазол / бетаметазона дипропионат: обзор затрат и осложнений при лечении распространенных кожных грибковых инфекций. Pediatric Dermatol 2002.
- Розен Т., Елевски Б.Е. Неэффективность крема клотримазола-бетаметазона дипропионата при лечении инфекций Microsporum canis. J Am Acad Dermatol 1995.
- Гольдштейн А.О. и др. Грибковые инфекции. Эффективное лечение заболеваний кожи, волос и ногтей. Гериатрия. 2000.
- Кроуфорд Ф., Холлис С. Местные методы лечения грибковых инфекций кожи и ногтей стопы. Кокрановская база данных Syst Rev 2007.
- Гупта А. К., Купер Е. А.. Обновление противогрибковой терапии дерматофитий. Микопатология 2008.

Грибок на теле – это группа заболеваний, которые развиваются в результате заражения грибковыми микроорганизмами. Эти болезни в медицине называют микозами. Чаще всего микозы поражают кожные покровы или слизистые оболочки, однако могут также появляться на ногтях и волосах. При этом грибок на коже тела заразен, поэтому важно на ранней стадии определить заболевание и начать лечение.
В клинике «Диана» опытные дерматологи помогут избавиться от кожного грибка на теле быстро, качественно, комфортно.
Как выглядит грибок на теле?
Грибковая инфекция проявляется комплексом симптомов, которые существенно снижают качество жизни человека. Медицине известны десятки разновидностей грибковой инфекции. Каждый тип микоза проявляется по-разному и локализируется на разных частях тела. В большинстве случаев микоз на теле принимает вид пигментного пятна с четко очерченными краями. Поражение обычно имеет правильную округлую форму и выступает над уровнем здоровой кожи. В зоне поражения кожа принимает ярко-красный, алый или коричневый окрас, появляется шелушение, иногда беспокоит зуд.
Микозы в области стоп проявляются в виде локального шелушения кожи. Она становится очень тонкой, а в зоне поражения появляются трещины, эрозии, которые долго не заживают. Грибок на коже стоп часто распространяется на ногтевую пластину, вызывая ее гниение и расслаивание.



Разные типы грибков размножаются на коже, покрытой волосами. Этот вид болезни характеризуется появление пятен с обильным шелушением и сухостью кожи. При этом волосы теряют блеск, становятся ломкими, тонкими. Зона поражения покрывается желтоватым налетом и очень чешется, что приводит к травмированию дермы. Грибковые пятна принимают розовый оттенок и часто становятся причиной очагового облысения.
От чего появляется грибок на теле?
Основная причина развития грибка на коже тела – заражение грибковыми спорами. Грибок в виде пятен на теле появляется после тесного контакта с инфицированным человеком, животным или предметом. Механизмы передачи микозной инфекции:
- проникновение спор через дыхательные пути;
- контактно-бытовое заражение – через рукопожатие, объятия, поцелуи, общие предметы обихода;
- при тактильном контакте с зараженной почвой, водой, пищей;
- проникновение микроорганизмов через микротравмы на коже человека и зоны избыточного потоотделения.




Заражение происходит при игнорировании правил личной гигиены, особенно в общественных местах. Например, после посещения сауны или бассейна пациенты часто жалуются на появление белых пятен – это грибок. При посещении общественных мест рекомендуется использовать отдельные полотенца, тапочки, постельное белье, дезинфицировать кожу с помощью специальных растворов.
Грибок тела: причины
В норме от размножения болезнетворных грибков человека защищает иммунная система. Поэтому активное деление микроорганизмов и внешнее инфицирование происходит обычно при ослаблении иммунитета. Защитные механизмы дают сбой при:
- перенесении тяжелых болезней, операций;
- после курса химиотерапии;
- нарушение обмена веществ;
- заражении ВИЧ;
- прогрессировании аутоиммунных заболеваний;
- длительной терапии антибиотиками;
- изменении микрофлоры половых путей и желудочно-кишечного тракта;
- приеме гормональных препаратов.
Когда иммунитет ослаблен, происходит резкий рост грибковых штаммов, жизнедеятельность которых негативно влияет на состояние кожи и тканей организма.
Внешние факторы, которые могут вызвать микозное поражение:
- игнорирование правил личной гигиены;
- несоблюдение рекомендаций врач после хирургического вмешательства;
- микоз половых органов;
- ожирение и избыточное потоотделение;
- игнорирование травм, эрозий, язв кожных покровов;
- психологическое переутомление и неврозы;
- плохое питание, недостаток витаминов и микроэлементов;
- индивидуальная предрасположенность организма к микозам;
- специфика трудовой деятельности (например, работа с землей, населенной спорами грибка).



Беременность и грибок на теле часто сопровождают друг друга. Во-первых, при беременности кардинально меняется гормональный фон, что влияет на иммунитет. Во-вторых, на фоне изменения состава микрофлоры половых путей у пациенток может развиваться кандидоз (молочница).
Грибок на теле: симптомы
Грибок на теле человека проявляется комплексом симптомов. Конкретные клинические проявления зависят от типа возбудителя. Но общими симптомами микозной инфекции выступают:
- пятна пигментного типа красного, коричневого, белого, розового цвета;
- зуд в области поражения;
- интенсивное шелушение воспаленной кожи;
- появление сопутствующих высыпаний;
- образование язв, трещин, которые не заживают;
- появление мокнущих ран;
- соединение нескольких очагов в единое пространство;
- постоянная боль в зоне поражения;
- желтоватый или белый налет на коже;
- неприятный запах от пораженных участков.
Грибок тела и признаки болезни зависят от зоны поражения, то есть к общим проявлениям добавляются специфические симптомы:
- кожа головы – избыточное отделение кожного сала или чрезмерная сухость, перхоть;
- ногтевая пластина – расслоение и крошение ногтя, гнойный запах, желтый оттенок;
- стопы – жжение, сильный зуд, пузырчатая сыпь между пальцами, распространение грибка по всему телу;
- системное поражение гладкой кожи – большие гиперемированные зоны, интенсивное шелушение, трещины и раны, экземное поражение.



Иногда микозная болезнь сопровождается общими симптомами:
- повышение температуры тела;
- интоксикация организма;
- длительный кашель неясной природы;
- ринит, не поддающийся лечению обычными методами;
- постоянная слабость.
Симптомы грибка кожи на теле проявляются сразу после инфицирования, реже на поздней стадии болезни.
Виды грибков на теле человека
Существует несколько сотен типов грибковых заболеваний, видовая принадлежность которых зависит от рода возбудителя:
- Microsporum, Trichophyton поражает ногти, волосы, кожные покровы, провоцируя дерматомикоз;
- Candida поражает слизистые оболочки, чаще половых путей, вызывая кандидоз;
- Malassezia furfur провоцирует себорейный дерматит, поражает волосы и ногтевую платину.

В медицинской практике чаще всего встречаются такие виды грибков на теле человека:
- Рубромикоз . Патология развивается после заражения красным трихофитоном. В зоне поражения – кожа стоп и рук, межпальцевое пространство, ногтевые платины. Инфекция проявляется красными грибком на теле в виде шелушащихся пятен. На поздней стадии болезни в зоне поражения появляются мелкие папулы и узелки;
- Микроспория . Возбудитель болезни микроорганизм рода микроспорум. Эта болезнь поражает участки тела, покрытые мелкими волосками. Очаг поражения имеет правильную округлую форму. Пораженные участки окрашены в темно-желтый цвет, а на солнце могут несколько светлеть. Поэтому болезнь называют солнечный грибок на теле. Воспаленная зона гиперемирована и покрыта мелкими пузырьками, чешуйками. Болезнь проявляется единичными воспаленными пятнами, в осложненных случаях появляется сразу несколько пораженных зон;
- Трихофития. Заболевание поражает открытые зоны кожных покровов (лицо, плечи, руки). Грибок Trichophyton на других частях тела встречается редко (только в запущенных случаях). Проявляется болезнь в виде крупных пятен алого цвета с воспаленными краями. Иногда пораженные участки шелушатся, чешутся. В тяжелых случаях грибковая инфекция сопровождается нагноением, образованием абсцессов. Заболевание очень заразно, поэтому требует особых мер личной гигиены;
- Себорейный дерматит. Патологию вызывают споры липофильных грибов. Болезнь поражает кожу и участки, покрытые волосами (голова, лобок, ресницы, область усов). В районе волосяного покрова образуются воспаленные участки, которые шелушатся или покрываются корочками. Железы начинают продуцировать больше кожного сала. Липофильный грибок на теле чешется, поэтому на их месте образуются расчесы, которые опасны присоединением вторичной инфекции;
- Дрожжевой грибок . В некоторых случаях появление неприятных признаков на теле вызывают микроорганизмы рода Candida. Этот тип грибов чаще поражает слизистые оболочки, но в запущенных случаях инфекция распространяется на кожные покровы. В зоне поражения появляются небольшие красные пятна с мелкими пузырьками. С развитием болезнь цвет пятен становится более ярким, появляются эрозии, отслаивается ороговевшая кожа.
Кожное поражение может перейти в форму глубокого микоза, при котором страдают внутренние органы и кости. Подкожный грибок на теле поражает жировую клетчатку, далее слизистые оболочки, ткани нервной системы. Характерный признак глубокого микоза – появление свищей, ран, бородавок на коже.
Часто грибок на теле появляется от пота, из-за активного размножения дрожжевых грибков типа малассезия. Это заболевание называют цветной грибок на теле, поскольку спина, плечи, подмышки покрываются пятнами разного цвета (коричневый, красный, темно-розовый). Пораженные участки зудят, шелушатся, покрываются чешуйками.
Лечение грибка на теле
Лечить микозы следует комплексно под контролем специалиста дерматолога. Если специалист не может поставить диагноз по внешним проявлениям, разновидность микоза определяется при помощи лабораторной диагностики. Точно определив тип возбудителя, врач назначит эффективное лечение.
Терапия состоит из таких направлений:
- Лекарственные средства для наружного применения. Начинают лечение с применения наружных противогрибковых средств (антимикотиков). Эти препараты выпускаются в форме мазей, кремов, лосьонов. Выбор противогрибкового средства зависит от вида возбудителя и его чувствительности к лекарственным средствам. Также пациенту могут назначать мази с размягчающим, отшелушивающим, противовоспалительным действием. Для облегчения состояния больного врач может дополнительно рекомендовать настои и отвары лекарственных трав в виде компрессов или ванночек.
- Лекарственные средства для внутреннего применения. Иногда антимикотики назначаются в виде таблеток для приема внутрь. Также пациенту могут быть прописаны антигистаминные препараты, иммуномодуляторы, витамины.
- Физиотерапия. После снятия острых кожных проявлений, дерматолог может рекомендовать физиотерапевтические процедуры. Для лечения грибка на теле применяется светотерапия, фототерапия, лазерное воздействие. Все эти методы активируют местные обменные процессы, запускают регенерацию тканей, обладают бактерицидным действием.
- Диетотерапия. Соблюдение диеты помогает ускорить лечение микоза. Разрабатывая рацион, предпочтение следует отдавать продуктам, способствующим укреплению иммунитета и активации регенеративных процессов. На время лечения специалисты рекомендуют отказаться от сладостей, простых углеводов, белого хлеба. В рацион желательно включить такие компоненты – чеснок, гвоздика, корица, лимон, корень имбиря, хрен, кисломолочные продукты.


После того, как симптомы микоза проходят, многие пациенты прекращают лечение. Это ошибка, поскольку после завершения лечения, симптомы могут вернуться. Терапия должна продолжаться, пока не завершится курс лечения, назначенный дерматологом.
Заметив первые симптомы грибка тела, следует немедленно обратиться к врачу-дерматологу. В клинике «Диана» в Санкт-Петербурге прием ведут дерматологи высшей врачебной квалификации.
Что такое вагинальный кандидоз (молочница)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Сосниной Анастасии Сергеевны, гинеколога со стажем в 15 лет.
Над статьей доктора Сосниной Анастасии Сергеевны работали литературный редактор Вера Васина , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Вагинальный кандидоз (кандидозный вагинит) — поражение слизистой оболочки влагалища дрожжеподобными грибами рода Candida. В быту эту болезнь называют молочницей .
Краткое содержание статьи — в видео:
Candida — это условно-патогенные микроорганизмы, факультативные анаэробы (организмы, способные жить как в присутствии кислорода, так и без него). Они обладают тропизмом — направлением роста на клетки богатые гликогеном, в частности клетки слизистой оболочки влагалища. Самый распространённый вид возбудителя, который встречается в 70—90 % случаев, — Candida albicans.
В последние годы растёт заболеваемость кандидозом, вызванным другими представителями рода Candida. Наиболее часто выявляются:
- С. glabrata (15 %);
- C. dubliniensis (6 %);
- C. tropicalis (3—5 %);
- C. parapsilosis (3 %);
- C. krucei (1—3 %).
Распространение новых видов микроорганизмов связано в первую очередь с бесконтрольным самолечением пациенток, приводящем к возрастающей устойчивости грибов к препаратам [3] [4] .
Частота кандидозного вагинита среди инфекционных заболеваний влагалища и вульвы составляет 30—45 %. Патология занимает второе место среди всех инфекционных заболеваний влагалища и является крайне распространённым поводом для обращения женщин за медицинской помощью. По данным J. S. Bingham (1999):
- к 25 годам около 50 % женщин репродуктивного возраста сталкивались с хотя бы одним диагностированным врачом эпизодом вагинального кандидоза;
- к началу периода менопаузы — около 75 % [17] .
Кандидозный вагинит редко наблюдается в постменопаузе, за исключением тех пациенток, которые получают гормональную заместительную терапию.
Предрасполагающими факторами заболевания являются:
- Механические — ношение синтетического белья, первый половой контакт, травматическое повреждение тканей влагалища, длительное применение внутриматочной спирали.
- Физиологические — беременность, менструация.
- Эндокринные — гипотиреоз, сахарный диабет.
- Иммунодефицитные состояния.
- Ятрогенные (приём антибиотиков, кортикостероидов, иммуносупрессоров, лучевая терапия, химиотерапия, онкологические заболевания, оральные контрацептивы).
- Прочие (авитаминоз, аллергические заболевания, хронические патологии гениталий и желудочно-кишечного тракта).
Заболевание, как правило, не передаётся половым путём, но установлено, что оно связано с характером половых контактов: анально-вагинальным и орогенитальным. Также не исключается вероятность развития кандидозного баланопостита у половых партнёров пациенток с вагинальным кандидозом.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы вагинального кандидоза
Основные симптомы при вагинальном кандидозе:
- жжение и зуд в области влагалища и вульвы;
- творожистые выделения из влагалища;
- расстройства мочеиспускания;
- боль при половом акте.
Зуд может усиливаться после водных процедур, полового акта, ночью во время сна и в период менструации [1] .
В целом симптомы вагинального кандидоза нарастают перед менструацией. При беременности проявление болезни также усугубляется, это связано со снижением иммунитета у беременных женщин.
Объективные признаки вагинального кандидоза:
- отёк и гипермия слизистой оболочки влагалища и наружных половых органов;
- белые или зеленовато-белые наложения на стенках влагалища;
- покраснение слизистой влагалища.
При осложнённом кандидозе на коже наружных половых органов появляются везикулы — пузырьки, возвышающиеся над уровнем кожи или слизистой и заполненные прозрачным или мутным содержимым, которые могут вскрываться и образовывать эрозии. При вагинальном кандидозе также могут наблюдаться трещины слизистой вульвы, задней спайки и перианальной области [2] .
Патогенез вагинального кандидоза
Грибы рода Candida относятся к условно-патогенной микрофлоре, которая присутствует как в окружающей среде, так и на поверхности кожных покровов и слизистых оболочках здорового человека (в полости рта, кишечнике, влагалище). При снижении защитных сил организма возможно повышение адгезивных свойств (способности прилипать) грибов с прикреплением их к клеткам эпителия влагалища, колонизацией слизистой оболочки и развитием воспалительной реакции [7] .
Вагинальный кандидоз зачастую затрагивает только поверхностные слои эпителия влагалища без проникновения возбудителя в более глубокие слои слизистой оболочки. Однако в редких случаях эпителиальный барьер преодолевается и происходит инвазия в подлежащую ткань с последующей гематогенной диссеминацией (распространением возбудителя инфекции из первичного очага заболевания по всему органу или организму посредством кровотока) [8] [9] .
Основные этапы патогенеза:
- Адгезия (прилипание) грибов на слизистой и колонизация.
- Инвазия (проникновение) в эпителий.
- Преодоление эпителиального барьера.
- Проникновение в соединительную ткань.
- Преодоление защитных механизмов ткани.
- Попадание в сосуды.
- Гематогенная диссеминация.
При вагинальном кандидозе воспаление происходит в верхних слоях эпителия влагалища. Причина состоит в том, что поддерживается динамическое равновесие между грибом, который не может проникнуть в более глубокие слои, и организмом, который сдерживает его распространение. Соответственно инфекция может долго развиваться в одном месте, проявляясь творожистыми выделениями из влагалища. Обострение заболевания происходит при сдвиге равновесия между развитием грибов и защитными силами организма.
Классификация и стадии развития вагинального кандидоза
Согласно национальным клиническим рекомендациям [18] , выделяют две формы вагинального кандидоза:
- острую — до трёх обострений в год;
- хроническую (рецидивирующую) — не менее четырёх обострений в год.
По классификации, предложенной D.A. Eschenbach, вагинальный кандидоз подразделяют на два типа:
У женщин различают три формы заболевания:
- вагинит (воспаление влагалища); (воспаление влагалища и вульвы); (воспаление шейки матки).
У мужчин выделяют:
- баланит (воспаление головки полового члена);
- баланопостит (воспаление крайней плоти и головки полового члена); (воспаление мочеиспускательного канала).
Для острой формы вагинального кандидоза характерны выраженные симптомы: обильные выделения из влагалища, жжение и зуд во влагалище и наружных половых органах. На фоне таких симптомов нередко снижается трудоспособность пациентки и развиваются неврозы. Острая форма вагинального кандидоза встречается наиболее часто и формируется в результате увеличения количества грибов рода Candida во влагалище на фоне снижения иммунитета пациентки.
Рецидивирующий вагинальный кандидоз — встречается у 10—15 % женщин репродуктивного возраста и проявляется четырьмя и более обострениями за год [11] .
Неосложнённая форма заболевания предполагает впервые выявленный или возникающий менее четырёх раз в год вагинальный кандидоз с умеренными проявлениями вагинита у пациенток без сопутствующих факторов риска (сахарный диабет, приём глюкокортикоидов, цитостатиков и др.).
При осложнённом вагинальном кандидозе наблюдаются яркие объективные симптомы: покраснение, отёк, образование язв, трещин слизистых оболочек и кожи перианальной области. Также характерны рецидивы четыре и более раз в год. Заболевание часто возникает на фоне сахарного диабета, ВИЧ-инфекции, терапии глюкокортикоидами и цитостатиками. Возбудителем заболевания в данном случае являются как C. albicans, так и другие грибы рода Candida.
Осложнения вагинального кандидоза
К осложнениям вагинального кандидоза у женщин относятся:
- стеноз влагалища;
- воспалительные патологии органов малого таза — сальпингит, оофорит и другие;
- заболевания мочевыделительной системы — цистит, уретрит[2] .
Стеноз влагалища развивается при воспалении стенок влагалища. При этом просвет влагалища сужается, а стенки влагалища становятся плохо растяжимы. Пациентки испытывают боль при половом акте.
Сальпингит — инфекционно-воспалительное заболевание фаллопиевой (маточной) трубы. Возникает при переходе инфекции восходящим путем из влагалища, не исключен также и гематогенный путь передачи. Сальпингит чаще всего протекает в сочетании с оофоритом — воспалением яичника. Поражение может быть как односторонним, так и двусторонним. Пациентки испытывают боль в области придатков, внизу живота слева или справа, повышается температура тела, возникает общее недомогание, слабость, а иногда и тошнота со рвотой. При несвоевременном лечении данного осложнения высок риск бесплодия, наступления внематочной беременности, возникновения спаечного процесса, приводящего к оперативному вмешательству, инфицированию органов брюшины и малого таза. Сальпингит особенно опасен в случаях, когда с кандидозом сочетаются другие инфекции [1] .
Уретрит — воспаление слизистой мочеиспускательного канала. Проявляется болезненным мочеиспусканием, чувством жжения в области уретры, выделением с мочой крови или гноя, дискомфортом при соприкосновении с бельём, слипанием краёв уретры, покраснением области вокруг мочеиспускательного канала.
Цистит — воспаление мочевого пузыря. Патология возникает при попадании возбудителя восходящим путём через уретру в мочевой пузырь. Симптомы цистита схожи с симптомами уретрита, однако есть некоторые отличия: частые позывы к мочеиспусканию при небольшом количестве мочи, чувство неполного опорожнения мочевого пузыря, боль, резь в конце мочеиспускания, помутнение мочи, повышение температуры тела, боли внизу живота.
На фоне вагинального кандидоза возрастает частота осложнений при беременности, а также увеличивается риск инфицирования плода.
Кандидоз плода может вызвать его внутриутробную гибель или приводить к преждевременным родам. После родов у женщин возможно развитие кандидозного эндометрита — воспалительного процесса в тканях, выстилающих внутреннюю полость матки.
Диагностика вагинального кандидоза
Диагностика вагинального кандидоза основывается на характерных жалобах пациентки, данных анамнеза, клинических проявлениях, выявленных при гинекологическом осмотре. В зеркалах видна гиперемия, отёк слизистой, белые налёты на стенках влагалища.
Независимо от этих признаков, подтверждение диагноза должно основываться на лабораторных данных:
- Микроскопия мазков вагинального отделяемого — позволяет выявить споры и мицелий гриба.
- Культуральный метод — посев влагалищного содержимого на искусственные питательные среды. Метод определяет количество, видовую принадлежность, чувствительность к противогрибковым препаратам, а также характер и степень заселения другими микроорганизмами. Культуральный метод дополняет микроскопию.
- Серологическая диагностика (РСК). Определяет антитела против антигенов грибов рода Candida. Такая диагностика имеет значение при генерализации процесса.
- Молекулярно-биологические методы. Направлены на обнаружение специфических фрагментов ДНК Candida spp. Применяют метод полимеразной цепной реакции (ПЦР).
- Иммунофлюоресцентная диагностика (Candida Sure Test) проводится в случае рецидивирующего течения вагинального кандидоза [15] .
К дополнительным методам диагностики относятся: изучение микробиоценоза кишечника, обследование на инфекции, передаваемые половым путём, внутривенный тест на толерантность к глюкозе [16] .
Дифференциальную диагностику проводят со следующими заболеваниями:
- генитальным герпесом; ;
- аэробным вагинитом;
- кожными заболеваниями (экземой, красным плоским лишаём, склеродермией, болезнью Бехчета и др.).
Лечение вагинального кандидоза
Показаниями к назначению терапии вагинального кандидоза являются жалобы пациентки, клинические проявления и лабораторное подтверждение наличия грибов рода Candida. Лечение не требуется при обнаружении грибов без каких-либо клинических проявлений (кандидозоносительство). Это правило обусловлено тем, что грибы рода Candida могут содержаться в небольшом количестве во влагалище и являются частью нормальной микрофлоры, если их количество не превышает пороговое значение 10 4 .
Механизм действия противогрибковых препаратов — нарушение синтеза эргостерола (вещества в составе клеточных мембран грибов), что приводит к образованию дефектов в мембране микроорганизма. В зависимости от дозы антимикотики проявляют фунгистатическое (замедление роста) или фунгицидное (полное уничтожение) действие [15] .
Существуют различные группы препаратов для лечения вагинального кандидоза:
- антибиотики (пимафуцин, амфотерицин В, нистатин, леворин);
- имидазолы (клотримазол, сертаконазол, кетоконазол, гино-певарил, миконазол);
- триазолы (итраконазол, флуконазол);
- комбинированные препараты ("Тержинан", "Полижинакс", "Пимафукорт", "Клион Д", "Макмирор комплекс");
- препараты разных групп (флуцитозин, гризеофульвин, дафнеджин, нитрофунгин, йодат поливинилпирролидон).
Лечение подбирается гинекологом индивидуально для каждой пациентки, учитывая клиническую картину, форму заболевания и степень выраженности симптомов. Но важно отметить, что при лечении молочницы при беременности флуконазол противопоказан, так как он может негативно повлиять на развитие плода [19] [20] .
При лечении острых форм вагинального кандидоза назначают местное лечение. Препарат не всасывается в системный кровоток, а действует в области влагалища и слизистой. Примеры схем лечения:
-
150 мг в виде вагинальных свечей один раз в сутки в течение трёх дней; один аппликатор крема на ночь вагинально в течение трёх дней; одна свеча на ночь один раз в сутки в течение восьми дней; одна таблетка на ночь в течение 10 дней.
При хроническом кандидозе наряду с местным лечением применяют системные антимикотики:
-
150 мг один раз внутрь; 200 мг внутрь два раза с интервалом 12 часов в течение одного дня или 200 мг в сутки в течение трёх дней.
При рецидивирующей форме заболевания (более четырёх эпизодов в год) применяют схему:
-
150 мг внутрь три раза с интервалом 72 часа в 1,4 и 7 день лечения.
Для купирования рецидивов препарат применяют в дозировке 150 мг один раз в неделю в течение шести месяцев.
В последние годы всё больше исследуется способность C. albicans формировать биоплёнки — вещества на поверхности колонии микроорганизмов, которые служат барьером для проникновения лекарственных средств и обеспечивают выживание. Основным полисахаридом, определяющим развитие резистентности к антибиотикам, является глюкан. Его рассматривают как одну из причин формирования резистентности к антимикотическим препаратам. Этим объясняется отсутствие эффекта при лечении у некоторых больных. Таким пациенткам можно порекомендовать препарат фентиконазол 600 мг в сутки с интервалом в три дня. Лекарство отличается от других способностью преодолевать биоплёнки, тем самым повышая эффективность лечения при резистентности к другим препаратам.
Прогноз. Профилактика
При своевременном обращении пациентки к врачу, лабораторном обследовании и отсутствии самолечения прогноз благоприятный. Самолечение опасно из-за риска рецидива заболевания, его хронизации и возникновения резистентности к препарату, неверно выбранному пациенткой или при неадекватной дозе.
Чтобы повысить эффективность терапии пациентки должны следовать схеме лечения, индивидуально назначенной гинекологом. Во время лечения и диспансерного наблюдения необходимо соблюдать половой покой или применять барьерные методы контрацепции. Повторно обратиться к врачу для контроля анализов следует через 7-10 дней [12] .
Читайте также:

