Как влияет герпес на мозги
Обновлено: 17.04.2024
Герпетический энцефалит - острое поражение головного мозга, вызываемое вирусом простого герпеса, чаще типа 1 (ВПГ-1), реже типа 2 (ВПГ-2). Большинство исследователей рассматривают его как осложнение герпетической инфекции.
Сезонные колебания герпетическому энцефалиту не свойственны. Два пика заболеваемости приходятся на 5-30 лет и возраст старше 50 лет. Более чем в 95% случаев возбудителем герпетического энцефалита служит вирус простого герпеса типа 1.
Что провоцирует / Причины Герпетического энцефалита :
Возбудитель относится к семейству герпеса (Herpes viridae).E это семейство входят также вирусы ветряной оспы, опоясывающего лишая, цитомегаловирусы и возбудитель инфекционного мононуклеоза. Содержит ДНК, размеры вириона 100-160 нм. Вирусный геном упакован в капсид правильной формы, состоящий из 162 капсомеров. Вирус покрыт липидсодержащей оболочкой. Размножается внутриклеточно, образуя внутриядерные включения. Проникновение вируса в некоторые клетки (например, в нейроны) не сопровождается репликацией вируса и гибелью клетки. Наоборот, клетка оказывает угнетающее влияние и вирус переходит в состояние латенции. Через некоторое время может происходить реактивация, что обусловливает переход латентных форм инфекции в манифестные. По антигенной структуре вирусы простого герпеса подразделяются на два типа. Геномы вирусов 1 и 2-го типа на 50% гомологичны. Вирус 1-го типа обусловливает преимущественно поражение респираторных органов. С вирусом простого герпеса 2-го типа связано возникновение генитального герпеса и генерализованная инфекция новорожденных.
Эпидемиология. Герпетический энцефалит составляет 11,5% среди острых энцефалитов. Заболевают чаще дети младшего возраста. Заболеваемость спорадическая, некоторые исследователи указывают на увеличение ее весной. Инфекция может передаваться капельным и контактным путем.
Патогенез (что происходит?) во время Герпетического энцефалита :
Патогенез заболевания герпетическим энцефалитом неоднороден. У детей и молодых людей в форме энцефалита может протекать первичный герпес. При этом вирус герпетического энцефалита, по- видимому, попадает в ЦНС со слизистой носа, транспортируясь по аксонам обонятельных нейронов в обонятельную луковицу. Однако большинство взрослых больных, страдающих герпетическим энцефалитом, либо имеют герпес в анамнезе, либо серопозитивны в отношении вируса простого герпеса типа 1. Приблизительно у 25% больных герпетическим энцефалитом в слизистой ротоглотки и ткани головного мозга обнаруживают разные штаммы вируса. В этих случаях энцефалит обусловлен повторным заражением иным штаммом вируса простого герпеса типа 1 с проникновением возбудителя в ЦНС.
Для объяснения причин энцефалита в тех случаях, когда в слизистой ротоглотки и ткани головного мозга обнаруживают один и тот же штамм вируса, предложено две гипотезы.
Согласно первой, реактивация вируса герпетического энцефалита в тройничном или вегетативных ганглиях сопровождается его распространением в ЦНС по нервам, иннервирующим среднюю черепную ямку. Согласно второй, вирус длительное время покоится в латентном состоянии непосредственно в ЦНС, где и реактивируется. Во всяком случае, с помощью олигонуклеотидных зондов ДНК вируса простого герпеса была обнаружена в ткани головного мозга взрослых людей, умерших не от герпеса.
Симптомы Герпетического энцефалита :
Кроме типичного некротического энцефалита выделяют псевдотуморозную и стволовую форму. Описаны также энцефаломиелиты и генерализованная герпетическая инфекция с преимущественным поражением ЦНС.
Характерная триада герпетического энцефалита - острое лихорадочное начало, развитие судорог джексоновского типа и нарушение сознания, развивающиеся обычно после кратковременной респираторной инфекции. Иногда внезапное развитие судорог и потеря сознания предшествуют лихорадке. Очаговые проявления встречаются в виде парезов глазодвигательных нервов, гемипарезов и различных афазий. В первые 3-5 дней заболевания состав спинномозговой жидкости может быть нормальным. В дальнейшем обнаруживаются лимфоцитарный плеоцитоз (30-400 х 109/л) и повышенное содержание белка (до 1,32 г/л). В крови выявляется лейкоцитоз (до 20 х 109/л) с палочкоядерным сдвигом, лимфопенией и высокой СОЭ. Коматозное состояние - неблагоприятный прогностический признак. Летальность до применения противогерпетических химиопрепаратов достигала 70-75%, в настоящее время составляет 20-25%. Высок удельный вес остаточных явлений в виде судорожных припадков, стойких интеллектуальных нарушений стационарного и прогрессирующего характера. У грудных детей развиваются также гидроцефалия и декортикация головного мозга. Клинический диагноз верифицируется вирусологическими и иммунологическими исследованиями, направленными на обнаружение антигена ВПГ и специфических антител, в том числе иммуноглобулинов класса J в сыворотке крови и спинномозговой жидкости.
Диагностика Герпетического энцефалита :
Отличить герпетический энцефалит от других вирусных энцефалитов и иных очаговых инфекционных и неинфекционных заболеваний ЦНС непросто. Самый чувствительный неинвазивный метод ранней диагностики - выявление ДНК вируса простого герпеса в спинномозговой жидкости с помощью ПЦР. Титр антител к вирусу простого герпеса и в спинномозговой жидкости, и в сыворотке при герпетическом энцефалите, как правило, повышается, но это редко происходит в первые 10 сут заболевания. Поэтому серологические методы пригодны только для ретроспективного подтверждения диагноза. Биопсия позволяет выявить антигены и ДНК вируса простого герпеса в ткани головного мозга и выделить из нее вирус в культуре клеток. Это высокочувствительный метод, сопряженный с низкой частотой осложнений. Кроме того, биопсия головного мозга дает возможность диагностировать и другие излечимые энцефалиты.
Лечение Герпетического энцефалита :
Пациентов, страдающих герпетическим энцефалитом, госпитализируют в палаты интенсивной терапии в связи с опасностью дыхательных расстройств и дисфагии. Широко используется противовирусный химиопрепарат ацикловир (зовиракс, виролекс) в таблетках и ампулах, который при коматозных состояниях назначается по 10-15 мг/кг на одно введение каждые 8 часов. Курс лечения - 7-12 дней. Одновременно назначают интерфероны и иммуномодуляторы, а также кортикостероиды (дексаметазон либо дексазон, 1-2 мг/кг каждые 6 часов). Курс лечения - 6-8 дней.
Профилактика Герпетического энцефалита :
Для предупреждения воздушно-капельного распространения инфекции следует проводить комплекс мероприятий как при ОРЗ. Соблюдать меры предосторожности для профилактики инфицирования новорожденных. Для предупреждения генитального герпеса используют презервативы, но при наличии высыпаний этого может оказаться недостаточно. Разрабатывается убитая вакцина для профилактики рецидивов герпетической инфекции. Эффективность ее еще недостаточно изучена.
К каким докторам следует обращаться если у Вас Герпетический энцефалит :
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Герпетического энцефалита , ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Герпетическая инфекция вызвана вирусами группы Herpesviridae, для нее характерно поражение кожи, слизистых, глаз, нервной системы i . В 1999 г. ВОЗ объявила о пандемии герпесвирусных инфекций, что подчеркивает медицинское и социальное значение этой проблематики в мире. Высокая заболеваемость герпесвирусными инфекциями, по мнению специалистов, будет определять будущее инфекционной патологии в обозримом будущем. Восприимчивость к инфекции не зависит от возраста и пола. Все типы герпеса могут стать причиной тяжелого недуга у взрослых и детей. Герпесвирусы способны поражать разные органы и системы человека, поэтому герпес можно рассматривать как общее системное заболевание организма.
Типы вирусов герпеса
Ветряная оспа. Вызывается вирусом герпеса типа 3, передается воздушно-капельным путем. Симптомы «ветрянки»: умеренная лихорадка и интоксикация, высыпания на коже и слизистых оболочках в виде папул. Заболевание чрезвычайно заразно. К ветряной оспе восприимчивость практически абсолютная, что обусловливает высокую заболеваемость в детстве, после чего остается прочный иммунитет. Несмотря на приобретенный иммунитет, вирус пожизненно присутствует в организме в латентном состоянии в нервных узлах. При ослаблении организма даже через много лет может возникнуть его активация в виде опоясывающего лишая. При типичной лёгкой форме общее состояние инфицированных удовлетворительное, тогда как при среднетяжёлом состоянии температура поднимается до 38.5-39ºС, обильная сыпь. Период высыпания составляет 4-5 дней, иногда и дольше. При тяжёлой форме общее состояние больного значительно нарушено. При сильном жаре до 39,5-40ºС резко выражены симптомы интоксикации – головная боль, слабость, раздражительность, нарушения сна, отсутствие аппетита, возможны рвота, жидкий стул.
Инфекционный мононуклеоз вызывается вирусом Эпштейна – Барр, он же вирус герпеса 4-го типа. Заболевание в основном поражает детей, может стать как причиной, так и следствием снижения иммунитета. Хроническая инфекция, вызванная вирусом Эпштейна-Барр, характеризуется длительным рецидивирующим течением и наличием клинических и лабораторных признаков вирусной активности. Заболевание может проявляться множеством симптомов от слабости и утомляемости, болей в теле до сыпи и кашля, головокружения, депрессии и астении. На пике инфекции повышается температура. Вирус Эпштейна-Барр может привести к развитию следующих заболеваний:
– болезнь Филатова (инфекционный мононуклеоз);
– болезнь Ходжкина (лимфогранулематоз);
– поражение головного и спинного мозга (рассеянный склероз) и других.
Простой герпес у взрослых (ПГ). Причиной недуга становится заражение ВПГ– 1 или ВПГ- 2. Болезнь проявляется зудящей сыпью в виде сгруппированных или одиночных пузырьков размером от одного до нескольких миллиметров на коже и/или слизистых оболочках, сопровождается отеком, покраснением. При тяжелом течении инфекция может поражать внутренние органы. Заболевание приобретает хронический характер и может рецидивировать. Эти вирусы остаются в организме навсегда, иногда сосуществуя с другими представителями группы.
Попав на слизистую оболочку или в верхние дыхательные пути, вирус активно размножается. Инфицирование происходит при контакте биологических жидкостей, содержащих вирус, со слизистыми, например во время интимных контактов, при поцелуях либо заносится грязными руками. Возможен перенос вируса из герпетического очага в другие места, например, из полости рта на конъюнктиву глаза, в области гениталий, на любые участки тела через микроповреждения кожи. Есть небольшая вероятность передачи вируса по воздуху со слюной.
Тяжелые последствия инфицирования ВПГ
Наряду с распространенными проявлениями инфекции на губах, во рту, носу, на лице, ягодицах и половых органах, герпес может поражать внутренние органы, мозговые оболочки, нервы, вызывая такие тяжелые состояния как менингит, энцефалит, неврит, менингоэнцефалорадикулит, стать причиной бронхита, пневмонии, поражения лимфокомпетентных органов: печени, селезенки, поджелудочной железы и даже сепсиса. Одними из критериев инфекционного энцефалита – воспаления головного мозга – являются нарушение психического или ментального статуса больного, лихорадка, судороги, неврологическая симптоматика, изменения на ЭКГ.
Как герпес влияет на нервную систему
Каждый вид вируса герпеса ассоциирован с определенными поражениями нервной системы: ВПГ-1 с менингоэнцефалитом, Варицелла-Зостер – чаще всего вызывает неосложненный герпетический менингит, он очень тропен к мозжечку, поэтому у детей могут возникать постветряночные осложнения (церебеллит). Вирусы Herpesviridae реализуют свою деятельность в клетках эпителия и нервных клетках. С током крови и лимфы ВПГ разносится по всему организму. За короткий промежуток (около трех часов) вирус проникает в нервные узлы, где пребывает в латентном состоянии. ВПГ-1, в основном поражающий слизистую оболочку ротовой полости, носоглотки, губ, находится постоянно в эндотелии сосудов, сосудистых нервных пучках, чувствительных ганглиях тройничного нерва и других черепно-мозговых нервов. ВПГ-2, вызывающий преимущественно поражение гениталий, промежности, анальной области, нижних конечностей, ягодиц, «живет» в ганглиях пояснично-крестцового отдела позвоночника. ВПГ-1 может распространяться по зрительному, обонятельному нерву и в дальнейшем проникать в центральную нервную систему. В нервных узлах вирус становится недосягаемым для клеток, отвечающих за защиту организма от агрессоров. Так как вирус способен распространяться из инфицированной клетки в соседние, минуя межклеточное пространство, он избегает контакта с противовирусными антителами. В стадии обострения вирус покидает разрушенную им клетку и переходит в кровь, где становится доступным для фагоцитов. Помимо влияния на нервную систему герпесвирусные инфекции вызывают дисбаланс системы интерферонов, угнетают клеточные и фагоцитарные реакции организма. Есть мнение, что герпес опосредовано оказывает негативное влияние на состояние сердечно-сосудистой системы, провоцируя образование бляшек и тромбов за счет повреждения сосудистых стенок и выработки большего количества холестерина.
Психоэмоциональное состояние при рецидивах герпеса
Влияние герпеса на нервную систему может быть достаточно интенсивным. При хронической герпетической инфекции вирус длительное время находится в организме, оказывая негативное влияние на иммунные клетки и клетки головного мозга. Психоэмоциональный стресс способствует утяжелению течения вирусной инфекции, и даже развитию психических расстройств, особенно у тех больных, кто к ним предрасположен ii .
Роль иммунитета в возникновения рецидивов ВПГ
Клеточный иммунитет играет важную роль в сценарии развития заболевания. Обострения могут быть связаны со снижением местного иммунитета при операциях, травмах, половых контактах с повреждением слизистой, применении определенных препаратов, интенсивной обработке лица при косметологических омолаживающих процедурах, солнечном ожоге и так далее. Существенную роль в патогенезе герпеса играет дефицит интерферонов, уровень которых может быть снижен в десять-двадцать раз против обычного iii . По результатам исследований в самих очагах герпетических поражений отмечалось снижение производства интерферонов. Аллергики обычно более тяжело переносят инфекцию.
Системное заболевание
В последнее время наблюдается учащение герпес ассоциированных заболеваний. Стоит отметить, что это не только кожный недуг, – герпетическая инфекция – это системное заболевание организма. Радикулиты, связанные с герпетическим поражением нервных структур поясничного и крестцового отделов позвоночника, могут обостряться после простуд и/или переохлаждения. Боль может отдавать в ноги, зону ягодиц, промежности. Вирусная этиология подтверждается тем, что помимо сильных длительных болей в области поясницы, крестца, ягодиц у больных появляются характерные герпетические высыпания. ВПГ может стать одной из причин паралича лицевого нерва, воспаления тройничного нерва. По мнению специалистов переохлаждение активизирует вирус, находящийся в спящем состоянии в ганглиях тройничного нерва. iv
Каким бывает лечение

Небольшое количество Мази аккуратно втирают на область поражения кожи три-четыре раза в сутки Продолжительность терапии от пяти дней до недели. Небольшую полоску геля наносят ватной палочкой или шпателем на предварительно подсушенную пораженную поверхность три-пять раз в день в течение пяти-шести дней. При необходимости курс можно продолжать до прекращения клинических проявлений. Лечение рекомендуется начинать сразу при появлении первых симптомов на коже и слизистых (боль, зуд, покалывание, отек и покраснение кожи). Если заболевание рецидивирующее, то предпочтительнее начинать лечение до появления симптомов или в самом начале (у женщин рецидивы могут быть связаны с менструальным циклом). Пациентам предписан щадящий режим, не рекомендуются водные процедуры. Для облегчения симптомов назначают антигистаминные, жаропонижающее и антисептические препараты для обработки очагов поражения кожи. После перенесенного заболевания можно провести курс дезинтоксикации.
Протоколы лечения Министерства здравоохранения РФ
Применение интерферона альфа отражено в следующих клинических рекомендациях, одобренных, в том числе, Министерством здравоохранения Российской Федерации (протоколах лечения):
– Оказание медицинской помощи детям больным инфекционным мононуклеозом v
– Оказание медицинской помощи детям больным ветряной оспой vi
– Оказание медицинской помощи детям больным цитомегаловирусной инфекцией vii
Герпетический энцефалит — это диффузное или очаговое поражение мозгового вещества, вызванное герпесвирусами ВПГ-1, ВПГ-2, Varicella Zoster. Основные симптомы болезни: фебрильная лихорадка, прогрессирующее угнетение сознания, судорожные приступы. По завершении острого периода инфекции в течение длительного времени сохраняются резидуальные неврологические нарушения. Для установления диагноза необходимо проведение ПЦР-диагностики ликвора, томографии головного мозга, электроэнцефалограммы. Лечение патологии включает противовирусные препараты, противоотечную, нейрометаболическую и противосудорожную терапию.
МКБ-10
Общие сведения
Энцефалит герпетического происхождения составляет до 15-20% всех вирусных воспалительных процессов в мозговой ткани. Симптомы встречаются с частотой 4-5 случаев на 1 млн. населения, причем до трети больных составляют дети, а еще около 20% приходится на возрастную категорию старше 60 лет. Заболевание не теряет своей актуальности в современной неврологии, поскольку для успешного исхода патологии необходимо вовремя поставить диагноз и начать лечение, а промедление в оказании медицинской помощи чревато смертью пациента.

Причины
Болезнь в 95% случаев вызывается вирусом простого герпеса 1 типа, что объясняется высокой распространенностью возбудителя. По данным ВОЗ, около 2/3 населения мира в возрасте до 50 лет инфицированы ВПГ-1. На втором месте по частоте находится Varicella Zoster Virus (VZV) — возбудитель ветряной оспы, опоясывающего герпеса. Энцефалит, вызванный ВПГ-2, встречается редко, преимущественно у иммунокомпрометированных пациентов.
Ведущим среди факторов риска служит сниженный иммунный статус. Герпетическая инфекция протекает латентно, активизируется на фоне нарушения общей резистентности организма (при переохлаждении, стрессе, менструации у женщин). В группе риска находятся люди с врожденными и приобретенными иммунодефицитами, больные, получающие лечение иммуносупрессивными препаратами. К триггерам относят реинфицирование другими штаммами герпесвирусов, сопровождающееся аутоиммунными реакциями.
Патогенез
Первичное заражение ВПГ-1, как правило, происходит в детстве при попадании вирусных частиц на слизистые оболочки, после чего возбудитель начинает размножаться, мигрирует в нервные ганглии, где длительное время находится в состоянии латентной инфекции. Заражение ВПГ-2 наблюдается после начала сексуальной жизни через слизистые половых путей, а дальнейший путь развития патогена сходен с ВПГ-1.
Симптомы болезни в большинстве случаев возникают при реактивации инфекции под действием провоцирующих факторов. Герпесвирусы проникают в головной мозг гематогенным путем либо по нервным стволам (через тройничный или обонятельный нерв). Из гассерова узла они распространяются на таламус, подкорковые ядра, кору больших полушарий. При распространении по ольфакторному тракту первой страдает лимбическая система (гиппокамп, височная кора).
Симптомы герпетического энцефалита
В типичном течении острого мозгового воспаления выделяется несколько последовательных стадий: ранняя, период разгара болезни, регресс признаков, стадия остаточных явлений. В 70% патология манифестирует с внезапно возникшей высокой лихорадки (более 39°С), сопровождающейся интенсивными головными болями в лобно-височной зоне, сильной сонливостью, рвотой, не связанной с приемом пищи.
На вторые-третьи сутки симптомы дополняются нарушениями сознания: больные начинают путаться во времени и пространстве, не узнают родственников, испытывают разнообразные галлюцинации. По мере усугубления тяжести состояния появляются фокальные или генерализованные судорожные припадки. Изредка наблюдается оперкулярный автоматизм — повторяющиеся причмокивающие или сосательные движения.
В среднем через 3 дня заболевание переходит в стадию разгара. Основное проявление — глубокое угнетение сознания вплоть до комы. Пациенты не отвечают на звуковые и тактильные раздражители, однако двигательные реакции на болевые стимулы остаются в пределах нормы. Также могут возникать симптомы декортикации или децеребрации, аритмичное дыхание, двусторонние моторные нарушения.
Если пациенту было предоставлено комплексное лечение, с 3-4 недели начинается обратное развитие симптомов герпетического энцефалита. Этот этап длится от нескольких месяцев до 1 года, характеризуется постепенным восстановлением временно утраченных неврологических функций. По окончании третьей стадии около 80% больных имеют стойкие резидуальные (остаточные) явления, которые могут сохраняться пожизненно.
Осложнения
В остром периоде прогностическим неблагоприятным является прогрессирование отека мозга, что чревато его вклинением. При височно-тенториальной форме вклинения возникает триада признаков: потеря сознания, гемипарез, анизокория. Симптомами транстенториальной формы являются отсутствие реакции зрачков на свет, фиксация глазных яблок по срединной линии, двусторонний гипертонус мышц. Зачастую нарушается работа дыхательного центра.
Патология имеет тяжелое течение, при отсутствии своевременной медицинской помощи летальность достигает 70%. Даже если проводится этиотропное лечение, смертельный исход регистрируется у 15-20% пациентов, чаще у младенцев, пожилых людей, больных из группы риска. У выздоровевших полный регресс неврологической симптоматики наблюдается только в 20% случаев, а остальные сталкиваются с резидуальными симптомами.
Наиболее опасным хроническим осложнением заболевания считается прогрессирующее вегетативное состояние (акинетический мутизм), характеризующийся необратимым разрушением высших психических функций. У больных сохранено сознание, витальные функции (дыхание, кровообращение), однако полностью отсутствует познавательная деятельность. Такие пациенты не говорят, не реагируют на внешние раздражители, требуют постоянного ухода.
К типичным последствиям герпетической формы энцефалита относится синдром Клювера-Бьюси, при котором развиваются тяжелые длительные расстройства психической и когнитивной сферы. Симптомы расстройства включают ажитированное состояние, агрессивность, патологическую гиперсексуальность. Также наблюдаются интеллектуальные нарушения, проблемы с концентрацией внимания, ослабление памяти.
Диагностика
Обследованием пациента занимаются инфекционисты, неврологи, врачи экстренной помощи и реанимационного отделения. Заподозрить энцефалит удается по острому началу, наличию фебрильной лихорадки, сочетанию общемозговых и очаговых симптомов. Для подтверждения заболевания, уточнению этиологии воспалительного процесса назначаются следующие методы исследования:
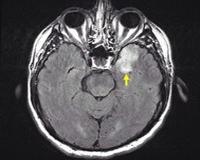
- Нейровизуализация. «Золотым стандартом» диагностики является МРТ головного мозга, чувствительность которой при выявлении очагов поражения достигает 100% на ранней стадии болезни. При недоступности этого метода либо на более поздних этапах герпетического энцефалита применяется КТ головного мозга.
- Электроэнцефалография. В острый период ЭЭГ показывает очаговые или диффузные нарушения биоэлектрической мозговой активности: высокоамплитудные дельта- и тета-волны, появление комплексов «острая‒медленная волна».
- Люмбальная пункция. Цереброспинальная жидкость имеет нормальную прозрачность, при микроскопическом исследовании обнаруживается лимфоцитарный плейоцитоз (около 100 клеток в 1 мл), повышение количества белка, снижение уровня глюкозы.
- ДНК-диагностика. Чувствительность ПЦР-исследования ликвора на герпесвирусы составляет 96-98%, а специфичность достигает 94%. Поскольку в ранний период инфекции не исключены ложноотрицательные результаты, тестирование обязательно повторяют на 4-й день заболевания.
Лечение герпетического энцефалита
Консервативная терапия
Герпетический энцефалит характеризуется быстрым нарастанием неврологического дефицита, прогрессированием общемозговых симптомов, поэтому комплексное лечение должно начинаться в максимально ранние сроки. Наилучшие шансы на полное выздоровление у пациентов, которые начали получать этиотропные препараты в первые сутки манифестации болезни. Лечение заболевания включает следующие группы медикаментов:
- Противовирусные средства. Препаратом выбора является ацикловир, вводимый внутривенно капельно при подозрении на герпетический энцефалит еще до лабораторного подтверждения диагноза. Критерий завершения терапии — отрицательный тест ПЦР ликвора.
- Интерфероны. При тяжелых формах энцефалита целесообразно сочетать иммуномодуляторы с этиотропными противовирусными медикаментами. Применяются интерфероны или индукторы интерферонов, усиливающие неспецифическую резистентность организма.
- Глюкокортикоиды. В основном назначаются для купирования мозгового отека. Также гормоны используются в случае рецидивирующей герпетической инфекции, при которой в организме развивается аутоиммунный процесс.
- Диуретики. Лекарства показаны при отеке-набухании головного мозга. Экстренная дегидратация проводится с помощью осмодиуретика маннитола или салуретика фуросемида. Также рекомендованы онкодегидратанты (альбумин), глицериновые растворы для зондового введения в желудок.
- Антиконвульсанты. Медикаменты «первой линии» для устранения судорожного синдрома — бензодиазепины. При их недостаточной эффективности лечение усиливается препаратами для наркоза, барбитуратами.
Реабилитация
Благотворное влияние на состояние ЦНС после перенесенного герпетического энцефалита оказывают витаминные комплексы (витамины группы В, аскорбиновая кислота) в сочетании с антиоксидантами. Восстановительное лечение также включает ноотропы и нейрометаболические препараты для улучшения когнитивных мозговых функций. Коррекция иммунологического статуса проводится адаптогенами, актопротекторами, неспецифическими иммуномодуляторами.
Для восполнения энергозатрат организма, стимуляции репаративных процессов показано адекватное по калорийности и витаминному составу энтеральное питание. Большое внимание уделяется физиотерапевтическим процедурам, массажу и лечебной физкультуре, направленным на улучшение двигательной функции. При наличии показаний рекомендуются занятия с логопедами, дефектологами.
Прогноз и профилактика
Несмотря на проводимое этиотропное лечение, прогноз при герпетическом энцефалите остается неблагоприятным, показатель летальности составляет 15-20%. У большинства выздоровевших сохраняется неврологический дефицит. Для предупреждения заболевания необходима рациональное лечение герпеса кожи и слизистых оболочек, своевременное консультирование больных с диссеминированной герпетической инфекцией.
2. Менингиты и энцефалиты: уч. пос. для врачей/ Д. А. Валишин, Р. Т. Мурзабаева, А. П. Мамон, М. А. Мамон, Л. В. Мурзагалеева. — 2012.
3. Герпетическое поражение нервной системы/ М.Н. Лебедюк, М.Э. Запольский, Ю.И. Горанский// Украинский журнал дерматологии, венерологии, косметологии. — 2011. — №2.
4. Герпетический энцефалит/ Т.В. Матвеева, Н.В. Токарева, Г.А. Шакирзянова// Неврология. — 2006. — №16.

Вирус герпеса может быть причиной деменции, считают ученые из США. Белок оптиневрин ограничивает распространение вируса на том этапе, когда он еще не успевает поразить нервные клетки, однако, если этого не происходит, у зараженного возрастает риск развития нейродегенеративных заболеваний. Исследователи полагают, что таким свойством могут обладать все герпесвирусы, поражающие человека.
Герпесвирусы — обширное семейство, насчитывающее почти 90 видов вирусов, поражающих млекопитающих, птиц, рыб, рептилий и земноводных. Человек уязвим лишь для восьми из них. При этом после заражения, например, вирусами простого герпеса I и II типа, избавиться от инфекции в организме уже невозможно. Вирус сохраняется в латентной форме, напоминая о себе в среднем несколько раз в год высыпаниями, преимущественно в районе губ или половых органов. Вирусом простого герпеса I типа, по разным оценкам, заражено до 90% населения планеты.
Ранее вирус простого герпеса I типа уже связывали с болезнью Альцгеймера — у людей с HSV-1 заболевание возникает чаще, а вирусная ДНК определяется в амилоидных бляшках.
Однако достаточно подробных исследований, посвященных связи вирусов герпеса с нейродегенеративными заболеваниями и поиску возможных механизмов, повышающих риски, не проводилось.

Заняться поиском факторов, с помощью которых вирусы делают мозг более предрасположенным к дегенерации нервных клеток, решили специалисты Иллинойсского университета в Чикаго. Свои выводы они изложили в статье в журнале Nature Communications.
Исследователи хотели выяснить, почему HSV-1 может стать смертельным для людей с ослабленным иммунитетом, но не наносит серьезного вреда здоровым людям. Герпесвирусы инфицируют центральную нервную систему и могут приводить к энцефалиту и прочим поражениям мозга. Однако в большинстве случаев организм подавляет первичную инфекцию прежде, чем она успевает нанести ЦНС серьезный ущерб.
В механизме защиты может играть роль белок оптиневрин, предположили ученые. Оптиневрин — рецептор, способный склонить белки вируса к аутофагии.
«Оптиневрин останавливает рост вируса, это происходит путем аутофагии — захвата частиц вируса внутри крошечных везикул, называемых аутофагосомами. Происходящая аутофагия очень избирательна. Это может быть важно для понимания того, как организм борется и с другими вирусами», — говорит доктор Дипак Шукла, один из авторов работы.
Чтобы проверить эту версию, исследователи использовали линию генетически модифицированных мышей, у которых не синтезировался оптиневрин. Их и обычных мышей ученые заразили HSV-1. У мышей без оптиневрина вирус беспрепятственно размножался в мозге, уничтожая нейроны и, в конечном итоге, приводя к смерти грызунов.
Ген, регулирующий выработку оптиневрина, может мутировать и естественным образом, отмечают авторы работы.
«Если у вас есть и мутировавший оптиневрин, и герпес, это катастрофа с точки зрения нейродегенерации», — говорит Шукла.
«Исследование также показывает, что при дефиците оптиневрина нарушается иммунный ответ, — добавляет Чандрашекхар Патил, соавтор исследования. — Оптиневрин необходим для подачи сигнала о притоке соответствующих иммунных клеток в место инфекции. Когда у вас его нет, возникают проблемы».
Поскольку вирус герпеса остается в нервных клетках, исследователи полагают, что он может быть фактором, повышающим риск развития нейродегенеративных заболеваний. Чтобы постоянно бороться с вирусом, иммунной системе приходится запускать воспалительные процессы, и это сказывается на состоянии нейронов не лучшим образом.
Мыши без оптиневрина, зараженные HSV-1, через 30 дней теряли способность распознавать объекты. По словам Шуклы, это может свидетельствовать, что наличие вируса вкупе с мутацией способно ускорить повреждение нейронов привести к когнитивным нарушениям.
По мнению авторов работы, результаты могут касаться всех видов герпесвирусов, поражающих человека. Хотя исследование проводилось на мышах, у ученых нет сомнений, что и в человеческом мозге отсутствие оптиневрина приведет к тем же последствиям — ускоренной дегенерации нервных клеток. Исследователи планируют дополнительно изучить возникающие естественным образом мутации гена, регулирующего выработку оптиневрина — так, известно, что они наблюдаются у людей с глаукомой. Теперь же предстоит выяснить, как они влияют на здоровье при наличии в организме HSV-1 и других вирусов герпеса.

ТАСС, 8 мая. Молекулярные биологи выяснили, какой механизм защищает вирус герпеса от врожденной иммунной системы и помогает ему проникать в клетки мозга человека. Изучение этого механизма позволит создать лекарства, которые защитят нервную систему от заражения герпесом, пишут ученые в Journal of Experimental Medicine.

"Наше исследование показывает, что вирус герпеса удаляет определенные метки с поверхности белка STING. Это помогает инфекции распространиться и открывает дорогу для развития вирусного энцефалита. Лекарства, которые смогут заблокировать эту способность вируса, дадут клеткам мозга шанс на борьбу с герпесом", – рассказал один из авторов исследования, биолог из Орхусского университета (Дания) Чиранджеви Бодда.
Герпес – одна из самых распространенных человеческих инфекций. Разновидности возбудителя герпеса поражают разные части тела: к примеру, вирус HHV1 вызывает простуду на губах, HHV2 проникает в половые органы, а вирусы HHV6 и HHV7 вызывают псевдокраснуху – непродолжительную лихорадку и сыпь.
Достаточно долгое время вирус герпеса, в особенности HHV1, считали достаточно безобидным. Однако недавно ученые выяснили, что он может быть одной из причин болезни Альцгеймера, рассеянного склероза, энцефалита, рака половых органов и других болезней. Кроме того, человек остается носителем герпеса всю жизнь, поскольку сейчас от этой инфекции нет вакцин и лекарств.
Бодда и его коллеги отмечают, что зачастую вирус герпеса поражает не только кожу или половые органы человека, он проникает еще и в клетки мозга, распространяясь через периферийные нервы. В некоторых редких случаях, а также у носителей ВИЧ и других людей с подорванным иммунитетом, из-за этого появляется вирусный энцефалит, и пациент в результате погибает.
Невидимый вирус
Как именно это происходит, ученые не знали, так как врожденный иммунитет нейронов и вспомогательных клеток мозга работает не так, как у клеток кожи и других органов, которые обычно поражает герпес. Датские и британские молекулярные биологи восполнили этот недостаток, экспериментируя на культурах клеток мозга мышей.
Для этих опытов ученые создали несколько мутантных штаммов вируса HHV1 из генома которых был удален один из генов. Заражая ими нейроны мышей, ученые пытались понять, какую роль играли эти участки ДНК в процессе заражения и скрытия вируса от белков врожденной иммунной системы.
Опыты показали, что ключевую роль в этом процессе играл вирусный ген и связанный с ним белок VP1-2. Когда герпес проникал в клетки мозга, этот белок начинал соединяться с молекулами белка STING, одного из главных стимуляторов врожденного иммунитета. VP1-2 "откусывал" от STING особые цепочки аминокислот, так называемые убиквитины.
В результате активность STING резко снижалась, защитные системы нейронов переставали видеть вирус. В свою очередь, после того, как ученые удалили VP1-2 из генома вируса герпеса, иммунитет мышей начинал атаковать вирусные частицы. В итоге герпес переставал распространяться или резко замедлялся.
Соответственно, блокировка работы белка VP1-2 с помощью различных лекарств теоретически может защитить мозг человека от энцефалита и других последствий проникновения герпеса в нервную систему. Как надеются ученые, опыты на мышах помогут им быстро создать первые прототипы подобных молекул.
Читайте также:

