Как можно вылечить себя от эпидермиса
Обновлено: 25.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Демодекоз: причины появления, симптомы, диагностика и способы лечения.
Определение
Демодекоз – паразитарное кожное заболевание, которое вызывает клещ-железница (Demodex). Клещ размножается в волосяных фолликулах, сальных железах кожи и мейбомиевых железах (видоизмененных сальных железах, располагающихся по краю века) и поражает в основном кожу лица и наружных ушных раковин, хотя в редких случаях может мигрировать на кожу груди и спины. Питательной средой, необходимой для размножения клеща, служит кожное сало (себум).
Носителями клеща могут быть многие люди, но заболевание проявляется остро только при нарушении микробного биоценоза кожи и снижении иммунитета.
В таких случаях клещ начинает активно размножаться, в результате чего на коже формируются асимметричные шелушащиеся розовые пятна, телеангиэктазии, розовая или красная сыпь, на месте которой затем возникают пустулы (пузырьки с гноем) или везикулы (пузырьки с прозрачной жидкостью). Кожа в этих местах воспаляется, утолщается и покрывается мокнущими корочками. При отсутствии лечения поражение кожи может усиливаться, захватывая более глубокие слои.
Причины появления демодекоза
Клещ-железница относится к условно-патогенным организмам и у 90% людей входит в состав нормального микробного биоценоза кожи лица, при этом никак себя не проявляя. Активное размножение клеща становится возможным, если биоценоз нарушается, а местный иммунитет снижается. Чаще всего изменение микробной среды происходит вследствие различных кожных заболеваний (воспалительных, бактериальных), использования иммуносупрессантов (препаратов, снижающих иммунную защиту), например, местных стероидных мазей. Распространению демодекоза способствуют нарушения в работе нервной, сосудистой и эндокринной систем, заболевания желудочно-кишечного тракта, патологии обменных процессов.
Немаловажным фактором развития заболевания служит повышенное образование кожного сала и изменение его состава. Увеличение поверхностных липидов в составе себума приводит к усиленному размножению патогенной флоры, которая, в свою очередь, инициирует активность клеща. Гиперпродукция кожного сала возникает у женщин в период гормональной перестройки, а также в результате эндокринных заболеваний и генетической предрасположенности. Существенную роль в активизации клеща играет уровень инсоляции, влияющий на усиление продукции себума.
В жаркое время года регистрируется всплеск заболеваемости демодекозом, что связано с повышенной выработкой провоспалительных веществ из-за чрезмерного воздействия ультрафиолетовых лучей.
Классификация заболевания
Демодекоз относится к группе паразитарных заболеваний кожи. Различают две клинические формы – первичный и вторичный демодекоз. При внезапном всплеске размножения клещей (более 5 особей на 1 см 2 кожи), отсутствии сопутствующих дерматитов (акне, розацеа, себореи) и успешном излечении после терапии с использованием противопаразитарных средств ставят диагноз «первичный демодекоз». Как правило, заболевание отмечают у пациентов старше 40 лет.
При наличии сопутствующих поражений кожи (акне, розацеа, перорального дерматита и т.д.), системных заболеваний (лейкоза, ВИЧ и др.) диагностируют вторичный демодекоз. Чаще всего он возникает у пациентов со значительно ослабленным иммунитетом. Иногда к вторичному демодекозу приводят терапия ингибиторами рецепторов эпидермального фактора роста, хроническая почечная недостаточность и УФ-воздействие. Заболевание может манифестировать в любом возрасте и характеризоваться значительной площадью поражения и выраженностью симптомов. Поражение век приводит к демодекозному блефароконъюнктивиту (воспалению век и их слизистой оболочки, прилежащей к глазу), который возникает как изолированно, так и параллельно с демодекозом кожи лица.
В зависимости от характера проявлений на коже различают:
- Акнеформный демодекоз. На коже присутствуют папулы и пустулы, напоминающие высыпания при угревой сыпи.
- Розацеаподобный демодекоз. Папулы появляются на фоне разлитой эритемы (покраснения кожи).
- Себорейный демодекоз. Сыпь на коже сопровождается пластинчатым шелушением.
- Офтальмологический демодекоз. Кожа век воспалена, присутствует чувство инородного тела в глазах.
На коже человека паразитируют два вида клеща Demodex folliculorum (длинный клещ) и Demodex brevis (короткий клещ).
В зависимости от вида клеща преобладают те или иные элементы поражения кожи. Развитие Demodex folliculorum чаще приводит к эритеме и слущиванию эпителия кожи. Demodex brevis вызывает формирование конусовидных папул, покрытых серыми чешуйками. Иногда отмечаются симметричные папулопустулезные элементы (пузырьки с прозрачной жидкостью или гноем), окруженные воспалительным инфильтратом.
Иногда размножение клещей приводит к присоединению вторичной гнойной инфекции, в ходе которой развиваются крупные гнойные пустулы и даже абсцессы.
При локализации клеща на коже век на краю ресниц и вокруг них образуются чешуйки и своеобразный «воротничок». Больной жалуется на зуд, усиливающийся под воздействием тепла и УФ-лучей, ощущение инородного тела в глазах, усталость глаз, чувство жжения. В углах глаз скапливается вязкое и клейкое отделяемое, особенно по утрам. Кожа становится сухой и истонченной, а пораженные демодекозом участки утолщаются и покрываются мокнущими корками.
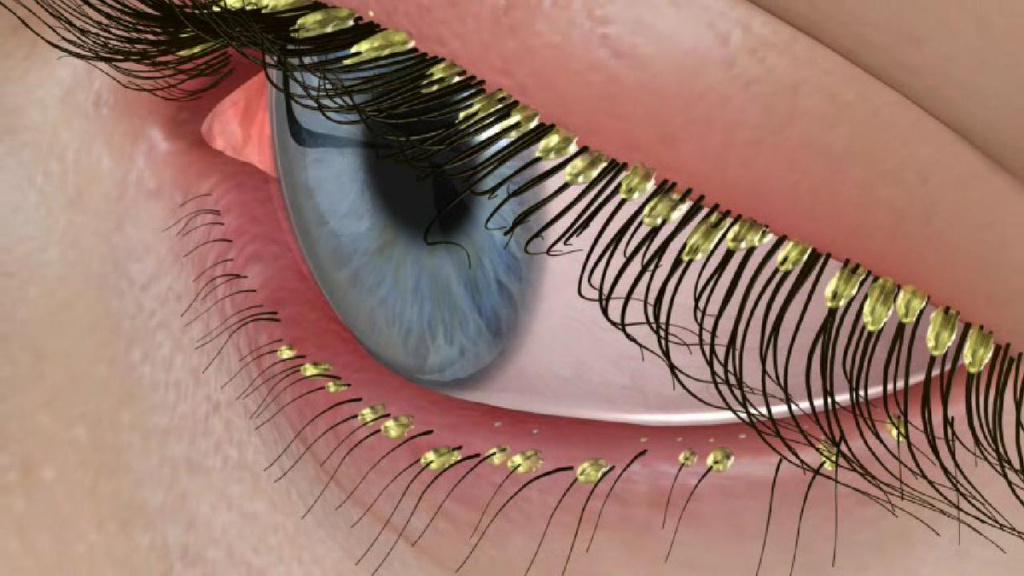
Длительное течение заболевания может привести к потере ресниц и замещению волосяных фолликулов рубцовой соединительной тканью.
Диагностика демодекоза
Выявить демодекоз можно лишь по совокупности клинических признаков и с помощью лабораторной диагностики. Кожные проявления при демодекозе могут существенно варьироваться, «маскируясь» под другие заболевания, что затрудняет постановку диагноза. Так, при акнеформном демодекозе папулы и пустулы напоминают угревую сыпь, при розацеаподобной форме папулы и пустулы появляются на фоне эритемы, при себорейной форме сыпь покрывается сероватыми корочками.
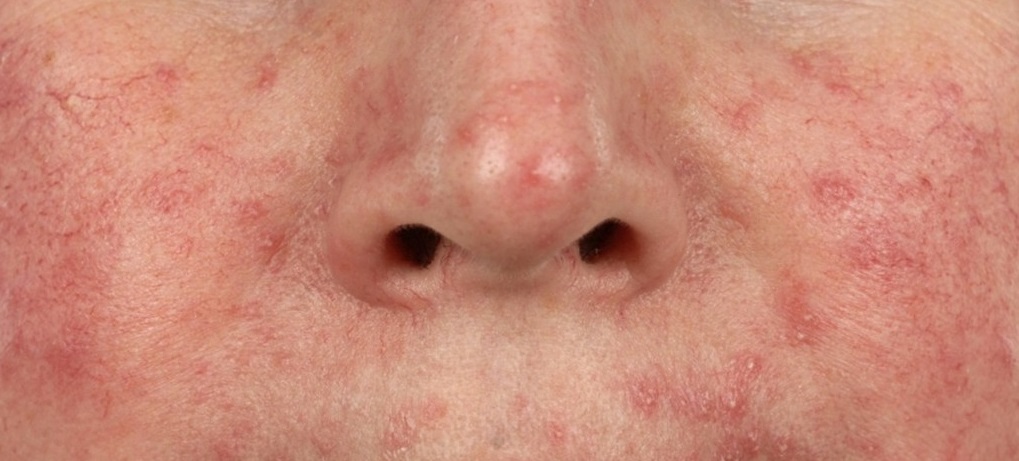
Такие разнообразные проявления демодекоза делают обязательной лабораторную диагностику для выделения клещей из очагов поражения.
Лабораторная диагностика предусматривает микроскопию секрета сальных желез и содержимого пустул.
Информацию о приеме биоматериала в медицинских офисах необходимо заранее уточнить, позвонив в справочную службу ИНВИТРО по телефону. Клещ-железница размерами 0,2-0,5 мм, рода Demodex (Demodex folliculorum, Demodex brevis), является частым эктопаразитом человека. Он вызывает демодекоз, относящи.
Новообразования (неоплазии) – это медицинское название опухолей, т. е. избыточного разрастания какой-либо ткани в организме. Опухоли – результат бесконтрольного размножения клеток, которые еще не достигли зрелости и потому утратили свою способность полноценно выполнять свои функции.
Опухоли могут возникать во внутренних органах и на поверхности кожи. Многие, не зная, какие бывают новообразования на коже, при появлении любого новообразования на коже ошибочно полагают, что это рак. На самом деле это не всегда так.
По основной классификации новообразования кожи делятся на доброкачественные и злокачественные. Еще существуют предраковые образования – пограничные между двумя основными видами. У каждого типа есть свои подвиды и особенности, а для постановки точного диагноза нужна правильная диагностика.
Доброкачественные новообразования кожи
У доброкачественных новообразований обычно не нарушается способность к дифференцировке клеток. Т. е. они сохраняют свои первоначальные функции и по структуре схожи с нормальными клетками. Еще такие клетки медленно растут, могут давить на соседние ткани, но никогда в них не проникают.
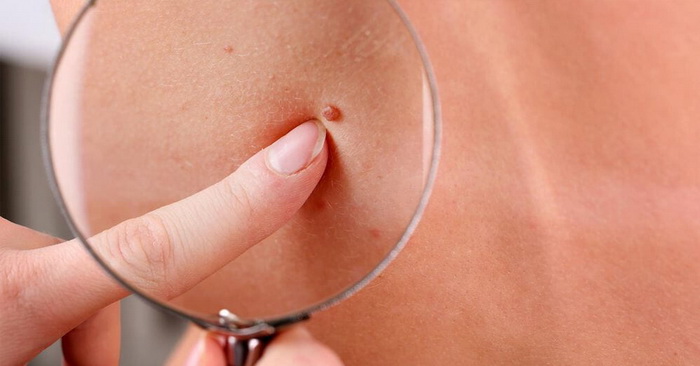
Виды доброкачественных новообразований кожи:
- Атерома – опухоль сальной железы, которая образуется из-за ее закупорки. Чаще всего встречается там, где больше всего сальных желез: на шее, спине, голове, в паховой области.
- Гемангиома – сосудистая опухоль, которая образуется из клеток кровеносных сосудов. Имеет цвет от красного до синюшно-черного.
- Папиллома и бородавки. Образование в виде небольшого узелка или сосочка. Причина – вирус папилломы человека (ВПЧ). Обычно возникают на фоне стрессов, снижения иммунитета, вегетативных расстройств. Часто появляются в области подмышек, паховой зоне. Еще папилломы – самые распространенные новообразования кожи век.
- Лимфангиома – опухоль из стенок лимфатических сосудов, которая формируется еще внутри утробы. Внешне это небольшие образования с бугристой поверхностью синюшной или красно-бурой окраски.
- Липома – опухоль жировой прослойки («жировик»). Располагается в подкожном слое, чаще всего в области верхней части спины, плечевого пояса, наружной поверхности бедер. Опухоль безболезненная, мягкая и подвижная.
- Фиброма – образование из соединительной ткани. Чаще встречается у женщин молодого и среднего возраста. Выглядят как новообразование на коже в виде шарика, выступающего над ее поверхностью.
- Нейрофиброма – опухоль из клеток оболочек нервов. Внешне выглядит как плотный бугорок размером 0,1-2,3 см.
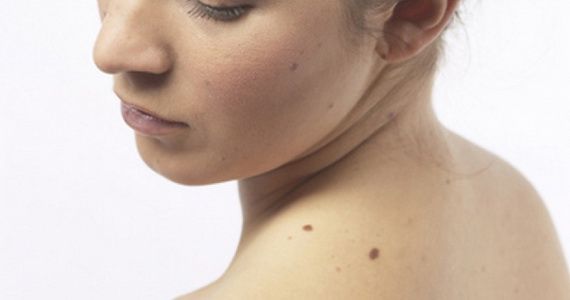
В отдельную группу новообразований относят невусы (родинки). Это новообразования кожи разного цвета: коричневого, красного, черного, фиолетового и пр. В большинстве случаев невус – это врожденный порок развития кожи. Но родинки могут появляться и в течение жизни, чаще всего под действием солнечного света. Невусы не имеют склонности к злокачественному перерождению, но в отдельных случаях это может происходить вследствие повреждения или травмы кожи на родинке.
Несмотря на отсутствие прямой опасности, все доброкачественные виды новообразований на коже лица, рук, ног и других частей тела требуют постоянного контроля. Необходимо следить, чтобы опухоли не разрастались, не увеличивались в размерах, не меняли цвет. В противном случае нужно обратиться к врачу.
Предраковые новообразования (преканкрозы)
Предраковыми называют новообразования, которые под воздействием врожденных или текущих причин получили склонность к злокачественному перерождению. Как правило, это хронические состояния, которые наблюдаются у человека в течение длительного времени.
Таким образом, предраковые опухоли – опасные новообразования на коже, которые могут приводить к развитию онкологических процессов. К ним относятся:
- Старческая кератома – кератоз, при котором на коже у пожилых людей возникают сухие корки и чешуйки. При их отслаивании может возникать легкая кровоточивость.
- Пигментная ксеродерма – наследственная опухоль, развивающаяся из-за повышенной чувствительности кожи к ультрафиолету. Встречается редко, представляет собой пигментные пятна, которые становятся бородавчатыми разрастаниями.
- Кожный рог – конусообразная опухоль, внешне напоминающая рог. Имеет желтый или коричневый цвет. возникает на открытых участках тела, которые регулярно подвергаются трению или сдавливанию. Характерен для людей пожилого возраста
- Болезнь Боуэна – внутриэпидермальный рак. Без лечения может трансформироваться в инвазивный рак кожи. На ранней стадии болезнь Боуэна представляет собой небольшое красновато-коричневое пятно размером 2-50 мм. имеет шелушащуюся поверхность, приподнятые неровные края. После удаления чешуек остается мокнущая, но не кровоточащая поверхность.
Злокачественные новообразования кожи
Самые опасные виды новообразований на коже – злокачественные. От доброкачественных они отличаются тем, что быстро растут, проникают в окружающие ткани и дают метастазы в отдаленные от очага области. Организм не контролирует деление клеток в таких опухолях, а сами они теряют способность выполнять свои первоначальные функции.
Признаки перерождения доброкачественной опухоли в один из видов злокачественных новообразований на коже:
- быстрое или резкое увеличение опухоли в размерах;
- появление язв, кровоточивость;
- распространение на соседние ткани;
- изменение цвета или степени насыщенности пигментации.
Основные виды злокачественных опухолей кожи:
- Меланома – наиболее распространенный вид. Чаще всего возникает из родинок из-за травмирования или избыточного воздействия ультрафиолета.
- Базалиома – плоскоклеточный рак кожи из атипичных клеток базального слоя эпидермиса. Внешне выглядит как белый узелок с сухой коркой на поверхности. По мере прогрессирование увеличивается в ширину и превращается в глубокую язву.
- Саркома Капоши. Представляет собой множественные опухоли пурпурного, фиолетового и лилового цвета. Они объединяются и превращаются в язвы.
- Липосаркома – злокачественная опухоль жировой ткани, возникающая на фоне липом и атером.
- Фибросаркома – новообразование из соединительной ткани, чаще всего нижних конечностей. Имеет темный сине-коричневый цвет, может заметно выступать над кожей.
Специалисты рекомендуют удалять как доброкачественные, так и злокачественные новообразования. Это оптимальный метод лечения, если к нему нет противопоказаний. В случае с доброкачественными новообразованиями и предраковыми состояниями при своевременном лечении прогноз благоприятный.
При злокачественных опухолях требуется больше усилий, и прогноз может быть не столь благоприятным, особенно если уже наблюдается метастазирование. Поэтому при подозрении на злокачественные процессы важно как можно раньше обратиться к врачу.
В представленной статье обобщены современные данные о строении и функции эпидермального барьера, рассмотрены вопросы его роли в развитии атопического дерматита.
This article summarizes current data on the structure and function of the epidermal barrier, we also considered its role in development of atopic dermatitis.
С тех пор как наземная жизнь стала угрожать млекопитающим обезвоживанием, все более становятся актуальными исследования структурных, клеточных, биохимических и регуляторных механизмов организма, участвующих в поддержании гомеостаза проницаемости эпидермального барьера [1].
Кожа обеспечивает жизненно важную функцию, защищая позвоночных от повседневных и экстремальных влияний факторов внешней среды, таких как воздействие антигенов, ультрафиолетового света, моющих средств, микроорганизмов, токсинов, наночастиц и иных повреждений [2]. Таким образом, эпидермальный барьер, являясь физическим барьером [3], обеспечивает защиту организма на границе двух сред, ограничивая как потерю воды из организма, так и попадание патогенных микроорганизмов в организм [4].
Важнейшая составная часть эпидермального барьера, от которой зависит проникновение раздражителей и аллергенов, находится в нижней части рогового слоя [5]. Несмотря на минимальные размеры (толщина около 7–35 мкм), он играет определяющую роль в формировании защитного барьера и способствует предотвращению чрезкожного проникновения патогенов. Кроме роли физического барьера, роговой слой участвует в терморегуляции, газообмене, гидратации, обеспечении врожденного иммунитета, а создавая определенную pH поверхности кожи (слегка кислую), обеспечивает дополнительную защиту от болезнетворных микроорганизмов [6].
Во время терминальной дифференцировки кератиноциты зернистого слоя «заменяют» свою клеточную мембрану на нерастворимый белковый слой — роговую оболочку [7]. Она придает прочность корнеоцитам и является «платформой» для прикрепления липидов. Роговая оболочка в основном сформирована структурными белками, такими как лорикрин, инволюкрин, филаггрин (ФЛГ) и малыми пролин-богатыми белками. Особенно важен филаггрин, объединяющий кератиновые волокна клеток, «скручивая» кератиноциты в уплощенные диски с большой площадью поверхности [8].
Вокруг корнеоцитов расположены холестерин, фосфолипиды и церамиды, создавая многослойную мембрану из липидных пластинок [3, 9]. Последние играют важную роль в регуляции водного гомеостаза кожи, помогают сохранять воду в организме, а также предотвращают проникновение патогенных микроорганизмов и аллергенов [10].
На границе между роговым и зернистым слоями происходит секреция ламеллярных телец, содержащих предшественники липидов, а также необходимые ферменты для переработки этих прекурсоров в зрелые составляющие липидной матрицы [11]. Перед секрецией происходит сборка ламеллярных телец в пластинчатом комплексе, посредством дифференцированной их упаковки с различным содержимым [12]. Кроме вышеупомянутых метаболитов липидов, липидные тельца доставляют в межклеточное пространство рогового слоя протеолитически активные ферменты, такие как сериновые протеазы семейства калликреина, а также их ингибиторов, в том числе и лимфоэпителиальный ингибитор сериновых протеаз типа Kazal-5 (LEKTI) [13].
Единство между корнеоцитами рогового слоя зависит прежде всего от корнеодесмосом. Подобно десмосомам, они поддерживают целостность тканей посредством молекул межклеточной адгезии с помощью кальций-зависимых взаимодействий между двумя представителями семейства кадгерина, внеклеточных трансмембранных гликопротеинов — десмоглеина и десмоколлина. Внутри корнеоцитов десмоглеин и десмоколлин соединяют кератиновые филламенты корнеодесмосом посредством «соединительной бляшки», состоящей из плакоглобина, десмоплакина и плакофиллина. Десмоглеин и десмоколлин перемещаются от оболочки корнеоцитов в липидную пластину между корнеоцитами и связывают воедино белки соседних клеток. Кроме того, в процессе кератинизации эпителия экспрессируется специфический белок с молекулярной массой 52 кДа — корнеодесмосин [8, 14]. После секреции в экстрацеллюлярное пространство корнеодесмосин перемещается в область между зернистым и роговым слоями и проникает в десмосому. Появление корнеодесмосина знаменует переход от десмосом к корнеодесмосомам [3, 12].
Во время «нормальной» десквамации рогового слоя самые поверхностные корнеоциты «уходят» с поверхности кожи, замещаясь кератиноцитами, подвергшимися терминальной дифференцировке [14, 15]. Таким образом, существует «тонкий» баланс между базальной клеточной пролиферацией и десквамацией рогового слоя. Это обеспечивает постоянное обновление клеток эпидермиса, а также способствует поддержанию одинаковой толщины эпителия [14, 16]. Caubet и соавт. [15] описали несколько деградационных протеаз, которые разрушают внеклеточные корнеодесмосомальные адгезивные белки, связывающие корнеоциты вместе.
В роговом слое среди протеаз, вовлеченных в процесс десквамации, присутствуют хемотрипсиновые (SCCE) и трипсиновые ферменты (SCTE), которые экспрессируются кератиноцитами зернистого слоя и находятся во внеклеточном пространстве рогового слоя [14]. Данные протеазы гидролизуют корнеодесмосин и десмоколлин [15]. Их активность контролируется семейством специфических ингибиторов, в которое входит LEKTI [17]. При этом скорость десквамации коррелирует с количеством ингибиторов протеаз, поступивших из ламеллярных телец [3].
На барьерную функцию эпидермиса влияют структура, дифференцировка, функциональная активность кератиноцитов, качественный и количественный состав липидов рогового слоя эпидермиса, наличие веществ, относящихся к естественному увлажняющему фактору, а также рН поверхности кожи [18]. При изменении каких-либо из перечисленных показателей барьерная функция эпидермиса нарушается, что приводит к усиленному испарению воды через роговой слой. У человека эпидермальный барьер восстанавливается на 60% через 12 часов, а полное восстановление занимает 72 часа [19]. Полагают, что быстрое восстановление эпидермального барьера происходит за счет массового выброса из клеток готовых ламеллярных телец. В медленную фазу восстановления усиливается синтез жирных кислот, холестерина, церамидов, а также образование новых ламеллярных гранул. Нарушение восстановления кожного барьера приводит к обезвоживанию эпидермиса и развитию выраженной сухости кожи, что и наблюдается при развитии атопического дерматита (АД) [20].
Повреждение эпидермального барьера способствует проникновению через кожу микробов, аллергенов и различных поллютантов (токсины, раздражающие и загрязняющие вещества). Проникновение агентов с антигенными свойствами увеличивает риск сенсибилизации, поскольку взаимодействие аллергенов и аллерген-представляющих клеток кожи инициирует воспаление [14]. Степень дисфункции барьера коррелирует со степенью воспаления и тяжестью АД [11]. Впервые Y. Werner и M. Lindberg (1985 г.) привели доказательства нарушений барьерной функции кожи, измерив трансэпидермальную потерю воды (ТЭПВ) у лиц с АД. Авторам удалось показать, что у больных АД нарушения эпидермального барьера отмечаются не только в очагах активного воспаления, но и на клинически неизмененной коже [10, 21].
Изменения в свойствах эпидермального барьера, которые наблюдаются при АД, включают увеличение ТЭПВ, изменения рН поверхности кожи, повышение ее проницаемости, увеличение бактериальной колонизации, изменение в экспрессии антимикробных пептидов, а также нарушение его целостности. При аномалии эпидермального барьера аллергены, раздражающие и другие вещества могут проникать через кожу, способствуя обострению АД [6].
В настоящее время нарушение функции кожного барьера является одним из ведущих этиопатогенетических факторов АД. По данным разных авторов у 30–66% больных АД протекает без изменения уровня общего IgE в сыворотке крови и специфичных IgE к аллергенам. Полагают, что именно у этих пациентов нарушение функции кожного барьера играет ведущую роль в развитии и прогрессировании заболевания [22].
В последние годы определен ряд генетических мутаций, приводящих к изменениям в роговом слое эпидермиса. Так, у больных АД определяются мутации гена профилаггрина [23], способствующие нарушению синтеза белка ФЛГ — одного из компонентов цитокератинового скелета, обеспечивающего ороговение кератиноцитов. В результате изменения терминальной дифференцировки кератиноцитов развивается их функциональная несостоятельность [24]. Кроме того, снижение экспрессии гена ФЛГ уменьшает уровень «натурального увлажняющего фактора» [25]. Дефицит ФЛГ и/или продуктов его деградации способствует сухости кожи, что коррелирует с клинической картиной нарушения эпидермального барьера при АД [26]. Более того, при уменьшении ФЛГ усиливается «раздражающий» эффект аллергенов на дендритные клетки, понижая при этом порог их чувствительности к воспалению, что демонстрирует важность этого белка в предотвращении пенетрации аллергенов [27].
Кроме того, у больных АД выявлены полиморфные варианты гена SPINK5, приводящие к дизрегуляции синтеза ингибитора сериновой протеазы LEKTI, который в норме блокирует избыточную продукцию SCCE [28]. Активность деградационных протеаз также значимо связана с дефектом кожного барьера при АД [23]. Разбалансировка функционирования этих ферментов ведет к усиленному отшелушиванию клеток и истончению рогового слоя, увеличивая проницаемость эпидермального барьера [14]. Установлено, что у больных АД изменена липидная мантия рогового слоя, предупреждающая ТЭПВ. Отмечается низкий уровень церамидов первого и третьего типов в сочетании с повышением уровня свободного холестерола [29]. Повышение уровня рН на поверхности кожи приводит к снижению синтеза липидов и активизации ферментов (в частности, SCCE), повреждающих корнеодесмосомы. Уменьшение количества веществ, относящихся к «натуральному увлажняющему фактору», также способствует нарушению функционирования эпидермального барьера [30].
Таким образом, у больных АД отмечается комплекс нарушений, приводящих к дисфункции кожного барьера, усилению ТЭПВ и обезвоживанию кожных покровов [14]. Из вышеуказанного следует, что пациенты с АД могут иметь дефект кожного барьера, в основе которого лежат как генетические, так и приобретенные механизмы. Этот дефект способны спровоцировать внешние факторы, такие как царапины, использование моющих средств, микробная колонизация, а также воздействие протеаз различных аллергенов (в частности, протеаз клещей домашней пыли) [10]. Распознание конкретных механизмов, участвующих в патогенезе воспалительных заболеваний кожи, в частности, АД, безусловно, будет способствовать поиску и разработке новых, более эффективных методов воздействия на патологический процесс с минимальным количеством системных эффектов [8].
Литература
- Elias P. M. The skin barrier as an innate immune element // Semin. Immunopathol. 2007. Vol. 29 (1); р. 3–14.
- De Benedetto A., Kubo А., Beck L. A. Skin barrier disruption — a requirement for allergen sensitization? // J. Invest. Dermatol. 2012. Vol. 132 (3); р. 949–63.
- Danby S. G., Cork M. J. New understanding of atopic dermatitis: the role of epidermal barrier dysfunction and subclinical inflammation. // J. Clin. Dermatol. 2010. Vol. 1 (2); р. 33–46.
- Котлуков В. К., Кузьменко Л. Г., Антипова Н. В. Наружные дерматологические средства серии «Бепантен» в практике педиатра // Медицинский совет. 2012. Т. 5; с. 81–85.
- Madison K. С. Barrier function of the skin: «la raison d’etre» of the epidermis // J. Invest. Dermatol. 2003. Vol. 121; р. 231–241.
- Lorena S. T., Morello III A. P., Mack Correa M. C. et al. The infant skin barrier: can we preserve, protect, and enhance the barrier? // Dermatol. Res. Pract. 2012. Doi: 10.1155/2012/198789.
- Candi E., Schmidt R., Melino G. The cornified envelope: a model of cell death in the skin // Nat. Rev. Mol. Cell Biol. 2005. Vol. 6; р. 328–340.
- Michael J. C., Simon G. D., Yiannis V. et al. Epidermal barrier dysfunction in atopic dermatitis // J. Invest. Dermatol. 2009. Vol. 129; р. 1892–908.
- Ревякина В. А. Современные тенденции в комплексной наружной терапии атопического дерматита у детей // Лечащий Врач. 2014. № 6, с. 38.
- De Benedetto А., Agnihothri R., McGirt L. Y. et al. Atopic dermatitis: a disease caused by innate immune defects? // J. Invest. Dermatol. 2009. Vol. 129; р. 14–30.
- Roelandt T., Thys B., Heughebaert C. et al. LEKTI-1 in sickness and in health // Int. J. Cosmetic Sci. 2009. Vol. 31 (4); р. 247–254.
- Ishida-Yamamoto A., Simon M., Kishibe M. et al. Epidermal lamellar granules transport different cargoes as distinct aggregates // J. Invest. Dermatol. 2004. Vol. 122; р. 1137–1144.
- Ishida-Yamamoto A., Deraison C., Bonnart C. et al. LEKTI is localized in lamellar granules, separated from KLK5 and KLK7, and is secreted in the extracellular spaces of the superficial stratum granulosum // J. Invest. Dermatol. 2005. Vol. 124; р. 360–366.
- Cork M. J., Robinson D. A., Vasilopoulos Y. et al. New perspectives on epidermal barrier dysfunction in atopic dermatitis: gene-environment interactions // J. Allergy Clin. Immunol. 2006. Vol. 118; р. 3–21.
- Caubet C., Jonca N., Brattsand M. et al. Degradation of corneodesmosome proteins by two serine proteases of the kallikrein family, SCTE/KLK5/hK5 and SCCE/KLK7/hK7 // J. Invest. Dermatol. 2004. Vol. 122; Р. 1235–1244.
- Goldstein A. M., Abramovits W. Ceramides and the stratum corneum: structure, function, and new methods to promote repair // Int. J. Dermatol. 2003. Vol. 42; р. 256–59.
- Chavanas S., Bodemer C., Rochat A. Mutations in SPINK5, encoding a serine protease inhibitor, cause Netherton syndrome // Nat. Genet. 2000. Vol. 25; р. 141–142.
- Мурашкин Н. Н. Нарушения дермального барьера как фактор хронизации дерматозов в детском возрасте, подходы к терапии: теоретические и практические инновации // Лечащий Врач. 2014. № 6, с. 19.
- Эрнандес Е., Марголина А., Петрухина А. Липидный барьер кожи и косметические средства // Косметика и медицина. 2005. Т. 6; с. 35–38.
- Тамразова О. Б. Синдром сухой кожи // Дерматология. Приложение к журналу Consilium Medicum. 2014. Т. 3; с. 25–31.
- Хлебникова А. Н. Увлажняющие средства в терапии хронических дерматозов // Клиническая дерматология и венерология. 2010. Т. 4; с. 32–39.
- Palmer C. N., Irvine A. D., Terron-Kwiatkowski A. et al. Common loss-of-function variants of the epidermal barrier protein filaggrin are a major predisposing factor for atopic dermatitis // Nat. Genet. 2006. Vol. 38 (4); р. 441–446.
- Молочков А. В., Тамразова О. Б. Ксероз кожи — основной патогенетический фактор развития атопического дерматита // Дерматология. Приложение к журналу Consilium Medicum. 2014. Т. 4; с. 48–54.
- Vasilopoulos Y., Cork M. J., Murphy R. et al. Genetic association between an AACC insertion in the 3’UTR of the stratum corneum chymotryptic enzyme gene and atopic dermatitis // J. Invest. Dermatol. 2004. Vol. 123; р. 62–66.
- Smith F. J., Irvine A. D., Terron-Kwiatkowski A. et al. Loss-of-function mutations in the gene encoding filaggrin cause ichthyosis vulgaris // Nat. Genet. 2006. Vol. 38 (3); р. 337–342.
- Nemoto-Hasebe I., Akiyama M., Nomura T. et al. Clinical severity correlates with impaired barrier in? laggrin-related eczema // J. Invest. Dermatol. 2009. Vol. 129 (3); р. 682–689.
- Fallon P. G., Sasaki T., Sandilands A. et al. A homozygous frameshift mutation in the mouse Flg gene facilitates enhanced percutaneous allergen priming // Nat. Genet. 2009. Vol. 41 (5); р. 602–608.
- Kato A., Fukai K., Oiso N. et al. Association of SPINK5 gene polymorphisms with atopic dermatitis in the Japanese population // Br. J. Dermatol. 2003. Vol. 148; р. 665–669.
- Пампура А. Н., Чусляева А. А. Современные подходы к терапии атопического дерматита у детей // Медицинский вестник Башкортостана. 2014. Т. 9 (1); с. 93–98.
- Eberlein-Konig B., Schafer T., Huss-Marp J. et al. Skin surface pH, stratum corneum hydration, transepidermal water loss and skin roughness related to atopic eczema and skin dryness in a population of primary school children // Acta Dermatol. Venereol. 2000. Vol. 80; р. 188–191.
С. В. Левашева 1 , кандидат медицинских наук
Э. И. Эткина, доктор медицинских наук, профессор
Л. Л. Гурьева, кандидат медицинских наук
Л. И. Бабенкова, кандидат медицинских наук
Л. Я. Данилова
С. Э. Якута
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Проблемная кожа - причины появления, при каких заболеваниях возникает, диагностика и способы лечения.
В дерматологии устойчивый термин «проблемная кожа» применяется для обозначения вполне определенного спектра косметических проблем: в первую очередь, это повышенная сальность кожи и связанные с ней проблемы, а также сухость кожи и ее возрастные изменения.
В широком смысле «проблемная кожа» – эта любая кожа с косметическими дефектами, вызванными внешними (воздействие окружающей среды) или внутренними (заболевания) факторами.
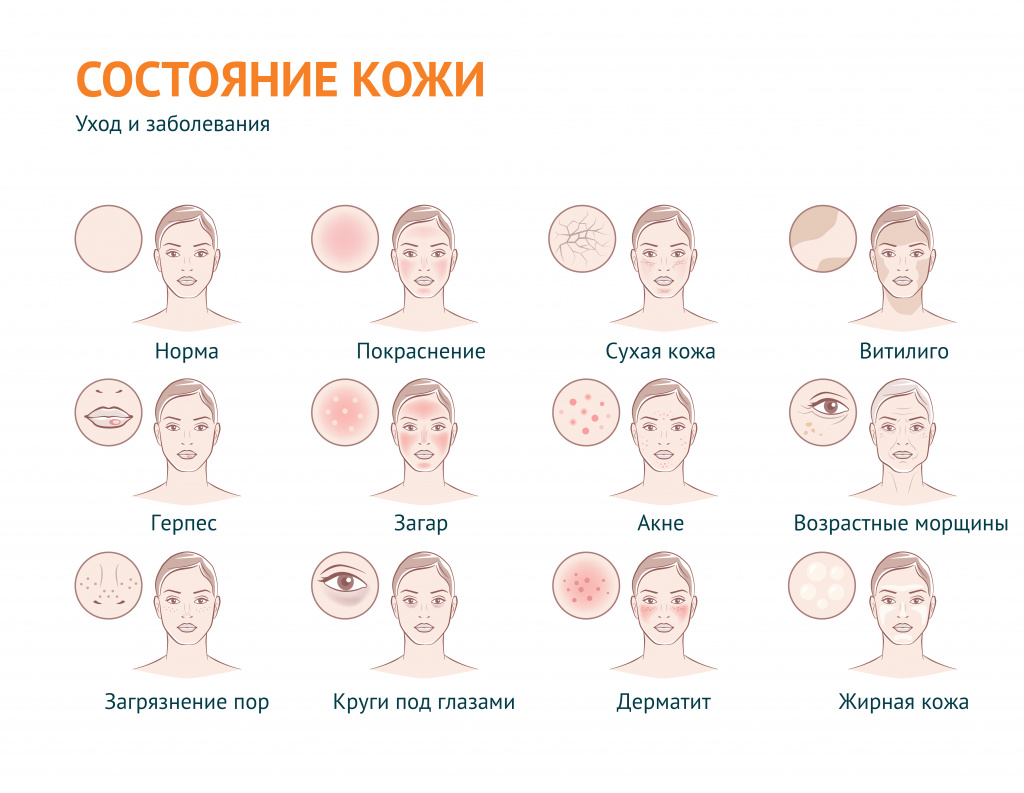
Под этим выражением подразумевают также наличие морщин и растяжек, пигментных пятен и веснушек, бородавок, шрамов, рубцов, сосудистых звездочек, грибковых поражений, бледности или покраснения и т. д.
Проблемная кожа может появиться в подростковом возрасте и быть следствием гормональной перестройки организма или (если речь идет о взрослом человеке) быть индикатором определенных заболеваний.
Жирная кожа – кожа с характерным сальным блеском, вызванным гиперсекрецией сальных желез. Поры жирной кожи расширены и, как правило, закупорены сальным секретом и загрязнениями (так называемыми «комедонами»). Нередко на жирной коже появляются акне (прыщи) – воспаление волосяного фолликула и сальной железы или их разновидности – фурункулы (когда в процесс воспаления вовлекается окружающая ткань). На лице наиболее предрасположена к появлению акне Т-зона – лоб, нос, подбородок. Как правило, на этих участках сальные железы более активны. На теле прыщи чаще всего появляются в пространстве между лопатками или в районе трицепсов.
О чем свидетельствует появление прыщей.
- Прыщи и избыточное оволосение по мужскому типу у женщин: возможная причина – гиперандрогения. Необходимо исследовать уровень половых гормонов.
- Прыщи у беременных чаще всего связаны с гормональной перестройкой организма.
- Белые высыпания у грудных детей могут быть связаны с избытком гормонов в молоке матери. В этом случае нужно проконсультироваться с педиатром.
- Большое количество закупоренных сальным секретом пор не только на лице, но и на теле может указывать на сниженную функцию щитовидной железы. Диагноз ставит эндокринолог.
Сухая кожа. Ксероз, или сухость кожи – это проблема, связанная со сниженным содержанием влаги в роговом слое эпидермиса. В такой коже замедляется метаболизм (обменные процессы). При этом нарушается ее барьерная функция. Кожа становится чувствительной к воздействию внешних факторов, быстро теряет упругость.
Сухой кожа лица, как правило, становится за пределами Т-зоны. На теле сухости часто подвержена кожа живота, поясницы, ног.
Комбинированная кожа. При этом типе кожи зоны наибольшей активности сальных желез лоснятся от кожного сала, остальные участки могут быть сухими, истонченными, склонны к появлению морщин и уязвимы перед внешними факторами.
Возрастная кожа. Чаще всего так называют сухую, истонченную кожу со сниженным тургором. Признаками возрастных изменений могут служить не только морщины, но и гиперпигментация, участки неравномерной пигментации, сосудистые пятна и т. д.
Жирная кожа, склонная к появлению прыщей, не обязательно связана с патологическим процессом. Часто это «визитная карточка» подросткового возраста (13-15) лет. У взрослых данная проблема требует более пристального внимания, поскольку может быть вызвана эндокринными нарушениями (например, болезнями щитовидной железы или гипофиза), заболеваниями желудочно-кишечного тракта, погрешностями в диете, злоупотреблением жирной пищей и простыми углеводами (продуктами, содержащими сахар в больших количествах).
- холецистит;
- колит;
- запоры;
- заболевания печени;
- гиперандрогения (повышенная выработка мужских гормонов);
- гипертрихоз (избыточный рост волос);
- сахарный диабет.
Особенно настороженно следует отнестись к появлению прыщей в детском возрасте (от двух до семи лет) лет. В этом случае следует исключить опухолевые образования надпочечников.
Проблема сухой кожи может быть возрастной (появляется у женщин в период менопаузы), носить перманентный характер либо быть связанной с сезонными климатическими колебаниями и т. п. Однако иногда сухость кожи может быть вызвана нарушениями питания (в частности, нехваткой витаминов А и Е), курением, злоупотреблением кофе, приемом некоторых лекарственных препаратов (например, диуретиков). Но не стоит забывать о том, что такое состояние кожи может быть одним из симптомов серьезных заболеваний, например, сахарного диабета, аллергии и целого ряда тяжелых хронических кожных болезней.
«Возрастная кожа» может появляться не только по мере естественного старения, но и в результате определенных заболеваний. В списке недугов-провокаторов традиционно лидируют сахарный диабет, гипотиреоз, заболевания половых желез, гипоталамо-гипофизарный синдром, легочные патологии, вызывающие кислородное голодание кожи.
Для начальной диагностики обратитесь к дерматовенерологу или терапевту. Возможно, после сбора анамнеза и получения результатов диагностики вас направят к другим специалистам – эндокринологу, гастроэнтерологу, хирургу или аллергологу.
Чаще всего выяснение причины проблемной кожи начинается со стандартных лабораторных исследований – клинического и биохимического анализа крови.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Утолщение кожи: причины появления, при каких заболеваниях возникает, диагностика и способы лечения.
Определение
Гиперкератоз – это аномальное утолщение верхнего слоя кожи (эпидермиса) в результате избыточной инсоляции, воздействия химических веществ, частого трения или давления. Кроме того, гиперкератоз может возникать на фоне некоторых заболеваний.
Утолщение кожи происходит в роговом слое эпидермиса, который является конечной точкой процесса дифференцировки кератиноцитов - клеток, содержащих белок кератин. Именно в роговом слое кератиноциты теряют воду и ядро и превращаются в чешуйки рогового слоя – корнеоциты.
При гиперкератозе происходит ускоренная дифференцировка кератиноцитов, а физиологическое слущивание роговых чешуек с поверхности кожи, наоборот, замедляется.
Разновидности гиперкератоза
В зависимости от происхождения выделяют приобретенный и наследственный гиперкератоз.
По клиническим проявлениям.
- Мозоли – часто встречающаяся разновидность гиперкератоза. Различают несколько видов мозолей, но все они появляются вследствие утолщения кожи в местах, наиболее подверженных механическому воздействию. Причем такое изменение кожи может быть связано как с усиленными физическими нагрузками, так и с различными хроническими заболеваниями, что характерно для пожилых пациентов.
- Роговая (тилотическая) экзема проявляется гиперкератозом ладоней и подошв.
- Псориаз - аутоиммунное воспалительное заболевание, при котором на коже формируются гиперкератотические чешуйчатые бляшки.
- Актинический кератоз обычно представлен небольшими красноватыми чешуйчатыми выпуклостями, которые появляются после избыточной инсоляции. Актинический кератоз – серьезное состояние с высокой вероятностью озлокачествления и требует обязательной консультации врача.
- Себорейный кератоз характеризуется маленькими коричневыми или черными пятнами, обычно локализующимися на лице, шее, плечах и спине. Это одно из наиболее распространенных доброкачественных новообразований кожи у взрослых.
- Фолликулярный гиперкератоз («гусиная кожа») характеризуется закупоркой устьев фолликулов ороговевшими клетками эпидермиса.
- Эпидермолитический гиперкератоз - редкое наследственное заболевание, которое проявляется сразу при рождении. Новорожденные имеют красноватую кожу, иногда покрытую небольшими волдырями.
Гиперкератоз кожи может возникнуть у людей, которые пренебрегают регулярными процедурами по уходу за кожей, в результате чего отмершие клетки рогового слоя скапливают и формируют кератомы – доброкачественные новообразования.
Наша кожа постоянно подвергается воздействию неблагоприятных внешних факторов, таких как хлорированная вода и моющие средства, УФ-излучение. В результате повреждается защитный липидный слой кожи, и влага начинает интенсивно испаряться с ее поверхности, а корнеоциты теряют способность к физиологическому слущиванию.
При сахарном диабете гиперкератоз становится следствием нарушения обмена веществ и ухудшения микроциркуляции кожи.
Ношение тесной или неудобной обуви, особенно при плоскостопии, врожденных патологиях стоп, ожирении, может стать причиной утолщение кожи на стопах.
Развитию гиперкератоза шейки матки (лейкоплакии) способствует вирус папилломы человека.
Причиной гиперкератоза может стать хроническое грибковое поражение, а также опоясывающий лишай.
Считается, что симптомы утолщения и сухости кожи могут быть вызваны дефицитом витаминов А, Е, D и С.
Гиперкератоз нередко становится следствием недостатка гормона эстрогена у женщин в период менопаузы.
Заболевания и состояния, при которых развивается гиперкератоз
- Сахарный диабет.
- Ожирение.
- Плоскостопие.
- Ихтиоз.
- Псориаз.
- Экзема.
- Менопауза.
- Грибковое поражение кожи.
- Опоясывающий лишай.
- Эритродермия.
- Атопический дерматит.
- Себорейный кератоз.
Чаще всего за первой консультацией по поводу утолщения кожи обращаются к врачу-дерматологу. После тщательного осмотра, сбора жалоб, выяснения медицинской и семейной истории пациента, проведения лабораторных и инструментальных исследований может потребоваться консультация врача-эндокринолога , врача-онколога , врача-инфекциониста.
Диагностика и обследования при утолщении кожи
Тщательный сбор анамнеза с учетом всех жалоб пациента, осмотр и проведение дополнительных методов диагностики помогут установить причину гиперкератоза.
-
Клинический анализ крови с развернутой лейкоцитарной формулой для выявления воспалительных процессов в организме.
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Читайте также:

