Как лечить желудок при дерматите
Обновлено: 28.04.2024
Для цитирования: Бутов Ю.С., Васенова В.Ю., Ильина Т.А., Хрусталева Е.А. Фосфоглив в терапии ряда дерматозов. РМЖ. 2006;5:353.
Группа таких заболеваний, как псориаз, экзема, атопический дерматит, липоидный некробиоз, характеризуются мультифакториальным генезом на фоне генетической предрасположенности [8,10], нейрогенных, иммунологических изменений [5,17] и обменных нарушений [14], включая поражение эндокринных желез [1], желудочно–кишечного тракта [9], в том числе и печени.
Так, у больных псориазом было обнаружено повышение активности печеночных ферментов, гиперхолестеринемия, снижение антитоксической функции печени, нарушение равновесия желчных кислот [3,8,11,12,20].
У больных экземой и атопическим дерматитом выявлялось нарушение липидного обмена, характеризующееся повышением уровня общих липидов, триглицеридов, снижением фосфолипидов в сыворотке крови и мембранах эритроцитов [13,14].
Наиболее значимые изменения обнаружены у больных липоидным некробиозом, что проявляется диспротеинемией, гиперхолестеринемией, повышением в сыворотке крови уровня триглицеридов, общих липидов, холестерина, b–липопротеидов и невысокой активностью альдолаз, трансаминаз [1,4,6].
Все вышеизложенное диктует проведение углубленых исследований у больных с названными дерматозами, направленное на коррекцию дислипидемических изменений и клинического течения.
К препаратам, обладающим направленным патогенетическим действием, следует отнести Фосфоглив – новый отечественный гепатопротектор, содержащий фосфолипид (фосфатидилхолин) растительного происхождения и натриевую соль глицирризиновой кислоты. Фосфатидилхолин является основным структурным компонентом фосфолипидного слоя биологических мембран, восстанавливает структуру и функции поврежденных мембран гепатоцитов, благодаря чему предотвращает потерю клетками ферментов и других активных веществ, нормализует белковый, липидный и жировой обмены, восстанавливает детоксикационную функцию печени, ингибирует формирование соединительной ткани печени, снижает риск возникновения фиброза и цирроза печени. Натрия глицирризинат подавляет репродукцию вируса в печени и других органах за счет стимуляции продукции g–интерферона, повышает фагоцитоз, увеличивает активность естественных киллеров и, что особенно важно в дерматологической практике, обладает противовоспалительным, иммуномодулирующим действием и др. Изучение фармакокинетических характеристик Фосфоглива было проведено в ГУ НИИ биомедицинской химии РАМН [7].
Фосфоглив прошел терапевтическую апробацию на разных клинических базах г. Москвы.
Однонаправленные данные при исследовании больных алкогольным поражением печени, жировым гепатозом, калькуллезным холециститом и острым гепатитом «В» в виде моно– и микстинфекции получили Ивашкин В.Т., Сторожаков Г.И., Альтшулер В.Б. (1998), Лучшев В.И. (1999), Гальперин Э.И. (2000) и др. – среди больных, получавших Фосфоглив, достоверно быстрее, чем в контрольной группе, купировались такие симптомы, как слабость, анорексия, гипергидроз, тошнота, быстрее происходила нормализация липидного спектра сыворотки крови (показатели общего билирубина, холестерина, триглицеридов), печеночных проб (снижение активности АлАТ, АсАТ) [16].
Комбинированная терапия Фосфогливом в сочетании с вифероном резистентных к монотерапии вифероном больных увеличивала число больных с ремиссией на 10–15% [19].
Учитывая повышенную заинтересованность печени и липидных нарушений в патогенезе экземы, псориаза, атопического дерматита и липоидного некробиоза, мы провели изучение клинической эффективности Фосфоглива при этих хронических дерматозах и его влияния на некоторые функциональные и биохимические показатели.
Под нашим наблюдением находился 171 больной, в том числе – 68 c псориазом, 40 – атопическим дерматитом, 34 – экземой, 29 – липоидным некробиозом. Распределение больных дерматозами по возрасту и полу приведено в таблице 1. В целом по группе количество мужчин составило 53,2%, женщин – 46,8%. Проведенный анализ показал, что наиболее значимые отклонения наблюдались у больных псориазом (69,1% из которых составили мужчины) и при липоидном некробиозе – 72,4% составили женщины. Значительные возрастные отклонения были выявлены у пациентов с атопическим дерматитом – 70,5 % составила группа до 30 лет.
Площади поражения у больных атопическим дерматитом и псориазом были значительными.
Из сопутствующих заболеваний у 67,3% больных констатирована патология ЖКТ и ГБС в виде гастритов, язвенной болезни желудка и двенадцатиперстной кишки, дискенезии желчевыводящих путей, жирового гепатоза и других состояний.
Для объективизации топической патологии некоторых паренхиматозных органов брюшной полости мы провели клинический и ультразвуковой анализ исследований у больных псориазом и липоидным некробиозом (рис. 1).
Клинические симптомы в виде тяжести в правом подреберье, отрыжки, изжоги, чувства горечи во рту подтверждали наличие внутрипеченочного холестаза. У большинства больных наблюдался параллелизм клинических симптомов с обширностью кожных поражений.
У ряда больных отмечалась повышенная активность печеночных ферментов и уровня холестерина в прогрессирующей фазе заболевания (табл. 2).
Анализ таблицы показал высокие уровни ГГТ, холестерина, АлАТ и АсАТ у больных псориазом и липоидным некробиозом по сравнению с контрольной группой. При атопическом дерматите выявлена наибольшая активность ЩФ.
Известно, что трансаминазы являются маркерами цитолитического синдрома, возникающего в печени под влиянием инфекционных или токсических факторов. Эти изменения иногда ограничиваются только клеточными мембранами, которые становятся высокопроницаемыми для внутриклеточных ферментов, а в ряде случаев распространяются и на цитоплазму, приводя к гибели гепатоцита.
Для более полного представления о состоянии липидного обмена мы провели исследование количественного соотношения липидов и фосфолипидов в сыворотке крови у больных псориазом и липоидным некробиозом (табл. 3).
Наиболее высокие показатели ОЛ, ТГ и СХ были у больных липоидным некробиозом. Изменения ферментативной активности в печени и липидно–фосфолипидного состава сыворотки крови указывают на тесную взаимосвязь между ними. Повышенный уровень ФЛ, СХ связан с процессами липидной пероксидации и отражает нестабильность и осмотическую неустойчивость мембран клеток. Увеличение уровня НЭЖК и ТГ обусловлено усилением процессов липолиза. Выявленные дислипидемии у больных псориазом и липоидном некробиозом свидетельствуют о мембрандеструктивных процессах, развивающихся как в печени, так, вероятно, и в клетках стенок сосудов, в кератиноцитах, что приводит к микрогемодинамическим нарушениям, усугубляет течение дерматозов и дает основание для назначения комплексной терапии. Терапевтический комплекс включал глюконат кальция, кетотифен, витамины группы А и В, а для стабилизации метаболических процессов – Фосфоглив по 2 капсулы 3 раза в день до 2–3 месяцев.
У всех исследуемых пациентов под влиянием комплексной терапии мы отметили значительное улучшение течения кожного процесса, положительную динамику с частичной нормализацией всех клинико–биохимических показателей крови. В этой связи особый интерес представили данные показателей холестерина и некоторых ферментов.
В таблицах 4 и 5 приведены результаты исследования активности печеночных ферментов и липидов сыворотки крови у больных различными дерматозами после лечения. Анализ приведенных данных показал значительное снижение уровней ГГТ, холестерина, АлАТ и АсАТ у больных псориазом и липоидным некробиозом. У пациентов с атопическим дерматитом наблюдалось только снижение АлАТ и АсАТ. Данные таблицы свидетельствуют о значительном снижении уровней ОЛ, ЭХ, ТГ у обследуемых, в наибольшей степени у больных липоидным некробиозом.
Фосфоглив способен встраиваться в структуру клеточных мембран, замещая дефекты липидного бислоя, что ведет к восстановлению барьерной функции кожи. По нашим наблюдениям, Фосфоглив не обладает аллергизирующими и токсическими свойствами, хорошо переносится.
Фосфоглив, включенный в терапевтический комплекс псориаза, атопического дерматита, экземы и липоидного некробиоза, положительно влияет на динамику течения дерматозов, снижает активность воспалительного процесса, способствует нормализации липидного состава сыворотки крови, свидетельствуя о липотропном и мембранстабилизирующем действии.
Литература
1. Абрамова Е.А. Липоидный некробиоз. Автореф. дисЕ к.м.н. Москва, 1985.
2. Арчаков А.И., Ипатова О.М., Торховская Т.И. Теоретические основы применения эссенциальных фосфолипидов и глицирризиновой кислоты в медицине. Симпозиум «Опыт клинического применения отечественного гепатопротектора «Фосфоглив». 8–ой российский национальный конгресс «Человек и лекарство». Москва, 2001
3. Балтабаев М. К., Хамидов Ш. А., Валиханов У. А., Хамидов Ф. Ш. Псориаз и метаболизм желчных кислот. Вестник дерматологии и венерологии N4, 2005, с.25–28
4. Бутов Ю.С., Хрусталева Е.А. Федорова Е.Г. и др. Уровень липидов и показатели клеточного иммунитета у больных псориазом. Российский журнал кожных и венерических болезней. 1999. №2. с.11–14.
5. Владимиров В.В. Материалы к патогенезу и терапии липоидного некробиоза. Автореф. дисЕ к.м.н. Москва, 1971.
6. Волкова Е.Н. Бутов Ю.С. Дислипидемический синдром при аллергических ангиитах кожи. Российский журнал кожных и венерических болезней. 1998. №3. с.18–22.
7. Довжанский С.И., Утц С.Р. Псориаз и псориатическая болезнь. Саратов: Издательство Саратовского университета. 1992. 270с.
8. Ильина Т.А. Влияние комплексной терапии (фосфоглив, липамид, доксилек) на клиническое течение липоидного некробиоза и показатели сывороточных и мембранных липидов. Автореф. дис. к.м.н., Москва, 2004
9. Ипатова О.М. Фосфоглив: механизм действия и применение в клинике. Под ред. академика РАМН Арчакова А.И. М.: Изд. ГУ НИИ биомедицинской химии РАМН, 2005. с.318
10. Кожные и венерические болезни. Руководство для врачей. В двух томах. Под ред. Скрипкина Ю.К., Мордовцева В.Н. 1999. 1600с.
11. Короткий Н.Г., Песляк М.Ю. Псориаз как следствие включения ?–стрептококков в микробиоценоз кишечника с повышенной проницаемостью (концепция патогенеза). Вестник дерматологии и венерологии N1, 2005, с.9–18
12. Заболевания кожи с наследственным предрасположением. Мордовцев В.Н., Алиева П.М., Сергеев А.С. Махачкала: Изд–во типографии ДНЦ РАН, 2002. 260с.
13. Никифоров А.П. Активность ферментов сыворотки крови у мужчин и женщин при некоторых патологических состояниях. Клиническая лабораторная диагностика. 1995. №1. с.14–15.
14. Повалий Т.М., Логинова Т.К., Шарапова Г.Я., Гусев С.А. Количественный анализ холестерина мембран кератиноцитов эпидермиса при псориазе. Вестник дерматологии и венерологии. 1997. №1. с. 4–6.
15. Рябова О.О. Нарушения липидного обмена у больных экземой. Харьковская медицинская академия последипломного образования. Дерматологiя та венерологiя № 4 (18) 2002 г.
16. Торопова Н.Г., Синявская О.А. Экзема и невродермит у детей. Иркутск: издательство Иркутского университета, 1993. 405с.
17. Фосфоглив. Лечение и защита печени. Пособие для врачей. (Учайкин В.Ф., Арчаков А.И., Ипатова О.М. и др., под ред. Учайкина В.Ф.) Москва, ГУ НИИ БМХ РАМН, 2004.
18. Фосфоглив. Отечественный гепатопротектор с противовирусной активностью. Пособие для врачей под ред. Учайкина В.Ф. (Учайкин В.Ф., Альтшулер В.Б., Гальперин Э.И., Ивашкин В.Т., Лучшев В.И., Сторожаков Г.И., и др.), Москва, 2002
19. Шарапова Г.Я., Короткий Н.Г., Молоденков М.Н. Псориаз. М: Медицина. 1993. 221с.
20. Учайкин В.Ф., Княжев В.А, Гальперин Э.И., Докучаев К.В., Торховская Т.И., Ковалев О.Б., Писарева Е.А., Конев В.А., Арчаков А.И. Гепатопротекторное действие фосфолипидного препарата «фосфоглив» у больных, оперированных по поводу хронического калькулезного холецистита. Хирургия. 2000. 3. с. 14–18.
21. Учайкин В.Ф., Ковалев О.Б., Чередниченко Т.В., Малиновская В.В. Противовирусная терапия хронических гепатитов В и С у детей. 10–й российский национальный конгресс «Человек и лекарство». Москва. 2003. с 385.
22. Хрусталева Е.А. Эффективность фосфоглива и мослецитина в комплексном лечении больных псориазом. Автореферат диссертации на соискание ученой степени к.м.н. Москва., 2001
23. Шарапова Г.Я., Резайкина А.В. Иммунология в дерматологии. Вестник дерматологии. 1993, №4, с.4–14
24. Torumova B., Pieterzak A., Miturska R., Activity of serum lipase EC 3.1.1.3. in psoriatic males. J. Europ. Acad. Dermatol. Venereol. 1997. V8. №2. p 158–160
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Д.м.н. Л.С. Круглова
Московский Научно-практический центр дерматовенерологии и косметологии Департамента здравоохранения г. Москвы
Современная медицинская наука дает возможность практикующему врачу рассматривать заболевания не только в узких рамках симптомокомплекса, но и с точки зрения изменения функциональных резервов организма человека в результате нарушения его адаптационных возможностей. Неуклонный рост заболеваемости атопическим дерматитом (АтД), наличие рецидивирующих, хронических форм создают потребность в интеграции лечебно-реабилитационных технологий, направленных на восстановление и сохранение здоровья, нарушенного данной патологией.
По современным представлениям человеческий организм является определенной экологической нишей для множества разнообразных микроорганизмов, которые в норме формируют своего рода различные биотопы, являющиеся достаточно сложными системами, сформировавшимися в процессе эволюции и со временем приобретшие определенную устойчивость применительно к особенностям макроорганизма. Биотопы отличаются не только многокомпонентностью, но и количественным разнообразием входящих в них представителей микрофлоры [1].
Постоянство бактериальной аутомикрофлоры организма человека позволяет рассматривать бактерий, существующих преимущественно в четырех локализациях - на коже и слизистой полости рта, кишечника, половых органов - как своеобразный прокариотический орган. Причем изменения в одном из биотопов могут приводить к нарушениям в других. Формирование микрофлоры биотопов организма, и в первую очередь кожи и кишечника, происходит уже с самого рождения ребенка при прохождении по родовым путям. В дальнейшем на формирование влияет много факторов: состав микрофлоры биотопов матери, вид вскармливания, а затем и характер питания, состояние соматического здоровья ребенка и состояние окружающей среды [2,3].
Из всех биотопов организма наибольшая численность и видовое разнообразие бактерий отмечается в биотопе кишечника: так, на площади в 200 м 2 обитает 10 12 -10 14 бактерий, может встречаться до 450 видов различных микроорганизмов, общая масса которых доходит до 5% массы самого кишечника [4,5]. При этом в разных отделах кишечника количество и состав микроорганизмов биоценоза различен. В тонком кишечнике микробов меньше - это преимущественно лактобациллы, стрептококки и веилонеллы, в толстом кишечнике их больше, причем преобладают кишечные палочки и анаэробные бактерии.
Многочисленные микроорганизмы обеспечивают такие важные функции, как выработка ферментов, участвующих в метаболизме белков, липидов, жиров, нуклеиновых и желчных кислот, формирование механизмов иммунной защиты, поддержание гомеостаза организма, продукция биологически активных веществ и витаминов, детоксикация эндогенных и экзогенных субстратов и многие другие.
Микрофлора кишечника условно подразделяется на защитную, сапрофитную и оппортунистическую (условно-патогенную). Защитная микрофлора наиболее многочисленная (до 95%) и в основном представлена лактобактериями, бифидобактериями и кишечной палочкой с нормальными ферментативными свойствами. Именно они обеспечивают постоянство микрофлоры за счет колониальной резистентности. Так, бифидобактерии, лактобактерии выделяют молочную, уксусную кислоты, другие вещества, обладающие избирательным антимикробным действием. Кислая среда, обусловленная жизнедеятельностью этих микроорганизмов, препятствует проникновению и закреплению на слизистой патологических микробов, не свойственных данному биотопу. Помимо этого, бифидобактерии стимулируют клеточное звено иммунитета и участвуют в синтезе иммуноглобулинов. Данные бактерии являются естественными биосорбентами и способны накапливать значительное количество соединений тяжелых металлов, фенолов, формальдегидов и других токсичных веществ [6,7]. Однако в соответствии с современными воззрениями, скорее всего, недостаточное количество лактобактерии является основным отягчающим фактором при атопическом дерматите.
Именно лактобактерии в значительной степени снижают всасывание аллергенов в кишечнике и стимулируют синтез иммуноглобулинов класса А, которые, особенно в раннем детском возрасте, являются основными антителами против пищевых аллергенов [8,9].
Сапрофитная микрофлора кишечника представлена эпидермальным и сапрофитным стафилококками, энтерококками и другими микроорганизмами, основной функцией которых является утилизация конечных продуктов метаболизма макроорганизма [5].
Оппортунистическая микрофлора может быть представлена различными микроорганизмами (3-гемолитический стрептококк, золотистый стафилококк, спороносные анаэробы, грамотрицательные энтерококки, грибы рода Candida ), которые при определенных условиях вызывают патологический процесс [5].
Таким образом, в кишечном микробиоценозе, как в единой системе, существуют корреляционные связи между различными видами бактерий. Нарушение колонизационной резистентности кишечника, связанное с изменением состава постоянной микрофлоры, способствует колонизации патогенными и условно-патогенными бактериями, нарушению основных функций, что и приводит к формированию дисбиоза [Мельникова, 1997; Билимова, 2000; Белова с соавт., 2004; Cammaro-ta, Ogava, 1998].
Согласно существующему в России медицинскому стандарту оказания специализированной помощи при патологии желудочно-кишечного тракта (ЖКТ) дисбиоз кишечника рассматривается, как своеобразный клинико-лабораторный синдром, который характеризуется изменением качественного и/или количественного состава аутомикрофлоры, с возможной транслокацией микроорганизмов в несвойственные для них биотопы; при этом данные изменения могут сопровождаться клиническими симптомами поражения кишечника. В широком понимании дисбиоз является проявлением общего нарушения в различных микробиотах организма, которое приводит к нарушению функционирования микробиот и сопровождается определенными симптомами, ассоциированными с различными патологическими состояниями [5,10,11].
При развитии дисбиоза защитная микрофлора кишечника перестает выполнять свои функции в достаточной степени, что приводит к формированию патологических состояний либо усугублению течения имеющейся соматической патологии [12,13]. Ассоциированные с дисбиозом заболевания в зависимости от преобладания механизмов, отягчающих течение болезни, условно подразделяются на 4 группы:
- заболевания органов пищеварения,
- гнойно-воспалительные заболевания,
- аллергические заболевания,
- заболевания, связанные с нарушением обмена веществ (метаболизма).
Безусловно, рациональные схемы лечения атопического дерматита должны включать методы детоксикации (в частности, энтеросорбции) и использование препаратов, восстанавливающих и поддерживающих нормальную микрофлору кишечника. Энтеросорбция является неинвазивным методом детоксикации и направлена на выведение из организма различных эндогенных и экзогенных аллергенов, токсинов, патогенных микроорганизмов и продуктов их жизнедеятельности. Известно, что на фоне проведения энтеросорбционных мероприятий происходит повышение функциональной активности клеточного и гуморального иммунитета, ускоряется регресс объективных и субъективных симптомов АтД [17,18].
Существенным является и то, что сорбенты позволяют снизить медикаментозную нагрузку, а в ряде случаев и обходиться без них. Требования к современным энтеросорбентам следующие: высокие сорбционные свойства (емкость); отсутствие токсических свойств и системной фармакокинетики; атравматичность для слизистых оболочек ЖКТ; хорошая эвакуаторная способность; высокая комплаентность [19].
Механизм процесса энтеросорбции зависит от двух факторов - характеристик сорбента и структуры подлежащих сорбции веществ. Сорбенты могут отличаться по ряду признаков: лекарственная форма, физические свойства и химическая структура. Одними из самых эффективных сорбентов являются природные органические на основе пищевых волокон, такие как лигнин, который не усваивается в пищеварительной системе человека и полностью ферментируется кишечными бактериями. Важнейшее свойство лигнина - высокая сорбционная активность.
Вместе с тем большой интерес представляет развитие относительно нового направления в лечении атопического дерматита - включение в комплекс терапевтических мероприятий пребиотиков , выделенных из естественных источников и обладающих определенными регулирующими свойствами в отношении функционирования биотопа кишечника. В отличие от пробиотиков, которые поставляют необходимые бактерии извне, пребиотики выступают в качестве питательной среды для развития собственной нормальной микрофлоры организма, что способствует более быстрому и устойчивому восстановлению нормальной аутомикрофлоры кишечника [20,21]. Как правило, в качестве пребиотиков используют вещества, содержащие бифидогенные факторы, стимулирующие рост и развитие полезных бактерий. Таким веществом, в частности, является лактулоза - синтетический стереоизомер молочного сахара - лактозы.
Таким образом, на сегодняшний день идеальным сочетанием можно считать комбинированные лекарст венные средства, содержащие пребиотик и адсорбент. Таким средством является препарат Лактофильтрум ® , включаюший сорбент и пребиотик. В качестве сорбента препарат содержит растительный компонент - лигнин, который обладает неспецифическим дезинтоксикационным действием. За счет большой площади поверх ности и развитой системы пор обладает высокой сорбционной емкостью и таким образом способен выводить из организма токсины, аллергены и патогенные микро организмы. В качестве пребиотика выступает лактулоза, положительное влияние которой на микрофлору кишечника обусловлено целым рядом фармакологических свойств. Так, продукты бактериального метаболизма лактулозы сдвигают рН среды в толстой кишке в кислую сторону, что при водит к подавлению размножения патогенных микроорганизмов и угнетению процессов гниения. Помимо этого, являясь пищевым субстратом для бактерий, лактулоза стимулирует рост собственных бифидобактерий и лактобактерий в толстом кишечнике, а это, в свою очередь, восстанавливает, нарушенные функции биотопа кишечника.
Активные составляющие препарата не инактивируются в агрессивных средах желудка и двенадцатиперстной кишки, что обеспечивает 100%-ю доставку непосредственно к месту действия.
Лактофильтрум ® производится из компонентов природного происхождения в таблетированной форме и удобен в применении. Препарат зарекомендовал себя как высоко безопасный, который практически не имеет противопоказаний к применению и побочных эффектов [22,23].
В клинических условиях под нашим наблюдением находилось 40 пациентов (средний возраст 18,9±2,3 года, продолжительность заболевания 11,4±2,7лет) с диагностированным по основным критериям атопическим дерматитом в стадии обострения. У большинства пациентов АтД носил распространенный характер - ДИШС (Дерматологический индекс шкалы симптомов) составил 18,2±2,3 балла, что соответствует среднетяжелому течению АтД. В зависимости от проводимого лечения пациенты были разделены на 2 сопоставимые по всем параметрам группы. В основную группу вошли 20 больных, которые получали препарат
Лактофильтрум ® по 2 таблетки 3 раза в сутки на протяжении 21 дня и фармакотерапию, соответствующую стандартам при данной патологии. Пациенты 2 группы (20 человек) получали традиционную медикаментозную терапию.
До лечения у 97,5% пациентов был диагностирован дисбиоз кишечника, причем у 52,5% пациентов он протекал с клиническими симптомами (метеоризм, усиление перистальтики, нарушение стула, дискомфортные субъективные ощущения). После комплексного лечения в основной группе у 95% пациентов отмечалась нормализация содержания лактобактерий, бифидобактрий и Е. coli. Такая же тенденция наблюдалась и в отношении клинических симптомов дисбиоза. В группе сравнения достоверно значимых изменений количественного содержания лактобактерий, бифидобактрий и Е. coli не отмечалось (рис.1).
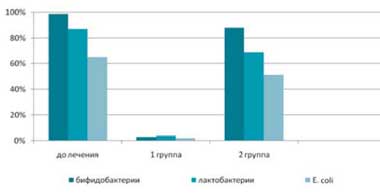
Рис. 1. Число пациентов с нарушением колониальной резистентности
до и после комплексного лечения, включающего применение Лактофильтрума ®
и традиционного медикаментозного лечения
Под влиянием комплексного лечения (1 группа) через 3 недели общие проявления всех объективных симптомов заболевания сохранялись в среднем лишь у 10% больных, в то время как в группе сравнения они были выражены в 54% случаев (рис. 2).
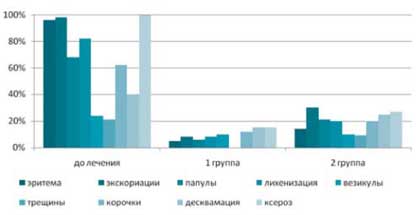
Рис. 2. Динамика регресса клинических симптомов у больных атопическим дерматитом под влиянием различных методов лечения
К концу лечения индекс ДИШС, отражающий тяжесть течения АтД, в основной группе снизился на 84%, в группе сравнения лишь на 53%. Анализ выраженности зуда с использованием опросника Behavioral rating scores (BRS) показал выраженное отрицательное влияние зуда на повседневную деятельность пациентов с АтД. Так, до лечения в 1-й группе значение BRS составило 7,1 ±0,4 баллов, во 2-й группе - 6,8±0,5 баллов. Уже через 1 неделю от начала лечения в 1-й группе отмечался более выраженный регресс субъективной симптоматики: снижение BRS на 55%, во 2-й группе - на 26%. К концу лечения в 1-й группе значение BRS составило 0,4±0,1 балла. В контрольной группе к концу лечения индекс снизился лишь на 58% (рис. 3). Эти данные находились в соответствии с показателями биохимических маркеров зуда (табл. 1).
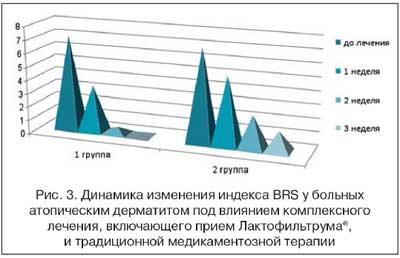
Таблица 1.
Динамика показателей гистамина и серотонина в сыворотке крови у больных АтД под влиянием комплексного лечения, включающего прием Лактофильтрума ® и традиционной медикаментозной терапии
| Изучаемый показатель | Контроль(n=20) | До лечения (n=40) | После лечения | |
|---|---|---|---|---|
| 1 группа (n=20) | 2 группа (n=20) | |||
| Серотонин (мкмоль/л) | 0,6±0,03 | 2,35±0,24Р1** | 0,81±0,32Р2*** | 1,46±0,22РГ**,РЗ* |
| Гистамин (мкмоль/л) | 0,8±0,06 | 2,14±0,62Р1** | 0,87±0,13Р2*** | 1,35±0,25Р1***,Р2** |
| Примечание: Р1 - сравнение с нормой; Р2 - сравнение с показателями до лечения; РЗ - сравнение с основной группой; *- р | ||||
Как видно из приведенных в таблице данных, после комплексной терапии, включающей применение Лактофильтрума ® отмечалось восстановление повышенных в исходном состоянии показателей серотонина и гистамина до нормальных значений - 0,81 ±0,32 и 0,87±0,13 (рВ процессе лечения с улучшением клинической картины заболевания пропорционально улучшались и показатели качества жизни (рис. 4). В результате анализа полученных данных, более выраженная положительная динамика дерматологического индекса качества жизни (ДИКЖ), особенно в первые дни терапии, была отмечена у пациентов 1 группы. Так, в первую неделю параметры ДИКЖ улучшились на 30% в 1 группе и лишь на 8% во 2 группе (рис. 5). К концу курса лечения ДИКЖ улучшился на 87 и 54% соответственно.
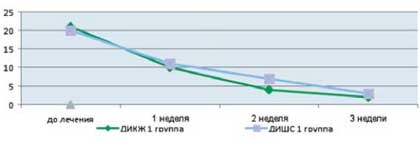
Рис. 4. Динамика изменения показателей, отражающих субъективные и объективные симптомы заболевания
у пациентов с АтД под влиянием комплексного лечения, включающего прием Лактофильтрума ®
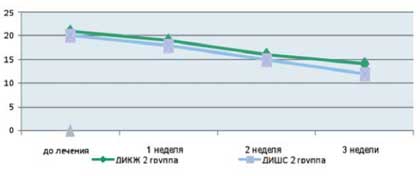
Рис. 5. Динамика изменения показателей, отражающих субъективные и объективные симптомы заболевания
у пациентов с АтД под влиянием традиционной медикаментозной терапии
Таким образом, по оценке самими пациентами эффективности и комфортности проводимого лечения, метод, включающий применение Лактофильтрума ® , является наиболее эффективным.
Выводы
Нарушение колониальной резистентости кишечника, приводящее к повышенной эндотоксинемии, аллергизации и нарушению гомеостаза, может отразиться на состоянии кожи и течении атопического дерматита.
Представители нормальной микрофлоры биоты кишечника выполняют физиологически важную функцию поддержания постоянства внутренней среды организма, принимают участие в формировании иммунобиологической реактивности макроорганизма. Нарушение нормоценозаспособствуетхронизации патологических процессов (в частности, атопического дерматита).
Включение препарата Лактофильтрум ® в комплекс терапии больных АтД приводит к более быстрому и выраженному регрессу кожных высыпаний и субъективных ощущений, нормализации функции биотопа кишечника, что в конечном итоге способствует значитель-номуулучшению качества жизни. Препарат не токсичен, не вызывает побочных эффектов, обладает высокой комплаентностью.
Литература
А.А. Алексеева, к.м.н., врач аллерголог-иммунолог, старший научный сотрудник отделения восстановительного лечения детей с аллергическими болезнями и заболеваниями органов дыхания НИИ ПП и ВЛ.
Научный центр здоровья детей РАМН, Москва
Атопический дерматит (АД) относится к числу распространенных аллергических болезней у детей и приобретает все большее медико-социальное значение. Существенным фактором риска является патология органов желудочно-кишечного тракта, особенно дисбиоз кишечника, который выявляется у 89–94,1% детей, больных атопическим дерматитом. Свидетельством этому служат как взаимосвязь степени выраженности дисбиоза с тяжестью клинических проявлений АД, так и то, что целенаправленное воздействие на микрофлору кишечника приводит к повышению эффективности лечения основного заболевания. В протоколы лечения атопического дерматита у детей наряду с элиминационной диетой, приемом антигистаминных средств, местной терапией в течение многих десятилетий включают энтеросорбенты. Особенно эффективными являются лекарственные средства, содержащие пребиотики и сорбенты. В статье представлен широкий опыт применения пребиотика со свойствами сорбента (препарат Лактофильтрум) в комплексной терапии атопического дерматита у детей.
Ключевые слова: энтеросорбенты, пребиотики, атопический дерматит, дисбиоз кишечника.
Проблема атопического дерматита приобретает в последние годы все большее медико-социальное значение, т.к. распространенность заболевания неуклонно растет. Атопический дерматит относится к числу распространенных аллергических болезней у детей и представляет собой хроническое воспалительное заболевание кожи, сопровождающееся зудом, обусловленное воздействием на сенсибилизированный организм ребенка различных аллергенов [1]. В типичных случаях заболевание начинается в раннем детском возрасте, может продолжаться или рецидивировать в зрелом возрасте и привести к физической и эмоциональной дезадаптации пациента. За последние три десятилетия распространенность заболевания, по данным эпидемиологических исследований, возросла и составляет в развитых странах, по мнению разных авторов, 10– 15% у детей в возрасте до 5 лет и 15–20% у детей школьного возраста [2].
Атопический дерматит — мультифакториальное заболевание, которое в большинстве случаев развивается у лиц с наследственной предрасположенностью и часто сочетается с другими аллергическими болезнями (бронхиальная астма, аллергический ринит, пищевая аллергия, рецидивирующие кожные инфекции), немаловажно и отрицательное влияние неблагоприятных воздействий внешней среды. Существенным фактором риска АД является патология органов желудочно-кишечного тракта, особенно дисбиоз кишечника, который выявляется у 89–94,1% детей, больных атопическим дерматитом [3–5]. Несомненно, кишечная микрофлора в силу большой функциональной нагрузки не может не участвовать в процессах патологических расстройств при АД.
Свидетельством этому служат как взаимосвязь степени выраженности дисбиоза с тяжестью клинических проявлений атопического дерматита, так и то, что целенаправленное воздействие на микрофлору кишечника приводит к повышению эффективности лечения основного заболевания [3, 6, 7]. Кроме того, рост заболеваемости атопическим дерматитом происходит параллельно с широким распространением кишечного дисбиоза в период новорожденности. Это может быть связано с тем, что нарушению микроэкологии кишечника и возникновению аллергических реакций способствуют одни и те же факторы. Среди них значительное место занимает лишение ребенка грудного молока с первых дней жизни, ранний перевод на смешанное и искусственное вскармливание, расширение спектра лекарственных препаратов, широкое внедрение химии в быт, неблагоприятная окружающая среда и т.д. [6].
В состав флоры содержимого толстого кишечника входят анаэробные и аэробные бактерии. Нормальная микрофлора на 95% состоит из анаэробных видов бактерий, главными из которых являются бифидобактерии и лактобактерии. Аэробные бактерии, представленные кишечными палочками, энтерококками и др., составляют сопутствующую микрофлору. К остаточной микрофлоре относят стафилококки, клостридии, протей, грибы. Самые многочисленные и незаменимые представители полезной микрофлоры — это бифидобактерии.
Бифидобактерии стимулируют перистальтику, предупреждая нарушения стула, повышают эффективность факторов иммунитета организма, инактивируют некоторые канцерогены и вырабатывают витамины. Типичными продуктами жизнедеятельности бифидобактерий являются молочная, уксусная, муравьиная и янтарная кислоты, аминокислоты и белки, витамины В1, В2, К, никотиновая, пантотеновая и фолиевая кислоты, пиридоксин, цианокобаламин. Производя молочную и уксусную кислоту, они препятствуют размножению патогенных микроорганизмов. Бифидобактерии стимулируют лимфоидный аппарат человека и участвуют в процессе синтеза иммуноглобулинов. В клеточной стенке данных бактерий содержится большое количество мурамил-дипептида, который активирует образование В- и Т-лимфоцитов и макрофагов. Указанные бактерии являются естественными биосорбентами и способны накапливать значительное число соединений тяжелых металлов, фенолы, формальдегиды и другие токсичные вещества, попадающие в организм хозяина из окружающей среды и влияющие на снижение иммунитета [3, 8]. Еще одна группа полезных микроорганизмов — лактобактерии, без участия которых нельзя представить нормальную жизнедеятельность организма. Лактобациллы заселяют организм новорожденного в раннем постнатальном периоде. Средой обитания лактобацилл являются различные отделы желудочно-кишечного тракта, начиная с полости рта и кончая толстой кишкой. Лактобациллы (Lactobacillus acitophilus) обеспечивают своевременное опорожнение кишечника. Эти бактерии стимулируют образование IgА, которые, особенно в раннем детском возрасте, нейтрализуют пищевые аллергены и уменьшают их всасывание в кишечнике [8–10]. Кроме прямого влияния лактобактерий на сенсибилизацию при атопическом дерматите, в настоящее время доказано опосредованное воздействие дисбиоза кишечника на состав микрофлоры кожи при АД: снижение содержания лактобактерий в кишечнике приводит к повышению уровня Staphylococcus epidermidis на коже, которые являются дополнительным источником аллергизации организма [11, 12].
Под дисбиозом понимают состояние экосистемы, при котором нарушается функционирование ее составных частей и механизмов их взаимодействия (в зарубежной литературе применяется термин «Bacterial overgrowth syndrome» — «синдром избыточного бактериального роста», включающий в себя изменение количественного и видового состава микроорганизмов, характерных для биотопа). Дисбиотические состояния приводят к изменениям в количественном и качественном составе микрофлоры человека, что создает условия для реализации вирулентного действия условно-патогенных микроорганизмов, обычно обнаруживаемых в содержимом кишечника в небольших количествах. Обильно развивается гнилостная или бродильная флора, грибы, преимущественно рода Candida, в кишечнике могут обнаруживаться микроорганизмы, в норме нехарактерные для него. Они не способны выполнять многие физиологические функции, присущие нормальной микрофлоре, как результат — утрачивается способность инактивировать токсические продукты кишечного содержимого, нарушается поглощающая способность кишечника [3, 8]. Это, как правило, приводит к нарушению ферментного статуса пищеварительного тракта, создавая условия для развития патологии полостного, пристеночного и мембранного пищеварения и всасывания. Наблюдается повышенное поступление бактериальных и инфекционных аллергенов в организм ребенка. Значительно повышенная антигенная стимуляция недорасщепленными макромолекулами пищевых веществ и бактериальными аллергенами при слабости иммунного ответа и неспособности организма к элиминации комплексов антиген-антитело приводит к отягощению атопического дерматита [12]. Известно, что кожа имеет физиологическую связь с различными органами и системами организма человека и является своеобразным экраном, отражающим многие патологические процессы. В генезе атопического дерматита важная роль принадлежит пищевой сенсибилизации.
Обязательным условием коррекции дисбиоза кишечника является выявление и устранение причины его возникновения, а также эффективная терапия основного заболевания [13, 14].
В связи с этим принципы лечения атопического дерматита включают воздействие на основные звенья патогенеза аллергического воспаления и устранение аллергена. Оптимальные рекомендации по терапии ребенка с атопическим дерматитом должны включать следующие основные позиции:
1) мероприятия по устранению аллергена (элиминационная диета и изменения аллергенного окружения);
2) сеансы психотерапии;
3) наружную терапию (увлажняющие и смягчающие средства; топические глюкокортикоиды; топические ингибиторы кальциневрина; антисептики и местные антибактериальные препараты при осложненных формах);
4) системное лечение (антигистаминные препараты, стабилизаторы тучных клеток; антибактериальная терапия; энтеросорбенты, при тяжелом течении — системная иммуномодулирующая терапия) [15].
В протоколы лечения атопического дерматита у детей наряду с элиминационной диетой, приемом антигистаминных средств, местной терапией в течение многих десятилетий включают энтеросорбенты.
Сорбенты выводят из организма токсичные вещества и уменьшают метеоризм, как правило, наблюдающийся при дисбиозе. Показано также, что аутомикроорганизмы обеспечивают более быстрое восстановление нормального состояния микрофлоры кишечника, чем вводимые извне [16]. Основой пребиотиков являются препараты, содержащие бифидогенные факторы, стимулирующие рост и развитие полезных бактерий (лактулоза, соевый олигосахарид, ксилобиоза и др.). В практике хорошо зарекомендовали себя препараты, содержащие лактулозу. Идеальным сочетанием являются лекарственные средства, содержащие пребиотики и сорбенты.
В последние годы активно используются препараты на основе гидролизного лигнина — природного полимера растительного происхождения, продукта переработки древесины хвойных и лиственных пород деревьев. К таким препаратам относится пребиотик со свойствами сорбента Лактофильтрум (ОАО «Сти-Мед-Сорб», Россия) — комплексный препарат, содержащий гидролизный лигнин и лактулозу. Действие лигнинов основано на способности сорбировать и прочно удерживать токсины экзогенного и эндогенного происхождения, патогенные микроорганизмы, присутствующие в энтеральной среде. Лигнины обладают более высокой сорбционной емкостью по сравнению с другими сорбентами. Это обусловлено наличием в них не только активной поверхности частиц, но и развитой пористой системы. Лигнины не травмируют слизистую оболочку кишечника и обладают репаративными свойствами по отношению к ней [17, 18]. Лактулоза, входящая в состав Лактофильтрума, является синтетическим дисахаридом. Она не подвергается расщеплению ферментами в тонком кишечнике. Активное вещество лактулозы начинает действовать в толстой кишке, где под влиянием кишечной микрофлоры трансформируется в низкомолекулярные органические кислоты, в основном молочную, уксусную, масляную и пропионовую. Благодаря подкислению кишечного содержимого подавляется рост гнилостной и болезнетворной микрофлоры, увеличивается осмотическое давление в просвете толстой кишки. Важно также, что лактулоза не сорбируется на поверхности лигнина, т.к. ее молекула невелика по размеру и несет на своей поверхности (как и большинство активных групп лигнина) отрицательный заряд [19, 20]. Особенностью комплекса пребиотика (лактулозы) и сорбента (лигнина) является суммарный эффект, направленный на формирование оптимального микробиоценоза кишечника [21]. Кроме того, препарат имеет существенное преимущество перед другими энтеросорбентами — он представлен не в виде порошка или геля, что затрудняет дозирование, а в таблетированной форме, существенно улучшающей его органолептические свойства.
В 2002 г. в отделении аллергологии Научного центра здоровья детей РАМН проводилось исследование, целью которого был анализ эффективности препаратов Фильтрум (препарат растительного происхождения, получаемый из гидролизного лигнина) и Лактофильтрум в комплексной терапии детей с атопическим дерматитом и бронхиальной астмой [22]. Было обследовано 30 детей с атопическим дерматитом в возрасте от 3 до 15 лет (18 девочек и 12 мальчиков). Степень тяжести определялась с помощью шкалы SCORAD. Практически у всех детей (более 70%) имелась сопутствующая патология желудочно-кишечного тракта. Обследованные пациенты были разделены на две группы. Первая группа в составе комплексной терапии получала препарат Фильтрум, вторая — Лактофильтрум. Препараты назначались в течение 2 нед за час-полтора до еды. В результате исследования была отработана оптимальная терапевтическая дозировка препаратов. На фоне проводимого лечения препаратами отмечалась более выраженная положительная динамика со стороны клинических проявлений атопического дерматита. Так, в первой группе, получавшей Фильтрум, купирование гиперемии составило в среднем 3,5 ± 1 день, в контрольной группе 4,7 ± 1,5 дня (p Другое исследование проводилось в 2009 г. на базе Курского государственного медицинского университета, в котором принимали участие 96 детей в возрасте от 3 до 6 лет, страдающих атопическим дерматитом [23]. Пациенты были разделены на 3 группы, в зависимости от применяемой терапии. Детям I группы (n = 30) в качестве традиционной терапии назначали антигистаминные, мембраностабилизирующие и витаминные препараты, а также ингибиторы кальциневрина. Дети II группы (n = 33) дополнительно к указанным препаратам получали Лактофильтрум 0,5 мг 3 раза в день, 10 дней. Детям III группы (n = 33) кроме того назначали препарат Гепон (является иммуномодулятором и оказывает противовирусное действие). У пациентов второй и третьей групп клиническая ремиссия наступала в среднем на 3–6 сут раньше, нежели у пациентов первой группы. Во всех группах на фоне проведенного лечения выявлены признаки нормализации функции желудочно-кишечного тракта. Оценка терапевтической эффективности проводилась на основании динамики клинических проявлений (индекс SCORAD), а также показателей иммунного статуса. В группе детей, получавших Лактофильтрум и Гепон, выявлено статистически достоверное снижение индекса SCORAD. Переносимость Лактофильтрума и Гепона в представленых дозах была хорошей у всех детей. Побочных реакций не выявлено. Следовательно, включение указанных препаратов в комплексное лечение атопического дерматита у детей дошкольного возраста способствует более быстрому наступлению клинической ремиссии, более выраженной динамике симптомов нарушения гастроинтестинальной системы и коррекции иммунологических показателей. Высокая терапевтическая и иммуномодулирующая эффективность, отсутствие осложнений и побочных реакций при их применении позволяют рекомендовать эти препараты в комплексном лечении детей дошкольного возраста, страдающих атопическим дерматитом.
Учитывая, что кишечная микрофлора может участвовать в поддержании патологических расстройств при атопическом дерматите, для коррекции дисбиоза кишечника у детей с АД целесообразно использование средств, содержащих пребиотики и энтеросорбенты (препарат Лактофильтрум).
СПИСОК ЛИТЕРАТУРЫ
1. Bos J.D., Sillevis Smitt J.H. Atopic dermatitis. YEADV. 1996; 7: 101–114. Consensus Conference on Pediatric Atopic Dermatitis. J. Am. Acad. Dermatol. 2003; 49: 1088–1095.
2. Гущина Н.С. Совершенствование лечения и реабилитации детей младшего школьного возраста, больных атопическим дерматитом, в условиях санаторно-лесной школы. Автореф. дисс. канд. мед. наук. Москва. 1996. 30 с.
3. Жадамбаа С-Э., Батбаатар Г., Горшкова Г.В. Основные факторы, влияющие на течение атопического дерматита. IV Annual Meeting of Mongolian Society of allergology and International Educational Exchange Program American Academy of Allergy, Asthma and immunology. Ulaanbaatar. 2006. P. 15–16.
4. Смирнова Г.И. Современные принципы патогенетической терапии атопического дерматита у детей. Вопросы современной педиатрии. 2006; 5 (2): 50–56.
5. Плаксина И.А. Распространенность и клинико-иммунологические особенности течения атопического дерматита, сопровождающегося дисбиозом кишечника. Автореф. дисс. канд. мед. наук. Краснодар. 2007. С. 21.
6. Тучков Д.Ю. Синдром диареи при атопическом дерматите у детей раннего возраста. Автореф. дисс. канд. мед. наук. Оренбург. 2004. С. 20.
7. Ардатская М.Д., Минушкин О.Н. Современные принципы диагностики и фармакологической коррекции. Гастроэнтерология, прилож. к журналу. Consilium Medicum. 2006; 8 (2).
8. Суворова К.Н., Куклин В.Т., Рукавишникова В.М. Детская дерматовенерология. Казань. 1996. 441 с.
9. Cremonini F. et al. Meta-analysis: the effect. Aliment. Pharmacol. Ther. 2002; 16: 1461– 1467.
10. Фокина Р.А. Особенности течения атопического дерматита в условиях Якутии у детей и подростков в сравнительном аспекте. Дальневосточный медицинский журнал. 2007; 18–19.
11. Галлямова Ю.А. Атопический дерматит и дисбактериоз. Лечащий врач. 2010; 10.
12. Куваева И.Б., Ладодо К.С. Микроэкологические и иммунные нарушения у детей. Москва. 1991.
13. Пинегин Б.В., Мальцев В.Н., Коршунов В.М. Дисбиозы кишечника. Москва. 1984.
14. Потемкина A.M. Атопический дерматит у детей, профилактика, лечение, диспансеризация. Казань. 1999. 40 с.
15. Nancy T.W. Probiotics. American J. of Health-System Pharmacy. 2010; 67 (6): 449–458.
16. Бондаренко В.М., Учайкин В.Ф., Мурашова А.О., Абрамов Н.А. Дисбиоз. Современные возможности профилактики и лечения. Москва. 1995.
17. Gibson G.B., Wang X. Bifidogenic properties of different types of fructooligosaccharides. Food Microbiol. 1994; 11: 491–498.
18. Duffy L.C., Zielezny M.A., Riepenhoff-Talty M. et al. Effectiveness of Bifidobacterium bifidum in experimentally induced MRV infection: dietary implications in formulas for newborn. Endocr Regulations. 1993; 27: 223–229.
19. Ballongue J., Crociani J., Grill J.P. In vitro study of the effect of lactulose and lactitol on growth and metabolism of intestinal bacteria. Gut. 1995; 37 (Suppl. 2): A48.
20.Bezkorovainiy A., Miller-Catchpole R. Biochemistry and physiology of bifidobacteria. Boca Raton: CRC Press. 1989. Р. 226.
21. Портнова И.В., Гамалеева А.В., Ревякина В.А. Энтеросорбенты в терапии аллергических заболеваний у детей. Лечащий врач. 2002; 4: 27.
28. Сароян А.С., Силина Л.В. Опыт применения лактофильтрума и гепона при атопическом дерматите у детей дошкольного возраста. Сборник тезисов НАДК. Уфа. 2009.
Атопический дерматит (АД) – хроническое рецидивирующее заболевание кожи, проявляющееся интенсивным зудом, высыпаниями в сочетании другими многочисленными признаками атопии (необычностью) – атопический ринит, бронхиальная астма, мигрень, гастродуоденит и др.
Атопический дерматит — симптомы
АД в мире страдают 5-15 % детей и 2-10 % взрослых, впервые выявленный в детстве АД продолжается у 45- 60 % взрослых пациентов. АД отличается хроническим рецидивирующим течением с возрастной динамикой клинических проявлений. По проявлениям заболевание возможно разделить на три периода.
- В младенческом возрасте (до 1.5-2 лет) заболевание носит острый характер, преобладают явления покраснения, отечности, мокнутия и коркообразования.
- В период от 2 лет до полового созревания болезнь носит характер хронического воспаления, на коже на первый план выступают явления гиперемии (эритемы) и шелушения, признаки вегетососудистой дистонии. Кожа в очагах поражения гиперпигментирована, из-за сильного зуда появляются множественные расчесы.
- У детей старшего возраста и взрослых преобладают явления инфильтрации (уплотнения) на фоне гиперемии застойного характера. На коже могут появляться зудящие высыпания, имеющие цвет нормальной кожи, которые сливаются в очаги сплошной папулезной инфильтрации. Обычно к 50 годам заболевание самостоятельно регрессирует.
Атопический дерматит – многофакторное заболевание, характеризующееся аномальным иммунным ответом на аллергены природного происхождения, наследственной предрасположенностью к заболеванию, хроническим рецидивирующим течением. Большое внимание уделяется различным факторам, запускающим процесс в коже и длительно поддерживающим хроническое течение заболевания. К таким факторам относятся бактериальные, вирусные, грибковые, паразитарные и кишечные инфекции, продукты питания и химические вещества (добавки к пище, лекарства), клещи из домашней пыли.
Атопический дерматит и хеликобактер пилори
В последние годы доказана связь атопического дерматита с болезнями органов пищеварения. Установлено, что большинство больных, страдающих АД, имеют хронический гастрит, гастродуоденит, синдром раздраженного кишечника с запорами, заболевания печени и желчного пузыря, нарушение микрофлоры кишечника и др. Нередко существование этих сопутствующих болезней является пусковым фактором атопического дерматита, как у детей, так и у взрослых.
Так, в последние десятилетия в возникновении заболеваний желудка доказана роль специфического микроорганизма – Helicobacter pylori (НР), повреждающего слизистую оболочку желудка. Его наличие способствует активному поступлению токсинов и аллергенов в организм, развитию хронического воспаления слизистой желудка. У больных атопическим дерматитом в 90% случаев при проведении эндоскопического обследования желудка выявляется хронический гастрит и в 82.5% ассоциированный с НР. Отмечена связь между степенью обсеменения бактериями слизистой желудка, активностью хронического гастрита и степенью тяжести АД, что явилось обоснованием к включению в план обследования больных АД на хеликобактериоз и лечебных мероприятий антихеликобактерной терапии. Клинически гастриты у большей части больных АД протекают бессимптомно.
Эрадикация хеликобактера приводит к разрешению заболевания почти у трети больных АД, к улучшению течения АД у остальных пациентов, и самое главное, удлинению периода ремиссии заболевания АД и перехода непрерывного течения заболевания к рецидивирующему.
Обязательным условием профилактики АД у больных хроническим гастритом, ассоциированным с НР, учитывая оральный путь инфицирования, является обследование на хеликобактериоз контактных лиц в семье и вне ее!
Защитная роль кишечника
Здоровье невозможно без нормального функционирования кишечника, которому принадлежит большая роль в детоксикации и иммунологических процессах, которые протекают в организме человека. Слизистая кишечника представляет собой место контакта организма с окружающей средой. Для сравнения: поверхность кожи составляет около 2 квадратных метров, площадь же слизистой оболочки желудочно-кишечного тракта – около 400 квадратных метров. Поэтому слизистую кишечника считают самой большой частью защитной системы организма.
Для надежной защиты от внешнего вмешательства в пищеварительном тракте важнейшим оказался микробиологический барьер.
- Защитная микрофлора кишечника наиболее многочисленная (95%) и представлена в основном бифидобактериями, лактобактериями и кишечной палочкой. Эти микроорганизмы выделяют молочную и уксусную кислоты и другие вещества, которые обладают антимикробным действием и препятствуют проникновению и закреплению на слизистой кишечника вредных микроорганизмов, которые не свойственны человеку. Они стимулируют иммунную систему организма человека, являются сорбентами, которые способны накапливать значительное количество тяжелых металлов и других токсических веществ.
- Сапрофитная микрофлора кишечника представлена стафилококками, энтерококками и другими микроорганизмами, основная роль которых — утилизация конечных продуктов обмена организма человека.
- Оппортунистическая микрофлора представлена различными микроорганизмами (стрептококки, золотистый стафилококк, грамотрицательные энтерококки, грибы рода кандид и др.), которые при определенных условиях вызывают патологический процесс.
Для человеческого организма исключительно важно поддержание требуемого состава и количества кишечных бактерий. Оптимальные условия могут быть нарушены вследствие неправильного питания, возбудителями диареи (бактерии и паразиты), дополнительными отрицательными факторами могут быть токсические вещества, поступающие из окружающей среды, например, тяжелые вещества – кадмий, свинец, ртуть, а также путешествия в другие страны с иными микроорганизмами. Отрицательным действием на флору обладают многие лекарственные средства и методы лечения, непереносимость продуктов питания, вредно одностороннее и несбалансированное питание, недостаточность пищеварительных ферментов.
Атопический дерматит и дисбактериоз
Многие кожные болезни, и в том числе Атопический дерматит, сопровождаются дисбактериозом, и при этом считается, что отягощающим фактором при АД является недостаточное количество лактобактерий. Именно лактобактерии в значительной степени снижают всасывание аллергенов в кишечнике и стимулируют образование иммуноглобулинов класса А, которые, особенно в раннем возрасте, являются основными антителами против пищевых аллергенов.
В настоящее время считают, что возникновение кожных заболеваний в определенной мере связано с нарушением микроэкологического баланса кишечника. У 80-95% больных атопическим дерматитом отмечается дисбактериоз кишечника, при этом наряду с дефицитом лактобактерий и бифидобактерий наблюдается избыточный рост золотистого стафилококка, кишечной палочки с измененными свойствами, грибов роста кандид, выделяющих токсины.
Эти нарушения требуют санации кишечника от вредных бактерий, проведения детоксикационной терапии (энтеросорбции) и создания условий для развития собственной микрофлоры пациента, регуляции работы кишечника (борьба с запорами). Энтеросорбция – неинвазивный метод детоксикации и направлена она на выведение из организма различных эндогенных и экзогенных аллергенов, токсинов, условно-патогенных микроорганизмов и продуктов их жизнедеятельности. Одним из самых эффективных сорбентов являются природные органические на основе пищевых волокон, таких как лигнин, который не усваивается в пищеварительной системе и обладает высокой сорбционной активностью.
Новое направление лечения АД представляет собой применение пребиотиков (лактулоза), полученных из естественных источников и выступающих в качестве питательной среды для развития своей собственной нормальной флоры кишечника. Сочетание сорбента и пребиотика представлено в препарате Лактофильтрум, который производится из компонентов природного происхождения в таблетированной форме, прост в употреблении — по 2 таблетки 3 раза в день в течение 3-4 недель.
В клинической практике выявлена корреляция между степенью выраженности дисбактериоза и проявлений АД. Кроме прямого влияния дисбактериоза на сенсибилизацию организма при АД, в настоящее время доказано опосредованное влияние на состав аутомикрофлоры кожи у больного АД.
Образование токсических веществ в кишечнике в дальнейшем действует не только на иммунную систему, но и нарушает детоксикационную функцию печени, образование и выделение желчи из печени, желчевыводящих путей и желчного пузыря.
Атопический дерматит и желчный пузырь
При обследовании больных, страдающих атопическим дерматитом, в 60% случаев определяется дискинезия желчевыводящих путей, у взрослых по гипотоническому типу, т.е. желчный пузырь плохо сокращается, и не выводятся токсические вещества из организма.
У 31% пациентов в желчном пузыре определяется густая желчь, с хлопьями или мягкими конкрементами (сладж желчи), что свидетельствует о нарушении качественного состава желчи, продуцируемой печенью. Таким образом, нарушается еще одна функция органов пищеварения, осуществляющая детоксикационную функцию организма.
При этом в комплекс лечения больных АД добавляются желчегонные препараты (желчегонные сборы трав, Хофитол, Гепабене, настой шиповника или Холосас, Холит и др.), а также назначаются препараты, улучшающие функцию печени и качество желчи, продуцируемой печенью (Урсофальк, Урсосан, Уролесан), препараты расторопши, гептрал, гепатосан и др., проводятся гуманные тюбажи желчного пузыря (с растительными маслами, медом, минеральной водой).
Клинический опыт показывает, что улучшение состояния микрофлоры кишечника, регуляция работы кишечника без запоров и улучшение работы печени и желчевыводящей системы и желчного пузыря способствует более эффективному лечению больных с атопическим дерматитом.
Питание при атопическом дерматите
Несколько слов о питании у больных АД. Питание для больных АД во многих случаях не играет настолько большой роли, как часто полагают. Существует огромное количество продуктов питания, для которых выявлена взаимосвязь с АД, но в конечном счете реальным фактором является только индивидуальная чувствительность. Существует целый спектр потенциально опасных продуктов, и каждый пациент должен составить индивидуальный рацион питания. Пациентам с АД необходимо соблюдать полноценное питание, избегать строгих диет, особенно в детском возрасте.
Продукты питания, которые могут оказывать негативное воздействие на Атопический дерматит:
- Острые, копченые продукты,
- пряности,
- алкоголь,
- овощи (перец, редис, квашеная капуста, сельдерей, помидоры),
- орехи,
- сладости (мед, сахар, сушеные фрукты, шоколад),
- крепкие мясные бульоны,
- маринады,
- кофе, какао,
- яйца, молоко,
- рыба,
- пищевые добавки, консерванты, пищевые красители.
Пациент и сам должен активно участвовать в процессе оздоровления своего организма. Особенно следует обратить внимание на такие важные мероприятия как:
- полноценное питание,
- отказ от сахара,
- употребление в пищу пищевых волокон (отруби, пектины, сложные углеводы),
- употребление кисломолочных продуктов, заквашенных лактобактериями, или препараты с лактобактериями,
- отказ от свинины.
Атопический дерматит — фитотерапия
Важное место в лечении и профилактике обострений играет фитодиетология. Она включает использование соков из клюквы, черной смородины, красной и черноплодной рябины, свекольный, сливовый, яблочный, черничный, тыквенный, капустный соки.
Лечение Атопического дерматита травяными сборами
Несколько прописей травяных сборов, применяемых при АД.
- Сбор 1. Трава череды 10.0, листья подорожника 10.0, листья крапивы 10.0, трава полыни 5.0, трава тысячелистника 5.0, трава зверобоя 15.0, трава хвоща 10.0, листья толокнянки 20.0. Смешать, приготовить настой из 1 чайной/столовой ложки (в зависимости от возраста). Принимать по 1/3 стакана 3 раза в день до еды, прием 1-2 месяца.
- Сбор 2. Трава трехцветной фиалки 20.0, корень девясила 10.0, трава зверобоя 15.0, трава хвоща 10.0, шишки хмеля 10.0, трава душицы 10.0, цветки ромашки 15.0, трава мяты перечной 5.0. Смешать. Доза и способ приготовления настоя. Принимать по 1/3 стакана 3 раза в день после еды в течение 1-2 месяцев.
- Атопический дерматит с сопутствующими запорами. К 1и 2 настою добавить слабительный сбор, настой плодов фенхеля (5.0:200.0), настой листьев подорожника (10.0:200.0), настой плодов тмина (5.09:200.0) или препараты лактулозы (Дюфалак, Нормаза, лактусан)
- Атопический дерматит при длительном течении процесса, особенно в зимне-весеннем периоде. Используются растительные лекарственные препараты с витаминными свойствами. Это настой листьев крапивы (15.0:200.), плодов шиповника (10.0:200.0), листьев черной смородины и ее плодов.
- Атопический дерматит с выраженными мокнутиями, отечностью и инфильтраций кожных покровов. Полезны настои плодов можжевельника (5.0:200.0), листьев почечного чая (3.5:200.0), травы хвоща полевого (10.0:200.0), мочегонного сбора.
- В целях улучшения показателей неспецифического иммунитета применяют настой цветков черной бузины (5.0:200.0), настой корня солодки (10.0:200.0), экстракт элеутерококка или настойку аралии по 2-3 капли (в зависимости от возраста ребенка) утром и вечером в течение 2 недель.
- Сбор для нормализации углеводного обмена. Настой листьев крапивы (10.0:200.0), отвар корня одуванчика (10.0:200.), настой листьев черники (10.0:200.0), отвар корня лопуха (5.0:200.0). Эти настои обладают противовоспалительным, противозудным свойством, оказывают нормализующее действие на желчевыводящие пути и поджелудочную железу.
Местное лечение Атопического дерматита
Для регенерации кожи используется и наружная терапия, принципом которой является: «влажное наносится на влажное». Рекомендуется использовать проницаемые воздухом влажные повязки. Компрессы накладываются трижды в день, каждая процедура продолжается 1 час. В качестве используемых средств используется черный и зеленый чай, ромашковый чай.
Примеры повязок на мокнущие поверхности:
- Повязка с настоем коры дуба: 2 столовые ложки дубовой коры разводятся в 500 мл воды и кипятятся в течение 15 минут, после чего настой процеживают, остужают, в него опускают ткань для компресса и неплотно накладывают на больное место. Достаточно применять такие компрессы 3-4 дня, но ежедневно нужно готовить свежий отвар.
- С этой же целью можно использовать отвар лапчатки (15г:200.0), настой травы зверобоя или тысячелистника (15г:200.0).
- Компресс из трехцветных фиалок: 2 чайные ложки сухих фиалок настаивают в чашке кипятка, получившийся настой сливают, остужают и используют для компрессов на пораженные места.
- Очень широко используются растворы соли, например ванны с солями Мертвого моря. При правильном комплексном лечении мучительный зуд исчезает быстро, но если он сохраняется, то втирание разведенного яблочного уксуса может в значительной степени облегчить зуд.
- После прекращения мокнутий применяются мази, кремы. Пример мази следующего состава: сок подорожника 15 мл, настойка ландыша 5 мл, настойка валерианы 5 мл, настойка календулы 5 мл, димедрол 1 г, паста цинковая 79 г. Смешать. Наносить на пораженные участки 2-3 раза в день тонким слоем после удаления ранее нанесенной мази растительным маслом.
Для очистки кожи не использовать мыло! Можно использовать масляно-молочную ванну: 1 столовая ложка оливкового масла и 200 мл молока добавляются в ванну.
Следует придерживаться правила: каждые 3-4 дня препараты наружной терапии следует менять между собой для предупреждения развития побочных эффектов.
Читайте также:

