Как лечить ожог после лучевой терапии в прямой кишке
Обновлено: 26.04.2024
Воспаление кишки после лучевой терапии - лучевой проктит и энтерит
Острые и хронические побочные эффекты возникают после облучения таза, как правило, по поводу рака предстательной железы или женских половых органов. Обычные дозы: рак простаты - 64-74 Гр, рак шейки матки - 45 Гр, рак эндометрия - 45-50 Гр, рак прямой кишки - 25-50,4 Гр, рак мочевого пузыря - 64 Гр.
Очаговое поражение прямой кишки может являться результатом брахитерапии: имплантации радиактивных зерен или внутриполостного облучения. Лучевое поражение может возникать в областях, располагающихся за пределами полей облучения: например, рассеянное облучение может привести к диффузному лучевому энтериту!
Повреждения зависят от общей дозы (обычно > 40 Гр), энергии пучка и очаговой дозы, размера фракции и поля, времени подведения, пролиферации и оксигенации тканей.
В развитии лучевых повреждений выделяют две фазы:
1. Острая: обычно самоограничивающаяся цитотоксичность радикалов и индуцированных повреждений ДНК быстро обновляющихся клеточных популяций (эпителий кишечника, костный мозг, придатки кожи и т.д.).
2. Хроническая: постоянные и необратимые повреждения, связанные с микроишемией в результате облитерирующего эндартериита, дегенерации эндотелия, неоваскуляризации, интерстициального фиброза, разрушения эпителия.
Роль превентивных препаратов (балсалазид, мизопростол, сукральфат и т.д.) при назначении лучевой терапии остается спорной.

а) Эпидемиология:
• Ранние повреждения: 30-70% больных, подвергнутых облучению таза в сроки < 3-6 недель от начала лечения.
• Хронические повреждения: через 1-20 лет после лучевого воздействия. По устаревшим данным: 20-25%, по новейшим данным - 3-8% (вероятно как результат усовершенствования методик расчета доз и симуляции).
б) Симптомы воспаления кишки после лучевой терапии:
• Острый проктит: диарея, отхождение слизи и крови со стулом, императивные позывы/инконтиненция, тенезмы, боль, перианальный дерматит. Системные явления нетипичны и чаще связаны с общими побочными эффектами лечения: анемия, анорексия, истощение/потеря веса. Острые симптомы разрешаются через 6-12 недель.
• Хронический лучевой проктит: кровотечение (изъязвление, телеангиэктазии), диарея, отхождение слизи со стулом, императивные позывы/инконтиненция (уменьшение резервуарной функции и адаптационной способности прямой кишки), тенезмы, перианальный дерматит.
Осложнения: кровотечение, обструкция (формирование стриктуры), образование свища (например, ректовагинального), инконтиненция (повреждение нервов, сфинктера, утрата резервуарной функции). Увеличение риска развития вторичных опухолей.

Прямокишечно-влагалищный свищ после лучевой терапии по поводу рака шейки матки
в) Дифференциальный диагноз:
• Рецидив опухоли, ВЗК (язвенный колит, болезнь Крона, недетерминированный колит), ишемический колит, инфекционный колит (включая псевдомембраиозный колит, обусловленный С. difficile), проктиты при ЗППП (например, гонорейный, венерическая лимфогранулема), СРК.
• Внимание: избегайте «быстрого» диагноза/лечения по поводу «геморроя» у больных с облученной прямой кишкой!
г) Патоморфология лучевого проктита и энтерита
Макроскопическое исследование:
• Гиперемированная/отечная слизистая, некрозы, изъязвления/свищевые отверстия, телеангиэктазии, стриктуры, укорочение кишки.
Микроскопическое исследование:
• Острое повреждение: изъязвление эпителия, мегануклеоз, воспаление собственной пластинки, отсутствие митотической активности.
• Хроническое повреждение: фиброз субинтимы артериол (облитерирующий эндартериит), дегенеративные изменения эндотелия, фиброз собственной пластинки, повреждение крипт, гипертрофия Ауэрбаховского сплетения мышечного слоя кишки.
д) Обследование при воспалении кишки после лучевой терапии
Необходимый минимальный стандарт:
• Ригидная или фибросигмоидоскопия: обычно достаточна для установления диагноза, полный осмотр кишки выполняется по общим показаниям.
• Внимание: биопсия патологических образований/язвы передней локализации противопоказана в связи с риском образования ятрогенного ректовагинального/ректовезикального свища!
Дополнительные исследования (необязательные):
• Рентгеноконтрастные исследования (с барием или гастрографином) в случаях невозможности выполнения колоноскопии (например, стриктура) или необходимости определения свищевого хода.
• Виртуальная колоноскопия: роль не определена, имеется риск перфорации.
• МРТ, ПЭТ, ПЭТ-КТ: роль не определена.
• Физиологические исследования: определение функции аноректум (например, адаптационная способность прямой кишки и т.д.).
• Лабораторные исследования: пищевой статус.
• Пассаж по тонкой кишке: признаки «короткой» кишки (укорочение?).
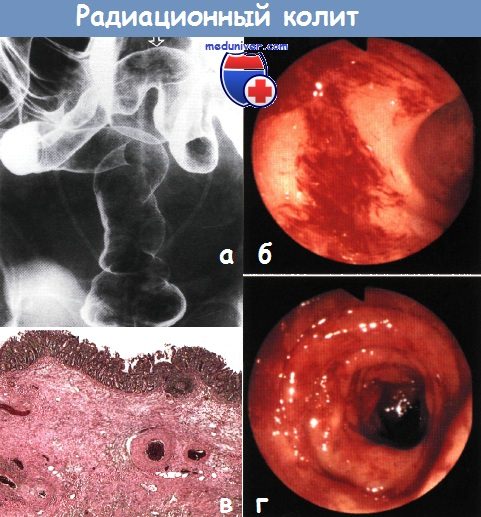
а - Лучевой проктосигмоидит. Ректосигмоидный отдел толстой кишки сужен, трубчатой формы, с потерей клапанов Хьюстона.
Слизистая оболочка ректосигмоидного соединения и дистальной части сигмовидной кишки (показано стрелкой) мелкозернистая. Стенты мочеточников в правильном положении. Клизма с барием, двойное контрастирование.
б,г - Эндоскопическая картина радиационного колита. Диагноз подтвержден наличием множественных телеангиэктазий.
в - Гистологическая картина лучевого энтерита. Наблюдаются подслизистый фиброз и утолщение стенки сосудов без признаков воспаления.
е) Классификация:
• Лучевой проктит: острый или хронический, локализованный или диффузный.
• Лучевой энтерит: острый или хронический, локализованный или диффузный.
• Вторичные осложнения, связанные с облучением (стриктура, свищ и т.д.).
ж) Лечение без операции воспаления кишки после лучевой терапии:
- Острый лучевой проктит: временные меры (регуляция стула, антидиарейные препараты, уход за перианальной кожей) и терпение; местные лекарственные препараты (сукральфат, стероиды или клизмы с ацетилсалициловой кислотой), отключение кишки при тяжелом, плохо переносимом заболевании.
- Хронические лучевые повреждения: лечение отсутствует, плохое состояние тканей => симптоматическая терапия:
• Антидиарейные препараты и спазмолитики.
• Местные противовоспалительные препараты: свечи/клизмы со стероидами, ацетилсалициловой кислотой, сукральфат, мизопростол.
• Пероральные антибиотики: метронидазол.
• Витаминные добавки: витамины С и Е.
• Потенциальные преимущества полного парентерального питания в домашних условиях.
• Восстановление целостности слизистой толстой кишки: клизма с жирными кислотами с короткой цепью (химически нестабильные соединения, малоприменимые на практике).
• Лазерная аблация: необходимость множественных сеансов.
• Инстилляция формалином: нанесение 50 мл 4% раствора формалина на 2-3 минуты на область поражения с последующим обильным промыванием физраствором. Обычно дает быстрые результаты, могут потребоваться повторные сеансы.
з) Операция при лучевом проктите и энтерите
Показания:
• Выраженные и устойчивые к лечению симптомы: кровотечение, тенезмы, отделяемое, инконтиненция.
• Обструкция: формирование стриктуры.
• Формирование свища.
• Невозможность исключения вероятного рецидива опухоли.
Хирургический подход:
• Иссечение области лучевых повреждений с реконструкцией или без (может быть очень сложным).
• Облегчение симптомов без резекции пораженных тканей: отключение пассажа кала/мочи.
и) Результаты лечения воспаления кишки после лучевой терапии:
• Острые лучевые реакции: самокупирующиеся обычно в течение 6-12 недель.
• Хронические лучевые повреждения: часто можно добиться ответа на консервативное лечение, требуются повторные сеансы лечения. В будущем ожидается снижение тяжелых повреждений (более совершенная техника облучения).
• Анастомозы в области облучения: повышенный риск несостоятельности => рекомендуется формирование временной отключающей стомы.
• Отключение кишки: некоторые симптомы (выделение слизи, крови, болевой синдром) могут сохраняться.
к) Наблюдение. Частые визиты до тех пор, пока сохраняется симптоматика. В дальнейшем - обычное наблюдение.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Человека, у которого диагностировано онкологическое заболевание, всегда волнует, как теперь изменится его жизнь. Помимо предстоящего лечения, возникают некоторые ограничения, противопоказания.
Не стоит бояться, что теперь вся жизнь будет состоять из сплошных запретов. В целом во время лечения и после наступления ремиссии можно вести привычную жизнь, заниматься любимыми делами, принимать пищу, которая нравится. Но важно соблюдать некоторые рекомендации, потому что от этого может зависеть успех в борьбе с заболеванием.

Какие продукты питания противопоказаны при онкологических заболеваниях?
Принципы здорового питания едины для здоровых людей и онкологических больных. К продуктам, способствующим развитию рака и в целом ухудшающим состояние здоровья, относят красное (баранина, свинина, говядина) и обработанное (соленое, копченое, гриль, барбекю, бекон) мясо, колбасы и сосиски, фастфуд, продукты с добавленными сахарами, в первую очередь кондитерские изделия и сладкую газировку.
Это не означает, что одна плитка шоколада или один бургер сразу же ухудшат состояние онкологического больного. Речь о регулярном употреблении. Важно, какую часть рациона составляют те или иные продукты. Всё «вредное», конечно, надо ограничить. Но иногда можно себя побаловать.
Некоторые химиопрепараты вызывают тошноту, запоры, потерю аппетита, приводят к изменению чувства вкуса, поражению слизистых оболочек. В таких случаях нужна специальная диета. Соответствующие рекомендации вы найдете в нашей статье «Побочные эффекты химиотерапии».
Еще один возможный побочный эффект химиопрепаратов — лейкопения, снижение уровня лейкоцитов в крови. Из-за этого ослабляется иммунная защита и возрастает риск развития инфекций, в том числе пищевых. Для пациента с лейкопенией запрещены следующие продукты:
- Недоваренное мясо. Стоит приобрести специальный пищевой термометр, чтобы проверять готовность продуктов.
- Сыровяленые и сырокопченые колбасы, мясо.
- Непастеризованное молоко и любые приготовленные из него продукты (сыры, йогурты).
- Суши из сырой рыбы.
- Немытые свежие овощи и фрукты.
- Яйца, вареные всмятку, продукты, приготовленные из сырых яиц (например, домашний майонез).
Рекомендуемые продукты питания при раке
Организм онкологического больного борется с опасным заболеванием, испытывает дополнительную нагрузку из-за лечения. Чтобы вовремя восстанавливать ресурсы, ему нужно достаточное количество белков и других нутриентов, калорий. При этом пища должна быть здоровой.
К продуктам с наиболее высоким содержанием белка и калорий относятся: фасоль, курятина, мясо, йогурты, рыба, яйца. Они особенно важны для онкологических пациентов, которые сильно потеряли в весе, страдают анорексией.
Некоторые больные, напротив, страдают избыточным весом, ожирением. Им рекомендуется есть больше овощей и фруктов, выбирать нежирное мясо, максимально ограничить продукты с высоким содержанием жиров (масло, майонез, десерты, жареное), соль.
Для каждого пациента в онкологии диету подбирают индивидуально. Важно учитывать не только потребности организма, но и личные предпочтения человека — пища должна быть вкусной. В «Евроонко» есть собственный ресторан, в нем работают профессиональные повара.
Сколько воды можно пить онкологическому больному?
У многих онкобольных повышен риск обезвоживания из-за рвоты, диареи, лихорадки, некоторых лекарственных препаратов, которые используются при лечении рака. Для профилактики этого состояния рекомендуется ежедневно выпивать 2¬—2,5 литра воды (проконсультируйтесь с врачом — потребности в жидкости индивидуальны и зависят от ряда факторов).
Лучше пить обычную воду. Для придания вкуса в нее можно положить дольку лимона. Можно пить травяные чаи. Чая и кофе следует избегать: в них содержится кофеин, который действует как мочегонное. В газировках и магазинных соках содержатся добавленные сахара — они вредны для здоровья.
При некоторых состояниях в онкологии потребление жидкости, напротив, рекомендуется ограничить. Такие пациенты получают соответствующие рекомендации от лечащего врача.
Витамины и рак
Витамины важны для организма человека, но их не стоит переоценивать. Тут не работает правило «больше — лучше». Витамины не лечат от рака, некоторые из них, напротив, способствуют прогрессированию опухоли и ухудшают течение заболевания. Вы можете узнать об этом подробнее из нашей статьи «Витамины и рак».
Курение
О том, что курение вредит здоровью и приводит к онкологическим заболеваниям, наверное, знают все еще со школьной скамьи. Но курильщиков это не останавливает: среди тех, у кого уже диагностирован рак, более половины не расстаются с вредной привычкой. Обычно это аргументируют тем, что всё самое страшное уже произошло, и бросать курить нет смысла.
На самом деле, смысл есть. Позаботиться о своем здоровье никогда не поздно. Например, одно исследование показало, что больные раком легкого, которые бросили курить сразу после того, как им был установлен диагноз, или незадолго до этого, в среднем живут дольше. После отказа от сигарет противоопухолевые препараты начинают работать эффективнее, снижается риск побочных эффектов, рецидива, сокращается восстановительный период после лечения, в целом улучшается самочувствие и появляется больше энергии. Мы подробно рассказывали об этом в статье «Если уже рак: курить или не курить?».
Посещение бань и саун
В прошлом веке в онкологии существовал строгий запрет на посещение бань и саун для больных и людей, которые находятся в ремиссии. Считалось, что высокая температура провоцирует развитие рака и способствует распространению злокачественных клеток в организме. В настоящее время известно, что всё не так однозначно. Температура выше 40 градусов повышает чувствительность опухолей к препаратам и помогает их уничтожать. Этот принцип даже используют в современных клиниках онкологии — например, во время гипертермической интраперитонеальной химиотерапии (HIPEC).
Конечно же, тут нет никакого призыва лечить рак с помощью бани, как предлагают некоторые народные целители. Онкологические больные должны лечиться в специализированных клиниках онкологии, в соответствии с актуальными протоколами. А после завершения лечения никто не запрещает посещать бани, сауны и спа.
Некоторые люди боятся, что высокие температуры в бане и сауне могут вызвать рак кожи. Этому нет никаких доказательств. Для кожи опасны только солярии, в которых есть ультрафиолетовые лучи. Высокие температуры повышают риск развития злокачественных опухолей кожи, только если они вызывают сильные ожоги.
Солнечный загар
Ультрафиолетовое излучение повреждает ДНК и может привести к злокачественному перерождению клеток. Это один из самых значимых факторов риска развития рака кожи и меланомы. Чрезмерного воздействия ультрафиолетовых лучей нужно избегать даже здоровым людям, а для онкологических больных они особенно опасны, потому что многие химиопрепараты и лучевая терапия повышают чувствительность кожи.
Во время лечения важно соблюдать эти рекомендации:
- Старайтесь не бывать на улице в пик солнечной активности (между 10.00 и 16.00).
- Максимально закрывайте тело одеждой. Но помните, что перегревание и дегидратация опасны для онкологических больных. Выбирайте «дышащие» ткани: льняные, бамбуковые, хлопчатобумажные.
- Надевайте шляпу с широкими полями. Это особенно важно, если в результате химиотерапии выпали волосы.
- Старайтесь находиться в тени.
- Не сидите подолгу возле водоемов. Вода отражает солнечные лучи.
- Когда собираетесь на улицу в жаркую погоду, возьмите бутылку с водой.
- Используйте солнцезащитный крем.
Читайте подробнее о влиянии ультрафиолетового излучения на кожу в нашей статье «Загар — прямая причина рака кожи».
Употребление алкоголя при онкологических заболеваниях
Алкоголь — один из факторов риска развития многих онкологических заболеваний. Но строгого запрета на его употребление для больных в современной онкологии нет.
Важно помнить о двух моментах:
- Риски зависят от объема и регулярности употребления алкогольных напитков. Существуют максимальные безопасные дозы: для мужчин 28 граммов этилового спирта в день (700 мл пива, 300 мл вина или 90 мл водки), для женщин вдвое меньше. Конечно же, это не повод каждый день выпивать всю «норму», особенно если у человека онкологическое заболевание. Но от одного бокала вина не случится ничего страшного.
- Многие химиопрепараты выводятся из организма через печень. Она же утилизирует алкоголь. Таким образом, при употреблении спиртного орган испытывает двойную нагрузку. Некоторые противоопухолевые препараты поражают слизистые оболочки. Поэтому, если человек, страдающий раком, хочет принять алкоголь, предварительно нужно посоветоваться с лечащим врачом.
Читайте подробности в статье «Алкоголь при онкологических заболеваниях» на канале «Евроонко» в Яндекс Дзен.
Можно ли делать онкологическим больным массаж?
Онкологическое заболевание не является абсолютным противопоказанием к лечебному массажу. Он не способствует распространению раковых клеток в организме, этому нет никаких научных доказательств. В целом онкологические больные могут посещать массажистов, существуют лишь некоторые небольшие ограничения:
- Предварительно нужно проконсультироваться с лечащим врачом.
- При онкологических заболеваниях противопоказан глубокий массаж.
- Не стоит посещать сомнительные массажные салоны: пользуйтесь услугами сертифицированных массажистов.
- При проведении массажа нужно учитывать общее ослабленное состояние организма пациента, влияние химиотерапии и лучевой терапии, а также все осложнения и сопутствующие патологии.
- Массаж нельзя делать на частях тела, на которых проводится лучевая терапия, если на коже имеются раны и другие повреждения.
- На конечностях с лимфедемой (отеком в результате нарушения оттока лимфы после удаления лимфатических узлов) нельзя делать классический массаж, но можно специальный лимфодренажный для уменьшения отека.
Почему нельзя заниматься самолечением при раке?
Лучевая терапия — это один из ведущих методов противоопухолевого лечения, основанный на использовании ионизирующего излучения. Может применяться как самостоятельный вид терапии, так и в рамках комбинированного/комплексного лечения (совместно с другими методами), в качестве радикальной, нео- и адъювантной, консолидирующей, профилактической и паллиативной терапии.
Эффективность данного метода основана на повреждении ДНК. Существуют различные механизмы, позволяющие более эффективно разрушать опухолевые клетки в сравнении с нормальными. Во-первых, опухолевые клетки более активно делятся, соответственно, их ДНК чаще находится в «рабочем» режиме, когда она менее устойчива к воздействию ионизирующего излучения. По той же причине большая часть острых лучевых реакций представлена мукозитами, то есть воспалением слизистых, которым также свойственно активное деление. Во-вторых, окружающие здоровые клетки способствуют восстановлению поврежденных, подвергшихся лучевому воздействию. Поэтому важно сделать так, чтобы в объём облучения попало как можно меньше здоровой ткани. В-третьих, современное оборудование для лучевой терапии, управляемое командой грамотных специалистов, позволяет подвести максимально высокие дозы прямо в мишень, существенно снижая дозу ионизирующего излучения, приходящуюся к окружающим здоровым органам и тканям.

Виды лучевой терапии
Уже несколько десятилетий человечество изучает воздействие ионизирующего излучение на организм человека. При этом акцентируется внимание как на положительном, так и отрицательном эффекте, возникающем при его применении. Разрабатываются новые методы, которые позволяют добиваться максимального лечебного эффекта при снижении отрицательного действия на организм. Улучшается оборудование для проведения лучевой терапии, появляются новые технологии облучения.
Сейчас классификация методов лучевой терапии довольно обширна. Мы остановимся только на самых распространенных методиках.
Контактная лучевая терапия
При контактной лучевой терапии источник излучения вводится непосредственно в опухоль или прилегает к ее поверхности. Это позволяет прицельно облучать новообразование с минимумом воздействия на окружающие его ткани.
К контактным видам лучевой терапии относятся:
- Аппликационная лучевая терапия. Применяется при лечении поверхностно расположенных опухолей, например, новообразований кожи, слизистых оболочек гениталий. В этом случае используются индивидуально изготовленные аппликаторы, которые накладываются непосредственно на поверхность новообразования.
- Внутриполостная лучевая терапия. Источник ионизирующего излучения вводится в просвет полого органа, например, в пищевод, мочевой пузырь, прямую кишку, полость матки или влагалища. Для облучения используются специальные аппликаторы (их называют эндостатами), которые заполняются радионуклидами.
- Внутритканевое облучение. Источник ионизирующего излучения вводится непосредственно в ткань опухоли. Для этого используются интростаты, которые могут иметь вид игл, шариков, трубочек, заполненных источником излучения.
Кроме того, существует такой вид лечения, как радионуклидная терапия. В этом случае используются открытые источники излучения в виде растворов радионуклидов (радиофармацевтический препарат — РФП), которые при попадании в организм прицельно накапливаются в опухолевых очагах и уничтожают их. Чаще всего РФП вводится внутривенно. Наибольшее распространение получили следующие виды радионуклидной терапии:
- Терапия радиоактивным йодом. Используется для лечения ряда видов рака щитовидной железы, поскольку йод избирательно накапливается в тиреоидной ткани.
- Применение остеотропных РФП используется для лечения метастазов в костях или костных опухолей.
- Радиоиммунотерапия — радионуклиды присоединяют на моноклональные антитела, чтобы добиться прицельного воздействия на опухолевую ткань.
Дистанционная лучевая терапия
При дистанционной лучевой терапии источник излучения находится на расстоянии от тела пациента, при этом на пути его прохождения могут лежать здоровые ткани, которые в процессе проведения терапии также подвергаются облучению, что приводит к развитию осложнений разной степени выраженности. Чтобы их минимизировать, разрабатываются различные технологии, позволяющие сконцентрировать максимальную дозу ионизирующего излучения непосредственно на в мишени (опухоли). С данной целью используются:
- Короткофокусная рентгенотерапия. При облучении используется рентгеновское излучение малой и средней мощности, которое способно проникать в ткани на глубину до 12 мм. Метод назван так из-за того, что источник располагается на коротком расстоянии от облучаемой поверхности. Таким способом лечат неглубокие опухоли кожи, вульвы, конъюнктивы и век, ротовой полости.
- Гамма-терапия. Этот вид излучения имеет большую проникающую способность, поэтому может использоваться для лечения более глубоко расположенных опухолей, нежели рентген-терапия. Однако сохраняющаяся большая нагрузка на окружающие органы и ткани приводят к ограничению возможности использования данного метода в современной онкологии.
- Фотонная терапия. Именно этим видом излучения проводится лучевое лечение большинства онкологических пациентов в современном мире. Достаточно высокая проникающая способность в сочетании с высокотехнологичными способами подведения дозы (IMRT и VMAT), достаточно совершенные системы планирования позволяют очень эффективно использовать этот вид излучения для лечения пациентов с приемлемыми показателями токсичности.
- Применение корпускулярного излучения (электроны, протоны, нейтроны). Эти элементарные ядерные частицы получают на циклотронах или линейных ускорителях. Электронное излучение используют для лечения неглубоких опухолей. Большие надежды возлагаются на протонную терапию, с помощью которой можно максимально прицельно подводить высокие дозы излучения к глубоко расположенным опухолям при минимальном повреждении здоровых тканей за счет выделения радиационной дозы на определённом отрезке пробега частиц, однако пока эти виды излучения играют сравнительно небольшую роль в лечении онкологических заболевания из-за своей высокой стоимости и ряда не до конца решённых технологических аспектов реализации метода.
Этапы лучевой терапии
Весь процесс проведения лучевой терапии делят на три этапа:
- Предлучевая подготовка (КТ-симуляция), этап выбора объёмов облучения и критических структур, этап дозиметрического планирования, верификации плана лучевой терапии.
- Этап облучения.
- Постлучевой этап.
Этап планирования
Как правило, этап планирования занимает несколько дней. В это время проводятся дополнительные исследования, которые призваны дать возможность врачу более точно оценить границы опухоли, а также состояние окружающих ее тканей. Это может повлиять на выбор вида лучевой терапии, режима фракционирования, разовой и суммарной очаговых доз. Основой же данного этапа является выполнение так называемой КТ-симуляции, то есть компьютерной томографии необходимого объёма с определёнными параметрами и в определённом положении тела пациента. Во время КТ-симуляции на кожу пациента и/или его индивидуальные фиксирующие устройства наносятся специальные метки, призванные помочь правильно укладывать пациента в дальнейшем, а также облегчить задачу навигации по время проведения сеансов облучения.
Затем врач-радиотерапевт рисует объёмы облучения и критических структур (тех, на которые будет предписано ограничение дозы) на полученных срезах КТ с учётом данных других диагностических модальностей (МРТ, ПЭТ). Далее формируется задача для медицинского физика, включающая определение доз, которые должны быть подведены к мишени, мишеням или отдельным её частям, а также тех, которые не должны быть превышены в объёмах здоровых органов и тканей. Медицинский физик разрабатывает дозиметрический план в соответствии с заданными параметрами, при соблюдении которых и успешной верификации данного плана на фантоме, можно считать пациента готовым к лучевой терапии.
На этапе подготовки к лучевой терапии пациенту рекомендуется придерживаться нескольких правил:
- Отказаться от средств, раздражающих кожу.
- Если на коже в месте воздействия имеются повреждения или элементы сыпи, следует проконсультироваться с врачом.
- Если предполагается лучевая терапия в челюстно-лицевой области, требуется санация полости рта.
- Воздержаться от загара.
- Главное правило на любом этапе: обсудить все нюансы предстоящих подготовки и лечения с лечащим врачом-радиотерапевтом и строго придерживаться полученных рекомендаций!
Этап облучения
Проведение этапа облучения будет зависеть от выбранного метода лучевой терапии.
Проведение дистанционной лучевой терапии
Продолжительность курса дистанционной лучевой терапии зависит от выбранного режима фракционирования, а также цели лечения. Паллиативные курсы, как правило, короче неоадъювантных и адъювантных, а те, в свою очередь, менее продолжительны, чем радикальные. Однако подведение радикальной дозы возможно и за один-несколько сеансов в зависимости от клинической ситуации. В таком случае курс дистанционной лучевой терапии называется стереотаксической радиотерапией или радиохирургией. Варьирует и кратность сеансов в день и в неделю: чаще всего используются схемы с пятью сеансами в неделю, однако могут быть предложены и 2-3 сеанса в день (гиперфракционирование) и схемы с 1-4 и 6 сеансами в неделю.
Во время облучения пациент в подавляющем большинстве случаев располагается лежа на столе специальной установки. Крайне необходимо соблюдать полную неподвижность во время сеанса облучения. Для достижения этого могут использоваться специальные фиксирующие устройства и системы иммобилизации.
Перед тем как включить установку, медперсонал покидает помещение, и дальнейшее наблюдение осуществляется через мониторы или окно. Общение с пациентом осуществляется по громкой связи. Во время выполнения сеанса, части аппарата и стол с пациентом совершают движения по заданной траектории. Это может создавать шум и беспокойство у больного. Однако бояться этого не стоит, поскольку вся процедура контролируется.
Сам сеанс лучевой терапии может длиться как 5-10, так и 60-120 минут, чаще — 15-30 минут. Само воздействие ионизирующего излучения не вызывает никаких физических ощущений. Однако в случае ухудшения самочувствия пациента во время сеанса (выраженной боли, судороги, приступа тошноты, паники), следует позвать медицинский персонал заранее оговоренным способом; установку сразу отключат и окажут необходимую помощь.
Контактная лучевая терапия (брахитерапия)
Брахитерапия проводится в несколько этапов:
- Введение в облучаемую зону неактивных проводников — устройств, в которые затем имплантируют источник ионизирующего излучения. При внутриполостной лучевой терапии используются приспособления, называемые эндостатами. Их устанавливают непосредственно в полость облучаемого органа и рядом с ним. При внутритканевой лучевой терапии используются интростаты, которые устанавливаются непосредственно в ткань опухоли по заранее просчитанной схеме. Для контроля их установки, как правило, используются рентгенологические снимки.
- Перемещение источника излучения из хранилища в интро- и эндостаты, которые будут облучать опухолевую ткань. Время облучения и особенности поведения пациента будут зависеть от вида брахитерапии и используемого оборудования. Например, при внутритканевой терапии, после установки источника ионизирующего излучения пациент может покинуть клинику и прийти на повторную процедуру через рекомендуемый промежуток времени. Весь этот период в его организме будет находиться интростат с радионуклидами, которые будут облучать опухоль.
Проведение внутриполостной брахитерапии будет зависеть от используемых установок, которые бывают двух типов:
- Установки низкой мощности дозы. В этом случае один сеанс облучения длится около 2-х суток. Под наркозом имплантируются эндостаты. После контроля правильности их установки и введения радионуклидов, пациент переводится в специальное помещение, где должен будет находиться все время, пока длится процедура, соблюдая строгий постельный режим. Разрешается только немного поворачиваться на бок. Вставать категорически запрещено.
- Установки высокой мощности дозы. Время облучения составляет несколько минут. Для установки эндостатов наркоза не требуется. Но во время процедуры все равно необходимо лежать абсолютно неподвижно. Внутриполостная лучевая терапия установкой высокой мощности проводится несколькими сеансами с интервалами от одного дня до одной недели.
Радионуклидная терапия
При радионуклидной терапии пациент принимает радиофармпрепараты внутрь в виде жидкого раствора, капсул или инъекций. После этого он помещается в специальную палату, имеющую изолированную канализацию и вентиляцию. По истечении определенного срока, когда мощность дозы снизится до приемлемого уровня, проводится радиологический контроль, пациент принимает душ и переодевается в чистую одежду. Для контроля результатов лечения проводится сцинтиграфия, после чего можно покинуть клинику.
Как вести себя во время лучевой терапии
Лучевая терапия является серьезным стрессом для организма. У многих пациентов в этот период ухудшается самочувствие. Чтобы его минимизировать рекомендуется придерживаться следующих правил:
- Больше отдыхать. Минимизируйте физическую и интеллектуальную нагрузку. Ложитесь спать, когда почувствуете в этом необходимость, даже если она возникла в течение дня.
- Постарайтесь сбалансировано и полноценно питаться.
- Откажитесь на время проведения терапии от вредных привычек.
- Избегайте плотной обтягивающей одежды, которая бы могла травмировать кожу.
- Следите за состоянием кожи в месте облучения. Не трите и не расчесывайте ее, используйте средства гигиены, которые вам порекомендует врач.
- Защищайте кожу от воздействия солнечных лучей — используйте одежду и головные уборы с широкими полями.

Побочные эффекты лучевой терапии
Лучевая терапия, как и другие методы противоопухолевого лечения, вызывает ряд осложнений. Они могут быть общими или местными, острыми или хроническими.
Острые (ранние) побочные эффекты развиваются во время проведения радиотерапии и в ближайшие недели после неё, а поздние (хронические) лучевые повреждения — через несколько месяцев и даже лет после ее окончания.
Общие реакции
Угнетенное эмоциональное состояние
Подавляющее большинство пациентов, проходящих лечение по поводу злокачественного новообразования, испытывают тревожность, страх, эмоциональное напряжение, тоску и даже депрессию. По мере улучшения общего состояния, эти симптомы стихают. Чтобы облегчить их, рекомендуется чаще общаться с близкими людьми, принимать участие в жизни окружающих. При необходимости рекомендуется обратиться к психологу.
Чувство усталости
Чувство усталости начинает нарастать через 2-3 недели от начала терапии. На это время рекомендуется оптимизировать свой режим дня, чтобы не подвергаться ненужным нагрузкам. В то же время нельзя полностью отстраняться от дел, чтобы не впасть в депрессию.
Изменение крови
При необходимости облучения больших зон, под воздействие радиации попадает костный мозг. Это в свою очередь приводит к снижению уровня форменных элементов крови и развитию анемии, повышению риска кровотечения и развития инфекций. Если изменения выражены сильно, может потребоваться перерыв в облучении. В ряде случаев могут назначать препараты, стимулирующие гемопоэз (кроветворение).
Снижение аппетита
Обычно лучевая терапия не приводит к развитию тошноты или рвоты, но снижение аппетита наблюдается довольно часто. Вместе с тем, для скорейшего выздоровления требуется полноценное высококалорийное питание с высоким содержанием белка.
Локальные осложнения
Побочные реакции со стороны кожи
Вероятность развития кожных реакций и их интенсивность зависят от индивидуальных особенностей пациента. В большинстве случаев через 2-3 недели в области воздействия возникает покраснение. После окончания лечения оно сменяется пигментированием, напоминающим загар. Чтобы предотвратить чрезмерные реакции, могут назначаться специальные кремы и мази, которые наносятся после окончания сеанса. Перед началом следующего их необходимо смыть теплой водой. Если реакция выражена сильно, делают перерыв в лечении.
Реакции со стороны полости рта и горла
Если облучают область головы и шеи, могут развиться лучевой стоматит, который сопровождается болью, сухостью во рту, воспалением слизистых, а также ксеростомия вследствие нарушения функции слюнных желез. В норме эти реакции проходят самостоятельно в течение месяца после окончания лучевой терапии. Ксеростомия может беспокоить пациента в течение года и более.
Осложнения со стороны молочной железы
При прохождении лучевой терапии по поводу рака молочной железы могут возникать следующие реакции и осложнения:
- Покраснение кожи груди.
- Отек груди.
- Боль.
- Изменение размера и формы железы из-за фиброза (в некоторых случаях эти изменения остаются на всю жизнь).
- Уменьшение объема движения в плечевом суставе.
- Отек руки на стороне поражения (лимфедема).
Побочное действие на органы грудной клетки
- Воспаление слизистой пищевода, которое приводит к нарушению глотания.
- Кашель.
- Образование мокроты.
- Одышка.
Последние симптомы могут свидетельствовать о развитии лучевого пневмонита, поэтому при их возникновении следует немедленно обратиться к вашему врачу.
Побочные реакции со стороны прямой кишки/петель кишечника
- Расстройство стула — диарея или наоборот, запоры.
- Боли.
- Кровянистые выделения из заднего прохода.
Побочные действия со стороны мочевого пузыря
- Учащенное болезненное мочеиспускание.
- Наличие примеси крови в моче иногда может быть настолько выраженным, что моча приобретает кроваво-красный цвет.
- Наличие патологических примесей в моче — кристаллы, хлопья, гнойное отделяемое, слизь.
- Уменьшение емкости мочевого пузыря.
- Недержание мочи.
- Развитие везиковагинальных или везикоректальных свищей.
Побочные эффекты при облучении опухолей забрюшинного пространства, печени, поджелудочной железы
- Тошнота и рвота.
- Ознобы после сеансов.
- Боли в эпигастрии.
Химиолучевая терапия
Лучевая терапия довольно редко проводится в качестве самостоятельного лечения. Чаще всего она сочетается с каким-либо другим видом лечения: хирургическим, а чаще всего — с лекарственным. Это может быть как вариант одновременной химиолучевой терапии, так и последовательной, а также варианты сочетания лучевой терапии с иммунотерапией, таргетной и гормональной терапии. Такие виды лечения могут иметь ощутимо более высокую противоопухолевую эффективность, однако необходимо тщательно оценить риски совместных побочных эффектов, поэтому принятие решения о любом объёме лечения с онкологической патологией должен принимать мультидисциплинарный онкологический консилиум.
Лучевой проктит — это воспаление прямой кишки, которое возникает на фоне лучевой терапии опухолей органов малого таза. Сопровождается данное состояние болью в прямой кишке и в области заднего прохода, болезненными позывами на дефекацию, диареей, выделением из прямой кишки слизи и крови.
Вероятность лучевого повреждения стенки кишки и развития проктита напрямую связано с суммарной очаговой дозой, полученной при ЛТ. Оптимальная переносимая суммарная очаговая доза в области малого таза составляет 40-50Гр. В этом случае вероятность развития осложнений составляет около 3-5%. При повышении СОД до 65 Гр, лучевой проктит развивается уже у половины пациентов.
Причины воспаления кишки после лучевой терапии
Основе лучевых поражений кишки лежат следующие механизмы:
- Повреждение кишечного эпителия, которое развивается под действием ионизирующего излучения. Это приводит к его очаговому некрозу, десквамации (отшелушиванию) и атрофии.
- Развитие неспецифического воспаления слизистой оболочки и подслизистой основы. Ткани инфильтрируются нейтрофилами, наблюдается гиперемия, отечность, кровоточивость.
- Из-за трофических нарушений (повреждаются артериолы) ухудшается кровоснабжение пораженных участков слизистой кишки, что еще больше усугубляет ишемию и некроз. В результате прогрессируют атрофические изменения с развитием фиброза подслизистого слоя.
- На этом фоне начинает присоединяться патогенная флора, которая вызывает инфекционные осложнения, вплоть до сепсиса.
Конечным результатом длительных трофических нарушений стенки кишки и некрозов становится формирование стриктур (сужение просвета), образование свищевых ходов, формирование телеангиоэктазий и развитие кровотечения из них.

Фазы лучевых повреждений
В зависимости от сроков появления, выделяют ранние и поздние лучевые повреждения. Ранние дают о себе знать непосредственно во время проведения лучевой терапии, либо в течение 100 дней с момента ее окончания. Этот период (100 дней, или три месяца) является крайним сроком восстановления эпителия, находящимся в сублетальном повреждении. На этом этапе этиологическим фактором выступает повреждение эпителия кишки с развитием воспалительных реакций. Если доза облучения невелика, эпителий довольно быстро восстанавливается, и, соответственно, слизистая оболочка приходит в норму. В среднем на это уходит около 2-4 недель с момента последнего сеанса облучения.
Поздние лучевые поражения развиваются через 100 дней после окончания ЛТ. В этот период на первое место выходят сосудистые нарушения из-за повреждения эндотелия. Его клетки некротизируются, и чтобы их восстановить, начинают активно пролиферировать оставшиеся эндотелиоциты. Это приводит к облитерации просвета сосудов, развитию тромбозов, ишемии и трофических нарушений. В результате развиваются лучевые васкулиты с кровотечениями, атрофические процессы, фиброзные изменения, разрастание рубцовой ткани.
Классификация лучевого проктита
В зависимости от степени тяжести, выделяют следующие виды лучевых проктитов:
- Катаральный проктит. Во время осмотра обнаруживается гиперемированная рыхлая отечная стенка кишки. Может быть повышенное выделение слизи. Эта форма проктита считается легкой.
- Эрозивно-десквамативный проктит. Эта форма проявляется очагами деструкции эпителия с образованием эрозии — дефекта ткани в пределах эпителиального слоя.
- Язвенный проктит — деструкция распространяется на более глубокие слои ткани и вовлекает в процесс слизистую оболочку с подслизистой основой.
- Свищевой проктит. Образуется сквозная перфорация стенки кишки с выходом в полость малого таза или с вовлечением в процесс рядом расположенных органов, например, мочевого пузыря или влагалища.
Существует классификация лучевого проктита, основанная на ректоскопической картине:
- Имеется локальное покраснение и рыхлость слизистой оболочки кишки, отмечаются телеангиоэктазии расширенные кровеносные сосуды).
- На фоне гиперемии и отечной слизистой кишки обнаруживаются язвы, покрытые серым струпом.
- На фоне воспалительных поражений обнаруживаются стриктуры кишечной стенки.
- На фоне язвенного поражения обнаруживаются стриктуры и свищи или кишечная перфорация.
Симптомы лучевого проктита
Симптомы острого лучевого проктита развиваются в течение 1-2 недель после начала облучения. Это могут быть:
- Диарея.
- Боли в области прямой кишки или внизу живота.
- Болезненные позывы на дефекацию.
- Выделение слизи из анального канала или ее примесь в стуле.
- Анальная инконтиненция.
- Кровотечение. У ряда пациентов кровотечения бывают обильными и приводят к острой геморрагической анемии, которая требует гемотрансфузии.
Если симптомы острого лучевого проктита отсутствуют, это не значит, что не возникнут отдаленные последствия. Частота поздних постлучевых проктитов составляет около 10% от общего числа случаев. При этом присутствует латентный период, который длится несколько месяцев или даже лет. Клиническая картина характеризуется следующими симптомами:
- Боли в правой подвздошной области или в прямой кишке.
- Частый стул, тенезмы.
- Наличие примесей крови в кале.
- При образовании стриктур могут отмечаться запоры и явления частичной кишечной непроходимости.
- При форсировании свищей, отмечаются патологические влагалищные выделения мутного цвета, пневматурия (примеси воздуха в моче), жидкий стул с примесями непереваренной пищи.
В зависимости от тяжести течения, выделяют несколько степеней заболевания:
1 степень — проктит с легким течением. Сопровождается слабо выраженной диареей, менее 5 раз в сутки, может присутствовать выделение небольшого количества слизи и крови.
2 степень — проктит с управляемым течением. Диарея умеренно выраженная, более 5 раз в сутки. Выделяется большое количество слизи, имеются кровотечения.
3 степень — проктит с тяжелым течением. Имеются стриктуры и кровотечения из прямой кишки, требующие хирургического вмешательства.
4 степень это жизнеугрожающее течение, которое требует немедленного вмешательства. Оно сопровождается кишечной непроходимостью, свищами, обильными кровотечениями.
Как диагностируют лучевой проктит
Диагностика заболеваний не представляет труда. Ключевым моментом здесь является наличие в анамнезе лучевой терапии и ее влияние на органы малого таза, учащение стула, и наличие в нем патологических примесей.
При затяжном течении рекомендуется проводить осмотр прямой кишки с помощью ректоскопа или эндоскопа. Это позволит обнаружить множественные эрозии, рубцовую деформацию, атрофические изменения и телеангиоэктазии и решить вопрос о необходимости эндокопического или хирургического лечения.
Как лечат лучевой проктит
При развитии симптомов лучевого проктита во время лучевой терапии, требуется пересмотр схемы облучения. При легком поражении достаточно увеличить интервалы между сеансами. В более тяжелых случаях встает вопрос об уменьшении суммарной очаговой дозы или даже отмене лучевой терапии. Помимо этого, требуется лечение, которое включает в себя несколько направлений:
- Диетическое питание. Важную часть лечения постлучевого проктита занимает диетическое питание. Пища должна содержать повышенное количество белка, достаточное количество макро и микронутриентов. Также она должна быть химически и физически щадящей, т. е. следует отказаться от острых, маринованных, консервированных продуктов. Кроме того, следует избегать грубой растительной клетчатки, чтобы она не травмировала и без того поврежденную стенку кишки.
- Консервативные методы — это медикаментозная терапия, лечебные клизмы, свечи и др. В рамках самостоятельного лечения используется только при легкой и умеренной патологии, в остальных случаях применяется в рамках комплексного лечения совместно с другими методами лечения.
- Эндоскопические методы — радиочастотная аблация, коагуляция аргоновой плазмой и др. В настоящее время эти методы являются золотым стандартом лечения хронических форм заболевания и в основном применяются для устранения кровотечений.
- Хирургические методы — удаление прямой кишки с выведением стомы или наложением колоанального анастомоза. Применяются в тяжелых случаях, когда имеется угроза жизни пациента. Хирургические операции применяются для устранения стриктур, свищей и перфораций стенки кишки.
Медикаментозная терапия лучевого проктита
Для лекарственной терапии используются следующие группы препаратов:
- Глюкокортикостероиды — это основная группа препаратов, применяемых при среднетяжелом и тяжелом течении проктита. ГКС оказывают мощное противовоспалительное действие.
- Анальгетики. Используются разные группы препаратов, в том числе наркотические.
- 5-аминосалициловая кислота (месалазин) — оказывает противовоспалительное и протективное действие, тем самым защищая пораженную слизистую и стимулируя ее восстановление.
- Антидиарейные препараты. Применяются обволакивающие и вяжущие средства, спазмолитики.
- Антибактериальные препараты. Их назначают для лечения или профилактики бактериальных осложнений проктитов.
Учитывая то, что прямая кишка является терминальным отделом пищеварительного тракта, многие препараты местного действия оказываются недостаточно эффективными при применении в формах, предназначенных для перорального приема. Поэтому отдается предпочтение формам для локального применения — свечи, клизмы, порошки и т. д. Они действуют непосредственно на стенку кишки и оказывают эффект в кратчайшие сроки.
Хирургическое лечение лучевого проктита и лучевых поражений прямой кишки
Хирургическое лечение направлено на устранение конкретных симптомов или осложнений постлучевого проктита. Это могут быть непрекращающиеся кровотечения, свищи и перфорации кишечной стенки, стрикруты. Очень редко хирургия применяется для устранения неконтролируемой боли.
Перед планированием операции важно учитывать, что радиационные повреждения снижают регенеративные возможности ткани, поэтому есть высокие риски развития осложнений, в том числе кровотечений, плохого заживления раны, присоединения инфекций и ее генерализация, а также долгосрочные отрицательные эффекты типа грубого рубцевания или несостоятельности анального сфинктера.
Таким образом, классические хирургические вмешательства в остром периоде являются рискованными, они не позволяют полностью контролировать кровотечение и могут привести к тяжелым, жизнеугрожающим осложнениям. Поэтому их в основном применяют для устранения отдаленных последствий лучевых проктитов.

Эндоскопические методы лечения
Более безопасными являются эндоскопические методы лечения. В их основе лежит деструкция пораженного отдела слизистой кишки с последующим ее некрозом и замещением здоровым эпителием. С этой целью используется в частности используется радиочастотная аблация. В основе метода лежит локальное контролируемое нагревание тканей с целью получения термального ожога. Источником энергии здесь выступают волны радиочастотного диапазона.
Во время процедуры в прямую кишку пациента вводят специальный катетер, который будет излучать волны и нагревать ткани. Стандартная глубина некроза составляет несколько десятых миллиметра, поэтому для обработки одного участка слизистой необходимо 1-3 импульса. Интенсивность энергии регулируется в автоматическом режиме с учетом текущей температуры обрабатываемой ткани. Это позволяет избежать «перегрева» и глубокого ожога.
Преимуществом эндоскопического лечения является его бескровность, высокая степень контроля при выполнении вмешательства, быстрый результат. Наибольшую эффективность оно оказывает при кровотечениях. Уже с помощью одной процедуры можно коагулировать все патологические кровеносные сосуды и остановить даже обильное кровотечение. Как правило, для максимального результата процедуру проводят 2-3 раза с интервалом в несколько месяцев.
Прогноз и профилактика лучевого проктита
Профилактика лучевого проктита сводится к усовершенствованию технологий проведения лучевой терапии:
- Применение технологий, позволяющих более детально планировать поля облучения, без вовлечения в процесс «незаинтересованных органов».
- Снижение суммарной дозы облучения.
- Замена дистанционной лучевой терапии на внутритканевую или брахитерапию.
- Применение во время лечения радиопротекторов.
В подавляющем большинстве случаев при лучевом проктите прогноз благоприятный — при адекватном лечении заболевание проходит и не сказывается на дальнейшей жизни человека. У 10% пациентов могут развиться тяжелые осложнения в виде свищей, перфораций, некупируемого болевого синдрома, требующие хирургического вмешательства. В ряде случаев необходима экстирпация прямой кишки с наложением анастомоза или выведением колостомы. Последний вариант приводит к инвалидности. Но даже в этом случае есть возможность в отдаленном периоде провести реконструктивную операцию по восстановлению непрерывности кишечника.
Необходимо учитывать, что лучевой проктит может стать препятствием для прохождения полного курса лучевой терапии. В этом случае необходим подбор других методов противоопухолевого лечения.
Лучевой проктит - это воспаление прямой кишки, развивающееся на фоне радиационной терапии рака тазовых органов. Местные симптомы включают болезненность в проекции прямой кишки, слизистые, гнойные или кровянистые выделения из анального отверстия. Кроме локальных проявлений лучевой проктит может сопровождаться общими симптомами: повышением температуры тела и выраженной слабостью. Для диагностики заболевания используется общий анализ крови, ректоскопия и исследование мазка со стенки прямой кишки. Лечение заключается в проведении местных противовоспалительных процедур, назначении антибактериальной терапии, антигистаминных препаратов и витаминотерапии.
МКБ-10
Общие сведения
Лучевой проктит представляет собой неспецифический воспалительный процесс, развивающийся в слизистой оболочке прямой кишки. Основной причиной заболевания является воздействие ионизирующей радиации при проведении лучевой терапии по поводу рака органов малого таза. Лучевой проктит является наиболее распространенной формой радиационного поражения кишечника, встречающейся в клинической проктологии. Поскольку около 60% пациентов с онкопатологией органов малого таза получают лучевую терапию, распространенность поражения прямой кишки у данной группы больных очень высока: лучевой проктит диагностируют примерно у 12% лиц, получающих радиационное лечение. Основная проблема, с которой приходится сталкиваться проктологам, наблюдающим таких пациентов, это частое развитие постлучевых стриктур прямой кишки, требующих оперативного вмешательства.

Причины
Лучевой проктит всегда является осложнением радиационной терапии онкопатологии органов малого таза. Чаще всего данное состояние развивается после проведения контактной гамма-терапии рака шейки и рака тела матки с использованием изотопов тория, реже – при применении чистого радия. Также лучевой проктит может быть следствием рентгенотерапии и дистанционной гамма-терапии рака органов малого таза. Радиационное повреждение прямой кишки возникает в том случае, когда суммарная очаговая доза излучения превышает 50 Гр (это толерантная доза, при которой частота поздних осложнений составляет около 5%). Вероятность патологии напрямую коррелирует с дозой облучения: риск развития лучевого проктита возрастает до 50% уже при показателе 65 Гр.
Воздействие радиационного излучения приводит к нарушению процессов пролиферации и созревания эпителия прямой кишки, к десквамации и атрофии клеток. Развивается неспецифическое воспаление слизистой и подслизистого слоя, в процесс может быть вовлечен и мышечный слой. Спустя несколько месяцев после лучевой терапии формируется воспалительный процесс в артериолах прямой кишки, приводящий к хроническому нарушению кровообращения в данной области, трофическим изменениям и рубцовому стенозированию. Недостаточная микроциркуляция часто становится причиной некрозов, язв, которые могут осложниться кровотечением, перфорацией, формированием свищей прямой кишки.
Классификация
В зависимости от сроков развития лучевой проктит классифицируют на ранний (возникает в первые 3 месяца после радиотерапии) и поздний (возникает позднее указанного срока). По характеру морфологических изменений, происходящих в прямой кишке, различают катаральный, эрозивно-десквамативный, некротический и инфильтративно-язвенный процесс. Отдельно выделяются такие осложнения лучевого проктита, как рубцовый стеноз, ректовезикальные и ректовагинальные свищи.
Симптомы лучевого проктита
Основным проявлением ранней формы заболевания являются болезненные позывы на дефекацию. Боль носит приступообразный характер и усиливается после опорожнения кишечника. Также пациентов может беспокоить зуд и дискомфорт в области заднего прохода. Из прямой кишки зачастую выделяется слизь, что является признаком воспаления слизистой оболочки кишечника. Иногда имеют место кровянистые выделения, указывающие на тяжелое течение заболевания. Помимо местных симптомов, лучевой проктит сопровождается общими клиническими проявлениями, такими как слабость и повышение температуры тела. Все симптомы ранней формы патологии обычно регрессируют спустя несколько дней после окончания противоопухолевой терапии. Однако через определенное время лучевой проктит может рецидивировать, а клиническая симптоматика часто возвращается в прежнем объеме.
Поздние лучевые поражения кишечника развиваются примерно в 10% случаев. При этом латентный период (промежуток времени между облучением и возникновением симптоматики) может длиться от нескольких недель до 5-10 лет. Характерны постоянные боли в области прямой кишки, частый стул небольшими порциями, а также развитие стеноза с явлениями частичной непроходимости. Возможно малосимптомное течение поздней формы лучевого проктита. В таком случае заболевание проявляется наличием слизи в кале и периодическим болевым синдромом в левой подвздошной области и в проекции прямой кишки.
На фоне лучевого проктита могут развиваться различные осложнения: кишечное кровотечение, язвы и эрозии, стеноз прямой кишки. Именно стриктура кишечника считается наиболее грозным и неблагоприятным осложнением с точки зрения прогноза. Если на фоне лучевой терапии рака органов малого таза у больного появляются слизистые или кровянистые выделения из анального отверстия, сопровождающиеся тенезмами и болью в области прямой кишки, это позволяет заподозрить лучевой проктит.
Диагностика
При появлении признаков лучевого проктита на фоне проведения радиотерапии пациента сразу же направляют к врачу-проктологу. Для диагностики данного заболевания используются клинические, лабораторные и инструментальные методы. Обследование начинается с объективного осмотра и выяснения жалоб. При лучевом проктите всегда прослеживается связь с проведением лучевой терапии. Из лабораторных методов применяется общий анализ крови, в котором, как правило, отмечаются воспалительные изменения, такие как лейкоцитоз, ускорение СОЭ и палочкоядерный сдвиг влево. Лабораторные диагностические методики позволяют определить степень тяжести воспаления, но они не могут применяться непосредственно для постановки диагноза лучевого проктита.
Ключевую роль в диагностике заболевания играет эндоскопия. Наиболее простым, доступным и информативным методом считается ректороманоскопия. При проведении этого исследования врач обнаруживает покраснение, отек слизистой и гиперпродукцию слизи в прямой кишке. Кроме того, методика позволяет выявить изменения, характерные для таких осложнений, как кровотечение, абсцедирование, образование язв. Язвы, как правило, локализуются на передней стенке прямой кишки; в ряде случае они могут приводить к формированию свищей. При ректоскопии обязательно проводится биопсия слизистой оболочки прямой кишки. Она дает возможность уточнить степень тяжести воспалительных и атрофических изменений слизистой. С целью определения наличия инфекционного агента проводится бактериологическое исследование мазка из прямой кишки.
Вследствие того, что симптомы лучевого проктита имеют много общего с неспецифическим язвенным колитом, основная дифференциальная диагностика должна проводиться между этими двумя заболеваниями. В пользу проктита свидетельствует факт проведения лучевой терапии в анамнезе. Кроме того, лучевой проктит отличает наличие язв на передней стенке и в средней трети прямой кишки. В то же время, при этом заболевании крайне редко поражается задняя стенка и нижняя часть прямой кишки. При неспецифическом язвенном колите воспалительные изменения являются диффузными и поражают весь ректальный отдел кишечника. Для окончательной дифференциальной диагностики между этими двумя заболеваниями используется биопсия.
Лечение лучевого проктита
При лечении лучевого проктита важно уменьшить негативное влияние ионизирующего излучения, которое приводит к запуску лучевых реакций. Больным назначают витамин С, витамины группы В, а также антигистаминные препараты, такие как хифенадин, клемастин, лоратадин и другие. При наличии выраженного воспаления и идентификации инфекционного возбудителя проводят антибактериальную и противовоспалительную терапию (в том числе, с использованием сульфаниламидных средств, глюкокортикоидов и облепихового масла).
Местная терапия является важным компонентом комплексного лечения лучевого проктита. Данный вид помощи в первую очередь предусматривает очищение кишечника и ликвидацию локальных воспалительных процессов: в период обострения пациентам показаны клизмы с раствором колларгола или отваром ромашки. Эффективными считаются масляные микроклизмы на основе рыбьего жира или винилина. Эти процедуры проводят после использования слабительных средств или очистительных клизм. Хороший эффект при лечении лучевого проктита дает теплый душ в области прямой кишки или сидячие ванны с использованием перманганата калия. Также целесообразно местное лечение глюкокортикостероидами, ректальными суппозиториями с месалазином и анестетиками.
В комплексной терапии лучевого проктита важную роль играет правильное питание. Диета при данном заболевании предусматривает полное исключение острой, соленой и кислой пищи, а также алкоголя, ограничение растительной пищи и сладких продуктов. Пищевой рацион при лучевом проктите должен содержать нежирное мясо, супы на бульонах без жира и кисломолочные продукты. Если симптомы заболевания регрессируют на фоне эффективного лечения, то диета может быть расширена. При развитии осложнений, таких как формирование свищей и сужений кишечника, используются хирургические методы лечения, в том числе реконструктивные вмешательства на прямой кишке.
Прогноз и профилактика
При лучевом проктите прогноз в основном благоприятный. Тяжелое течение патологии отмечается при сочетании поражения нескольких отделов кишечника, развитии осложнений в виде свищей, кровотечений. Своевременное комплексное лечение позволяет уменьшить вероятность возникновения обострений. Профилактика лучевого проктита заключается в использовании современных методик и протоколов лечения онкозаболеваний органов малого таза, которые оказывают меньший негативный эффект на здоровые ткани.
1. Лучевые ректиты при комплексном лечении рака органов малого таза (обзор литературы) / Клименко К.А., Цаллагова З.С. // Вестник Российского научного центра рентгенорадиологии Минздрава России - 2014-
2. Лучевые повреждения прямой кишки и мочевого пузыря у больных раком шейки матки / Жариков Г.М., Винокуров В.Л., Заикин Г.В. // Мир медицины - 2000 - №7-8
3. Радиационные (лучевые) поражения кишечника / Бурковская В.А. // Гастроэнтерология Санкт-Петербурга - 2013 - №3-4
Читайте также:

