Как лечить кожные заболевания уколами
Обновлено: 03.05.2024
Пиодермии (гнойничковые болезни кожи) являются наиболее распространенными кожными заболеваниями во всех возрастных группах. По-видимому, это обусловлено тем, что возбудители пиодермий – стафилококки и стрептококки – часто обнаруживаются в окружающей человека среде (в воздухе, пыли помещений, а также на одежде, коже человека).
Бактериальные инфекции кожи являются междисциплинарной проблемой, они встречаются в практике хирургов, терапевтов, педиатров, гинекологов.
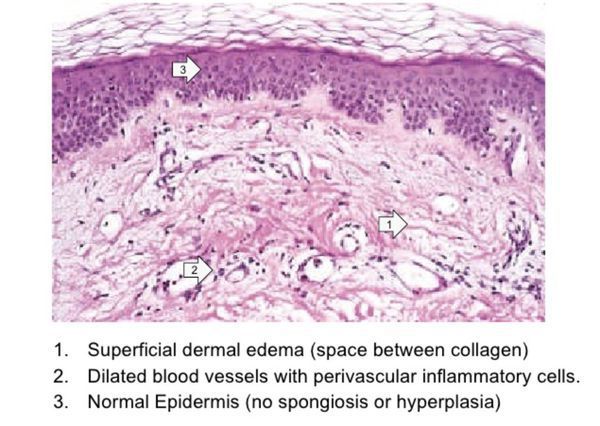
Пиодермии (от греч. pyon – гной, derma – кожа) составляют обширную группу различных по клиническим формам, течению и прогнозу дерматозов, в основе которых лежит гнойное воспаление кожи, ее придатков и подкожной жировой клетчатки (рис. 1).
Заболевания кожи, связанные с деятельностью бактерий, как патогенных, так и условно-патогенных, характеризуются нозологическим многообразием. Инфекционный процесс при пиодермиях порой не ограничивается лишь локальным эффектом – развитием воспаления, но может нанести серьезный урон общему состоянию организма (например, синдромы стафилококкового и стрептококкового токсического шока), приводит к возникновению заболеваний, протекающих без воспалительных явлений (точечный кератолизис) [1, 2].
Возбудителями пиодермии являются в основном стафилококки и стрептококки, относящиеся к грамположительной микробной флоре. Возникновение нагноения кожи под влиянием стафилококков и стрептококков объясняется воздействием на нее различных продуктов метаболизма, выделяемых пиогенными кокками в процессе их жизнедеятельности (экзотоксины, энтеротоксины, ферменты и др.).
В российской дерматологии общепризнанной является классификация пиодермий, предложенная Jadasson (1949) в модификации А.А. Каламкаряна (1954) и С.Т. Павлова (1957), согласно которой пиодермии в зависимости от возбудителя традиционно разделяют по этиологическому принципу – стафилодермии и стрептодермии, а также смешанные – стрептостафилодермии. По протеканию заболевания выделяют острые и хронические формы; по глубине поражения – поверхностные и глубокие, а по механизму возникновения – первичные и вторичные.
Клинические проявления гнойничковых болезней кожи разнообразны. Наиболее распространенными являются фолликулиты, вульгарный сикоз, фурункул, карбункул, гидраденит, импетиго, хроническая язвенная пиодермия. У грудных детей может развиться эпидемическая пузырчатка новорожденных и др.
Пиодермия часто осложняет зудящие кожные заболевания (так называемая вторичная пиодермия), особенно чесотку, экзему, нейродермит, атопический дерматит. Нередко вторичная пиодермия наблюдается при пузырчатке, опоясывающем герпесе, микозах, язвенно-некротическом ангиите.
Лечение гнойничковых заболеваний кожи остается одним из актуальных вопросов терапии дерматозов [3].
Лечение пиодермий всегда должно быть комплексным и включать особый режим поведения и ухода за кожей, диету, местные и системные препараты, а также физиотерапевтические процедуры.
В лечении гнойничковых заболеваний кожи необходимо соблюдать основной принцип, а именно – проводить этиотропное лечение, т. е. воздействующее на возбудителя, и патогенетическое – для устранения способствующих пиодермии факторов и коррекции сопутствующей патологии.
Режим больного пиодермией в первую очередь предполагает рациональный уход за кожей, как в очаге поражения, так и вне его.
При локализованных формах заболевания не рекомендуется мыть кожу лишь в очаге поражения и вблизи него, а при диссеминированном процессе мытье запрещается вообще.
Волосы в области расположения пиодермических элементов необходимо состричь (не брить!).
Непораженную кожу обрабатывают, особенно тщательно в окружности очага поражения, дезинфицирующими растворами (1–2% спиртовой раствор салициловой кислоты, 0,1% водный раствор перманганата калия и др.).
С целью предотвращения распространения инфекции ногти должны быть коротко острижены, дважды в день их обрабатывают 2% спиртовым раствором йода.
При длительно текущих процессах, а также при множественных высыпаниях особое внимание следует уделить диете: питание должно быть регулярным, полноценным, богатым витаминами; резко ограничивают количество соли и углеводов; полностью исключается алкоголь.
Для местного лечения поверхностных форм пиодермий используют спиртовые растворы (салициловой кислоты, камфоры), анилиновые красители (фукорцин, 1% бриллиантовый зеленый, 0,1% калия перманганат), топические антисептические и антимикробные препараты. При необходимости, принимая асептические меры, вскрывают покрышку фликтен и пустул с последующим промыванием 3% раствором перекиси водорода (водорода пероксид) и смазыванием дезинфицирующими растворами: нитрофуралом 0,1%, йода раствором спиртовым 5%. В качестве антисептических средств широко применяют хлоргексидин (0,5% спиртовой или 1% водный раствор хлоргексидина биглюконата), диоксидин, эвкалипта листьев экстракт, микроцид, повидон-йод и др.; для наружного лечения также эффективны аэрозоли, т. к. они равномерно наносятся на поверхность, быстро проникают в кожу: триамцинолон, гидрокортизон + окситетрациклин, лифузоль, декспантенол. На распространенные множественные очаги наносят мази, содержащие антибиотики и сульфаниламиды: 2% мазь, крем фуцидина, 2% мазь мупироцина, сульфадиазин, бацитрацин + неомицин, сульфатиазол серебра, левомеколь, гелиомициновая мазь 4%, линкомициновая мазь 2%, гентамициновая мазь 0,1%. Курс лечения составляет 7–14 дней.
Топические комбинированные глюкокортикостероидные препараты с противовоспалительным и антибактериальным действием назначают при вторичной пиодермии основных дерматозов (атопического дерматита, чесотки, экземы и др.): фуцикорт, фузидовая кислота, гидрокортизон + окситетрациклин, лоринден С, целестодерм с гарамицином, травокорт и др. Курс лечения 7–14 дней.
При лечении поверхностных форм пиодермий (остиофолликулиты, фолликулиты, импетиго, эктима) хороший терапевтический эффект был получен при использовании сульфатиазола серебра – 2% крема аргосульфан [4].
После первичной обработки глубоких ограниченных очагов стафилококковой инфекции показаны также рассасывающие средства, ферменты, мази, ускоряющие репаративные процессы в коже, обеспечивающие глубокое проникновение лекарственного препарата и ограничивающие распространение гноя: ихтаммол, 0,25% раствор трипсина, химотрипсин, левосин, пиолизин, актовегин, солкосерил, цинка гиалуронат.
Для лечения язвенных поражений при пиодермии применяют эпителизирующие мази и повязки, для очищения от некротических масс – ируксол, трипсин, химотрипсин. В последнее время впечатляющий эффект при лечении язвенных дефектов при пиодермии получен от применения 2% крема аргосульфан. В качестве действующего начала содержит серебряную соль сульфатиазола, которая обладает мощным антибактериальным эффектом на грамотрицательные и грамположительные микроорганизмы (стафилококки, стрептококки, вульгарный протей, кишечная палочка, клостридии и др). и более чем на порядок превосходит аналогичное действие одних сульфаниламидов. Ионы серебра, содержащиеся в креме, ослабляют сенсибилизирующие свойства сульфаниламидов, а благодаря связыванию с РНК микробных клеток они обладают и бактериостатическим действием. Серебряная соль сульфатиазола обладает слабой растворимостью и всасываемостью с раневой поверхности, что позволяет длительно поддерживать более-менее постоянную концентрацию препарата в очаге воспаления. Сульфатиазол, как составная часть крема, подавляет размножение микроорганизмов. Гидрофильная основа крема, имеющая оптимальное значение рН и содержащая большое количество воды, обеспечивает местное анальгезирующее действие и увлажнение раны, способствуя репарации тканей. Препарат наносится на очаги поражения 2–3 р./сут.
Мы применяли аргосульфан при лечении гангренозной пиодермии. Его применение в составе комплексной терапии позволило добиться у всех больных полного или почти полного клинического излечения. Это выражалось в уменьшении или исчезновении болевых ощущений при перевязках и вне их, в очищении язвенного дефекта от некротических тканей и появлении зрелых грануляций и краевой эпителизации в области язв, а также в отсутствии или резком снижении роста микрофлоры. Использование аргосульфана у всех пациентов приводило к быстрому рубцеванию язв (в среднем в течение 20–22 дней в зависимости от глубины и обширности дефекта), при этом в процессе лечения больные не отмечали никаких побочных эффектов от проводимой местной терапии.
В целях санации всей кожи рекомендуют общее ультрафиолетовое облучение или обтирание визуально здоровой кожи дезинфицирующими средствами. При отсутствии эффекта от наружного лечения глубоких поражений на лице, шее (фурункул, карбункул), при пиодермиях, осложненных лимфангитом, лимфаденитом, показано этиотропное лечение антибиотиками широкого спектра действия (парентерально или внутрь).
Системные антибиотики при пиодермиях применяют при длительном хроническом течении процесса, большой его распространенности, наличии общих явлений (лихорадка, головная боль, недомогание) и регионарных осложнений (лимфаденит, лимфангиит), локализации глубоких пиодермий на лице, особенно в области носогубного треугольника.
Лечение больных хронической пиодермией системными антибактериальными препаратами должно быть основано на результатах бактериологического анализа с определением чувствительности к ним микрофлоры.
В последние годы препараты пенициллина практически не применяются в терапии пиодермии. В настоящее время наиболее эффективными и в то же время вызывающими наименьшее число побочных реакций являются антибиотики – макролиды (эритромицин, джозамицин, кларитромицин и др.), линкомицин, тетрациклины (тетрациклин, метациклин, доксициклин). Можно назначать также рифампицин, цепорин, цефазолин, цефалотин, цефотаксим, цефтриаксон и другие антибиотики, устойчивые к β-лактамазам и имеющие широкий спектр действия. Разовые и курсовые дозы антибиотиков, способ их введения подбирают индивидуально в зависимости от клинической картины и течения процесса.
Реже антибиотиков, обычно при их непереносимости, применяются сульфаниламидные препараты, которые менее эффективны и нередко вызывают токсидермии. Обычно используют препараты пролонгированного действия (сульфамонометоксин, ко-тримоксазол и др.).
В амбулаторной практике целесообразно применять только антибиотики для приема внутрь с высокой биодоступностью и длительным периодом полувыведения (что позволяет снизить количество приемов в течение суток), при этом воздействие на микрофлору кишечника должно быть минимальным.
При лечении в условиях стационара предпочтение отдают парентеральному введению антибактериальных препаратов. При ступенчатом лечении вначале антибиотик назначают парентерально, а при положительной динамике состояния больного (через 3–7 сут) переходят на его применение внутрь. При первичных инфекциях кожи выбирают антибиотики пенициллинового ряда, альтернативные препараты – цефалоспорины II и III поколения, линкозамиды и фторхинолоны. При легкой или средней форме протекания болезни назначают лекарственные формы для приема внутрь.
При остром течении болезни антибиотик назначается курсом не менее чем на 5–7 сут, при хроническом – на 7–10 сут.
Помимо антибактериальной терапии при хронических формах пиодермии широко применяется иммунотерапия. К средствам активной специфической иммунотерапии относятся стафилококковый анатоксин (нативный и адсорбированный) и стафилококковый антифагин, стафилопротектин, представляющий собой смесь цитоплазматического стафилококкового антигена и анатоксина (препарат вводят подкожно в область нижнего угла лопатки 2 р./нед.). Первая инъекция в дозе 0,3 г, последующие четыре – по 0,5 г. Больным с тяжелыми заболеваниями внутренних органов, что является противопоказанием для проведения активной иммунотерапии, назначают антистафилококковый γ-глобулин или антистафилококковую гипериммунную плазму.
С целью стимуляции неспецифических факторов иммунитета используют аутогемотерапию, пирогенал, продигиозан, диоксометилтетрагидропиримидин, спленин, настойку китайского лимонника, экстракт элеутерококка, гемотрансфузии.
В терапии рецидивирующих, упорно протекающих пиодермий широко применяются иммуностимуляторы, особенно в тех случаях, когда есть возможность подтвердить факт иммунных нарушений: препараты тимуса (тималин, тактивин и др.), препараты γ-глобулинов (γ–глобулин внутримышечный и др.), синтетические химические вещества (левамизол, диуцифон, изопринозин), стерильный фильтрат культуральной жидкости некоторых видов самопроизвольно лизирующихся актиномицет (актинолизат), азоксимера бромид (полиоксидоний). Перспективны стимуляторы выработки интерферонов (оксодигидроакридинилацетат натрия, меглюмина акридонацетат и др.). При всех хронических, вялотекущих формах пиодермии показаны аскорбиновая кислота и витамины группы В и препараты, улучшающие микроциркуляцию (пентоксифиллин, ксантинола никотинат и др.).
При различных формах хронических глубоких пиодермий (язвенно-вегетирующая, гангренозная пиодермии) к антибиотикотерапии присоединяют системные глюкокортикоиды (преднизолон 30–60 мг/cут, метилпреднизолон, бетаметазон), цитостатики (азатиоприн 150 мг/сут, проспидия хлорид).
При лечении абсцедирующего и подрывающего фолликулита Гоффманна применяют изотретиноин из расчета 0,5–1 мг/кг массы тела в течение нескольких месяцев или комбинацию системных антибиотиков и глюкокортикоидов.
В комплексную терапию пиодермий входят физиотерапевтические процедуры: ультрафиолетовое облучение, сухое тепло, УВЧ, низкоэнергетическое лазерное излучение, wiRA-терапия – коротковолновое инфракрасное излучение, прошедшее фильтрацию через воду (780–1400 нм).
Профилактика пиодермий, как первичная (у лиц без гнойничковых заболеваний в анамнезе), так и вторичная, предусматривающая предупреждение рецидивов пиодермии, заключается в проведении определенных мероприятий на производстве и в быту.
На производстве необходимо устранение факторов, приводящих к нарушению санитарно-технических и санитарно-гигиенических норм, производственному травматизму и микротравмам.
Одним из средств борьбы с пиодермиями является своевременная обработка микротравм, для чего применяют растворы анилиновых красителей, спиртовой раствор йода, а также пленкообразующий аэрозоль нитрофурал.
Следует проводить лечение выявленных общих заболеваний, на фоне которых могут развиться гнойничковые поражения кожи (сахарный диабет, болезни пищеварительного тракта, ЛОР-органов и др.).
Вторичная профилактика пиодермии включает периодические медицинские осмотры, учет и анализ заболеваемости, диспансеризацию больных, проведение противорецидивной терапии (стафилококковый анатоксин, витамины, общие УФО, уход за кожей, санация фокальной инфекции).
В лечении заболеваний кожи наряду с другими лекарственными средствами используют глюкокортикоиды. Эти препараты вводят местно, непосредственно в патологический участок.
Когда целесообразно проводить внутриочаговые инъекции?

Глкюкокортикоиды или глюкокортикостероиды – это гормоны, выделяемые корой надпочечников. Созданные на их основе синтетические аналоги зарекомендовали себя как отличные противовоспалительные средства. Однако использование этих лекарств ограничено из-за выраженных побочных эффектов со стороны внутренних органов, обмена веществ. По этой причине глюкокортикоиды противопоказаны при многих сопутствующих заболеваниях.
Особенно выражены негативные последствия глюкокортикоидов при их продолжительном приеме внутрь, внутримышечном или внутривенном введении. В этой связи предпочтительны местные инъекции непосредственно в патологический очаг. Во-первых, здесь создается максимальная концентрация препарата. А во-вторых, нет побочных эффектов, или они минимальны.
Глюкокортикоидом, предназначенным для местного инъекционного введения, является Дипроспан. Действующее вещество здесь – Бетаметазон в виде двух солей. Одна соль Бетаметазона легко растворимая, быстро всасывается, и препарат начинает действовать в первые часы после введения. Другая соль наоборот, всасывается медленно, но действует дольше. Благодаря этому создается пролонгированный (удлиненный) эффект Дипроспана, и нет необходимости в его частом введении.
- укрепляет клеточные мембраны, снижает их проницаемость;
- суживает капилляры кожи;
- блокирует вещества, ответственные за развитие воспалительных реакций;
- препятствует экссудации – появлению воспалительного выпота;
- угнетает аллергические реакции.
Поэтому к местным инъекциям Дипроспана прибегают при болезнях кожи и при многих заболеваниях с кожными проявлениями. Среди них:
- атопические и аллергические дерматиты;
- экземы;
- псориаз;
- системная красная волчанка;
- гипертрофический плоский лишай.
Эффективен Дипроспан и при других кожных заболеваниях, сопровождающихся мокнутием, зудом, отеком и покраснением кожи.
Внутриочаговая терапия на основе глюкокортикостероидов показана для лечения различных патологий кожи, в числе которых отмечаются следующие:

Методика подкожного введения препаратов
Форма выпуска Дипроспана – суспензия в ампулах по 1 мл. Для подкожного введения используют инсулиновые шприцы, снабженные тонкими иглами. После предварительной обработки кожи антисептиками суспензию Дипроспана вводят подкожно так, чтобы обколоть патологический участок. Болезненность инъекций незначительна, поэтому обезболивание не требуется. Внутривенно вводить суспензию Дексаметазона нельзя.
Количество подкожно введенного препарата зависит от вида патологии и от площади поражения, но не должно превышать 2 мл. У многих пациентов клинический эффект в виде уменьшения симптомов воспаления отмечается уже на 2-3 день после инъекций. При необходимости инъекции повторяют, но не ранее чем через 7-12 дней. Обычно на курс лечения приходится от 1 до 3 сеансов подкожных инъекций. При правильной дозировке побочные эффекты не развиваются.
Тем не менее, следует учитывать, что Дипроспан замедляет регенерацию кожи. Его нельзя использовать, если воспаление носит острый инфекционный бактериальный характер, сопровождается образованием гноя. Нельзя его вводить и при грибковых поражениях (микозах) кожи. Среди других противопоказаний: остеопороз, сахарный диабет, гипертоническая болезнь, туберкулез, герпетическая инфекция в стадии обострения. Дипроспан противопоказан беременным и кормящим.
Немедленные побочные реакции инъекций в очаг поражения кожи
- Болевые ощущения. Процедура доставляет определенную боль, однако степень ее выраженности незначительная. Наибольший дискомфорт пациент испытывает при проведении инъекций в такие участки тела, как стопы и ладони.
- Кровотечение. В местах введения инъекций могут выступать капли крови. Это вполне закономерная реакция, не требующая каких-либо мер реагирования.
- Аллергическая реакция. Диагностируется крайне редко. Возникает при наличии у пациента индивидуальной непереносимости к компонентам вводимых медикаментов.
Возможные последующие осложнения

Внутренние побочные эффекты
При внутриочаговой глюкокортикостероидной терапии вероятность развития внутренних побочных эффектов, как например, стремительный набор массы тела, излишний рост волос крайне низка. Это объясняется тем, что в кровоток стероид поступает в очень малой концентрации, не провоцирующей развития никаких негативных реакций.
Эффект от инъекционного введения глюкокортикостероидов
Терапия на основе глюкокортикостероидных средств проводится при необходимости купирования кожных патологических проявлений, облегчения жжения, зуда, иных ощущений пациента, когда менее агрессивные способы лечения оказываются не результативными. Лечебный эффект от проведения инъекций в очаг поражения кожи достигается благодаря способности глюкокортикостероидов вступать во взаимодействие с особыми рецепторами, расположенными в эпидермисе и фибробластах кожного покрова. При этом медикаменты проявляют множество различных эффектов:
- противовоспалительный эффект. Достигается, прежде всего, за счет подавления активности процесса высвобождения фосфолипазы А2, которая выступает в роли главного фермента для образования лейкотриенов и простагландинов, являющихся медиаторами воспаления;
- иммунносупрессивное действие. Глюкокортикостероиды подавляют активность лейкоцитов, мигрирующих к очагу воспаления, а также непосредственно вторгаются в работу фибробластов, тучных клеток, гранулоцитов;
- антипролиферативный эффект. Глюкокортикостероиды препятствуют чрезмерному размножению отдельных клеток, что делает их результативными в лечении таких заболеваний как экзема или псориаз. Эффект достигается за счет ингибирования митоза и синтеза ДНК, образования коллагена и активности фибробластов;
- Сосудосуживающий эффект. Глюкокортикостероидные средства проявляют высокую активность при патологиях кожи, которые сопровождаются гиперемией и отечностью;
Какие препараты используются для инъекций в очаг поражения кожи?

Среди всего многообразия глюкокортикостероидов для инъекционного введения в лечении дерматологических заболеваний особо востребованными являются такие лекарственные средства, как:
- Гидрокортизон;
- Преднизолон;
- Медроп;
- Флостерон;
- Кеналог.
Основные принципы терапии
- Инъекционное введение глюкокортикостероидов целесообразно проводить при отсутствии терапевтического эффекта от применения других средств, характеризующихся меньшей активностью.
- Начинать рекомендуется с наименьшей терапевтической дозы с последующим ее увеличением до требуемого объема.
- Доза глюкокортикостероидных средств для проведения инъекций в очаг поражения должна подбираться индивидуально в каждом конкретном случае и зависеть от тяжести заболевания, характерных особенностей организма, возраста пациента и массы его тела.
Особенности проведения
Внутриочаговые инъекции глюкокортикостероидами проводятся в условиях медицинского центра. Подготовительные мероприятия, специальная подготовка не требуется. До начала выполнения инъекции специалист выясняет у пациента наличие аллергической реакции в анамнезе, состояние его здоровья (наличие тяжелых патологий, хронических заболеваний). Основная задача врача на данном этапе – удостоверится в отсутствии у пациента противопоказаний к проведению инъекционного введения глюкокортикостероидных препаратов в область поражения кожи. Пациент должен сообщить медицинскому работнику обо всех принимаемых им на момент проведения манипуляции лекарственных препаратах, в особенности о средствах, разжижающих кровь (варфарин, аспирин и т.п.). Указанные мероприятия направлены на достижение терапевтического эффекта при минимизации вероятности развития возможных осложнений и негативных побочных действий.
Что такое крапивница? Причины возникновения, диагностику и методы лечения разберем в статье доктора Меркуловой Ирины Юрьевны, аллерголога со стажем в 12 лет.
Над статьей доктора Меркуловой Ирины Юрьевны работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Крапивница — одно из распространённых заболеваний в мире, характеризующееся кожными высыпаниями в виде волдырей. Иногда крапивница сопровождается ангионевротическим отёком (отёком Квинке — частным случаем крапивницы, т. н. гигантская крапивница). [1] Крапивница — самостоятельное заболевание, и её следует отличать от тех случаев, когда волдыри могут служить только симптомом других состояний, которые к ней не относятся: острой анафилактической реакции, при проведении кожных скарификационных проб и т. д . [2]
Причинами возникновения крапивницы могут служить:
- лекарственные препараты (антибиотики, витамины, НПВС, иАПФ, рентгеноконтрастные вещества);
- продукты питания (рыба, ракообразные, орехи, молоко, мёд, пищевые добавки, фрукты, специи при перекрёстной аллергии у пациентов с сезонными и круглогодичными аллергическими ринитами, аллергией на латекс);
- укусы насекомых;
- паразиты (простейшие, гельминты);
- аэроаллергены (пыльца деревьев и трав, шерсть и выделения животных, бытовая или книжная пыль, плесень),
- вирусные, бактериальные, грибковые инфекции (ЛОР-органов, мочеполовой системы, пищеварительной системы, в т.ч. хеликобактерная);
- химические вещества (соли, краски, строительные и ремонтные смеси, косметика);
- латекс (часто у медицинских работников, а также тех, кто вынужден часто пользоваться изделиями из латекса по роду своей деятельности);
- психогенные факторы;
- физическая нагрузка (в т.ч. профессиональный спорт);
- аутоиммунные заболевания (если есть системная красная волчанка, аутоиммунный тиреоидит, ревматоидный артрит и т. д.);
- новообразования;
- генетические факторы;
- УФ-излучение;
- температура (высокая и низкая);
- давление (при сдавлении кожи тугой одеждой, сумками/ранцами, ремнями, в т. ч. у профессиональных спортсменов);
- вибрация (часто у тех, кто по профессиональной необходимости вынужден иметь дело с вибрацией);
- обычная вода. [2]
Если причина не может быть идентифицирована даже после детального сбора анамнеза и проведения аллергологических тестов, то такую крапивницу называют идиопатической. Хроническая идиопатическая крапивница может быть связана с заболеваниями щитовидной железы, гормональным дисбалансом и в очень редких случаях с раковой опухолью. Даже если крапивница хроническая, она, скорее всего, пройдёт со временем.
Что такое нервная крапивница
Психогенные факторы, такие как стресс и яркие эмоции, могут провоцировать развитие острой крапивницы. Также они могут приводить к обострению хронической формы заболевания.
При таком многообразии провоцирующих факторов у трети пациентов причины крапивницы остаются неизвестными. Это связано с несовершенством диагностических возможностей и является предметом научного поиска для учёных по всему миру. [1]
Заразна ли крапивница
Крапивница не заразна и от человека к человеку не передаётся.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы крапивницы
Основные симптомы крапивницы:
- кожный зуд;
- высыпания на коже в виде волдырей.
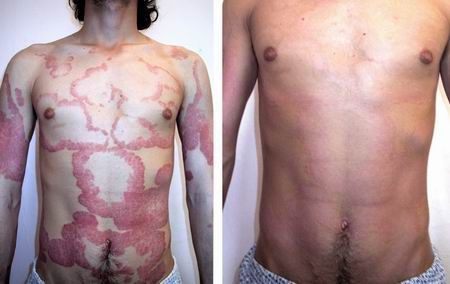
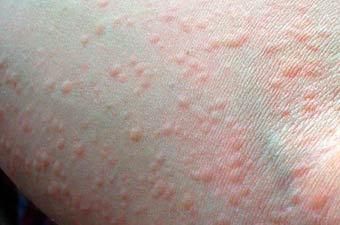
Зуд кожи бывает разной интенсивности — от незначительного зуда до нестерпимого, особенно вечером и ночью. Волдыри могут быть различной формы, сливаться между собой, быть абсолютно любого диаметра (от нескольких миллиметров до нескольких десятков сантиметров), и появляться на любом участке кожи и иногда слизистых. Чаще бледные в центре с покраснением по периферии. В местах скопления большого количества рыхлой подкожно-жировой клетчатки (веки, уши, губы, пальцы, половые органы) крапивница может проявляться в своей гигантской форме — в виде отека Квинке. [2]
Главное отличие высыпаний — это их мономорфность, т. е. сыпь на коже при крапивнице всегда представлена только волдырём. Волдырь — это локальный отёк кожи (мини-отёк Квинке), который бледнеет при надавливании на него. Следующая отличительная черта высыпаний при крапивнице — это то, что волдыри бесследно исчезают в течение 1-2 суток. Это главные отличительные диагностические черты, которые не позволяют перепутать крапивницу с любыми другими заболеваниями, сопровождающимися высыпаниями на коже. Редко интенсивные высыпания могут сопровождаться незначительным повышением температуры тела, снижением давления, слабостью, болями в области эпигастрия или живота схваткообразного характера, жидким стулом. [1]
Крапивница у детей
По приблизительным данным, заболевание встречается у 0,3 − 7 % детей [11] . Симптомы крапивницы у них одинаковы со взрослыми.
Патогенез крапивницы
В основе любой крапивницы лежит активация тучных клеток с их дальнейшей дегрануляцией и высвобождением медиаторов.
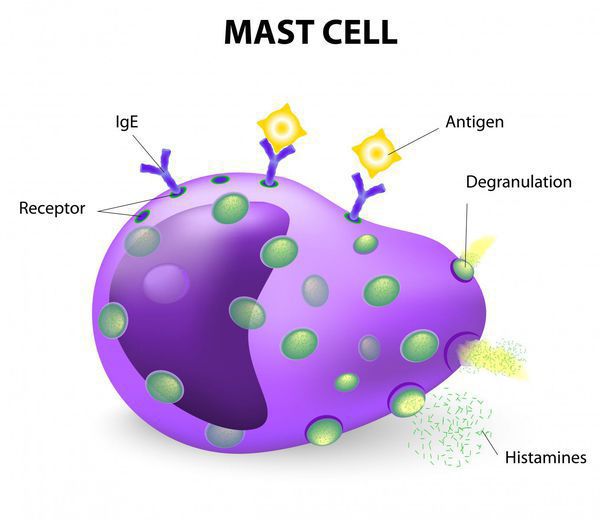
К активации тучных клеток приводят различные механизмы:
1. иммунные (с участием иммунной системы) с вовлечением медиаторов — гистамина, лейкотриенов, брадикинина, простогландинов, ФАТ и т. д. В зависимости от антигена (провоцирующего фактора) развивается крапивница:
- аллергическая (атопическая) при контакте с пищевыми и аэроаллергенами;
- инфекционно-аллергическая при наличии вирусной, грибковой или бактериальной инфекции;
- аутоиммунная при наличии аутоиммунного тиреоидита, системных заболеваний.
2. псевдоаллергические, неиммунные (реализуемые без участия иммунной системы) под влиянием лекарственных препаратов, продуктов-гистаминлибераторов (шоколад, кофе, клубника, копчёности), физического воздействия (высокие и низкие температуры, давление, инсоляция, вибрация и т. д.), ядов насекомых, химических веществ, воды и т. д. [2]
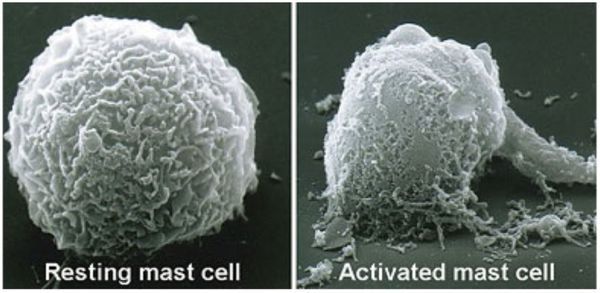
Тучных клеток, т. е. тех, которые реализуют клинические проявления болезни, при хронической крапивнице в организме больного человека в 10 раз больше по сравнению со здоровым. И они чересчур «отзывчивы» к провоцирующему фактору даже при его минимальной активности. Это состояние называется «феномен преходящей гиперреактивности» тучных клеток. [1]
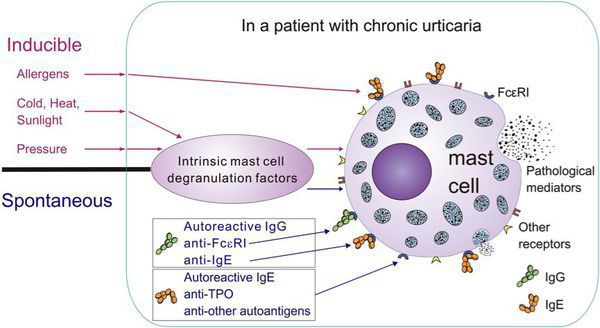
Классификация и стадии развития крапивницы
Выделяют иммунные (в т. ч. IgE-опосредованные), неиммунные, аутоиммунные и смешанные механизмы развития крапивницы.
IgE-опосредованная крапивница связана с выработкой иммуноглобулинов, специфических к аллергену. Такой механизм характерен для острой аллергической крапивницы и встречается чаще всего.
Не-IgE-опосредованная крапивница возникает без выработки специфических иммуноглобулинов. Предполагается, что при этом происходит стимуляция Т-лимфоцитов (клеток иммунной системы) и выработка цитокинов — сигнальных белков, усиливающих иммунный ответ и воспалительную реакцию.
Механизм развития крапивницы при воздействии физических факторов, например тепловых, связан с нарушением нейроиммунной регуляции.
Виды крапивницы по длительности течения:
- острая крапивница (менее 6 недель);
- острая рецидивирующая (длительность ремиссии больше длительности обострения, длительность обострения менее 6 недель);
- хроническая крапивница (более 6 недель). [2]
По степени активности крапивница бывает: [2]
Кроме того, крапивница может быть проявлением ряда заболеваний: наследственного ангионевротического отёка, уртикарного васкулита, пигментной крапивницы (мастоцитоз), семейной холодовой крапивницы (васкулита) и т. д. [2]
Осложнения крапивницы
- отёк Кивнке, или ангионевротический отёк в области гортани с риском развития асфиксии;
- анафилактический шок и другие варианты анафилактической реакции;
- тяжёлые формы крапивницы и ангионевротического отёка, устойчивые к лечению в амбулаторных условиях. [1]
Диагностика крапивницы
Чтобы диагностировать крапивницу, не требуется специфической лабораторной диагностики, в то время как выявление причин заболевания может этого потребовать. [3]
В первую очередь нужно как можно раньше обратиться к врачу аллергологу-иммунологу. Если на время визита высыпаний нет — постараться предоставить врачу фотографии высыпаний/отёков для наибольшей информативности (при условии, что клинические проявления не были тяжёлыми и не требовали экстренной помощи во время фотофиксации).
Врач аллерголог-иммунолог во время приёма соберет подробный анамнез заболевания, анамнез жизни, аллергоанамнез, проведёт физикальное обследование (осмотр, измерение АД, ЧСС, ЧДД, температуры тела, послушает сердце и лёгкие, пропальпирует периферические лимфоузлы, живот). В большинстве случаев этого комплекса диагностики будет достаточно для постановки диагноза и подбора терапии. [2]
Более чем в 90% случаев острая крапивница купируется в течение двух недель и не требует специального обследования, за исключением тех случаев, когда провоцирующий агент установлен. [1]
Какие анализы сдают при крапивнице
Если наблюдаются частые рецидивы острой крапивницы или есть хроническое заболевание, потребуются:
- общий анализ крови с лейкоцитарной формулой и подсчётом СОЭ;
- исследование некоторых биохимических показателей крови;
- обследование на наличие вирусных гепатитов В, С;
- проведение провокационных тестов (кубик льда при подозрении на холодовую крапивницу, горячая грелка при тепловой, водный компресс при аквагенной, тест с физической нагрузкой при подозрении на холинергическую крапивницу и т. д.);
- определение показателей антител к тиреоидной пероксидазе и тиреоглобулину с проведением внутрикожной пробы с аутологичной сывороткой;
- скарификационные пробы с неинфекционными аллергенами и/или наличие специфического иммуноглобулина Е в крови к какому-либо аллергену. [2]
При необходимости дальнейшего диагностического поиска будет целесообразным проведение:
- УЗИ внутренних органов (щитовидная железа, брюшная полость, малый таз);
- ФГДС или рентгеноскопии желудка;
- рентгенологического исследования органов грудной клетки и придаточных пазух носа;
- вирусологического или бактериологического обследования на наличие инфекционных агентов;
- анализа уровня антител к белку Cag A хеликобактера, лямблиям, гельминтам;
- ревмопробы (АНФ, АТ к ДНК, СРБ);
- исследования компонентов комплемента С3, С4 и т. д. [3]
Важным диагностическим тестом у пациентов с крапивницей являются кожные пробы. [9] Они информативны у пациентов с атопической крапивницей и отрицательны у пациентов с псевдоаллергической (при соблюдении сроков проведения тестов и сопутствующей подготовки к тестированию). [5] Также информативен билирубиновый тест на фоне элиминационной пробы (проводят в стационаре, назначается лечебный голод с приёмом только воды, душем и очистительными клизмами). При положительном результате элиминации, уменьшении или купировании симптомов подтверждают аллергический генез крапивницы. У пациентов с аллергической крапивницей уровень билирубина снижен или в пределах нормы, у пациентов с псевдоаллергической крапивницей — повышен. [4]
Лечение крапивницы
Лечение крапивницы состоит из нескольких этапов:
- Элиминация или устранение провоцирующих факторов, триггеров (отменить или заменить лекарственные препараты, избегать перегрева, переохлаждения, инсоляции, отказаться от тесной одежды и не носить тяжести, минимизировать физическую нагрузку и т. п.);
- Выявление и лечение очагов хронической инфекции у профильного специалиста;
- Соблюдение гипоаллергенной диеты (при устранении продукта-аллергена улучшение наступает через 1-2 суток при атопической крапивнице и через 2-3 недели при псевдоаллергической);
- Медикаментозное лечение крапивницы в соответствии с четырьмя линиями терапии в зависимости от эффекта (блокаторы Н1-гистаминовых рецепторов, антилейкотриеновые препараты, анти-IgE-препараты, и т. д.); [10] Лекарства назначает лечащий врач в зависимости от симптомов пациента. Антигистаминные средства бывают двух поколений:
- препараты первого поколения для лечения крапивницы не используются;
- препараты второго поколения — основный метод лечения крапивницы, к ним относятся, например, дезлоратадин и левоцетиризин;
- препараты третьего поколения не существуют, упоминание о них — это маркетинговый ход.
- Вспомогательная терапия, при неэффективности классической — блокаторы Н2-гистаминовых рецепторов, антидепрессанты, стабилизаторы мембран тучных клеток, системные ГКС, иммунодепрессанты, фотодесенсибилизаторы, гистаглобулин, плазмаферез и т. д.; [6]
- Глюкокортикоиды применяют при тяжёлом течении крапивницы. Например при развитии ангионевротического отёка может быть назначен преднизолон.
- Аллерген-специфическая иммунотерапия при подтверждённом аллергическом генезе крапивницы — наиболее эффективный метод лечения;
- Если развивается асфиксия на фоне ангионевротического отёка гортани, может потребоваться экстренная интубация или трахеостомия. [3]
- Энтеросорбенты — убедительных данных об их эффективности при крапивнице нет, в клинических рекомендациях и международных стандартах они не упоминаются.
Стоит помнить, что любая местная терапия в виде крема или мази при крапивнице неэффективна и применяться не должна.
Как снять зуд от крапивницы
Уменьшить зуд можно при помощи антигистаминных препаратов второго поколения, антилейкотриеновых и анксиолитических средств, например "Атаракса". Все препараты применяют только по назначению врача и по рекомендованным схемам. Лечение крапивницы народными средствами бесполезно и опасно.
Нужно ли при крапивнице вызывать скорую помощь
Немедленная медицинская помощь и госпитализация потребуются:
- При тяжёлых формах острой крапивницы и ангионевротического отёка в области гортани с риском удушья. В таких случаях пациент теряет голос, его дыхание становится свистящим и прерывистым.
- При развитии анафилаксии — острой, угрожающей жизни аллергической реакции. Её симптомы включают хрипы, одышку и снижение артериального давления.
Также госпитализация необходима при обострениях хронической крапивницы и ангионевротического отёка, устойчивых к амбулаторному лечению.
Неотложная помощь при отёке Квинке
При отёке Квинке следует:
- немедленно прекратить контакт с предполагаемым провоцирующим агентом;
- вызвать скорую;
- принять одну таблетку антигистаминного препарата второго поколения.
Особенности питания и образа жизни при хронической крапивнице
Рекомендуется не употреблять подтверждённые и предполагаемые аллергены, пищевые добавки и неизвестные ароматизаторы.
Больным с доказанной непереносимостью ацетилсалициловой кислоты следует исключить приём нестероидных противовоспалительных препаратов (НПВП). Остальным пациентам с крапивницей нельзя принимать ацетилсалициловую кислоту и НПВП при обострении заболевания.
Рекомендуется отказаться от тесной одежды и подъёма тяжестей, избегать длительных пеших походов.
Также важно исключить факторы, способствующие переохлаждению: одежду не по сезону, холодные пищу и напитки, длительное пребывание на морозе.
При солнечной крапивнице нужно избегать прямого воздействия солнца, ношения открытой одежды и отказаться от отдыха в южных регионах.
Можно ли принимать ванную или душ при крапивнице
Ограничений на водные гигиенические процедуры при крапивнице нет.
Прогноз. Профилактика
Прогноз при острой крапивнице, как правило, благоприятный. На исход заболевания влияют такие факторы как возраст, пол, длительность болезни, сочетание с ангионевротическими отёками, наличие провоцирующих факторов, ответ на медикаментозную терапию и элиминационные мероприятия. [8] При осложнении крапивницы асфиксией, вызванной отёком гортани, тяжёлыми анафилактическими реакциями, устойчивостью тяжёлых форм крапивницы и ангионевротического отёка к терапии прогноз может быть неблагоприятным (вплоть до смертельного исхода). Это особенно опасно, если медицинская помощь недоступна, невозможно быстро начать экстренные лечебные мероприятия и т. д. [4]
За какое время можно вылечить крапивницу
В течение 6 недель острая крапивница купируется более чем у 75 % пациентов. В хроническую форму болезнь переходит у четверти пациентов [7] . Такая форма крапивницы длится дольше 6 недель, иногда несколько лет, с периодами ремиссии или без них.
С целью профилактики неблагоприятных исходов крапивницы (при наличии соответствующих симптомов) необходимо:
- незамедлительно обратиться к врачу (первичного звена, врачу аллергологу-иммунологу, в экстренных ситуациях — вызвать скорую помощь);
- соблюдать рекомендации по диете, организации быта, образу жизни;
- неукоснительно соблюдать рекомендации врача по лечению, не бросать принимать препараты при первых признаках улучшения, не менять схему, кратность и дозу препаратов, рекомендованных врачом;
- иметь в домашней и автомобильной аптечке, в сумочке препараты для экстренного купирования симптомов, особенно если крапивница сопровождается ангионевротическим отёком, приобрела тяжёлую форму, не получается полностью исключить провоцирующий фактор;
- предупредить родственников/близких/друзей о вашем заболевании и принципах помощи, пока скорая будет спешить на помощь. [2]
Можно ли делать прививки, если у ребёнка крапивница
Хроническая крапивница — не причина отказываться от прививок. При её обострении и острой форме болезни следует дождаться ослабления симптомов и потом вакцинироваться.
Последнее время дерматологами часто используется термин «стероидчувствительные дерматозы» (СЧД), который подразумевает обширную группу разнообразных кожных заболеваний, при которых глюкокортикостероидные препараты обладают клинической эффективностью, часто выступают в качестве препаратов первой линии, а иногда являются единственным решением терапевтической проблемы в конкретном случае. Чаще всего кортикостероиды при СЧД применяются в виде наружных средств, однако при тяжело протекающих дерматозах необходимой становится системная стероидная терапия, являясь подчас единственной эффективной, и по показаниям может быть квалифицирована как терапия неотложных состояний.
- КЛЮЧЕВЫЕ СЛОВА: Дипроспан, дерматоз, бетаметазон
Последнее время дерматологами часто используется термин «стероидчувствительные дерматозы» (СЧД), который подразумевает обширную группу разнообразных кожных заболеваний, при которых глюкокортикостероидные препараты обладают клинической эффективностью, часто выступают в качестве препаратов первой линии, а иногда являются единственным решением терапевтической проблемы в конкретном случае. Чаще всего кортикостероиды при СЧД применяются в виде наружных средств, однако при тяжело протекающих дерматозах необходимой становится системная стероидная терапия, являясь подчас единственной эффективной, и по показаниям может быть квалифицирована как терапия неотложных состояний.
Известно, что системная глюкокортикоидная терапия обладает рядом как серьезных побочных эффектов, так и противопоказаний при наличии сопутствующих заболеваний, что может ограничивать их применение или вовсе делать его невозможным в отдельных случаях. Кроме того, схема применения оральных кортикостероидов при завершении терапии предполагает постепенное, иногда длительное снижение дозировок, что резко ухудшает комплаентность лечения. Полезной альтернативой этому представляются дюрантные препараты, среди которых заслуженной популярностью пользуется парентеральный комбинированный стероид Дипроспан, обладающий таким пролонгированным действием и свободный от ряда побочных эффектов, свойственных в частности оральным стероидам.
Дипроспан содержит 2 мг бетаметазона динатрия фосфата и 5 мг бетаметазона дипропионата. Первый компонент, будучи легкорастворимым, обеспечивает быстрое всасывание активного вещества (пиковая концентрация в крови достигается уже через несколько минут после введения препарата), и клинический эффект его проявляется в первые же часы от начала лечения. Второй компонент, обладающий более медленной абсорбцией, создает условия для пролонгированного действия комбинированного стероида в организме: на 10-й день после инъекции с мочой выводится 40% введенной дозы, а на 19-й день – 51,9%. За счет высокой дисперсности суспензии, округлости формы частиц и малой величины кристаллов солей препарата Дипроспан не оказывает повреждающего воздействия на ткани при производстве инъекции и не требует применения анестетика.
Метааналитическая оценка результатов многочисленных международных многоцентровых клинических исследований прошлых лет по изучению эффективности Дипроспана у больных аллергическими и ревматическими заболеваниями обнаруживает у него целый ряд достоинств. Так, при внутримышечном применении Дипроспана средняя продолжительность наступившего улучшения в состоянии больных составила 20 дней; общий противовоспалительный эффект в 51,5% случаев был отличный, в 37,6% – хороший и в 10,9% – умеренный. Была констатирована высокая эффективность препарата при аллергических заболеваниях, дисгидротической экземе и атопическом дерматите, не поддающихся лечению другими кортикостероидами. Кроме того, было показано, что эффективность Дипроспана заметно выше ряда других системных стероидов, в частности триамцинолона ацетонида. При этом коэффициент безопасности, представляющий собой отношение дозы, вызывающей синдром Кушинга, к дозе, обладающей противовоспалительным действием, составляет у Дипроспана 2,6. Для сравнения коэффициенты дексаметазона, триамцинолона, преднизолона и гидрокортизона были 2,3, 1,6, 1,4 и 1,3 соответственно, что с очевидностью указывает на более высокую безопасность Дипроспана по сравнению с другими кортикостероидами (1, 2).
Основными показаниями к применению Дипроспана являются острые и упорные хронические иммунозависимые состояния, требующие применения кортикостероидов вообще. Среди дерматологических заболеваний сюда относятся аллергический и атопический дерматиты, острые и распространенные экземы, псориаз, особенно эритродермический вариант, псориатический артрит, гнездная плешивость, красная волчанка, гипертрофический плоский лишай, акантолитическая пузырчатка и др. Отдельного внимания заслуживают тяжелые острые дерматологические состояния в виде обширных мокнущих и отечно-воспалительных процессов или универсальных эритродермий с выраженными общими симптомами интоксикаций, которые требуют фактически экстренных терапевтических противовоспалительных мероприятий, среди которых Дипроспан с его быстрым и мощным курирующим эффектом и становится препаратом первой линии.
Дозы Дипроспана в каждом конкретном случае зависят от выраженности воспалительных симптомов дерматоза, его тяжести и массы тела больного. Обычно применяют 1-2 мл в/м с интервалом 10-15 дней в большинстве случаев на курс 2-3 инъекции. Побочные эффекты препарата, будучи общими для всех кортикостероидов, как правило, мало выражены и могут возникать лишь при его нерациональном применении: длительная непрерывная терапия, повышенные дозы и др. Противопоказания для применения Дипроспана также идентичны другим кортикостероидам: туберкулез, остеопороз, сахарный диабет, язва желудка, инфекции кожи; не рекомендуется назначать препарат при беременности и во время лактации.
Более десяти лет назад в отечественной литературе стали появляться работы, показавших высокую эффективность Дипроспана при различных СЧД в случаях их тяжелого, затяжного течении (2).
Согласно результатам этих и других исследований, Дипроспан обладает высокой безопасностью, в том числе и в детском возрасте, он оказался весьма пригодным для применения в амбулаторной практике и признан как полезная альтернатива не только оральной стероидной терапии, но и эффективным при внутриочаговом введении (3). Кроме того, Дипроспан относится к препаратам первого выбора при острых, тяжелых и распространенных аллергодерматозах, демонстрируя свои возможности в качестве ургентной терапии (6).
Как известно, атопический дерматит (АД) встречается с частотой до 5-8% в популяции и преимущественно у детей и людей молодого работоспособного возраста.
В основе патогенеза АД лежит генетическая предрасположенность к заболеванию в виде фенотипических особенностей функционирования иммунной системы, характеризующихся гиперактивным состоянием Т-хелперов и в острых фазах заболевания с доминированием цитокинового профиля второго типа. Именно эти основные особенности патогенеза АД и объясняют эффективность иммуносупрессивной терапии как в виде наружных кортикостероидов, так и системных, применяемых в особо тяжелых случаях. Именно при островоспалительных и генерализованных формах АД и находит применение Дипроспан в виде скоропомощной этапной терапии, позволяющей быстро вывести больного из критического состояния с последующим переходом на другие виды лечения.
Как показывают наблюдения прошлых лет, Дипроспан при АД назначают в дозе 1-2 мл в/м 1 раз в 7-12 дней в зависимости от выраженности воспалительных процессов в коже и зуда. На курс лечения приходится как правило от 1 до 3 инъекций. Обычно на 2-3 день после первой инъекции значительно уменьшается зуд и заметно стихают островоспалительные явления. По данным большинства работ, практически у всех больных лечение с применением Дипроспана к концу курса приводило к значительному улучшению или клинической ремиссии и повышению качества жизни пациентов (1).
В одной из наших последних подборок под наблюдением находилось 35 больных АД в возрасте от 19 лет до 35 лет, среди которых был 21 мужчина и 14 женщин в возрасте от 20 до 32 лет. У всех больных клиническая картина АД характеризовалась особо выраженными воспалительными явлениями, распространенностью кожного процесса, сильным зудом и упорством к различным видам обычной терапии. При формировании группы наблюдения принципиальным критерием отнесения больного к такой тяжелой, распространенной форме дерматоза служил показатель Дерматологического индекса шкалы симптомов (ДИШС) не ниже 19 или не менее 70% от максимально возможного показателя ДИШС (максимум ДИШС – 27). Разовая доза для в/м введения препарата в 2,0 мл применялась у 27 больных и 1,0 мл – еще у 8 больных, имевших массу тела менее 60 кг. Количество инъекций на курс составило: 1 инъекция у 6 больных, 2 – у 23 и 3 инъекции у 6 больных. Введение препарата проводили с интервалом в 10-14 дней, в зависимости от показаний. У всех больных лечение переносилось без побочных явлений.
1. Кочергин Н.Г., Константинова В.А. Опыт применения Дипроспана при аллергодерматозах. Российский журнал кожных и венерических болезней. 1998. № 1. С. 25-27.
2. Кочергин Н.Г. Основные аспекты патогенеза, клиники и современной терапии атопического дерматита. Докт. дисс., 2001.
3. Belousova T., Tepljuk N., Kochergin N. Intralesional Betamethasone in granuloma faciale. Ann.Dermat.Venereol. juillet 2002. Cahier2. P. 1S691.
5. Kimball A.B., Gladman D., Gelfand J.M. et al. National Psoriasis Foundation clinical consensus on psoriasis comorbidities and recommendations for screening. J. Am. Acad.Drmatol. 2008. V. 58. P. 1031-1042.
6. Kochergin N.G., Belousova T.A., Novoselov B.S. Betamethasone efficacy in dermatoses. Clinical Dermatology 2000. Abstracts. Singapore. 1998. P. 141.
Для цитирования: Белоусова Т.А., Каюмова Л.Н., Горячкина М.В. Системные антибиотики в терапии бактериальных инфекций кожи и мягких тканей: фокус на макролиды. РМЖ. 2011;21:1317.
Эпидемиология Бактериальные инфекции кожи, вызывающие ее гнойное воспаление, были выделены в группу инфекционных дерматозов французским ученым H. Leloir в 1891 г. под названием пиодермиты (pyon – гной, derma – кожа). За рубежом пиодермии обычно относят к обширной группе инфекций кожи и мягких тканей (ИКМТ), включающей, помимо инфекций кожи и ее придаточных образований, инфекции подкожно–жировой клетчатки и нижележащих тканей.
Литература
1. Jones M.E., Karlowsky J.A., Draghi D.C, Thornsberry C., Sahm D.F., Nathwani D. Epidemiology and antibiotic susceptibility of bacteria causing skin and soft tissue infections in the USA and Europe: a guide to appropriate antimicrobial treatment. Int J Antimicrob Agent 2003; 22:406–19.
2. Н.Н. Мурашкин, М.Н. Глузмина, Л.С. Галустян. Гнойничковые поражения кожи в практике детского дерматолога: свежий взгляд на старую проблему. РЖКВБ: Научно–практический журнал, 2008, №4, с. 67–71.
3. Белькова Ю.А. Пиодермии в амбулаторной практике. Болезни и возбудители. Клиническая микробиология и антимикробная химиотерапия: № 3, том 7, с. 255–270, 2005.
4. Т.А. Белоусова, М.В. Горячкина. Бактериальные инфекции кожи: проблема выбора оптимального антибиотика. РМЖ 2005, том 13, №16, с. 1086–1089.
5. Таха Т.В., Нажмутдинова Д.К. Рациональный выбор антибиотикотерапии при пиодермиях. РМЖ 2008, том 16, №8, с. 552–555.
6. Новоселов В.С., Плиева Л.Р. Пиодермии. РМЖ 2004, том 12, №5, с. 327–335.
7. Масюкова С.А., Гладько В.В., Устинов М.В., Владимирова Е.В., Тарасенко Г.Н., Сорокина Е.В. Бактериальные инфекции кожи и их значение в клинической практике дерматолога. Consilium medicum 2004, том 6, №3, с. 180–185.
8. T. File. Diagnosis and antimicrobial therapy of skin and soft tissue infections. Ohio, USA. Клиническая микробиология и антимикробная химиотерапия: № 2, том 5, с. 119–125, 2003
9. Шляпников С.А., Федорова В.В. Использование макролидов при хирургичесаких инфекциях кожи и мягких тканей. МРЖ,2004.–т.12,№4,с204–207
10. Гучев И.А., Сидоренко С.В, Французов В.Н. Рациональная антимикробная химиотерапия инфекций кожи и мягких тканей. Антибиотики и химиотерапия. 2003, т.48, 10, с.25–31
11. Parsad D., Pandhi R., Dogras S. A guide to selection and appropriate use ofmacrolides in skin infection Am J Clin Dermatol 2003; 4:389–97
12. Яковлев С.В., .Ухтин С.А. Азитромицин: основные свойства, оптимизация режимов применения на основе фармакокинетических и параметров. Антибиотики и химиотерапия. 2003 т. 48, №2. – с. 22–27
13. Туровский А.Б,.Колбанова И.Г Макролиды в лечении инфекций дыхательных путей с позиций ЛОР–врача: «за» и «против» Consilium medicum, 2010г.,№4, том.12, с.11–14.
14. Прохорович Е.А. Азитромицин. От клинической фармакологии к клинической практике. РМЖ 2006, том 14, №7, с. 567–572
15. Бердникова Н.Г. Актуальные аспекты применения азитромицина (Азитрал) в терапии внебольничных пневмоний у взрослых. РМЖ 2006, том 14, №22, с. 1625–1628.
16. Хрянин А.А., Решетников О.В. Макролиды в лечении хламидийной инфекции у беременных (эффективность, безопасность, экономичность). РМЖ 2008, том 16, №1, с. 23–27.
17. Серов В.Н., Дубницкая Л.В., Тютюнник В.Л. Воспалительные заболевания органов малого таза: диагностические критерии и принципы лечения. РМЖ 2011, том 19, №1, с. 46–50.
18. Талашова С.В. Некоторые аспекты применения антибактериальных препаратов в педиатрии на примере макролидов. РМЖ 2009, том 17, №7, с. 464–466
19. Мазанкова Л.Н., Ильина Н.О. Место азалидов в педиатрической практике. РМЖ 2008, том 16, №3, с. 121–125.
20. Соловьев А.М., Поздняков О.Л., Терещенко А.В. Почему азитромицин считается препаратом выбора для лечения урогенитальной хламидийной инфекции. РМЖ 2006, том 14, №15, с. 1160–1164.
21. Гуров А.В., Изотова Г.Н., Юшкина М.А. Возможности применения препарата Азитрал в терапии гнойно–воспалительных заболеваний ЛОР–органов. РМЖ 2011, том 19, №6, с. 405.
22. Klani R. Double–blind, double–dummy comparison of azithromycin and cephalexin in the treatmen of skin and skin structure infection. Eur.J. Clin. Microbiol. Infect.Dis. 1999,Oct. 10 (10) – p.880–84
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Читайте также:

