Кагоцел при опоясывающем лишае
Обновлено: 24.04.2024
Назначают ацикловир внутрь 800 мг 5 раз в сутки в течение 7-10 дней.
При неэффективности ацикловира альтернативными средствами являются:
- Валацикловир 1000 мг 3 раза в сутки в течение 7 дней или,
- Фамцикловир 500 мг внутрь 3 раза в сутки в течение 7 дней.
При отсутствии эффекта в указанные сроки или рецидивировании заболевания необходимо продолжение противовирусной терапии до прекращения появления кожных высыпаний.
Лечение опоясыающего герпеса у детей
Ацикловир 20 мг/кг массы тела внутрь 4 раза в сутки в течение 5 дней.
Лечение пациентов с ослабленным иммунитетом (пациенты со злокачественными новообразованиями, реципиенты трансплантированных внутренних органов, ВИЧ- инфицированные пациенты)
Ацикловир 10 мг/кг массы тела внутривенно капельно 4 раза в сутки.
По достижении контроля над инфекцией внутривенное введение препарата может быть прекращено, а до окончания курса лечения (по поводу основного заболевания) противовирусный препарат может быть назначен перорально.
При небольшой степени иммуносупрессии целесообразно пероральное применение ацикловира (800 мг 5 раз в день), валацикловира (1000 мг 3 раза в день) или фамцикловира (500 мг 3 раза в день).
Лечение болевого синдрома при опоясывающем герпесе
Целесообразно поэтапное лечение зостер-ассоциированного болевого синдрома во всех его фазах. Так, при лечении острой герпетической невралгии противоболевая терапия состоит из трех основных этапов:
- 1-й этап: аспирин, парацетамол, НПВС;
- 2-й этап: опиоидные анальгетики, включая трамадол;
- 3-й этап: препараты с центральным анальгетическим действием (трехциклические атидепрессанты, антиконвульсанты).
Важным моментом является наблюдение за динамикой болевого синдрома в острой стадии, так как усиление болей со временем может указывать на прогрессирование инфекционного процесса.
Кортикостероиды
Добавление к противовирусным средствам глюкокортикостероидных препаратов в течение 3 недель в постепенно уменьшающейся дозировке (60 мг преднизолона ежедневно в течение 7 дней с последующим снижением дозы) приводит к сокращению острого болевого синдрома. Наиболее целесообразна комбинированная терапия при поражении ветвей тройничного нерва. Наряду с уменьшением острой боли у пациентов, получавших комбинированное лечение, наблюдалось улучшение сна, возвращение к повседневной нормальной активности и сокращение приема анальгетиков. При назначении глюкокортикостероидов необходимо учитывать противопоказания: артериальную гипертензию, сахарный диабет, язвенную болезнь желудка и двенадцатиперстной кишки, нередко наблюдаемые у лиц пожилого возраста.
Невральные блокады
Симпатические и эпидуральные блокады используются при крайне тяжелом болевом синдроме. Имеются единичные рандомизированные клинические испытания, показавшие эффективность однократного эпидурального введения стероидов и местных анестетиков в плане облегчения острой боли. Терапия с применением многократных эпидуральных инъекций анестетика и метилпреднизолона без противовирусного лечения при опоясывающем герпесе давала снижение частоты постгерпетической невралгии по сравнению с внутривенным введением ацикловира и преднизолона. Эти данные позволяют полагать, что «агрессивное» обезболивание является вполне эффективным при опоясывающем герпесе.
Лечение постгерпетической невралгии
В настоящее время для лечения постгерпетической невралгии выделяют 5 основных групп лечебных средств: антиконвульсанты, трициклические антидепрессанты, пластырь с лидокаином, капсаицин, опиоидные анальгетики.
Антиконвульсанты
Габапентин и прегабалин — два наиболее часто используемых для купирования невропатической боли, связанной с ПГН, антиконвульсанта. Схема применения габапентина. Начальная доза: 1-й день 300 мг вечером; 2-й день по 300 мг 2 раза (днем и вечером); 3-й день по 300 мг 3 раза. Титрование: 4-6-й день 300-300-600 мг; 7-10-й день 300-600-600 мг; 11-14-й день 600-600-600 мг. Суточная терапевтическая доза 1800-3600 мг, поддерживающая доза 600—1200 мг/сут. Прегабалин обладает с габапентином сходным механизмом действия, однако не требует медленного титрования и поэтому более удобен при клиническом применении. Препарат назначают два раза в сутки. Начальная доза — 75 мг два раза, суточная терапевтическая доза 300-600 мг.
Антидепрессанты
Препараты этой группы, особенно трициклические (нортриптилин и амитриптилин), являются важными компонентами в лечении боли при ПГН. Благодаря активации нисходящих серотонин- и норадреналинергических антиноцицептивных систем и способности блокировать натриевые каналы антидепрессанты блокируют восприятие боли.
Пластырь с 5% лидокаином
Апплицируется на зону воздействия в начале хронизации боли или сразу после установления диагноза ПГН. Пластырь накладывают на интактную, сухую, невоспаленную кожу, т. е. во время активных герпетических высыпаний.
Капсаицин
Препарат, изготовляемый из красного перца, оказывает раздражающее действие и используется в виде мази или пластыря. Препарат должен наноситься на область поражения 3—5 раз в день для поддержания длительного эффекта.
Опиоидные анальгетики
Оксикодон, метадон, морфий также могут использоваться в лечении ПГН. Они уменьшают невропатическую боль благодаря связыванию опиоидных рецепторов в ЦНС либо ингибированию обратного захвата серотонина или норадреналина в периферических нервных окончаниях — нервных синапсах.
Наружное лечение
На эрозии наносят водные растворы красителей, мази, кремы и аэрозоли, содержащие противовирусные средства (пенцикловир, ацикловир, оксолин, панавир и др.).
Материал подготовил: Раводин Роман Анатольевич, дерматовенеролог, дерматоонколог, дерматокосметолог. Доктор медицинских наук, доцент
Так проявляется одна из форм герпетической инфекции — вирусного заболевания, для которого типично образование пузырьков на коже и слизистых оболочках. Что вызывает эту болезнь, и существуют ли лекарственные препараты против герпеса, которые могли бы раз и навсегда избавить от него?
Герпес: враг нервных клеток
Простуда на губах (простой или лабиальный герпес) является результатом инфицирования вирусом герпеса 1 типа — ВПГ-1. Но иногда причиной пузырьков на губах может являться вирус герпеса 2 типа (ВПГ-2), который обычно чаще поражает слизистую гениталий, промежности, нижних конечностей и т.д. Это важно знать и помнить, поскольку данное заболевание легко передаётся от человека к человеку при непосредственных контактах 1 .
То, что с герпетической инфекцией знакомы практически все — не миф. По разным данным, от 90 до 95% жителей земного шара заражено вирусом простого герпеса. Он передаётся от больного (или носителя вируса) к здоровому человеку при поцелуях, половых контактах. Также возможен механический перенос вируса из герпетического очага в другие места, например, занос руками вируса из полости рта при герпетическом стоматите на конъюнктиву глаза, в области гениталий, на любые участки тела через микроповреждения кожи. Достаточно незаметной трещинки на губах или потёртости в области гениталий, чтобы вирус проник через кожу и нашёл «свою» нервную клетку 1 . Присутствие вируса в слюне обеспечивает возможность его передачи воздушно-капельным путем, хотя этот путь заражения к ведущим не относится.
ВПГ обладает уникальными биологическими свойствами.
Тканевой тропизм (специфичная чувствительность) к эпителиальным (слизистая и кожа) и нервным клеткам.
Способность к персистенции — непрерывному или цикличному размножению (реплицированию) в инфицированных клетках.
Способность к латенции (без проявления симптомов) в организме инфицированного человека.
Вирусы простого герпеса способны существовать и воспроизводиться только в ганглиях (узлах) нервной ткани. ВПГ-1 «предпочитает» чувствительные ганглии тройничного нерва (в Гассеровом узле) и других черепно-мозговых нервов, поскольку их ветви как раз проходят в области губ, носоглотки и ротовой полости. ВПГ-2, вызывающий преимущественно поражение гениталий, промежности, анальной области, нижних конечностей, ягодиц, персистирует в ганглиях пояснично-крестцового отдела позвоночника (седалищный нерв) 1 .
Распространение ВПГ-1 возможно также по зрительному нерву при офтальмогерпесе и обонятельному нерву при поражении носоглотки с последующим проникновением в центральную нервную систему (ЦНС), реже гематогенным путем (с кровью по системному кровотоку).
Виды герпетической инфекции
Из восьми вирусов герпеса, известных сегодня, пять могут вызывать заболевания 1 :
ВПГ-1 — «простуду на губах» или «герпетическую лихорадку»;
ВПГ-2 — генитальный герпес (реже «простуду на губах»);
варицелловирус или ВПГ-3 — опоясывающий лишай и ветрянку;
ВПГ-4, известный как вирус Эпштейна-Барр, — инфекционный мононуклеоз;
ВПГ-5 — цитомегаловирусную инфекцию 1 .
Первые три вируса наиболее распространены, легко передаются от человека к человеку. Но если от ветряной оспы существует прививка, то от «герпетической лихорадки» и опоясывающего лишая защититься довольно сложно, только очень тщательно соблюдая личную гигиену. Противовирусных препаратов от герпетической инфекции (ВПГ-1), которые были бы способны полностью вывести вирус из организма, в мире пока не существует. В случае, если инфекция уже попала в организм, от её проявлений (симптомов) могут помочь меры профилактики рецидивов (повторных проявлений, возвращений болезни).
Виды и симптомы герпеса
Многие ошибочно считают, что опасность герпеса заключается в неприятных симптомах и возможности передачи инфекции при контактах. На самом деле болезненные пузырьки на слизистой лишь один, хоть и самый распространённый, но всё же не единственный вариант течения и признак заболевания.
Лабиальный герпес характеризуется появлением тех самых пузырьков на губе. Как правило, сразу после попадания вируса на слизистую они не образуются, или же появляется небольшая ранка во рту, которая остаётся незамеченной. Однако по прошествии времени, после проникновения и инфицирования нервных клеток, ВПГ-1 активизируется под воздействием провоцирующих факторов, снижающих активность иммунитета:
тяжёлые физические нагрузки;
стресс, тревога (поэтому в народе считается, что пузырьки на губе «появляются от испуга»);
ожоги, в том числе солнечные;
Герпетический стоматит — воспаление слизистой оболочки рта, при котором пузырьки образуются внутри ротовой полости: на щеках, дёснах, языке, мягком и твёрдом нёбе.
Генитальный герпес проявлениями похож на ВПГ-1, но пузырьки и корочки образуются на слизистых наружных половых органов, промежности, анальной области, коже нижних конечностей, ягодиц.
Герпетический панариций — поражение мягких тканей пальцев на руках и ногах в результате проникновения ВПГ через повреждённую кожу. Это опасное течение инфекции: в области воспаления скапливаются другие возбудители, которые по волокнам сухожилий могут перейти на суставы и вызвать их тяжёлое воспаление.
«Герпес гладиаторов» возникает на месте травм у единоборцев, футболистов, регбистов при соприкосновении «язвочек» и высыпаний инфицированного спортсмена с поврежденной поверхностью кожи и слизистой другого спортсмена (рана, царапина) во время игры или борьбы. Язвочки при этой форме образуются на шее, ушах, лице, глазах, спине, ногах: в тех местах, где произошел тесный контакт кожных покровов здорового и больного человека.
Герпес-конъюнктивит (офтальмогерпес) проявляется очень болезненными многочисленными мелкими пузырьками на веках, роговице, конъюнктиве.
Герпетический энцефалит и менингит поражают мозг. Если вовремя не начать лечение, то болезнь может закончиться летальным исходом.
Герпетические поражения кожи — экзема, дерматит, сикоз (пузырьки образуются на волосяных фолликулах) — характеризуются высокой болезненностью, частыми рецидивами, тяжелым реагированием на терапию 1 .
Значение иммунных факторов в профилактике обострений и их лечении
Герпетические инфекции проявляются циклами: если на слизистой появляются пузырьки или корочки, то это стадия активности, а если их нет — стадия ремиссии. Но отсутствие проявлений вовсе не означает, что вирус не опасен: он так и живёт в нервных клетках, просто система иммунитета сдерживает его. Даже если симптомы заболевания отсутствуют, возможность заразить другого человека сохраняется: например, при контакте с такими травмами, как царапины или раны 1 .
Рецидивы проявления герпеса вызывают провоцирующие факторы, снижающие силу иммунной защиты. Под их влиянием вирус «просыпается», рассылает свои частицы по нейронам, откуда они проникают в кожу, слизистые, конъюнктиву. Образуется очаг воспаления, появляются пузырьки и другие симптомы. Всё это происходит очень быстро, в течение 7-10 часов 1 .
При хорошо работающей иммунной системе и своевременной профилактике факторов риска стойкий иммунитет развивается довольно быстро, что приводит к снижению частоты развития рецидивов (более редким проявлениям болезни), уменьшению выраженности проявлений заболевания (уменьшение размера пузырьков, болезненности, ускорение эпителизации (заживления) ранок) и более быстрому выздоровлению. Выработка антител против ВПГ-1 приводит к тому, что организм становится защищённым и от других герпес-вирусов. То есть, если человек перенёс герпетический панариций, то генитальной формы у него, скорее всего, не возникнет 1 .
Индукторы интерферона как средство от герпеса: помощь иммунитету в борьбе с рецидивами
Одним из препятствий для разрушительной деятельности вирусов, в том числе вирусов герпеса, являются интерфероны: организм вырабатывает их при проникновении или активизации патогена. Интерфероны — это несколько групп особых белков, предотвращающих размножение возбудителей вирусных инфекций.
Эволюционно герпес-вирусы «научились» противодействовать интерферонам и другим факторам иммунитета. Из-за этого может возникать дефицит выработки собственных защитных сил человека и, соответственно, более частые рецидивы высыпаний, с длительным и тяжёлым течением.
Предупредить развитие подобного варианта могут противовирусные препараты, эффективные при герпесе, в частности, индукторы интерферона.
Они способствуют выработке собственных эндогенных противовирусных белков Т- и В-лимфоцитами, энтероцитами и другими иммунокомпетентными клетками.
Они могут оказывать прямое противовирусное действие 2,3 .
Кагоцел: лекарство от герпеса в таблетках
В качестве препарата-индуктора интерферонов используется Кагоцел. Проведённые клинические и наблюдательные исследования, а также клинический опыт применения препарата позволили получить достоверные данные о его интерфероногенной способности. На фоне его приёма повышается противовирусный ответ организма со стороны практически всех клеток иммунной системы 1 .
Приём всего одной эффективной дозы Кагоцела позволяет достичь максимальных значений уровня интерферонов в крови в течение 48 часов после приема, и этот эффект сохраняется до 4-5 суток, то есть как раз в течение всего периода рецидивирующей активности ВПГ4.
Схема приёма препарата в таблетках проста. Препарат для лечения герпеса у взрослых рекомендовано принимать внутрь, вне зависимости от приёма пищи, запивая водой, по 2 таблетки 3 раза в день в течение 5 дней. Таким образом, на курс требуется 30 таблеток 4 .
Он не обладает токсическими свойствами, не оказывает канцерогенного действия, не накапливается в органах и тканях, не имеет негативного влияния на плод и эмбрион 4 .
Противовирусный препарат Кагоцел доказал свою безопасность и активность в качестве средства для лечения простого герпеса в период обострения. Препарат от герпеса в таблетках Кагоцел легко дозировать, его приём не требует манипуляций с отмериванием нужного количества (как, например, любые препараты, дозируемые в каплях), и потому он может назначаться в амбулаторной практике и приниматься дома, а не в лечебном учреждении 4 .
Одной из актуальных проблем современной клинической медицины являются вирусные заболевания, в том числе вирусные дерматозы. Особое место среди них занимает простой герпес (ПГ).
Одной из актуальных проблем современной клинической медицины являются вирусные заболевания, в том числе вирусные дерматозы. Особое место среди них занимает простой герпес (ПГ).
Термин «герпес» (от греч. hеrро – «ползти») известен в медицине почти 25 веков. Лихорадочный герпес («простуда») был описан римским врачом Геродотом еще в 100 г. до н. э. Упоминания о нем встречаются в трактатах таких знаменитых врачей прошлого, как Гиппократ, Авиценна и Парацельс.
Через 110 лет, прошедших со времени выделения возбудителя заболевания – вируса простого герпеса (ВПГ) – и последовавшего за этим активного изучения вопросов эпидемиологии, патогенеза, клиники и терапии ПГ, актуальность многих аспектов проблемы остается достаточно высокой.
По современным оценкам, частота инфицированности населения ВПГ приближается к 100%. Сероэпидемиологические исследования показали, что уже сегодня свыше 95% взрослого населения имеют антитела к вирусу того или иного типа, при этом была выявлена стойкая тенденция к росту числа инфицированных. Так, количество носителей только 2 типа ВПГ за последние 15 лет увеличилось примерно на 20% [1].
Такая же ситуация наблюдается в отношении заболеваемости ПГ. Сегодня можно говорить о том, что частота развития клинических проявлений инфекции крайне высока. Она занимает второе место среди вирусных поражений человека, уступая лишь гриппу. Ряд исследований свидетельствуют о том, что, по одним данным, в 20–25% случаев, а по другим – в 60–70% герпетическая инфекция проявляется клинически [2].
Все более возрастающий интерес к проблеме ПГ со стороны врачей различных специальностей связан с рядом объективных моментов.
В частности, с крайне выраженным клиническим полиморфизмом заболевания – от ограниченных поражений кожи, слизистых и глаз до системных, генерализованных форм с вовлечением в вирусный процесс жизненно важных внутренних органов, а также развитием на фоне хронической персистенции ВПГ бесплодия, невынашивания беременности и злокачественных новообразований [3, 9].
В связи с этим в настоящее время наряду с понятием ПГ все большее распространение получает термин «герпетическая болезнь» (ГБ), который как нельзя лучше отражает системный характер негативного действия ВПГ на организм в целом.
Доказано, что местом «обитания» или персистенции ВПГ 1–2 типов, являются чувствительные паравертебральные ганглии вегетативной нервной системы. Механизмы, сдерживающие развитие герпетической инфекции, известны. Это факторы неспецифической (интерфероновой) и специфической (иммунной) систем защиты. Образование интерферонов (ИФН) является врожденной реакцией организма на внедрение вирусов. ИФН (прежде всего α и β) подавляют внутриклеточное размножение вирусов сразу же после внедрения в организм, с помощью естественных киллеров удаляют инфицированный материал и, окружая незараженные клетки, защищают их от вирусной инвазии. На следующем этапе образование ИФН-α и -β увеличивается, начинается синтез ИФН-γ, увеличивается экспрессия генов интерлейкина 1 (ИЛ-1), фактора некроза опухолей (ФНО) и других цитокинов с последующим развитием Т- и В-клеточного иммунитета. Считают, что реакции первого этапа способны уничтожить вирус или блокировать его дальнейшее распространение в течение неопределенно долгого периода времени.
Причиной реактивации вируса, проявляющейся в виде клинических обострений, являются дефекты в системах сдерживания герпетической инфекции, образующиеся под влиянием разнообразных факторов. Триггерами активации латентной инфекции могут быть: стресс, хронические заболевания, сезонные ОРВИ, экологическая обстановка, социально-экономические факторы, недостаточное питание и пр. В большинстве своем они носят презумптивный характер и часто анамнестически не определяются, что ограничивает эффективность лечебных воздействий.
В основе герпетических заболеваний лежат нарушение иммунологического и интерферонового статусов, вторичная негативная иммунная перестройка (угнетение реакций клеточного иммунитета, интерферон-продуцирующей способности лейкоцитов).
Открытие с помощью методов молекулярной биологии механизмов репликации ВПГ, а также изучение взаимодействия вирусов герпеса с чувствительными клетками позволили создать ряд эффективных химиотерапевтических средств, обладающих противогерпетической активностью.
В первую очередь это ацикловир, валацикловир и фамцикловир, которые являются надежными противовирусными средствами. Клинический опыт применения этих препаратов показал, что, быстро и эффективно купируя острые проявления герпесвирусной инфекции (ГВИ), они не предотвращают повторного рецидивирования хронической ГВИ. Существуют и другие недостатки этих препаратов: формирование резистентности штаммов вируса к химиопрепаратам, сохранение терапевтического эффекта только на фоне приема препарата, возможные токсические эффекты (энцефалопатии, диспепсия, поражение печени, органов кроветворения, снижение артериального давления).
Поэтому необходимы меры по активизации системы собственной защиты (интерферонов) для лечения и профилактики вирусных инфекций. Существует два способа такой активизации: введение готовых продуктов (синтетических ИФН) и стимуляция образования собственных ИФН с помощью индукторов.
- гриппоподобный синдром (ухудшение общего состояния, повышение температуры, головные боли, высокая утомляемость);
- диспепсические явления (снижение аппетита, рвота, ускорение моторики, изжога);
- кожные реакции;
- лейко- и тромбоцитопения, снижение гематокрита;
- повышение уровня печеночных ферментов, развитие протеин- и альбуминурии;
- возможность формирования аутоантител к ИФН.
Применение индукторов интерферона имеет преимущества по сравнению с использованием синтетических интерферонов, что обусловлено следующими факторами:
- образование эндогенного ИФН – более физиологичный процесс, чем постоянное введение больших доз чужеродного ИФН, который к тому же быстро выводится из организма и блокирует по принципу отрицательной обратной связи синтез аутологичных ИФН;
- индукторы ИФН не приводят к образованию в организме антител к ИФН и большей частью низкоаллергенны;
- индукторы ИФН вызывают пролонгированное образование эндогенного ИФН в физиологических дозах;
- индукторы ИФН обладают наряду с прямой противовирусной активностью иммунокорригирующим эффектом, что позволяет отнести их к новому поколению препаратов с универсальным действием.
В последние годы для лечения и профилактики часто рецидивирующего ПГ стал широко применяться новый отечественный пероральный индуктор интерферона Кагоцел® [4, 10, 11].
Кагоцел® – гетероцепный полимер молекулярной массой 120–130 кДа, полученный путем химического синтеза из растительного сырья – водорастворимой карбоксиметилцеллюлозы и низкомолекулярного полифенола. После введения в молекулу карбоксиметилцеллюлозы полимера низкомолекулярного полифенола образуется новое соединение с высокой биологической активностью (рис.).
С помощью экспериментальных и клинических исследований была установлена мощная иммуномодулирующая активность препарата Кагоцел®. Основным его свойством является способность индуцировать продукцию ИФН. Он вызывает образование в организме человека смеси так называемых поздних ИФН-α и ИФН-β, которые обладают высокой противовирусной активностью. Кагоцел® стимулирует продукцию ИФН практически во всех популяциях клеток, принимающих участие в иммунном ответе организма на внутриклеточные агенты: Т- и В-лимфоцитах, макрофагах, гранулоцитах, фибробластах, эндотелиальных клетках. При приеме внутрь одной дозы препарата титр ИФН в сыворотке крови достигает максимальных значений через 48 ч. ИФН-ответ организма на введение Кагоцела® характеризуется продолжительной (до 4–5 суток) циркуляцией ИФН в кровотоке. Продукция ИФН в сыворотке крови достигает высоких значений лишь через 48 ч после приема Кагоцела®, в то время как в кишечнике максимум продукции ИФН отмечается уже через 4 ч.
Кагоцел® выпускается в виде таблеток по 0,1 г, содержащих 12 мг активного вещества. Другие компоненты таблеток – крахмал картофельный, кальция стеарат, лудипресс. При назначении в терапевтических дозах Кагоцел® нетоксичен, не накапливается в организме. Препарат не имеет мутагенных и тератогенных свойств, неканцерогенен и не обладает эмбриотоксическим действием. Наибольшая эффективность при лечении Кагоцелом® достигается при его назначении не позднее 4 суток от начала острой инфекции.
Экспериментальные исследования показали, что Кагоцел® в культуре клеток Vero подавляет репродукцию ВПГ 1 и 2 типа, включая мутантные штаммы ВПГ-1,
резистентные к ацикловиру. По мнению авторов, выявление прямой антигерпетической активности, а также эффективности препарата Кагоцел® в отношении мутантных резистентных к антигерпетическим препаратам штаммов ВПГ расширяет перспективы клинического применения препарата, в частности, для комбинированной терапии.
Проведенные клинические испытания эффективности препарата Кагоцел® в терапии хронической рецидивирующей герпетической инфекции показали, что под его влиянием происходит нормализация показателей системы ИФН как α-, так и β-звена у 80–86% больных. Соответственно уменьшаются продолжительность рецидива и сроки реэпителизации эрозивных элементов. В противоположность большинству других индукторов ИФН Кагоцел® стимулирует длительную продукцию ИФН: при однократном его применении ИФН циркулирует в организме пациента на терапевтическом уровне в течение 1 недели, что позволяет эффективно использовать Кагоцел® в профилактических целях.
Указанные свойства обосновывают перспективность клинического применения препарата Кагоцел® в терапии герпесвирусной инфекции.
- лечение герпетической инфекции, включая генитальный и рецидивирующий герпес;
- лечение и профилактика гриппа и других острых респираторных вирусных инфекций (ОРВИ).
Представляют интерес результаты многоцентрового когортного открытого контролируемого исследования препарата Кагоцел® при лечении генитального и лабиального герпеса, проведенного Т.И. Долгих и соавт. [4]. Критерии включения – лица обоего пола в возрасте от 18 до 65 лет с первичным эпизодом и рецидивами генитального и лабиального герпеса. Диагноз герпеса устанавливался на следующих основаниях:
- клиническая картина – наличие клинических признаков, субъективных ощущений, локализация воспалительного процесса на гениталиях и гладкой коже;
- данные лабораторных исследований – лабораторные показатели герпесвирусной инфекции (ПЦР), общий анализ крови.
Всего под наблюдением находились 146 пациентов: 63 мужчины и 83 женщины.
По данным ПЦР-исследования, ВПГ-1 был определен у 30 (20,5%) больных, ВПГ-2 – у 49 (33,5%), 1 и 2 типы ВПГ – у 23 (15,8%), ВПГ без определения типа – у 18 (12,3%), отрицательный результат был получен у 6 (4,1%) пациентов, у 20 (13,8%) больных исследований не проводилось.
Больные были разделены на 3 группы. Пациенты I группы получали только Кагоцел® (106 больных: 48 мужчин и 58 женщин), II – Кагоцел® и Ацикловир (10 больных: 4 мужчин и 6 женщин), III – только Ацикловир (30 больных: 12 мужчин, 18 женщин).
Схема лечения Кагоцелом® больных основной группы была следующей: при первичном эпизоде и рецидивах – по 2 табл. 3 раза в сутки в течение 5 дней. Больным III группы при первичном эпизоде и рецидивах назначали по 1 табл. (200 мг) Ацикловира 5 раз в день в течение 5 дней; больные II группы получали одновременное лечение Кагоцелом® и Ацикловиром по указанным схемам. Выраженность клинических признаков – боли, зуда, жжения, эпителизации эрозий, очищения от высыпаний – оценивалась в баллах до лечения, на 5-й день лечения и через 10 дней после его окончания. Сравнительный анализ клинической оценки эффективности лечения показал, что наилучшие результаты получены у больных
I и II групп: эволюция клинических проявлений завершилась через 5,6 и 3,2 дня соответственно, тогда как в III группе этот срок составил 6,4 дня. При наблюдении в течение года после лечения рецидивов не отмечалось у 22,2% пациентов, у 11% был один рецидив, у 38,9% – два рецидива и у остальных – три рецидива. При оценке безопасности Кагоцела® ни у одного больного не было отмечено побочных действий и случаев отмены препарата, а также не наблюдались неблагоприятные или серьезные неблагоприятные явления.
Другое сравнительное рандомизированное клиническое исследование эффективности лечения больных генитальным герпесом с применением Кагоцела® проведено Г.И. Мавровым и соавт. в Институте дерматологии и венерологии АМН Украины [8].
Оно включало 46 больных (24 мужчины и 22 женщины, возраст от 25 до 31 года), страдающих рецидивирующим генитальным герпесом, с давностью заболевания от 1 года до 5 лет. Частота эпизодов высыпаний на гениталиях составляла 8–15 в год.
Рандомизацию проводили с помощью генератора случайных чисел (четное число – основная группа, нечетное – группа сравнения).
В результате было сформировано 2 группы по 23 человека. Кагоцел® получали только пациенты из основной группы по следующей схеме: по 2 табл. 3 раза в сутки в течение 5 дней (на курс 30 табл.).
В качестве этиотропной терапии все пациенты получали Ацикловир по 800 мг 4 раза в сутки.
При обследовании выявлено, что состояние системы ИФН у больных на фоне рецидива заболевания характеризовалось значительными нарушениями. У 37 пациентов до начала лечения наблюдалось резкое снижение титров индуцированного ИФН-α. При этом показатели ИФН-γ находились в пределах нормы у 28 больных. До лечения показатели сывороточного ИФН были повышены у 43 пациентов. У 15 пациентов наблюдалась спонтанная продукция ИФН, которая в норме отсутствует.
В результате комбинированной терапии (Кагоцел® в сочетании с Ацикловиром) отмечались постепенная нормализация показателей ИФН-статуса и улучшение клинической картины заболевания. Показатели индуцированных ИФН-α и ИФН-γ нормализовались у 20 пациентов из основной группы (n = 23). Нормализация показателей ИФН-статуса соответствовала улучшению клинической картины заболевания у большинства больных.
У данных пациентов также сократилась продолжительность рецидива с 6,4 ± 2,3 суток (в группе сравнения) до 3,5 ± 1,8 суток (в основной группе). Частота рецидивов на протяжении 6 месяцев снизилась с 6,1 ± 2,2 до 2,2 ± 1,5 в основной группе, до 3,1 ± 2 в группе сравнения.
Таким образом, в результате лечения Кагоцелом® в сочетании с Ацикловиром продолжительность течения рецидива в среднем сокращалась с 5–8 до 3–4 суток, что подтверждалось нормализацией показателей ИФН-статуса к моменту окончания рецидива. Была показана хорошая переносимость Кагоцела® и обоснована целесообразность его включения в комплексную терапию рецидивирующего генитального герпеса.
Клинико-иммунологическая эффективность препарата Кагоцел® также подтверждается в проспективном когортном рандомизированном исследовании, проведенном Т.И. Долгих и соавт. в Омской государственной медицинской академии [5], в которое были включены 23 пациента (18 женщин и 5 мужчин) в возрасте от 17 до 49 лет с верифицированным диагнозом герпетической инфекции с проявлением лабиального (8 пациентов) и генитального (15 пациентов) герпеса и давностью заболевания от 1 года до 14 лет.
Кагоцел® назначали пациентам по 2 табл. 3 раза в день в течение 5 дней.
Подтверждение активности инфекционного процесса с уточнением этиологической расшифровки проводилось на основе наличия специфического IgA к ВПГ 1 и
2 типов и результатов прямых методов исследований лейкоцитарной взвеси и/или соскобов из очагов инфекции: «ранние» белки ВПГ-1 и ВПГ-2 выявляли в реакции иммунофлюоресценции, а ДНК – методом ПЦР.
Содержание ИФН-α и ИФН-γ (спонтанного и стимулированного фитогемагглютинином), а также компонентов комплемента С3 и С4 оценивали до назначения иммунотропной терапии и в динамике через 10 и 30 дней.
Оценка эффективности препарата показала улучшение состояния у 87,5% пациентов. Через 10 дней после лечения Кагоцелом® отмечено уменьшение клинических проявлений: болевой синдром купирован у 98% пациентов, зуд и жжение сохранялись лишь у 6% пациентов с проявлениями генитального герпеса, отек и гиперемия имели место у 4% пациентов. В 98% случаев значительно уменьшилась кратность рецидивов (0–2 раза в год вместо 3–12 раз), а длительность обострения сократилась до 3–8 дней (до лечения – 8–14 дней).
На 10-й день после проведения терапии Кагоцелом® у всех пациентов при исследовании лейкоцитарной взвеси ДНК и ранние белки вируса не определялись, что свидетельствовало о прекращении его репликации.
Установлено, что через 30 суток после окончания терапии Кагоцелом® статистически значимо изменяются все изученные показатели иммунного статуса. Продукция ИФН-α по сравнению с исходными данными возросла с 2,5 (0,6; 3,6) до 5,27 (3,25; 7,13) пг/мл, т.е. в 2,1 раза. Отмечено увеличение содержания спонтанного ИФН-γ с 21,9 (18,1; 28,1) до 33,48 (27,30; 46,15) пг/мл, а уровень стимулированного ИФН-γ увеличился с 450,5 (279,4; 740,6) до 848,34 (663,38; 1345,7) пг/мл, т.е. в 1,5 и 1,9 раза соответственно.
- препарат Кагоцел® в виде монотерапии является эффективным средством для лечения поражений, вызванных ВПГ;
- применение Кагоцела® прерывает развитие клинических проявлений герпесвирусной инфекции и позволяет снизить частоту рецидивов в 3–4 раза;
- Кагоцел® хорошо переносится пациентами, побочных явлений терапии препаратом не отмечалось.
Особо отметить следует уменьшение числа рецидивов ПГ у пациентов, получивших курс терапии препаратом Кагоцел®. Таким образом, Кагоцел® целесообразно использовать не только в качестве средства, купирующего обострение ВПГ, но и в целях профилактики заболевания, что значительно улучшает качество жизни больных, страдающих рецидивирующим простым герпесом.
Умеренная стоимость, хорошая переносимость препарата наряду с его клинико-иммунологической эффективностью (прямое противовирусное действие, повышение неспецифической и специфической резистентности организма) позволяют рекомендовать Кагоцел® для лечения и профилактики рецидивов простого герпеса.
Опоясывающий герпес или, как его еще называют, опоясывающий лишай, – одно из самых непонятных для обычного человека заболеваний вирусной природы. Его часто путают с другими видами лишая (розовый, стригущий, чешуйчатый), к которым приводят грибковые инфекции кожи, а также различные аутоиммунные процессы.
В случае опоясывающего лишая к появлению клинических симптомов и высыпаниям на коже приводит вирус герпеса 3 типа, Varicella zoster. Этот вирус также вызывает хорошо известную ветряную оспу. Выходит, что один и тот же вирус вызывает сразу два заболевания? Но как такое может быть? Давайте разбираться!
Когда организм человека встречается с вирусом Varicella zoster впервые, чаще всего развивается ветряная оспа. И обычно это происходит в детском возрасте, хотя в редких случаях заболевание может развиться и у взрослого человека. О том, что происходит, когда вирус дает о себе знать во второй раз, читайте далее. Также узнаете о том, как подобрать лекарство от опоясывающего герпеса.
Всем известно, что вирусы герпеса никогда не покидают организм, и Varicella zoster здесь не исключение. Проникая в скопления нервных клеток, он «впадает в спячку» и часто остается с нами навсегда, никак себя не проявляя. Однако, под воздействием внешних факторов вирус все-таки может «проснуться», вызывая при этом опоясывающий лишай. Также к развитию опоясывающего герпеса может привести контакт с больным ветряной оспой. Это происходит, когда человек, чаще пожилой, у которого снижены показатели иммунитета, контактирует с больным ребенком. Даже самое название вируса представляет интерес: «варицеллой» чаще называют именно ветряную оспу, а «зостер», что в переводе означает «ремень», ассоциируется с лишаем, так как характерная для этого заболевания сыпь появляется именно в области нижней части спины и живота.
Итак, мы выяснили, что опоясывающий герпес (опоясывающий лишай, герпес зостер, herpes zoster, ОГ) является вирусным заболеванием кожи и нервных тканей, которое возникает как результат реактивации вируса герпеса III типа (Human herpesvirus) подсемейства Alphaherpesviridae, семейства Herpesviridae. Встречается он примерно у 15 человек из 100 и проявляется у каждого четвертого взрослого из тех, кто ранее переболел ветряной оспой.
Важно помнить, что опоясывающий герпес у взрослых требует иного подхода к терапии: лекарства, которые педиатр рекомендует детям от ветряной оспы, не помогут. Терапию для лечения опоясывающего герпеса должен назначать врач-терапевт или врач-дерматолог после осмотра пациента и с учетом его анамнеза.
Как вирус герпеса зостер проникает в организм и как проявляется
Чаще всего первичное инфицирование вирусом, вызывающим ОГ, происходит в детском возрасте, когда ребенок заражается ветрянкой воздушно-капельным путем. После выздоровления вирус длительное время продолжает персистировать в области периферических нервных сплетений, спинальных ганглий (ограниченных скоплений нейронов) и ганглий мозга. К реактивации вируса могут привести иммунодефицитные состояния, когда естественная защита ослабевает и заболевание получает возможность «развернуться» в полную мощь.
Главные факторы, которые могут спровоцировать появление ОГ:
- возрастные изменения в организме – согласно данным статистики, это заболевание чаще всего встречается среди людей старше 50 лет;
- аутоиммунные и онкологические заболевания, в том числе сахарный диабет, лучевая и химиотерапия, состояние после тяжелых травм;
- беременность и вследствие этого повышенная нагрузка на организм;
- ВИЧ-инфекция – с ОГ сталкиваются почти 25% ВИЧ-инфицированных лиц, что в восемь раз превышает средний показатель заболеваемости пациентов среднего и старшего возраста;
- трансплантация органов, когда необходим прием иммуносупрессивных препаратов, предназначенных для искусственного угнетения иммунитета в целях предупреждения отторжения органа; i
- рецидив хронических заболеваний, затрагивающих сердечно-сосудистую систему, почки, печень и легкие;
- длительное лечение антибиотиками, цитостатиками, глюкокортикостероидами;
- частые стрессы, отсутствие достаточного отдыха, переутомление, переохлаждение или перегрев.
Опоясывающий герпес: симптомы и лечение
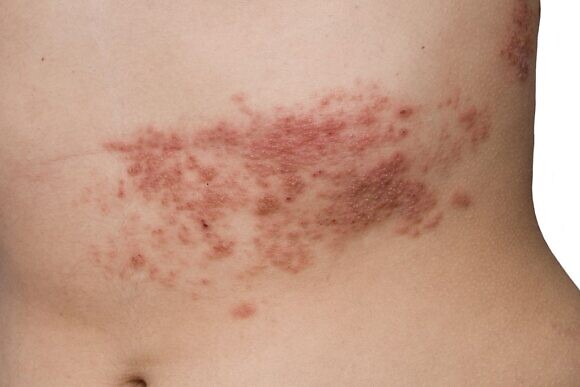
В отличие от ветряной оспы, при опоясывающем лишае не наблюдается резких вспышек заболеваемости, как в детских коллективах, также отсутствует и сезонная зависимость. Хотя некоторые ученые отмечают, что ОГ чаще встречается в теплое время года и поздней осенью. Тяжесть течения заболевания зависит от возраста. Дети, которые тоже болеют опоясывающим лишаем после перенесенной ветрянки, а также лица молодого возраста обычно переносят болезнь более благоприятно, чем пожилые люди.
Среди основных симптомов опоясывающего герпеса – кожные проявления и неврологические расстройства. Большинство инфицированных сталкивается с общеинфекционными клиническими признаками, которые проявляются в виде повышения температуры тела, головной и мышечной боли, тошноты, слабости, увеличения регионарных лимфатических узлов. Интенсивность проявления этих симптомов варьируется у каждого пациента. Продолжительность начального периода составляет примерно четыре-пять дней.
Клинические признаки ОГ могут быть похожими на плеврит, невралгию тройничного нерва и даже синдром острого живота, например, аппендицит, который требует немедленной помощи специалиста. Поэтому при общем плохом самочувствии и появлении на коже высыпаний любой природы необходимо сразу же обратиться к врачу.
В месте высыпаний перед появлением сыпи могут ощущаться легкие зуд и жжение. Потом на коже появляются розовые пятна круглой или неправильной формы, которые не склонны к слиянию, они отечные и немного приподнятые над поверхностью кожи. Затем на коже появляются везикулы с жидким серозным содержимым. Через несколько дней пузырьки подсыхают, на их месте появляются серозные корки, которые со временем отпадают и на их месте появляются пигментированные участки кожи. При правильном лечении снижается температура тела и исчезают симптомы общей интоксикации организма.
Как лечить опоясывающий герпес геморрагической, гангренозной абортивной и других форм
Кроме наиболее часто встречаемой формы опоясывающего лишая, о которой идет речь выше, также встречаются другие, которые могут выглядеть не совсем обычно и даже пугающе для неподготовленного человека. Например, при геморрагической форме везикулы заполняются кровянистым содержимым, поэтому на теле сыпь выглядит как пятна темно-коричневого цвета. Иногда везикулы не заживают бесследно, по разным причинам их дно некротизируется, после чего на коже остаются рубцы. Абортивная форма ОГ характеризуется появлением практически незаметных визуально папул (пузырьки не образуются), поэтому пациент не обращается к врачу.
При буллезной форме пузырьки на коже достаточно крупные, они могут сливаться в единый конгломерат с неровными краями. Их повреждение может приводить к инфицированию ранки, после чего может начаться гнойный процесс. В самых тяжелых случаях везикулы сливаются в обширные области, которые со временем некротизируются. В этом случае речь идет уже о гангренозной форме. Чаще эта форма развивается у пожилых людей, у лиц с язвенной болезнью и сахарным диабетом. В данном случае пациенту может быть необходима госпитализация и комплексное лечение.
Одна из главных целей лечения опоясывающего герпеса у взрослых, которые не требуют лечения в стационаре, – максимально быстрое купирование клинических симптомов заболевания (высыпаний и субъективных ощущений). Это обусловлено тем, что в зависимости от длительности цитопатического (приводящего к дегенеративным изменениям в клеточных структурах) действия вируса варицелла-зостер на клетки пораженных нервов значительно возрастает риск развития постгерпетической невралгии и других осложнений.
Возможные последствия отказа от лечения опоясывающего герпеса
ОГ приводит к многочисленным поражениям периферического и центрального отделов нервной системы. Чаще всего встречается такое осложнение, как постгерпетическая невралгия. Она проявляется в виде сильных болей, которые сохраняются или появляются через несколько недель и даже месяцев после появления первых высыпаний. Человек ощущает жгучие, резкие и приступообразные боли в области расположения сыпи. Этот симптом особенно усиливается по ночам. Особенно часто с таким осложнением болезни сталкиваются пожилые люди. Также встречаются случаи, когда вирус опоясывающего герпеса поражает брюшные мышцы и мочевой пузырь.
Кроме того, ОГ может поразить нервы, которые находятся в черепе. Подобное поражение может затронуть мозговые оболочки, что приводит к массе проблем со здоровьем. Одна из них – это поражение офтальмической ветви тройничного нерва, что неблагоприятно влияет на зрение.
Исследователи утверждают, что персистирующая, т.е. упорно протекающая и периодически вспыхивающая герпетическая инфекция может привести иммунную защиту организма к так называемой клеточной депрессии. Без поддержки в виде правильного лечения и возможности полноценно защитить себя организм может столкнуться с самыми разными осложнениями со стороны функционирования различных органов и систем.
Диагностика и правильное лечение опоясывающего герпеса у взрослых
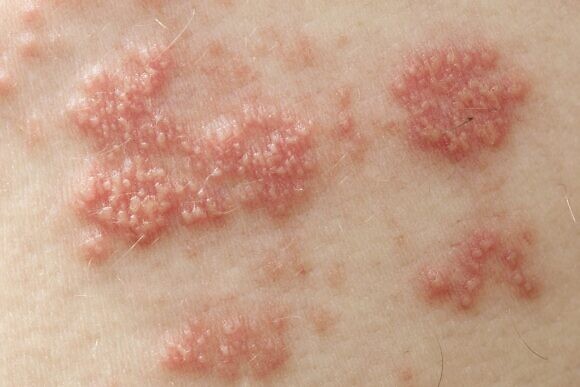
При подозрении на опоясывающий герпес необходимо обращаться к врачу-терапевту для осмотра и начала курса лечения. Также может понадобиться помочь врача-дерматолога и врача-иммунолога, а при выраженном болевом синдроме – врача-невролога.
Диагностика ОГ является преимущественно клинической, для подтверждения диагноза может потребоваться проведение лабораторных исследований. Также необходимо дифференцировать это заболевание от других похожих. Для этой цели широко применяется метод полимеразной цепной реакции (ПЦР), иммуноферментный анализ (ИФА) и иммунофлуоресцентный анализ, которые обычно не оставляют сомнений в диагнозе. Кроме того, могут потребоваться результаты общего и биохимического анализа крови, общего анализа мочи. При развитии генерализованной формы врач может дополнительно назначить анализ на ВИЧ.
Лечение ОГ чаще всего проводят амбулаторно, оно должно быть комплексным и включать как этиологические, так и патогенетические средства. Эффективность терапии во многом зависит от сроков начала лечения: чем раньше вы обратитесь к врачу и начнете лечение, тем быстрее наступит выздоровление и тем ниже будут риски развития осложнений.
Опоясывающий герпес: лечение народными средствами
Не стоит слепо доверять советам родственников и знакомых, не имеющих медицинского образования. Любые настойки, ванночки, растирания и аппликации на кожу могут принести вред, усилить зуд и расширить область появления высыпаний. Ведь во многих случаях народная медицина может не только не помочь избавиться от заболевания, но и быть небезопасной.
Опасность кроется и в том, что во время экспериментов с самолечением заболевание прогрессирует, у человека ухудшается самочувствие и могут развиться осложнения, что усложняет процесс лечения тогда, когда все же появляется решимость обратиться к врачу. Помните, что аргумент «даже если не поможет, то не навредит» в этом случае не работает. При подозрениях на опоясывающий лишай необходимо сразу же обратиться к врачу и начать лечение проверенными лекарственными препаратами.
Опоясывающий герпес: лечение, препараты и методы терапии
В настоящее время все методы лекарственного лечения и профилактики ОГ можно объединить в три основные группы, куда входят химиотерапия (прием ациклических нуклеозидов), иммунотерапия и комбинация этих двух групп, где пациент одновременно принимает химио- и иммуномодулирующие препараты.
Также применяют витамины B1, В6 и В12, аскорбиновую кислоту, рутин и при необходимости – антигистаминные препараты. При сильном болевом симптоме пациенту показан прием НПВП и анальгетиков.
Многие врачи придерживаются мнения, что приема только ациклических нуклеозидов в качестве основного лечения недостаточно, подобная монотерапия себя не оправдала. i Эти препараты наиболее эффективны только в первые 72 часа от начала развития болезни, они способны подавлять только вирусы герпеса в стадии активной репликации – процессе создания двух дочерних молекул ДНК на основе родительской молекулы ДНК. Они не оказывают влияния на те вирусы, которые уже существуют и находятся в латентном, т.е. «спящем» состоянии. Кроме того, ациклические нуклеозиды не помогают восстанавливать иммунитет.
Для лечения опоясывающего герпеса на теле пациентам необходима иммунокоррекция. Поэтому в этом случае будет уместной стратегия сочетания ациклических нуклеозидов и препаратов интерферона альфа-2b, которая признана врачами обоснованной и наиболее эффективной, что отражено в клинических и методических рекомендациях.
Интерфероны – «универсальные» бойцы, которые в отличие от антител не ориентированы на определенные патогены, а представляют неспецифический (врожденный) иммунитет и
способны бороться с любыми вирусными частицами. Интерфероны способны останавливать размножение и распространение вирусных частиц или бактерий.
Противовирусный препарат ВИФЕРОН в лечении опоясывающего герпеса
Одним из препаратов, применяемых для лечения герпеса, является ВИФЕРОН – противовирусный и иммуномодулирующий препарат, который обладает рядом уникальных фармакологических свойств.
ВИФЕРОН в своем составе сочетает рекомбинантный интерферон а-2b и комплекс антиоксидантов (витамины Е и С), в присутствии которых возрастает специфическая противовирусная активность главного действующего вещества, а также усиливается его иммуномодулирующее действие, что позволяет повысить эффективность собственного иммунного ответа организма на патогенные микроорганизмы. ii
Препарат представлен в виде ректальных суппозиториев (свечи), которые обеспечивают системное действие, то есть на весь организм в целом, а также в виде мази и геля, которые способны бороться с вирусами в «воротах» инфекции: в данном случае на поверхности кожи. Наличие как местных, так и системных форм позволяет применять препараты линейки ВИФЕРОН одновременно, усиливая тем самым эффекты проводимой терапии.
Препарат в форме свечей удобен в применении и для взрослых: он не перегружает желудочно-кишечный тракт (ЖКТ), что особенно актуально для людей, страдающих гастритом и другими заболеваниями ЖКТ, а также для тех, кто принимает большое количество таблетированных препаратов (пожилые пациенты и лица с сопутствующими заболеваниями).
Для лечения герпесвирусных инфекций у взрослых применяются свечи в дозировке 1 000 000 МЕ, у беременных женщин – 500 000 МЕ с последующими поддерживающими курсами с использованием дозировки 150 000 МЕ.

ВИФЕРОН Гель в виде полоски не более 0,5 см наносят на предварительно подсушенную пораженную поверхность 3-5 раз в день в течение 5-6 дней.
Сочетание ациклических нуклеозидов с препаратом ВИФЕРОН гарантированно сокращает сроки купирования ОГ и позволяет значительно снизить риск развития осложнений за счет комбинированного противовирусного действия (нарушение размножения вируса варицелла-зостер и препятствие прямому токсическому воздействию). iii
Как применять мазь при опоясывающем герпесе
Любая противогерпетическая мазь при опоясывающем герпесе может применяться в качестве дополнения к системной терапии, но не вместо нее.
Национальное научное общество инфекционистов и Московский научно-практический центр дерматовенерологии и косметологии рекомендуют включать препарат ВИФЕРОН в комплексную терапию опоясывающего герпеса у детей и взрослых, включая беременных женщин. iv
Справочно-информационный материал
Автор статьи
Врач общей практики
iii Халдин А.А., Васильев А.Н., Д.В. Баскаков Д.В. Виферон: опыт применения в дерматологической практике // Ремедиум Приволжье. – январь-февраль 2009. – С.20-22.
iv Потекаев Н.Н., Халдин А.А., Жукова О.В., Дмитриев Г.А. Методические рекомендации. Простой герпес. Опоясывающий герпес. Цитомегаловирусная инфекция. Московский научно-практический центр дерматовенерологии и косметологии ДЗМ. – 2019. – 32 с.

Хронический стресс влияет не только на наше настроение, но и на физическое состояние. На прием к врачу приходят пациенты с разными жалобами и одна из самых частых — появление сыпи на лице, шее и даже с переходом на грудь. Сыпь проявляется как крапивница и ее оттенок зависит от тона кожи: от красного до фиолетового. Такую сыпь и называют стрессовой. Более того, при уже существующих кожных болезнях, стресс — это причина рецидива и ухудшения симптомов.
Стрессовая сыпь
В 2018 году было проведено исследование с участием студентов-медиков. Результаты показали, что обучение сопровождается высокими нагрузками и стрессом, что и стало причиной развития кожных болезней с характерными симптомами в виде сыпи.
У части студентов стрессовая сыпь проявлялась в виде крапивницы чаще на лице, груди и шее. Хотя выраженной закономерности уровня стресса и выраженности сыпи не было обнаружено. У студентов, подвергшихся стрессу, отмечались более частые обострения экземы, псориаза, розацеа и других кожных болезней. Известно, что характерным симптомом являются кожные высыпания.
Проявления стрессовой сыпи
Стрессовая сыпь может выглядеть по-разному, и все зависит от тона кожи: красные, темные или же фиолетовые пятна, зудящие и выступающие над поверхностью кожи. От чего зависит размер поражения неизвестно, но, в некоторых случаях, очаги сливаются между собой и локализуются не только на лице, но и переходят на шею и грудь.
Сложнее определить причину и тип сыпи при хронических кожных болезнях, ведь симптоматика схожа. Нередко на фоне обострения основного заболевания кожи происходит резкое ухудшение состояния, что и говорит о присоединении стрессовой сыпи.
Почему появляется такая сыпь?
При стрессе в организме вырабатывается гормон – кортизол. При его большой концентрации и постоянной выработке, он негативным образом влияет на иммунную систему, что делает организм восприимчивым к болезням и аллергенам. Эти условия и обеспечивают обострение хронических болезней, в том числе и кожных.
Уже на фоне стрессовой сыпи кортизол ухудшает симптомы и провоцирует обострение хронических кожных заболеваний.
Другие виды высыпания на лице
Причины, по которым появляются высыпания на коже разнообразны. И, в первую очередь, врач исключает хронические дерматологические болезни, а уже потом рассматривает иные причины.
Первоначально врачи исключают следующие патологии:
Розацеа
В основном, сыпь локализуется в области лица. К числу характерных симптомов относят: покраснение, которое внешне похоже на солнечный ожог. Некоторые люди с розацеа страдают от жжения, зуда и покалывания.
Атопическая экзема
Хроническое заболевание кожи, которое характеризуется периодами обострений и ремиссии. Обычно симптомы сводятся к сухости, шелушению, покраснению и зуду.
Псориаз
Это хроническое заболевание кожи, при котором характерно образование покраснений, шелушений и белых чешуек.
Потница
Формируется при значительном потоотделении из-за чрезмерного раздражения кожи.
Контактный дерматит
Основная причина болезни – действие определенного аллергена, которым может быть: косметика, пища и др.
Опоясывающий герпес (лишай)
Это весьма серьезное инфекционное заболевание, которое характеризуется появлением сыпи на одной части тела по ходу определенного нерва. Заболевание имеет серьезное течение и яркую клиническую картину. На первое место выходит боль, выраженный зуд и, в последнюю очередь, пациента интересует сформировавшаяся сыпь.
Какое лечение необходимо?
Лечение стрессовой сыпи чаще проходит в домашних условиях, однако консультация врача нужна обязательно. Только доктор сможет провести диагностику, исключить иные причины появления сыпи, которые требуют серьезного лечения.
В 2019 году было опубликовано исследование, в котором было доказано, что кокосовое масло обладает противовоспалительным и спазмолитическим действием и, следовательно, его можно рассматривать как средство лечения и профилактики кожных высыпаний.
Алоэ вера уменьшает зуд. Снять раздражение и улучшить состояние кожи поможет холодный компресс. Масло ромашки обладает антиоксидантным, противомикробным и противовоспалительным действием. Это масло по нескольку капель можно добавлять в уходовую косметику, которая используется ежедневно.
Для снятия зуда и отека рекомендованы безрецептурные антигистаминные препараты, а также лосьоны с каламином для облегчения симптомов сыпи.
Однако симптоматического лечения недостаточно, нужно позаботиться об устранении основной причины, то есть хронического стресса. В этом помогут медитативные практики, поддержка психолога и др. В сложных случаях может потребоваться прием лекарственных препаратов, но их рекомендует исключительно врач.
Когда необходима помощь врача
Стрессовая сыпь обычно проходит в течение нескольких дней. Однако при появлении симптомов консультация врача обязательна для исключения других причин появления кожной сыпи, в том числе, и инфекционной природы.
Поводом для посещения врача будет ухудшение состояния, то есть увеличение площади поражения, присоединение других симптомов, например, повышения температуры.
Затруднение дыхания, глотания, отек губы – повод немедленно вызвать скорую помощь. Это может свидетельствовать о развитии аллергической реакции, представляющей угрозу для здоровья и жизни человека.
Резюме
Хронический стресс – причина появления сыпи на лице, которая выглядит как крапивница. Если уже диагностировано хроническое заболевание кожи, то стресс — это причина обострения. Поэтому для точного определения причины появления сыпи, необходима консультация врача, который и назначит соответствующее лечение.
Несмотря на существующие методы лечения стрессовой сыпи, при частом появлении симптомов, нужно пройти полное обследование и выявить причину. Только на этих условиях может быть разработана тактика лечения, которая принесет результаты.
1. Gada A. Ben Saif, Hala M. Alotaibi, Abdullatif A. Alzolibani. // Linking Psychological Stress to Skin Symptoms in Medical Students. // J Saudi Med.// Jan, 2018.39(1)
2. Sandip R. Varma, Tiyagarajan O. Shivaprakasam, Ilavarasu Arumugam. // In Vitro Anti-Inflammatory and Dermal Properties of Extra Virgin Coconut Oil. // Journal of Traditional and Complementary Medicine. // January, 2019. 9(1).
Читайте также:

