Ингибиторы 5-альфа-редуктазы при акне
Обновлено: 26.04.2024
Рассмотрены современные препараты и методики, с помощью которых можно успешно бороться с различными проявлениями акне, вызванными синдромом гиперандрогении у женщин.
Рассмотрены современные препараты и методики, с помощью которых можно успешно бороться с различными проявлениями акне, вызванными синдромом гиперандрогении у женщин.
Многочисленные исследования, проведенные в нашей стране и за рубежом, выявили широкую распространенность гиперандрогенных состояний среди женщин репродуктивного возраста. По данным литературы, у 10–30% женщин в мире имеются те или иные признаки синдрома гиперандрогении (СГА). Согласно современным представлениям, СГА характеризуется симптомокомплексом, обусловленным патологией биосинтеза, транспорта и метаболизма андрогенных гормонов. Кожа является главным звеном метаболизма половых стероидных гормонов. Действие андрогенов осуществляется через специфические андрогеновые рецепторы, которые обнаруживаются в различных андрогензависимых тканях. Основные мишени для половых гормонов в коже – эпидермис, волосяные фолликулы, сальные железы, меланоциты, фибробласты. Под воздействием андрогенов усиливается дифференцировка и митотическая активность клеток эпидермиса [1, 2].
Причиной гиперандрогении (ГА) могут быть различные органические или функциональные нарушения деятельности эндокринных желез (яичников, надпочечников), заболевания гипоталамо-гипофизарной системы (болезнь Иценко – Кушинга, ожирение), сахарный диабет 2 типа, шизофрения, применение лекарственных средств (анаболических стероидов, транквилизаторов, противотуберкулезных препаратов, циклоспорина, глюкокортикоидов), повышение активности фермента 5-альфа-редуктазы в органах-мишенях, снижение синтеза полового секс-стероид-связывающего глобулина (ПССГ) печенью. В развитии СГА большую роль играет генетическая предрасположенность [2, 3].
Юношеские угри (acne vulgaris) относятся к одному из наиболее распространенных заболеваний кожи молодого возраста, встречаются у 85% юношей и девушек в возрасте от 12 до 24 лет. Пик заболеваемости, как правило, приходится на 15–16 лет. Однако в последние годы растет число женщин, у которых дебют угревых высыпаний приходится на 25 лет и старше. Так, в США с 1990 по 1999 г. средний возраст больных акне увеличился с 26,5 до 40,5 лет. Проявление угревых высыпаний и их торпидное течение в старших возрастных группах классифицируется как acne tarda. Было выявлено, что в подростковом возрасте заболеваемость акне практически одинакова среди обоих полов, в то время как поздние угри существенно чаще встречаются у женщин [5–8]. По данным Е.А. Аравийской и соавт. [7], примерно 20% женщин отмечают регулярное появления угрей в области подбородка за 2–7 дней до начала менструального цикла.
Известно, что развитие и течение дерматоза во многом зависит от семейной (генетической) предрасположенности, а также типа, цвета кожи, национальных особенностей. Акне, или угревая болезнь (УБ), является генетически обусловленным наследственным мультифакториальным заболеванием с высоким семейным накоплением (до 50%). Генетические нарушения определяют течение заболевания и детерминируют тип секреции, количество, размеры, чувствительность сальных желез к различным агентам [5].
В патогенезе УБ ведущее значение отводится четырем факторам. Инициальным звеном является наследственно обусловленная ГА, которая может проявляться в виде абсолютного увеличения количества андрогенов овариального или надпочечникового происхождения в крови и при экскреции с мочой. ГА может иметь функциональный (синдром поликистозных яичников, неклассическая форма врожденной дисфункции коры надпочечников) или опухолевый генез. Кроме повышения уровня андрогенов, ГА может иметь рецепторную форму, связанную с повышенной активностью 5-альфа-редуктазы 1-го типа, которая переводит тестостерон в более активный метаболит дигидротестостерон. Последний является непосредственным стимулятором пролиферации и созревания себоцитов [9, 10].
Под действием гормональной стимуляции увеличивается объем кожного сала, в котором снижается концентрация незаменимой альфа-линоленовой кислоты – основного регулятора дифференцировки кератиноцитов протока сально-волосяного фолликула (СВФ) – и увеличивается экспрессия фермента трансглутаминазы. Это приводит к преобладанию процессов дискератоза и пролиферации над десквамацией эпителия СВФ, что в конечном итоге ведет к фолликулярному гиперкератозу и закрытию протока СВФ. Клинически это проявляется появлением открытых и закрытых комедонов, в зависимости от уровня закупорки СВФ [7, 11].
Обтурация сально-гипертрофической пробкой протока СВФ создает благоприятные условия для размножения факультативных анаэробов Propionibacterium acnes и Propionibacterium granulosum, а также других представителей сапрофитной и условно-патогенной микрофлоры (Staphylococcus epidermidis, Staphylococcus aureus, Pityrosporum ovale). Антигены микроорганизмов привлекают к СВФ из периферической крови фагоциты и нейтрофилы, которые продуцируют интерлейкины, стимулируют систему комплемента. Эти провоспалительные цитокины активируют фермент циклооксигеназу, в результате чего из арахидоновой кислоты образуется главный медиатор воспаления – лейкотриен В4 (ЛТВ4). ЛТВ4 стимулируют нейтрофилы, Т-лимфоциты, моноциты и эозинофилы, с последующим высвобождением ими гидролитических ферментов и монооксида азота. Это вызывает разрушение стенки сальной железы с выходом ее содержимого в дерму, что и обусловливает воспалительную реакцию в виде образования папул, пустул, узлов и кист. Таким образом, высыпания при угревой болезни представлены акне-элементами в разной стадии эволюционного развития и характеризуются ложным полиморфизмом. Разрешение папул, пустул и комедонов проходит бесследно. Узлы и кисты оставляют после себя очаги депигментации, келоидные, гипотрофические или гипертрофические рубцы [11, 12].
При оценке степени тяжести акне (СТА) наиболее часто используется классификация Американской академии дерматологии: I СТА характеризуется наличием комедонов и до 10 папул; II СТА – комедоны, папулы, до 10 пустул; III СТА – комедоны, папулы, пустулы, до 5 узлов; IV СТА отличается выраженной воспалительной реакцией в глубоких слоях дермы с формированием множественных болезненных узлов и кист.
Единственным недостатком этой классификации является отсутствие степеней тяжести заболевания в зависимости от распространенности процесса. Поэтому, помимо классического деления с учетом степени тяжести акне, целесообразно разделять пациентов на подгруппы в зависимости от локализации и распространенности процесса (А, В, С): А – при локализации высыпаний в одной анатомической области, В – при локализации высыпаний в двух анатомических областях (например, лицо и спина), С – при вовлечении в патологический процесс трех и более анатомических областей. Данная классификация наиболее полно отражает степень вовлеченности кожного покрова в патологический процесс.
Клинические проявление акне у женщин широко варьируют. Они отличаются степенью выраженности фоновой гиперфункции сальных желез, распространенностью процесса, количественным соотношением воспалительных (папул, пустул) и невоспалительных (комедонов) элементов, а также наличием проявлений постакне (рубцов и пигментных пятен). Среди клинических форм у пациенток с УБ преобладает папуло-пустулезная форма – 70–80% случаев. Комедональные и конглобатные угри встречаются у 10–15% больных [4, 5].
Изменения кожи и ее придатков сопровождаются выраженными косметическими дефектами и локализуются, как правило, на открытых участках кожи, что негативным образом отражается на психоэмоциональной сфере пациенток, вызывая тревогу, депрессию, существенно снижая самооценку и способствуя развитию дисморфофобии, что, в свою очередь, приводит к различной степени выраженности социальной дезадаптации, ограничению в выборе профессии, личной и семейной неустроенности и значительному снижению качества жизни. Ряд исследователей отмечают, что женщины с акне более психологически уязвимы по сравнению с мужчинами, при этом было установлено, что среди лиц с акне отмечается большое количество (64%) неработающих женщин [13, 14].
Исследования, проведенные отечественными дерматологами, показали, что психоэмоциональные расстройства (ПЭР) различной степени выраженности наблюдаются у 41,3% больных с угревой болезнью и значительно чаще встречаются у женщин [15, 16]. В клинической картине преобладают расстройства депрессивного характера, в ряде случаев сочетающиеся с тревожной, ипохондрической, астеноневротической симптоматикой. У женщин отмечается более высокий уровень тревожности по сравнению с мужчинами. Было установлено, что субъективная оценка больными степени тяжести поражения кожи четко коррелировала с выраженностью ПЭР и в большинстве случаев была существенно завышена по отношению к объективной степени тяжести акне. У пациентов с УБ описан весь спектр пищевых психопатологических расстройств – от нервной анорексии до нервной булимии. При обследовании 480 пациентов с различными дерматозами самый высокий уровень депрессии как реакции на кожное заболевание был выявлен у пациентов, страдающих тяжелым псориазом и угревой болезнью. 5,6% больных псориазом и 7,2% пациентов с акне высказывали суицидальные мысли, что значительно превышало распространенность суицидальных идей среди пациентов в общемедицинской практике [15, 16].
Таким образом, дерматологу при обследовании женщин с УБ необходимо тщательно собрать анамнез, обращая внимание на семейную отягощенность, связь появления первых признаков и обострений заболевания с менструальным циклом. Необходимо выяснить особенности менструального цикла пациентки, а также влияние беременностей и родов на течение дерматоза. Следует тщательно расспросить о сопутствующих заболеваниях, особенно нейроэндокринно-обменного характера, употребляемых продуктах и принимаемых лекарственных средствах. При осмотре следует обратить внимание не только на локальные проявления заболевания, но и отметить особенности строения тела, тип оволосения, степень развития вторичных половых признаков, оценить наличие избыточной массы тела у пациентки, так как нередко ожирение сопровождает ГА, а сама жировая ткань может быть источником образования андрогенов.
Для исследования дерматологического статуса пациенток с акне помимо клинической оценки степени тяжести заболевания целесообразно использовать неинвазивные дерматологические методы исследования, которые не только помогают объективизации патологического процесса, но и служат критерием эффективности и безопасности терапии при УБ. Рекомендуется использовать следующие методы: себометрию, рН-метрию, корнеометрю, а также исследование микрорельефа кожи.
Для выявления психоэмоциональных нарушений целесообразно провести тестирование по госпитальной шкале тревоги и депрессии HADS, разработанной A.S. Zigmond и R.P. Snaith в 1983 г. для оценки выраженности тревожно-депрессивной симптоматики в общей медицинской практике. Для определения качества жизни следует провести исследование по Дерматологическому индексу качества жизни (ДИКЖ), русифицированному Н.Г. Кочергиным (2001 г.), – варианту индекса Finlay, оценивающего влияние дерматологического заболевания на качество жизни больного.
Лечебная тактика при акне у женщин зависит от стадии, распространенности клинических симптомов заболевания, наличия патологических изменений в гормонально-эндокринном статусе. При выборе терапии необходимо учитывать возраст пациентки и сопутствующую патологию. Современные подходы к терапии включают назначение различных системных и наружных препаратов, влияющих на различные звенья патогенеза УБ. Системная терапия назначается при III–IV СТА, при упорном течении процесса при II СТА, а также при распространенности высыпаний и отягощенности гормонально-эндокринного статуса при любой стадии акне.
При I СТА проводится только местная терапия. Назначаются топические ретиноиды (Дифферин), антибактериальные и противовоспалительные средства (Базирон АС, Зинерит), препараты азелаиновой кислоты (Скинорен), комбинированные препараты (Изотрексин, Клензит-С). При этом приоритет отдается топическим ретиноидам и бензоил пероксиду. При II СТА назначают местные средства в сочетании с системными антибиотиками (доксициклин, тетрациклин), при упорном течении – комбинированные оральные контрацептивы (КОК) с антиандрогенным эффектом (Джес, Ярина, Диане-35, Жанин). Следует отметить, что среди всех перечисленных КОК только Джес может быть назначен дерматологом самостоятельно, так как в показаниях к препарату указывается лечение угревой болезни средней степени тяжести. При тяжелых формах акне у женщин при противопоказаниях к назначению КОК применяются системные ретиноиды – препараты Роаккутан, Акнекутан. Установлено, что степень выраженности положительных результатов терапии тяжелых форм акне системными ретиноидами является дозозависимой.
Длительный прием препарата приводит к выраженному подавлению активности сальных желез, что гистологически подтверждается уменьшением их размеров. Для достижения наибольшей эффективности лечения, увеличения продолжительности ремиссий и снижения частоты рецидивов оптимально использование курсовой дозы 120–150 мг/кг. При наличии гормонально-эндокринных нарушений на любой стадии заболевания (при отсутствии противопоказаний) назначаются КОК с антиандрогенным эффектом, при необходимости – в комбинации с топическими противоугревыми средствами. Для достижения выраженного терапевтического эффекта следует назначать КОК на длительный срок – от 6 месяцев до года, изотретиноин необходимо применять в течение 3–6 месяцев, системную антибактериальную терапию нужно проводить не менее месяца. В качестве дополнительной терапии необходимо использовать средства лечебной косметики, которые являются важным лечебным компонентом терапевтической программы ведения пациенток с УБ. При выборе косметических средств следует учитывать данные аппаратных методик, позволяющих оценить степень выраженности жирности кожи и ее увлажненности, рН кожи, а также учитывать основу препарата и тип кожи пациентки.
После удачного купирования воспалительных проявлений акне врачу часто приходится сталкиваться с трудностями в коррекции постакне. Для разрешения дисхромий успешно применяются: лечебный массаж (курс 15 процедур) в сочетании с электрофорезом с витамином С; криомассаж (5–6 мин, 2–3 раза в неделю, курс 10–15 процедур), мезотерапия, пилинги – как поверхностные с альфа-гидроксикислотами, так и глубокие с трихлоруксусной кислотой. Хороший синергический эффект дает совместное использование вместе с поверхностными и глубокими пилингами азелаиновой кислоты в качестве препилинговой подготовки и постпилингового ухода, особенно у пациентов со смуглой кожей, с целью профилактики гиперпигментации и обострений акне.
Для коррекции атрофических рубцов применяются химические пилинги (чаще срединные), микродермабразия, лазерная шлифовка, инъекции филлеров, криотерапия, мезотерапия, эффективны комбинированные методы терапии. Для лечения гипертрофических рубцов используют очаговое введение кортикостероидов; электрофорез с кортикостероидами, лидазой, коллагеназой; букки-терапию; фонофорез с Контрактубексом, Мадекасолом; криодеструкцию; мазевую терапию (Медерма, Куриозин, Контрактубекс); хирургическое иссечение рубцов при большой площади поражения.
Таким образом, в арсенале врачей сейчас имеется достаточное количество современных высокоэффективных, безопасных препаратов и методик, с помощью которых можно успешно бороться с различными проявлениями акне у женщин. Однако следует помнить, что перед назначением противоугревой терапии пациентку необходимо тщательно обследовать с учетом не только дерматологического, но и эндокринно-гинекологического статуса. При лечении заболевания следует также учитывать наличие психоэмоциональных нарушений у большого процента пациенток с акне, редукция которых может служить одним из критериев эффективности проводимой терапии. Лечение пациентов с угревой болезнью – это забег на длинную дистанцию. Конечный результат лечения во многом зависит от установления доверительных отношений между врачом и пациентом, индивидуального подхода в каждом клиническом случае и рационально подобранной противоугревой терапии.
Среди различных заболеваний, сопровождающихся акне или акнеподобной сыпью, наиболее распространенными являются полиморфные себорейные акне. Этот термин отражает характерные клинические особенности, связанные с изменениями в фолликулярных воронках и са
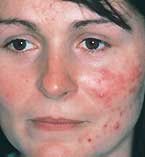
Среди различных заболеваний, сопровождающихся акне или акнеподобной сыпью, наиболее распространенными являются полиморфные себорейные акне.
Этот термин отражает характерные клинические особенности, связанные с изменениями в фолликулярных воронках и сальных железах, которые происходят при усиленном тканевом андрoгенном ответе. Ключевыми звеньями данного процесса считают гиперкератинизацию и повышение адгезии активированных фолликулярных кератиноцитов, увеличение продукции сальных желез, активизацию анаэробной липофильной резидентной микрофлоры и развитие воспаления в области сальных протоков и фолликулярной воронки (см. таблицу 1).
- Гиперкерати-низация и аномальная дифференцировка фолликулярных кератиноцитов: повышение адгезии фолликулярных кератиноцитов ретенционный фолликулярный гиперкератоз
- Увеличение сальных желез, повышение секреции кожного сала в анаэробных условиях облитерации воронки
- Повышение пролиферации и липолитической активности резидентной микрофлоры сальных протоков; хемоаттрактанты (микробные ферменты, жирные кислоты)
Такие изменения столь часто отмечаются в пубертатном периоде, что их относят к числу ранних признаков полового развития и при легких проявлениях рассматривают как физиологическое состояние («физиологическое акне»), а не патологию. Примерно в 80% случаев акне определяются как «минимальные», «физиологические», в 15—20% — как «клинические», т. е. требующие лечения. Клинические акне классифицируются как болезнь (нозологическая форма), чем и объясняется частое употребление термина «угревая болезнь» (хотя он не принят в международной номенклатуре).
Клинически выраженные и тяжелые полиморфные себорейные акне классифицируются как мультифакторное заболевание со свойственной мультифакторной патологии клиническим полиморфизмом. В классификациях акне, учитывающих возрастные и клинико-морфологические критерии, перечисляется более 20 вариантов заболевания. На формирование этих форм акне оказывают влияние многочисленные генетические и негенетические факторы, которые могут изменить нормальный тканевой ответ периферических гормонозависимых органов-мишеней, усилить андрогенную стимуляцию, внести вклад в индивидуальный иммунный ответ. Эти факторы сильно варьируют в зависимости от пола пациента.
Поэтому вопросы диагностики, прогноза и выбора лечения у пациентов женского и мужского пола необходимо рассматривать отдельно.
Различия, касающиеся частоты возникновения и особенностей течения акне у девочек и мальчиков, проявляются рано, уже при неонатальных и младенческих, а затем при пубертатных акне. Комедональные акне и милиумы у девочек появляются раньше, с началом полового развития (в препубертате за два-два с половиной года до менархе), раньше, чем у мальчиков, достигают пика частоты и скорее исчезают — у здоровых девочек без генетического предрасположения к периферической гиперандрогении. После начала циклического функционирования яичников и особенно с третьей-четвертой декады жизни отличия и особенности течения акне у лиц женского пола становятся заметнее, что связано с разными эпидемиологическими факторами, с дисфункциями репродуктивных органов и нейроэндокринной системы, а также с особенностями косметического ухода за кожей у женщин.
Многие термины, употребляющиеся в литературе и использующиеся в практической диагностике, отражают общепринятые представления о связи постювенильных акне и акне взрослых с гормональными влияниями у женщин: «предменструальные акне», «постменструальные акне», «постменопаузальные акне», «гиперандрогенные акне» у женщин, «поздние акне у женщин», «эндокринные акне у женщин». Появился термин «гиперандрогенная дермопатия у женщин», в числе кожных симптомов которой фигурируют себорейные полиморфные акне, себорея, гирсутизм, гиперандрогенная алопеция, в редких случаях пигментно-сосочковая дистрофия кожи (чернеющий акантоз). Из числа эндокринных акне у женщин наиболее пристальное внимание в последнее время уделяется синдрому поликистозных яичников: заболеванию с гиперандрогенией овариального генеза, связанному преимущественно с нарушением гонадотропной функции гипоталамо-гипофизарной системы. У 30% женщин это заболевание дебютирует гиперандрогенными акне (С. Л. Гомболевская, 1997). Кроме того, дерматологи стали больше обращать внимание на связь постювенильных акне с поздней или мягкой формой акне среди женщин, себореей и гирсутизмом с помощью теста с ЛКТГ-стимуляцией для выявления дефицита 21-гидроксилазы.
Большое значение при поздних акне у женщин придают геперпролактинемии (Н. М. Рудных, 2000). Основным клиническим проявлением ее является синдром персистирующей галактореи-аменореи, которому могут сопутствовать ожирение, гирсутизм и акне, а у некоторых больных — нарушения функции щитовидной железы. К числу причин патологической гиперпролактинемии относят аденомы гипофиза, гипоталамический синдром пубертатного периода, нарушения дофаминергического контроля секции ЛГ и пролактина, ятрогенные формы гиперпролактинемии (на фоне приема эглонила, фенотиазинов и других психотропных препаратов, морфина, циметидина, эстрогенов и проч.), нейроэндокринные заболевания, фиброзно-кистозную мастопатию и др.
В ряде ранних исследований, посвященных причинам возникновения акне и себореи у женщин, анализировалось значение «себотрофических стимулов» питуитарного происхождения, повышающих скорость кожного саловыделения у женщин, в том числе на фоне увеличения «маммотрофических гормонов» при опухолях молочных желез, иногда во время беременности, после родоразрешения, при вскармливании детей грудью, при этом рассматривалась роль повышения пролактина и меланоцитстимулирующего гормона как «себотрофических гормонов». Так, А. Аленькина при обследовании 62 беременных женщин с разнообразными кожными поражениями отмечала у пяти из них появление акне во время беременности (2003).
В специальной литературе неоднократно отмечалось, что кроме хронических заболеваний с гиперандрогенией появление и рецидивы акне у женщин могут вызывать и менее значительные и кратковременные изменения эндокринного баланса, связанные с менструальным циклом, с функциональной гиперпролактинемией, употреблением контрацептивов с большим количеством прогестеронов или прекращением использования оральных контрацептивов, с приемом анаболических стероидов и ряда других лекарств, с временной дисфункцией гипоталамуса, переходящей функциональной гиперплазией с усилением секреции надпочечников и половых желез; причем такие временные акне могут усугубляться вследствие длительного использования комедогенной косметики. Следует отметить, что сейчас чаще встречаются случаи допинговых (боди-билдинговых) акне у молодых женщин, принимающих анаболики с витаминами, а также акне, спровоцированные продолжительной инсоляцией.
В классификациях акне выделяют группу тяжелых деструктивных форм и редких синдромов с внекожной патологией. У женщин такие формы встречаются реже, чем у мужчин. Среди пациентов, обследованных Т. А. Сысоевой, наблюдается женщина 20 лет с акне и индуративным отеком лица. Причины возникновения таких синдромов недостаточно изучены.
Во многих случаях персистирующие постювенильные акне и поздние акне не сопровождаются эндокринными заболеваниями и гиперандрогенемией. Такие формы рассматривают как идеопатические акне, т. е. не имеющие отношения к внекожным причинам и заболеваниям других систем. Ранее их связывали с семейной десквамацией, себорейным диатезом, особой конституциональностью, кератозом Дарье. В настоящее время их относят к периферическим формам кожной гиперандрогении, которые характеризуются увеличением чувствительности рецепторов к андрогенам в клетках сальных желез и в фолликулярных кератиноцитах или же повышенной активностью 5-альфа-редуктазы, обеспечивающей периферическое превращение тестостерона в дигидротестостерон, являющийся наиболее сильным андрогеном для кожных клеток. В пубертатном периоде происходит не только увеличение секреции половых гонадотропинов и половых гормонов, но и повышается чувствительность рецепторов в периферических гормонозависимых тканях, активизируется превращение тестостерона в дигидротестостерон до конца полового созревания. Время стабилизации этих процессов, уровень чувствительности рецепторов и активности ферментов стероидного метаболизма в коже могут варьировать. Разная экспрессивность и аллельные вариации генов, детерминирующих развитие сальных желез, их функциональную способность, активность ферментов, аффинность рецепторов, могут играть роль в количественных вариациях кожного фенотипа и определяют у одних пациентов возникновение преходящих, а у других — персистирующих клинических форм акне. Поэтому считают, что наследственность, семейные проявления акне являются существенными прогностическими признаками в отношении дальнейшего течения акне после окончания полового созревания (W. N. Meigel, 1999).
Частота выявления эндокринной и гинекологической патологии в разных лечебных учреждениях неодинакова и зависит от возраста пациентов и профиля учреждения. Среди девочек с акне при многопрофильном тщательном обследовании, проведенном в детской поликлинике, в единичных случаях обнаруживали менструальные дисфункции. (И. Е. Юдина, 2003). В более старшей группе — среди подростков и девушек, обращавшихся с более тяжелыми формами акне в РМАПО, Т. А. Сысоева (2003) у 36 из них (8%) выявляла патологию репродуктивной и эндокринной системы, в том числе кисты яичников, сальпингоофорит, менструальные дисфункции (у 24,4% по гипоменструальному типу), у одной больной синдром поликистозных яичников, еще у одной — позднюю форму врожденной адреналовой гиперплазии. В косметологическом отделении многопрофильной поликлиники у практически здоровых женщин с акне легкой и умеренной степени тяжести при обследовании обнаруживалась мастопатия, патология щитовидной железы, временные отклонения гормональных показателей, у 6,6% диагностированы гиперандрогенные акне, у 8,86% — предменструальные акне (М. В. Камакина, 2002).
Практика показывает, что пациентки с постювенильными и поздними акне, а также девочки с тяжелыми резистентными акне должны тщательно обследоваться у дерматолога, гинеколога и эндокринолога (см. таблицу 2). Выявленные нарушения и уточненный диагноз с учетом этиопатогенеза акне определяют прогноз и план лечебных мероприятий (см. таблицу 3).
- Естественный физиологический регресс с началом взрослого возраста, бесследное исчезновение акне легкой и умеренной степени тяжести.
- Рубцовые постакне после регрессии активных юношеских акне, ксероз, себорея, синусы, тракты.
- Формирование нейрогенных экскориированных акне молодых девушек на фоне полиморфных себорейных акне.
- Персистирующие юношеские акне (постювенильные акне) до 25 (30) лет.
- Непрерывное течение с переходом в акне взрослых или ремиссия до начала акне взрослых, которые не исчезают на четвертой-пятой-шестой декаде жизни (поддерживают эндокринные или периферические факторы).
- Постепенное утяжеление акне после менархе у девочек с начинающимся синдромом поликистозных яичников или поздней мягкой формой врожденной гиперплазии надпочечников, формирование гиперандрогенной дермопатии.
- Обострения предменструальных акне при циклическом процентном повышении уровня прогестерона в течение ряда лет у молодых женщин.
- Обострение акне при транспортной форме гиперандрогенемии (снижение образования в печени белка, связывающего половые гормоны или нарушение связывания с ним андрогенов), чему способствуют заболевания печени, ожирение, снижение андрогенов.
- Формирование идиопатических акне при конституциональной (генетической) рецепторной форме периферической гиперандрогении.
- Периферическая гиперандрогения вследствие усиления стероидного биосинтеза в коже, повышения активности 5-альфа-редуктазы, увеличения уровня дигидротестостерона.
- Экзогенное провоцирование акне и переход в более тяжелую форму из-за использования косметических акнегенных средств, медикаментов, под влиянием физических воздействий.
Выбор средств и тактика лечения акне у женщин и мужчин тоже имеют свои отличия. Гормональное лечение оральными контрацептивами назначается только женщинам, тогда как самый мощный из используемых у мужчин системных препаратов — роаккутан — применяется у женщин лишь в исключительных случаях. При лечении акне у женщин реже используются системные антибиотики. При выборе наружной терапии учитываются потребности женщины в привычном косметическом уходе за кожей лица, использовании макияжа, а также нежелание пациенток пользоваться такими наружными средствами, которые могут вызвать ирритантный дерматит (раздражение с краснотой и шелушением), пусть даже на короткое время.
Мы назначаем системные антибиотики, преимущественно юнидокс солютаб, курсом в 10 дней только при выраженной пустулизации.
При особых формах акне у женщин применяется специальное лечение: глюкокортикоиды в комбинации с антиандрогенами внутрь (при врожденной гиперплазии надпочечников), кетотифен (при индуративном отеке лица).
В наружной терапии приоритет отдается современным патентованным препаратам: при комедональной форме (более выраженной у детей и подростков) — дифферину, скинорену; при пустулизации — базирону АС, далацину-Т; при индуративных элементах у женщин с поздним акне наиболее выраженным действием обладает топический спиронолактин.
Поскольку лекарственные средства патогенетического действия нередко имеют серьезные побочные эффекты, обязательным компонентом лечения является назначение адъювантных препаратов. В своей практике мы использовали гепатопротекторы и литовит с цеолитами, имеющий селективные сорбентные и ионообменные свойства. Лечебную косметику мы тоже рассматриваем как обязательное дополнение к патогенетической антиакнефармакотерапии. Патентованные фармакологические препараты нередко вызывают раздражение, хотя и кратковременное. Поэтому успокаивающие чувствительную и раздраженную кожу косметические средства необходимо применять в процессе патогенетической наружной терапии, особенно при комбинированном лечении базироном АС и дифферином. При раздражении кожи после медикаментов мы назначали апезак (реструктурирующая эмульсия); для увлажнения и улучшения текстуры кожи — гифак плюс (крем и очищающий гель); для рассасывания индуративных акне — патчи (пластыри) локально, на элементы.
Таким образом, выбор препаратов и тактика лечения женщин с полиаморфными акне основаны на следующих положениях (см. таблицу 4).
ВГМУ, Профессорская клиника Юцковских, Владивосток
Профессорская клиника Юцковских, Владивосток
Владивостокский государственный медицинский университет
Андрогензависимые синдромы кожи у женщин: роль антиандрогенной терапии на современном этапе
ВГМУ, Профессорская клиника Юцковских, Владивосток
ВГМУ, Профессорская клиника Юцковских, Владивосток
Профессорская клиника Юцковских, Владивосток
Владивостокский государственный медицинский университет
Одной из сложных задач современной дерматологии и косметологии остается лечение андрогензависимых синдромов кожи. Синдромы гиперандрогении (ГА) часто служат причиной психологического дискомфорта и отрицательно влияют на качество жизни женщин. Синдромы ГА у женщин являются частыми причинами психологического дистресса. Внешние проявления избытка андрогенов отмечаются у 10—30% женщин в популяции и становятся существенным косметическим дефектом, отражающимся на нервно-психическом статусе женщины, приводя к раздражительности, депрессивным состояниям, снижая качество жизни и обусловливая социальные проблемы в виде ограничений в выборе профессии и сложностей в трудоустройстве, снижая чувство достоинства женщин. В патогенезе этих процессов большое значение уделяется роли гормонов. Под влиянием избытка андрогенов у женщин развивается синдром ГА, что клинически проявляется себореей, гирсутизмом, андрогензависимой алопецией.
Заболевания, при которых имеются признаки повышенной продукции андрогенов, относятся к междисциплинарной патологии и требуют пристального внимания и знаний не только гинеколога, но и в равной степени затрагивают сферу интересов эндокринологов, дерматологов, косметологов.
Кожа человека является комплексом андрогенчувствительных структур (сальные и потовые железы, волосяные фолликулы). Под влиянием андрогенов находятся многие важные функции кожи: митотическая активность клеток, активность сальных желез, рост волос, выраженность пигментации. Являясь тканью-мишенью для половых стероидных гормонов, например андрогенов, кожа принимает активное участие в метаболизме стероидных половых гормонов, в частности, в экстрагландулярном образовании из стероидов-предшественников.
Источником андрогенов в организме женщины являются яичники и кора надпочечников. Их синтез происходит под стимулирующим действием лютеинизирующего гормона (ЛГ) и адренокортикотропного гормона (АКТГ). Основной андроген надпочечников — дигидроэпиандростерон (ДГЭА) и его сульфат (ДГЭАС), яичников — тестостерон (Т) и андростендион (А). Действие половых гормонов на кожу осуществляется через специфические андрогенные рецепторы (АР) сосочкового слоя дермы, фибробласты, кератиноциты, эпителиальные клетки просвета апокриновых желез и секреторный отдел эккриновых сальных желез, а также в себоцитах и волосяных фолликулах.
Мишенями для половых стероидов в коже являются эпидермис, волосяные фолликулы, сальные железы, меланоциты и фибробласты. Под воздействием андрогенов усиливаются дифференцировка и митотическая активность клеток эпидермиса, увеличивается синтез межклеточных липидов, увеличивается толщина эпидермиса, стимулируется рост и пигментация волос, усиливается продукция кожного сала, снижается синтез глобулина, связывающего половые стероиды (ГСПС) в печени. В то же время под воздействием эстрогенов тормозится рост волос в андрогензависимых зонах, угнетается продукция кожного сала, усиливается синтез ГСПС.
Важным патогенетическим звеном при ГА является нарушение связывания андрогенов со специфическим ГСПС. Связанные с ГСПС стероиды недоступны для соединения с рецепторами в тканях-мишенях и оказания биологического эффекта. Биологический эффект в клетках-мишенях оказывает лишь свободная фракция половых стероидов. Она же ответственна за клинические проявления андрогенного эффекта.
Таким образом, ГА в организме женщины сопровождается избыточной секрецией мужских половых гормонов или повышенной чувствительностью тканей к неизмененному уровню андрогенов. Совокупность признаков поражения кожи и ее придатков, возникающих в результате избытка андрогенов в женском организме (себорея, гирсутизм, андрогензависимая алопеция), можно обозначить термином «гиперандрогенная дермопатия».
ГА может проявляться в виде абсолютного увеличения количества гормонов (абсолютная ГА) или повышенной чувствительностью рецепторов к нормальному или сниженному содержанию андрогенов в организме (относительная ГА).
Акне. В клетках сальных желез — себоцитах тестостерон под действием фермента α5-редуктазы 1-го типа переходит в самый активный метаболит — дигидротестостерон, который служит непосредственным стимулятором роста и созревания себоцитов, образования кожного сала. Основными причинами относительной ГА являются повышенная активность фермента α5-редуктазы 1-го типа, повышенная плотность ядерных дигидротестостероновых рецепторов, увеличение свободной фракции тестостерона в крови. Таким образом, в патогенезе акне ведущая роль принадлежит гормональному фактору, приводящему к гипертрофии и повышенному функционированию сальных желез, фолликулярному гиперкератозу в протоке сально-волосяного фолликула (СВФ), активизации микроорганизмов с последующим воспалением.
Себорея. Себорея — патологическое состояние кожи, обусловленное нарушением функции сальных желез, изменением состава их секрета. Возникновение синдрома ГА — себореи, связано с избытком андрогенов. Проявляется в местах, богатых сальными железами, — на лице, волосистой части головы, верхней части груди, в межлопаточной области. Развитию себореи способствуют нарушения функции половых желез (в частности, нормального соотношения между эстрогенами и андрогенами), надпочечников, щитовидной железы, а также иммунной, пищеварительной, центральной и вегетативной систем. Различают сухую и жирную себорею. У некоторых больных может быть смешанная себорея: на одних участках имеются симптомы сухой, а на других — жирной себореи.
Огромная роль в патогенезе себореи отводится наследственности. Генотип — врожденные качества, заложенные в генах. Структура кожного покрова является врожденной и неизменной на протяжении всей жизни, несмотря на то что поверхность кожи может постоянно меняться — трескаться, шелушиться, менять цвет (тускнеть), стать более грубой, тем не менее структура ее всегда индивидуальная, не меняющаяся.
При повышенном уровне мужских половых гормонов может изменяться тип кожи. Она становится жирной, поры на лице и себорейных участках расширяются, рН достигает 6, появляется склонность к дисхромиям.
Жирную себорею подразделяют на жидкую и густую, в зависимости от консистенции кожного сала, что определяется его физико-химическим составом. Участвуя в формировании водно-липидной мантии, кожное сало оказывает выраженное бактерио- и фунгицидное действие на большинство микроорганизмов. Компоненты липидной пленки на поверхности кожи являются производными сальных желез и эпидермиса и на 60% представлены триглицеридами, на 20—25% — эфирами воска, на 10—15% — скваленом, на 1—3% — эстерифицированными стеролами и на 0,5—2% — свободным стеролом. В увеличенном объеме кожного сала снижается концентрация незаменимой α-линоевой кислоты, которая подавляет экспрессию фермента трансглутаминазы. α-Линоевая кислота является основным регулятором дифференцировки кератиноцитов. Трансглутаминаза участвует в синтезе кератина 1-й и 10-й фракций, белков инволюкрина, лорикрина и филлагрина — основных компонентов цементирующего межклеточного вещества. Уменьшение количества линолевой кислоты приводит к повышению рН кожного сала, в итоге значительно нарушается барьерная функция эпителия и создаются условия для роста микроорганизмов на поверхности кожи и внутри сально-волосяных фолликулов.
Основными критериями оценки типов кожи на приеме у врача-косметолога являются характеристика салообразования — повышенное, пониженное, умеренное; степень расширения пор — расширенные, умеренно-расширенные, точечные; состояние липидной субстанции эпидермиса после умывания — чувство стянутости, дискомфорт, шелушение, покраснение.

Сравнивая различные состояния кожи здоровых пациентов и пациентов с себореей посредством неинвазивных методов морфофункциональной диагностики кожи (себуметрии, корнеометрии, рН-метрии) с применением аппарата SOFT PLUS, CATELLANI GROUP (Италия), мы получили следующие результаты (табл. 1).

Одним из объективных методов оценки состояния кожи является ультразвуковое исследование (УЗИ). У пациента с нормальной кожей при УЗИ видны сглаженность рельефа эпидермиса, равномерное распределение эхосигнала; эпидермис четко отграничен от дермы, дерма дифференцирована на отделы, расположение волокон дермы линейное (рис. 1, а). Рисунок 1. Ультразвуковая картина кожи в норме (а) и у пациента с себореей (б). У пациента с себореей отмечаются изменение эхоструктуры эпидермиса, нарушение его рельефа, протоки сальных желез расширены; отсутствует четкая граница между эпидермисом и дермой, эхогенность субэпидермального отдела дермы снижена (рис. 1, б).
Еще одним симптомом ГА является гирсутизм.

Гирсутизм. Под гирсутизмом (рис. 2) Рисунок 2. Гирсутизм у пациентки (из фотоархива ООО «Профессорская клиника Юцковских»). следует понимать увеличение у женщин количества волос на лице, груди, животе, вокруг сосков, а также на спине и бедрах. При усиленном оволосении женщин еще говорят о гипертрихозе. Между терминами «гирсутизм» и «гипертрихоз» существует разница: первый обозначает мужской тип роста волос у женщин, а второй — количественное увеличение волос на теле. Гирсутизм чаще всего является признаком некоторых эндокринных заболеваний, вызванных поражением гипоталамо-гипофизарной области, коры надпочечников и яичников. Но гирсутизм не всегда связан с нейроэндокринной патологией.
Выделяют следующие формы гирсутизма, не связанные с патологией яичников или надпочечников: конституциональный, экзогенный, идиопатический. Конституциональная форма гирсутизма носит наследственный характер. При этом виде повышенного оволосения продукция андрогенов в норме. К этой форме гирсутизма относится избыточное оволосение у женщин отдельных национальностей (жительницы стран Востока и Средиземноморья). Экзогенная форма гирсутизма возникает в тех случаях, когда приходится вводить андрогены в виде инъекций лекарственных препаратов. Гирсутизм может развиваться при применении таких препаратов, как кортикостероиды, стрептомицин. Предположение об идиопатическом гирсутизме возникает в тех случаях, когда не обнаруживается эндокринная патология и исключается экзогенный и конституциональный гирсутизм. Этот диагноз ставится при нормальном и повышенном содержании свободного тестостерона и невозможности установить причину заболевания. Учитывая, что достаточно часто гирсутизм служит проявлением ГА, целесообразно применение антиандрогенных препаратов. При гирсутизме косметическое устранение волос (эпиляция) эффективно только при условии удаления или угнетения источника повышенной секреции андрогенов.

Алопеция. В развитии андрогенной алопеции (рис. 3) Рисунок 3. Андрогенная алопеция у пациентки (из фотоархива ООО «Профессорская клиника Юцковских»). основная роль принадлежит α5-редуктазе — ферменту, который восстанавливает тестостерон до дигидротестостерона (ДГТ). ДГТ сокращает фазу роста волосяного фолликула, что приводит к его уменьшению и постепенной атрофии. Одновременно сокращается продолжительность жизненного цикла волоса, в результате чего наблюдается усиленное выпадение волос. Исследования показали, что уровень андрогенов у женщин с андрогенной алопецией часто не превышает норму. Это свидетельствует о том, что в патогенезе андрогенной алопеции основную роль играет повышенная чувствительность фолликулов к действию ДГТ. Женская андрогенная алопеция носит диффузный характер и редко приводит к облысению. При андрогенной алопеции на голове всегда остается венчик волос в затылочной и височных областях. Суть феномена состоит в том, что волосяные фолликулы в этих зонах не имеют рецепторов, способных воспринимать действие андрогенов. Поэтому исключается одна из обязательных причин андрогенной алопеции — гормональная активность — и волосы в этих областях генетически «застрахованы» от выпадения.
Современные подходы к лечению различных форм ГА включают назначение системных и наружных препаратов. Выбор методов лечения ГА должен основываться на адекватной клинической оценке степени тяжести синдромов ГА. Следует всегда учитывать состояние эндокринного фона, сопутствующие заболевания и состояния.

По нашим данным, за последние 5 лет значительно увеличилась обращаемость пациентов с синдромами ГА, особенно с такими, как алопеция и гирсутизм (рис. 4). Рисунок 4. Динамика обращаемости пациентов с синдромами гиперандрогении (по данным ООО «Профессорская клиника Юцковских», 2005—2009 гг.).
Механизм антиандрогенного действия КОК заключается в снижении продукции гонадотропинов (ЛГ), редукции уровня циркулирующих андрогенов, увеличении связывания андрогенов, снижении секреции андрогенов надпочечниками, ингибировании α5-редуктазы, связывании андрогенных рецепторов.
Первым КОК антиандрогенного действия был препарат диане-50, созданный на основе синтезированного в 1961 г. ципротерон-ацетата. В 1985 г. были созданы диане-35 (со снижением дозы эстрогенного компонента) и препарат андрокур (10 или 50 мг ципротерона ацетата).
Проведенные в 40 странах Европы два плацебо-контролируемых исследования с участием 1072 женщин в возрасте 14—45 лет с проявлениями акне показали, что применение КОК Джес по сравнению с плацебо к концу 6-го месяца способствует выраженному регрессу как невоспалительных, так и воспалительных акне. К окончанию терапии в среднем по группе акне регрессировали на 56%; состояния клинического излечения удалось достичь у 22% пациенток. Наиболее выраженное улучшение наблюдалось у женщин в возрасте от 14 до 22 лет.
В другом исследовании, посвященном оценке косметических аспектов приема антиандрогенного КОК на основе дроспиренона, к концу 6-го месяца терапии было продемонстрировано уменьшение себореи (на 71%), акне (на 75%) и гипертрихоза (показатель Ферримана—Галлвея — на 43%). При оценке толщины эпидермиса (корнеометрия) выявлено повышение гидратации на 26%, что было обусловлено как влиянием эстрогена в составе КОК, так и снижением концентрации андрогенов и/или их активности. Патоморфологически повышение гидратации эпидермиса обусловлено стимуляцией эстрогенами синтеза гиалуроновой кислоты. Определение снижения уровня испарения жидкости с поверхности кожи (на 35%) с помощью теваметрии (TEWL) также свидетельствовало об улучшении состояния кожи.
Важнейшим преимуществом Джес является хорошая переносимость, в частности, отсутствие влияния на массу тела, а иногда ее снижение. Это объясняется тем, что дроспиренон, входящий в состав препарата, дает антиминералокортикоидный эффект и препятствует задержке жидкости в организме, которая часто служит причиной увеличения массы тела при приеме КОК. Джес эффективно уменьшает проявления предменструального синдрома, в частности, появление акне в период, предшествующий менструации.
Таким образом, патогенетически оправдано и клинически актуально использование для лечения себореи, гирсутизма, андрогензависимой алопеции современных КОК, в частности Джес, которые подавляют секрецию гонадотропинов, стимулируют синтез ГСПС и снижают активность α5-редуктазы. Применение КОК, оказывающих антиандрогенный эффект, может улучшить не только гормональные параметры и классические проявления ГА, но и общее состояние, а также качество кожи, повышая гидратацию и улучшая характеристики, отражающие состояние кожи.
Так как диагностика и лечение различных форм ГА находятся на стыке нескольких специальностей (гинекология, эндокринология, дерматология), то только их объединение позволит добиться высоких результатов в лечении себореи, гирсутизма и андрогензависимой алопеции.
ГБОУ ВПО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России, Москва, Россия, 117997
Современные патогенетические подходы к наружной терапии и средствам ухода за кожей при угревой болезни
Журнал: Клиническая дерматология и венерология. 2016;15(5): 67‑71
ГБОУ ВПО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России, Москва, Россия, 117997
Как известно, при лечении угревой болезни дерматологи и косметологи большое значение придают местной терапии и базовому уходу за пораженной кожей. В последние годы на рынке регулярно появляются новые препараты для местного применения, а также средства по уходу как за здоровой, так и за проблемной кожей. В настоящем обзоре освещены основные патогенетические механизмы возникновения угревой болезни и коррекция различных состояний кожи при данном дерматозе.
ГБОУ ВПО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России, Москва, Россия, 117997
Лечение угревой болезни (акне, угри) — одного из самых распространенных дерматозов до сих пор остается непростой задачей, несмотря на многочисленные исследования, посвященные изучению патогенеза заболевания и разработке новых методов фармакотерапии. Акне — полиморфное мультифакториальное заболевание, у большинства пациентов с хроническим течением, в основе которого лежит патология пилосеборейного комплекса, связанная с его функциональной активностью и развитием воспалительных и невоспалительных высыпаний на участках кожи, богатых сальными железами. По данным ряда авторов, юношеские угри в той или иной степени наблюдаются у 90% подростков. Заболевание обычно начинается в 12—14 лет, пик заболеваемости приходится на 15—18 лет. У большинства больных процесс имеет физиологический характер и к возрасту примерно 20 лет проходит полностью.
Примерно у 20% подростков инволюция акне происходит значительно медленней, приобретает хронический рецидивирующий характер, в отдельных случаях с формированием к 30—40 годам поздних акне (acne tarda).
Как активная фаза кожного процесса, так и косметически значимый постэруптивный исход в рубцевание и пигментация плохо поддаются лечению, а самое неприятное, могут сопровождаться значительными психологическими расстройствами и существенно снижать качество жизни пациентов. Степень негативного влияния различных проявлений акне на качество жизни не коррелирует с объективным состоянием пациентов: даже легкая степень акне может обусловливать выраженную дисморфофобию, депрессию, а в некоторых случаях быть причиной более тяжелых психических расстройств. При сравнении с другими хроническими заболеваниями, такими как бронхиальная астма и эпилепсия, угревая болезнь характеризуется более выраженным влиянием на социальную и психологическую компоненты качества жизни.
В этиологическом аспекте детерминирующую роль в возникновении и тяжести течения угревой болезни играют генетические факторы. Известно, что вероятность акне у подростка выше в случаях заболевания обоих родителей, а также у 80% монозиготных близнецов.
Экзо- и эндогенные факторы могут иногда ухудшать течение заболевания либо провоцировать рецидивы. К числу таких факторов относят излишнее употребление углеводов, неблагоприятные профессиональные условия, стрессы, влажный климат, неграмотное и неумеренное использование косметических средств по уходу за кожей. Тем не менее основной роли в патогенезе угревой болезни эти факторы не играют.
В основе патогенеза акне лежат четыре взаимо-связанных фактора: патологический фолликулярный гиперкератоз, избыточное образование секрета сальных желез, микробная колонизация Propionibacterium acnes (P. acnes) и воспаление. Кроме этого, на характер и объем секреции сальных желез влияют андрогены, запуская механизм развития заболевания. В периоды гормональных кризов, особенно в пубертатный период, наблюдается резкое повышение уровня стероидных гормонов.
Но все же пусковым моментом при акне чаще являются не непосредственное повышение содержания андрогенов в организме (абсолютный гипер-андрогенизм), а генетически обусловленное увеличение количества и/или повышенная чувствительность рецепторов клеток сальных желез к производным тестостерона (относительный гиперандрогенизм). Уровень метаболитов тестостерона в коже повышается при активации 5-альфа-редуктазы, что наряду с повышенной экспрессией рецепторных клеток сальных желез ведет к усилению пролиферации себоцитов. Возникающий избыток кожного сала с нарушением его качественного состава (в частности, недостаток сквалена и линолевой кислоты), гиперплазия и гиперкератинизация фолликулярного эпителия, происходящая главным образом в нижней части воронки сально-волосяного фолликула, ведет к образованию пробок в протоках и обструкции. Формированию микрокомедонов способствуют повышенная адгезия корнеоцитов и снижение дезинтеграции десмосом, дисбаланс межклеточных липидов, особенно церамидов. Формирующиеся комедоны бывают открытые (черные) или закрытые (белые).
Следующим этапом развития угревой болезни является усиленное размножение анаэробных липофильных комменсалов P. acnes. Этот процесс является следствием предыдущего, поскольку липофильная резидентная микрофлора получает избыток питательного субстрата.
Эти микроорганизмы вызывают воспаление с помощью как иммунных, так и неиммунных механизмов. Пропионибактерии акне обладают ферментативной активностью, позволяющей расщеплять триглицериды, что приводит к высвобождению свободных жирных кислот, оказывающих раздражающее действие, и к развитию воспалительной реакции. Пропионибактерии акне продуцируют хемотоксические факторы, вызывающие приток полиморфно-ядерных лейкоцитов, а также способствуют выделению из эпителия протоков провоспалительных цитокинов, включая ИЛ-1 и ИЛ-2, ФНО-α. Воспалительная реакция поддерживается III (иммунокомплексным) и IV (клеточно-опосредованным) типами иммунных реакций. Защитные макрофагальные реакции в конечном итоге приводят к микрорубцеванию фолликула и вторичному уменьшению сальной железы.
В клинической картине среди высыпных элементов различают невоспалительные и воспалительные акне.
К невоспалительным относят открытые и закрытые комедоны, к воспалительным – фолликулярные папулы и пустулы, связанные с сальной железой. Это поверхностные элементы. К глубоким воспалительным элементам относят узловатые формы акне, различающиеся по глубине залегания и размеру воспалительного инфильтрата, который может быть ограничен одной перифолликулярной областью (индуративные акне) или же при распространении включает соседние фолликулы с двумя комедонами или более (конглобатные акне). Узловатые акне при интенсивном нагноении могут переходить в абсцедирующие, кистозные и флегмонозные. Их рассматривают как последовательные переходные формы в динамике воспалительных элементов или как результат осложнений при воздействии агрессивной микробной инфекции. К осложненным формам относят поражения с неблагоприятным исходом при конглобатных акне: келоидные, рубцующиеся колликвативные акне. Наиболее типичной локализацией акне считают лицо, верхнюю часть груди и спины. Следует отметить, что воспалительные акне также могут возникать на голове, шее, ягодицах и других частях тела.
Что касается определения степени тяжести угревой болезни, то до сих пор не существует единой классификации. Наиболее удобна классификация, предложенная Американской академией дерматологии, которая предлагает деление на четыре степени тяжести:
— I степень характеризуется наличием комедонов невоспалительного характера, возникших в результате закупорки устьев фолликула – единичных папул;
— при II степени отмечается папулезная сыпь и незначительное количество пустул;
— при III степени, наряду с выраженной папулезно-пустулезной сыпью, отмечаются до 3—5 узлов;
— IV степень отличается выраженной воспалительной реакцией в глубоких слоях дермы с формированием множественных болезненных узлов и кист.
Однако большинство исследователей выделяют три степени тяжести заболевания — легкую, среднюю и тяжелую.
Легкая степень угревой болезни диагностируется при наличии закрытых и открытых комедонов, практически без признаков воспаления и менее 10 папулезно-пустулезных элементов. При средней степени тяжести в клинической картине отмечается более 10, но менее 40 папулопустулезных элементов. Тяжелая степень характеризуется наличием более 40 папул и пустул, а также наличием узлов и кист.
Принципиально выбор терапии при угревой болезни должен основываться на анализе двух основных критериев: степени тяжести кожного процесса и характера его течения. Назначение соответствующей терапии должно осуществляться с учетом типа кожи, пола, возраста, сопутствующих заболеваний и эффективности предшествующих методов лечения.
К основным группам препаратов для лечения угревой болезни относят себостатические, антибактериальные, противовоспалительные и устраняющие фолликулярный гиперкератоз.
Показанием для назначения системной терапии являются акне средней и тяжелой степени, психосоциальная дезадаптация, а также образование рубцов и неэффективность наружного лечения.
Наружная терапия и соответствующие средства по уходу за кожей назначают пациентам независимо от степени тяжести заболевания.
Перед началом лечения угревой болезни каждому пациенту следует сообщить, что это заболевание требует длительного лечения и грамотного ухода за кожей, предполагая тем самым важность терпения со стороны пациентов.
В лечении угревой болезни важное место отводится местной терапии и грамотному уходу за проблемной кожей, хотя во всех случаях лечение должно быть комплексным.
Для наружной терапии угревой болезни в настоящее время используют топические ретиноиды, антимикробные (бензоил пероксид) и антибактериальные препараты, комбинированные лекарственные средства, азелаиновую и салициловую кислоты. Все эти препараты для наружного применения действуют на определенные звенья патогенеза.
Механизм действия топических ретиноидов заключается в регулировании и нормализации процесса ороговения фолликулярного эпителия (фолликулярная кератинизация), а также в уменьшении воспаления и метаболизма арахидоновой кислоты, что объясняет антикомедоногенное действие.
Однако побочных действий топических ретиноидов, вызывающих сухость кожи, раздражение слизистых при контакте с препаратом, практически избежать невозможно.
Антимикробные препараты (бензоил пероксид) и топические антибиотики проявляют неспецифическую противомикробную активность, уменьшая количество Propionibacterium acnes, Stafilococcus epidermidis и других микроорганизмов за счет окислительного эффекта свободного кислорода. Эти препараты оказывают также кератолитическое действие, улучшают оксигенацию тканей, подавляют продукцию кожного сала в сальных железах. Сочетанное применение этих средств предотвращает появление бактериальной резистентности.
Азелаиновая и салициловая кислоты также обладают кератолитическим, антибактериальным и противовоспалительным действием. При акне применение салициловой кислоты оправдано с позиций угнетения процесса фолликулярной кератинизации и разрыхления комедонового детрита.
Все эти препараты можно применять в зависимости от степени тяжести либо самостоятельно, либо в комбинации друг с другом.
Особое внимание следует уделять правильному очищению и увлажнению кожи, так как действие наружных лекарственных препаратов зачастую сопровождается обезвоживанием кожи, раздражением. Важной задачей является выбор современных средств, способных обеспечить оптимальную защиту и очистку кожи, не повреждая при этом липиды рогового слоя. Следующим этапом ухода за кожей является ее адекватное увлажнение. В настоящее время выделяют три группы веществ, оказывающих увлажняющее действие: обеспечивающие прямое увлажнение, сохраняющие липидный слой и кератолитические средства.
Всем этим требованиям отвечает широко известная линия Себиум, в которую входит целая гамма средств по лечению и уходу за смешанной и жирной кожей с тенденцией к акне, разработанная «Дерматологической Лабораторией Биодерма» (Франция).
1. Хорошо зарекомендовавшие себя средства для мягкого очищения проблемной кожи Мусс Себиум и Мицеллярная вода Себиум Н20 обладают себорегулирующим и антисептическим действием. Они не содержат щелочи, спирта и ароматизаторов, вследствие чего не вызывают раздражения и ощущения сухости. Как средство дополнительного ухода при полиморфном акне можно рекомендовать крем Себиум Глобаль, который обладает противовоспалительным, кераторегулирующим, увлажняющим действием, нормализует липидный профиль. Крем Себиум Гидра интенсивно увлажняет и восстанавливает кожу после применения топических ретиноидов или бензоил пероксида, оказывает противовоспалительное и успокаивающее действие.
В состав препаратов всей линии Себиум входят сбалансированные компоненты, позволяющие воздействовать на все звенья патогенеза при угревой болезни: глюконат цинка, сопорозные липиды, инфламин, эфиры АНА и запатентованный комплекс Флюидактив, защищающий сквален от окисления (так как окисленный сквален обладает комедоногенным эффектом) и нормализующий качество кожного сала, что препятствует появлению гиперкератоза.
Высокая концентрация глюконата цинка оказывает бактерицидное действие на Р. acnes, включая штаммы, устойчивые к эритромицину, а также обладает себорегулирующим эффектом, ингибируя 5-альфа-редуктазу.
Сопорозные липиды, входящие в состав средств, являются продуктом процесса ферментации дрожжей Candida bombicola. Они ингибируют активность липаз, препятствуя освобождению свободных жирных кислот, оказывающих раздражающее действие и приводящих к воспалению.
Инфламин представляет собой сочетание ламинарии и рамнозы. Экстракт ламинарии блокирует продукцию основных медиаторов воспаления (ИЛ-1a и ИЛ-6), а рамноза ингибирует ИЛ-8, тем самым ограничивая развитие воспалительных реакций.
Кератолитический эффект препаратов достигается сочетанием эфиров АНА с салициловой кислотой, при этом входящая в состав яблочная кислота активно стимулирует эксфолиацию липидов рогового слоя.
Таким образом, грамотное и обоснованное назначение местной терапии в сочетании со средствами базового ухода за кожей, несомненно, обеспечит успех в лечении такого порой длительно протекающего хронического дерматоза, как угревая болезнь.
Читайте также:

